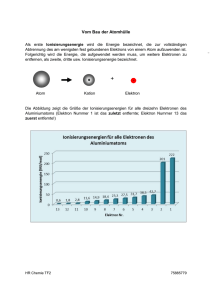
4 0,0000 0,0000 1,0000 0,0000
Werbung

Skript zum Seminarthema: Erstellungskonzept eines Programms zur Durchführung von HÜCKEL-Rechnungen zum Einsatz in der Lehre Erster Betreuer: Prof. Dr. Horst Schäfer Zweiter Betreuer: Prof. Dr. Gerhard Raabe Erstellt von: Daniel Dautaj 1 Inhalt Erich Hückel ............................................................................................................................................. 3 Einleitung ............................................................................................................................................. 4 Grundlagen der Quantenmechanik ......................................................................................................... 4 Der Welle-Teilchen-Dualismus der Materie ........................................................................................ 5 Das Unbestimmtheitsprinzip ............................................................................................................... 6 Das Elektron im Kasten.................................................................................................................... 6 Chemische Bindungen ............................................................................................................................. 9 Orbitale ................................................................................................................................................ 9 Die σ-Bindung ...................................................................................................................................... 9 Die π-Bindung.................................................................................................................................... 10 Theoretische Grundlagen des HÜCKEL-Verfahrens............................................................................... 11 Die Separierbarkeit von 𝝅-Elektronen und 𝝈-Elektronen ................................................................. 11 Die Matrixelemente des HÜCKEL-Operators..................................................................................... 14 Die Umsetzung ...................................................................................................................................... 20 Input-File ........................................................................................................................................... 20 Output-File ........................................................................................................................................ 21 Quellenangaben: ................................................................................................................................... 25 2 Erich Armand Arthur Joseph Hückel Bild: Erich Hückel (Wikipedia) Erich Hückel wurde am 06.08.1896 als Sohn von Marie und Armand Hückel in Berlin geboren. Er hatte zwei Brüder, Rudi und Walter. Walter machte sich später als Ordinarius für Organische Chemie einen Namen. Erich Hückel studierte Mathematik und Physik in Göttingen und gilt als eine der großen Persönlichkeiten der Quantenchemie. Erich Hückel fertigte seine Dissertation auf experimenteller Basis über Streuung von Röntgenstrahlen bei Peter Debye an. Danach arbeitete er zwei Jahre lang als Mathematikassistent und wechselte anschließend an die Eidgenössischen Technischen Hochschule nach Zürich, wo er an der Debye-Hückel-Theorie arbeitete. Es ist leider nicht ganz klar, wer den größeren Beitrag zur dieser Theorie geleistet hat. Aber Hückel investierte seine Zeit schon in dieser frühen Phase seines Lebens in noch offene Fragen auf dem Gebiet der Physikalischen und Organischen Chemie. Hier entwickelte er entsprechende Theorien, die auf sehr pragmatischen Verfahren basierten. Auf der Grundlage einfacher Annahmen fand er Wege die schließlich nicht nur zu plausiblen Erklärungen führten, sondern auch zu überprüfbaren Voraussagen. Später bei Donnan in London vollendete er seine vermutlich wichtigste Arbeit, nämlich die auf dem Gebiet der organischen Quantenchemie. Im Jahr 1930 arbeitete er als Dozent an der Technischen Hochschule in Stuttgart und sieben Jahre später wurde er auf eine Professur in Marburg berufen. Hier beschäftigte er sich mit der quantenmechanischen Beschreibung ungesättigter und konjugierter Moleküle, die insbesondere auf dem Gebiet der Farbstoffchemie eine wichtige Rolle spielten (und immer noch spielen). Obwohl er Theoretiker war, versuchte er seine Theorie im Rahmen starker approximativer Methoden einfach darzustellen, wie z.B. im Fall cyclischer Moleküle. Weiterhin beschäftigte er sich mit der Bedeutung der 3 Konnektivität der Atome für die Spinmultiplizität was später die Grundlage für die Hundsche Regel bildete. Die moderne Organische und Physikalische Chemie basiert heute zu einem nicht unwesentlichen Teil auf den von Erich Hückel erarbeiteten Methoden und Theorien, wie z.B. der Hückel-Molekularorbitaltheorie, der Theorie der Elektrolyte oder der quantentheoretischen Deutung der thermodynamischen Eigenschaften des Benzols. Erich Hückel wurde 1965 der Otto-Hahn-Preis für Chemie und Physik verliehen. Einleitung Um das Erstellungskonzept des Programms zur Durchführung von HÜCKELRechnungen zu realisieren, sollte man sich einen Überblick über die Grundlagen der HÜCKEL-Theorie verschaffen. Diese basiert auf der Theorie der chemischen Bindung und setzt daher notwendigerweise Kenntnisse der Physik voraus. Da bei der Beschreibung atomarer Vorgänge die klassische Physik versagt, muss man sich zunächst einen Überblick über das in diesem Zusammenhang wichtigste Teilgebiet der Physik, nämlich das der quantenmechanischen Vorgänge verschaffen. Hierauf kann in diesem Zusammenhang nicht genauer eingegangen werden, da dies über den Rahmen der Seminararbeit hinausgehen würde. Grundlagen der Quantenmechanik Durch die Einführung der der auf der Planckschen Quantentheorie beruhenden Bohrschen Postulate stellte Niels Bohr das ursprünglich von Ernest Rutherford erarbeitete Modell zur Bewegung der Elektronen auf kreisförmigen Bahnen um den Atomkern eine neue Grundlage. Die aus den Bohrschen Vorstellungen folgenden diskreten Energiezustände der Elektronen in einem Atom wurden später von Franck und Hertz durch Elektronenstoßexperimente gestützt. Später versuchte Sommerfeld, die Bohrschen Vorstellungen des Atommodells zu erweitern, indem er für die Elektronen nicht nur kreisförmige sondern auch elliptische Bewegungen einführte. Im Fall des Heliumspektrums versagte die Theorie schließlich. Damit zeigte sich, dass die aus makroskopischen Erscheinungen gewonnen Anschauungen, wie z.B. Kreisbahnen, im atomaren Bereich keine Gültigkeit mehr besitzen. Anders formuliert versagen die Gesetze der klassischen Physik im atomaren Bereich vollständig und besitzen dort keine Gültigkeit mehr. Die Aufgabe der grundlegenden klassischen Vorstellungen war der Anfang der modernen Quantentheorie. 4 Der Welle-Teilchen-Dualismus der Materie Je nach durchgeführtem Experiment kann Licht entweder als aus Teilchen bestehend oder aber als eine elektromagnetische Wellenerscheinung interpretiert werden. Licht breitet sich im Vakuum mit der konstanten Geschwindigkeit 𝑐 = 2,998 ∙ 1010 𝑐𝑚 𝑠 −1 aus. Die Geschwindigkeit ist proportional zur Frequenz ν und der Wellenlänge λ: 𝑐 =𝜈∙𝜆 Der Wellencharakter des Lichts kann durch Beugungsexperimente gezeigt werden. Die Interpretation des Lichtes als Strom von Photonen, liegt der Erklärung des photoelektrischen Effekts von Einstein (1905) zu Grunde. Wenn mit Licht eine Metallplatte aus Cäsium bestrahlt wird, werden Elektronen des Metalls aus der Plattenoberfläche freigesetzt („Photoelektronen“). Durch Erhöhung der Lichtintensität wird dabei die Anzahl der freigesetzten Elektronen erhöht, ihre Energie aber nicht verändert. 𝐸 = ℎ𝜈 (ℎ = 6,626 ∙ 10−34 J s ist bekannt als Plancksche Konstante oder Plancksches Wirkungsquantum) In diesem Teilabschnitt der Quantenmechanik wurde gezeigt, dass Teilchen je nach durchgeführtem Experiment Welleneigenschaften oder Teilcheneigenschaften zeigen. Der Welle-Teilchen Dualismus erfordert eine neue Theorie, die im Rahmen der Quantenmechanik beschrieben wird. Ein Teilchen kann man leicht als ein Punkt im Raum mit den entsprechenden Koordinaten lokalisieren. Im Gegenteil dazu lässt sich aber für eine Welle nur ihre Amplitude an einer Stelle des Raumes angeben und das führt uns zum nächsten Thema. 5 Das Unbestimmtheitsprinzip Das Elektron im Kasten Elektron in einem eindimensionalen Kasten Als ein einführendes Beispiel im Rahmen der angewandten Quantentheorie bietet sich die Behandlung eines Teilchens (in unserem Fall ein negativ geladenes Teilchen, ein Elektron) mit der Masse m an, das sich in einem eindimensionalen Kasten entlang der x-Achse zwischen 0 und a bewegt. Dazu könnte man sich als klassisches Analogon die Bewegung einer Billardkugel auf einem Billardtisch vorstellen. Mit der Restriktion, dass sich die Billardkugel zwischen zwei Banden im Abstand a geradlinig und eindimensional bewegt. Dabei muss außerdem beachtet werden, dass die Reflexion der Kugel immer senkrecht zu den Tischbanden erfolgt. Als weitere Randbedingung soll im Bereich zwischen x = 0 und x = a das Potential verschwinden, d.h. dass auf das Elektron in diesem Bereich keine Kräfte wirken. Im Gegenteil dazu ist das Potential sowohl bei x = 0 als auch bei x = a unendlich groß. Als Folge wird das Elektron an diesen Grenzen durch unendlich große Kräfte in den Kasten zurückgetrieben. Außerhalb des Kastens kann man das Elektron demnach nicht antreffen. In der klassischen Physik wird die Gesamtenergie eines Teilchens in Form der Hamiltonfunktion (H = T + V) angegeben. Wobei T die klassische kinetische Energie und V die klassische potentielle Energie ist. Die kinetische Energie ist eine Funktion des Impulses und die potentielle Energie eine Funktion der entsprechenden Ortskoordinaten (z.B.: 𝑝𝑥 , 𝑥). Aufgrund der Heisenbergschen Unschärferelation besitzen atomare Teilchen nicht gleichzeitig scharfe Werte für Ort und Impuls. Daher müssen die klassischen Ausdrücke für die 6 kinetische Energie (T) und die potentielle Energie (V) durch die entsprechenden Operatoren T und V ersetzt werden. Die Summe dieser Operatoren bezeichnet man als Hamilton-Operator ℋ: 𝓗ℋ = 𝑻 + 𝑽 Wenn man von der Schrödinger-Gleichung unter Einsatz des Hamilton-Operators ausgeht ℋφ = Eφ erhält man die Eigenwertgleichung der Energie 𝑻 𝑽 ⏞ ћ2 𝜕 2 𝜕2 𝜕2 ⏞ − ( + + ) + 𝑉(𝑥, 𝑦, 𝑧) 𝜑(𝑥, 𝑦, 𝑧) = 𝐸𝜑(𝑥, 𝑦, 𝑧) 2𝑚 𝜕𝑥 2 𝜕𝑦 2 𝜕𝑧 2 [ ] Die Funktion 𝜑(𝑥, 𝑦, 𝑧) bezeichnet man als Wellenfunktion des betrachteten Systems. Da sich unser Elektron nur in der x-Richtung bewegt, lautet die Schrödinger-Gleichung für das Elektron im eindimensionalen Kasten wie folgt: − ћ2 𝑑2 𝜑(𝑥) = 𝐸𝜑(𝑥) 2𝑚 𝑑𝑥 2 Die Lösung dieser Gleichung liefert die Energieeigenwerte und die normierbaren Eigenfunktionen für ein Elektron im Kasten. Eine Lösung ist z.B. eine Sinusfunktion A·sin(Bx) an, da zweimaliges Differenzieren wieder zur gleichen Sinusfunktion führt. Als Ergebnis der Rechnung wird folgende Gleichung erhalten: 2 𝜋𝑛 𝜑𝑛 (𝑥) = √𝑎 sin ( 𝑎 𝑥) Für die zugehörigen Energien erhält man: 𝐸𝑛 = ℎ2 8𝑚𝑎2 𝑛2 mit n = 1,2,3…. Man kann die Richtigkeit dieser Gleichung zeigen, indem man den angegebenen Ausdruck für φn in die entsprechende Schrödinger-Gleichung einsetzt. Außerdem kann man leicht zeigen, dass für φn die Normierungsbedingung erfüllt ist. 7 Es gilt: 𝑎 𝑎 2 𝜋𝑛 ∫ 𝑠𝑖𝑛 ( 𝑥) 𝑑𝑥 = 1 2 0 𝑎 Wir entnehmen der Energiegleichung, dass eine diskrete Folge von Energieeigenwerten 𝐸1 = (ℎ2 ⁄8𝑚𝑎2 ), 𝐸2 = (ℎ2 ⁄8𝑚𝑎2 ) 4, … auftritt. Das betrachtete System befindet sich nur in solchen Zuständen, die durch die angegebenen Energiewerte charakterisiert sind. Im klassischen Fall könnte sich das Elektron mit jeder beliebigen Energie bewegen, die Quantenmechanik zeigt hingegen, dass man bei Messungen an diesem hypothetischen System für die Energie nur die angegebenen ganzzahligen Vielfachen von ℎ2 ⁄8𝑚𝑎2 erhält. Es tritt somit eine „Quantelung“ der Energie auf. Die möglichen Zustände 𝜑𝑛 und die zugehörigen Energieeigenwerte En werden durch die verschiedenen Werte der Quantenzahl n∈N festgelegt. Die Quantenmechanik beschränkt die Werte der Energie, wobei der niedrigste mögliche Energieeigenwert nicht E = 0, sondern E = E1 ist. Den Zustand mit dem niedrigsten Energieeigenwert (also den Zustand φ1 ) nennt man den Grundzustand des Systems. Bild: Die vier niedrigsten Energieeigenwerte und die zugehörigen Wellenfunktionen für ein Elektron in einem eindimensionalen Kasten der Länge a 8 Chemische Bindungen Orbitale Bevor auf die chemischen Bindungen eingegangen wird, wird kurz der Begriff des „Orbitals“ erklärt. Ein Orbital ist eine Funktion (im Idealfall eine Eigenfunktion des enstprechenden Hamiltonsoperators), die Elektronen eines Atoms (Atomorbital) oder eines Moleküls (Molekülorbital) beschreibt. Das Betragsquadrat eines Orbitals an einer Stelle des Raumes gibt die Wahrscheinlichkeitsdichte für den Aufenthalt eines Elektrons an dieser Stelle des Raumes an. Im Fall von Atomen gibt es z.B.: s, p, d, f Orbitale. Das energieärmste ist das s-Orbital, gefolgt von p, d, … wobei außerdem beachtet werden muss, dass energiegleiche (entartete) Orbitale zunächst einfach, mit Elektronen gleichen Spins besetzt werden (Hundsche Regel). Nach dem Pauli Prinzip können die Orbitale mit maximal zwei Elektronen entgegengesetzten Spins besetzt werden. In dieser Arbeit werden die s- und p- Orbitale näher betrachtet, wobei der gefüllte Teil, ein positives Vorzeichen und der nicht gefüllte, ein negatives Vorzeichen des Orbitals symbolisiert. Im Fall der p-Orbitale kann man Funktionen definieren, die entlang der Achsen der entsprechenden Raumkoordinaten orientiert sind. Das sind die 𝑝𝑥 , 𝑝𝑦 , 𝑝𝑧 Orbitale. Die σ-Bindung Einer σ-Bindung liegt ein bindendes σ-Molekülorbital zugrunde, das durch verschiedene Überlappungsmöglichkeiten der s- und p-Orbitale gebildet werden kann. 9 𝛔-Bindung im einen Ethen-Molekül Die π-Bindung Man bezeichnet Bindungen, die bei der Überlappung von 2 p-Orbitalen entstehen und parallel zur Knotenebene ausgerichtet sind, als π-Bindungen. Die entsprechenden Orbitale nennt man Orbitale. 10 -Bindung in C2H4 H H C C H H -Bindung in C2H4 𝛑-Bindungen im Ethen-Molekül Theoretische Grundlagen des HÜCKEL-Verfahrens Die Separierbarkeit von 𝝅-Elektronen und 𝝈-Elektronen Im Rahmen der einfachen HÜCKEL-Theorie werden 𝜋-Elektronensysteme berechnet, ohne die gleichzeitige Gegenwart von 𝜎-Elektronen explizit zu berücksichtigen. Um an dieser Stelle Missverständnisse zu vermeiden, sei ausdrücklich darauf hingewiesen, dass die Betonung auf „explizit“ liegt. Separierbarkeit bedeutet hier nicht, dass die 𝜋-Elektronen die gleichzeitige Anwesenheit von 𝜎-Elektronen (und umgekehrt) überhaupt nicht „spüren“, sondern dass man die Wechselwirkung der 𝜋-Elektronen mit den 𝜎-Elektronen in Form eines effektiven Operators der potentiellen Energie 𝑉𝑒𝑓𝑓 berücksichtigt. Dieser Vorstellung zufolge bildet das Gerüst der 𝜎-Elektronen zusammen mit den Kernen ein effektives Feld, in dem sich die 𝜋-Elektronen bewegen. Man nimmt nun weiterhin an, dass sich auch die Wechselwirkungen der Elektronen in 𝜋-Orbitalen untereinander mit in diesen effektiven Operator hineinstecken lassen. Jedes 𝜋Elektron bewegt sich demnach in einem effektiven Feld, welches einerseits durch das 𝜎 gebundene Molekülgerüst und andererseits durch die restlichen 𝜋-Elektronen erzeugt wird. Der Hamiltonoperator ℋ für ein System aus n 𝜋-Elektronen lautet dann: 11 1 ℋ(1,2, … 𝑛) = Σni=1 (− Δ(i) + 𝑉𝑒𝑓𝑓 (i)) = Σni=1 ℋ(𝑖) 2 Er besteht also aus einer Summe von n Einelektronoperatoren (ℋ(𝑗)). Legt man diese Vorstellungen zugrunde, dann kann man leicht zeigen, dass die Matrixelemente des Operators ℋ zwischen π- und σ-Funktionen +∞ ∫ 𝜑 𝜎 (𝑖)ℋ(𝑖)𝜑 𝜋 (𝑖)𝑑𝜏 −∞ unter der Voraussetzung einer strengen Planarität des π-Systems den Wert Null annehmen. Tauscht man in ℋ(𝑗) 1 ℋ(𝑗) = − ∆(𝑗) + 𝑉𝑒𝑓𝑓 (𝑗) 2 𝑥𝑗 , 𝑦𝑗 und 𝑧𝑗 gegen 𝑥𝑗 , 𝑦𝑗 und −𝑧𝑗 aus d.h. spiegelt man an der Molekülebene Molekülebene So ändert man an dem Operator der kinetischen Energie 𝜕2 𝜕2 𝜕2 ∆(𝑗) = 2 + + 𝜕𝑥𝑗 𝜕𝑦𝑗2 𝜕𝑧𝑗2 nichts. Ähnlich leicht verständlich ist, dass 𝑉𝑒𝑓𝑓 (𝑗) in gleichen Abständen oberhalb (+𝑥𝑗 , +𝑦𝑗 , −𝑧𝑗 ) der Molekülebene gleich sein muss. 12 Bei einer 2𝑝𝑧 -Funktion kehrt sich bei der Spiegelung an der Molekülebene das Vorzeichen um. Da aber ℋ(𝑗) in einem Punkt oberhalb und dem gespiegelten Punkt unterhalb der Molekülebene gleich ist ergibt ℋ(𝑗)𝜑𝜋 (𝑗) eine Funktion, die ebenfalls bei der Spiegelung an der Molekülebene (d.h. bei Ersatz von (𝑥𝑗 , 𝑦𝑗 , 𝑧𝑗 ) durch (𝑥𝑗 , 𝑦𝑗 , −𝑧𝑗 )) ihr Vorzeichen wechselt. Multipliziert man nun noch die Funktion ℋ(𝑗)𝜑𝜋 (𝑗) mit der 𝜎-Funktion 𝜑𝑗𝜎 , die oberhalb und unterhalb der Molekülebene das gleiche Vorzeichen hat, so besitzen diese Produkte oberhalb und unterhalb in gleichen Abständen von der Molekülebene die gleichen Beträge bei unterschiedlichen Vorzeichen. Summiert man über alle Produkte (d.h. führt man die Integration aus), so ergibt sich: +∞ 𝜑 𝜎 (𝑗)ℋ(𝑗)𝜑 𝜋 (𝑗) 𝑑𝑡𝑗 = 0 ∫ −∞ Bei der Bildung des Energieerwartungswertes +∞ Ε𝜙𝑗′ = ′ ∫−∞ ∅∗𝑗 ℋ ∅𝑗 𝑑𝑡 +∞ ′ ∫−∞ ∅𝑗∗ ∅𝑗 𝑑𝑡 unter Verwendung einer Linearkombination 𝑛 ∅′𝑗 = ∑ 𝑐𝑖𝑗 𝜑𝑖 𝑖=1 bei der i=1…m die Atomfunktionen mit π-Symmetrie und i=m…n die Atomfunktionen mit σ-Symmetrie beschrieben, so erhält man eine geblockte Säkulardeterminante in der der eine Block das π- und der andere Block das σ-System beschreibt. 𝐻11 − Ε 𝐻12 ⋯ 𝐻1𝑚 𝐻21 𝐻22 − Ε ⋯ 𝐻2𝑚 | ⋮ ⋮ ⋱ ⋮ 𝐻𝑚1 𝐻𝑚2 ⋯ 𝐻𝑚𝑚 − Ε | | 0 0 | 𝐻𝑚+1,𝑚+1 − Ε 𝐻𝑚+1,𝑚+2 ⋯ 𝐻𝑚+1,𝑛 | = 0 𝐻𝑚+2,𝑚+1 𝐻𝑚+2,𝑚+2 − Ε ⋯ 𝐻𝑚+2,𝑛 | ⋮ ⋮ ⋱ ⋮ 𝐻𝑛,𝑚+1 𝐻𝑚,𝑚+2 ⋯ 𝐻𝑛,𝑛 − Ε 13 Dieser Block der oberen Determinante beschreibt das σ-System. 𝐻𝑚+1,𝑚+1 − Ε 𝐻𝑚+2,𝑚+1 | ⋮ 𝐻𝑛,𝑚+1 𝐻𝑚+1,𝑚+2 𝐻𝑚+2,𝑚+2 − Ε ⋮ 𝐻𝑚,𝑚+2 ⋯ 𝐻𝑚+1,𝑛 ⋯ 𝐻𝑚+2,𝑛 |=0 ⋱ ⋮ ⋯ 𝐻𝑛,𝑛 − Ε Was wir nun im Folgenden betrachten werden, ist die Determinante 𝐻11 − Ε 𝐻12 𝐻21 𝐻22 − Ε | ⋮ ⋮ 𝐻𝑚1 𝐻𝑚2 ⋯ 𝐻1𝑚 ⋯ 𝐻2𝑚 |=0 ⋱ ⋮ ⋯ 𝐻𝑚𝑚 − Ε die das π-System beschreibt. Die Matrixelemente des HÜCKEL-Operators In der HÜCKEL-Theorie gibt man weder für die Funktionen, noch für den HÜCKELOperator einen analytischen Ausdruck an, sondern definiert beide Größen über ihre Eigenschaften oder besser gesagt in ihrer Wirkung aufeinander. Die in dem LCAOAnsatz für die HÜCKEL-Molekülorbitale verwendeten Funktionen 𝜑𝜇 , besitzen das gleiche Symmetrieverhalten wie 2𝑝𝑧 - Funktionen und sind orthonormiert +∞ 𝜑𝜇∗ 𝜑𝜇 𝑑𝜏 = 1 ∫ −∞ +∞ ∫ 𝜑𝜇∗ 𝜑𝜗 𝑑𝜏 = 1 −∞ oder bildlich dargestellt: Dies zeigt den Unterschied zu den 2𝑝𝑧 - Funktionen an zwei benachbarten Zentren. Zwischen solchen Funktionen besteht eine, wenn auch kleine Überlappung: 14 +∞ 𝑆𝜇𝜈 = ∫ −∞ 2𝑝𝑧𝜇 2𝑝𝑧𝜗 𝑑𝜏 Die Annahme: +∞ ∫ 𝜑𝜇 𝜑𝜗 𝑑𝜏 = 𝛿𝜇𝜗 −∞ darf auf keinen Fall mit der Orthogonalitätsbedingung verwechselt werden, die für die an einem Zentrum lokalisierten Eigenfunktionen eines Operators mit verschiedenen Eigenwerten gilt. Die HÜCKEL-Molekülorbitale Ψ𝑖 , die man als Linearkombination dieser Funktionen ansetzt 𝑛 Ψ𝑖 = ∑ 𝑐𝑖𝜇 𝜑𝜇 𝜇=1 müssen ebenfalls normiert sein, wobei gilt: +∞ Ψ∗i Ψi dτ = 1 ∫ −∞ Unter Berücksichtigung unserer Annahme folgt hieraus 𝑛 2 ∑ 𝑐𝜇𝑖 =1 𝜇=1 Der HÜCKEL-Operator Näherungen)definiert: wird durch die folgenden Beziehungen (HÜCKEL- Sind die Zentren μ und υ benachbart, dann gibt man dem sogenannten Resonanzintegral den Wert β (β<0) +∞ 𝐻𝜇𝜐 ≝ ∫−∞ 𝜑𝜇 ℋ𝜑𝜈 𝑑𝜏 = 𝛽 mit β < 0 Sind die Zentren nicht benachbart, dann gibt man dem Resonanzintegral den Wert Null: +∞ 𝐻𝑢𝑣 ≝ ∫ 𝜑𝑢 ℋ𝜑𝑣 𝑑𝜏 = 0 −∞ Dem sogenannten Coulombintegral gibt man den Wert: +∞ 𝐻𝜇𝜇 ≝ ∫ 𝜑𝜇 ℋ𝜑𝜇 𝑑𝜏 = 𝛼𝑢 −∞ 15 α Entspricht der Energie eines Elektrons in einem 𝑝2 -Orbital, d.h. α < 0. Die Parameter α und β gewinnt man in der Regel experimentell, z.B. aus spektroskopischen Daten. Als Beispiel für die Anwendung des HÜCKEL-Verfahrens soll in der Bachelorarbeit das π-System der Allyl-Spezies (𝐶𝐻2 − 𝐶𝐻 − 𝐶𝐻2 ) berechnet werden. In dieser Arbeit wird auf die Hauptpunkte und Ihre Bedeutung eingegangen. Weitere Details werden in der anschließend durchgeführten Bachelorarbeit bestimmt. Zuerst setzen nun das HÜCKEL-Molekülorbital als Linearkombination der HÜCKELAtomorbitale an 𝜓 = 𝑐1 𝜑1 + 𝑐2 𝜑2 + 𝑐3 𝜑3 und bildet den Erwartungswert der Energie: +∞ Ε𝜙 = ∫−∞ 𝜓 ∗ ℋ 𝜓𝑑𝜏 +∞ ∫−∞ 𝜓 ∗ 𝜓𝑑𝜏 Wobei die 𝑐𝑖 , 𝑖 = 1,2, … 𝑛 Koeffizienten nach dem LCAO-MO-Ansatz (linear combination of atomic orbitals for molecular orbitals) bestimmt werden. Wobei das Prinzip gilt, dass jedes System den Zustand der niedrigsten Energie anstrebt. Danach nähern wir ϕ an ψ an, in dem wir 𝜕Ε 𝜕𝑐𝑖 bilden. Später erhalten wir das Säkulargleichungssystem aus dem wir dann die Säkulardeterminate daraus bilden, die in unseren Fall eine 3x3 Determinante ist. Aus der Säkulardeterminante lassen sich die Eigenvektoren berechnen. Eigenwerte und die zugehörigen Im Fall des Allylsystems ergeben sich die Eigenwerte: 𝜺𝟏 = 𝜶 + 𝜷√𝟐; 𝜺𝟐 = 𝜶; 𝜺𝟑 = 𝜶 − 𝜷√𝟐; 16 Diese Werte werden in einem Graphen durch die Software „Gnuplotter“ gezeichnet. Da die Benutzung dieser Software eine gewisse Einarbeitung erfordert wird der Graph ungefähr so aussehen. Dieser Graph ist mit der Software ChemBioDrawUltra Version 12 erstellt worden und das MO-Schema (Molecular Orbitals) der Allylsysteme lässt sich folgendermaßen darstellen: Bild: MO-Schema der Allylsysteme Sowohl im Falle des Kations als auch im Falle des Radikals und des Anions ist das tiefste π-Energieniveau mit zwei Elektronen, deren Spin antiparallel ausgerichtet ist, besetzt. Beim Kation ist das Niveau bei E = α leer, beim Radikal einfach und beim Anion doppelt besetzt. Betrachtet man noch einmal die Abbildung der π-Energieniveaus, dann erkennt man leicht eine bedeutende Unzulänglichkeit der einfachen HÜCKEL-Theorie: Die Energie der Elektronen in den besetzten Orbitalen besitzt sowohl im Falle des Radikals als auch im Falle des Anions unabhängig von der Besetzungszahl (das ist die Anzahl der Elektronen in einem Molekülorbital) den gleichen Wert. Man sieht leicht ein, dass die Energie eines π-Elektrons im HOMO (highest occupied molecular orbital) des Anions höher und damit ungünstiger als im HOMO des Radikals ist. Die Ursache ist die elektronische Abstoßung zwischen den beiden Elektronen im HOMO des Anions. Die Vernachlässigung dieser Abstoßung führt dazu, dass die Elektronenaffinität (das ist die Energie, die freigesetzt wird, wenn ein Elektron in das energetisch günstigste nicht vollbesetzte Molekularorbital gebracht wird) der einfachen HÜCKEL-Theorie zufolge von Allylkation und Allylradikal gleich sind, was mit Sicherheit nicht der Realität entspricht. Die HÜCKEL-Theorie sollte auf Grund der nur impliziten (d.h. der 17 im Rahmen der Verwendung von α und β) Berücksichtigung der elektronischen Abstoßung immer dann schlechte Ergebnisse liefern, wenn die Anionen oder stark polare Moleküle berechnet werden. Für alternierende Kohlenwasserstoffe mit gleichmäßiger Verteilung der π-Elektronen sollte man bessere Ergebnisse erhalten als für nicht-alternierende aromatische Kohlenwasserstoffe. So berechnet man z.B. nach dem einfachen HÜCKEL-Verfahren für den nicht alternierenden Aromat Azulen Bild: Nicht alternierender Aromat Azulen ein Dipolmoment, welches siebenmal so hoch ist wie das experimentell messbare. Tatsächlich zeigen genauere (und damit aufwendigere) Rechenverfahren, sowie experimentelle Untersuchungen, dass die Energie für ein π-Elektron im HOMO des Allylradikals tiefer liegt als die für das Allylanion. Abhilfe von diesem Mangel kann dadurch geschaffen werden, dass man das Coulombintegral eines Zentrums als Funktion der Ladung an diesem Zentrum ansetzt. In der sogenannten ω-Technik setzt man das Coulombintegral des Zentrums x wie folgt an: 𝛼𝑥 = 𝛼0 + (1 − 𝑞𝑥 )𝜔 Wobei 𝑞𝑥 die Ladung des Atoms x ist und ω ein Parameter, der durch Anpassung an experimentelle Befunde optimiert wird. Hierdurch wird eine bessere Berücksichtigung der elektronischen Abstoßung ermöglicht. Tatsächlich sind die unter Verwendung dieser Rechentechnik berechneten Dipolmomente für Kohlenwasserstoffe besser in Übereinstimmung mit dem experimentellen Befund als die nach dem einfachen HÜCKEL-Verfahren. Wir haben die π-MO‘s als eine Linearkombination der Atomfunktionen angesetzt: 3 ∅i = ∑ 𝑐𝑖𝜇 𝜑𝜇 𝜇=1 Als nächstes sollten die LCAO-Koeffizienten für die π-Molekülarorbitale des Allylsystems berechnet werden. Bei der Bestimmung des jeweiligen Koeffizienten sollte man mit der Normierungsbedingung anfangen: 18 𝑐12 + 𝑐22 + 𝑐32 = 1 Zur Berechnung der Koeffizienten muss man die jeweiligen Energieeigenwerte ε in das Säkulargleichungssystem einsetzen und pro Einsatz im Säkulargleichungssystem erhält man einen Satz von drei c-Koeffizienten. Somit erhält man für alle drei Allyl-Spezies für das höchste π-MO 3 1 1 1 ∅3 = ∑ 𝑐𝑖𝑗 𝜑𝑖 = 𝜑1 − 𝜑2 + 𝜑3 2 2 √2 𝑖=1 oder bildlich auch dargestellt: Bild: HOMO des Allyl-Systems So wie in der unteren Abbildung sollen die Ergebnisse zusammengefasst und dargestellt werden. Aus den Werten der umgeformten Säkulardeterminante wird unser Input-ASCII-File bestehen. 19 Die Umsetzung Input-File Wie in der Aufgabenstellung beschrieben, sollte das zu erstellende Programm mit der Programmiersprache Fortran-90 entwickelt werden. Das Programm sollte ein InputASCII-File einlesen. Ein Input-File (oder anders genannt als TXT-Datei) wird folgendermaßen aussehen: 1. Butadien 2. 4 3. 0 4. 1 2 1.0 5. 2 3 1.0 6. 3 4 1.0 7. 1 1 0.0 8. 2 2 0.0 9. 3 3 0.0 10. 4 4 0.0 Die Zeilennummerierung wird kein Bestandteil des Input-Files sein, sondern wurde hier nur eingeführt damit man die Bedeutung der einzelnen Zeilen besser erklären kann. Die erste Zeile zeigt uns, um welches Molekül es sich dabei handelt und in unserem Fall geht es um das Butadien-Molekül. Die zweite Zeile zeigt uns die Anzahl der Zentren (N= 4) oder mit anderen Worten ausgedrückt, gibt sie uns die Anzahl der Kohlenstoffatome an. Daraus kann man sofort erkennen, dass man im Fall des Butadiens eine 4x4 - Matrix erhält. Die dritte Zeile zeigt uns die Ladung des Moleküls, die in unserem Fall gleich 0 gesetzt ist. Die Ladung des Moleküls wird zur Berechnung der Besetzungszahlen und der Gesamtenergie verwendet. Von der vierten bis zur zehnten Zeile werden die meisten Elemente der Matrix aufgefüllt. Die erste Ziffer entspricht der Zeile der Matrix (i), die zweite Ziffer entspricht der Spalte der Matrix (j). Die dritte Zahl entspricht im Fall der Nichtdiagonalelemente dem Resonanzintegral und im Fall der Diagonalelemente dem Coulombintegral. Die entsprechenden Werte besetzen die Position (i,j) der Matrix. 20 Von der vierten bis zu sechsten Zeile werden die Elemente der oberen Nebendiagonale mit dem reellen Wert 1.0 besetzt. Dieser Wert besitzt laut Aufgabestellung der Bachelorarbeit die Einheit β. Für eine CC-Bindung setzt man in der Regel β=1. Hinsichtlich der Konnektivität der Atome bedeutet das, dass zwischen den beiden Zentren eine Bindung besteht. Der Wert 1.0 entspricht dem Zahlenwert des Betrags des Resonanzintegrals einer C-C -Bindung. Von der siebten bis zum zehnten Zeile werden die Elemente der Hauptdiagonalen mit dem reellen Wert 0.0 aufgefüllt. Dieser Wert entspricht per definitionem dem Zahlenwert des Coulombintegrals eines Kohlenstoffatoms. Output-File Nachdem das Inputfile durch eine Methode eingelesen wurde, sollte eine Matrix die vorher mit Nullen vorbesetzt wurde, mit den Werten aus den Input-Files aufgefüllt werden. Anhand einer Spiegelung an der Hauptdiagonalen kann dann die untere Hauptdiagonale mit den gleichen Werten wie die obere Hauptdiagonale aufgefüllt werden. Man erkennt an den Elementen der Matrix ob es sich um ein zyklisches oder offenkettiges Molekül handelt. Wenn die Anfangs- und Endwerte mit dem reellen Wert 1.0 besetzt sind, dann handelt es sich um ein geschlossenes zyklisches Molekül, bei dem Wert 0.0 handelt es sich um ein offenkettiges Molekül. Danach sollte die Matrix unter Verwendung des Jakobi-Verfahrens diagonalisiert werden. Das Jacobi-Verfahren, das auch als Gesamtschritt-Verfahren bezeichnet wird ist ein lineares, stationäres Iterationsverfahren. Wenn man ein Gleichungssystem der Form A ∙ x = b, wobei A є R ⁿ*ⁿ, n ϵ N regulär ist mit direkter Löser die bei exakter Arithmetik nach endlich vielen Schritten die exakte Lösung x ergibt. Nachdem die Energieeigenwerte und ihre Eigenvektoren mit den entsprechenden Methoden berechnet worden sind, sollten diese Ergebnisse in einem Output-ASCIIFile gespeichert werden. So könnte ein solches Output-File aussehen: +++++++++++++++++++++++++++++++ HUECKELRECHNUNG FUER BUTADIEN 21 +++++++++++++++++++++++++++++++ ************** HUECKELMATRIX ************** 1 2 3 4 1 0,0000 1,0000 0,0000 0,0000 2 1,0000 0,0000 1,0000 0,0000 3 0,0000 1,0000 0,0000 1,0000 4 0,0000 0,0000 1,0000 0,0000 **************************** EINELEKTRONENENERGIENIVEAUS **************************** -1,6180 -0,6180 0,6180 1,6180 ********************************** GESAMTENERGIE = ALPHA +4,4721 BETA ********************************** ******************* KOEFFIZIENTENMATRIX ******************* 1 2 3 4 1 0,3717 -0,6015 -0,6015 -0,3717 2 0,6015 -0,3717 0,3717 0,6015 3 0,6015 0,3717 0,3717 -0,6015 4 0,3717 0,6015 -0,6015 0,3717 22 ************* DICHTEMATRIX ************* 1 2 3 4 1 1,0000 0,8944 0,0000 -0,4472 2 0,8944 1,0000 0,4472 0,0000 3 0,0000 0,4472 1,0000 0,8944 4 -0,4472 0,0000 0,8944 1,0000 ********************** FREIE VALENZ DER ATOME ********************** 1 2 3 4 0,33757 0,39036 0,39036 0,39757 Die Koeffizientenmatrix Molekülorbitale. enthält die LCAO-Koeffizienten der einzelnen Dabei gibt der Spaltenindex das Molekülorbital und der Zeilenindex das Zentrum im Molekül an. 1 1 0,3717 (𝑐11 ) 2 0,6015(𝑐21 ) 3 0,6015(𝑐31 ) 4 0,3717(𝑐41 ) 2 3 4 ∅1 = 0,3717 ∙ φ1 + 0,6015 ∙ φ2 + 0,6015 ∙ φ3 + 0,3717 ∙ φ4 23 Die Bedeutung der DICHTEMATRIX, die oft auch als Bondorder-Matrix bezeichnet wird, wird deutlich wenn man in den Ausdruck für die Energie eines Molekülorbitals +∞ ∅1∗ ℋ∅1 𝑑𝜏 𝜀1 = ∫ −∞ die LCAO-Entwicklung für ∅1 einsetzt. 𝑛 𝜀1 = ∑ 𝑛 ∑ 𝑘=1 𝑜𝑐𝑐 𝐻𝑘𝑙 ∑ 𝑙=1 𝑛𝑖 𝑐𝑘𝑖 𝑐𝑙𝑖 𝑖=1 𝑜𝑐𝑐 𝑝𝑘𝑙 = ∑ 𝑛𝑖 𝑐𝑘𝑖 𝑐𝑙𝑖 𝑖=1 𝑝𝑘𝑙 bezeichnet man als einen Element der Dichte- oder Bondordermatrix . Die Summe der Diagonalelemente 𝑝𝑘𝑘 ist gleich der Zahl der π-Elektronen am Zentrum k. 𝑛𝑖 ist die Besetzungszahl des i-ten MO’s und occ entspricht der Nummer des höchstens besetzten MO’s und 𝐻𝑘𝑙 ist das Element der HÜCKEL-Matrix. Daraus lässt sich dann die Gesamtenergie des π-Systems berechnen. In diesem Zusammenhang sei darauf hingewiesen, dass man bei alternierenden πElektronensystemen im Grundzustand für alle Diagonalelemente der Dichtematrix den Wert 1.0 erhält. Die Nicht-Diagonalelemente sind ein Maß für einen Bindungsgrad zwischen zwei Zentren. An dieser Stelle wäre die Programmierung mit der Programmiersprache Fortran-90 am Ende. Wie vorher bereits erwähnt wurde, sollen die Ergebnisse mit einen Plotter-Software gezeichnet werden. Zur Zeit ist geplant, hierfür die freie Gnu-Plotter-Software zu verwenden, aber es muss nicht unbedingt dieses Programm benutzt werden, es kann auch eine andere Software benutzt werden. Die Benutzung dieses Plotters erfordert eine Einarbeitung in seine Programmiersprache. Zurzeit wird in Betracht bezogen, dass der Fortran-90-OutputASCII-File von einem nachgeordneten Programm eingelesen wird. In diesem Programm sollen die Daten aus dem Outputfile in ein für den Plotter „verständliches“ Format umgewandelt werden. 24 So könnte der Energiegraph des Butadien-Moleküls aussehen: Und so kann eine Strichzeichnung des offenkettigen Moleküls Butadien aussehen: Quellenangaben: Zu der hier verarbeiteten Theorie: Vorlesung von Prof. Dr. Gerhard Raabe G. Raabe, Skript zur Vorlesung „Einführung in die Grundlagen der Theorie der Chemischen Bindung“ von Prof. Dr. Fleischhauer 25 26