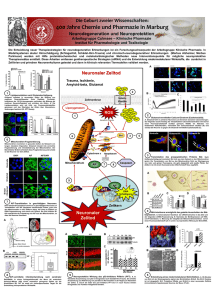
Glutamat und Neurotoxizität
Werbung

Glutamat und Neurotoxizität Stanislav Maksimov Teil I Glutamat und Glutamatrezeptoren Glutamat • Proteinogene Aminosäure • Dominierender excitatorischer Neurotransmitter im ZNS • Glu ist die Vorstufe des inhibitorischen Signalmoleküls GABA Glutamat Synthese GABA-Synthese aus Glu Ionotrope Glu-Rezeptoren Typen: • Kommen im ZNS • Tetra- und Pentamere • Leiten K+, Na+, Ca2+ NMDA • NR1, NR2A-D, NR3A AMPA • GluR1-4 Kainat • GluR5-7, KA1,2 Topologie von GluR-Ionenkanällen Membrantopologie Natives Kanal GluR-Zyklus Journal of Neuroscience 2007 Ionotrope Glu-Rezeptoren NMDAR • Binden Glu und Gly (co-Agonist) • Für die Aktivierung muss der Mg2+ block durch die Depolarisation entfernt werden (durch schnelle non-NMDAR) • Langsamere Kinetik als bei non-NMDAR • Spielen eine dominierende Rolle bei der Glu-vermittelten Neurotoxizität • Besitzen feine Regulationsmechanismen Teil II Glutamat-vermittelete Neurotoxizität (NT) Historisches • 1957: L-Glu-Injektionen zerstörten die innere Retinaschicht bei Mäusen (Lucas & Newhouse) • Glu-vermittelte NT wurde vom drastischen Anschwellen der Retinazellen gefolgt • Die Auswirkungen waren am stärksten bei den Zellen ausgeprägt, die Glu-R exprimierten • Die toxische Wirkung von GluR konnte durch die entsprechenden Antagonisten reduziert werden Komponenten der Glu-vernitteletn NT Frühe Phase: • Anschwellen von Zellen durch den verstärkten Na+Einstrom Spätere Phase: • Verstärkter (unkontrollierter) Ca2+-Einstrom führt zur Aktivierung zahlreicher zellulärer Antworten Zellschäden und -tod Ca2+ in einer Zelle • Einer der wichtigsten sekundären Botenstoffe • Reguliert zahlreiche Prozesse (Zellproliferation und –wachstum, Genexpression, Energiemetabolismus, Apoptose usw.) • Sehr niedrige intrazelluläre Konzentration (~ 0,1 µM) • Ca2+-Haushalt muss sehr streng kontrolliert werden „Source-specifity“-Hypothese • Toxische Wirkung von Ca2+ ist nicht unbedingt der [Ca2+]i direkt proportional • Ca2+-Einstrom über NMDAR führt zu einer stärkeren Toxizität als der über non-NMDAR • Der Weg des Ca2+-Eintritts ist wichtig • NMDAR sind mit Ca2+-sensitiven Elementen (Enzyme, Ca2+-bindende Proteine) assoziiert oder befinden sich in ihrer Nähe NMDAR und postsynaptische Dichte (PSD) • MAGUKs (Klasse der PSD-Proteine) kommen in großen Mengen in Hirnsynapsen vor und sind in das Clustering der Membranrzeptoren involviert • NMDAR sind mit spezifischen PSDProteinen assoziiert (u.a. mit dem Factin) • PDZ-Domänen von PSD-95, können mit NMDAR und nNOS interagieren (Scaffold-Funktion) • NOS kann durch Ca2+ aktiviert werden Auswirkung der Glu-NT auf Mitochondrien • Mitochondrien können viel Ca2+ aufnehmen • Bei übermäßiger Ca-Aufnahme bricht das elektrochemische H+-Potential über die innere Mitochondrienmembran zusammen und die ATPSynthese wird runter reguliert • Störungen in der Elektronentransportkette führen zur erhöhten ROS-Produktion (z.B. O2-) ROS in Glu-abhängigen NT • O2- und NO reagieren zu ONOO- (Peroxynitrit) • NO und ONOO- können Enzyme der Atmungskette inhibieren • ROS reagieren mit Lipiden, Proteinen und DNA • Aktivierung von ATP-verbrauchenden DNAReparaturenzymen => rascher Verbrauch der Energiereserven • Wichtige Mediatoren der Glu-NT (direkte oder indirekte ) Glu-NT kann Apoptose induzieren • Cytochrom c tritt aus Mitochondrien aus und wird von Apaf1(apoptosis protease-activating factor) gebunden • Apaf-1 wird durch diese Bindung aktiviert und bildet Oligomere • Apaf-1 Oligomere rekrutieren Initiator-Procaspase 9 die sich gegenseitig aktivieren • Apoptosom (Apaf-1/Caspase9-Komplex) aktiviert Effektor-Caspase 3 • Caspase 3 spaltet Zytoskelett-Proteine und aktiviert DNase (DFF40/CAD), die ihrerseits DNA degradiert Alternative Induktion des programmierten Zelltods • Gehirnverletzung und ONOO--Behandlung sind mit dem Austritt von AIF (apoptosis inducing factor) aus den Mitochondrien assoziiert (normalerweise in Mitochondrienmatrix) AIF • ist in die Caspase-unabhängige Apoptose-Induktion involviert • ist mit DNA-Fragmentierung und ChromosomenKondensation assoziiert • verändert die Permeabilität von Mitochondrienmembran Ca2+-abhängige Toxizität Wann tritt die Glu-vermittelte NT auf • Bei mechanischen Schäden des Gehirns • Bei Schlaganfall • Bei Störungen der Gehirndurchblutung was u.a. zur Hypoxie führt (Ischämie) Therapieansätze Blockieren der Glu-Rezeptoren • inaktiviert Ionenkanäle => unterbindet Ca2+-Einstrom • nur bei akuten Fällen • kann nicht auf Dauer eingesetzt werden Entkopplung der Glu-Rezeptoren von den abwärts liegenden Signalelementen • Ionenkanäle bleiben Funktionsfähig • Ca2+-abhängige „dowstream signalling“ wird uneffizienter • Ca2+ kann immer noch in die Zelle gelangen => Nebenwirkungen möglich Offene Fragen • Welche [Ca2+]i ist für die Zelle toxisch? • Signalübertragungs-Komponente stromabwärts von NMDAR und die Signalweiterleitung • Beteiligung unterschiedlicher NMDAR an Glu-NT • Mechanismen der toxischen Wirkung von ROS Fragen? Kritik?