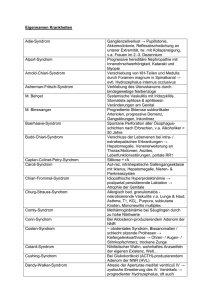
Dermatomyositis
Werbung

ADDITIONAL SLIDE KIT IDIOPATHISCHE MYOSITIDEN Autor: Dr. med. Guido Schwegler Naumburger, Schlieren Supervision: Prof. Dr. med. Matthias Sturzenegger, Bern Zur Verfügung gestellt durch:* CSL Behring AG Letzte Aktualisierung: November 2013 * Dieses Additional Slide Kit wurde von einem unabhängigen Team von Neurologen erstellt und dient ausschliesslich Informationszwecken. Vorwort Die korrekte Klassifikation von Myopathie-Syndromen gewinnt zunehmend an klinischer Relevanz angesichts der in den letzten Jahren verfügbaren neuen Therapieformen. Proximal betonte symmetrische Extremitätenparesen können Ausdruck eines genetischen Enzymdefektes sein, wie z.B. eines Mangels der sauren Maltase (alpha-Glukosidase). Diese GlykogenspeicherMyopathie ist durch Enzymersatz behandelbar. Ähnlich verteilte Paresemuster sind aber auch ein typisches Merkmal der Myositiden, die akut bis chronisch verlaufen können. Auch hier gibt es Formen die effizient zu behandeln sind: diese zu erkennen, ist die Kunst. Die Klassifikation der Myositiden ist im Fluss. Neue Ergebnisse zu antigenen Strukturen im Muskel und zu Autoantikörpern im Serum sowie zu immunogenetischen Mechanismen haben vor allem im Bereich der idiopathischen inflammatorischen Myopathien (IIM), einer Gruppe von seltenen, wahrscheinlich autoimmunen, Myositiden zu Erkenntnissen bezüglich Therapieantwort und Prognose geführt. Die Muskelbiopsie ist aber nach wie vor zur exakten Diagnostik unverzichtbar – auch hier haben immunhistochemische Methoden neue Erkenntnisse geliefert. Leider gibt es aufgrund der Seltenheit dieser Krankheitsbilder bezüglich effizienter Therapieverfahren nur sehr spärliche evidenzbasierte Daten, im Wesentlichen beschränkt auf die Dermatomyositis. In diesem Slide kit sollen Klinik, Diagnostik, Differentialdiagnostik und Therapie der Dermatomyositis (DM), Polymyositis (PM), Inclusion body myositis (IBM) und nekrotisierenden autoimmunen Myositis (NAM) im Lichte der aktuellen Literatur vorgestellt werden. Prof. Dr. med. Mathias Sturzenegger IDIOPATHISCHE MYOSITIDEN 2 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 3 Gebrauchshinweise Ansichtsoptionen des Slide Kits Folien Folien Bildschirmansicht: Klicken Sie im Menü ‚Ansicht‘ auf ‚Normalansicht‘. Folien inkl. Notizen Folien und Notizenseiten mit Hintergrundinformationen Bildschirmansicht: Klicken Sie im Menü ‚Ansicht‘ auf ‚Notizenseite‘. IDIOPATHISCHE MYOSITIDEN 4 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 5 1. Definition Definition Idiopathische Myositiden (Synonym: Idiopathische inflammatorische Myopathien (IIM)) Definition: Heterogene Gruppe erworbener Myopathien mit folgenden Gemeinsamkeiten: Klinisch progrediente, meist symmetrische, Muskelschwäche und entzündliche Veränderungen in der Muskelbiopsie. Zu dieser Gruppe gehören: • Dermatomyositis • Polymyositis • Sporadische Einschlusskörperchenmyositis (Inclusion body Myositis) • Nekrotisierende autoimmune Myositis IDIOPATHISCHE MYOSITIDEN 6 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 7 2. Klassifikation Klassifikation der Myopathien allgemein Hereditäre Erworbene Muskeldystrophien Myositiden • Immunogen • Erregerbedingt Kongenitale Myopathien mit Strukturbesonderheiten Toxische Myopathien (z.B. Statine) Metabolische Myopathien Critical illness Myopathie • Mitochondriale • Glycogenosen • Lipidmyopathien Ionenkanalmyopathien Endokrine Myopathien (z.B. Hypo- oder Hyperthyreose) [Leitlinien DGN, 5. Auflage 2012] IDIOPATHISCHE MYOSITIDEN 8 2. Klassifikation Klassifikation der Myositiden Idiopathische Myositiden (IIM) Begleitmyositis immunologischer Systemkrankheiten Erregerbedingte Myositiden Sonderformen Dermatomyositis (DM) Mischkollagenose Bakteriell Eosinophile Myositis Polymyositis (PM) Systemischer Lupus erythematodes Parasiten (z.B. Trichinose) Makrophagische Myofasziitis Nekrotisierende autoimmune Myositis (NM oder NAM) Sjögren Syndrom Viral (z.B. CoxsackieViren) Granulomatöse Myositis Sporadische Einschlusskörperch en-myositis (sIBM) Rheumatoide Arthritis Mykotisch Fokale oder noduläre Myositis Overlap syndrome (OS) [DGN Leitlinien, 5. Auflage] [The inflammatory myopathies, LJ Kagan, 2009] IDIOPATHISCHE MYOSITIDEN 9 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 10 3. Epidemiologie Epidemiologie Inzidenz der idiopathischen Myositiden 1:100’000 Sie stellen damit die weitaus grösste Gruppe erworbener, behandelbarer Myopathien dar, sowohl im Kindes- (v.a. DM), wie auch im Erwachsenenalter (sIBM, DM). [Dalakas, 2011a, Dimachkie, 2012 b] Dematomyositis (DM) ist die häufigste IIM bei jungen Erwachsenen. Sporadische Inclusion Body Myositis (sIBM) • Häufigste Form der IIM bei > 50-jährigen • Prävalenz: Niederlande: 4.9/1 Mio; Australien: 9.3; USA: 70 (age adjusted) IDIOPATHISCHE MYOSITIDEN 11 3. Epidemiologie Epidemiologie Häufigkeit der Myositiden im Vergleich Dermatomyositis und sIBM >> Polymyositis/nekrotisierende Myositis Dermatomyositis s IBM NM PM Greis Kind 50 Jahre Manifestationsalter und Häufigkeit IDIOPATHISCHE MYOSITIDEN 12 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 13 4. Klinik Klinik Dermatomyositis Polymyositis sIBM Nekrotisierende Myositis Frauen-Männer 2:1 2:1 1:3 1:1 Erkrankungsalter 5-15 // 45-65 >18 >50 >18 Proximal symmetrisch Paresemuster Proximal symmetrisch Proximal symmetrisch Asymmetrisch Quadriceps, Unterarmflexoren, Fusssenker Progressionsgeschwindigkeit ++ + (+) ++ Hautveränderungen + - - - Assoziation mit Paraneoplasie Ja Fraglich Nein Ja In Anlehnung an [DGN Leitlinien, 2012] IDIOPATHISCHE MYOSITIDEN 14 4. Klinik Klinik Dermatomyositis Polymyositis sIBM Nekrotisierende Myositis Myalgien Häufig Selten Nein häufig Muskelatrophien (+) + ++ + CK normal bis 50-fach erhöht bis 50-fach bis 10-fach bis 50-fach Assoziation mit Kollagenosen + (+) - (+) Ansprechen auf Immuntherapie ja ja Selten ja In Anlehnung an [DGN Leitlinien, 2012] IDIOPATHISCHE MYOSITIDEN 15 4. Klinik Klinik der Dermatomyositis Hautbefall Amyopathische Dermatomyositis Muskelbefall Dermatomyositis Adermatopathische Dermatomyositis Typische Muskelbiopsie mit perivaskulären/perimysialen Infiltraten und perifaszikulärer Atrophie. Gefässgebundener Autoimmunprozess. IDIOPATHISCHE MYOSITIDEN 16 4. Klinik Klinik der Dermatomyositis Muskelbefall Proximales Myopathie-Syndrom • Schulter- und Beckengürtel • Quadriceps • Oberarme • Nackenmuskeln • Symmetrisch • Manchmal Myalgien IDIOPATHISCHE MYOSITIDEN 17 4. Klinik Klinik der Dermatomyositis Rash und poikilodermes Exanthem mit typischer Verteilung • V-Sign (Decolletée, s. nebenan) • Shawl-Sign (Schal, im Nacken) • Heliotropes livides Lidödem • Gottron-Papeln (über Metacarpophalangeal und proximalen Interphalangealgelenken) 45 jährige Patientin mit subakuter Dermatomyositis: Ausgeprägtes V-sign. [Dalakas und Hohlfeld, 2003] [The inflammatory myopathies, 2012] IDIOPATHISCHE MYOSITIDEN 18 4. Klinik Klinik der Dermatomyositis Hautbefall 45-jährige Patientin: Subakute Dermatomyositis, mit lichenoid verdickter und papulös auslaufendem Exanthem am Handrücken. Exkoriationen als Zeichen des assoziierten Pruritus. Dieselbe Patientin: Man beachte die vielfältigen, nicht uniformen Aspekte des Exanthemes am proximalen Oberschenkel: Poikiloderm. IDIOPATHISCHE MYOSITIDEN 19 4. Klinik Klinik der Dermatomyositis Verlauf Variables Ausmass an Muskelschwäche Wenig Atrophie Tetraparese Ablassung des Exanthemes «Mechanikerhände» subcutane Calcinose Rash, Exanthem Konventionelles Röntgen: subkutane Kalzinose [aus Dalakas, Hohlfeld, 2003] IDIOPATHISCHE MYOSITIDEN 20 4. Klinik Klinik der Dermatomyositis Sonderformen der Dermatomyositis Häufigkeit Tumor- assoziiert (paraneoplastisch) Dermatomyositis kann dem Tumornachweis bis 2 Jahre vorausgehen Männer: Kleinzelliges Lungen-Ca Frauen: Ovarial-Ca 15-25%* Juvenile Dermatomyositis** Wie adulte Dermatomyositis, aber mehr extramuskuläre Manifestationen • Muskelkontraktionen (Spitzfuss) • Subkutane Kalzinose • Krankheitsgefühl («Misery») • Gastrointestinale Vaskulitis • Lipodystrophie • Arthritis • … Anti-Synthetase-Ak-Syndrom (Jo-1, Anti-PL7,…) - Myositis plus Interstitielle Pneumopathie 10-25% *[Dimachkie, Barohn, 2012] ** [Dalakas, Hohlfeld, 2003] IDIOPATHISCHE MYOSITIDEN 21 4. Klinik Klinik der Dermatomyositis Dermatomyositis und Polymyositis assoziierte Krankheiten und Antikörper Autoimmune Krankheiten Antikörper Overlap Syndrom (v.a. Dermatomyositis assoziiert) • Sharp Syndrom • Systemische Sklerose (SS) Kollagenosen • Systemischer Lupus erythematodes In 5-8% assoziiertes Polymyositis-Syndrom • Sjögren ……. anti-U1-RNP anti PML-SC, anti-Scl-70 ……. ANA anti-native DNA, Anti-Sm… anti-SSA, anti-SSB *[The inflammatory Myopathies, 2011] ** [Dalakas, Hohlfeld, 2003] IDIOPATHISCHE MYOSITIDEN 22 4. Klinik Klinik der Polymyositis Muskelbefall Proximales Myopathie-Syndrom • Schulter- und Beckengürtel • Quadriceps • Oberarme • Nacken (Kopfflexoren) • Symmetrisch • Oft schmerzlos IDIOPATHISCHE MYOSITIDEN 23 4. Klinik Klinik der Polymyositis Polymyositis Verlauf Progredient über Wochen und Monate Paresemuster Klassisches Myopathiesyndrom: proximal symmetrisch Extramuskuläre Symptome Nur wenn Teilsymptom einer systemischen autoimmunen Erkrankung Inzidenz Sehr selten IDIOPATHISCHE MYOSITIDEN 24 4. Klinik Klinik der sporadischen Inclusion Body Myositis (sIBM) Muskelbefall (Paresemuster) Typisch: distale OE: Unterarme • Fingerbeuger • Handgelenksbeuger • Fingerflexoren deutlich mehr betroffen als Extensoren. Typisch: proximale UE: • Quadricepsbefall prominent • Quadrizeps-Beteiligung oft viel stärker als Hüftflexoren Typisch: oft asymmetrisch Typisch: ausgeprägte Atrophien Dysphagie in bis zu 70 % Andere Muskeln variabel stark mitbetroffen IDIOPATHISCHE MYOSITIDEN [Needham und Mastaglia, 2007] 25 4. Klinik Klinik der sporadischen Inclusion Body Myositis (sIBM) • CK leicht erhöht oder normal • Keine pulmonale oder kardiale Beteiligung • Keine Assoziation mit Neoplasien • Seltene Assoziation mit Kollagenosen (SLE, Sjögren, Sarkoidose, in ca. 15%) • Alter > 50 J. • M:F = 3:1 • Schmerzlos Typische Atrophie der Handgelenk- und Fingerbeuger mit Dellenbildung am medialen Unterarm (Pfeil) [Needham und Mastaglia, 2007] IDIOPATHISCHE MYOSITIDEN 26 4. Klinik Klinik der sporadischen Inclusion Body Myositis (sIBM) Leitsymptome der sporadischen Inclusion body Myositis • Extrem chronischer Verlauf (Jahrzehnte!) • Quadricepsatrophie 80-jähriger Patient mit schweren Atrophien der Kniestrecker. Ursache ist eine sIBM. IDIOPATHISCHE MYOSITIDEN 27 4. Klinik Diagnosekriterien der sIBM Modified Diagnostic Criteria 2008 Pathologisch definierte Einschlusskörpermyositis • Gemäss den Kriterien von Griggs: Invasion nicht-nekrotischer Fasern durch mononukleäre Zellen und „rimmed vacuoles" (umrandete Vakuolen), sowie entweder intrazelluläre Amyloidablagerungen oder 15-18 nm grosse filamentöse Einschlüsse Klinisch definierte Einschlusskörpermyositis • • Klinische Merkmale • Dauer der Schwäche > 12 Monate • Alter > 35 Jahre • Schwäche der Fingerbeuger > Schulterabduktion UND Kniestrecker > Hüftbeuger Pathologische Merkmale • Invasion nicht-nekrotischer Fasern durch mononukleäre Zellen und „rimmed vacuoles" oder erhöhte • MHC-1, aber keine intrazellulären Amyloidablagerungen oder 15 bis 18 nm grosse filamentösen Einschlüsse [Aus Hilton-Jones D, Miller A, Parton M, et al. Inclusion body myositis. Neuromuscul Disord 2010;20(2):142–147] IDIOPATHISCHE MYOSITIDEN 28 4. Klinik Diagnosekriterien der sIBM Modified Diagnostic Criteria 2008 Mögliche IBM • Klinische Merkmale • Dauer der Schwäche > 12 Monate • Alter > 35 Jahre • Schwäche der Fingerbeuger > Schulterabduktion ODER Kniestrecker > Hüftbeuger • Pathologische Merkmale • Invasion nicht-nekrotischer Fasern durch mononukleäre Zellen und „rimmed vacuoles" oder erhöhte • MHC-1, aber keine intrazellulären Amyloidablagerungen oder 15 bis 18 nm grossen filamentösen Einschlüsse [Aus Hilton-Jones D, Miller A, Parton M, et al. Inclusion body myositis. Neuromuscul Disord 2010;20(2):142–147] IDIOPATHISCHE MYOSITIDEN 29 4. Klinik Klinik der nekrotisierenden autoimmunen Myositiden (NAMs) Proximales Myopathiesyndrom • Schulter- und Beckengürtel • Quadriceps • Oberarme • Symmetrisch • Myalgien meist fehlend oder gering • CK hoch bis sehr hoch (median 2000 U/l)* • Meist rasch progredient * [Ellis et al., 2012] IDIOPATHISCHE MYOSITIDEN 30 4. Klinik Klinik der nekrotisierenden autoimmunen Myositis (NAM) Sonderformen der nekrotisierenden Myositis • Statininduzierte NAM (SANAM) • Progression der Myopathie nach Absetzen der Statine! Selten auch erst nach Absetzen der Statine Beginn einer nekrotisierenden Myopathie Paraneoplastische NAM • • SRP-Antikörper assoziierte NAM (Signal recognition particle) • Subakute Myopathie mit Pipestem Kapillaren Systemische Vaskulitis/Cardiomyopathie Adenokarzinom Rasch progredient, schwer verlaufend [Dimachkie and Barohn, 2011] IDIOPATHISCHE MYOSITIDEN 31 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 32 5. Diagnose Diagnose-Verfahren IDIOPATHISCHE MYOSITIDEN 33 5. Diagnose Elektromyographie Dermatomyositis, Polymyositis, sIBM und NAM zeigen ein ähnliches Bild im EMG Spontanaktivität pathologisch Positive scharfe Wellen, Fibrillationen, komplex repetitive Entladungen Motorische Einheiten myopathisch Polyphasierate↑ Dauer↓ Amplitude↓ Rekrutierung myopathisch Schon bei geringer Innervation viele verschiedene motorische Einheiten Interferenzmuster myopathisch Dichtes Interferenzmuster Amplitude↓ (<2 mV) IDIOPATHISCHE MYOSITIDEN 34 5. Diagnose Creatininkinase (CK) Metabolische(systemi sch) Myopathien Myositiden Dysthyreose, Alkoholismus Toxisch, mechanische Myopathien(Rhabdom yolysen) Trauma, Sport, viral, medikamentös (Fibrate, Statine) Serum Creatininkinase ↑ Metabolische Myopathien Motoneuronerkrankungen (McArdle’s disease, Myoadenylat-DeaminaseMangel….) IDIOPATHISCHE MYOSITIDEN 35 5. Diagnose Antikörper Antikörper Klinisches Syndrom Besonderes Anti MI-2 Dermatomyositis Juvenile Dermatomyositis Paraneoplastische Dermatomyositis Anti-Jo1 Anti-Synthetase Syndrom Arthritis, Interstitielle Pneumopathie, (Dermato-)Myositis, RaynaudSyndrom Anti-PL7 Anti-PL12 Anti-OJ Anti-EJ Anti-KS …… Anti-Synthetase Syndrom Interstitielle Pneumopathie Myositis, plus….. Anti-SRP Nekrotisierende Myopathie mit systemischer Beteiligung Klinisch wenig relevante AK IDIOPATHISCHE MYOSITIDEN 36 In ca. 35% bei Nekrotisierender autoimmuner Myositis nachweisbar 5. Diagnose MRI MRI Oberschenkel: Chron. Polymyositis mit fettigem Umbau und Atrophie des gesamten Quadriceps (ventral,Pfeil) bei intakten „hamstring“(dorsal) (axial T1 ohne KM) [aus Schulze et al, 2009] MRI Oberschenkel: Bekannte Dermatomyositis mit erhöhter Signalintensität gewisser Muskeln („Myositis“) (insbesondere Vastus lat.) und auch erhöhtem Signal des subcutanen Bindegewebes(„Dematitis“) (Pfeil re). Axial STIR. [aus Schulze et al, 2009] IDIOPATHISCHE MYOSITIDEN 37 5. Diagnose Biopsie Diagnostisches Hauptinstrument, die offene Muskelbiopsie Pitfalls Lösungsansatz Falscher Muskel: • zu stark betroffen • zu wenig betroffen Vorbehandlung mit Steroiden Pathologe mit fehlender Expertise MRI basierende Auswahl des Zielmuskels Biopsie zeitlich forcieren Zusammenarbeit mit Referenzzentren IDIOPATHISCHE MYOSITIDEN 38 5. Diagnose Biopsie Biopsie Unterscheidung zwischen Resultat Dermatomyositis Polymyositis Einfach Dermatomyositis sIBM/NAM Einfach Polymyositis sIBM Schwierig, v.a. im Spätstadium Fehleranfällig Oft Zweitbiopsien nötig NAM sIBM/DM/PM Meist einfach Polymyositis, NAM, sIBM Hereditäre Muskeldystrophien mit Entzündungszeichen Schwierig, Spezialfärbungen (Immunhistochemie, etc.) nötig; aber klinisch seltene Fragestellung [Dalakas, 2011a] IDIOPATHISCHE MYOSITIDEN 39 5. Diagnose Muskelbiopsie Dermatomyositis: Typisches Verteilmuster der entzündlichen Infiltrate: perifaszikulär (schwarze Pfeile) und perivaskulär Im Zentrum des Faszikels gut erhaltene Muskelstruktur ohne entzündliche Infiltrate. [Quelle: Dalakas und Hohlfeld, 2003] IDIOPATHISCHE MYOSITIDEN 40 5. Diagnose Biopsie Sporadische Inclusion body Myositis: A) Entzündliche Infiltrate in myopathisch veränderter Muskelarchitektonik, zahlreiche „rimmed vacuoles“ B) Rimmed vacuole (→) C) CD8+ Lymphozten D) Homogene MHC I Expression an der Oberfläche nicht betroffener Muskelfasern [Needham und Mastaglia, 2007] IDIOPATHISCHE MYOSITIDEN 41 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 42 6. Differentialdiagnose Differentialdiagnose Dermatomyositis Differentialdiagnose Dermatomyositis mit geringem oder fehlendem Hautbefall Entzündliche Myopathien Polymyositis Nekrotisierende autoimmune Myositis Kollagenosen (besonders SLE) Anti-Synthetase Syndrome Sarkoidose Toxische oder metabolische Myopathien Statinmyopathie, Amiodarone Alkohol Steroidmyopathie Dysthyreose ….. Neuromuskuläre Transmissionsstörungen Myasthenia gravis Lambert Eaton Syndrom Neuropathien Guillain Barré Syndrom CIDP (Chron. Inflammatorische demyelinisierende Polyneuroradikulitis) IDIOPATHISCHE MYOSITIDEN 43 6. Differentialdiagnose Differentialdiagnose sporadische Inclusion body myositis Engere Differentialdiagnose der sIBM Polymyositis Klinisch und histologisch oft schwierig gegeneinander abzugrenzen sIBM sehr viel häufiger Motoneuronkrankheiten • Amyotrophe Lateralsklerose, insbes. Varianten mit unterem Motoneuronbefall EMG wegweisend Bei geringstem Zweifel: Biopsie Hereditäre Myopathien • Fazioskapulohumerale MD • Myotone Dytrophie Curschmann Steinert • Myofibrilläre MD • ……….. Genetik! Evtl. Biopsie Morbus Pompe behandelbar IDIOPATHISCHE MYOSITIDEN 44 6. Differentialdiagnose Differentialdiagnose sporadische Inclusion body myositis Die beiden häufigsten Muskeldystrophien mit Manifestation im späteren Erwachsenenalter: • Myotone Dystrophie Curschmann Steinert • Fazioskapulohumerale Muskeldystrophie (FSHD) Die FSHD ist sehr variabel im Phänotyp! Typische Schulterpartie bei FSHD: Man beachte die Asymmetrie der Trapeziusatrophie, Poly-hill Sign (↓) [Pradhan, 2002; Hassan et al., 2012] IDIOPATHISCHE MYOSITIDEN 45 6. Differentialdiagnose Differentialdiagnose nekrotisierende autoimmune Myositis Myotoxizität der Statine: verschiedene Pathomechanismen Art der Statin-Myotoxizität Therapie Hyper-CK-emia (CK < 2000) Asymptomatisch Beobachten; Statin absetzen nicht zwingend Myalgie mit oder ohne CK-Erhöhung Statin absetzen. Karenzfrist von 2-3 Monaten. Reexposition mit weniger myotoxischem Statin Muskelschwäche plus CK-Erhöhung ohne Inflammation Statin absetzen Muskelschwäche plus CK-Erhöhung mit Inflammation: Statin-induzierte nekrotisierende autoimmune Myositis Statin absetzen Therapie mit Steroiden (?), intravenösen Immunglobulinen (?) Rhabdomyolyse (CK > 10’000) Statin absetzen Adaptiert nach [Dalakas, 2009] IDIOPATHISCHE MYOSITIDEN 46 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 47 7. Pathophysiologie Pathophysiologie Polymyositis • Primärer Angriffsort: Muskelfaser Dermatomyositis • • • Primärer Angriffsort Vaskulär: Endothel der endomysialen Kapillaren Humorale Autoimmunität (Antikörper, Komplement) T-Zell-vermittelt (CD8) Inclusion body Myositis • • • IDIOPATHISCHE MYOSITIDEN 48 Primärer Angriffsort: Muskelfaser T-Zell-vermittelt (CD8) Zusätzlich degenerativer Prozess (Protein Dysregulation) 7. Pathophysiologie Dermatomyositis Kleingefässvaskulitis des Muskels, ischämische Muskelfaserschädigung Adaptiert nach [Dalakas und Hohlfeld, 2003] IDIOPATHISCHE MYOSITIDEN 49 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 50 8. Therapie Therapie Generell unterschiedliches Ansprechen der IIM auf immunsuppressive Therapie und intravenöse Immunglobuline Myositis Ansprechen auf Therapie Dermatomyositis ++ Polymyositis, Autoimmune nekrotisierende Myositis + Sporadische Inclusion body Myositis -/(+) Keine Zulassungsstudien vorhanden. Alle eingesetzten Immuntherapeutika sind off label. IDIOPATHISCHE MYOSITIDEN 51 8. Therapie Dermatomyositis, Polymyositis, Nekrotisierende autoimmune Myositis First Line Initialtherapie 0-4 Wochen Erhaltungstherapie 1-12 Monate Langzeittherapie >1 Jahr Prednison 60-100 mg Prednison absteigend bis zur Cushingschwelle: jeden 2. Tag 15 mg Jeden 2. Tag ≤15 mg Azathioprin Intravenöse Immunglobuline Methotrexat Mycophenolat Mofetil Azathioprin Intravenöse Immunglobuline Methotrexat Mycophenolat Mofetil Add on Therapie («Steroide sparen») [Leitlinen DGN, 2012; Dimachkie und Barohn, 2012; Dalakas, 2011b] IDIOPATHISCHE MYOSITIDEN 52 8. Therapie Dermatomyositis, Polymyositis, Nekrotisierende autoimmune Myositis Osteoporose Prophylaxe nicht vergessen! Prednison ≥ 5 mg > 3 Monate Calcium ≥ 1 g/d Vitamin D 800-1200IE/d + Biphosphonat Sofern T-score* unter -1.5 oder T-score <1.0 plus 2 von 3 RF *T-score: Ausmass der Osteopenie in der Osteodensitometrie Risikofaktoren: ≥20 mg Prednison/d, Alter >50, postmenopausal Adaptiert gemäss: www.rheuma-net.ch IDIOPATHISCHE MYOSITIDEN 53 8. Therapie Therapie Dermatomyositis, Polymyositis, Nekrotisierende autoimmune Myositis Prednison hochdosiert Nach 1-2 Monaten keine Verbesserung Diagnose überprüfen Intravenöse Immunglobuline Prednison rascher als gewöhnlich ausschleichen (?) [Dalakas, 2011b] IDIOPATHISCHE MYOSITIDEN 54 8. Therapie Dermatomyositis, Polymyositis, Nekrotisierende autoimmune Myositis Second Line Therapie Add On Therapie zu Prednison Medikament Startdosis Maximaldosis Erhaltungsdosis Wirkungseintritt Azathioprin 2-3 mg/kgKG 3 mg/kgKG 1-3 mg/Kg KG 3-6 Monate Intravenöse Immunglobuline 2 g/KgKG Verteilt auf 2-5 Tage (ja nach Präparat) 2 g/kgKG alle 3-4 Wochen 1-2 g/KgKG alle 48 Wochen Innert 3-10 Tage Methotrexat 7.5 mg/Woche (i.m) 30 mg/Woche (i.m./i.v.) 7.5-15 mg/Woche 4-6 Wochen Mycophenolat Mofetil 2 x 500 mg 2 x 1500 mg 2 x 1000 mg 1-2 Monate Therapiedurchführung www.rheuma-net.ch [Dimachkie und Barohn, 2012; Dalakas, 2011b] IDIOPATHISCHE MYOSITIDEN 55 8. Therapie Dermatomyositis, Polymyositis, Nekrotisierende autoimmune Myositis Hoch aktive Verläufe/Therapie-Nonresponder First Line Bei sehr aktiven Verläufen Non Responder Initialtherapie 0-4 Wochen Erhaltungstherapie 1-12 Monate Langzeittherapie >1 Jahr Methylprednisolon i.v. 5 x 1000 mg/d Intravenöse Immunglobuline Prednison Absteigend bis zur Cushingschwelle jeden 2. Tag 15 mg Prednison Jeden 2. Tag ≤15 mg Intravenöse Immunglobuline (2g/kg Körpergewicht) Intravenöse Immunglobuline Intravenöse Immunglobuline Rituximab Ciclosporin, Mycophenolat mofetil, Cyclophosphamide TNFα – Blocker (Etanercept) Rituximab Ciclosporin, Mycophenolat mofetil, Cyclophosphamide TNFα – Blocker (Etanercept) Andere 3. Line Substanzen [Leitlinen DGN, 2012; Dimachkie und Barohn, 2012] IDIOPATHISCHE MYOSITIDEN 56 8. Therapie Dermatomyositis, Polymyositis, Nekrotisierende autoimmune Myositis Individuelle Therapieversuche bei ungünstigen klinischen Verläufen unter First- oder Second Line Therapie 3rd Line Therapie Dosis Studienlage Rituximab (Ocrelizumab)* 2 x 1 g (Tag 0 und 15) + Alemtuzumab** 0.3mg/kg Tag 0,1,2,3 (+) Ciclosporin 5 mg/kgKG (Spiegel 100-300 ng/ml) (+) Etanercept*** 50 mg/Woche Cyclophosphamid 0.7-1g/m2 + (+) Tacrolimus, Rapamycin (+) ……. *[Kosmidis und Dalakas, 2010; Ibrahim et al, 2012] **[Mann und Vencovscy, 2011] ***[Muscle Study Group, 2011] IDIOPATHISCHE MYOSITIDEN 57 8. Therapie Sporadische Inclusion body Myositis (sIBM) Steroide und andere Immunsuppressiva sind meistens nicht wirksam! Es wurden sogar beschleunigte Verläufe unter Immunsuppressiva beschrieben. Mögliche Ursachen des weitgehend fehlenden Effektes der Steroide und anderer immunregulatorischer Strategien: • Zu kurze Therapiedauer (Studien) • Diagnose meist erst nach vielen Jahren Krankheitsdauer • Sehr langsamer Krankheitsverlauf • Neurodegenerative Pathomechanismen 6 Monate Therapie mit intravenösen Immunglobulinen* Falls Therapieeffekt nachweisbar (Zunahme der Kraft, der Mobilität, Abnahme der Dysphagie) -> Weitere Zyklen mit intravenösen Immunglobulinen *Achtung: Off label use [Needham und Mastaglia, 2007; DGN Leitlinien 2012] IDIOPATHISCHE MYOSITIDEN 58 8. Therapie Erfolgsbeurteilung (Monitoring) • Es sollen, wenn immer möglich, zu Beginn einer Therapie die Kriterien zur Beurteilung eines Therapieerfolges definiert werden; dies ist wichtig, wenn es darum geht, Nebenwirkungen in Kauf zu nehmen oder, bei fehlender klinischer Effizienz, auf eine andere Strategie zu wechseln. • Primär sollen klinische Kriterien (Muskelkraft, (z.B. Arme über Kopf heben, Treppensteigen), Muskelschmerzen) beurteilt werden. • Aber auch Laborwerte im Verlauf, wie die CK und allfällige systemische Entzündungsparameter sind zuverlässige Kriterien zur Beurteilung des Ansprechens auf eine Therapie. • Spontanaktivität im EMG sollte bei Therapieansprechen verschwinden. Ist bei im Verlauf zunehmenden Paresen keine Spontanaktivität vorhanden, sollte die Möglichkeit einer steroidinduzierten Myopathie erwogen werden. • Die MRT ist bezüglich Aktivitätsbeurteilung einer Myositis noch wenig erforscht. IDIOPATHISCHE MYOSITIDEN 59 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 60 9. Prognose Prognose Dermatomyositis, Polymyositis und nekrotisierende autoimmune Myositis Remission ohne Erhaltungsimmunsuppressive Therapie: Selten! Ausnahme juvenile Dermatomyositis Remissionen/stable disease in Dermatomyositis und Polymyositis 20-40% Rest: schleichende Progression trotz Therapie • Schlechte Prognose • • Mortalität (Dermatomyositis und Polymyositis) Statin induzierte nekrotisierende autoimmune Myositis (SANAM) Paraneoplastische Myositiden Assoziierte interstitielle Pneumopathie 2-3-fach erhöht (pulmonale, kardiale, infektiöse, maligne Komplikationen) [Dimachkie und Barohn, 2012] IDIOPATHISCHE MYOSITIDEN 61 9. Prognose Sporadische Inclusion body Myositis Sporadische Inclusion body Myositis Progressionstempo Langsam über 5-20 Jahre Gehhilfe ~ 5 Jahre nach Beginn Rollstuhl ~ 10-15 Jahre nach Beginn Dysphagie Häufig im Verlauf Funktionell am meisten betroffen Beine Mortalität Nicht erhöht [www.neuromuscular.wustl.edu] IDIOPATHISCHE MYOSITIDEN 62 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 63 10. Ausblick Ausblick Studien mit monoklonalen Antikörpern Alemtuzumab Anti CD52 B und T-Zell-Depletion Rituximab Anti CD 20 B-Zelldepletion Eculizumab Gegen Komplement (C5) gerichtet Anti-……….. [Dalakas, 2011b] IDIOPATHISCHE MYOSITIDEN 64 Inhalt 1. Definition Seite 06 2. Klassifikation 08 3. Epidemiologie 11 4. Klinik 14 5. Diagnose 33 6. Differentialdiagnose 43 7. Pathophysiologie 48 8. Therapie 51 9. Prognose 61 10. Ausblick 64 11. Referenzen 66 IDIOPATHISCHE MYOSITIDEN 65 11. Referenzen Referenzen Amato AA, Barohn RJ. J Neurol Neurosurg Psychiatry 2009; 80: 1186– 1193 Needham M and Mastaglia FL, Lancet Neurol 2007;6:620-31 Pradhan S. Muscle Nerve 2002;25(5):754-5 Dalakas MC and Hohlfeld R. Lancet 2003;362:971-82 Dalakas MC. J Neurol Neurosurg Psychiatry 2009;80:832-38 Rothwell S, Cooper RG, Lamb JA, Chinoy H. Curr Opin Rheumatol 2013, 25:735–741 Dalakas MC. Neuropathology and Applied Neurobiology 2011(a);37:226–242 Tansley SL, Betteridge ZE, McHugh NJ. Curr Opin Rheumatol 2013, 25:772–777 Dalakas MC. Curr Opin Neurol 2011(b);24:457-62 The inflammatory Myopathies, editor Lawrence J Kagan, Humana Press 2009 Dimachkie MM and Barohn RJ. Semin Neurol 2012;32:227-236 (IIM) Schmidt J and Dalakas MC. Exp Opin Med Diagn 2010;4:241-50 Dimachkie MM and Barohn RJ. Semin Neurol 2012;32:237-245 (IBM) Schoser B. Z Rheumatol 2009;68:665-677 Ellis E et al. Muscle Nerve 2012;45(2):189-194 Schulze M et al, AJR 2009; 192:1708–1716 Ernste CF, Reed AM. Mayo Clin Proc 2013; 88 (1): 83-105 www.rheuma-net.ch (Therapieempfehlung der Schweizerischen Gesellschaft für Rheumatologie SGR) Fernandez C et al. Neurology 2006;66:1585-87 Fernandez C, Bardin N, De Paula AM, et al. Medicine 2013; 92: 15-24 www.neuromuscular.wustl.edu Hassan L et al, Muscle Nerve 2012;46(3):421-5 Ibrahim H et al, J Clin Neuromuscul Dis 2010;12:91-102 Kosmidis ML and Dalakas MC, Ther Adv Neurol Disord 2010;3:93-105 Leitlinien der DGN, 5. Auflage, 2012 (Myositis) Mann HF and Vencovscy J, Curr Opin Rheumatol 2011;23:605-11 Mohassel P and Mammen AL. Muscle Nerve 2013; epub ahead Muscle study group. Ann Neurol 2011;70:427-36 IDIOPATHISCHE MYOSITIDEN 66