V06_ADMEmodel
Werbung
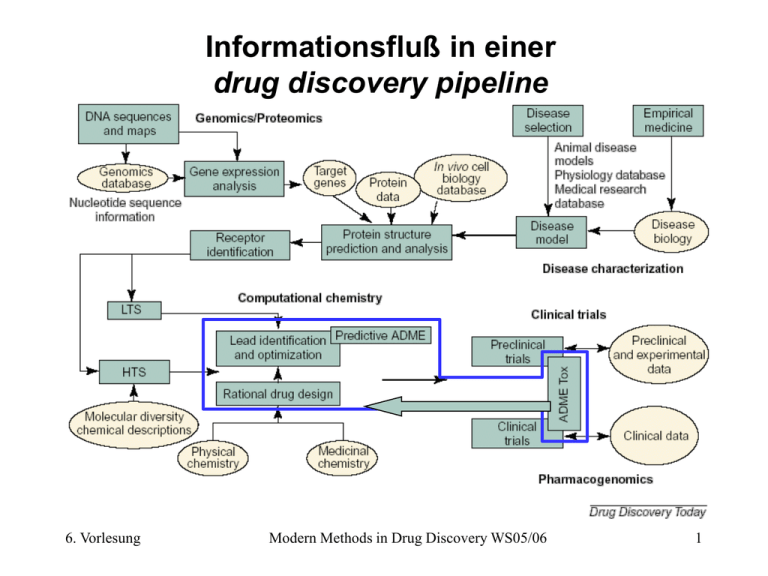
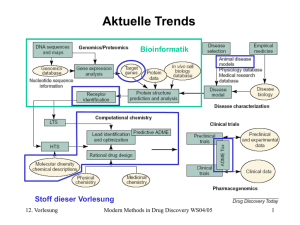
Informationsfluß in einer drug discovery pipeline 6. Vorlesung Modern Methods in Drug Discovery WS05/06 1 eADMET Prediction early Absorption Distribution Metabolism Elimination Toxicology 6. Vorlesung Pharmacokinetic Bioavailability Modern Methods in Drug Discovery WS05/06 2 ADME Modelle (I) Folgende Modelle werden für das in silico design benötigt Primäre Modelle Sekundäre Modelle Löslichkeit intestinale Absorption Bioverfügbarkeit Metabolische Stabilität Blut-Hirn-Schranke Permeation Mutagenizität Cardiatische Toxizität (hERG) Plasmaprotein Bindung Transport (Aufnahme und Efflux) Allgemeine Toxizität Hepatotoxizität (PXR, CAR) Nephrotoxizität Immunogenizität Neurotoxizität (Rezeptorbindung) Drug-Drug Wechselwirkungen (Cytochrom P450) 6. Vorlesung Modern Methods in Drug Discovery WS05/06 3 ADME Modelle (II) 6. Vorlesung Modern Methods in Drug Discovery WS05/06 4 Warum ist die Voraussage der ADME Parameter so wichtig ? Gründe die zum Fehlschlag eines potentiellen Wirkstoffs führen 6. Vorlesung Modern Methods in Drug Discovery WS05/06 5 Warum ist die Voraussage der ADME Parameter so wichtig ? (II) Zeil ist es, ungeeignete Verbindungen möglichst frühzeitig zu erkennen: • Schonung von Resourcen • Vermeidung unnötiger klinischer Tests • Je später ein Wirkstoff zurückgezogen werden muß, desto teuerer wird es. „Fail early, fail fast, fail cheap“ 6. Vorlesung Modern Methods in Drug Discovery WS05/06 6 Komponentenauswahl für das High Throughput Screening (HTS) R2 R1 N R3 Typischer eADME Filter 6. Vorlesung Modern Methods in Drug Discovery WS05/06 7 Solvatation kontra Löslichkeit gas / vapour Sublimation Dampfdruck(A) Löslichkeit(A) = Dampfdruck(ideales Gas) exp -DGsolv(A) RT Solvatation Feststoff (kristallin) DGsolv Lösen logS Solvens (wäßrige Lösung) 6. Vorlesung Modern Methods in Drug Discovery WS05/06 8 Löslichkeitsmodelle (I) Die Berechnung der Löslichkeit aus einem thermodynamischen Zyklus (Gitterenergie, Solvatationsenergie) wäre prinzipiell möglich, jedoch ist 1. Die Voraussage der Gitterenergie praktisch kaum möglich da dies die Raumgruppe des Kristalls erfordert 2. Die Berechnung der Solvatationsenerge selbst fehlerbehaftet ist Deshalb kommen vorwiegend QSAR Ansätze zur Anwendung 6. Vorlesung Modern Methods in Drug Discovery WS05/06 9 Löslichkeitsmodelle (II) Deskriptoren: Konnektivitätsindices r2=0.89, q2= 0.84, se = 0.98, n=120, F=297.80 Lit. C. Zhong et al. J.Pharm.Sci. 92 (2003) 2284 6. Vorlesung Modern Methods in Drug Discovery WS05/06 10 Löslichkeitsmodelle (III) Weitere Ansätze zeigen, daß die verwendeten Deskriptoren die Lipophilie, H-Brückenbindungseigenschaften und Flexibilität der Verbindungen wiedergeben müssen Lit: A. Cheng et al. J.Med.Chem. 46 (2003) 3572 D. Butina et al. J.Chem.Inf.Comput.Sci. 43 (2003) 837 Neben klassischen QSAR-Gleichungen kommen zunehmend auch Neuronale Netze zum Einsatz Lit: A. Yan et al. J.Chem.Inf.Comput.Sci. 43 (2003) 429 J.K. Wegener et al. ibid 43 (2003) 1077 6. Vorlesung Modern Methods in Drug Discovery WS05/06 11 Absorption Wieviel und wie schnell wird der Wirkstoff aufgenommen ? Praktischerweise sollte ein Pharmakon oral appliziert werden können Es wird nach der Magenpassage vom Darm ins Blut resorbiert. (Über die Pfortader zunächst in die Leber) 6. Vorlesung Modern Methods in Drug Discovery WS05/06 12 Absorption im duodenum (I) Aufnahme des Wirkstoffes in den Blutkreislauf Ausschnitt aus der Darmwand 6. Vorlesung Modern Methods in Drug Discovery WS05/06 13 Absorption im duodenum (II) Aufnahme des Wirkstoffes in den Blutkreislauf A B C D A B C D' A Transcellulär (passive Diffusion) B Paracellulär C Aktiver Transport D Transcytosis Ausschnitt aus der Darmwand 6. Vorlesung Modern Methods in Drug Discovery WS05/06 14 Absorption im duodenum (III) Modell der Zellmembran Phospholipid De Groot et al. Science 294 (2001) 2353 6. Vorlesung Modern Methods in Drug Discovery WS05/06 15 Caco-2 Zellen Monolayer Experimenteller Ansatz zur Voraussage der intestinalen Absorption Monolayer aus einer Kultur von Zellen die eigentlich von einem Dickdarmkrebs stammen. Vorteil: Reproduzierbare Ergebnisse, relativ gute Übereinstimmung mit in vivo Studien Nachteil: Diese Zellen besitzen etwas andere metabolische Eigenschaften als Zellen des Dünndarms (MDR1 Transporter überexprimiert) Daneben kommen neuerdings auch synthetische Membranen zum Einsatz 6. Vorlesung Modern Methods in Drug Discovery WS05/06 16 Welche Faktoren bestimmen die passive Diffusion durch Lipiddoppelschichten ? Kleine Moleküle sollten die Membran schneller durchdringen als größere Deskriptor: Molekülgewicht (MW) und Molekülform Phospholipiddoppelschichten sind im Inneren lipophil Deshalb sollten lipophile Moleküle sie schneller passieren Deskriptor: logP (water/n-octanol partition coefficient) Phospholipiddoppelschichten weisen eine hydrophile äußere Oberfläche auf Deskriptoren: Anzahl von H-Brücken Donoren und Akzeptoren Beobachtung: Die Permeation geht mit der Lösungswärme einher 6. Vorlesung Modern Methods in Drug Discovery WS05/06 17 Molekülbasierte Deskriptoren zur Voraussage der ADME Eigenschaften logP Wasser/Octanol Verteilungskoeffizient Lipinski‘s rule Topologische Indices Polar surface area Similarität / Dissimilarität QSAR quantitative structure activity relationship QSPR quantitative structure property relationship 6. Vorlesung Modern Methods in Drug Discovery WS05/06 18 Lipinski´s Rule of 5 Kombination von Deskriptoren zur Abschätzung der intestinalen Absorption. Schlechte Aufnahme der Verbindung, wenn Molekülmasse > 500 logP > 5.0 > 5 H-Brücken Donoren (OH und NH) >10 H-Brücken Akzeptoren (N und O) Schlechte Diffusion Zu lipophil Zuviele H-Brücken mit den Kopfgruppen der Membran C.A. Lipinski et al. Adv. Drug. Delivery Reviews 23 (1997) 3. 6. Vorlesung Modern Methods in Drug Discovery WS05/06 19 Polar Surface Area (PSA) Die PSA ist definiert als der Bereich der van der Waals Oberfläche des Moleküls, der von den polaren Stickstoff- und Sauerstoffatomen, sowie den an sie gebundenen Wasserstoffen herrührt. Maß für die Ausbildung von H-Brücken Wie bei allen 3D Deskriptoren ist auch die PSA im Prinzip abhängig von der Konformation. 6. Vorlesung Modern Methods in Drug Discovery WS05/06 20 Absorptionsmodelle Neue Arbeiten zeigen allerding, daß auch ohne Berücksichtigung verschiedener Konfomere eine gute Korrelation zur Caco-2 Absorption und Aufnahme im Menschen (%FA) besteht. Vollständige Aufnahme (>90%) wenn PSA<60 A2 Schlechte Aufnahme (<10%) wenn PSA>140 A2 Lit: D.E. Clark, J.Pharm.Sci. 8 (1999) 807; Drug Discovery Today 5 (2000) 49; K. Palm et al. J.Med.Chem. 41 (1998) 5382 6. Vorlesung Modern Methods in Drug Discovery WS05/06 21 Pharmacokinetik und Bioverfügbarkeit „Quantitative Auseinandersetzung des Organismus mit einem einverleibten Pharmakon“ Der Köper/Organismus wird als offenes System betrachet, daß nach jeder Störung/Arzneimittelzugabe versucht, den Gleichgewichtszustand wiederherzustellen Magen Darm Haut Blutplasma Nieren Lungen interstitielle Flüssigkeit (ECF) Liquor cerebrospinalis intrazelluläre Flüssigkeit Dazu teilt man den Körper in eine Reihe von Räumen (compartments) auf, zwischen denen ein Fließgleichgewicht herrscht 6. Vorlesung Modern Methods in Drug Discovery WS05/06 22 Distribution / Invasion Der Gesamtweg des Medikamentes läßt sich in Einzelschritte aufteilen: 1) 2) 3) 4) Diffusion im Lösungsmittel D. durch Gewebs- und Gefäßmembranen Transport durch das Blut a) D. zu den target Rezeptoren b) D. in andere Kompartimente c) D. in Eliminationsorgane 5) Irreversible Elimination Invasion (nach Dost) ≈ Distribution Hohe Eliminationskonstante: Kurzzeitnarkotika Niedrige Eliminationskonstante: Antibiotika 6. Vorlesung Modern Methods in Drug Discovery WS05/06 23 Verteilungsvolumen und Dosierung Dosis D Volumen V Konzentration yo yo D V Die Dosisierung richtet sich nach dem Verteilungsvolumen 6. Vorlesung Modern Methods in Drug Discovery WS05/06 24 Invasion / System exposure (II) Nur mittels intravenöser Gabe ist die volle Konzentration sofort verhanden. Ansonsten überschneiden sich Invasion und Elimination. Dies entspricht physicochemisch einer Folgereaktion k Inv [A]t [A]0 e -k El t e -k Invt Bateman Funktion k Inv k El 11 10 Nur Invasion ▬▬ Nur Elimination ▬▬ Rasche Invasion ▬▬ Rasche Elimination ▬▬ 9 Konzentration 8 7 6 5 Therapeutische Bandbreite 4 3 2 1 0 0 6. Vorlesung 10 20 30 Zeit t 40 50 60 Modern Methods in Drug Discovery WS05/06 25 Das Dost‘sche Prinzip (I) Konzentration Wie verhält sich der Konzentrationsverlauf bei unterschiedlichen Dosen ? Zwischen zwei Meßzeiten 5 erhält man die Fläche S volle Dosis D (Transit) unter der Kurve 4 halbe Dosis durch Integration der 3 Batemanfunktion als 2 S 1 0 0 10 20 30 Zeit t 40 50 D Cltot 60 Total clearance: Volumen das pro ln 2 Cl V [Volumen/Z eit] tot Zeiteinheit geklärt wird t0 korrespondierende Flächen entsprechen dem Verhältnis der Dosen 6. Vorlesung Modern Methods in Drug Discovery WS05/06 26 Das Dost‘sche Prinzip (II) Die Referenzkurve erhält man durch intravenöse Gabe der Dosis Occupancy = meßbare Konzentration Transit = bereits irreversibel eliminierte Menge Transfer = Occupancy + Transit = absorbierte Menge Availments = noch zur Invasion anstehende Menge 6. Vorlesung Modern Methods in Drug Discovery WS05/06 27 Daten für Pharmakokinetische Modelle Chemische Daten Biologische Daten Verteilungskoeffizienten Metabolische Umsatzraten Vmax, Km, Ki Löslichkeit Dampfdruck Diffusionsgeschwindigkeit Proteinbindungskonstanten Anatomische Abmessungen Blutfluß durch Organe Organvolumina Atmung Körpergewicht Alter, Geschlecht, Ausmaß körperlicher Aktivität 6. Vorlesung Modern Methods in Drug Discovery WS05/06 28 Pharmakokinetische Modelle (I) Kompartimentmodelle Annahme: keine metabolische Umsetzung in den Verteilungsräumen Darm k12 k23 Leber Blut k32 k24 Niere Konzentrationverlauf läßt sich über lineare Differentialgleichungen berechnen 6. Vorlesung Modern Methods in Drug Discovery WS05/06 29 Pharmakokinetische Modelle (II) Blutkreislauf als elektrisches Netzwerk (1930) Per Analogrechner simulierbar (variable Steckverbindungen zwischen den Modulen) Anwendbarkeit: Narkotika (geringe Metabolisierung, lipophil, werden abgeatmet) 6. Vorlesung Modern Methods in Drug Discovery WS05/06 30 Distribution Je nach Ziel muß der Wirkstoff vom Plasma aus weitere Kompartimente erreichen. Bei Wirkstoffen die auf das zentrale Nervensystem wirken muß die Blut-Hirn-Schranke passiert werden. Umgekehrt sollten andere Wirkstoffe die Barriere nicht überwinden. Auch der aktive Transport von Stoffen kommt in Betracht 6. Vorlesung Modern Methods in Drug Discovery WS05/06 31 Eiweißbindung / Distribution (I) Die Konzentration von Wirkstoffen kann durch Bindung an Eiweiße verringert werden. Dies gilt sowohl für das Plasma, die extracelluläre und die interstitielle Flüssigkeit. AB AB mit vhin k hin [A][B] AB A B mit vher k her [AB] Im Gleichgewicht ist keine Veränderung meßbar, und damit k hin [A][B] k her [AB] k hin [AB] K [A][B] k her Die Bindung erfolgt gemäß der Langmuir‘sche Absorptionsisotherme (Absorptionswärme unabhängig vom Belegungsgrad) und erfüllt damit das Massenwirkungsgesetz Neben Proteinen können auch Mucopolysaccharide (Binde- und Stützgewebe) absorbieren 6. Vorlesung Modern Methods in Drug Discovery WS05/06 32 Metabolismus (I) (Bio-)chemische Reaktionen von Xenobiotica im Körper First pass effect: Extensive Umsetzung von vorwiegend lipophilen Molekülen, solchen mit MW>500, oder die eine spezifische Affinität zu bestimmten Transportern haben, bei der ersten Passage durch die Leber Phase I: Oxidation, Reduktion und Hydrolyse Cytochrom P450 Enzyme Phase II: Konjugation mit kleinen Molekülen (z.B. Glutamin) Phase III: Elimination durch Transporter 6. Vorlesung Modern Methods in Drug Discovery WS05/06 33 Metabolismus (II) Experimentelle (in vitro) Methoden: Leber Mikrosomen vom Menschen, Hepatocyten und rekombinante P450 Isozyme (exprimiert in E. coli) 6. Vorlesung Modern Methods in Drug Discovery WS05/06 34 Elimination / Exkretion Unter Elimination werden alle Vorgänge zusammengefaßt, die zur Entfernung eines Stoffes aus einem Kompartiment führen. Diese können auch metabolischer Art sein. Lipophile Stoffe können über die Galle, hydrophile Stoffe über den Harn ausgeschieden werden. Allgemein gilt: MW <300 300-500 >500 Galle Galle & Harn Harn 6. Vorlesung Modern Methods in Drug Discovery WS05/06 35 Elimination / Clearance Überblick der metabolischen Pfade 6. Vorlesung Modern Methods in Drug Discovery WS05/06 36 Elimination / Clearance (III) Physicochemisch gesehen ist die Eliminierung eines Stoffes ein Zerfallsprozess 1. Ordnung (abhängig von der jeweils vorhandenen Konzentration des Stoffes) A B mit v k[A] k rate constant of eliminatio n d [A] dt k[A] | und Integratio n führt zu dt [A] [A]t - [A]o t [A] t d [A] k dt bzw. ln kt oder [A] [A] 0 0 [A] t [A] 0 e -kt mit der Halbwertsz eit t 1 6. Vorlesung 2 ln 2 k Modern Methods in Drug Discovery WS05/06 37 Was ist die Blut-Hirn Schranke (BBB) ? Querschnitt durch ein Blutgefäß endothelial cell astrocyte foot process tight junctions between endothelial cells blood lumen brain extracellular fluid neuron pericyte Nach: J.-M. Scheerman in Pharmacogenomics, J.Licinio & Ma-Li Wong (Eds.) Wiley-VCH (2002) pp. 311-335. 6. Vorlesung Modern Methods in Drug Discovery WS05/06 38 Wozu dient die Blut-Hirn Schranke ? Die in silico Vorhersage der Permeabilität der Blut-Hirn Schranke (BBB) einer Verbindung im Rahmen der vorklinischen Entwicklung ist besonders wichtig, da • Nur Substanzen die auf das zentrale Nervensystem (CNS) wirken, sollen die Blut-Hirn Schranke effektiv überwinden. • BBB-Screening ist besonders „teuer“ (Tierversuche kaum vermeidbar: Mikrodialyse, Isotopenmarkierung) 6. Vorlesung Modern Methods in Drug Discovery WS05/06 39 Blood-Brain Barrier (BBB) Als Maß für das Durchdringen der Blut-Hirn Schranke wird der Logarithmus des Verhältnis der Konzentrationen angegeben logBB = log([im Hirn]/[imBlut]) Bereich: -2.00 bis +1.00 Vorwiegend im Blut -1.0 < logBB < 0.3 vorwiegend im Hirn Experimentell ist der logBB Wert nur schwer zugänglich (Isotopenmarkierung, Mikrodialyse) und auch Modelle aus künstlichen Membranen (Endothelial Zellen) sind noch in der Entwicklung Lit. D. E. Clark, J. Pharm. Sci. 8 (1999) 815 6. Vorlesung Modern Methods in Drug Discovery WS05/06 40 Blood-Brain Barrier (II) Im Gegensatz zur Absorption aus dem Duodenum spielt hier die Polarität der Verbindungen eine große Rolle, die nicht durch die PSA beschrieben werden kann. Bsp: Benzol 3-Methylpentan PSA logBB ClogP Polarisierbarkeit(AM1) 0 -0.69 2.1 13.8 0 2.01 3.7 14.8 Entsprechend läßt sich eine QSRP-Gleichung aufstellen logBB = a PSA + b ClogP + c mit r = 0.887 Lit. D. E. Clark, J.Pharm.Sci. 8 (1999) 815 F. Lombardo et al. J.Med.Chem. 39 (1996) 4750 6. Vorlesung Modern Methods in Drug Discovery WS05/06 41 Bisher benutzte Deskriptoren Folgende Terme korrelieren direkt mit logBB: ● logP fragment based (MlogP, ClogP,...) ● Polar surface area contributions from N, O and H atoms ● hydrogen-bond donors and acceptors ● size and shape 6. Vorlesung numerical count molecular volume and globularity Modern Methods in Drug Discovery WS05/06 42 Deskriptoren für Größe und Form Bezug zur Molekülform haben: Molekülvolumen, Globularität, Anzahl drehbarer Bindungen Globularität: Verhältnis der Oberfläche (unter der Annahme das Molekül wäre eine Kugel) zur tatsächlichen Oberfläche. Immer < 1 Hauptkomponenten der Molekülgeometrie: Ausdehnung des Moleküls im dreidimensionalen Raum 6. Vorlesung Modern Methods in Drug Discovery WS05/06 43 Neue Deskriptoren für Größe und Form - Deskriptoren wie etwa die Globularität sind korreliert mit dem Molekülgewicht und der Anzahl der H-Atome + Ersatz durch drei Terme die aus der Molekülgeometrie abgeleitet werden PCGC PCGA PCGB 6. Vorlesung Modern Methods in Drug Discovery WS05/06 44 BBB-Model mit 12 Deskriptoren Deskriptoren hauptsächlich aus QM Rechnungen: Elektrostatische Oberfläche, Hauptkomponenten der Geometrie,H-Brücken Eigenschaften 2.5 r2=0.866, adj. r2=0.844, se=0.308, n=90 predicted logBB 1.5 0.5 -0.5 -1.5 -2.5 -2.5 -1.5 -0.5 0.5 1.5 2.5 observed logBB Lit: M. Hutter J.Comput.-Aided.Mol.Des. 17 (2003) 415. 6. Vorlesung Modern Methods in Drug Discovery WS05/06 45 ADME - Historische Entwicklung 1960 Corwin Hansch QSAR für kleine Datensätze logP für Toxizität 1980 in vitro Studien ersetzen in vivo Studien 1990 Erste in silico ADME Modelle (Computer) Docking in Proteinstrukturen Homologiemodellierung von Proteinen (CYP P450) 1997 Lipinski‘s Rule of Five zur Absorption 2002 X-Ray Struktur von human CYP2C9 2004 X-Ray Struktur von human CYP3A4 6. Vorlesung Modern Methods in Drug Discovery WS05/06 46 Web-basierte online Tools Eine Reihe von Instituten und Firmen haben Server für die Vorhersage von ADME-Eigenschaften. Diese basierend zumeist auf einem Java-Applet mit dem die Moleküle gezeichnet werden können, bieten die Eingabe als SMILES-String oder als eines der vielen Formate für 3D-Strukturen an. Eine Zusammenfassung mit Hyperlinks bietet das Virtual Laboratory http://146.107.217.178/online.html Lit. I.V. Tetko, Mini Rev.Med.Chem. 8 (2003) 809 6. Vorlesung Modern Methods in Drug Discovery WS05/06 47