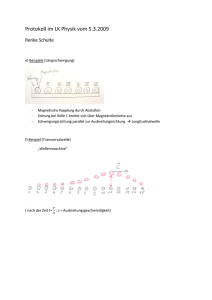
Wechselwirkung von Strahlung mit Materie
Werbung

Wechselwirkung mit Strahlung in unterschiedlichen Aggregatzuständen: Gas, Flüssigkeit Wechselwirkung mit elektromagnetischer Strahlung • Kohärente Schwingung der Elektronenhülle als Gesamtheit • Photoeffekt bei inneren Elektronen • Anregung von Valenzelektronen: – Abhängig von der Kopplung an die Nachbarschaft, deshalb gibt es Unterschiede für • • • • Freie Atome Moleküle Flüssigkeiten Festkörper – Isolator, Halbleiter, Leiter, Supraleiter Die gesamte Elektronenhülle schwingt bei der Entstehung kohärenter Strahlung B Anregende und emittierte Welle sind phasengleich Wechselwirkung der gesamten Elektronenhülle mit Röntgenstrahlung Gas Flüssig Fest Unabhängig von der Kopplung an die Nachbarschaft Frequenzbereiche der Oszillatoren Technische Schwingkreise Molekülschwingungen Valenz Elektronen Innere Orbitale m Kernreaktio nen 780 nm rot 3,8 1014Hz 380 nm Violett 7,9 1014Hz Wechselwirkung der inneren Elektronen mit Röntgenstrahlung • Röntgenstrahlung liege im passenden Energiebereich Gas Flüssig Fest Anregung durch Photoeffekt, Emission inkohärenter, für das Element charakteristischer Strahlung, unabhängig von der Kopplung an die Nachbarschaft Der Photoeffekt Ein Photon ionisiert ein Atom auf einer inneren Schale Die Lücke wird unter Emission von FluoreszenzStrahlung aufgefüllt B B Frequenzbereiche der Oszillatoren Technische Schwingkreise Molekülschwingungen Valenz Elektronen Innere Orbitale m Kernreaktio nen 780 nm rot 3,8 1014Hz 380 nm Violett 7,9 1014Hz Wechselwirkung der Valenzelektronen mit elektromagnetischer Strahlung im Bereich des sichtbaren Lichts Gas Flüssig Fest Abhängig von der Kopplung an die Nachbarschaft Beispiele für Emission und Absorption an freien Atomen Absorptionslinien von Wasserstoff vor der „Weissen“ Strahlung der Sonne (an der Oberfläche ca. 6000 K) Abbildung: Emissionsspektrum der Quecksilberdampflampe und Absorptionslinien im Sonnenspektrum. Quelle: Meyers Enzyklopädisches Lexikon Unterschied zwischen Gas, Flüssigkeit und Festkörper bezüglich der Valenzelektronen: • Unterschiedliche Kopplung zwischen benachbarten Atomen – Ungekoppelte Pendel gleicher Bauweise zeigen eine einzige Eigenschwingung – Zwei identische, gekoppelte Pendel zeigen zwei unterschiedliche Frequenzen „in der Nähe“ der Eigenfrequenz Kopplung „spaltet die Eigenfrequenz auf“ Erinnerung an das „Schlüsselexperiment“ Doppelpendel Schwingungart Symmetrie Erste Eigenschwingung Spiegelsymmetrisch Zweite Eigenschwingung „Anti“Spiegelsymmetrisch Beliebig, das ist eine Überlagerung beider Eigenschwingungen Unsymmetrisch Muster Wirkung der Kopplung: Vergleich der Spektren von Gasen/Flüssigkeiten/Festkörpern C6H6 flüssig C6H6 gasförmig Die Verbreiterung der Linien in der Flüssigkeit durch die Kopplung zwischen den Molekülen ist klar zu erkennen Beispiel für Anregung in Molekülen in Festkörpern und in flüssiger Phase • Pigmente, Farbmittel in Form von feinverteilten Festkörpern, die sich in Lösungsmitteln nicht auflösen lassen, – Beispiel: Schwarzpigmente Graphit, Ruß Weißpigmente Titandioxid • Farbstoffe, meist echte Lösungen – Beispiel: Farbstoff-Moleküle, z. B. Indigo – Farben der Metall-Komplexe: Kopplung des Zentralatoms (-ions) an die Ligandenhülle erzeugt neue Niveaus (z. B. blaues CuSO4) • Je mehr Oszillatoren gekoppelt werden, desto mehr Eigenfrequenzen stehen für die Anregung zur Verfügung: Deshalb gibt es Weiß nur als Pigment oder als Kolloidteilchen (z. B. in Milch) Im Infrarot-Bereich gibt es bei Molekülen zusätzlich : • Wechselwirkung zwischen mechanischen Schwingungen mit elektromagnetischen Wellen • Bei Molekülen mit Dipolmoment wird durch die Absorption eines Lichtquants die mechanische Schwingung angeregt • Beispiel: Vier Schwingungen in CO2 , 3N Freiheitsgrade, abzüglich drei Freiheitsgrade zur Impuls- und zwei Freiheitsgrade zur Drehimpulserhaltung – CO2 ist ein lineares Molekül, sonst wären drei Rotationsfreiheitsgrade abzuziehen Frequenzbereiche der Oszillatoren Technische Schwingkreise Molekülschwingungen Valenz Elektronen Innere Orbitale m Kernreaktio nen 780 nm rot 3,8 1014Hz 380 nm Violett 7,9 1014Hz Beispiel CO2, erste Streckschwingung, symmetrisch Beispiel CO2, zweite Streckschwingung antisymmetrisch Beispiel CO2, erste Deformationsschwingung Beispiel CO2, beide Deformationschwingungen Symmetrieeigenschaften dieser Schwingungen bei Drehung und Spiegelungen Drehachse Spiegelebene vertikal Spiegelebene horizontal ja ja ja ja ja nein nein ja ja nein ja nein Ist die Schwingung invariant gegenüber der Symmetrieoperation? Beispiel CO2, erste Deformationsschwingung Infrarot Anregung • Kraft des Feldes auf die Ladungen des Moleküls, ein Dipol, regen die Schwingung an E (t ) E0 sin t p(t ) q l (t ) 1 N/C Feldstärke der Welle Dipolmoment des 1 Cm Moleküls l (t ) F (t ) / k 1m Hookesches Gesetz für die rückstellende Kraft F (t ) 2 E (t ) q 1N Kraft auf die Ladungen p(t ) q 2 E0 / k sin t 1 Cm Schwingender Dipol 2 Anregung bei der Raman-Spektroskopie • Stoß der Photonen auf die Massen des Moleküls (Dipol) regen die Schwingung an • Elektrische Anregung: Kohärente und inkohärente Streuung Die gesamte Elektronenhülle schwingt bei der Entstehung kohärenter Strahlung B Anregende und emittierte Welle sind phasengleich Beispiel für die Entstehung inkohärenter Strahlung und Impulsübertrag durch Stoß mit dem Photon B Zusammenfassung • • Anregung freier Atome liefert scharfe Linien Moleküle zeigen zwei Effekte: 1. Durch Kopplung an den Nachbarn Feinstruktur der Linien des freien Atoms 2. Schwingungs-Spektren zeigen die Kopplung an mechanische Schwingungen des Moleküls • • In Lösungen verbreitert die Kopplung an die Atome des Lösungsmittels die Linien noch stärker Im Bereich der Röntgenstrahlung ist die Linienbreite von der Bindung unabhängig finis