Erstes Medikament beschichtetes resorbierbares
Werbung

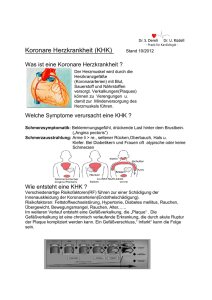
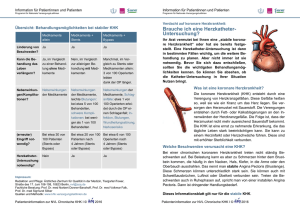
Innovation: Erstes Medikament beschichtetes resorbierbares Gefäßgerüst bei Koronarer Herzkrankheit Anwendung: Minimal-invasive Chirurgie in der Kardiologie Zu den häufigsten Todesursachen in Deutschland zählt die Koronare Herzkrankheit (KHK). Dabei handelt es sich um eine chronische Erkrankung des Herzens, ausgelöst durch arteriosklerotische Veränderungen der Herzkranzgefäße (im Volksmund auch „Verkalkung“ genannt). Sowohl Kalk- als auch Bindegewebsablagerungen führen dazu, dass sich der Durchmesser betroffener Herzkranzarterien, immer mehr verkleinert. Es entwickelt sich eine so genannte Koronarstenose (Koronar = die Herzkranzgefäße betreffend, Stenose = Verengung, hier von Blutgefäßen). Durchblutungsstörungen sind die Folge, weil das Herz durch die verengten Gefäße nicht mehr ausreichend Blut pumpen und damit den Körper weder mit Sauerstoff noch Nährstoffen ausreichend versorgen kann. Ein typisches Symptom der KHK ist die Angina pectoris. Darunter versteht man einen anfallsartigen Schmerz in der Brust. Eine KHK kann zu Myokardinfarkt, Herzinsuffizienz, Herzrhythmusstörungen sowie plötzlich auftretendem Herztod führen. Zum Herzinfarkt kommt es, wenn sich das Blutgefäß komplett verschließt. Es gibt mehrere Möglichkeiten, eine KHK zu behandeln. Zunächst kann versucht werden, durch eine konservative medikamentöse Therapie die Risikofaktoren wie Bluthochdruck und hohe Cholesterinwerte zu senken und Symptome wie Angina pectoris zu lindern. Wenn es die Krankengeschichte erfordert, kann auch eine Bypass-Operation notwendig sein. Bei dieser Operation am offenen Herzen werden die Engstellen mit Hilfe von Gefäßprothesen überbrückt, also Umleitungen (engl. Bypass) geschaffen. In den letzten Jahren haben sich aber immer mehr die minimal-invasiven Herzkatheterbehandlungen durchgesetzt. Am Anfang stand die Ballonangioplastie oder PTCA (Perkutane transluminale koronare Angioplastie). Bei diesem Eingriff führt der Arzt über die Beinarterie an der Leistenbeuge einen Führungskatheter (langer, dünner, flexibler Schlauch) in die Arterie und weiter über die Hauptschlagader (Aorta) bis zum Herzen vor. Durch diesen Katheter wird jetzt bis zum betroffenen Herzabschnitt ein dünner Draht geschoben, der als Schiene für einen Ballonkatheter dient. Ist der Ballon in der verengten Stelle platziert, wird er mit röntgensichtbarer Flüssigkeit gefüllt und mehrere Sekunden mit hohem Druck aufgedehnt. Ablagerungen und Verkalkungen werden in die elastische Gefäßwand gedrückt, wodurch das Gefäß geöffnet und der Blutfluss wieder hergestellt wird. Allerdings können sich die Blutgefäße nach dieser Ballondilatation häufig erneut verengen (Restenosen). Um das zu verhindern, werden zusätzlich kleine Metallstützen (Stents) eingesetzt, die beim Aufblasen des Ballons an die Gefäßwand gepresst werden, um die Arterie offen zu halten. Doch auch bei dieser Methode sind Gefäßverschlüsse innerhalb des Stents möglich, wenn auch im Vergleich seltener als bei einer reinen Ballondilation. Ursache bei beiden Verfahren ist eine Verletzung der Gefäßwand. Das Immunsystem des Körpers antwortet auf diese Verletzung, indem glatte Muskelzellen aus der Gefäßwand sich unkontrolliert vermehren und im schlimmsten Fall durch den Stent in das Gefäß wuchern. Daher wurden diese unbeschichteten Stents weiterentwickelt und mit einem Medikament versehen. Diese Medikament-freisetzenden Stents (Drug-Eluting-Stents, DES) wurden © www.aktion-meditech.de - frei für redaktionelle Verwendung Anfang 2001 zur Behandlung der KHK eingeführt. Sie bestehen aus einem Metallstent mit einer Oberflächenbeschichtung, aus der nach und nach ein Wirkstoff abgeben wird, um lokal das Wachstum der Muskelzellen zu hemmen. Doch auch dieses Implantat verbleibt lebenslang als Fremdkörper in der Arterie, obwohl die Stützaufgabe bereits nach einigen Monaten erfüllt ist. Bei einem möglichen herzchirurgischem Eingriff zu einem späteren Zeitpunkt, kann das zu Komplikationen führen. Außerdem kann es bei Einsätzen von DES zu einer späten Stentthrombose, also einem Gefäßverschluss durch ein Blutgerinnsel, kommen. Zur weiteren Verbesserung der Behandlungsergebnisse wurden neue temporäre, resorbierbare Gefäßgerüste aus Kunststoffpolymeren entwickelt, die über einen Zeitraum von etwa zwei bis drei Jahren biologisch abgebaut werden. Innovation Ziel der Therapie mit resorbierbaren Gefäßgerüsten ist, zunächst das Gefäß zu öffnen, wie mit klassischen Medikament-freisetzenden Stents. Darüber hinaus löst sich aber in der zweiten Phase das Gerüst auf, d.h. es bleibt kein Permanentimplantat im Gefäß zurück, wodurch die Rückkehr in einen natürlicheren Zustand ermöglicht wird. Die abbaubaren Gerüste sind flexibler als die Metallstützen und passen sich daher leichter dem normalen Gefäßverlauf an. Damit kann die zuvor verengte und damit auch unflexibel gewordene Ader wieder pulsieren und seine ursprüngliche Funktion übernehmen. Eine starre Gefäßstütze aus Metall verbleibt als permanentes Implantat und schränkt das Gefäß ein. Spätestens nach der vollständigen Auflösung* des Gerüsts nach etwa 2 bis 3 Jahren bleibt eine stabilisierte und offene Ader zurück; eine natürlichere Beweglichkeit kann somit erreicht werden. Seit Ende 2012 ist das weltweit erste biologisch abbaubare Medikament freisetzende Gefäßgerüst (bioresorbable vascular scaffold, BVS) für die Behandlung von KHK-Patienten in der Europäischen Union zugelassen. Basis des Produktes ist eine Polymilchsäure (Bio-Kunststoff), die bereits aus anderen bioresorbierbaren Technologien in der Medizin, wie selbstauflösenden Fäden, bekannt ist. Aus einer ebenfalls aus Polymilchsäure bestehenden Beschichtung wird ein Medikament an die Gefäßwand abgegeben, um unerwünschte Zellwucherungen zu begrenzen und Wiederverengungen vorzubeugen. Das Gefäßgerüst ist ein maschenartiges Geflecht, das entwickelt wurde, um verengte Herzkranzgefäße zu öffnen und dadurch den Blutfluss wieder herzustellen. Es stützt das Gefäß ab bis es soweit geheilt ist, dass es selbstständig offen bleibt. Dann löst* es sich auf natürlichem Weg auf und zerfällt in Wasser und CO2. Der Patient behält keinen permanenten metallischen Stent zurück und das Gefäß kann durch den BVS zu einer natürlicheren Funktion und Beweglichkeit zurückkehren. Es besteht daher die Hoffnung, dass Spätthrombosen weiter reduziert und keine antithrombotische Langzeitbehandlung notwendig wird, was mit klinischen Studien noch zu untermauern ist. Das neuartige Gefäßgerüst erhielt seine Zulassung aufgrund einer klinischen Studie, bei der Patienten mit einer KHK nach dem Implantieren noch bis zu drei Jahre nachbeobachtet worden sind. Mittlerweile erhielten bereits über 10.000 Patienten in mehr als 30 Ländern das resorbierbare Gefäßgerüst. Um die Qualität der neuen Behandlungsweise sicherzustellen, werden die Anwender intensiv auf das neue System geschult. © www.aktion-meditech.de - frei für redaktionelle Verwendung 2 Vorteile für die Patienten Ø Kein dauerhaftes Implantat, sondern ein natürlich abbaubares temporäres Gefäßgerüst Ø Gefäße sind erneuten Interventionen wie auch Bypass-Operationen zugänglich, da die Arterien nicht dauerhaft durch Metallstents blockiert werden Ø Gefäß kann möglicherweise seine natürliche Gefäßbewegung wieder aufnehmen Ø Direkt im Anschluss an den Eingriff ist, im Gegensatz zur Therapie mit Metallstents, eine nicht-invasive Bildgebung möglich, weil keine metallischen Stents die Auswertung der Aufnahmen stören Ø Möglicherweise lassen sich Spätthrombosen weiter reduzieren und der Bedarf für antithrombotischer Langzeittherapie senken, da kein Fremdkörper im Blutgefäß zurückbleibt. Dies wird in klinischen Studien untersucht. Ø Fazit Der BVS ist das erste zugelassene vollständig* abbaubare Wirkstoff-freisetzende KunststoffGerüst zur Behandlung der Koronaren Herzkrankheit (KHK) weltweit. Im Gegensatz zu herkömmlichen Behandlungsmethoden bei KHK wie PTCA, Metall-Stents und DES bietet der BVS eine nachhaltige Therapie, bei der kein Fremdkörper auf Dauer zurückbleibt, mit der möglichen Aussicht Langzeitkomplikationen vorzubeugen, weil eine geringere Gefahr einer erneuter Gefäßverengung besteht. *Kleine Platinmarker an den Gerüstenden verbleiben im Gefäß zur Röntgenkontrolle Stand: Mai 2013 Quellen und wichtige Studien: Quellen und Studien sind auf Nachfrage bei der Redaktion erhältlich. _________________________________________________________________________ Herausgeber: Aktion Meditech, www.aktion-meditech.de Pressekontakt: Haas & Health Partner Public Relations GmbH Große Hub 10c, 65344 Eltville Ralf Steinmetz Tel. 06123-70 57 -39 Fax 06123-70 57 -57 [email protected] © www.aktion-meditech.de - frei für redaktionelle Verwendung 3