1 Einleitung
Werbung

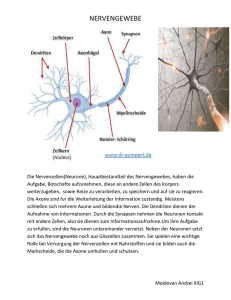
1 Einleitung Der Begriff hereditäre sensomotorische Neuropathien (HMSN), auch als Charcot-Marie-Tooth Krankheit (CMT) bekannt, bezeichnet sowohl eine histopathologisch und klinisch als auch genetisch äußerst heterogene Gruppe von hereditären motorischen und sensorischen Neuropathien. Diese sind vorwiegend charakterisiert durch langsam progrediente Muskelschwäche (besonders des peronealen Kompartimentes), Muskelatrophien, sensible Defizite, skeletale Deformitäten (z.B. Pes cavus) und durch eine Abschwächung bis Verlust der Muskeleigenreflexe. Der klinische Grad der Erkrankung variiert sehr stark. Die Variationsbreite hängt einerseits von dem zugrunde liegenden Gendefekt ab, andererseits scheint auch ein Gen-Dosis-Effekt mitverantwortlich für den Phänotyp zu sein (Marques et al., 1999; Reilly et al., 2002). In zwei epidemiologischen Beobachtungen ergab sich eine Prävalenz der Erkrankung von 10.8 pro 100.000 Einwohner in Italien, 17.5 pro 100.000 Einwohner in Japan sowie 28.2 pro 100.000 Einwohner in Spanien (Berciano et al., 2003). Der Beginn der Erkrankung liegt vorwiegend in der ersten Lebensdekade, kann aber auch erst während der Adoleszenz eintreten. Der Verlauf ist langsam progredient und die Ausprägung der Symptomatik höchst variabel. Das Krankheitsbild wurde unter anderem im Jahre 1886 von Charcot, Marie und Tooth beschrieben, weshalb die Bezeichnungen HMSN und Charcot-Marie-Tooth (CMT) in Reminiszenz auch synonym verwendet werden. Generell werden hereditäre Neuropathien gegenwärtig in zwei Hauptgruppen eingeteilt: Syndrome, bei denen Neuropathien im Vordergrund stehen oder sogar die einzige Ausprägung der Erkrankung darstellen und Erkrankungen, in denen Neuropathien Teil einer neurologischen oder Multisystemerkrankung sind, wie zum Beispiel die familiäre Amyloid Polyneuropathie, Porphyrien, hereditäre Ataxie oder Lipidstoffwechselstörungen (Berciano et al., 2003). In dieser Arbeit wird ausschließlich auf die erstgenannte Gruppe unter besonderer Berücksichtigung vier verschiedener Gene, welche direkt oder indirekt an dem Prozess der Myelinisation beteiligt sind, eingegangen. Weitere Erkrankungen, die in dieser Arbeit Berücksichtigung finden, sind die hereditäre Neuropathie mit Neigung zu Druckläsionen [(HNPP), engl. hereditary neuropathy with liability to pressure palsies], Dejerine-Sottas-Syndrom (HMSN III) und die kongenitale Hypomyelinisationsneuropathie. Die „Ad Hoc Working Group of the Peripheral Nervous System“ präsentiert 1999 im Italian Journal of Neurology Leitlinien für die Diagnose von CMT und verwandten Neuropathien. Gemäß dieser Arbeitsgruppe sollte die Diagnose nach folgenden Schritten ablaufen: Identifikation des Vererbungsmodus, Elektrophysiologie, molekulargenetische Untersuchung und besonderen Fällen vorbehalten, eine Nervenbiopsie (Pareyson et al., 1999). 1 Einleitung Die CMT folgt meist einem autosomal-dominanten Erbgang. In ca. 10% der Fälle kommt eine CMTX (Cx32), also ein X-chromosomal gebundener Erbmodus vor (Pareyson et al., 2003). Die autosomal rezessiven Formen sind hingegen eher selten. Auch treten sporadische Fälle auf, welche wahrscheinlich auf de novo Mutationen zurückzuführen sind. Die Vererbung ist nicht immer leicht zu verfolgen, da es erstens einen hohen Grad an Variabilität des Phänotyps und zweitens oligosymptomatische Patienten gibt, die sich häufig der Diagnose entziehen. Deshalb ist auch eine klinische, elektrophysiologische und molekulargenetische Untersuchung von erstgradigen Verwandten nötig, um die Vererbung zu verifizieren. Für die elektrophysiologische Diagnostik ist nicht nur die bloße Präsenz einer Nervenleitungsverzögerung entscheidend, sondern auch der Grad und das Muster. Die demyelinisierende CMT1 zeigt eine diffuse Verlangsamung der Nervenleitgeschwindigkeiten (NLG), welche per definitionem in motorischen Fasern unterhalb von 38m/s liegt. Konträr dazu ist die Nervenleitgeschwindigkeit bei der axonalen CMT2 vollständig erhalten oder nur mild abgeschwächt und liegt über dem Limit von 38m/s (Pareyson et al., 1999). Die CMTX bietet ein eher unspezifisches Bild. Die Nervenleitgeschwindigkeit ist bei männlichen Patienten wesentlich stärker herabgesetzt als bei weiblichen. Obwohl es eine große Variationsbreite gibt, findet sich bei den meisten männlichen Patienten eine intermediäre NLG, die zwischen der CMT1 und CMT2 (30-45m/s) liegt, während die weiblichen Patienten eher unbeeinflußt bleiben (Lewis et al., 2000; Dubourg et al., 2001). Andere besondere Merkmale der CMTX sind eine Asymmetrie, eine größere Verzögerung der NLG des Nervus medianus gegenüber dem Nervus ulnaris, eine nicht uniforme Verzögerung über den gesamten Nervenstrang und sogar eine Blockade (Lewis et al., 2000; Dubourg et al., 2001). Die breite Mehrheit der CMT1 Fälle (60-90%) ist auf eine Duplikation auf dem Chromosomenlocus 17p11.2 zurückzuführen, welcher dem Genlocus für das periphere myelin Protein 22 (CMT1A) entspricht; Mikromutationen, die entweder PMP22 (1%) oder Myelin Protein zero (P0, MPZ; CMT1B; 4-5%) betreffen, sind eher selten (Valentijn et al., 1992; Warner et al., 1996). Ferner besteht eine Kausalität zwischen der CMT1 und dem Gen EGR2 (Warner et al., 1998) und vor Kurzem wurde ein neues relevantes Gen, das putative protein degradition gene (LITAF/SIMPLE), im Zusammenhang mit der CMT1 identifiziert (Street et al., 2003). Der axonale Typ, CMT2, ist ebenfalls genetisch sehr heterogen und weist neben MPZ auch andere assozierte Gene wie das neurofilament light gene (NEFL) auf (De Jonghe et al., 2001). Auch wurden über Mutationen im small GTP-ase late endosomal protein RAB7 (CMT2B) und GARS (glycyl-t-RNA synthetase) berichtet. Einer autosomal-rezessiven Form der axonalen CMT2 konnten Mutationen im Lamin A/C nuclear envelope protein gene (LMNA) zugeschrieben 1 Einleitung werden (De Sandre-Giovannoli et al., 2002). Histopathologische Merkmale der CMT1 sind segmentale De- und Remyelinisierugsprozesse, die durch Vermehrung von Schwann-Zellen und endoneuralem Kollagen zur Ausbildung von sogenannten Zwiebelschalendeformationen führen. Regelmäßig finden sich auch hypermyelinisierte Nerven-fasern, oft auch assoziiert mit atrophischen Nervenfasern (Schröder 1996). Im Gegensatz dazu die CMT2, welche primär eine Beteiligung des Axons aufweist, wie der Erhalt oder die nur mild abgeschwächte Nervenleitgeschwindigkeit sowie eine normale distale Latenz beweisen. Im histologischen Präparat findet sich eine reduzierte Anzahl großer myelinisierter Nervenfasern sowie Ansammlungen regenerierender Axone. Im Sinne von stattfindender Degeneration und Regeneration zeigen sich in Nervenbiopsien axonale Aussprossungen als Ausdruck chronischer Umbauvorgänge, auch sieht man zwiebelschalenformationsähnliche Strukturen (Kleopa et al., 2002). Bei CMTX-Patienten ähneln die morphologischen Charakteristika ebenfalls einem primär axonalen Geschehen, bei dem demyelinisierende Anzeichen erst sekundär nachzuweisen sind (Hahn et al., 1990; Hahn et al., 1993; Senderek et al., 1998). So offenbaren Nervenbiopsie-Querschnitte einen progredienten Ausfall insbesondere großkalibriger, myelinisierter Fasern, begleitet von reichlich Gruppen regenerierter Nervenfasern. Diese dünn myelinisierten regenerativen Axone bilden typische Gruppierungen und werden von konzentrisch angeordneten Schwann-Zellfortsätzen umgeben, so daß sie letztendlich Zwiebelschalenformationen ähneln. Darüber hinaus lassen sich Büngner’sche Bänder und strukturelle Veränderungen axonaler Komponenten als Zeichen chronischer Faserverluste darstellen (Senderek et al., 1998). Das Dejerine-Sottas-Syndrom (DSD) ist eine seltenere Erkrankung, die wie die CMT genetisch sehr heterogen ist. Viele klinische Symptome sowie pathologische und elektrophysiologische Kriterien manifestieren sich in beiden Erkrankungen, was einige Autoren veranlaßte, DSD nicht als eigene Krankheitsentität, sondern vielmehr als Variante der CMT zu betrachten. Die diagnostischen Kriterien basieren auf der Ausprägung oder genauer der Intensität des Phänotypes. Zeichen der Erkrankung sind: Beginn der Erkrankung im Alter von zwei Jahren, schwere motorische und sensible Defizite mit Beteiligung proximaler Muskelgruppen. Eine Ataxie scheint ein häufiges Symptom, ebenso wie die Skoliose. Die Nervenleitgeschwindigkeit motorischer Fasern kann auf unter 12m/s reduziert sein; histologisch finden sich Zeichen einer schweren Demyelinisation und Hypomyelinisation (Tyson et al., 1997; Pareyson, 1999; Plante-Bordeneuve et al., 2002). Auch zeigen sich hier charakteristische Zwiebelschalendeformitäten. Marklose Axone können auch betroffen sein, es zeigt sich zwar keine absolute Verringerung ihrer Anzahl, wohl aber eine Reduktion ihrer durchschnittlichen Stärke. 1 Einleitung Die kongenitale hypomyelinisierende Neuropathie (CH) ist eine seltene Subform der DSD mit kongenitalem Krankheitsbeginn. Im histologischen Präparat beweisend sind Zeichen einer puren Hypomyelinisation ohne kompaktes Myelin und ohne Zerfall des Myelins (Warner et al., 1996). Andere Autoren berichten auch über ein verstärktes Auftreten von Zwiebelschalendeformitäten (Bornemann et al. 1996), andere wiederum nicht (Seitz et al.1986). DSD konnte mit einigen Genen assoziiert werden, welche auch in kausalem Zusammenhang mit dem CMT-Syndrom stehen: PMP22, MPZ, EGR2 und PRX (Valentijn et al., 1992; Roa et al., 1993; Warner et al., 1996; Boerkoel et al., 2001,). Die meisten veröffentlichen Fälle scheinen de novo Mutationen zu sein. Selten sind autosomal rezessive, autosomal dominante oder homozygote Fälle. Die hereditäre Neuropathie mit Neigung zu Drucklähmung (engl. Hereditary neuropathie with liability to pressure palsies HNPP, tomaculous neuropathy) ist eine autosomal dominante Erkrankung, charakterisiert durch akut einsetzende und transiente Episoden fokaler Neuropathien, welche typischerweise schmerzlos sind und rekurrent verlaufen. Die Erkrankung kann nach einem trivialen Trauma auftreten oder durch Druck ausgelöst werden. Vielfach läßt sich aber ein auslösendes Ereignis nicht eruieren (Pareyson et. al., 1996). Episodisch verlaufende Mononeuropathien an typischen Stellen für Nervenkompression ist ein Hauptsymptom der HNPP (Windebank et al., 1993). Die am häufigsten betroffenen Segmente sind der Nervus ulnaris, radialis und der peronaeus sowie der Plexus brachialis. Aber auch andere Nerven können betroffen sein, so daß es zu atypischen Symptomen kommt (Mouton et al., 1999). Bei der Hälfte der Patienten kommt es zu einer vollständigen Restitutio innerhalb von Tagen bis Monaten. Bei einigen Patienten mit HNPP verbleiben Defizite, andere entwickeln eine progressiv verlaufende generalisierte senso-motorische Neuropathie (Gouider et al., 1995). Während akuter Episoden von Drucklähmungen können elektrophysiologische Untersuchungen Leitungsblöcke aufzeigen (Sellman et al., 1987). Zusätzlich zu den fokalen Veränderungen kommt es, besonders in den oberen Extremitäten zu einer diffusen Verzögerung der distalen Latenz sowie der NLG sensorischer Nerven. Die motorische Nervenleitgeschwindigkeit ist minimal verzögert, die distale motorische Latenz durchweg verlängert. HNPP-Patienten klagen oft über durch Druck ausgelöste Paraesthesien, wie z.B. nach Übereinanderschlagen der Beine, Aufstützen der Ellenbogen etc. In ca. einem Drittel der Fälle zeigt sich bei den Patienten ein pes cavus. Der Ausprägungsgrad der Erkrankung reicht von asymptomatisch bis zum Vollbild einer schweren generalisierten Neuropathie (Stögbauer et al., 2000). Auch zeigt die Elektrophysiologie unterschiedliche Schweregrade. Histopathologisch findet sich eine typische fokale Myelinverdickung (Tomacula) mehrerer Fasern, welche eine wurstartige Umfangszunahme bis auf 300% verursachen kann. Ca 25% der Fasern können so verändert sein. Ein weiteres, allerdings nicht eindeutiges Charakteristikum sind segmentale/paranodale 10 1 Einleitung De- und Remye­linisationsvorgänge, wie sie auch bei der CMT1 zu finden sind. Auch sind die Tomakula zwar Hauptcharakteristikum der HNPP, können aber in fortgeschrittenen Stadien fehlen (Schröder 1999) oder bei anderen Erkrankungen wie der CMT1 (Thiex und Schröder 1998), der Anti-MAG-Neuropathie oder der chronischen inflammatorischen demyelinisierenden Polyneuropathie (CIDP) (Pareyson et al., 2004) ebenfalls auftreten. HNPP ist meist mit einer Deletion der 17p11.2 Region assoziert (Stögbauer et al., 2000), selten wurde auch eine kausale PMP22 Mutation demonstriert (Van de Wetering et al., 2002). Eine allgemeingültige Klassifikation des Komplexes der hereditären Neuropathien ist zum gegenwärtigen Zeitpunkt nach wie vor schwierig. Einerseits werden Einteilungen ausschließlich in Bezug auf klinische und neuropathologische Ausprägungen verwandt, gleichwohl halten auch Einteilungen auf molekular-genetischer Ebene verstärkt Einzug in die momentanen Klassifikationen, woraus sich deutliche Schwierigkeiten ergeben: Erstens identifiziert die Molekulargenetik immer neue kausale Gene, zweitens sind die Daten über die Genotyp-Phänotyp Korrelation zum heutigen Zeitpunkt nach wie vor unvollständig. Auch findet sich ein zunehmend unterschiedlicherer Gebrauch der Bezeichnungen HMSN und CMT. HMSN wird eher in der klinischen Literatur verwandt, wohin gegen die Molekularbiologie die Bezeichnung CMT favorisiert. Die meisten Klassifikationen zeigen eine grundlegende Einteilung in Anlehnung an elektrophysiologische Kriterien, CMT1 (demyelinisierend) und CMT2 (axonal), und eine weitere Unterteilung nach dem Vererbungsmodus (autosomal dominant, rezessiv und X-chromosomal gebunden). Weitere Subklassen werden numerisch oder alphabetisch belegt, worüber es aber bis heute unter den bekannten Autoren keine generell akzeptierte Übereinkunft gibt (Reilly et. al., 2002). Diese Arbeit befaßt sich ausschließlich mit der Identifizierung von Mutationen des MPZ-, des PMP22-, des Connexin32- und des EGR2-Gens, also mit Genen, die für myelinassoziierte Proteine kodieren. An entsprechender Stelle wird allerdings auf alle relevanten Genloci, sofern für das Verständnis und die Vollständigkeit notwendig, eingegangen. Die Identifikation wurde anhand von Archivmaterial des Neuropathologischen Institutes der RWTH-Aachen (Direktor i.R.: Univ.-Prof. Dr. med. J. M. Schröder) durchgeführt. Es handelte sich hierbei sowohl um Glutaraldehyd- als auch Formalin-fixierte und in Paraffin eingebettete Nervus-suralis-Biopsien sowie um Muskelbiopsien. Auch wurde DNA aus Frischmaterial (Blut und Nerv) verwandt. Zusätzlich wurden Proben der Neurologischen Abteilung des Klinikums OPNI, Budapest (Ungarn), dem Probenumfang hinzugefügt. Das Material wurde zuvor nach histomorphologischen Gesichtspunkten vorselektiert. Es wurden nur Patienten in die Untersuchung auf eine genetische Aberration aufgenommen, bei denen eine CMT, eine hereditäre Neuropathie mit Neigung zu 11 1 Einleitung Druckläsionen (HNPP), oder ein Dejerine-Sottas-Syndrom (HMSN III) unter klinischen und oder neuropathologischen, respektive licht- und elektronenmikroskopischen Gesichtspunkten diagnostiziert wurde. Ziel dieser Arbeit ist neben der Etablierung und Optimierung der angewandten Verfahren auch ein besseres Verständnis der Genotyp-Phänotyp Korrelation zu erreichen. Das exponentiell wachsende Wissen über die molekulargenetischen Grundlagen des Erkrankungsmechanismus und die Identifikation immer neuer kausaler Gene sowie das wachsende Verständnis über die Bedeutung der molekulargenetischen Ursachen für effektive Therapiestrategien machen ein etabliertes, möglichst unkompliziertes Screeningverfahren für die moderne Medizin unumgänglich. Nicht zuletzt können die gewonnenen Erkenntnisse über die Genprodukte und deren Bedeutung für die physiologische oder pathophysiologische Aktivität den Boden für zukünftige, vielleicht sogar kausale Therapien bereiten. Auch zeigt diese Arbeit, daß aus entsprechend behandelten Materialien, welche über Jahre hinweg archiviert worden sind, noch eine effektive DNA-Extraktion erfolgen kann. Damit kann retrospektiv eine Klassifizierung, ggf. eine Reklassifierung durchgeführt werden. Die so gewonnenen Daten bieten eine Grundlage zur Erstellung genetischer Stammbäume und sichern Erkenntnisse über Vererbungsmodi. Auf diese Weise wird eine kompetente humangenetische Beratung für betroffene Familien möglich. 1.1 Historische Entwicklung Die Erstbeschreibung von Erkrankungen mit ähnlichen Symptomen wie die heute als HMSN subsummierten Krankheitsentitäten reicht bis in das späte 19. Jahrhundert zurück. Virchow beschrieb 1855, noch vor den in die Nosologie eingegangenen Autoren Charcot und Marie (Frankreich) und Tooth (England) eine Familie mit „progressiver distaler Muskelatrophie“. Andere berühmte Ärzte wie Aran (1855), Hemptenmacher (1862), Eulenberg (1856) und Friedrich (1873) veröffentlichten zu dieser Zeit Krankheitsfälle, die durch eine fortschreitende distale Muskelatrophie gekennzeichnet waren (Pearce et al., 2000). Virchow, Hemptenmacher, Eichhorst zeigten auf, daß gewisse Krankheitssymptome in aufeinanderfolgenden Generationen betroffener Familien auftraten, was den Schluß auf einen dominanten Vererbungsmodus zuläßt (Lindkvist et al., 1999). Schulz (1884) faßte erstmalig die klinischen Symptome dieser Krankheitsgruppe zusammen, wobei er sich auf vorangegangene Arbeiten und Fallbeschreibungen von Friedreich und Eichhorst stützte. Auch beobachtete er, ähnlich wie Eulenberg, einen Krankheitsverlauf bei mehreren Geschwistern, was auf einen rezessiven Erbgang rückschließen läßt. Herringham (1889) beschrieb eine Sippe, in der Erkrankungsfälle ausschließlich bei männlichen Angehörigen auftraten, was wiederum einen X-chromosomal gekoppelten Vererbungsmodus nahe legt. 12 1 Einleitung Die in die Nosologie eingegangenen französischen Neurologen Jean Martin Charcot (1825-1893) und sein Schüler Pierre Marie (1854-1940) publizierten im Februar 1886 unter dem Titel: „Sur une forme particulière d`atrophie musculaire progressive, souvent familiale, débutant par les pieds et les jambes et atteignant plus tard les mains“ das Krankheitsbild der peronealen Muskelatrophie, welches sie an fünf Kindern am Hôpital de Salpetière in Paris studierten (Bonduelle et al., 1994; Sorensen et al., 1996). Nahezu zeitgleich veröffentlichte Howard Tooth (1856-1926) im Jahre 1886 eine Arbeit an der Cambridge University in England zum Thema „The peroneal type of progressive muscular atrophy“. Alle drei Autoren zeigten auf, daß ein langsamer, aber progredienter Verlauf der Erkrankung mit vorwiegend distal akzentuierter Parese und Muskelatrophie symptomatisch sei. Initial sei zunächst die untere, im weiteren Verlauf auch die obere Extremität betroffen. Auch beschrieben sie einen eher von motorischen Defiziten geprägten als einen das sensible System betreffenden Verlauf sowie charakteristische Fußdeformitäten. Der Krankheitsbeginn variierte von einem juvenilen bis adoleszenten Typ. Zwar herrschte Übereinkunft über die Symptomatik, Charcot und Marie gingen allerdings von einer ursächlichen Erkrankung des Myelons aus, wohingegen Tooth, ähnlich wie Hoffmann, der den Begriff der „neuralen Muskelatrophie“ prägte, eher das pathologische Korrelat im peripheren Nervensystem vermuteten. 1893 beschrieben Dejerine, der Nachfolger Charcots auf dessen Lehrstuhl für Nervenkrankheiten am Hôpital de la Salpetrière in Paris war, und sein Kollege Sottas die Krankengeschichte zweier Geschwister phänotypisch offenbar gesunder Eltern unter dem Begriff der „progressiven hypertrophischen Neuritis“. Bei diesen Patienten waren deutlich verdickte Nervenstämme zu tasten. Es zeigten sich ferner eine generalisierte Muskelschwäche, Areflexie sowie ein Sensibilitätsverlust und ein besonders schwerwiegender, früh einsetzender Verlauf (Dejerine und Sottas 1893, Schurch und Dollfus 1998). Eine von Roussy und Lévy 1926 unter dem Namen „Dystasie aréflexique héréditaire“ publizierte Erkrankung, auch als Roussy-Levy-Syndrom bezeichnet, betrifft ein Krankheitsbild, welches eine ähnliche Klinik mit Hohlfußdeformitäten, progredienter Muskelatrophie und Areflexie beinhaltete, aber zusätzlich eine cerebelläre Ataxie, Intentionstremor und Pyramidenbahnzeichen aufwies. Anfang des 20. Jahrhunderts wurde erstmalig von Davidenkow 1927 der Versuch unternommen, alle bis dato beschriebenen hereditären Neuropathien in einer zwölf Subtypen umfassenden Klassifikation zu einen. Während der nächsten fünfzig Jahre setzte sich die klinische und pathologische Beschreibung verschiedener Formen hereditärer sensomotorischer Neuropathien fort. Es wurde eine bemerkenswerte Anzahl von Klassifikationsschemata, klinischen Erscheinungsbildern und Eponymen publiziert, welchen es allerdings an Klarheit und Allgemeingültigkeit mangelte (Dyck und Lambert, 1968). Mitte der fünfziger Jahre, als die Elektrophysiologie Einzug in die Klinik erhielt, wur- 13 1 Einleitung de es bedingt möglich, die HMSN/CMT adäquat zu klassifizieren. Henriksen war 1956 einer der ersten, der die CMT Typ 1 mit deutlich verlangsamter Nervenleitungsgeschwindigkeit von der CMT Typ 2 mit annähernd normaler NLG abgrenzte. Unter Einbezug einer weiteren technischen Neuerung, der Elektronenmikroskopie, konnten, wie eingangs beschrieben, histomorphologische Korrelate sowie eine eher axonale von einer markscheidendegenerativen (demyelinisierenden) Veränderung den Beobachtungen der Elektrophysiologie gegenübergestellt werden. Diese Untersuchungen zeigten, daß es zumindest zwei unterschiedliche pathologische Prozesse gibt, welche zu ähnlichen klinischen Erscheinungsbildern führen. Erst als die Genetik verstärkt in die klinische Diagnostik einbezogen wurde, konnte gegen Ende des zwanzigsten Jahrhundert die HMSN-Forschung weiter voran getrieben werden. 1982 zeigten Bird und Kollegen in einer der ersten Kopplungsstudien neurologischer Erkrankungen, daß in Familien mit CMT Typ1 kausale Gene der demyelinisierenden Form mit dem Duffy-BlutgruppenLocus auf Chromosom 1 gekoppelt sind (Bird et al., 1982). Nachfolgende Studien, basierend auf DNA-Polymorphismen, belegten allerdings eine Kopplung mit dem kurzen Arm des Chromosoms 17 (Vance et al., 1989), wieder andere bewiesen eine X-chromosomale Kopplung. Diese Tatsachen unterstützten die Spekulationen, daß mehr als ein Gen in ursächlichem Zusammenhang mit der Erkrankung stehen könnte. Während der zurückliegenden 10 Jahre wurde das Wissen über genetische Ursachen der CMT und verwandten Neuropathien stark erweitert. Bis zum heutigen Zeitpunkt wurden mindestens 23 Gene und 30 chromosomale Loci mit relevantem Bezug zu hereditären sensomotorischen Neuropathien identifiziert (Dubowitz et al., 2005). Zwar konnten in den letzten Jahren immer neue Gene, respektive chromosomale Loci, in Korrelation zu der HMSN Erkrankung gebracht werden, aber es zeigten sich auch in einigen Fällen Diskrepanzen: Die Charcot-Marie-Tooth Erkrankung Typ2A wurde zunächst einer 9.3 cM großen Region auf Chromosom 1p35-36 zugeschrieben und es konnte in einer japanischen Familie eine „missense-Mutation“ im KIF1B-Gen (c.293A→ T; p.Gln98Leu) als pathologisches Korrelat identifiziert werden (Zhao et al., 2001). Weitere Untersuchungen anhand einer türkischen CMT2A-Familie, in der durch Linkage-Studien der CMT2A-Locus in einer 9.3 cM großen Region auf Chromosom 1-p35-36 zu finden war, konnten allerdings keine Mutation innerhalb des KIF1B-Gens identifizieren (Bissar-Tadmouri et al., 2004). Diese Ergebnisse scheinen die Kausalität des KIF1B-Gen für die CMT2A zu widerlegen. Um solchen Neuerungen Rechnung zu tragen, wird in dieser Arbeit eine Einteilung zu Gunsten nach Genen favorisiert (siehe Tabelle Dubowitz et al., 2005), anstelle eher auf klinischen Symptomen oder histomorphologischen Untersuchungen beruhender Klassifikationen. 14 1 Einleitung In für das Verständnis relevanten Passagen und aus historischen Gründen wird aber auch auf frühere Klassifikationen sowie auf früher als eigenständige Krankheitsentitäten verstandene Subtypen eingegangen. 1.2 Biologische Hintergründe und Embryologie Der Aufbau der Markscheide wird am besten verständlich, wenn man sich die enge Beziehung zwischen Axonen und Schwann-Zellen während der Entwicklung vor Augen führt. Die meisten peripheren Nerven bestehen sowohl aus motorischen als auch aus sensorischen Axonen, welche in ihrer Länge von Schwann-Zellen umhüllt sind. Während der Entwicklung des peripheren Nervensystems (PNS) enstehen Schwann-Zellen aus der Neuralleiste (Crista neuralis), migrieren und kontaktieren die sich entwickelnden peripheren Axone (Harrison, et al., 1924; Le Douarin u. Dupin, 1993). In Invaginationen der noch unreifen, sich proliferierenden Schwann-Zellen kommen gruppenweise mehrere nackte Axone zu liegen. In einem weiteren Schritt kommt es zu einer Differenzierung in myelinbildende und nicht myelinbildende Schwann-Zellen. Schwann-Zellen, welche in einer eins zu eins Relation mit einem Axon stehen, das sogenannte Promyelinationsstadium, initiieren den Prozess der Myelinbildung. Im Gegensatz kommt es bei Schwann-Zellen, die sich nicht mit einem Axon assoziiert haben, nicht zu einer Akitivierung der Myelin-Gen-Expression (Webster et al., 1993; Mirsky et al., 1996; Scherer et al., 1997; Benninghoff, Anatomie Band 2 Auflage 15). Es zeigt sich also, daß alle unreifen Schwann-Zellen das Potential zu Myelinbildung haben. Nur durch die Beeinflussung des mit ihnen in Beziehung stehenden Axons kann dieses auch abgerufen werden; es scheint also die Integrität dieser Axon-Schwann-Zell Interaktion verantwortlich für die Expression wichtiger myelinverwandter Proteine und der zugrundeliegende mRNA zu sein 12 (Griffin et. al., 1993; Scherer et. al., 1997). Abbildung 1: Schematische Darstellung der Myelinisation durch Schwannzellen. Aufgezeigt sind der Prozeß der Transkription, Translation, „Protein-Trafficking“ sowie die „myelin-compaction“ (Kamholz et al., 2000) 15 1 Einleitung Axonale Degeneration führt zur sogenannten Waller’schen Degeneration, wobei die Myelinscheide phagozytiert, myelinisierende Schwann-Zellen dedifferenzieren und die Expression der mRNA herunterreguliert wird. Sollten sich aber die Axone regenerieren, kommt es zu erneutem Einscheiden und Expression der myelinassozierten Proteine und der zugrundeliegenden mRNA. Fast alle myelinbezogenen Proteine und deren mRNA werden in dieser Art und Weise beeinflußt, auch die für diese Arbeit relevanten Proteine wie MPZ, peripheres Myelin Protein 22 (PMP22), Connexin 32 (Cx32). Ferner zeigen auch Proteine wie das Myelin-assoziierte Glycoprotein (MAG), Myelin basic Protein (MBP) und Periaxin dieses Verhalten. Während die Axon-Schwann-Zell-Interaktion und deren Bedeutung für den Prozeß der Myelinisierung momentan noch Gegenstand der Forschung ist, sind zwei Transskriptionsfaktoren bekannt, nämlich Oct-6 (a POU domain family) und EGR2 (ein Zink-Finger-Protein), welche essenziell für die normale Entwicklung myelinisierender Schwann-Zellen (Topilko et. al., 2001) sind. Vor Kurzem konnte in einem Versuch mit entweder Oct-6 -/-, oder EGR2 -/„Knock-out-Mäusen“ gezeigt werden, daß ein Fehlen dieser Gene ursächlich für eine drastisch reduzierte Anzahl an myelinisierten Axonen ist, was wahrscheinlich auf ein Ausbleiben der Schwann-Zellen-Differenzierung zurückzuführen ist. Es kommt zu einem Überschuß an sogenannten Promyelin-SchwannZellen (Kleopa et. al., 2002). Die primäre Funktion der Myelinscheide ist die signifikante Erhöhung der axonalen Nervenleitgeschwindigkeit, ohne den Durchmesser der Axone wesentlich zu beeinflussen. Dies wird durch die saltatorische Erregungsleitung, also einem Sprung des Nervimpulses zwischen zwei elektrisch erregbaren Regionen des Axons, den sogenannten Ranvier-Schnürringen, erreicht. Die Ranvierschen Schnürringe liegen zwischen elektrisch isolierten Arealen, also zwischen den Bereichen des Axons, welche von Myelinscheiden umgeben sind. Ergo reduziert sich durch eine geringere Myelindichte die Geschwindigkeit der Erregungsfortleitung. Der Schlüssel für das Verständnis, wie Mutationen in den oben genannten Genen eine Neuropathie verursachen, liegt in der Architektur myelinisierter Axone. Myelin ist eine multilamilläre Spirale spezialisierter Zellmembranen, die die Axone einscheidet. Die Myelinscheide hat zwei Regionen, eine kompakte und eine nicht kompakte. Jede Domäne enthält eigene spezialisierte Proteine (Abbildungen 1 und 2). MPZ, PMP22 und MBP sind Myelinstrukturproteine, die am Aufbau und der Intigrität der kompakten Regionen beteiligt sind. Die nichtkompakte Region wird nochmals in zwei Subdomänen untergliedert, die paranodale und die juxtaparanodale Zone (Paranodium). Die paranodale Zone bildet die Abgrenzung gegenüber den Ranvierschen Schnürringen. In ihr laufen die zungenförmigen zytoplasmatischen Fortsätze der Markscheidenlamellen [im Elektronenmikroskop Hauptlinien (major dense lines)] aus, welche 16 1 Einleitung untereinander durch tight und gap junktions sowie Desmosomen verbunden sind und auch mit der axonalen Membran respektive mit der nodalen Gap-Substanz interagieren. Diese Region enthält Schwann-Zell-Proteine wie MAG, Connexin32, Neurofascin155 und axonale Proteine wie Caspr und Contactin, die alle an der Interaktion der Schwann-Zellen untereinander sowie der Interaktion zwischen axonalen Strukturen und den Schwann-Zellen mitverantwortlich sind. Die juxtaparanodale Zone entgegen enthält K+-Kanäle sowie das Protein Caspr2, welche durch die Axone exprimiert werden (Gemignani et al., 2001). Im folgenden Kapitel sollen nun die speziellen Funktionen der Proteine MPZ, PMP22, Connexin32 sowie des Transkriptionsfaktors EGR2 im Detail beleuchtet und in Relation zu den hereditären Neuropathien gebracht werden. Abbildung 2: Schematische Ansicht eines myelinisierten Axons und einer myelinisierenden Schwann-Zelle sowie die Lokalisation der Proteine, welche mit hereditären Neuropathien assoziiert sind. Die in der oberen Abb. rot umrandete Region ist unten vergrößert dargestellt. Illustriert sind die zytoskelettalen Elemente des Axons sowie die Anordnung der Proteine in den Paranodien, der juxtaparanodalen Region und den Ranvierschen-Schnürringen (Shy et al., 2002). 17 18 2 Hereditäre sensomotorische Polyneuropathien unter spezieller Berücksichtigung der Gene PMP22, MPZ (P0), Connexin32 sowie EGR2 2.1 Peripheres Myelin Protein 22 (PMP22) PMP22 stellt eine wichtige Komponente des peripheren Nervensystems dar. PMP22 ist ein 160 Aminosäuren umfassendes Glykoprotein, das die Plasmamembran viermal durchzieht. Es macht 2-5% des Gesamtproteins im peripheren Nervensystem in Säugetierzellen aus (Jetten et al., 2000). Das Protein hat mutmaßlich vier transmembranöse Domänen (TM), zwei extrazelluläre Schleifen (EC) und eine intrazelluläre Schleife (IC) sowie einen zytoplasmatischen N und C Terminus (N und C) [D`Urso u. Müller, 1997]. Die Aminosäuresequenz und die angenommene Sekundärstruktur sind in der folgenden Graphik schematisch dargestellt. Abbildung 3: Bekannte Mutationen des PMP22 Leserahmens. Die Buchstaben geben Hinweis auf die Aminosäurereste. Die Farben implizieren die korrespondierenden Neuropathien (Shy et al., 2002) 19 2 Hereditäre sensomotorische Polyneuropathien unter spezieller Berücksichtigung ... Zusammen mit dem Glykoprotein P0 findet sich PMP22 vornehmlich innerhalb des kompakten Myelins. PMP22 und P0 sind essentiell für die Myelinscheide. P0 scheint dabei durch trans-homophile Interaktion zwischen gegenüberliegenden Molekülen eine Adhäsion der unterschiedlichen Schichten zu generieren (Shapiro et al., 1996; Carenini et al., 1999; Arroyo et al., 2000). PMP22 ist entweder direkt mit P0 assoziiert, oder geht selbst Interaktionen mit gegenüberliegenden Membranschichten in trans-Konfigurität, oder cis-Konfigurität mit derselben Membranschicht ein (D’Urso et al., 1999). Diese Interaktionen verstärken die Adhäsion unterschiedlicher Schichten innerhalb des kompakten Myelins und scheinen auch eine wichtige Grundlage für die Regulation der Schwannzell-Proliferation und der Myelin-Produktion durch PMP22 zu sein (Shapiro et al., 1996; Carenini et al., 1999; Jetten et al., 2000). Das PMP22-Gen umfaßt annäherungsweise 40kb und beinhaltet vier kodierende Exone (Exon 2 bis 5), sowie zwei 5‘ nichttranslatierte Exone (Exon 1A und 1B) (Suter et al., 1994). Die Expression von PMP22 wird durch zwei Promotoren reguliert, welche upstream der Exone 1A und 1B lokalisiert sind. Es finden sich zwei gewebespezifische Formen (neuronal und nichtneuronal) der Transkripte. Transkripte, die das 1A Exon beinhalten, werden präferiert in myelinisierenden Schwann-Zellen gebildet, während 1B Transkripte eher in nichtneuronalen Geweben gefunden werden (Suter et al., 1994). Das alternative 1B Transkipt ist in Lungen-, Intestinalgewebe und in Herz- und Skelettmuskeln präsent. Ferner konnten PMP22 Transkripte durch insitu Hybridisationen während der embryonalen Entwicklung in murinalem Gewebe lokalisiert werden (Baechner et al., 1995; Parmantier et al., 1997). Während der Entwicklungsphase ist PMP22 in allen drei Keimblättern und in Zellen der Neuralleiste exprimiert (Hagedorn et al., 1999). In der postnatalen Entwicklungsphase findet sich PMP22 in den dorsalen Spinalganglien, den Motorneuronen der Spinalnerven sowie in den motorischen Kernen gewisser Hirnnerven (Parmantier et al., 1995; Parmantier et al., 1997; Paratore et al., 2002). In Einklang mit diesen Beobachtungen findet sich bei Patienten mit spezifischen Mutationen des Gens (z.B. W28R) eine sensoneurale Taubheit, welche entweder Folge einer Demyelinisierung des achten Hirnnervens darstellt oder aufgrund einer Fehlentwicklung des Innenohres, welches ein Derivat der Neuralleiste ist, zu werten ist (Boerkoel et al., 2001). Die weitere Bedeutung des PMP22 außerhalb des peripheren Nervengewebes ist noch nicht hinreichend geklärt. Allerdings wird eine Rolle als Regulator des Zellwachstums vermutet (Suter et al., 1994). Erstmalig im Rahmen einer Kopplungsstudie konnte aufgezeigt werden, daß ein Zusammenhang der Erkrankung mit dem Chromosomenlocus 17p11.2-12 besteht (Vance et al., 1989). Weitere Versuche mit positionellem Clonieren, um die Lokalisation der CMT1A zu spezifizieren, führten zur Identifikation einer DNA Tandem Duplikation auf Chromosom 17p11.2-12 (Raeymaekers et al., 1991; Lupski et al., 1992). Die Größe der Duplikation beträgt ca. 1,5 Megaba- 20 2 Hereditäre sensomotorische Polyneuropathien unter spezieller Berücksichtigung ... sen und repräsentiert eine genetische Distanz von ca. sechs Centimorgen (Raeymaekers et al., 1991). Die Duplikation tritt sehr häufig als de-novo Ereignis auf; bei ca. 90% der Patienten mit sporadischer CMT1A vermutet man eine de-novo Genese. Es wurde zunächst ein alleiniger autosomal-rezessiver Erbgang antizipiert. Wesentlich frequenter präsentiert sich die de-novo Duplikation als Resultat einer fehlerhaften Spermatogenese. 10% der Fälle sind aber auch auf einen maternalen Ursprung, Fehler während Oogenese, zurückzuführen (Blair et al., 1996). Die Indentifikation der Duplikation in 17p11.2-12 warf Fragen nach den zugrundeliegenden molekularen Mechanismen auf: Erfolgt eine Frakturierung spezifischer Gene im Bereich der Bruchstellen oder resultiert der Phänotyp eher aus der zusätzlichen Kopie (sog. trisomatic overexpression) des Gens im Sinne eines Gendosiseffektes? Beobachtungen von Menschen und anderen Organismen halfen diese Fragen zu beantworten. Es konnte eine geringe Anzahl Patienten mit einer partiellen oder totalen Trisomie des Chromosomes 17p selektiert werden, welche konforme phänotypische Charakteristika der CMT1A aufwiesen (Feldman et al., 1982; Magenis et al., 1986). Dies unterstützte die Hypothese eines Gendosiseffektes. Weiteren Aufschluß über die CMT1 Pathogenese ergaben erst Tierversuche: Die dominanten Trembler (Tr) Mutationen (Trembler-J pmp22 Leu16Pro und Trembler pmp22 Gly150Asp) bei Mäusen resultieren in schwerer Demyelinisierung und teilweise Amyelinisierung, also ähnlichen Symptomen wie sie bei der CMT1 auftreten. Der Tr Locus (Chromosom 11 bei Mäusen) ist synthän mit dem menschlichen Chromosom 17p. Ein Gen, das growth arrested-specific gene (gas3), konnte dem Tr Locus zugeordnet werden, als eine Punktmutation im PMP22 Gen identifiziert wurde, welches dem gas3 identisch ist. Diese Beobachtungen führten zu der Annahme, daß PMP22 auf Chromosom 17p11.2-12 lokalisiert ist und kausal für die CMT ist. Diese Hypothese konnte bewiesen werden, als PMP22 eindeutig dem Chromosomlocus 17p11.2-12 zugeordnet werden konnte (Patel et al., 1990). Das PMP22-Gen wird in einem Gesamtabstand von ca. 1,5MB von zwei homologen repetetiven Sequenzen (ca.24kb) flankiert, den sogenannten distalen und proximalen CMT1A-Rep. Der hohe Grad der Homologenität kann zu einem ungleichen Crossing-over während der Meiose führen. Sowohl die Deletion und damit die HNPP als auch die Duplikation als Ursache einer CMT1A sind reziproke Produkte des gleichen Pathomechanismus (Chance et al., 1993). Die CMT1A ist per defenitionem mit dem Chromosom 17 verbunden und nahezu immer durch die Vererbung einer PMP22-Duplikation verursacht (Lupski et al., 2001). In großen Studien zeigte sich ein Beginn der Erkrankung zwischen dem 2. und 76. Lebensjahr mit einem Häufigkeitsgipfel gegen Ende der zweiten Lebensdekade (Biruok et al., 1997). Muskelschwäche, Atrophie, Hypaesthesien der unteren Extremitäten sowie Areflexie sind klinische Zeichen der Erkrankung. In einem mittleren Alter von vierzig Jahren zeigten sich milde oder keine 21