UV/VIS-Spektroskopie
Werbung

UV/VIS-Spektroskopie
1
UV/VIS-Spektroskopie
In diesem Versuch werden optische Eigenschaften schwacher Säuren mit einem Spektrometer
untersucht. Die pH-Abhängigkeit des spektralen Verlaufs der Absorption wird beobachtet,
und die molaren Absorptionskoeffizienten am isosbestischen Punkt und am Absorptionsmaximum werden bestimmt. Daraus ergeben sich die Dissoziationsgrade bei verschiedenen pHWerten sowie die Dissoziationskonstante KS der Säure.
Stichworte
•
•
•
•
•
•
•
•
Lambert–Beersches Gesetz
Absorbanz, Absorption, Transmission
Säure/Base-Gleichgewicht, pH-Wert
Dissoziation, Dissoziationskonstante
isosbestischer Punkt
Puffer, Puffergleichung
elektromagnetische Strahlung und elektromagnetisches Spektrum
Lichtbeugung und Lichtbrechung
Absorption elektromagnetischer Strahlung
Fällt Licht der Intensität I auf ein absorbierendes Medium, hier eine Lösung der Konzentration
c, so wird es abgeschwächt. Die Abschwächung dI ist proportional zum durchlaufenen Weg
ds, der Konzentration c und der eingestrahlten Intensität I:
dI = k() I c ds
(1)
Der Proportionalitätsfaktor k() ist der wellenlängenabhängige molare Absorptionskoeffizient
(früher: Extinktionskoeffizient). Nach Integration erhält man das Lambert-Beersche Gesetz
It = I0 ek()cs = I0 10()cs
(2)
Dabei ist I0 die eingestrahlte und It die transmittierte Intensität. k und unterscheiden sich nur
hinsichtlich ihrer Exponentialbasis: = k lg e. wird daher häufig als dekadischer molarer
Absorptionskoeffizient bezeichnet. Die dimensionslose Größe
A = ()cs
(3)
heißt Absorbanz (veraltet: Extinktion, optische Dichte), das Verhältnis T = It / I0 Transmissionsgrad oder Durchlässigkeit. Eine Absorbanz von 1 heißt, dass 10% der eingestrahlten Intensität transmittiert werden (10% Transmissionsgrad bzw. 90% Absorptionsgrad). Anstelle des
Transmissionsgrads T wird auch oft der Absorptionsgrad 1 T angegeben.1
1
Leider herrscht in der deutschen Literatur – auch in der Lehrbuchliteratur – eine beträchtliche Verwirrung hinsichtlich der Benennung der Größen A und T. Es gibt nicht nur mehrere Begriffe für ein- und dieselbe Größe
(Absorbanz, Extinktion, optische Dichte), sondern ein Begriff bezeichnet je nach Autor unterschiedliche Größen.
So wird die Absorbanz A beispielsweise auch als Absorptionsmaß (www.photometer.ch), Absorptionsvermögen
Apparatives Praktikum Physikalische Chemie für Studierende der Biologie
TU Braunschweig, Institut für Physikalische und Theoretische Chemie, Dr. Christof Maul
WS2015/6
UV/VIS-Spektroskopie
2
Absorptionsmessungen können sowohl zur qualitativen als auch zur quantitativen Analyse
verwendet werden. Für die qualitative Analyse sind die Lage des Maximums bzw. der Maxima und die Intensität und Form der Absorptionsbanden von Bedeutung, da sie für die absorbierende Substanz charakteristisch sind. Zwar ist eine eindeutige Identifizierung von unbekannten Substanzen in Gemischen oft nicht möglich, aber für reine Substanzen ist die Zuordnung einer Struktur durch Vergleich des Spektrums mit den betreffenden katalogisierten
Spektren in der Regel durchführbar.
Quantitative Bestimmungen mit dem Spektrometer werden meist bei der Wellenlänge (oder in
dem Wellenlängenbereich) des Maximums der stärksten Absorptionsbande durchgeführt. Ist
allerdings der Absorptionsgrad zu groß (> 90 %), so geht man zweckmäßigerweise zu einer
schwächeren Bande über, da sonst die Lichtintensität am Detektor zu gering wird. Quantitative Analysen werden überwiegend mit Hilfe von Kalibrierkurven durchgeführt. Für mehrere
Kalibrierlösungen verschiedener Konzentrationen der zu bestimmenden Substanz trägt man
die gemessene Absorbanz A auf der Ordinate gegen die Konzentration c auf der Abszisse auf,
so dass man nach Gl. (3) eine Kalibriergerade mit der Steigung ε(λ)s erhält, die durch den Koordinatenursprung geht. Nach der Erstellung der Kalibrierkurve misst man die Absorbanz der
Lösung mit der unbekannten Konzentration der betreffenden Substanz. Aus der Kalibrierkurve ergibt sich dann sofort der zur gemessenen Absorbanz zugehörige Konzentrationswert.
Alle Messungen müssen bei der gleichen Wellenlänge, mit der gleichen Referenzküvette und
bei gleicher Temperatur durchgeführt werden. Für genaue Messungen ist eine Temperaturkonstanz von etwa ±1 K erforderlich.
Die Dissoziation schwacher Säuren
Die Dissoziation von Säuren
HA H+ + A−
4
kann spektrometrisch untersucht werden, wenn sich die optischen Eigenschaften, d.h. der
spektrale Verlauf der Absorptionskoeffizienten, von undissoziierter Säure HA und Säure-Anion A− ausreichend unterscheiden. Das System ist charakterisiert durch die Gesamtkonzentration c der Säure, die Konzentration cHA der undissoziierten Säure und die Konzentration cA−
der dissoziierten Säure, wobei gilt, dass c = cHA + cA−.
Der Dissoziationsgrad α gibt den in Lösung dissoziiert vorliegenden Anteil an, d.h.
α =
cA
c
-
=
cA
-
cA +c HA
(5)
-
(Wedler, 4. Aufl.), oder sogar nur als Absorption (Atkins, 3. Aufl.) bezeichnet. Daher soll hier der Begriff Absorption keine Verwendung finden und die Größe 1 – T als Absorptionsgrad bezeichnet werden. Extinktion und
Extinktionskoeffizient sind veraltete Bezeichnungen und werden deshalb hier nicht verwendet. Insbesondere für
optische Dichte existieren widersprüchliche Definitionen, so dass auch diese Bezeichnung hier vermieden wird.
Nach IUPAC ist Absorbanz = absorbance, Absorptionsgrad = absorptance, Transmissionsgrad = transmittance.
Apparatives Praktikum Physikalische Chemie für Studierende der Biologie
TU Braunschweig, Institut für Physikalische und Theoretische Chemie, Dr. Christof Maul
WS2015/6
UV/VIS-Spektroskopie
3
Für einen schwachen Elektrolyten nimmt er stark ab, wenn die Konzentration c vergrößert
wird. Starke Elektrolyten dagegen liegen in Lösung immer vollständig dissoziiert vor (α = 1).
Das Massenwirkungsgesetz liefert die Dissoziationskonstante KS der Säure gemäß:
KS =
cH cA
+
cHA
-
= cH
+
α
1−α
(6)
wobei für cA = c und für cHA = (1)c eingesetzt wurde. Für ungepufferte Systeme gilt außerdem c H =cA =α c . Gl. (6) wird dann zum Ostwaldschen Verdünnungsgesetz
+
-
KS =
α2 c
1−α
(7)
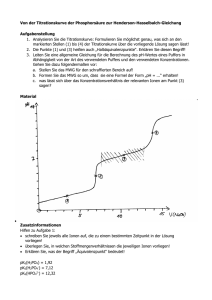
Ein typischer Verlauf der Absorptionsspektren schwacher Säuren in Abhängigkeit vom pHWert ist in Abbildung 1 dargestellt. Am isosbestischen Punkt iso sind die Absorptionskoeffizienten der undissoziierten Säure und des Anions gleich groß: HA(iso) = Aiso = iso. Der
isosbestische Punkt ist folglich der Schnittpunkt aller Spektralkurven (Absorbanzen in Abhängigkeit von der Wellenlänge) gleich konzentrierter Lösungen unterschiedlichen pH-Werts.
Durch Photometrie einer Lösung unbekannter Konzentration am isobestischen Punkt lässt sich
daher die Gesamtkonzentration c unabhängig vom pH-Wert bestimmen.
Sofern sich die am Dissoziationsgleichgewicht beteiligten Teilchen genügend stark in ihrem
optischen Verhalten unterscheiden, eröffnen Absorbanzmessungen darüber hinaus einen Weg
zur direkten Messung des Dissoziationsgrads α.
Abbildung 1:
Schematischer spektraler Verlauf der Absorbanz für wässrige Lösungen einer schwachen Säure
bei unterschiedlichen pH-Werten. Der Schnittpunkt der Spektralkurven bei iso ist der isosbestische Punkt, an dem die Absorbanz nur von der Gesamtkonzentration der Säure und nicht mehr
vom Dissoziationsgrad abhängt.
Apparatives Praktikum Physikalische Chemie für Studierende der Biologie
TU Braunschweig, Institut für Physikalische und Theoretische Chemie, Dr. Christof Maul
WS2015/6
UV/VIS-Spektroskopie
4
Die Absorbanz A() einer schwachen Säure HA der Konzentration c im Dissoziationsgleichgewicht ist gegeben durch
A() = HA() (1-) c s + A c s
(8)
wenn man voraussetzt, dass das Lösemittel Wasser und die Protonen in dem betrachteten
Wellenlängenbereich nicht absorbieren (Wasser = H+ = 0). HA() und A sind die Absorptionskoeffizienten der undissoziierten Säure bzw. des Anions.
In einem Wellenlängenbereich, in dem auch HA verschwindet, rührt die messbare Absorbanz
ausschließlich vom Anion her und Gleichung (8) geht in
A() = A c s
(9)
über. Damit kann der Dissoziationsgrad
= A()/{Acs}
(10)
gemessen werden, sofern Acs bekannt ist. Acs kann gemessen werden, wenn sicher
gestellt ist, dass α = 1 ist, also wenn z.B. ein Überschuss einer Base zugegeben wird.
Aus der Definitionsgleichung (6) der Dissoziationskonstante KS erhält man
A(λ )
pK S = pH−lg α = pH −lg
1−α
ϵ A ( λ)cs−A(λ)
(11)
-
A c s ist die Absorbanz AA() des Anions bei vollständiger Dissoziation (α = 1). Damit
wird aus Gleichung (11)
pK S = pH −lg
A(λ)
AA (λ)−A(λ )
(12)
-
−pK
so dass die Dissoziationskonstante K S = 10
aus den Absorbanzwerten bestimmt werden
S
kann, wenn der pH-Wert der Lösung bekannt ist.
UV/VIS-Spektrometer
Ein modernes Labor-Spektrometer ist in der Regel als Zweistrahlgerät aufgebaut, in dem die
Messung der Proben- und der Referenz-Intensität parallel erfolgt und die gewünschte Größe
(Absorbanz A oder Transmissionsgrad T) direkt angezeigt wird. Die im Praktikum eingesetzten Labor-Spektrometer sind solche Zweistrahl-UV/VIS-Spektrometer, die einen Wellenlängen-Durchstimmbereich von 200 nm bis 1100 nm besitzen.
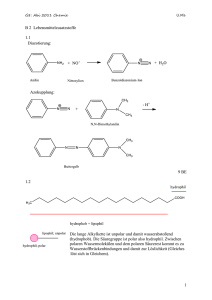
Abbildung 2 zeigt schematisch den Strahlengang im Spektrometer. Probenküvette und Referenzküvette werden simultan vom Messlicht durchstrahlt. Die Strahlung einer Deuteriumlampe (für den UV-Bereich) oder einer Halogenlampe (für den sichtbaren VIS-Bereich) wird
durch einen Hohlspiegel auf den Eintrittsspalt des Monochromators fokussiert. Der Monochromator zerlegt die einfallende Strahlung spektral durch Beugung an einem optischen GitApparatives Praktikum Physikalische Chemie für Studierende der Biologie
TU Braunschweig, Institut für Physikalische und Theoretische Chemie, Dr. Christof Maul
WS2015/6
UV/VIS-Spektroskopie
5
ter. Durch Veränderung der Gitterstellung (Auftreffwinkel) kann die Wellenlänge selektiert
werden, die durch den Austrittsspalt in den Proben- und den Referenzraum gelangt. Der nutzbare Spektralbereich liegt zwischen 190 und 1100 nm. Ein zweiter Hohlspiegel parallelisiert
die Strahlung wieder, die dann von einem halbdurchlässigen Spiegel (Strahlteiler) in einen
Proben- und einen Referenzstrahl aufgetrennt wird.
Abbildung 2:
schematischer Strahlengang in einem UV/VIS-Spektrometer. Das Licht der Strahlungsquelle
wird von einem Monochromator aufgetrennt, von einem Strahlteiler aufgetrennt und gelangt
durch die Proben- bzw. die Referenzküvette zu den Detektoren, die die transmittierte Intensität
It und die eingestrahlte Intensität I0 registrieren.
Der Probenstrahl gelangt über einen Planspiegel durch die Probenküvette, die die zu vermessenden Probe enthält, auf einen Photodetektor, der die Intensität It misst. Der Referenzstrahl
gelangt über einen zweiten Planspiegel durch die Referenzküvette, die das Lösemittel enthält,
auf einen zweiten Photodetektor, wo die Intensität I0 gemessen wird. Ein Rechner ermittelt
I
daraus je nach Einstellung entweder die Absorbanz A = lg I oder den Transmissionsgrad
I
T = I der Probe.
0
t
t
0
In einem Einstrahlspektrometer findet keine Auftrennung in einen Proben- und einen Referenzstrahl statt. Hier müssen die Intensitäten It für die Probenküvette und I0 für die Referenzküvette im selben Strahlengang nacheinander gemessen werden.
Apparatives Praktikum Physikalische Chemie für Studierende der Biologie
TU Braunschweig, Institut für Physikalische und Theoretische Chemie, Dr. Christof Maul
WS2015/6
UV/VIS-Spektroskopie
6
Eigenschaften optischer Materialien und von Lösemitteln
Eine Übersicht über die Durchlässigkeitsbereiche verschiedener Substanzen, die beim Bau optischer Geräte Verwendung finden, zeigt die folgende Tabelle. Im kurzwelligen Ultraviolett
(UV) unterhalb von 200 nm sind nur noch wenige Substanzen (CaF 2, LiF, Saphir) lichtdurchlässig. Unterhalb von 185 nm absorbiert Sauerstoff sehr stark, so dass man hier nicht mehr in
Luft arbeiten kann, sondern im Vakuum oder in Stickstoff- oder Argon-Atmosphäre messen
muss (VUV- oder Vakuum-UV-Bereich). Strahlung im Bereich von 2 bis 120 nm wird von jeder Art Materie schon in dünnen Schichten praktisch völlig absorbiert.
Tabelle 1:
Durchlässigkeitsbereiche verschiedener Substanzen
Material
Durchlässigkeitsbereich, m
CsI
CsBr
KBr
NaCl
CaF2
LiF
Glas
Quarz*
0.16 - 55
0.16 - 40
0.21 - 38
0.20 - 16
0.13 - 9
0.12 - 7
0.35 - 3
0.20 - 3.5
So wie für das Küvettenmaterial nur bestimmte Substanzen verwendet werden können, eignen
sich auch nicht alle Lösemittel für die UV/VIS-Spektrometrie. Während im sichtbaren Spektralbereich neben Wasser zahlreiche organische Flüssigkeiten als Lösemittel zur Verfügung
stehen, deren Absorption so gering ist, dass sie ohne Schwierigkeit mit der Referenzküvette
korrigiert werden kann, ist für den UV-Bereich die Auswahl wesentlich kleiner, speziell bei
Wellenlängen unterhalb 230 nm. Die folgende Tabelle enthält für die UV-Spektrometrie geeignete Lösemittel. Angegeben ist dabei die untere Wellenlängengrenze, bei der mit 1 cm
Schichtdicke gegen Wasser in der Vergleichsküvette die Absorbanz 1 gemessen wird.
Tabelle 2: einige Lösemittel für die UV-Spektrometrie
Lösungsmittel
Hexafluor-i-propanol
Trifluorethanol
n-Pentan
Acetonitril
n-Hexan
Ethanol
Methanol
Glycerin
Cyclohexan
untere Wellenlänge, nm
<190
<190
190
191
195
200
205
205
205
Apparatives Praktikum Physikalische Chemie für Studierende der Biologie
TU Braunschweig, Institut für Physikalische und Theoretische Chemie, Dr. Christof Maul
WS2015/6
UV/VIS-Spektroskopie
7
Ausführung und Auswertung der Messung
Bestimmen Sie mit dem Labor-Spektrometer für eine schwache Säure die Dissoziationsgrade
für verschiedene pH-Werte durch Messung der Absorbanzen mit dem UV/VIS-Spektrometer. Berechnen Sie daraus die Dissoziationskonstante KS. Bestimmen Sie außerdem die molaren Absorptionskoeffizienten ε am Absorptionsmaximum λmax und am isobestischen Punkt λiso.
Zur Messung der Dissoziationskonstanten stellen Sie je 1 Liter einer wässrigen 10 -3m p-Nitrophenollösung her. Verdünnen Sie die 10-3m p-Nitrophenollösung mit 0.1m NaOH, 0.1m HCl
und mit den im Anhang angegebenen 5 Pufferlösungen jeweils auf 10-4m. Gegebenenfalls sind
die Pufferlösungen neu anzusetzen. Nehmen Sie insgesamt 7 Absorptionsspektren auf, eines
für das Phenolat-Anion (A−, alkalisch, α = 1), eines für das undissoziierte p-Nitrophenol (HA,
sauer, α = 0) und 5 für das teildissoziierte p-Nitrophenol bei den pH-Werten 6.4, 6.8, 7.2, 7.6
und 8 (0 < α < 1).
Bestimmen Sie dazu zunächst in einer Übersichtsmessung den interessierenden Spektralbereich, in dem Sie das Spektrometer dann durchstimmen. Entnehmen Sie aus den Kurven den
isosbestischen Punkt iso für p-Nitrophenol sowie das Absorptionsmaximum max des Anions.
Bestimmen Sie die zugehörigen Absorptionskoeffizienten (iso) und (max). Überlegen Sie,
ob bei der Messung zur Bestimmung der Dissoziationskonstanten KS am Absorptionsmaximum max des Anions die undissoziierte Säure stört und bei welcher anderen Wellenlänge gegebenenfalls zusätzlich zu messen ist. Ermitteln Sie die Dissoziationsgrade für die 5 gepufferten Lösungen sowie die Dissoziationskonstante KS nach Gl. (11).
Ermitteln Sie den Fehler K aus den 5 Einzelmessungen und vergleichen Sie mit dem Literaturwert!
Anhang: Puffergemische nach McIlvain
pH
Lösung A (ml)
Lösung B (ml)
8.0
2.75
97.25
7.6
6.35
93.65
7.2
13.05
86.95
6.8
22.75
77.25
6.4
30.75
69.25
Lösung A: 0.1m Zitronensäure
Lösung B: 0.2m Dinatriumhydrogenphosphat
Apparatives Praktikum Physikalische Chemie für Studierende der Biologie
TU Braunschweig, Institut für Physikalische und Theoretische Chemie, Dr. Christof Maul
WS2015/6