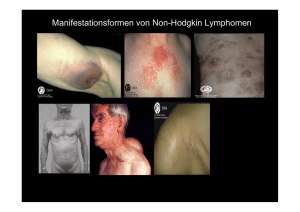
Blindheit durch ein Mantelzell-Lymphom
Werbung

D E R B E S O N D E R E FA L L Schweiz Med Forum 2007;7:485–487 485 Blindheit durch ein Mantelzell-Lymphom Julia Collecutta, Monika Jermanna, Niels Willib, Lorenz Josta a b Onkologie, Medizinische Universitätsklinik, Kantonsspital Bruderholz Kantonales Institut für Pathologie, Kantonsspital Liestal Summary Blindness Resulting from Mantle Cell Lymphoma A 62-year-old patient presented with bilateral swelling of the upper lateral eyelids, submandibular and cervical lymphomas, and B symptoms. Lymph node and bone marrow biopsies and CT scans of the neck, thorax, and abdomen confirmed stage IVB mantle cell lymphoma with blastoid cells. Partial remission was achieved after six cycles of chlorambucil and prednisone. However, systemic and mediastinal recurrences were diagnosed 9 and 17 months later, respectively, and were treated with various chemotherapy regimens. Nine months after completing the systemic therapy, the patient presented with a personality change, unsteady gait, and weight loss. Lymphomatous infiltration of the leptomeningeae was diagnosed. Complete remission was achieved with intrathecal chemotherapy and whole-brain irradiation. A further orbital relapse accompanied by loss of vision occurred four months later and proved refractory to a therapy with bortezomib. The patient died shortly thereafter from progressive systemic lymphoma. Mantle cell lymphomas (MCL) account for about 6% of all lymphomas. A blastoid variant is found in 20% of cases and is characterized by a shorter median survival. Loss of vision due to orbital lymphoma has mostly been attributed to nerve compression whereas our case exhibited not only CNS involvement (which is rare in MCL, occurring in only about 4%) but also direct lymphomatous infiltration of the optical nerves. Fallbeschreibung Ein 62jähriger Mann präsentierte sich mit Schwellungen an beiden oberen Augenlidern und beidseits submandibulär und zervikal vergrösserten Lymphknoten. Es bestanden ein Gewichtsverlust von 5 kg in vier Monaten und Nachtschweiss. Der Visus und die Motilität des rechten Auges waren durch die Schwellung beeinträchtigt. Links bestand seit 1964 eine Amaurosis infolge einer traumatischen Korneaperforation. Im Augenspital wurde eine Konjunktivitis diagnostiziert mit indolenten, harten und verschieblichen Resistenzen in beiden lateralen Oberlidern. Eine Magnetresonanztomographie des Neurokraniums (Abb. 1 x) zeigte ausgedehnte multifokale Tumormanifestationen innerhalb des Conus muscularis im Bereich des Oberlids beidseits, links mit Verdrängung des Nervus opticus nach medial und rechts mit Volumenvermehrung des Nervus opticus. Im Röntgen-Thoraxbild zeigten sich beidseits polyzyklisch vergrösserte Hili. Zur Diagnostik erfolgte eine inguinale Lymphknotenexzision. Die Histologie und die flowzytometrische Analyse ergaben die Diagnose eines blastären Mantelzell-Lymphoms (CD19, CD20, Cyclin D1 stark positiv, CD23 schwach positiv und CD10 negativ) (Abb. 2, 3 x). Das zum Staging durchgeführte CT von Hals, Thorax und Abdomen ergab vergrösserte Lymphknoten zervikal, supra- und infraklavikulär, axillär, mediastinal, hilär, paraaortal und inguinal sowie eine leichtgradige Splenomegalie. Im Blutbild war eine leukämische Ausschwemmung nachweisbar (36,5% von 9300 x 109/L Leukozyten). Bei unserem Patienten bestand somit initial ein Stadium IV B eines blastären MantelzellLymphoms. Es wurde eine Chemotherapie mit sechs Zyklen Chlorambucil (Leukeran®) und Prednison durchgeführt, die radiologisch zu einer guten Partialremission führte. Neun Monate später wurde bei einem Rezidiv in beiden Orbitae, das sich mit einer progredienten Schwellung jedoch ohne Visusbeeinträchtigung manifestierte, eine perkutane Radiatio beider Orbitae mit 40 Gy in 20 Fraktionen durchgeführt. Wiederum neun Monate später kam es zu einem ausgedehnten Rezidiv mit multiplen mediastinalen, abdominalen und peripheren Lymphomen und einer Splenomegalie ohne B-Symptomatik. Es wurde erneut eine Chemotherapie mit sechs Zyklen R-CHOP (Rituximab, Cyclophosphasmid, Doxorubicin, Prednison und Vincristin) durchgeführt, was radiologisch zu einer partiellen Remission führte. Acht Monate später traten mediastinal ein Lokalrezidiv und B-Symptome auf. Nach einer Drittlinienchemotherapie mit sechs Zyklen R-ESHAP (Rituximab, Etoposid, Methylprednisolon, Ara-C, Cisplatin) wurde erneut eine gute partielle Remission dokumentiert. Für eine beim MantelzellLymphom nicht erwiesen wirksame Erhaltungs- Abbildung 1 Initiales Schädel-MRI: lymphomatöse Infiltration beider Orbitae. D E R B E S O N D E R E FA L L Abbildung 2 Histologie des inguinalen Lymphknotens: blastäres Mantelzell-Lymphom mit grossen rundlich bis ovalen und zum Teil gekerbten Zellkernen und prominenten Nukleolen (Vergrösserung 400x). Schweiz Med Forum 2007;7:485–487 486 rungen auf. Im MRI ergab sich der Verdacht einer leptomeningealen Lymphominfiltration entlang des Hirnstamms, der Medulla oblongata und des Rückenmarks. Im Liquor waren maligne Zellen nachweisbar (Zellzahl 192/mm3; Normalwert: 93/mm3), davon 10% Segmentkernige und 90% Mononukleäre. Es erfolgten eine Ganzhirnradiatio mit 40 Gy in 20 Fraktionen unter Auslassung der Orbitaregion sowie eine intrathekale Chemotherapie mit Ara-C, Methotrexat und Hydrocortison während fünf Monaten mit nachfolgend kompletter Remission. Vier Monate später trat orbital erneut ein Rezidiv auf, das trotz Behandlung mit drei Zyklen Bortezomib im Verlauf zur Erblindung des funktionellen rechten Auges führte. Der Patient verstarb einige Wochen später an seinem generell progredienten Tumorleiden. Kommentar Abbildung 3 Immunhistochemische Reaktion: Positivität für Cyclin D1 in der Lymphknotenhistologie (Vergrösserung 400x). Abbildung 4 Nervus opticus mit peri- und neuraler Lymphominfiltration (dunkelblau) in der Autopsie (Vergrösserung 40x). therapie mit Mabthera bestand nur eine befristete Kostengutsprache. Neun Monate nach dem Ende derselben traten eine Gangunsicherheit, eine Wesensveränderung und mnestische Stö- Das Mantelzell-Lymphom (MCL) gehört zur Gruppe der B-Zell-Non-Hodgkin-Lymphome mit einem tiefen Malignitätsgrad (WHO-Klassifikation 2001). Ungefähr 6% aller Lymphome sind MCL. Die jährliche Inzidenz liegt bei 2:100 000 mit einer Prävalenz des männlichen Geschlechts (3:1) und einem Altersmedian von 65 Jahren. Etwa 85% der Patienten befinden sich bei der Erstdiagnose in einem fortgeschrittenen Erkrankungsstadium (III oder IV). Bei ungefähr 60% der Patienten besteht bereits bei der Diagnosestellung eine Knochenmarkinfiltration und bei etwa 25% auch eine leukämische Ausschwemmung. Die mediane Überlebenszeit liegt bei unter drei Jahren. Das klinische Bild ist meist durch vergrösserte Lymphknoten und eine Splenomegalie (45–60%) geprägt. Extranodale Manifestationen sind beim MCL häufiger als bei anderen Lymphomsubtypen. Gehäuft tritt insbesondere ein gastrointestinaler Befall auf. Zu den Differentialdiagnosen gehören die chronisch lymphatische Leukämie und andere Lymphomsubtypen. Eine definitive Diagnose ist oft erst durch eine immunhistochemische Bestimmung bzw. eine flowzytometrische Analyse möglich. In 85–90% der Fälle [1] kommt es zu einer charakteristischen Translokation t(11;14)(q13;q32). Diese chromosomale Aberration führt zu einer Deregulation und einer Überexpression von Cyclin D1, was eine Tumorzellproliferation verursacht [2]. Bei unserem Patienten wurde histologisch und immunhistochemisch die Diagnose eines blastären MCL gestellt, eine Variante des MCL, welche in ungefähr 20% nachweisbar ist [3]. Der Verlauf der blastären Variante ist aggressiver und die mediane Überlebenszeit kürzer. Gegenüber der normalen Variante wird die Überexpression von Cyclin D1 und/oder CDK4 vermehrt gefunden, D E R B E S O N D E R E FA L L und der Proliferationsindex (MIB-1 = Ki67-Expression) beträgt statt ungefähr 30% meist etwa 50–80%. Zusätzlich besteht ein komplexeres zytogenetisches Profil [4] mit tetraploiden Chromosomen, Cyclin-D1-Amplifikationen, einer höheren p53-Mutationsrate und einer höheren Inzidenz an p16-Deletionen. Unser Patient zeigte nicht nur die seltene Diagnose eines blastären Mantelzell-Lymphoms und dessen seltenen ZNS-Befall [5], sondern auch einen Befall beider Nervi optici (Abb. 4 x). In der neueren Literatur wurde bei einem Orbita- Schweiz Med Forum 2007;7:485–487 487 befall durch Mantelzell- [6, 7] oder die häufigeren diffus-grosszelligen sowie vor allem durch die MALT-Lymphome vom Marginalzonentyp [8, 9] wegen des Drucks infolge eines Lymphombefalls anderer orbitaler Stukturen eher Schädigungen des Nervus opticus beschrieben, während in unserem Fall eine klare lymphomatöse Infiltration nachweisbar war. Ein Befall des ZNS scheint gemäss retrospektiven Daten wie bei unserem Fall bei blastären Varianten und leukämischer Ausschwemmung gehäuft vorzukommen [10]. Literatur Korrespondenz: Dr. med. Lorenz Jost Onkologie Medizinische Universitätsklinik Kantonsspital CH-4101 Bruderholz [email protected] 1 Thieblemont C, Nasser V, Felman P, Leroy K, Gazzo S, et al. Small lymphocytic lymphoma, marginal zone B-cell lymphoma, and mantle cell lymphoma exhibit distinct geneexpression profiles allowing molecular diagnosis. Blood. 2004;103(7):2727–37. 2 Fernandez V, Hartmann E, Ott G, Campo E, Rosenwald A. Pathogenesis of mantel-cell lymphoma: all oncogenic roads led to dysregulation of cell cycle and DNA damage response pathways. J Clin Oncol. 2005;26:6364–9. 3 Zoldan MC. Large-cell variants of mantle-cell lymphoma: cytologic characteristics and p53 anomalies may predict poor outcome. BR J Haematol. 1996;93:475–86. 4 Hua S, Sanger W, Onciu M, Lai R, Schlette EJ, Medeiros LJ. Mantle cell lymphoma with 8q24 chromosomal abnormalities: a report of 5 cases with blastoid features. Mod Pathol. 2002;15:1266–72. 5 Oinonen R, Franssila K, Elonen E. Central nervous system involvement in patients with mantle cell lymphoma. Ann Hematol. 1999;78:145–9. 6 Looi A, Gascoyne RD, Chhanabhai M, Connors JM, Rootman J, White VA. Mantle cell lymphoma in the ocular adnexal region. Ophthalmology. 2005;112(1):114–9. 7 Hon C, Chan RT, Ma ES, Shek TW, Yau K, Au WY. Lymphomatous proptosis as a novel feature of mantle cell lymphoma. Leuk Lymphoma. 2006;47(1):71–5. 8 White WL, Ferry JA, Harris NL, Grove AS Jr. Ocular adnexal lymphoma. A clinicopathologic study with identification of lymphomas of mucosa-associated lymphoid tissue type. Ophthalmology. 1995;102(12):1994–2006. 9 Coupland SE, Hellmich M, Auw-Haedrich C, Lee WR, Stein H. Prognostic value of cell-cycle markers in ocular adnexal lymphoma: an assessment of 230 cases. Graefes Arch Clin Exp Ophthalmol. 2004;242(2):130–45. 10 Valdez R, Kroft SH, Ross CW, Schnitzer B, Singleton TP, Peterson LC, et al. Cerebrospinal fluid involvement in mantle cell lymphoma. Mod Pathol. 2002;15(10):1073–9.