Kein Herz aus Stahl, sondern aus Titan - RWTH
Werbung

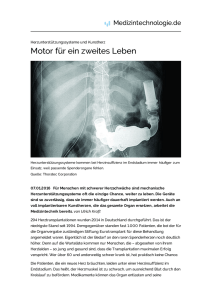
Kein Herz aus Stahl, sondern aus Titan Was kann man tun, wenn ein Herz zu schwach wird, um alleine zu schlagen? Die moderne Medizin hält einige Lösungen parat. Viele verschiedene Hilfsmittel, wie zum Beispiel Schrittmacher oder Unterstützungssysteme, werden verwendet. Aber die Herzen einiger Patienten sind so krank, dass sie auch mit Unterstützung nicht mehr in der Lage sind, ihre Träger am Leben zu erhalten. In solchen Fällen ist eine Organtransplantation die einzig mögliche Lösung. Allerdings gibt es nicht annähernd genug Spenderherzen. Etwa 400 Herzen gibt es pro Jahr für fast 1.000 Patienten, die auf der Warteliste stehen. Und die Patienten auf der Warteliste bilden auch nur die Spitze des Eisbergs. Nicht alle Menschen, deren Herzen nicht mehr richtig funktionieren, schaffen es darauf. Krebsleiden, HIV oder Erkrankungen anderer Organe schließen Betroffene prinzipiell als Kandidaten für eine Organtransplantation aus. Für all diese Patienten ist ein künstliches Herz, also eine Art Prothese, die einzige Chance. Wissenschaftlerinnen und Wissenschaftler des Instituts für Angewandte Medizintechnik (AME) der RWTH Aachen haben sich mit dem Herz- und Diabeteszentrum NRW in Bad Oeynhausen und dem renommierten Herzchirurgen Prof. Dr. Reiner Körfer zusammengeschlossen. Zusammen haben sie ein solches Kunstherz entwickelt: das ReinHeart. In der Aachener Arbeitsgruppe Kardiovaskuläre Technik (CVE) arbeiten Forscher aus ganz verschiedenen Fachbereichen zusammen an dieser Innovation, die tausenden Herzpatienten die Hoffnung auf ein neues Herz zurückgeben kann. Ein Kunstherz als Ersatz Im Gegensatz zu anderen Kunstherz-Systemen ist das ReinHeart nicht als kurzfristiger Behelf, sondern als dauerhafter Ersatz für das kranke Herz gedacht. Bisher sind Kunstherzen noch keine Alternative zu Spenderorganen. Sie werden nur verwendet, um die Zeit bis zur Transplantation zu überbrücken. Das Problem ist, dass sie noch nicht kompakt genug sind, um komplett implantiert zu werden. Stattdessen werden sie über Schläuche bzw. Kabel von einer externen Energiequelle mit Druckluft oder Strom versorgt. Entlang dieser Hautdurchführungen können Bakterien in den Körper gelangen, was sehr gefährlich ist. Deshalb beschränkt man die Nutzung auf möglichst kurze Zeiträume. Der Arbeitsgruppe Kardiovaskuläre Technik ist es nunmehr gelungen, ein Kunstherz zu entwickeln, das vollständig implantiert werden kann. Die gesundheitsgefährdenden offenen Stellen können durch eine transkutane Energieversorgung vermieden werden. Dabei wird die Spannung drahtlos mittels Spulen über die Haut übertragen. Das funktioniert im Prinzip genau so wie das Aufladen einer elektrischen Zahnbürste, die in der Ladestation steht. Die einzigen Elemente der Herzprothese, die nicht implantiert werden und somit außerhalb des Körpers getragen werden, sind die Steuerungseinheit und ein Akku. Sie werden an einem Gürtel befestigt, sodass der Patient kaum eingeschränkt wird. Die äußere Induktionsspule kann einfach mit Pflaster an der Brust befestigt werden; dort, wo das Gegenstück im Körperinneren liegt. Eine besonders große Herausforderung für die Forscher war es, alle Bauteile so klein zu gestalten, dass sie vollständig implantiert werden können. Durch einen besonderen Antrieb und ganz viel elektrotechnische Feinarbeit haben sie es aber geschafft: Das ReinHeart ist nur minimal größer und schwerer als ein natürliches Herz. „Dadurch ist es für etwa 80 Prozent der Patienten passend“, erklärt Diplom-Ingenieur Thomas Finocchiaro von der CVE. Auf den ersten Blick ist das Kunstherz recht unscheinbar. Es sieht aus wie eine kleine Plastikbox mit vier Ausgängen und einem Metallring in der Mitte. Aber der Teufel steckt im Detail. Innerhalb des silbernen Titanringes versteckt sich der komplette Antrieb für das Herz, das mehr als 300 Liter Blut pro Stunde pumpt. Das ist ein elektromagnetischer Linearantrieb, bei dem immer abwechselnd eine Druckplatte gegen eine der Herzkammern gedrückt wird. Durch die Verkleinerung des Volumens entleeren sich dann die Pumpkammern. Mit dem neuen Antrieb konnte auch der Verschleiß minimiert werden. Da kein Getriebemehr verwendet wird, werden die Bauteile wesentlich weniger belastet und somit die Langlebigkeit des Antriebs erheblich gesteigert. Rechts und links neben der Pumpeinheit sind die Pumpkammern – das Gegenstück zu den natürlichen Herzkammern – zu finden. Diese bestehen aus Polyurethan, also Kunststoff, und sind in ihrer Form so optimiert, dass der Durchfluss des Blutes durch die Herzkammern verbessert wird. Wenn das Blut nämlich nicht ständig in Bewegung bleibt, kann es verklumpen und sogenannte Thromben bilden. Diese können Adern verstopfen oder sogar zu Schlaganfällen führen. An den vier Ausgängen des ReinHeart werden die Vorhöfe des natürlichen Herzens, die Aorta und die Pulmonalarterie, die zur Lunge führt, angeschlossen. Damit der Übergang zwischen dem Kunstherzen und den körpereigenen Strukturen möglichst gut gelingt, hat das CVE-Team sogar eigenhändig eine Art biokompatiblen Schlauch entwickelt, der an diesen Stellen als Adapter fungiert. Zusätzlich zu dieser Pumpeinheit, die den Platz des Herzens einnimmt, werden noch zwei weitere wichtige Elemente implantiert: ein Volumenkompensator, der mögliche Druckschwankungen ausgleichen kann, und ein Akku. Der Akku speichert immer etwas von der Energie, die von der externen Versorgungseinheit übertragen wird. Das ermöglicht es dem Träger, die Stromversorgung kurzfristig abzulegen, zum Beispiel beim Duschen oder Schwimmen. Mindestens eine Stunde kann er so ohne externe Versorgungseinheit auskommen. Erste Tests Im Moment befindet sich das ReinHeart noch in der Testphase. In verschiedenen Labortests werden die Haltbarkeit der einzelnen Bestandteile und ihre Funktion überprüft. Die Ergebnisse sind vielversprechend. Das (vorläufige) Ziel der Wissenschaftler vom CVE ist es, eine Haltbarkeit von fünf Jahren zu erreichen. „Nach diesem Zeitraum beträgt auch die Überlebensrate nach einer Herztransplantation nur noch ca. 70 Prozent. Wenn das Kunstherz also eine Lebensdauer von mindestens fünf Jahren erreicht, kann es als wirkliche Alternative zur Herztransplantation angesehen werden “, so Finocchiaro. Eine große Zukunftsvision wäre es, wenn das Kunstherz eines Tages den Empfänger bis an sein Lebensende begleiten würde. Finocchiaro betont aber: „Ein natürliches Herz hat eine Lebensdauer von über 80 Jahren. Das ist mit technischen Mitteln zurzeit einfach nicht zu erreichen.“ Erste Funktionstests des Kunstherzens in lebenden Tieren wurden auch schon durchgeführt. Dabei wurde Kälbern das ReinHeart implantiert. Auch die Ergebnisse dieser Tests lassen auf Großes hoffen: Das Kunstherz hat über mehrere Stunden die komplette Kreislauffunktion übernommen. Für Mitte des Jahres sind erste Langzeittierversuche geplant, in denen die Kälber die Kunstherzen über einen Zeitraum von bis zu drei Monaten tragen sollen. Diese Testreihen werden bis Mitte 2013 dauern. Im Anschluss daran könnten erste klinische Versionen des ReinHeart hergestellt werden, die für den Einsatz im Menschen vorgesehen sind. Erste Implantationen in menschliche Patienten können vermutlich 2015 stattfinden. Nele Messelken Kontakt: Dipl.-Ing. Thomas Finocchiaro Lehr- und Forschungsgebiet Kardiovaskuläre Technik (CVE) Institut für Angewandte Medizintechnik (AME) Helmholtz-Institut für Biomedizinische Technik der RWTH Aachen Pauwelsstraße 20 52074 Aachen Telefon: 0241/80-856 50 E-Mail: [email protected] www.cardiovascular-engineering.com Bildunterschrift: „ReinHeart“ bedeutet Hoffnung für tausende Menschen, die kein Spenderherz erhalten können. Das kleinste voll implantierbare Kunstherz wird jetzt an der RWTH Aachen entwickelt. Foto: CVE/AME – RWTH Aachen