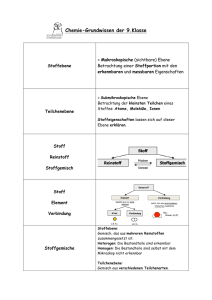
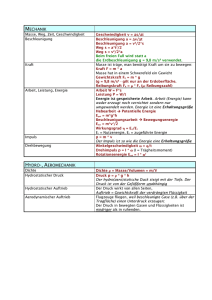
A Atome
Werbung

Chemie Technische Berufsmaturit€t BMS AGS Basel A Atome Entwicklung der Atomlehre Nach Demokrit sind alle Stoffe aus kleinsten, unteilbaren Teilchen, den Atomen, aufgebaut, die alle aus derselben Urmaterie bestehen und sich in Gestalt und Gr•sse unterscheiden. Im Mittelalter fand diese Theorie wenig Anklang (Elementenlehre). Dalton verkn‚pfte sie dann mit dem Begriff des Elements: Ein Element besteht aus gleichartigen, unteilbaren Atomen. Die Atome verschiedener Elemente haben unterschiedliche Eigenschaften und Massen und verbinden sich in bestimmten Massenverh€ltnissen zu Verbindungen. Heute weiss man, dass auch die Atome nicht unteilbar sind. Beim Zerfall von Atomen entstehen neue Elemente. Diese Vorg€nge werden nicht in der Chemie beschrieben. In der Chemie gilt das Gesetz der Unzerst•rbarkeit der Elemente. relative Masse Ein Kohlenstoffatom hat eine absolute Masse von etwa 2ƒ10-23 g. Damit der Umgang mit so kleinen Massen besser handhabbar ist, hat man eine auf die Masse eines Kohlenstoffatoms bezogene Masseinheit definiert: Die relative Masse Mr gibt die Masse eines Teilchens (Atoms) in der Masseneinheit 1 u an. 1 u entspricht 1/12 der Masse des h€ufigsten Kohlenstoffatoms Stoffmenge Die Stoffmenge n beschreibt die Menge der in einer Probe enthaltenen Teilchen. 1 Mol Ein Mol entspricht der Stoffmenge von 12 g Kohlenstoff. Avogadrokonstante Die Avogadrokonstante ist die Teilchenzahl der Stoffmenge 1 Mol: NA = 6,02ƒ1023/mol Molare Masse Die Molare Masse M ist die Masse der Stoffmenge 1 Mol des Stoffes in g/mol. Sie entspricht der relativen Masse Mr in g. Atombau und PSE 12 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel Elementsymbole Das Elementsymbol dient zur Abk‚rzung des Elementnamens, bedeutet aber auch 1 Atom oder die Stoffmenge 1mol des betreffenden Elements. Substanzformeln Die Substanzformel einer Verbindung gibt das Atomzahlenverh€ltnis der beteiligten Elemente und damit auch ihr Massenverh€ltnis an. Beispiel SO3: • Atomzahlenverh€ltnis S : O = 1 : 3 • Massenverh€ltnis S : O = 32 g : 48 g = 2 : 3 Aufgaben 1. Was bedeutet das Wort „Atom“ ? 2. Worin unterscheiden sich die Atomlehren von Demokrit und Dalton ? 3. a) b) c) d) Wie viele u und wie viele g wiegt ein Kupferatom (Cu) ? Aus wie vielen Atomen bestehen 100 g Kupfer? Welche Masse hat 1 mol Kupferatome ? Welche Masse in u und in mg haben 1020 Kupferatome ? 4. a) Geben Sie Ihre eigene Masse in der atomaren Masseneinheit 1 u an ! b) Wie vielen Kohlenstoffatomen entspricht diese Masse ? 5. Welche Bedeutungen hat das Elementsymbol H qualitativ und quantitativ ? 6. In welchem Atomzahlenverh€ltnis und in welchem Massenverh€ltnis liegen die Elemente Phosphor und Sauerstoff in der Verbindung P2O5 vor ? 7. Bei der Verbrennung von 3,47 g Aluminium entstehen 6,56 g Aluminiumoxid. Wie lautet die Substanzformel von Aluminiumoxid ? 8. In einer Verbindung, die aus Kohlenstoff C, Wasserstoff H und Sauerstoff O besteht, wurden 52,2 % C und 13,0 % H ermittelt. Welche Substanzformel hat die Verbindung ? B Atombau Kern - HÄlle - Modell Das Atom besteht aus einem sehr kleinen, schweren, positiv geladenen Kern und einer fast masselosen, sehr grossen, gleichstark negativ geladenen H‚lle. Atomkerne werden auch als Nuklide bezeichnet. Atombau und PSE 13 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel GrÅssen- und MassenverhÇltnisse Kern H‚lle Masse Gr•sse Ladung 2’000 1 1 10’000 1 1 Elementarteilchen Symbol + Proton Neutron Elektron p n0 e- Aufenthaltsort Masse in u Ladung in e Kern Kern H‚lle 1 1 0,0005 +1 0 -1 Zusammensetzung von Atomen Ordnungszahl Sie entspricht der Anzahl Protonen im Kern und bestimmt die Elementsorte und deren Stellung im Periodensystem. Massenzahl Sie entspricht der Anzahl Kernteilchen (p+ + n0). Neutronenzahl Sie ergibt sich als Differenz aus der Massenzahl und der Ordnungszahl. Elektronenzahl Sie entspricht im neutralen Atom der Anzahl Protonen. Isotopenschreibweise Massenzahl Ordnungszahl Elementsymbol Beispiele: 23 11 Na 35 17 Cl p+ n0 e- 11 17 12 18 11 17 Atombau und PSE 37 17 Cl 238 92 14 U p+ n0 e- 17 92 20 146 17 92 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel Isotopen Isotopen sind Atomkerne gleicher Ordnungszahl (gleiches Element), aber verschiedener Massenzahl. Die relative Atommasse eines Elementes ergibt sich als Durchschnittswert ‚ber das nat‚rliche Isotopengemisch und ist in den meisten Periodensystemen angegeben. Aufgaben 1. Geben Sie ein anschauliches Beispiel an f‚r den Gr•ssenvergleich von H‚lle und Kern ! 2. Vergleichen Sie Kern und H‚lle bez‚glich Masse und Ladung ! 3. Unterscheiden Sie die Begriffe Atommasse und Massenzahl ! 4. a) Geben Sie die Isotopenschreibweise f‚r ein Nuklid an, das 82 Protonen und 125 Neutronen enth€lt ! b) Geben Sie dazu ein Isotop an ! 40 5. Gegeben sind die folgenden Atome: 35 ; 40 17 Cl 18 Ar ; 20 Ca ; a) Welche Atome sind zueinander Isotopen ? b) Welche Atome haben die gleiche Neutronenzahl ? c) Welche Atome haben die gleiche Anzahl Kernteilchen ? 37 17 Cl 6. Suchen Sie in der Literatur Beispiele von nat‚rlichen Isotopengemischen ! RadioaktivitÇt Atomkerne sind nur innerhalb eines bestimmten Verh€ltnisses von Neutronen und Protonen stabil. Ebenso sind Kerne mit einer Masse von ‚ber cˆ. 250 u oder energetisch angeregte Kerne nicht best€ndig. Sie zerfallen unter Aussendung von Energie in Form von schnellen Teilchen oder elektromagnetischer Strahlung, sie sind radioaktiv. Beim radioaktiven Zerfall entstehen neue, unter Umst€nden wiederum radioaktive Stoffe. Der radioaktive Zerfall l€uft von selbst ab und l€sst sich nicht stoppen. Er ist unabh€ngig von Druck, Temperatur und chemischer Umgebung ! Kennzeichnende Gr•ssen f‚r den radioaktiven Zerfall eines Nuklids sind die AktivitÇt A und die Halbwertzeit T. Die Aktivit€t A ist das Verh€ltnis aus der Anzahl Zerf€lle eines Pr€parates und der Zeit. Masseinheit: 1 Bq (Becquerel) = 1 Zerfall/s Die Aktivit€t einer Substanz nimmt mit der Zeit exponentiell ab. Die Halbwertzeit T gibt an, in welcher Zeit sich die Anfangsaktivit€t auf 50% verringert hat. Atombau und PSE 15 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel Die Halbwertzeit ist ein statistischer Wert ‚ber eine sehr grosse Anzahl von Kernen. Vom einzelnen Kern kann man nicht sagen, ob er sofort oder erst nach unabsehbarer Zeit zerf€llt. A 1 1 /2 1 1 /4 /8 3T 2T T Beispiele von radioaktiven Atomkernen mit ihren Halbwertzeiten: 137 24 131 Cs I T = 30 a T = 8,1 d Na Po 214 t T = 15 h T = 0,15 ms Radioaktive Strahlung Die im Zusammenhang mit radioaktiven Zerf€llen ausgesendeten, energiereichen Teilchen oder elektromagnetischen Wellen nennt man radioaktive Strahlung. Von den heute bekannten Strahlungsarten sind die -, die - und die -Strahlung von Bedeutung. Alpha-Strahlung ‰berschwere Kerne senden beim -Zerfall sog. -Teilchen aus. Das sind zweifach positiv geladene Heliumkerne. Ihre Geschwindigkeit ist etwa 104 km/s. Wegen ihrer verh€ltnism€ssig grossen Masse haben sie eine grosse Energie. Als energiereiche, geladene Teilchen besitzen sie eine starke ionisierende Wirkung aber nur eine kleine Reichweite (in Luft cˆ. 1,6 cm). Beta-Strahlung Kerne mit Neutronen‚berschuss wandeln Neutronen unter Aussendung eines Elektrons in Protonen um: --Strahlung. Kerne mit Neutronenmangel wandeln Protonen unter Aussendung eines Positrons (ein mit dem Elektron vergleichbares Teilchen mit positiver Ladung) in Neutronen um: +-Strahlung. Ein -Teilchen verl€sst den Kern mit nahezu Lichtgeschwindigkeit. Mit seiner viel kleineren Masse ergibt sich aber nur ein etwa halb so grosser Energieinhalt gegen‚ber der Strahlung. Damit hat ein -Teilchen eine weniger stark ionisierende Wirkung, daf‚r aber eine gr•ssere Reichweite. Gamma-Strahlung Befindet sich ein Kern in angeregtem Zustand (erh•hter Energieinhalt aus einem Stoss oder als Restenergie eines fr‚heren Zerfalls), so kann er durch Aussendung einer elektromagnetischen Welle (-Strahlung) in einen tieferen Energiezustand ‚bergehen. Die -Strahlung tritt deshalb vorwiegend als Begleitstrahlung auf. Atombau und PSE 16 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel Sie hat eine Wellenl€nge im Bereich von 1 pm und eine nochmals um etwa die H€lfte kleinere Energie als die Betastrahlung. Sie geh•rt aber zu den energiereichsten elektromagnetischen Wellen, die es gibt. Als masselose und ungeladene Welle hat sie nur eine kleine ionisierende Wirkung, aber eine umso gr•ssere Reichweite. Beim Durchgang durch Materie kann sie jedoch zu angeregten Kernen und damit zu weiteren Zerfallsreaktionen mit entsprechender Strahlung f‚hren. Aufgaben 1. In welchem Bereich liegt etwa das Neutronen-Protonen-Verh€ltnis stabiler Nuklide ? 2. Welchen Teil der Anfangsaktivit€t hat eine Probe einer radioaktiven Substanz mit einer Halbwertzeit von 16 h nach 2 Tagen noch ? 3. In welchem Zeitraum sinkt die Aktivit€t einer Probe von 234 Th auf etwa 1 % der Anfangsaktivit€t ? 4. Welche der Strahlungsarten ist die gef€hrlichste ? 5. In der Sonne findet u.a. die Kernfusion von Deuterium 2H und Tritium 3H zu 4He statt. Notieren Sie die Reaktionsgleichung in der Isotopenschreibweise ! Schalenmodell der HÄlle Die Elektronen bewegen sich in der H‚lle entsprechend ihrem Energieinhalt in einem bestimmten Abstand um den Kern. Elektronen mit ann€hernd gleichem Energieinhalt (Kernabstand) werden in Schalen zusammengefasst. Es gibt sieben, von K bis Q bezeichnete oder mit der Schalennummer n von 1 bis 7 durchnummerierte Schalen, die nach aussen hin zunehmend vielen Elektronen Platz bieten: 2 Anzahl e = 2 ƒ n Beispiele: H O S Orbitalmodell der HÄlle Die modernen quanten- und wellenmechanischen Modellvorstellungen gehen davon aus, dass man f‚r Elektronen nicht genaue Umlaufbahnen angeben kann. Man ordnet ihnen R€ume zu, in denen sie sich mit einer entsprechenden Wahrscheinlichkeit aufhalten k•nnen, sog. Ladungswolken oder Orbitale. Sie bieten jeweils Platz f‚r zwei Elektronen mit entgegengesetzt gerichtetem Drehsinn. Atombau und PSE 17 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel Schalen Orbitale mit vergleichbarem Durchmesser (€hnlichem Energieinhalt) geh•ren zu einer Schale. NebenzustÇnde, Unterschalen Orbitale innerhalb einer Schale k•nnen verschiedene r€umliche Formen aufweisen. Diese bezeichnet man als Nebenzust€nde. Je gr•sser die Schale, umso mehr Nebenzust€nde hat sie und je h•her der Nebenzustand, umso mehr Orbitale geh•ren dazu (verschiedene r€umliche Ausrichtungen). Schale s-Orbitale p-Orbitale d-Orbitale f-Orbitale K L M N und h•her 1 1 1 1 3 3 3 5 5 7 Energiestufenschema Der Energieinhalt eines Elektrons in der H‚lle steigt mit der Schalennummer und innerhalb einer Schale mit dem Nebenzustand. Dies f‚hrt dazu, dass sich die Energieb€nder der einzelnen Schalen ‚berlappen k•nnen. Atombau und PSE 18 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel Elektronenkonfiguration Die Einordnung der Elektronen in die Orbitale erfolgt so, dass jedes neu hinzukommende Elektron das niedrigste noch freie Energieniveau einnimmt. Von den Orbitalen eines gleichen Nebenzustandes erh€lt zun€chst jedes Orbital nur ein Elektron, bevor mit der vollen Besetzung mit zwei Elektronen begonnen wird. Beispiele (in der Kurzschreibweise): 2 2 6 2 5 17Cl: 1s 2s 2p 3s 3p 2 2 6 2 6 2 79Au:1s 2s 2p 3s 3p 4s 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d9 Es ergeben sich folgende GesetzmÇssigkeiten: • Die letzte Schale hat nie mehr als 8 Elektronen (s und p). • d-Elektronen werden in der zweitletzten Schale aufgef‚llt. • f-Elektronen werden in der drittletzten Schale aufgef‚llt. Aufgaben 1. Zeichnen Sie die Schalenmodelle von 12Mg und 17Cl ! 2. Erkl€ren Sie die Begriffe Orbital, Schale, Nebenzustand ! 3. Gegeben ist das Atom 107 47 Ag . Wie sind die Elektronen auf die Schalen und Nebenzust€nde verteilt (Kurzschreibweise) ? 4. a) Wie viele Elektronen hat Eisen auf der €ussersten Schale ? b) Wie viele Elektronen hat Iod auf der zweit€ussersten Schale ? C Periodensystem Grundidee • • • • Anordnung der Elemente entsprechend ihren Eigenschaften. Die Elemente sind nach steigender Ordnungszahl angeordnet. Nach jedem Edelgas beginnt eine neue Zeile (Perioden K-Q). Elemente mit €hnlichen Eigenschaften stehen untereinander. Zusammenhang mit dem Aufbau der ElektronenhÄlle Perioden Die Elemente einer Periode haben gleich viele Schalen. Die Periodennummer bezeichnet die €usserste Schale. Atombau und PSE 19 RRi Chemie Technische Berufsmaturit€t BMS AGS Basel Hauptgruppen Hauptgruppenelemente haben ihre energiereichsten Elektronen in den s- und p-Orbitalen der €ussersten Schale. Die Elemente einer Hauptgruppe haben, der Gruppennummer entsprechend, gleich viele Elektronen auf der €ussersten Schale. Nebengruppen Nebengruppenelemente haben ihre energiereichsten Elektronen in den d- und f-Orbitalen der zweit- resp. dritt€ussersten Schale. Auf der €ussersten Schale haben alle zwei sElektronen. In einer Gruppe haben sie gleich viele d-Elektronen auf der zweit€ussersten resp. f-Elektronen in der dritt€ussersten Schale. Valenzelektronen Unter den Valenzelektronen versteht man die Elektronen, die zur Bindungsbildung eingesetzt werden k•nnen. Sie bestimmen somit das chemische Verhalten des Elementes. Die Valenzelektronenzahl der Hauptgruppenelemente entspricht der Hauptgruppennummer. Elektronenschreibweise (Lewisformel) Die Valenzelektronen werden als Punkte (einfach besetzte Orbitale) oder als Striche (doppelt besetzte Orbitale) um das Elementsymbol angeordnet. Beispiele: Calcium Ca Kohlenstoff C Schwefel S Brom Br Aufgaben 1. Worin liegt die Bedeutung des Periodensystems f‚r die Chemie ? 2. Wie viele Valenzelektronen hat Stickstoff N ? Zeichnen Sie die Elektronenstrichformel ! 3. Wie viele Schalen hat Uran U ? Welche sind vollst€ndig gef‚llt ? 4. Warum gibt es nur 8 Hauptgruppen ? 5. Welche Gemeinsamkeiten haben die Nebengruppenmetalle im Aufbau der H‚lle ? 6. Warum steht Wasserstoff H in der ersten Hauptgruppe, ist aber kein Alkalimetall ? Atombau und PSE 20 RRi