Praktikumsskript - Institut für Klinische Neurobiologie
Werbung

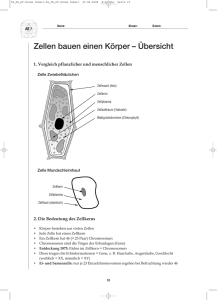
-Skript zum Praktikum Spezielle Biowissenschaften II Institut für Klinische Neurobiologie 28.11. bis 02.12. 2016 Bitte Laborkittel mitbringen und leeren USB Stick !!! Treffpunkt am 28.11.2016 um 8:50 Uhr am Eingang von Haus E4, Versbacherstr. 5 Zusammenfassungen der Vorträge Nervenzellen, Gliazellen, extrazelluläre Matrix, Prof. Sendtner Motorik (Kleinhirn, Basalganglien, Rückenmark), Dr. Jablonka Hippokampus, Dr. Blum Synaptologie, Dr. Götz Ionenkanäle, Prof. Villmann Kursprogramm Zellkultur Teil Immunohistochemischer Teil Ionenkanäle und Elektrophysiologie Nervenzellen, Gliazellen, extrazelluläre Matrix, Prof. Sendtner Neurotrophe Faktoren wurden ursprünglich als Überlebensfaktoren für embryonale Nervenzellen entdeckt. Viktor Hamburger und Rita Levi-Montalcini, die für die Entdeckung von Nerve Growth Factor (NGF) den Nobel-Preis erhalten hat, konnten zeigen, dass Proteine, die in sehr geringen Mengen im Innovationsgebiet von sensorischen, sympathischen und motorischen Nervenzellen produziert werden, für deren Überleben während der Embryonalentwicklung notwendig sind. Während der Embryonalentwicklung werden bei höheren Wirbeltieren verschiedene Populationen von Nervenzellen, darunter spinale Motoneurone, die sensorischen und sympathischen Nervenzellen der Hinterwurzel bzw. Paravertebralganglien, im Überschuss gebildet. Ca. 50% der postmitotischen Neurone, nachdem sie Kontakt mit dem Zielgewebe gemacht haben, gehen dann wieder zugrunde. Viktor Hamburger konnte in einer Reihe detaillierter Untersuchungen zeigen, dass dieser „physiologische“ Zelltod nicht endogen programmiert ist, sondern durch Signalmoleküle aus dem Innervationsgebiet der jeweiligen Nervenzelltypen gesteuert wird. Diese Befunde waren Ausgangspunkt für Rita Levi-Montalcini für die Identifikation und Reinigung (zusammen mit S. Cohen) eines ersten neurotrophen Faktors, Nerve growth factor (NGF). Abb.1: Assay mit explantierten sympathischen Ganglien (R. Levi-Montalcini) nach Zugabe von Gewebeextrakten, die NGF enthielten NGF ist prototypisches Mitglied einer großen Familie von Neurotrophinen, der neben NGF auch BDNF, NT-3 sowie NT-4/5 bei Säugern angehören. Bei Fischen wurden weitere Mitglieder der NeurotrophinFamilie gefunden, NT-6 und NT-7. Diese neurotrophen Faktoren vermitteln ihre Wirkung auf das Überleben von Nervenzellen über hochaffine Rezeptoren, die ihre Liganden mit einer Affinitätskonstante (KD) von 10-12 M binden. Wesentlicher Bestandteil dieser hochaffinen Rezeptoren sind Transmembranproteine der Tropomyosin-Rezeptorkinase (Trk)-Familie, von denen Trk-A spezifisch NGF bindet, Trk-B sowohl BDNF als auch NT-4/5 erkennt, und Trk-C bevorzugt NT-3 bindet. Abb.2: Schematische Darstellung der Bindung von Mitgliedern der Neurotrophinfamilie an Trk Rezeptoren und den p75NTR Rezeptor. Neben diesen Transmembrantyrosinkinaserezeptoren existiert ein niederaffiner Neurotrophin-Rezeptor (p75NTR), der alle bekannten Neurotrophine mit ähnlicher Affinität (KD 10-9 M) bindet. Aufgrund der hohen Bindungsaffinität von Neurotrophinen an hochaffine Rezeptoren (KD von 10-12M) ist verständlich, dass nur sehr geringe Mengen dieser Neurotrophine (weniger als 1ng/g Gewebe) ausreichen, um ca. 2 die Hälfte der während der frühen Embryonalentwicklung generierten Neurone am Leben zu halten. Typisch für Mitglieder der Neurotrophinfamilie ist die hohe Spezifität für bestimmte Zellpopulationen: NGF wirkt nur auf sympathische Neurone der paravertebralen Ganglien sowie eine Subpopulation sensorischer Neurone, jedoch nicht auf motorische Nervenzellen sowie propriozeptive sensorische Neurone. NT-3 wirkt insbesondere auf -Motoneurone sowie schnell leitende Subgruppen von sensorischen Nervenzellen, BDNF auf motorische Nervenzellen sowie Subgruppen sensorischer Neurone. Die Elimination des NGF-Gens führt zu einem fast vollständigen Absterben sympathischer Nervenzellen in den Paravertebralganglien, die Mäuse sind so nicht überlebensfähig und sterben spätestens in der 3. postnatalen Woche. Ähnliche Beobachtungen wurden auch bei BDNF- und NT-3-defizienten Mäusen gemacht, bei denen die jeweiligen Neuronengruppen, die von diesen Faktoren abhängig sind, selektiv zugrunde gehen. Die Injektion bzw. transgene Überexpression von Neurotrophinen bewirkt nicht nur erhöhtes Überleben, sondern auch erhöhte neuronale Aktivität sowie Faseraussprossen. So führt z.B. die Injektion von NGF bei neugeborenen Mäusen und Ratten zu einem Aussprossen von Schmerz-leitenden Fasern und einer erhöhten Sensibilität. Abb3: Wirkung einer Injektion von NGF bei neugeborenen Ratten auf Überleben und Faseraussprossen bei langsamleitenden sensorischen Neuronen Die Funktion des Nervensystems wird nicht nur durch die neurotrophen Faktoren der NeurotrophinFamilie, sondern auch durch andere Familien von neurotrophen Faktoren beeinflusst und reguliert. Zu diesen Faktoren gehören die Mitglieder der Glia-derived-neurotrophic-factor (GDNF-)Familie sowie die neurotrophen Zytokine der Ciliary neurotrophic factor (CNTF)/Leukemia-inhibitory factor (LIF)/Cardiotrophin-1 (CT-1)-Familie. Besonders die Mitglieder der letzten Familie werden erst relativ spät während der Entwicklung exprimiert, einzelne Faktoren, insbesondere CNTF erst postnatal, dann aber in sehr hohen Mengen. CNTF wird nicht im Zielgewebe von responsiven sensorischen und motorischen Nervenzellen exprimiert, sondern in myelinisierenden Schwannzellen. Nach Nervläsion steht dieser Faktor so direkt zur Verfügung und kann so das Überleben von axotomierten Nervenzellen verbessern. So ergibt sich ein komplexes Bild über die Wirkung von neurotrophen Faktoren: neben der klassischen Wirkung auf das Überleben spezifischer Gruppen von Nervenzellen während der Embryonalentwicklung sind sie notwendig für die Regulation synaptischer Aktivität, für die Aufrechterhaltung von Nervenzellverbindungen und Axonen sowie für die Regeneration nach Läsion. 3 Extrazelluläre Matrix Der Extrazellulärraum erfüllt nicht nur Aufgaben für die Stabilität der Architektur des Nervensystems, sondern ist auch aktiv in Regelprozesse einbezogen, die die Funktionalität von Glia- und Nervenzellen beeinflussen. Diese Regelmechanismen spielen gerade für Neurone eine große Rolle. Verschiedene Bestandteile der extrazellulären Matrix sind für das Auswachsen von Nervenfasern von großer Bedeutung, und sie beeinflussen die Funktionalität von synaptischen Verbindungen. Neben den klassischen Matrixmolekülen wie Fibronectin, Laminin und Collagen, die über Integrin-Rezeptoren Signale in den Nervenzellen vermitteln, enthält die extrazelluläre Matrix eine Reihe von Bestandteilen, die als klassische Signalmoleküle über Tyrosinkinaserezeptoren Differenzierung, Zellwanderung, Überleben, Axonwachstum und synaptische Aktivität beeinflussen. Dazu gehören einerseits an Heparin gebundene Wachstumsfaktoren, zum anderen Signalmoleküle, die Axonwachstum stimulieren bzw. blockieren, aber auch Proteine wie Agrin, die eine wesentliche Rolle bei der Bildung spezifischer Synapsen, z.B. an der neuromuskulären Endplatte spielen. Empfohlene Literatur: Albert, Bray, Lewis et al: Molecular Biology of the Cell, 3. Auflage 1994, Kapitel IV/19, Cell Junctions, Cell Adhesion, and the extracellular Matrix S. 949-1011 Literatur: Alberts: Molecular Biology of the Cell: Kapitel 21: Cellular mechanisms of development Kandel (4. Auflage) Part VIII: Develoment of the Nervous System. 4 Motorik (Kleinhirn, Basalganglien, Rückenmark), Dr. Jablonka Motorische Hirnrinde: Repräsentationsfelder und Verteilung kortikaler Motorneurone im Gyrus Präcentralis Projektion von der motorischen Großhirnrinde zum Rückenmark Das Rückenmark hat vom Großhirn unabhängige Schaltkreise Projektion vom Rückenmark zum Muskel Kleinhirn: Das Kleinhirn (Cerebellum) besteht aus einem unpaarigen Mittelteil (Vermis) und Kleinhirnhemisphären. Die Gliederung kann nach verschiedenen Gesichtspunkten erfolgen: • Nach phylogenetischen Aspekten in das Archicerebellum, das Palaeocerebellum und das Neocerebellum. • Makroanatomische Einteilung entsprechend transversalen Fissuren in den Lobus anterior der durch die Fissura prima vom Lobus posterior getrennt ist, und der wiederum durch die Fissura posterolateralis vom Lobus flocculo-nodularis • Nach Verbindungen und funktionellen Aspekten in das Spinocerebellum (Bewegungsausführung, ~Lobus anterior) Cerebrocerebellum (Bewegungsplanung, ~Lobus posterior) und das Vestibulocerebellum (Gleichgewichtssteuerung, ~Lobus flocculo-nodularis) • Gliederung des Kleinhirns entsprechend transversalen Fissuren in 10 Folien, die mit römischen Ziffern von I bis X bezeichnet werden. Im Kleinhirn unterscheidet man wie im Großhirn zwischen Rinde und dem Mark mit den zentralen Kernen. Die Rinde schickt ihre Efferenzen in die Kleinhirnkerne. Im Cerebellum gibt es 5 verschiedene Neuronentypen, 2 afferente Fasertypen sowie Gliazellen 5 Basalganglien Die Funktion wird indirekt über den Kortex vermittelt, neuronale Schaltkreise der Basalganglien entwerfen komplexe Erregungsmuster, sie dienen der Einleitung (Initiierung) und der Erleichterung (Fazilitation) von Willkürbewegung, zugleich werden ungewollte oder unwillkürliche Bewegungen unterdrückt. Axonaler Transport und Motoneuronerkrankungen Die Fortsätze von motorischen Nervenzellen des Rückenmarks können beim erwachsenen Menschen oft Längen von ca. 1 Meter erreichen. Jede Nervenzelle muss ständig Proteine und andere Strukturelemente transportieren, um die Funktion auch in vom Zellkörper entfernten Kompartimenten, insbesondere den präsynaptischen Kompartimenten in der Axonterminale aufrecht zu erhalten. Verschiedene Proteine, aber auch mRNAs werden im Zellkörper synthetisiert und in Axonen und Dendriten transportiert. Dieser Vorgang wurde bereits 1948 beschrieben und wird als axonaler bzw. dendritischer Transport bezeichnet. Erst in den vergangenen Jahren wurden die molekularen Mechanismen dieses Transports entlang von Mikrotubuli detailliert aufgeklärt. Bei Untersuchungen über den axonalen Transport stellte sich heraus, dass in beiden Richtungen Substanzen transportiert werden. Der anterograde Transport erfolgt vom Zellkörper zur Synapse hin und dient, in Axonen, vor allem dem axonalen Wachstum sowie synaptischen Plastizitätsprozessen. Beim gegenläufigen retrograden Transport werden Substanzen durch das Axon zum Zellkörper befördert. Hierbei handelt es sich zum Teil auch um Signalproteine und Komplexe, die zum Zellkörper transportiert werden, darunter Rezeptoren für neurotrophe Faktoren mit ihren Liganden. Nach der Geschwindigkeit kann man langsamen von schnellen axonalen Transport unterscheiden. Die Mikrotubuli bilden die Grundlage für zahlreiche zelluläre Bewegungsformen wie beispielsweise der intrazelluläre Transport von Membranvesikeln in den Axonen der Nervenzellen. Diese Bewegungen beruhen entweder auf der Polymerisation und Depolymerisation von Mikrotubuli oder auf der Aktivität der Mikrotubulus-Motorproteine Dynein und Kinesin. Abbildung 1: Dyneinkomplex sowie Kinesine sind Motorproteine für den retrograden bzw. den anterograden Transport. Störungen des axonalen Transport beim Menschen oder bei der Maus sind eine der möglichen Ursachen für Motoneuronerkrankungen, und treten, als Ursache oder sekundär bei fast allen Formen 6 dieser Erkrankungen auf. Motoneuronerkrankungen sind degenerative Erkrankungen der Motoneurone im Rückenmark, die zu Muskelschwäche und -atrophie führen. Die Motoneuronerkrankungen können verschiedenen Ursprungs sein. Die mit am weitesten verbreitete Motoneuronerkrankung ist die sogenannte amyotrophe Lateralsklerose (ALS). Sporadische Formen der ALS beginnen im Erwachsenenalter und betreffen kortikospinale sowie spinale Motoneurone. Das Mausmodel für die sporadische Form der ALS ist die progressive motoneuronopathy mouse (pmn). Abbildung 2: Pmn-Mutante rechts, gesundes Geschwistertier links Das Krankheitsgen der pmn Mutante wurde durch positionelle Klonierung identifiziert und kodiert für ein sogenanntes Tubulinspezifisches Chaperon E (Tbc E), einen Cofaktor, der die Heterodimerisierung von α und β Tubulin unterstützt. Isolierte embryonale Tbc E-defiziente Motoneurone zeigen Störungen im Axonwachstum und weisen überdurchschnittlich viele axonale Schwellungen auf. In diesen axonalen Schwellungen liegt eine gestörte Kolokalisation von Tubulin und seinem assoziierten Protein p-Tau vor. Abbildung: Verteilung von p-Tau und Tubulin in Kontroll- und Tbc E-defizienten Motoraxonen von isolierten Motoneuronen. Aber nicht nur Komponenten für die Bildung der Mikrotubuli, auch die Motorproteine können bei Dysfunktion zu Motorneuronerkrankungen führen (z.B. Loa und Cra Mäuse). Letzten Endes ist jedoch das Ziel der Untersuchung der pathomechanistischen Ereignisse, die zu Motoneuronerkrankungen führen, eine mögliche Therapie dagegen zu entwickeln. Erste Therapieansätze wurden bei der pmn Mutante entwickelt. Durch CNTF Gabe ist es gelungen, den pmnPhänotyp zu mildern. 7 Literatur: Fundamental Neuroscience, second edition Principles of Neural Science (Kandel), fourth edition 8 Aufbau von und Reizleitung an Synapsen, Dr. Götz Tiere nehmen Reize der Umgebung wahr und reagieren darauf in ihrem Verhalten, z. B. durch Bewegungen. Eine sehr große Zahl von Nervenzellen oder Neuronen (etwa 1011 beim Menschen) ist an der Erfüllung dieser Leistung beteiligt. Die Hauptaufgaben der Neurone sind Empfang, Integration und Weiterleitung von Information als elektrisches oder chemisches Signal. Die Neurone sind durch Kontaktstellen, Synapsen, untereinander oder mit anderen Zelltypen, wie z. B. Muskelzellen, verschaltet. Der Begriff Synapse wurde von Charles Sherrington eingeführt, um die Kontaktregion zu beschreiben. Neurale Schaltkreise werden strukturell durch Axone, Dendriten und die sie verbindenden Synapsen definiert. Neuronale Fortsätze haben in der Regel eine hohe Dichte an Synapsen. Ein typisches Neuron besitzt etwa eintausend synaptische Verbindungen. Ermöglicht wird dies durch die komplexe Struktur von Nervenzellen mit ihren ausgeprägten Fortsätzen und der damit verbundenen großen Oberfläche. Bei Neuronen mit langen Axonen kann die Oberfläche sogar Millionen von µm2 betragen. Eine hohe Zahl an Synapsen kann auch durch weit verzweigte Dendritenbäume und deren axonale Kontakte zustande kommen, wie es z. B. bei den Purkinjezellen mit ihren etwa 200.000 Synapsen der Fall ist. Abbildung. Weitverzweigter Dendritenbaum im Kleinhirn (Cerebellum). Im Cerebellum bildet jede Purkinjezelle viele Tausend Parallefasesynapsen aus, und zwar in einen hochgradig verzweigten Dendritenbaum, welcher Synapsen mit den Axonen (Parallelfasern) der Körnerzellen (granule cells) bildet. Bild aus Wong und Ghosh, Nature Reviews Neuroscience, 3, 803-812, 2002. Synapsen werden je nach Form der Erregungsübertragung und Art der Erregung in elektrische und chemische Synapsen untergliedert. Die große Mehrheit der Synapsen im Gehirn sind chemische Synapsen, d. h., sie setzen Neurotransmitter frei, um eine Reizantwort in der postsynaptischen Zelle auszulösen. Man unterscheidet erregende von hemmenden Neurotransmittern. Der wichtigste erregende Neurotransmitter im Gehirn ist Glutamat (exzitatorische Synapse). Die wichtigsten hemmenden Transmitter im ZNS sind Gamma-Aminobuttersäure (GABA) und Glyzin (inhibitorische Synapse). Andere Transmitter sind Noradrenalin, Acetylcholin, Dopamin, Serotonin. Acetylcholin vermittelt zum Beispiel die Erregungsübertragung zwischen Nerv und Muskel an der neuromuskulären Endplatte. 9 Im Fall der elektrischen Synapse erfolgt die Erregung der postsynaptischen durch die präsynaptische Nervenzelle durch eine direkte strukturelle Verbindung, sog. gap-junction Kanäle. Der synaptische Spalt misst nur rund 3,5 nm. Elektrische Synapsen arbeiten verzögerungsfrei. Die Erregungsübertragung kann in beide Richtungen laufen. Sie kommen vor allem dort vor, wo eine schnelle Reizübertragung notwendig ist, wie z. B. in der Vertebratenretina oder dem Lidreflex. Abbildung. Struktur und molekulare Organisation von Zell-Zell-Kanälen (gap junctions). Zell-ZellKanäle werden zwischen gegenüberliegenden Membranen von zwei benachbarten Zellen ausgebildet. Jeder Halb-Kanal, auch Connexon genannt, besteht aus sechs Connexin Untereinheiten und bildet eine Pore aus, durch die Ionen und kleine Moleküle bis zu einer Masse von 1.000 Da passieren können. Bild aus Bloomfield und Völgyi, Nature Reviews Neuroscience, 10, 495-506, 2009. Im Unterschied zur elektrischen Synapse gibt es bei der chemischen Synapse keine strukturelle Verbindung zwischen dem prä- und postsynaptischen Neuron. Alle chemischen Synapsen besitzen ein präsynaptisches Terminal. Diese spezialisierten Vergrößerungen können entweder am Ende des Axons (Endknöpfe oder Boutons terminaux) oder auch entlang des Axonschafts (Boutons en passant) lokalisiert sein. Im Gehirn gibt es auch Synapsen zwischen Axonen und zwischen Dendriten. Die postsynaptische Region (post-synaptic density) ist durch den synaptischen Spalt (etwa 20-40nm weit) vom präsynaptisches Terminal getrennt. Die Mehrheit der glutamatergen exzitatorischen Synapsen im Gehirn ist in dendritischen Dornfortsätzen (englisch spines) lokalisiert. Diese wachsen oft mit einem schmaleren Hals aus der Dendritenoberfläche empor und enden mit einem mehr oder weniger voluminösen Kopf, in dem sich auch die zugehörige Synapse befindet. Die Dornfortsätze bilden sich während der Entwicklung aus und werden später bis ins adulte Alter reizabhängig verändert. Um bei der Synapsenbildung die präsynaptische aktive Zone in Nachbarschaft zur Postsynapse räumlich korrekt ausbilden zu können, werden vielfältige Signale benutzt. So wird z. B. von Motoneuronen Agrin freigesetzt, welches einen Transmembranrezeptor auf den Muskelzellen aktiviert und so das Klustern von Acetylcholinrezeptoren in der neuromuskulären Endplatte induziert. Um einen Reiz zu übertragen, setzt die Präsynapse Neurotransmitter aus synaptischen Vesikeln frei. Die synaptischen Vesikel sind an Stellen lokalisiert, die man „aktive Zonen“ nennt. Ein präsynaptisches Aktionspotential führt zum Kalzium (Ca2+)-Einstrom nach Öffnung spannungsgesteuerter Ca2+-Kanäle in 10 der aktiven Zone. Die Erhöhung der intrazellulären Ca2+-Konzentration führt dann zur Fusion der Vesikel mit der präsynaptischen Membran und dementsprechend der Neurotransmitter-Freisetzung in den synaptischen Spalt. Die Neurotransmitter diffundieren durch den synaptischen Spalt und binden an passende Rezeptoren der postsynaptischen Zellmembran. Neurotransmitter-Rezeptoren sind zusammen mit mehr als 500 anderen Proteinen in der „postsynaptischen Dichte“ (postsynaptic density) konzentriert. Die Bindung der Neurotransmitter an postsynaptische Rezeptoren führt zur Aktivierung von Ionenkanälen, wodurch sich das Membranpotential in der postsynaptischen Zelle ändert. Abbildung. Glutamaterge Synapsen des Gehirns. In der aktiven Zone befinden sich Vesikel mit dem Neurotransmitter Glutamat. Die präsynaptische Region ist vom Dornfortsatz im postsynaptischen Dendriten durch einen Synapsenspalt getrennt. In der postsynaptischen Membran des Dendriten befinden sich Glutamatrezeptoren (AMPA, α-amino-3-hydroxy-5-methlisoxazole-4-propionic acid, und NMDA, N-methly-D-aspartate, Rezeptoren), die von Gerüstproteinen zusammengehalten werden und die „postsynaptische Dichte“ (postsynaptic density) bilden. Synaptische Aktivität setzt Glutamat in den Synapsenspalt frei. Dadurch wird der NMDA Rezeptor aktiviert; durch den Einstrom von Ca2+-über den NMDA Rezeptor kann sich die Morphologie und Stärke der Synapse verändern. Bild aus Cohen und Greenberg, Annu. Rev. Cell Dev. Biol. 24, 183-209, 2008. Der Ca2+-Einstrom über den NMDA Rezeptor verändert sowohl lokal die Synapse als auch die Transkription von Genen und die Synthese von Proteinen, die stabil die neuronale Funktion verändern können. Im adulten Gehirn stattfindende Schaltkreisveränderungen werden durch den Begriff der funktionellen und strukturellen synaptischen Plastizität beschrieben. Hiermit wird das Phänomen erfasst, dass eine Stimulation von Neuronen die Stärke der synaptischen Übertragung verändern kann. Diese Änderungen können sowohl durch Änderungen der Morphologie als auch der Physiologie der Synapse verursacht werden. Die am besten untersuchten Formen dieser Reiz-abhängigen Anpassung der Synapsenstärke ist die sog. Hebb'scher Plastizität, die LTP (long-term potentiation) und LTD (long-term depression) umfasst. Man glaubt, dass die bei der synaptischen Plastizität verstärkten, neu gebildeten oder verschwindenden Synapsen die Basis für Langzeitgedächtnis und Lernvorgänge sind. LTP und LTD der synaptischen Aktivität werden kurzfristig durch lokale Synapseneffekte gesteuert, z. B. die Lokalisierung der AMPA Rezeptoren in der Synapse oder außerhalb der Synapse. Dies gilt ebenso für 11 die Verteilung der NMDA Rezeptoren, da synaptische NMDA Rezeptoren Signalwege des neuronale Überlebens aktivieren, während extrasynaptische Lokalisierung Signalwege aktiviert, die zum Zelltod führen können. Eine Fehlverteilung der NMDA Rezeptoren wird als ein möglicher molekularer Pathomechanismus bei der Huntington´schen Erkrankung diskutiert. Langfristige Änderungen der Synapsenstärke erfolgen dadurch, dass der Ca2+-Einstrom Signalwege aktiviert, die die Expression von Genen im Zellkern reguliert. Die aktivitätsgesteuerte Expression von mRNA und Proteinen erlaubt es, dass der Zellkern die Synapsen verändern kann. Als ein Beispiel sei hier der selektive Transport der mRNA für den Wachstumsfaktor BDNF (Brain-Derived Neurotrophic Factor) in den Dornfortsatz des Dendriten erwähnt. Die Translation der BDNF mRNA erfolgt aktivitätsabhängig im Dornfortsatz, wodurch das BDNF Protein freigesetzt wird und über die Bindung an präsynaptische BDNF-Rezeptoren die Präsynapse verändern kann (sog. retrograder Signalweg). Literatur: Principles of Neural Science, 4th Edition. Herausgeber Eric R. Kandel, James H. Schwartz, Thomas M. Jessell. McGraw-Hill, New York. 12 Neuronale Schaltkreise für die Untersuchung synaptischer Plastizität: der Hippocampus und das Kleinhirn (Dr. Blum) „When an axon of cell A is near enough to excite a cell B and repeatedly or persistently takes part in firing it, some growth process or metabolic change takes place in one or both cells such that A’s efficiency, as one of the cells firing B, is increased“ (Donald Hebb, 1949) Die Signalübertragung zwischen Nervenzellen findet vorwiegend an Synapsen statt. Adaptive Prozesse an Synapsen (synaptische Plastizität), als Folge eines zeitlich und räumlich synchronisierten Informationsflusses über Synapsen, spielen eine bedeutende Rolle für die verschiedenen Formen von Lernen und Gedächtnis. Im Jahr 1973 beschrieben zwei Studien durch T.V.P Bliss, T. Lømo, und Gardner-Medwin erstmals das Phänomen der Langzeitpotenzierung (LTP, long-term potentiation). In ihren Experimenten konnten die Autoren zeigen, dass wiederholte, zeitlich koordinierte Reize von hippocampalen Eingangsstrukturen eine signifikante und langanhaltende Verstärkung von Synapsen im hippocampalen Schaltkreis hervorrufen. Erstbeschreibung der LTP. In Folge einer kurzen, aber intensiven synaptischen Reizung werden die aktivierten Synapsen zwischen Neuronen langanhaltend verstärkt. In dem gezeigten Experiment wurde durch das Auslösen von Aktionspotenzialserien auf den Axonen des Tractus perforans (PP) die glutamaterge Synapse der Körnerzellen im Gyrus dentatus (AD) so stark gereizt, dass die Effizienz der synaptischen Transmission im dendritischen Bereich der Körnerzellen, als auch die Erregbarkeit der Körnerzellen langfristig gesteigert war. Der definierte „starke Gebrauch“ von Synapsen kann folglich schnelle, molekulare Änderungen hervorrufen, die dieselben Synapsen mit stark erhöhten Erregenden PostSynaptischen Potentialen (EPSPs) auf Einzelreize reagieren lässt. In Anlehnung an das Hebb’sche Postulat aus dem Jahr 1949 werden aktivitätsabhängig modifizierbare synaptische Verbindungen zwischen zwei Neuronen auch Hebb’sche Synapsen genannt. Heute wird das Phänomen der LTP als geeignetes Modell zur Erforschung der molekularen Grundlagen des Lernens erachtet, da es viele Kriterien eines neuronalen Korrelats des Gedächtnisses erfüllt. Die bedeutendsten neuronalen Schaltkreise zur Erforschung der synaptischen Plastizität sind die des Hippocampus und des Kleinhirns. Beide Modellsysteme sind strukturell einfach aufgebaut und verschaltet, bieten experimentellen Zugang unter in situ und in vitro Bedingungen und erlauben zumindest punktuell eine Kausalbeziehung zwischen Vorgängen synaptischer Plastizität auf zellulärer Ebene und der Gedächtnisbildung auf Verhaltensebene. 13 Hippocampus Funktionell ist der Hippocampus die zentrale Struktur des deklarativen Gedächtnisses (Fakten, Ereignisse, räumliche Zusammenhänge) und vermittelt auch Kontext-abhängige Elemente des Lernens. Die hippocampale Formation Hippocampus besteht aus dem Rindenband (Cornu ammonis; CA) und in dem Zellband (Gyrus dentatus, AD). Synaptische Plastizität kann im Hippocampus auf zwei Ebenen untersucht werden: (1) ausgehend von der Betrachtung des trisynaptischen, erregenden Schaltkreises des Hippocampus; (2) ausgehend von der Integration neugenerierter Körnerzellen in den bestehenden hippocampalen Schaltkreis im Rahmen der adulten Neurogenese. Der trisynaptische Schaltkreis: 1. Synapse: Input von Neuronen des entorhinalen Cortex, die ihre Axone über den Tractus perforans mit vielen Synapsen im Dendritenbaum der Körnerzelle des Gyrus dentatus verbinden. 2. Synapse: Die Axone der Körnerzellen (sog. Moosfasern) verbinden sich mit Pyramidenzellen in der CA3 Region. 3. Synapse: Eine Axonkollaterale der CA3 Pyramidenzelle (sog. Schafferkollaterale) projiziert zu Pyramidenzellen der CA1 Region. Die generalisierte Betrachtungsweise vieler Lehrbücher suggeriert einen einheitlichen molekularen Mechanismus synaptischer Lernvorgänge, wie sie an der Synapse CA3-CA1 (Schafferkollaterale-CA1) beobachtet wurden. Hier braucht die LTP einen postsynaptischen ionotropen Glutamatrezeptor (Typ NMDA) und ein postsynaptisches Ca2+ Signal. Zwar wird an allen Synapsen des trisynaptischen Schaltkreises LTP unter glutamaterger Übertragung beobachtet, doch gilt es als erwiesen, dass synaptische Plastizität an der Moosfasersynapse NMDA-Rezeptor-unabhängig ist, ein präsynaptisches Ca2+ Signal braucht und somit eine bevorzugt präsynaptische Komponente trägt. Die Kommunikation der Postsynapse mit der Präsynapse bei der synaptischen Plastizität ist weitgehend ungeklärt. Dennoch häufen sich Hinweise, dass das Neurotrophin BDNF (siehe Beitrag Prof. M. Sendtner) hier eine wesentliche Rolle spielt. Seit 1995 ist bekannt, dass die Freisetzung von BDNF im Rahmen der Induktion von LTP eine funktionelle Rolle spielt und sich über die Rezeptortyrosinkinase TrkB vermitteln kann. Die molekularen Signalübertragungsmechanismen, sowie Modelle, die die schnelle Sekretion des Proteins BDNF erklären können, sind jedoch umstritten. Adulte Neurogenese im Hippocampus Jüngste Forschungen konnten in der Zone unterhalb des Körnerzellbands des Gyrus dentatus (subgranular zone) funktionelle, adulte Neurogenese nachweisen. Hier entstehen aus teilungsfähigen Vorläuferzellen mit Eigenschaften astrozytärer Gliazellen lebenslang glutamaterge Körnerzellen. Erst im Jahr 2008 konnte nachgewiesen werden, dass neugenerierte Körnerzellen sich in das bestehende neuronale Netzwerk des Hippocampus funktionell und synaptisch integrieren. 14 Körnerzellen, die sich im adulten Gyrus dentatus neu gebildet haben. Die Zellen wurden mit einem Virus markiert, der nur in teilungsfähigen Zellen zum Ausdruck kommt und so die Entwicklungs-linie der hippocampalen Stammzellen darstellen kann. Bild aus: Toni et al. 2008 Kleinhirn und synaptische Lernvorgänge Die physiologische Aufgabe des Kleinhirns ist Kontrolle –Kontrolle der Halte- und Stützmotorik, der Bewegungskoordination, der Zielmotorik und ihrer Kurskorrektur, sowie ballistischer Bewegungen. Menschen mit Kleinhirndefekten sind in ihrem motorischen Lernen stark beeinträchtigt und zeigen einen gewissen Verlust bewegungsbezogener kognitiver Funktionen. Eine Besonderheit der Kleinhirnphysiologie ist die eindeutige Zuordnung der zellulären Grundlage des afferenten und efferenten Informationsflusses. Zentrale Schaltstelle ist die Purkinjezelle, die über die Moosfaser- und Kletterfasereingänge eine Efferenzkopie des motorischen Vorhabens erhält und optimierend in die Bewegung eingreift. Die Purkinjezelle besitzt im Vergleich zu anderen principal neurons des ZNS einige ungewöhnliche Eigenschaften. Sie besitzt (1) eine hohe, basale Aktivitätsrate, (2) kein klassisches Ruhemembranpotential, und (3) kommuniziert inhibitorisch über den Transmitter GABA. Die Projektion der Purkinjezelle zu den Kleinhirnkernen ist die einzige Efferenz aus dem cerebellären Kortex, einer zentralen Struktur des motorischen Lernens. Interessanterweise können synaptische Lernvorgänge an Purkinjezellsynapsen mit einer reziproken Form der synaptischen Plastizität, der LTD (Langzeitdepression, long term depression) korreliert werden. Hierbei wird durch koordinierte Stimulation der Kletterfaser- und Moosfasereingänge die Synapse der Parallelfaser zur Purkinjezelle in ihrer synaptischen Stärke langzeitig geschwächt und somit das Feintuning des cerebellären outputs bestimmt. Tiermodelle, bei denen diese spezifische synaptische Übertragung gestört ist, zeigen in Verhaltensversuchen eine starke Beeinflussung der motorischen Fähigkeiten und des motorischen Lernens, bis hin zu einer ausgeprägten Ataxie. Wird eine Parallelfaser repetitiv gereizt, so können in PF-Purkinjezellsynapsen zwei Typen von Ca2+ Signalen beobachtet werden. (1.) Ein schnelles Ereignis wird durch Glutamatrezeptoren vom AMPA-Typ initiiert (postsynaptische Depolarisierung) und öffnet unmittelbar spannungsabhängige, dendritische Ca2+ Kanäle. (2.) Ein langsameres Ereignis vermittelt über metabotrope Glutamatrezeptoren (mGluR1) die Freisetzung von Ca2+ aus dem Endoplasmatischen Retikulum (ER). Die Freisetzung von Ca2+ aus dem ER führt wiederum zur Aktivierung von Ionenkanälen in der Plasmamembran, die erneut eine lokale Depolarisierung des Dendriten bewirken. Verantwortlich für dieses Signal sind sogenannte TrpIonenkanäle (Trp, transient receptor potential channels). Aus der riesigen Familie der Trp-Kanäle, die man häufig auch als sensorische Kanäle des Nervensystems bezeichnet, wurde der Kanal TrpC3 als maßgeblich für die synaptische Transmission an der PF-Purkinjezelle ermittelt. Mausmodelle denen dieser Kanal fehlt, zeigen starke Defekte der motorischen Koordination (Hartmann et al. 2008). Ein natürlich vorkommendes Mausmodell mit motorischen Defekten (moonwalker) zeigt eine Mutation im Gen, das für den Kanal TrpC3 kodiert. 15 Diese Befunde belegen eindringlich die Nützlichkeit einer detaillierten anatomischen, physiologischen und molekularen Beschreibung synaptischer Systeme. Dieses Wissen erlaubt ein besseres Verständnis klinischer Phänomene und hilft bei der Entwicklung neuartiger Therapien. Neuronaler Schaltkreis im cerebellären Kortex und Orte synaptischer Plastizität (1-5). Der cerebelläre Schaltkreis bietet innerhalb eines definierten Informationsflusses (Pfeile) die Möglichkeit Formen der synaptischen Plastizität zu untersuchen. An Purkinjezellsynapsen wird LTD durch Koinzidenz von zwei Signalen hervorgerufen, die über Kletterfasern (CF) und Parallelfasern (PF) vermittelt werden (CF-PF pairing). Signale, die zur Vermittlung der Purkinjezell-LTD führen, sind gut beschrieben und bieten eine experimentelle Grundlage zur Untersuchung der molekularen Mechanismen synaptischer Plastizität. Eine Purkinjezelle der Ratte unterhält bis zu 175.000 Synapsen zu Parallelfasern und bis zu 26.000 zu Kletterfasern. Es konnte gezeigt werden, dass postsynaptische Ca2+ Signale in einzelnen Purkinjezellsynapsen ursächliche Mediatoren der Purkinjezell-LTD darstellen können. Jüngere Forschungen haben einen Mechanismus der synaptischen Plastizität offengelegt, der unabhängig von NMDA-Typ Glutamatrezeptor ist. Literatur: *Fundamental Neuroscience; *Principles of Neural Science, *Physiologie des Menschen. Milner, Squire & Kandel (1998) Cognitive Neuroscience and the study of memory. Neuron 20: 445 ff. Ito M. (2002) The molecular organization of cerebellar long-term depression. Nature Rev Neurosci 3: 896-902. 16 Ionenkanäle, Prof. Villmann Die außerordentliche Komplexität des menschliches Gehirns ist begründet durch seinen komplizierten Aufbau, die Vielfalt seiner Funktionen wie Wahrnehmung und Bewegungskontrolle sowie Gedächtnis. Zusätzlich unterteilt man in verschiedene Organisationsebenen von Genen, über Moleküle, Zellen, Zellsysteme bis zum Verhalten des Organismus. Die neurobiologischen Fragestellungen nähern sich dem in ausschnitthaften spezialisierten Vorgehen ähnlich einem Puzzle, wodurch in einem überschaubaren engen Bereich möglichst viel über die Funktion des Nervensystems herausgefunden und dann zur Rekonstruierung der globalen Zusammenhänge benutzt wird. Während neurotrophe Faktoren für die Entstehung und Erhaltung neuronaler Faserverbindungen unentbehrlich sind, übermitteln Neurotransmitter die neuronale Erregung von Nervenzelle zu Nervenzelle. Exzitatorische (erregende) sowie inhibitorische (hemmende) Neurotransmitter binden an entsprechende Ionenkanäle, die integrale Membranproteine darstellen. Diese sind nicht einfach Löcher in der Membran, sondern hochspezialisierte Tunnelproteine, die (1) Ionen transportieren, (2) spezifische Ionen erkennen und selektieren und sich spezifisch (3) als Folge eintreffender elektrischer, mechanischer oder chemischer Signale öffnen bzw. schließen. Dabei kann die Flussrate bis zu 100 Millionen Ionen pro Sekunde durch einen einzigen Ionenkanal betragen! Ionenkanal spannungs-gesteuert liganden-gesteuert mechanisch gesteuert Stimulus Veränderung der Spannung chem. Transmitter Veränderung von Druck und Dehnung Tabelle 1 Spannungsgesteuerte und ligandengesteuerte Ionenkanäle Stimulus der Ionenkanäle spannungsgesteuert ligandengesteuert ionotrop Beispiele metabotrop exzitatorisch inhibitorisch cAMP gekoppelt IP3, DAG, Arachidonsäure gekoppelt Tyrosinkinasen NO, CO, Stimulation von cGMP Synthese spannungsgesteuerte Na+ Kanäle Glutamatrezeptoren GABA Rezeptoren Glutamatrezeptoren Glutamatrezeptoren TrkA, TrkB, TrkC, p75 passieren Membran spannungsgesteuerte K+ Kanäle nikotinischer Acetylcholinrezeptor Glycinrezeptoren -adrenerger Rezeptor Insulinrezeptor sehr kurze Halbwertzeit einwärts rektifizierende K+ Kanäle 5HT3 Rezeptor zwei Porendomänen K+ Kanäle spannungsgesteuerte Ca2+ Kanäle Serotoninrezeptoren muskarinischer Acetylcholinrezeptor Dopaminrezeptoren Histaminrezeptoren keine Bindung an Rezeptoren, direkter Effekt auf benachbarte Zellen Die Signalübertragung an der chemischen Synapse findet zwischen prä- und postsynaptischen Neuronen statt. Neurotransmitter werden in Vesikeln im präsynaptischen Neuron gespeichert. Durch einen elektrischen Impuls, das Aktionspotential, fusionieren die Vesikel mit der präsynaptischen Membran und schütten ihren Inhalt durch Exozytose in den synaptischen Spalt aus. An diesem Prozess, den man in mehrere Phasen unterteilt: (I) docking, (II) priming, (III) fusion, release und (IV) recycling, sind zahlreiche Protein-Protein-Interaktionen (SNARE-Proteine) beteiligt (siehe Abbildung 1). Nach Diffusion über den synaptischen Spalt, löst die Bindung des Neurotransmitters an den Rezeptor eine Konformationsänderung aus, die letztlich zur Öffnung des Ionenkanals führt. Diesen Transduktionsprozeß bezeichent man als „gating“ des Kanals. Dadurch wird es dem Aktionspotential ermöglicht zur nächsten Nervenzelle überzuspringen - „jump the gap“. 17 Die Forschung der letzten 15 Jahre führte zur detaillierten Aufklärung des Fusionsund Freisetzungsprozesses von Neurotransmittern. Maßgeblich daran beteiligt ist die Forschungsgruppe um Thomas C. Südhof (Standford University); Brose et al., Science 1992, Ushkaryov et al., Science 1992; Schoch et al., Nature 2002; Tabuchi et al., Science 2007; Kaeser et al., PNAS 2012. http://www.hhmi.org/research/investigators/sudhof.html Abb. 1 Doch was genau passiert nach Bindung des Liganden an den Rezeptor? Wie sehen diese membranassoziierten Proteine aus und wie durchspannen sie die Membran (Abb.2)? Abb. 2 Verschiedene Familien besitzen ähnliches Design. (A) spannungsgesteuerte Na+-, K+-, Ca2+-Kanäle, (B) einwärtsrektifizierende K+ Kanäle, (C) Zwei-Poren K+Kanäle, (D) Nach Klonierung der Ionenkanäle zwischen 1980 und 2000 führten biochemische und molekularbiologische Experimente zu einem deutlich verbesserten Verständnis von Struktur und Funktion von Ionenkanälen so z.B. zum „Ball and Chain“ Modell für spannungsgesteuerte Ionenkanäle (Abb.2). 18 Abb. 2 (nach Bezanilla, Physiological Reviews, 2000). Spannunsgesteuerte Ionenkanäle besitzen Spannungssensoren (Transmembrandomäne 4), die sich durch den hohen Anteil basischer Aminosäuren entsprechend der Ladung ihrer Umgebung in der Membran bewegen (siehe Wechsel von closed nach open). Dadurch wird eine Konformationsänderung verursacht, der „Ball“ (Domäne im N-terminus) bewegt sich zur Ionenkanalpore und verschließt diese (Wechsel von open zu inactivated). Das erregte Neuron kann für eine bestimmte Zeit nicht erneut aktiviert werden – Refraktärzeit. Doch erst durch das Aufklären der Kristallstrukturen ist es möglich bzw. wird es möglich sein, diese Konformationsänderungen bis in den atomaren Bereich hinein zu beschreiben (Abb. 3). Abb. 3 (nach Bocquet et al., Nature 2009). Aufsicht auf prokaryotische Cys-Loop Rezeptoren (A=GLIC aus Gloebacter violaceus und B=ELIC Erwinia chrysanthemi) sowie Seitenansicht der Ionenkanaldurchmesser. Helixrückgrat und Seitenketten die in die Pore hineinragen: Hydrophobe, polare und negativ geladene Aminosäuren sind gelb, grün und rot dargestellt. C, Sequence Alignment der Ionenkanalporen verglichen mit nikotinischem Acetylcholinrezeptor (nAChR) 1. D, Porendurchmesser. Mit Hilfe von elektrophysiologischen Messmethoden wie der Patch-Clamp Technik war/ist es möglich, die Eigenschaften von Ionenkanälen zu beschreiben. Für die Entdeckung dieser Methode erhielten die deutschen Wissenschaftler Bert Sakmann und Erwin Neher 1991 den Nobelpreis für Medizin. Die verschiedenen Konfigurationen und der prinzipielle Aufbau sind in Abb. 4 dargestellt. Auf kleinste Veränderungen von Reizen aus der Umwelt so z.B. die Reaktion von Rezeptoren im Auge auf ein einzelnes Photon aus dem Licht, oder ein einziges Molekül eines Geruchsstoffes auf Rezeptoren im olfaktorischen System müssen Nervenzellen schnell reagieren, indem die starken Veränderungen in den elektrischen Potentialdifferenzen über die Membranen von Nervenzellen weiterleiten. Während eines Aktionspotentials wechseln die Membranpotentiale mit bis zu 500V /s. Die Verarbeitung dieser 19 Signale wird über Ionenkanäle vermittelt. Somit ist ziemlich klar, dass Störungen in der Signalweiterleitung unweigerlich mit pathophysiologischen Veränderungen im zentralen Nervensystem einhergehen was am Beispiel motorischer Bewegungsstörungen näher erläutert werden soll. Abb.4 Durch Ansaugen der Zelle an die Patch-Pipette entsteht eine hochohmige Verbindung (im Gigaseal) zwischen der Membran und der Pipette (aus Borosilikatglas). Dies nennt man die „cell attached“ Konfiguration. Diese Konfiguration erlaubt es, den Membranfleck der intakten Zelle, auf ein bestimmtes Potential zu klemmen. Durch Anlegen eines kurzzeitigen Pipettenunterdrucks, wobei die Verbindung zwischen dem Rand der Spitzenöffnung der Patch-Pipette und der Membran nicht leidet, wird die „whole-cell“- Konfiguration hergestellt. Somit wird die gesamte Zellmembran auf das angelegte Potential der Spannungsklemme gebracht. Es gibt noch zwei weitere Konfigurationen, welche Messungen an von der Zelle abgetrennten Membranfetzen ermöglichen. Die „inside-out“-Konfiguration entsteht, wenn man aus der „cell-attached“ Konfuguration mit einem Ruck die Patch-Pipette von der Zelle wegreißt. Bei der „outside-out“-Konfiguration startet man mit der „whole-cell“Konfiguration, wobei die Pipette langsam von der Zelle weggezogen wird. Störungen in der inhibitorischen Neurotransmission Inhibitorische Neurotransmitter sind -Aminobuttersäure (GABA) und Glycin. Während Glycin der wichtigste inhibitorische Neurotransmitter im Hirnstamm und im Rückenmark ist, besitzt GABA eine weitaus größere Bedeutung in höheren Hirnarealen wie z.B. dem Hippocampus. Glycin/GABA gefüllte Vesikel schütten nach Einstrom von Ca2+ Ionen in die Präsynapse als Folge der Aktivierung spannungsgesteuerter Ca2+-Kanäle ihren Inhalt in den synaptischen Spalt aus. Glycin bindet an Glycinrezeptoren, was zu einem Chlorid-Einstrom in die Zelle führt. Diese Rezeptoren werden über das Ankerprotein Gephyrin an der postsynaptischen Membran verankert (Abb. 5). Mutationen in den Genen welche für die verschiedenen Glycinrezeptor und Untereinheiten kodieren, gehen beim Menschen sowie bei Nagern mit motorischen Bewegungsstörungen einher. Diese werden als postsynaptische Komponente der motorischen Bewegungsstörung Hyperekplexie diskutiert. Die Ursache ist in der fehlenden Feedback-Kontrolle (siehe Bild Projektion Rückenmark-Muskel, Dr. Jablonka) der erregten Motorneurone zu suchen, so dass ein Ungleichgewicht zwischen Exzitation/Inhibition vorliegt. Durch eine Übererregung des Muskels kommt es zur Muskelsteifheit. Weiterhin können die Defekte auch in präsynaptischen Proteinen vorliegen z.B. führen Mutationen im Glycintransporter 2 ebenso zu Hyperekplexie (zweithäufigste Ursache dieser Erkrankung). Außerdem kann eine derartige Bewegungsstörung auch durch Autoimmunantikörper hervorgerufen werden (Abb.5), die die Funktion des Ionenkanals beeinflussen. Der genaue Mechanismus ist bislang unbekannt. 20 Abb. 5 Inhibitorische Synapse. GlyRA adulter Rezeptor Komplex aus 2 und 3 Untereinheiten. GlyRN = neonataler GlyR Komplex, extrasynaptisch bestehend aus 2 Untereinheiten, homomerer Komplex. Verankerung über Gephyrin. VIAAT = vesicular inhibitory amino acid transporter, mGluR = metabotroper Glutamatrezeptor, GABAB = metabotroper GABA-Rezeptor, GlyT1/2 Glycintransporter. Literatur: Principles of Neural Science (Kandel), 5th edition From Molecules to Networks (Byrne and Roberts), 1st edition 2004 Patch-Clamp-Technik (Numberger/Draguhn), Spektrum Verlag 1996 21 Neurobiologie Kursprogramm Uhrzeit Gruppe 1 08.30 Montag 28.11. 09.00 Nervenzellen, Gliazellen, extrazelluläre Matrix Nervenzellen, Gliazellen, extrazelluläre Matrix DRG-Präparation, Tier-OP Ionenkanäle Mausperfusion Waschen der Schnitte 10.30 DRG-Präparation, Tier-OP Mausperfusion 2. Antikörper auf Cerebellum und Hippo. Schnitte 11.00 DRG-Präparation, Tier-OP Gewebe einbetten, 2. Antikörper auf Cerebellum und Hippo. Schnitte 11.30 Zellkultur DRGs Pause Pause 12.00 Pause Pause Pause 12.30 Pause Gewebe schneiden Waschen und Eindeckeln 13.00 Zellkultur DRGs, PC12 Gewebe schneiden Waschen und Eindeckeln 13.30 Zellkultur DRGs, PC12 Gewebe schneiden Waschen und Eindeckeln 14.00 Zellkultur DRGs, PC12 Zellkultur DRGs, PC12 Blocken Waschen und Eindeckeln FV1000, konfokale Mikroskopie Pause FV1000, konfokale Mikroskopie FV1000, konfokale Mikroskopie FV1000, konfokale Mikroskopie Ephys Demo 09.30 10.00 14.30 15.00 Zellkultur DRGs, PC12 15.30 Zellkultur DRGs, PC12 16.0017.30 Zellkultur DRGs, PC12 Dienstag 29.11. Mittwoch 30.11. Donnerstag 01.12. Freitag 02.12. Ionenkanäle Motorik (Kleinhirn, Basalganglien, Rückenmark) Motorik (Kleinhirn, Basalganglien, Rückenmark) Waschen der Schnitte Hippokampus Synaptologie Hippokampus Synaptologie Rezeptor Internalisierung, Labeln Konfokale Bilder Rezeptor Internalisierung, Labeln Rezeptor Internalisierung, Fluoreszenz Markieren Rezeptor Internalisierung, Fluoreszenz Markieren Modulator Inkubation Modulator Inkubation Rezeptor Internalisierung, Fluoreszenz Markieren Rezeptor Internalisierung, Fluoreszenz Markieren Fixieren Eindeckeln Auswertung Internalisierung Mausperfusion Blocken, 1. Antikörper auf Cerebellum und Hippoc. Schnitte Blocken, 1. Antikörper auf Schnitte Blocken, 1. Antikörper auf Schnitte Blocken, 1. Antikörper auf Schnitte 22 Pause Ephys Demo cLabs – virtuelle Rezeptoren Abschlussbespre chung Abschlussbespre chung Uhrzeit Gruppe 2 08.30 Montag 28.11. 09.00 10.00 Nervenzellen, Gliazellen, extrazelluläre Matrix Nervenzellen, Gliazellen, extrazelluläre Matrix Mausperfusion 10.30 Mausperfusion 2. Antikörper auf Cerebellum und Hippo. Schnitte 11.00 Mausperfusion 2. Antikörper auf Cerebellum und Hippo. Schnitte 11.30 Gewebe einbetten, Pause 12.00 Pause Pause 12.30 Pause Waschen und Eindeckeln 13.00 Gewebe schneiden Waschen und Eindeckeln 13.30 Gewebe schneiden Waschen und Eindeckeln 14.00 Gewebe schneiden 14.30 Blocken 15.00 Blocken, 1. Antikörper auf Cerebellum und Hippoc. Schnitte Blocken, 1. Antikörper auf Schnitte Blocken, 1. Antikörper auf Schnitte Blocken, 1. Antikörper auf Schnitte 09.30 15.30 16.00 16.3017.30 Dienstag 29.11. Mittwoch 30.11. Donnerstag 01.12. Freitag 02.12. Ionenkanäle Motorik (Kleinhirn, Basalganglien, Rückenmark) Motorik (Kleinhirn, Basalganglien, Rückenmark) Rezeptor Internalisierung, Labeln Hippokampus Synaptologie Hippokampus Synaptologie DRG-Präparation, Tier-OP Auswertung Internalisierung Rezeptor Internalisierung, Labeln Rezeptor Internalisierung, Fluoreszenz Markieren Rezeptor Internalisierung, Fluoreszenz Markieren Modulator Inkubation Modulator Inkubation Rezeptor Internalisierung, Fluoreszenz Markieren Rezeptor Internalisierung, Fluoreszenz Markieren Fixieren Eindeckeln DRG-Präparation, Tier-OP konfokale Bilder DRG-Präparation, Tier-OP Abschlußbesprec hung Zellkultur DRGs Abschlußbesprec hung Waschen und Eindeckeln FV1000, konfokale Mikroskopie FV1000, konfokale Mikroskopie Pause Zellkultur DRGs, PC12 Zellkultur DRGs, PC12 Ephys Demo Zellkultur DRGs, PC12 FV1000, konfokale Mikroskopie FV1000, konfokale Mikroskopie Waschen der Schnitte Ephys Demo Zellkultur DRGs, PC12 Ionenkanäle Waschen der Schnitte Waschen der Schnitte Pause cLabs – virtuelle Rezeptoren Ephys Demo 23 Pause Pause Zellkultur DRGs, PC12 Zellkultur DRGs, PC12 Zellkultur DRGs, PC12 Uhrzeit Gruppe 3 08.30 Montag 28.11. 09.00 Nervenzellen, Gliazellen, extrazelluläre Matrix Nervenzellen, Gliazellen, extrazelluläre Matrix Rezeptor Internalisierung, Labeln Rezeptor Internalisierung, Labeln Hippokampus 13.00 Rezeptor Internalisierung, Fluoreszenz Markieren Modulator Inkubation Modulator Inkubation Rezeptor Internalisierung, Fluoreszenz Markieren Pause 13.30 Pause 14.00 Ephys Demo 14.30 Ephys Demo 15.00 Ephys Demo Zellkultur DRGs, PC12 15.30 Ephys Demo Zellkultur DRGs, PC12 16.00 cLabs – virtuelle Rezeptoren 09.30 10.00 10.30 11.00 11.30 12.00 12.30 16.3017.30 Dienstag 29.11. Mittwoch 30.11. Donnerstag 01.12. Freitag 02.12. Hippokampus Motorik (Kleinhirn, Basalganglien, Rückenmark) Motorik (Kleinhirn, Basalganglien, Rückenmark) Mausperfusion Ionenkanäle Synaptologie Ionenkanäle Synaptologie Waschen der Schnitte konfokale Bilder DRG-Präparation, Tier-OP DRG-Präparation, Tier-OP Mausperfusion Waschen der Schnitte Auswertung Internalisierung DRG-Präparation, Tier-OP Mausperfusion 2. Antikörper auf Cerebellum und Hippo. Schnitte Abschlußbesprec hung Zellkultur DRGs Gewebe einbetten 2. Antikörper auf Cerebellum und Hippo. Schnitte Abschlußbesprec hung Pause Pause Pause Pause Pause Pause Zellkultur DRGs, PC12 Gewebe schneiden Waschen und Eindeckeln Zellkultur DRGs, PC12 Zellkultur DRGs, PC12 Gewebe schneiden Gewebe schneiden Waschen und Eindeckeln Waschen und Eindeckeln Zellkultur DRGs, PC12 Zellkultur DRGs, PC12 Blocken, Waschen und Eindeckeln FV1000, konfokale Mikroskopie Blocken, 1. Antikörper auf Cerebellum und Hippoc. Schnitte Blocken, 1. Antikörper auf Schnitte Blocken, 1. Antikörper auf Schnitte Blocken, 1. Antikörper auf Schnitte Blocken, 1. Antikörper auf Schnitte 24 FV1000, konfokale Mikroskopie FV1000, konfokale Mikroskopie FV1000, konfokale Mikroskopie Waschen der Schnitte Einführungs-Vorlesungen 28.11. bis 02.12.: Beginn Montag 28. Nov. 9.00 Uhr, HS MSZ, Versbacherstr.5, 97078 Würzburg Treffpunkt am 28.11.2016: 8:50 Uhr Haus E4, Versbacherstr. 5 Montag, 28. 11. 2016 9:00 Uhr Nervenzellen, Gliazellen, extrazelluläre Matrix, Prof. Sendtner Dienstag, 29. 11. 2016 8.30 Uhr Hippokampus, Dr. Blum Mittwoch, 30. 11. 2016 8.30 Uhr Motorik (Kleinhirn, Basalganglien, Rückenmark), Dr. Jablonka Donnerstag, 01. 12. 2016 8.30 Uhr Ionenkanäle, Prof. Villmann Freitag, 02. 12. 2016 8:30 Uhr Synaptologie, Dr. Götz Für den praktischen Teil werden die Studenten in drei Gruppen aufgeteilt (2x 7 und 1x 6 Studenten). 25 ZELLKULTUR TEIL Neuronale Zellen brauchen zum Überleben und zur Differenzierung Signale von neurotrophen Faktoren und extrazellulären Matrixproteinen (siehe Vorlesung Prof. Sendtner). Um das Überleben und das Wachstumsverhalten von primären Neuronen in Gegenwart bzw. Abwesenheit von neurotrophen Faktoren sowie Matrixproteinen zu untersuchen, werden primäre sensorische Neurone aus Hinterwurzelganglien (DRGs) von 8-9 Tage alten Hühnchenembryonen oder von 12-14 Tage alten Mausembryonen isoliert und unter den unten genannten Bedingungen kultiviert. I. Präparation von Maus-Hinterwurzelganglien (DRGs) I. Vorbereitung 1. Lösungen F14-Medium + 10% Horse Serum (HS): 1Dose F14 Pulver (Life Tech/INVITROGEN) in 900ml Wasser lösen, 10ml Penicillin/Streptomycin-Lsg. (1:100 verd., EK: 100mg/l Streptomycin Sulfat, 60,6mg/l Penicillin G) zugeben, mit 1M NaOH auf pH 7,3 einstellen (=> rote Farbe!), 1,97g NaHCO3 zufügen und auf 1l auffüllen; CO2 einleiten bis die Lösung lachsfarben ist, 10% HS zugeben, steril filtrieren Phosphate buffered saline; PBS 1% Trypsin (in Hanks balanced salt solution, HBSS; Life Tech/INVITROGEN) 2. Kulturschalen a) Am Vortag: Kulturschalen mit Poly-D,L-Ornithin (Sigma; 0,5mg PORN/ml 0,15M Boratpuffer pH 8,35) über Nacht bei 4°C beschichten b) Vor der Präparation: - 3x mit HBSS waschen - Beschichtung mit Laminin-111 Lösung (1:400 aus 1mg/ml-Maus-Laminin-Stammlösung in HBSS/HEPES verdünnen, EK: 2,5µg/ml) 3. Im Labor vorbereiten Eisbad, Präparierbesteck, 10cm-Petrischale zum Präparieren, 6cm-Petrischale mit PBS zum Sammeln und Versäubern, Pasteurpipette, Eppendorfgefäß mit 1ml PBS 26 II. Präparation - E13 Tage alte Mausembryonen werden aus den Muttertieren präpariert und in einer Petrischale gesammelt Köpfe der Embryonen abschneiden, Körper in Petrischale legen Zum Präparieren wird der Embryo auf den Bauch gelegt, die Haut entfernt und das Rückenmark freipräpariert. Dann werden die Hinterwurzelganglien (DRGs), die seitlich entlang des Muskels laufen, abgetrennt. DRGs in 3 cm Petrischale mit PBS sammeln Die Ganglien von überschüssigem Gewebe befreien und in 3 cm Petrischale mit frischem PBS überführen. III. Aufarbeitung in der Zellkultur (Gewinnen und Kultivieren der sensorischen Neurone) - - DRGs mit 1 ml Pipette aus der Petrischale aufsammeln, dabei leicht schwenken (damit nichts hängen bleibt) und in 15 ml Röhrchen sammeln. Falkon leicht schütteln (damit DRGs nach unten wandern) und Volumen mit Pipette auf ca. 1 ml reduzieren. 50 µl 1 % Trypsin dazugeben und leicht schwenken. 30 min bei 37°C im Brutschrank inkubieren. Überstand mit Pasteurpipette vorsichtig abnehmen bis auf ca. 300 ml. Ca. 10 mal mit 200 µl - Pipette triturieren (Auflösen des Zellverbands, Vereinzeln der sensorischen Neurone). 15 ml Röhrchen mit 9.5 ml Kulturmedium füllen. Zellsuspension auf NUNC-Petrischale (10 cm) zum Pre-Plating geben. 2 h bei 37°C im Brutschrank inkubieren. Petrischale vorsichtig 2 mal schwenken und Inhalt in 15 ml Röhrchen überführen. 8 min bei 400 g zentrifugieren. Absaugen bis auf 500 µl, resuspendieren Neubaur-Zählkammer mit 10 µl Zellsuspension befüllen und Zellen zählen (4 Eckquadrate auszählen; Mittelwert bilden; Mittelwert x 10 = Zellen pro 1 µl Zellsuspension) Auf PORN bzw. PORN und Laminin-111 beschichtete 24-Wells ausplattieren, dazu Laminin-111 absaugen und gleichzeitig 500 µl Kulturmedium mit bzw. ohne NGF (10 ng/ml Endkonzentration) zugeben. Errechnete Zellmenge an Zellsuspension in jede Vertiefung zugeben. IV. Kultur Kulturmedium: F14 + 10% HS, Inkubation bei 37°C und 5% CO2 Faktoren: NGF (Endkonz.: 10ng/ml) und eine Kontrolle ohne neurotrophen Faktor. Die Zellen werden auf Poly-Ornithin (PORN) oder PORN + Laminin-111 beschichteten Schalen ausplattiert. 27 II. In vitro Analyse des Proliferations- und Differenzierungspotentials embryonaler neuraler Stammzellen der Maus. Das Nervensystem von Säugetieren entsteht aus dem Neuroektoderm, das in Neuralrohr und Neuralleiste strukturiert wird. Aus diesen Strukturen entstehen sowohl Nervenzellen als auch Stützzellen (Glia). Neurale Stammzellen können sowohl in Nervenzellen als auch Glia differenzieren, im Gegensatz zu späteren neuronalen Stammzellen, deren Differenzierungspotential auf Nervenzellen beschränkt ist. Frühe neurale Stammzellen bilden das Neuroepithel; sie proliferieren durch symmetrische Zellteilungen. Unter bestimmten Stimuli können sie alternativ durch asymmetrische Zellteilung sich selbst erneuern, wobei die zweite Tochterzelle in ein postmitotisches Neuron differenziert. Im Praktikumsteil sollen Zellkulturtechniken für neurale Stammzellen erlernt werden, um die Signale für Mitose und Differenzierung untersuchen zu können. Dazu generieren Sie adhärente Kulturen neuraler Stammzellen, die aus Mäuseembryonen gewonnen wurden, behandeln sie mit Wachstumsfaktoren (EGF und bFGF) und analysieren die Zellproliferation. In einem zweiten Versuchsansatz untersuchen Sie die Differenzierung neuraler Stammzellen zu Neuronen. Kultur embryonaler neuraler Stammzellen der Maus. Neurale Stammzellen können entweder als Neurosphären in serumfreiem Neurobasal-Medium mit dem Supplement B27 und den beiden Wachstumsfaktoren EGF (20 ng/ml) und Fibroblastenwachstumsfaktor-2 (FGF-2 oder bFGF, 10 ng/ml) kultiviert werden. Alternativ wachsen sie adherent auf Zellkulturplastik, wenn zusätzlich Heparin (5µg/ml) zum Medium zugegeben wird. Ziel 1: Nachweis der neuronalen Differenzierung und des Zellüberlebens unter differenzierenden Bedingungen. Dazu werden 10.000 Zellen auf beschichteten Glasplättchen in 4-well Zellkulturschalen (Nunc #14444) ausgesät. Dies ermöglicht die Lebendbeobachtung ebenso wie Immunfärbungen (zum Nachweis z. B. der Apoptose, etc.) nach der Fixierung der Zellen. Nach 24 h Inkubation werden die Schalen mikroskopiert und Photos gemacht. Dann werden die adhärenten Zellen einmal mit PBS gewaschen und mit 4% PFA in PBS fixiert. Ziel 2: Nachweis des EGF und bFGF Effekts auf die Proliferation. Dazu werden 10.000 Zellen auf beschichteten Glasplättchen in 4-well Zellkulturschalen (Nunc #14444) ausgesät. 2 Stunden später erfolgt die Zugabe der Wachstumsfaktoren. Zum Nachweis der Proliferation wird der Zellproliferationsmarkers Bromodeoxyuridine (BrdU) zugegeben. Nach 24 h Inkubation werden die 28 Schalen mikroskopiert und Photos gemacht. Dann werden die adhärenten Zellen einmal mit PBS gewaschen und mit 4% PFA in PBS fixiert. Well 1 Well 2 Well 3 Well 4 kein Faktor EGF (Endkonzentration 20ng/ml) bFGF (Endkonzentration 10ng/ml) EGF plus bFGF Durchführung: Als erstes werden die 10mm Gläschen, die bereits am Vortag mit Poly-D,L-Ornithin beschichtet wurden, mit Laminin beschichtet (siehe DRG Versuch). Die Wachstumsmedien für Differenzierung und Proliferation werden angesetzt. Jede Gruppe befüllt eine 4 Well-Platte für den Proliferationsansatz und eine weitere Platte für die Differenzierung. Die neuralen Stammzellen sind auf 3-cm Schalen der Firma Falcon kultiviert. Es wird in einer Sterilwerkbank gearbeitet und wie folgt verfahren: - Medium absaugen - Vorsichtig mit 2.5ml PBS waschen - 1ml PBS zugeben - 40µl 1% Trypsin zugeben - Schale vorsichtig schwenken und 2 min im Brutschrank inkubieren - Im Mikroskop die Ablösung der Zellen von der Schale prüfen - 40µl 1% Trypsininhibitor und 500µl Neurobasal/B27 zugeben - Zellen durch „Triturieren“ mit einer blauen Spitze/Pipette dissoziieren - In ein 15ml Falconröhrchen überführen - Zentrifugation 1.400rpm, 4min, RT - Überstand absaugen (verwerfen) - Zum Zellpellet 500µl Neurobasal/B27 zugeben und lösen (5-mal triturieren) - Erneute Zentrifugation 1.400rpm, 4min, RT - Überstand absaugen (verwerfen) - Zum Zellpellet 500µl Neurobasal/B27 zugeben und lösen (10-mal triturieren) - Zellzahl bestimmen (Neubauer Zählkammer) - Ggf. Photo davon machen - Berechnen der benötigten Zellmenge (µl) pro well - Mischen von Medium mit den Zellen (=>Zellsuspension) - Aussäen von 500µl Zellsuspensiopro Well, dazu wird vorher die Laminin-Lösung abgesaugt. - Ggf. Zugabe der Faktoren gemäß Schema - Ggf. Zugabe des Zellproliferationsmarkers Bromodeoxyuridine (BrdU, Endkonzentration von BrdU im Medium 10μM) Kulturmedium: Neurobasal Medium, Gibco 21103 29 2% B27, Gibco #17504-044 100 U/ml Penicillin 10 μg/ml Streptomycin 1% Glutamax 1% MEM Non-essentaial amino acids, Gibco 11140 Wachstumsfaktoren (Stammlösungen): 20 ug/ml EGF 10 ug/ml FGF-2 Turnover von Rezeptorproteinen und Basics der Elektrophysiologie Nach Translation im Cytoplasma werden Rezeptorproteine über die Kompartimente ER, ER-Golgi intermediäres Kompartiment, cis-, trans- Golgi zur Plasmamembran transportiert. Ihre Degradation erfolgt nach Endozytose über den endosomalen/lysosomalen Abbau oder nach Ubiquitinierung über das Proteasom. Außer Markierung durch Ubiquitin kann intrazelluläre Phosphorylierung des Ionenkanalproteins, eine posttranslationale Modifikation, ein Signal für eine Internalisierung des Proteins sein. Diese lässt sich im Zellkulturmodell durch die Zugabe von Aktivatoren bestimmter Proteinkinasen untersuchen. Die Untersuchung von Rezeptor Turnover in der Plasmamembran ist nicht nur ein wichtiges Kriterium zur Aufklärung der Pathomechanismen bei Hyperekplexie, wo im Patienten identifizierte rezessive Mutationen mit einer gestörten Biogenese einhergehen, sondern ist auch bei Autoimmunerkrankungen von Bedeutung. Eine verstärkte Internalisierung von Rezeptorproteinen ist bei Myasthenia gravis (nAChR) oder Panencephalitis (NMDAR) beobachtet worden. Inhibitorische Glycinrezeptoren besitzen in intrazellulären Domänen zahlreiche Erkennungssequenzen für Proteinkinasen. Bislang konnte eine Phosphorylierung nur für die Proteinkinase C (PKC) gezeigt werden. Stimuliert man Zellen mit PMA (Phorbol-12-myristat-13-acetat), einem hochaffinen Modulator der PKC, wird der Glycinrezeptor nach Aktivierung der PKC phosphoryliert und verstärkt internalisiert. Diese Internalisierung hat eine Verringerung der Zelloberflächenexpression zur Folge und führt daher zu einer verminderten inhibitorischen Neurotransmission. Ziel des Versuches ist es, die verstärkte Internalisierung nach Zugabe des positiven Modulators PMA zu verfolgen. 30 Zur Untersuchung der Internalisierungsraten von Glycinrezeptoren werden kultivierte HEK293 (humane embryonale kidney) Zellen mit der entsprechenden Plasmid-DNA, die für den humanen Glycinrezeptor 1 kodiert, 24h vor Versuchsbeginn transfiziert. Die Kontrolle der Transfektionseffizienz wird mit HEK293 Zellen, die parallel mit GFP (green fluorescent protein) transfiziert wurden, überprüft. I. Versuchsvorbereitung - II. HEK293 Zellen werden auf 3 cm Kulturschalen mit 4 Deckgläschen mit einer Dichte von 180.000 Zellen pro Schale ausgesät nach 24h werden die Zellen nach der Calciumphosphatpräzipitationsmethode (Chen and Okayama 1987) transfiziert nach 18h werden die Zellen mit Vollmedium (MEM Medium + Zusätze FCS, L-Glu, Pen/Strep) gewaschen nach wieder 24h wird der Internalisierungsassay durchgeführt Versuchsdurchführung - - III. Zellen auf eine mit Parafilm beschichtete feuchte Kammer überführen mit Erstantikörper (mab2b, 1:500 in Vollmedium verdünnt, pro Deckgläschen 50 µl) auf Eis 30 min inkubieren vorsichtiges Waschen mit Extrazellulär Puffer (ECS physiologischer Puffer der für elektrophysiologische Messungen verwendet wird), d.h. vorsichtiges Eintauchen, so werden überschüssige Antikörper-Reste entfernt jetzt Inkubation mit erstem secondary Antikörper durchführen, wieder 30 min auf Eis (goat-anti-mouse Cy3, 1:500 in Vollmedium verdünnen), OHNE LICHTEXPOSITION!! Zellen wieder vorsichtig 3x waschen mit ECS-Puffer Modulator in Vollmedium verdünnt zugeben (200 nM PMA) jetzt Zellen für 20 min und 40 min bei 37ºC inkubieren (Zellkulturschrank) INTERNALISIERUNG bei 37ºC! Zellen wieder 3x waschen (ECS-Puffer) mit zweiten secondary Antikörper inkubieren (donkey-anti-goat-DyLight 488; 1:500 in Vollmedium) für 30 min auf Eis IM DUNKELN!! Zellen 3x vorsichtig in PBS waschen Zellen mit 4% PAFA 4%Sucrose PBS für 5 min Raumtemperatur fixieren Zellen 2x mit PBS waschen, 1x mit VE Wasser Zellen mit Aqua-mount bzw. Mowiol einbetten und im Kühlraum unter Ausschluss von Licht trocknen lassen Versuchsauswertung - jede Gruppe wertet mindestens 10 Zellen pro Zeitpunkt (0 min, 20 min, 40 min) nach Aufnahme am konfokalen Mikroskop aus 31 (+) Modulator Klon transfiziert GlyRa1 wt Zelle # 0 min PMA (-) Modulator 0 min ohne 20 min PMA 40 min PMA Modulator 20 min ohne Modulator 40 min ohne Modulator 1 2 3 4 5 6 7 8 9 10 Mittelwert SD - anschließend wird anhand der Tabelle die Auswertung mit einem Balkendiagramm graphisch dargestellt (Vergleich PMA und unbehandelt) IV. Ergänzende Protokolle und Material Transfektion mit HBS-Puffer: OPTIONAL - 0.1xTE bei 37ªC warm stellen folgende Lösungen zusammen pipettieren, Reihenfolge beachten: (fett-gedruckte Zahlen gelten für 3 cm Schalen) 10 µl /2 µl DNA (aus 1 µg/µl stock) für 10cm/3cm Schale 10 µl /1 µl GFP-DNA (aus 1 µg/µl stock) für 10cm/3cm Schale 430 µl /87 µl 0.1x TE -Puffer 50 µl /10µl CaCl2 (2.5 M) Endkonzentration 125mM gut mischen ! 500 µl/100µl 2x HBS (tropfenweise zugeben Schütteln und abzentrifugieren und 20 min bei RT (oder schnelle Methode 1 min bei 37 ªC) inkubieren (bei Falcon tubes 2 min) Mischung tropfenweise zu den Zellen geben und Präzipitatbildung im Mikroskop überprüfen Schalen über Nacht in 5 % CO2-Brutschrank inkubieren, 37ºC. Zellen nach ca. 24h 2x mit Vollmedium waschen. 32 2x HBS Puffer: 50 mM HEPES (1.19 g) 12 mM Dextrose (Glucose) (0.237 g) 10 mM KCl (0.075 g) 280 mM NaCl (1.63 g) 1.5 mM Na2HPO4 x 2H2O (0.0267 g) mit H2O auf 100 ml auffüllen, pH 6.95 WICHTIG mit NaOH Elektrophysiologische Messungen Die physiologischen Eigenschaften von Ionenkanälen lassen sich mit Hilfe elektrophysiologischer Ableitungen beschreiben. Wie bereits erwähnt, können Mutationen im Glycinrezeptor zu einer verminderten Zelloberflächenexpression führen. Dies kann mit einer reduzierten Kanalleitfähigkeit einhergehen, ebenso können aber auch die Kanaleigenschaften wie die Desensitisierung (Kanal schließt in Anwesenheit des Agonisten/Liganden) des Ionenkanals verändert sein. Diese Veränderungen werden am elektrophysiologischen Setup mit Hilfe der Patch Clamp Technik demonstriert. Dazu werden HEK293 Zellen 24h vor Messbeginn mit Plasmid-DNA, die für den humanen Glycinrezeptor 1 Wildtyp sowie den Punktmutanten P250T und S231R transfiziert (P250T führt zu einer schnelleren Desensitisierung, S231R zu einer deutlich reduzierten Maximalstromantwort). Anschließend sollen verschiedene Ableitsituationen virtuell mit Hilfe des Computer-Programms cLabsNeuron untersucht werden. Zunächst werden Simulationen zu den Basisfunktionen neuronaler Membraneigenschaften mit ihren elektrischen Equivalenten wiederholt. Im Ionenkanal-Modul werden die ‘gating’ Mechanismen sowie die pharmakologischen Eigenschaften spannungsgesteuerter Na+- und K+ -Kanäle verdeutlicht. Die virtuelle Membran wird de-/repolarisiert und der Einfluß auf den Ionenstrom beobachtet. 33 IMMUNHISTOCHEMISCHER TEIL Die Antikörperfärbungen an hippokampalen und cerebellären Gewebeschnitten von jungen und adulten Mäusen, veranschaulichen den Aufbau und die Komplexität dieser Hirnregionen (siehe Vorlesung Prof. Sendtner, Dr. Jablonka, Dr. Blum). Es sollen anhand von Antikörperfärbungen die unterschiedlichen neuronalen Schichten und Zelltypen in der Kleinhirnrinde einer adulten und einer postnatalen Maus (Tag 5-8) untersucht und dokumentiert werden, um die Entwicklung des Cerebellums deutlich zu machen. Außerdem werden Schnitte des Hippokampus und Rückenmarks einer adulten Maus angefertigt und mit konfokaler Mikroskopie ausgewertet. Für die mikroskopische Untersuchung der Zellen in einem Gewebe wird das Gewebe zunächst präpariert, fixiert, eingebettet und geschnitten (siehe: Herstellung von Vibratom-Schnitten). Die meisten Gewebe bestehen aus einer Vielzahl unterschiedlicher Zelltypen, und die Immunhistochemie macht es möglich, einzelne Zelltypen im Gewebe bzw. auch von Strukturen innerhalb der Zellen darzustellen. Dieser Vorgang wird hier am Beispiel des Cerebellums beschrieben. Purkinjezellen und Interneurone des Cerebellums sollen mit Antikörpern gegen Parvalbumin identifiziert werden. Die Axone der Korbzellen, die Afferenten der Moosfasern und Kletterfasern sowie die Efferenten der Purkinje-Zellen sollen mit Anti-Phospho-Neurofilament detektiert werden. Herstellung von „free floating sections„ mit dem Vibratom Mäuse werden mit 4% Paraformaldehyd in Phosphatpuffer (PFA) perfundiert und das Gehirn wird freipräpariert. Nach einer kurzen Postfixation wird das Gewebe in Agarose eingebettet und mit einem Vibratom in 50-80 µm dicke Scheiben geschnitten. Chemische Fixierung: Das Gewebe wird in Paraformaldehyd (4 % in der Pufferlösung PBS, pH 7.4, PFA) eingelegt. Durch Quervernetzung von Proteinen bleibt die Gewebsstruktur erhalten, Enzyme werden inaktiviert, das Gewebe wird härter und kann gelagert werden. Einbetten: Fixiertes Gewebe wird in 6%-iger Agarose eingegossen. Beim Abkühlen des Polymers entsteht ein hartes Präparat, das bei Raumtemperatur geschnitten werden kann. Trimmen: Das Präparat wird auf einem Probenhalter befestigt und mit einem Skalpell oder einer Rasierklinge vorgeschnitten, so dass die interessante Gewebeseite exponiert wird (siehe Vorlesung). Schneiden: Der getrimmte Gewebeblock wird entsprechend dem Klingenverlauf des Vibratoms auf einem Probenhalter mit Sekundenkleber festgeklebt. Der Probenhalter wird im Vibratom befestigt. Die vibrierende Rasierklinge wird in der Wanne (gefüllt mit PBS) an der Schnittfläche entlanggeführt. Die Schnitte werden mit einem Pinsel abgefischt und in einer 24-well Platte, gefüllt mit PBS pH 7.4, gesammelt. Die Dicke der Schnitte wird durch den Vorschub des Probenhalters reguliert. 34 Indirekte Fluoreszenzfärbung von bestimmten Proteinen und Antigenen mit Antikörpern Zellen werden zunächst mit einem Detergenz (z.B. Triton X100, Tween 20) während des Blockings permeabilisiert, um den Antikörpern den Zugang zum Zytoplasma zu ermöglichen. Dann werden die Erstantikörper auf den Schnitt gegeben. Dabei ist wichtig, dass die beiden Antikörper in Tieren unterschiedlicher Gattungen produziert worden sind, z.B anti-Parvalbumin im Kaninchen (polyklonal) und anti-SMI-31 (monoklonal) in der Maus. Nach einem Waschgang bleiben nur dort Antikörper zurück, wo sie an ihr jeweiliges Antigen gebunden sind - also die einen an den Purkinje-Zellen und Interneuronen, die anderen an den Axonen. Nun werden die Zweitantikörper zugegeben, die gegen Antikörper der Tiere gerichtet sind, von denen die Erstantikörper stammen. Die anti-KaninchenZweitantikörper sind mit einem roten Fluorochrom konjugiert (z.B. Cy3, Dylight 549, Alexa 549), die antiMaus-Zweitantikörper tragen ein grünes Fluorochrom (Alexa 488, Dylight 488). Diese Sekundärantikörper werden fast immer durch Immunisierungen von Ziegen (goat) oder Esel (donkey) mit IgG-Fraktionen der Erstantikörperspezies induziert und aus deren Serum gereinigt. Nach Abwaschen der nicht-gebundenen Antikörper kann nun mit dem Fluoreszenzmikroskop oder einem konfokalen Laserscanning-Mikroskop die Verteilung der Immunfärbung im Gewebeschnitt untersucht werden. Dabei muss das optische System so eingerichtet sein, dass Anregungs- und Emissionslicht der beiden Fluorochrome gut voneinander getrennt sind. Nur dann ist eine getrennte Darstellung der beiden Signale möglich. Blockierung: Mit PBS + BSA 10 % + Triton X-100 0,1 % werden unspezifische Bindungsstellen im Gewebe abgeblockt und Fette + Eiweiße aus Zellmembranen herausgelöst. Dadurch wird das Gewebe eingängiger für den Antikörper und somit eine bessere Färbung erzielt. 45 minbis 1 h bei RT sollten bei dieser Schnittdicke ausreichen. In der gesamten Prozedur kann BSA auch durch Serum ersetzt werden. Hier wird bevorzugt Serum verwendet, welches der Spezies der Sekundärantikörper entspricht. 1. Antikörper: Der Erstantikörper, welcher spezifische Proteine erkennt, wird in PBS + BSA + Triton X100 verdünnt und 4 h bei RT oder über Nacht bei 4° C mit dem Gewebe inkubiert. Nach der Inkubationszeit wird 3-4x 10 min mit PBS gewaschen, um den überschüssigen, nicht gebundenen Antikörper zu entfernen. Achtung: ungebundener Antikörperüberschuß führt zu hohem Background. 2. Antikörper: der unspezifische Zweitantikörper, welcher den Erstantikörper erkennt und an diesen bindet, ist mit einem Fluoreszenzfarbstoff gekoppelt. Dieser wird ebenso in PBS + BSA + Triton X-100 verdünnt, zupipettiert und für 1 1/2 h bei RT inkubiert. Anschließend wird wieder 3x mit PBS gewaschen und das Gewebe auf ein Objektträger gezogen. Fluorezenzgefärbte Schnitte werden in einem Einbettmedium (hier Aquafluomount) eingedeckelt und mit Nagellack umrandet. Die Färbungen können im Dunkeln bei 4 ° C gelagert werden. Warum welcher Puffer: Phosphat oder Tris-Puffer um einen für Antikörper-Antigen günstigen pH-Wert zu erhalten. BSA oder Serum zum Blockieren unspezifischer Interaktionen. 35 Tween 20, Triton X-100 oder andere Detergenzien um die Diffusion zu verbessern, unerwünschte unspezifische, insbesondere hydrophobe Bindungen abzuschwächen, und um das Eindringen der Antikörper in die Zellen zu erleichtern. Um ein rasches Ausbleichen der Fluorochrome durch freie Radikale zu vermindern, werden „anti-fade„ oder „anti-bleaching„ Reagentien im Einbettmedium eingesetzt. Das Einbettmedium muss in seinem Brechungsindex an den der Deckgläser angepasst sein. Fluorophore Absorptionsmax. (nm) Emissionsmax. (nm) Cyanine, Cy2 492 510 Fluorescein, FITC 492 520 Alexa 488 / Dylight 488 495 510 Indocarbocyanine, Cy3 550 570 Alexa 549 / Dylight 549 550 570 Aminomethylcoumarin, AMCA 350 450 Texas Red, TR 596 620 Indodicarbocyanine, Cy5 650 670 36 Calbindin is a calcium-binding protein belonging to the troponin C superfamily. Calbindin immunoreactivity was detected by immunohistochemistry in the kidney, pancreatic islets, and brain. Two different proteins presenting calbindin immunoreactivity, one of molecular mass 28 kD and the other of 29 kD, were identified in the central nervous system. Both molecular species are present in the brain of all vertebrates except fish. Parvalbumin, a high affinity calcium-ion binding protein, is expressed in high levels only in fastcontracting muscles and at lower levels in brain and several endocrine tissues. In the hippocampus it is an excellent marker for interneurons, the so called PV+ fast spiking basket cell and it labels dendrites, the soma and the axonal projections. SMI 31 stains phosphorylated neurofilament. It reacts broadly with thick and thin axons and some dendrites, but not Purkinje cell dendrites! Nerve cell bodies and other cells and tissues are unreactive except for peripheral axons. NF: Cytoplasmic intermediate filaments (IF) can be divided into 5 subclasses based on their biochemical properties, immunologic specificity and tissue distribution: keratin, filaments in epithelial cells, vimentin filaments in cells of mesenchymal origin, desmin in muscle cells, glial filaments in astrocytes, and neurofilaments in neurons. The different types of intermediate filament proteins share common structural features. Neurofilaments are composed of 3 neuron-specific proteins with apparent molecular weights of 68,000 (called NF-L for light), 125,000 (NF-M for medium), and 200,000 (NF-H for heavy) on SDS-gel electrophoresis. The different sequence data show that the intermediate filament proteins contain a similar alpha-helical domain of conserved length capable of forming coiled-coils. GFAP: Glial fibrillary acidic protein is an intermediate-filament (IF) protein that is highly specific for cells of astroglial lineage. The predicted amino acid sequence indicated that GFAP shares structural similarities with other IF proteins found in nonepithelial cell types. Considerable sequence divergence in the amino-terminal region of GFAP suggested that the tissue-specific functions of this IF protein may be mediated through this region of the molecule. GFAP is a useful marker of astroglia, but is not a general marker for astroglia in the CNS. NeuN reacts with most neuronal cell types including granule cells of the cerebellum and the hippocampus but not with precursors in proliferative zones. Staining is strongest in nuclei. No staining of Purkinje cells! Doublecortin is a marker of immature neurons. In the adult, it is preferentially expressed in neurogenic niches of the lateral ventricle or the subgranular zone of the hippocampus (hilus). MAP-2 (Microtubule associated protein 2) serves as a marker for neuronal dendrites and somata. 37 1st antibody Cerebellum Maus Monoclonal Polyclonal adult Parvalbumin 1:1000 Neurofilament 1:200 P8-10 Parvalbumin 1:1000 Neurofilament 1:200 adult Neu N 1:400 Calbindin 1:1000 P8-10 Neu N 1:400 Calbindin 1:1000 adult Calbindin 1:1000 GFAP 1:50 P8-10 Calbindin 1:1000 GFAP 1:50 adult Neu N 1:400 Doublecortin 1:400 adult Neu N 1:400 Parvalbumin adult Neu N 1:400 Neurofilament 1.200 adult Neu N 1:400 GFAP 1/10 (1/200) Hippocampus 1:1000 Spinal Cord 2nd antibody Anti-mouse: Donkey-anti-mouse IgG Dylight 549 1:600 Anti-rabbit: Donkey anti-rabbit IgG Dylight 488 1:600 38 Immunohistochemistry of the vibratome sections • After vibratome sectioning, slices are stored in 1x PBS, pH 7.4 • blocking: PBS / horse serum 10% / Triton X-100 0,3 % / 0.1 % Tween 20 -> 45 min. / RT / shaker (alternative: BSA 10%) • 1st antibody: PBS / 10% horse serum / 0,1 % Triton X-100 / 0,1% Tween 20 -> overnight / +4°C / shaker • washing: PBS, 0.1 % Triton X-100, 0,1 % Tween 20 -> 3 x 10-15 min / RT / shaker • 2nd antibody: PBS / 10% horse serum / 0,1 % Triton X-100 / 0,1% Tween 20 -> 60 - 90 min. / RT / shaker / dark • washing: 1x PBS, 0.1 % Triton X-100, 0,1 % Tween 20 -> 3 x 15 min. / RT / shaker / dark (DAPI during last washing step in PBS (2mg/ml Stock solution, 1/5000, 5 min) • washing: 1x PBS, 1 x 5 min. / RT / shaker / dark • mounting: Aqua-Fluomount -> +4°C 39 Struktur und Klassifizierung von Antikörpern Antikörper werden als Antwort auf die Präsenz fremder Moleküle produziert. Vor allem werden sie von Plasmazellen produziert und zirkulieren durch Blut und Lymphe. Antigen-Antikörper Komplexe werden durch Phagozytose durch Makrophagen entfernt. Antikörper bilden eine große Familie von Glykoproteinen, mit gemeinsamen strukturellen und funktionellen Eigenschaften: Funktionell werden sie durch ihre Eigenschaft definiert, gleichzeitig Antigene und spezialisierte Zellen oder Proteine des Immunsystems zu binden. Strukturell gesehen, bestehen sie aus einer oder mehr Kopien einer Yförmigen Einheit, welche aus 4 Polypeptiden besteht: 2 „light chain„ und 2 „heavy chain„ Molekülen. Es gibt 5 Klassen: IgG, IgM, IgA, IgE und IgD unterschieden durch die Zahl der Untereinheiten und des Typs des „heavy chain„ Polypeptids: IgG IgM IgA IgE IgD Heavy Chain Light Chain oder oder oder oder oder Struktur Valenz 2 10 2, 4 oder 6 2 2 Konzentration im Serum 8-16 mg/ml 0,5-2 mg/ml 1-4 mg/ml 10-400 ng/ml 0-0,4 mg/ml Funktion Sekundäre Immunantwort Primäre Immunantwort Schutz der Schleimhäute Schutz gegen Parasiten ? Der IgG-Typ ist am häufigsten (siehe Tabelle) und soll daher näher beschrieben werden: IgG Moleküle besitzen 3 Protein-Domänen. 2 davon sind identisch und bilden die Arme des Ys. Jeder dieser Arme 40 enthält eine Antigen-Bindungsstelle. Die 3 Domänen können durch Proteasen-Verdau mit Papain getrennt werden. Die beiden Antigen-bindenden Domänen heißen auch Fab Fragmente (fragment having the antigen binding site) während die Domäne an der Basis in die Immun-Regulation involviert ist als Fc-Domäne bekannt ist (fragment that crystallizes). Die heavy chains haben ein Molekulargewicht von etwa 55.000 Dalton, die light chains ca. 25.000 Dalton. Die IgG-Moleküle werden nach ihrere Sequenz wiederum in verschiedene Unterklassen geteilt. Bei der Maus z.B. in IgG1, IgG2a, IgG2b und IgG3. Die Region eines Antigens, welches durch einen Antikörper gebunden wird, ist ein „Epitop„. Diese Epitope sind Oberflächenstrukturen aus direkt benachbarten Aminosäuren (mindestens 6) oder aus getrennten Sequenzen, die nur im gefalteten Polypeptid beisammen liegen. Die Antigen-Antikörper Interaktion ist nicht-kovalent und reversibel. Die Affinität ist ein Maß für die Stärke der Interaktion und beschreibt die Menge an Antikörper-Antigen Komplexen im Equilibrium. Entscheidend für dieses Equilibrium ist die Diffusionsrate (abhängig von Gewebe, Dicke und Einbettung) und die Affinität (abhängig vom Antikörper). 41 Herstellung von Antikörpern: Als Antigene werden entweder gereinigte Proteine oder synthetisch hergestellte Peptide verwendet. Polyklonale Antikörper: Das Antigen wird in ein geeignetes Tier injiziert (Kaninchen, Maus, Ratte, Ziege, Hamster, Meerschweinchen, Huhn). Durch wiederholte Injektionen („boost“) wird die Immunreaktion verstärkt. Aus dem entnommenen Blut wird Serum gewonnen. Dieses Serum oder daraus gereinigte Antikörper werden verwendet (Vor allem IgGs). Bis zu 1mg/ml (=10% der IgGs) Antigen-spezifische Antikörper sind möglich. Monoklonale Antikörper: Aus immunisierten Mäusen werden Antikörper-sekretierende Zellen mit Myelomzellen fusioniert. Die entstehenden Hybridomyzellen werden als einzelne Klone gezüchtet und die Qualität und Spezifität der monoklonalen Antikörper getestet. Vorteile: Spezifisch, homogen und unbegrenzte Produktions-Menge. Nachteil: Aufwendige Herstellung der Hybridomazelllinien. 42