Anorganische Chemie I 1. OÜ PD Dr. A. Mezzetti Fragenkatalog VI
Werbung

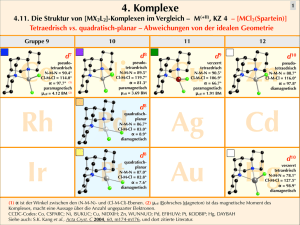
Anorganische Chemie I PD Dr. A. Mezzetti 1. OÜ Fragenkatalog VI Abgabetermin: 4.11.2008 1. Aufgabe Triphenylphosphin reagiert mit NiBr2·3H2O in siedendem Butanol unter Bildung eines dunkelgrünen, paramagnetischen Komplexes A (µeff=2.97 BM). Komplex A ist neutral und enthält Ni, Br und PPh3. Die Elementaranalyse lautet: 58.25 % C, 4.2 % H, 21.60 Br. Der analoge Komplex B mit P(CH3)3 ist dunkelrot und diamagnetisch. – Empirische Formel von A? (1 Punkt) – Oxidationszahl, Elektronenkonfiguration und gesamte Elektronenzahl in A und B? (1 Punkt) – Diskutieren Sie die Struktur von A und B anhand des VB-Modells! (1 Punkt) – Diskutieren Sie die Struktur von A und B anhand des KFT-Modells! (1 Punkt) – Vergleichen Sie die Eigenschaften von A und B und erklären Sie die Unterschiede! (1 Punkt) 2. Aufgabe [Fe(CO)5] (C), ein diamagnetischer Komplex, reagiert mit OH– unter Bildung von [Fe(CO)4]2– (D). – Oxidationszahl, Elektronenkonfiguration und gesamte Elektronenzahl in C und D? (2 Punkte) – Diskutieren Sie die Struktur von C und D anhand des VB-Modells! (2 Punkte) – Diskutieren Sie die Struktur von D anhand des KFT-Modells! Ist dieser Ansatz in diesem Fall nützlich? (1 Punkt) 3. Aufgabe Disproportionierung von Co(II) zu Co(I) und Co(III) wird durch bestimmte P(OR)3-Liganden ausgelöst: 2 Co2+ + 11 P(OR)3 → [Co(P(OR3))5]+ (E) + [Co(P(OR3))6]3+ (F) Komplex E ist trigonal-bipyramidal. E und F sind beide diamagnetisch. – Oxidationszahl, Elektronenkonfiguration und gesamte Elektronenzahl in E und F? (1 Punkt) – Diskutieren Sie die Struktur von E und F anhand des VB-Modells! (1 Punkt) – Diskutieren Sie die Struktur von F anhand des MO-LCAO-Modells (nur σ-Bindung)! (1 Punkt) – Anhand der KFT entwerfen Sie ein qualitatives Aufspaltungsmuster für die Energien der dOrbitale. Wieso ist E diamagnetisch? (2 Punkte) 1. Aufgabe Triphenylphosphin reagiert mit NiBr2·3H2O in siedendem Butanol unter Bildung eines dunkelgrünen, paramagnetischen Komplexes A (µeff=2.97 BM). Komplex A ist neutral und enthält Ni, Br und PPh3. Die Elementaranalyse lautet: 58.25 % C, 4.2 % H, 21.60 Br. Der analoge Komplex B mit P(CH3)3 ist dunkelrot und diamagnetisch. – Empirische Formel von A? (1 Punkt) – Oxidationszahl, Elektronenkonfiguration und gesamte Elektronenzahl in A und B? (1 Punkt) – Diskutieren Sie die Struktur von A und B anhand des VB-Modells! (1 Punkt) – Diskutieren Sie die Struktur von A und B anhand des KFT-Modells! (1 Punkt) – Vergleichen Sie die Eigenschaften von A und B und erklären Sie die Unterschiede! (1 Punkt) – Empirische Formel von A aus der Elementaranalyse (1 Punkt): 100 g Komplex enthalten: m(X) n(X) n(X)/n(Br) 58.25 g C 4.850 mol C 17.9 4.2 g H 4.17 mol H 15.4 21.60 g Br 0.2703 mol Br 1 Das Molverhältnis zeigt, dass 1 Mol Br auf ein Mol PPh3 entfällt. Somit ist die Summenformel [NiBr2(PPh3)2], weil der neutrale Komplex 2 Bromliganden enthalten muss. Die prozentuale Zusammensetzung ist C, 58.19 %, H, 4.07 %, Br, 21.51. – Oxidationszahl, Elektronenkonfiguration und gesamte Elektronenzahl in A und B? (1 Punkt) Ni(II) → d8 – 16 Elektronen für beide Komplexe Diskutieren Sie die Struktur von A und B anhand des VB-Modells! (1 Punkt) 4L high-spin d8 Komplex A: d low-spin d8 s px py pz 4L Komplex B: d – sp3, tetraedrisch s px py pz dsp2, quadratisch planar Diskutieren Sie die Struktur von A und B anhand des KFT-Modells! (1 Punkt) Vierfach-koordinierte Komplexe können entweder tetraedrisch oder planar-quadratisch sein: [NiBr2(PPh3)2] und [NiBr2(PMe3)2] haben beide die d8-Elektronenkonfiguration aber unterschiedliche Eigenschaften. Das qualitative Aufspaltungsdiagramm zeigt, dass tetraedrische Komplexe Licht mit grösseren Wellenlängen absorbieren als planar-quadratische Komplexe. Der grüne Komplex [NiBr2(PPh3)2] absorbiert rotes Licht (niedrigere Energie), die rote Farbe von [NiBr2(PMe3)2] stammt aus der Absorption im grünen Bereich (höhere Energie). Somit könnte [NiBr2(PPh3)2] tetraedrisch sein, [NiBr2(PMe3)3] planar-quadratisch. Die magnetischen Eigenschaften der beiden Komplexe erhärten diese Hypothese (siehe Schema). 2. Aufgabe [Fe(CO)5] (C), ein diamagnetischer Komplex, reagiert mit OH– unter Bildung von [Fe(CO)4]2– (D). [Fe(CO)5] (C) !CO 2 OH – – # !!!" [Fe(COOH)(CO)4] """" [FeH(CO)4]– 2– OH – !!!! " [Fe(CO)4] –H 2O (D) – Oxidationszahl, Elektronenkonfiguration und gesamte Elektronenzahl in C und D? (2 Punkte): Komplex C: Fe(0) d8 18 Elektronen Komplex D: Fe(–2) d10 18 Elektronen – Diskutieren Sie die Struktur von C und D anhand des VB-Modells! (2 Punkte) CO ist ein stark-Feld-Ligand. Deshalb erwarten wir low-spin-Komplexe. Somit bleibt in der d8-Elektronenkonfiguration ein d-Orbital unbesetzt: 5L low-spin d8 Komplex C: dsp3 d s px py pz 4L s px py pz d10 Komplex D: d sp3, tetraedrisch Das VB-Modell sagt nichts darüber aus, ob Komplex C quadratisch-pyramidal oder trigonalbipyramidal ist. Wir werden in einer späteren Übung sehen, dass π-Akzeptor-Liganden die trigonale-bipyramidale Struktur stabilisieren. Wegen seiner d10- Elektronenkonfiguration kann Komplex D nur tetraedrisch sein. – Diskutieren Sie die Struktur von D anhand des KFT-Modells! Ist dieser Ansatz in diesem Fall nützlich? (1 Punkt) Das VB-Modell besagt, dass Komplex D als d10-System tetraedrisch und diamagnetisch ist (siehe oben). Hingegen ist der KFT-Ansatz für solche Komplexe nicht hilfreich, da die gesamte LFSE = 0 ist: t2 (xy, xz, yz) !t e (z2, x2–y2) 3. Aufgabe Disproportionierung von Co(II) zu Co(I) und Co(III) wird durch bestimmte P(OR)3-Liganden ausgelöst: 2 Co2+ + 11 P(OR)3 → [Co(P(OR3))5]+ (E) + [Co(P(OR3))6]3+ (F) Komplex E ist trigonal-bipyramidal. E und F sind beide diamagnetisch. – – Oxidationszahl, Elektronenkonfiguration und gesamte Elektronenzahl in E und F? (1 Punkt): Komplex E: Co(I) d8 18 Elektronen Komplex F: Co(III) d6 18 Elektronen Diskutieren Sie die Struktur von E und F anhand des VB-Modells! (1 Punkt): 5L low-spin d8 Komplex E: dsp3 d low-spin d6 s px py pz 6L Komplex F: d s px py pz d2sp3, oktaedrisch Wie oben erwähnt, sagt das VB-Modell nichts darüber aus, ob Komplex E quadratischpyramidal oder trigonal-bipyramidal ist. Wir werden in einer späteren Übung sehen, dass πAkzeptor-Liganden die trigonale-bipyramidale Struktur stabilisieren. – Diskutieren Sie die Struktur von F anhand des MO-LCAO-Modells (nur σ-Bindung)! (1 Punkt): Komplex F ist low-spin d6, was auf die t2g6e0-Elektronenkonfiguration hinweist. Das σbindende MO-LCAO-Schema zeigt, dass die nicht-bindenden t2g-Orbitale vollständig besetzt sind, die σ-antibindenden eg-Orbitale bleiben aber unbesetzt: (Zusatzinformation / Update (nicht notenwirksam!): Wie gelernt, werden die t2g-Orbitale durch π-Akzeptoren stabilisiert. Dies stabilisiert Komplex F zusätzlich) – Anhand der KFT entwerfen Sie ein qualitatives Aufspaltungsmuster für die Energien der dOrbitale von E (sorry, fehlt in der Aufgabestellung!). Wieso ist E diamagnetisch? (2 Punkte): Aus der Charaktertafel erkennt man, dass die d-Orbitalen in drei Sätzen aufgespaltet werden: (a’1: z2; e’: x2–y2, xy; e’’: xz, yz) Ein qualitatives Aufspaltungsmuster für die Energien der d-Orbitale eines fünffach-koordinierten Komplexes mit D3h-Symmetrie kann man durch das Entfernen eines Liganden aus einem oktaedrischen Komplex entwickelt werden. Zuerst soll man bemerken, dass in der trigonalen bipyramidalen Struktur die d(x2–y2)- und d(xy)–Orbitale entartet sind. Somit besitzen sie die gleiche Energie. Gegenüber dem oktaedrischen Komplex wird das d(x2–y2)-Orbital stark stabilisiert, weil ein Ligand vollständig entfernt, und ein weiterer zur Überlappung mit dem d(xy)-Orbital gebracht wird. Dadurch steigt die Energie des d(xy)-Orbitals an. In der D3h-symmetrischen Struktur sind die Energien der d(x2–y2)- und d(xy)–Orbitale gleich: Oh D3h L L L M L L L Oh –L D3h L L M L L L für d8: a1 ' a1' e' e' e'' e'' (siehe Skript, S. 98) Der Komplex ist diamagnetisch, weil die 8 Elektronen nur die e’- und e’’-Orbitale besetzen. Obwohl die a1’–e’-Energiedifferenz kleiner ist als die eg–t2g-Aufspaltung in einem oktaedrischen Komplex, ist P(OR)3 ein stark-Feld-Ligand und stabilisiert low-spin-Komplexe. Kommentar: Beim genaueren Hinsehen der Tabelle im Skript erkennt man, dass alle Wechselwirkungen – entweder Stabilisierungen oder Destabilisierungen – in der TBP-Struktur kleiner sind als im ursprünglichen oktaedrischen Komplex. KFT-Erklärung: Trigonal-bipyramidalen Komplexen enthalten fünf anstatt sechs Liganden, die weniger "gezielt" auf die Orbitale gerichtet sind. Die Situation in der trigonalen Ebene (xy-Ebene) ist entscheidend: 3 Liganden destabilisieren 2 Orbitale (e'). In oktaedrischen Komplexen destabilisieren 4 Liganden nur 1 Orbital (x2–y2)! MO-LCAO-Erklärung: In oktaedrischen Komplexen sind 2 Orbitale σ-antibindend, in trigonal-bipyramidalen Komplexen sind 3 Orbitale σ-antibindend. Somit sind die antibindende Wechselwirkungen in den TBP-Komplexen auf mehr Orbitale verteilt, was die Energiedifferenz zwischen nichtbindenden und antibindenden Orbitalen verkleinert.



![[Co(L)4]2+](http://s1.studylibde.com/store/data/005646305_1-2327cc16f5a9c36cd559ea8082a99824-300x300.png)