IEP - SINUS Bayern
Werbung

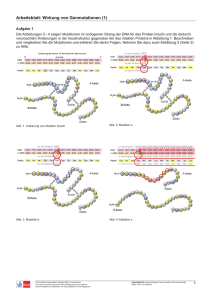
Aufgabenkultur SINUS Bayern Chemie Gymnasium Jgst. 11 Der isoelektrische Punkt von Aminosäuren Die Schülerinnen und Schüler leiten aus textlichen und graphischen Informationen das pHWert-abhängige Ladungsmuster bei Aminosäuren ab und erschließen daraufhin das Prinzip der Elektrophorese. Zur Einübung werden in Gruppenarbeit Aufgaben zur Ionenwanderung entwickelt und im Wechsel mit einer anderen Gruppe gelöst. Ziele • Fachwissen: Kenntnis des isoelektrischen Punkts Anwendung in der Elektrophorese • Erkenntnisgewinnung: Finden und Erklären von Strukturen und Beziehungen in gegebenen Daten; Ziehen geeigneter Schlussfolgerungen O - C O H2N C H CH3 O - C O + H3N C H CH3 O C OH + H3N C H CH3 Hinweise zum Einsatz im Unterricht • Zeitbedarf 25 Minuten - 10 Minuten • Erforderliches Vorwissen Aufbau von Aminosäuren • Materialliste Arbeitsblätter M1 (Information, Aufgaben) und M2 (Vordruck für Übungsphase) M3 (Formeln der Aminosäuren, IEP), ausschneiden und laminieren • Ablauf Das Thema ist fachlich so klar strukturiert, dass sich die Schüler/innen die Ladung eines Aminosäuremoleküls in Abhängigkeit vom pH-Wert selbst erarbeiten können. Dabei nutzen sie sowohl Text- als auch Grafikinformationen und bearbeiten die gestellten Aufgaben. In der anschließenden Übungsphase werden Kleingruppen gebildet und jede Gruppe entwickelt eine Aufgabe. Dazu wählt sie die Formeln von drei Aminosäuren aus und gibt einen pH-Wert für eine geplante Elektrophorese vor. Auf der Rückseite des Arbeitsblattes skizziert sie den eigenen Lösungsvorschlag. Eine zweite Gruppe löst die Aufgabe (Zuordnung der Aminosäuren, Bestimmung der Ladung und der Wanderungsrichtung) und vergleicht mit dem Lösungsvorschlag; evtl. schließt sich eine Diskussion an. Jeweils zwei Gruppen tauschen ihre Aufgaben aus. Verfasser: Klaus Blachut, Alexander Petrovici, Holbein-Gymnasium Augsburg Anlagen: Arbeitsblätter M1 bis M3 1/1 Das Prinzip der Elektrophorese In der nebenstehenden Abbildung ist eine Elektrophoresekammer im Längsschnitt und in der Aufsicht zu sehen. Das Verfahren der Elektrophorese dient der Trennung von Aminosäuregemischen (auch Proteine und DNS). In der Pufferlösung wird ein bestimmter pH-Wert eingestellt, das zu trennende Gemisch auf die Papier- oder Acetatfolienstreifen gebracht. Häufig ist die Startlinie – wie in der Abbildung dargestellt – in der Mitte des Papierstreifens zu finden, sodass die Aminosäuren sich in beide Richtungen bewegen können. Eine Gleichspannung wird angelegt. Die Aminosäuren werden entsprechend ihrer Ionenladung, die wiederum vom pH-Wert abhängt, getrennt. Kationen wandern zum Minuspol, Anionen zum Pluspol. Die Molekülgröße wirkt sich auf die Wanderungsgeschwindigkeit aus: je größer ein Molekül ist, desto langsamer ist seine Wanderungsgeschwindigkeit im elektrischen Feld. Abb. 1: Elektrophoresekammer zur Auftrennung von Aminosäurengemischen Aufgaben: Asparaginsäure 2-Aminobutandisäure IEP=3,0 Glycin 2-Aminoethansäure IEP=6,0 Lysin 2,6-Diaminohexansäure IEP=10,0 Abb. 2: Die Bestandteile eines Aminosäuregemischs werden mithilfe von Vergleichsproben identifiziert. pH=2 1. Zeichne die Lewisformeln der drei angegebenen Aminosäuren und entwickle eine Argumentation, die die Unterschiede der IEP begründet. 2. Wie sehen die Elektropherogramme (Papierstreifen nach erfolgter Elektrophorese) eines Gemischs von Glycin, Lysin und Asparaginsäure bei pH=2, pH=6 und pH=10 aus? (Eintrag in Abb. 3) 3. Betrachte die nebenstehende Abbildung und fasse in eigene Worte, wie Elektrophoreseanalysen in der Praxis durchgeführt werden. Bei welchem pH-Wert könnte die Elektrophorese gemacht worden sein? (Begründung!) Start + - pH=6 + - pH=10 + - Abb. 3: Elektropherogramme eines Gemisches von Glycin, Lysin und Asparaginsäure Klaus Blachut, A. Petrovici, Holbein-Gymnasium Augsburg (SINUS Bayern) Aufgabe: Sortiere die Aminosäuren danach, ob sie im elektrischen Feld zum Plus-oder Minuspol der Versuchsanordnung wandern. Beachte dabei, dass die Größe der Teilchen und die Ladung der Teilchen Einfluss auf Richtung und Geschwindigkeit haben. Startlinie pH= O C OH O C OH H2N C H H H2N C H CH3 Glycin (IEP 5,97) Alanin (IEP 6,01) O C OH H2N C H CH2 H3C C OH H2N C H H3C CH CH3 Valin (IEP 5,97) O H2 N C H H3C CH CH2 CH3 CH3 C C OH CH Leucin (IEP 5,98) O O O Isoleucin (IEP 6,02) C OH H2 N C H CH2 SH Cystein (IEP 5,07) OH H2 N C H CH2 CH2 S O C OH H2N C H CH2 OH O C OH H2 N C H H3C CH OH CH3 Methionin (IEP 5,74) Serin (IEP 5,68) Threonin (IEP 5,87) O C OH H2 N C H O HC HC C H CH CH HC O C H CH2 HN H2 C C CH CH OH OH C C CH2 Prolin (IEP 6,48) Tyrosin (IEP 5,66) O C OH H2N C H CH2 C HO O Asparaginsäure (IEP 2,77) HC HC H C C H C OH H2N C H CH2 C H2 N O O C OH CH2 C C C CH N H O C OH H2 N C H CH2 CH2 HO C O Glutaminsäure (IEP 3,22) C OH H2 N C H H2N C H CH2 H2 N OH Tryptophan (IEP 5,89) O O C H2 N C H CH2 HC Phenylalanin (IEP 5,48) O H2 N C H CH2 C OH C CH2 CH2 CH2 CH2 C CH2 O NH2 Asparagin (IEP 5,41) Glutamin (IEP 5,65) Lysin (IEP 9,74) O C OH H2 N C H O OH CH2 H2 N C H CH2 H2 C CH2 C HN NH H2 N C HC CH CH N NH2 Arginin (IEP 10,76) Histidin (IEP 7,59)