Originalartikel lesen - Österreichische Ärztezeitung
Werbung
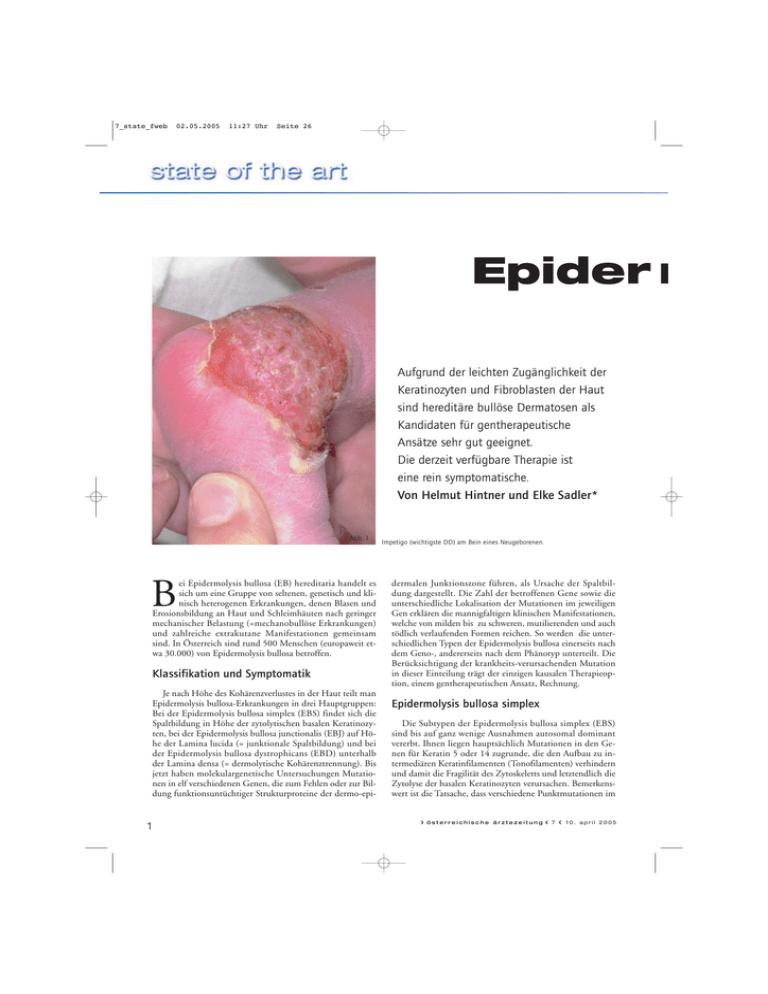
7_state_fweb 02.05.2005 11:27 Uhr Seite 26 Epider m Aufgrund der leichten Zugänglichkeit der Keratinozyten und Fibroblasten der Haut sind hereditäre bullöse Dermatosen als Kandidaten für gentherapeutische Ansätze sehr gut geeignet. Die derzeit verfügbare Therapie ist eine rein symptomatische. Von Helmut Hintner und Elke Sadler* Abb. 1 B ei Epidermolysis bullosa (EB) hereditaria handelt es sich um eine Gruppe von seltenen, genetisch und klinisch heterogenen Erkrankungen, denen Blasen und Erosionsbildung an Haut und Schleimhäuten nach geringer mechanischer Belastung (=mechanobullöse Erkrankungen) und zahlreiche extrakutane Manifestationen gemeinsam sind. In Österreich sind rund 500 Menschen (europaweit etwa 30.000) von Epidermolysis bullosa betroffen. Klassifikation und Symptomatik Je nach Höhe des Kohärenzverlustes in der Haut teilt man Epidermolysis bullosa-Erkrankungen in drei Hauptgruppen: Bei der Epidermolysis bullosa simplex (EBS) findet sich die Spaltbildung in Höhe der zytolytischen basalen Keratinozyten, bei der Epidermolysis bullosa junctionalis (EBJ) auf Höhe der Lamina lucida (= junktionale Spaltbildung) und bei der Epidermolysis bullosa dystrophicans (EBD) unterhalb der Lamina densa (= dermolytische Kohärenztrennung). Bis jetzt haben molekulargenetische Untersuchungen Mutationen in elf verschiedenen Genen, die zum Fehlen oder zur Bildung funktionsuntüchtiger Strukturproteine der dermo-epi- 1 Impetigo (wichtigste DD) am Bein eines Neugeborenen. dermalen Junktionszone führen, als Ursache der Spaltbildung dargestellt. Die Zahl der betroffenen Gene sowie die unterschiedliche Lokalisation der Mutationen im jeweiligen Gen erklären die mannigfaltigen klinischen Manifestationen, welche von milden bis zu schweren, mutilierenden und auch tödlich verlaufenden Formen reichen. So werden die unterschiedlichen Typen der Epidermolysis bullosa einerseits nach dem Geno-, andererseits nach dem Phänotyp unterteilt. Die Berücksichtigung der krankheits-verursachenden Mutation in dieser Einteilung trägt der einzigen kausalen Therapieoption, einem gentherapeutischen Ansatz, Rechnung. Epidermolysis bullosa simplex Die Subtypen der Epidermolysis bullosa simplex (EBS) sind bis auf ganz wenige Ausnahmen autosomal dominant vererbt. Ihnen liegen hauptsächlich Mutationen in den Genen für Keratin 5 oder 14 zugrunde, die den Aufbau zu intermediären Keratinfilamenten (Tonofilamenten) verhindern und damit die Fragilität des Zytoskeletts und letztendlich die Zytolyse der basalen Keratinozyten verursachen. Bemerkenswert ist die Tatsache, dass verschiedene Punktmutationen im ❯ österreichische ärztezeitung ❮ 7 ❮ 10. april 2005 7_state_fweb 02.05.2005 11:27 Uhr Seite 27 DFP - Literaturstudium r molysis bullosa hereditaria Abb. 2 Keratin-Gen zu ganz unterschiedlichen klinischen Bildern führen: Findet sich der Defekt innerhalb der Stabdomäne des Proteins, ist eine Aggregation der Tonofilamente trotz der strukturellen Änderung des Aggregationsprodukts möglich; dies führt zu milderen Verlaufsformen wie der EBS WEBERCOCKAYNE (EBS-WC) oder EBS KÖBNER (EBS-K). Sind hingegen die hochkonservierten N- und C-terminalen Enden des Proteins betroffen, resultiert eine schwerere Verlaufsform (EBS Dowling-Meara (EBS-DM) mit palmoplantaren Hyperkeratosen, Narbenbildung, Milien und Beteiligung der Mundschleimhaut), weil eine End-zu-End-Aggregation der Keratinfilamente verhindert wird. Eine seltene Variante ist die EBS mit Muskeldystrophie (EBS-MD), bei der eine Mutation im Plektin-Gen vorliegt. Plektin ist nicht nur ein Strukturprotein der Hemidesmosomen, sondern auch der „Z-discs“ von Myofibrillen, welche diese mit den Aktinfilamenten verankern. Patienten mit EBS mit Muskeldystrophie leiden von Geburt an an Blasenbildung und an einer etwa im zweiten Lebensjahrzehnt einsetzenden Muskeldystrophie, an der die Patienten schließlich meist im dritten Lebensjahrzehnt versterben. Ausgeprägte Atrophie und Erosionen bei REBD-HS. Epidermolysis bullosa junctionalis In der Hauptgruppe der autosomal rezessiv vererbten Epidermolyis bullosa junctionalis (EBJ) wird zwischen der schwerwiegenden, meist tödlich verlaufenden HERLITZVariante (EBJ-H) und der milderen non-HERLITZ-Variante (EBJ-nH, generalisierte atrophisierende benigne EB = GABEB) unterschieden. Bei der EBJ-H führen homozygote Mutationen im Laminin 5 Gen permanent zum Auftreten von Blasen, die mit atrophen Narben abheilen und oft zu chronischen, nicht heilenden granulomatösen Erosionen führen. Weiters finden sich Onychodystrophie, Verlust der Nägel, eine Beteiligung der Mundschleimhaut mit Mikrostomie, Ankyloglossie, Zahnschmelzhypoplasie (bei allen Patienten mit EBJ!) und exzessive Karies sowie Organmanifestationen in Form einer Beteiligung besonders des Respirations(oft lebensbedrohlich), aber auch des Gastrointestinalund/oder Urogenitaltraktes. Den EBJ-nH-Formen liegen einerseits kombinierte heterozygote Mutationen in den Laminin 5-Genen, bedeutend häufiger aber homozygote © alle abb hintner ❯ österreichische ärztezeitung ❮ 7 ❮ 10. april 2005 2 7_state_fweb 02.05.2005 11:27 Uhr Seite 28 Epidermolysis bullosa dystrophicans Ihr liegen Mutationen im Gen für Typ-VIIKollagen (Col7A1), dem Hauptprotein der Ankerfibrillen, zugrunde. Entsprechend dem Vererbungsmodus unterscheidet man zwischen der milder verlaufenden autosomal dominanten EBD (DEBD) und den schwerwiegenden autosomal rezessiven Formen (REBD), bei denen man wiederum zwischen der äußerst belastenden Verlaufsform REBD-Hallopeau-Siemens (REBD-HS) Abb. 3 und der etwas milderen REBD-non-HallopeauVereinfachte Darstellung der dermo-epidermalen Junktionszone. Es sind hauptsächlich Siemens (REBD-nHS) unterscheidet. Die relativ die für die Epidermolysis bullosa hereditaria wichtigen Strukturproteine dargestellt. milde Verlaufsform der DEBD erklärt sich daKeratin 5 (K5), 14 (K14) und Plektin bei der EBS, Laminin 5, a6b4-Integrin und durch, dass sowohl das „Wildtype“-Allel als auch bullöses Pemphigoid-Antigen 2 (BP Ag2) bei EBJ und Typ-VII-Kollagen bei EBD. das mutierte Allel gleichermaßen exprimiert werden und somit 12,5 Prozent der Ankerfibrillen ei Mutationen des COL-17A1-Gens (kodiert für das Bulne normale Struktur aufweisen. Vorzeitige Stop-Codons in löse Pemphigoid Antigen 2 = BPAg2 = Typ-XVII-Kollabeiden Allelen führen bei den rezessiven Formen hingegen gen) zugrunde. Die Hautmanifestationen gleichen jenen zum völligen Fehlen von Ankerfibrillen, und dementspreder EBJ-H mit generalisierter Blasenbildung, Erosionen, chend schwerwiegend ist auch die Symptomatik dieser PatienKrusten und atrophen Narben. ten: Generalisierte Blasenbildung, Erosionen, ausgedehnte Verkrustungen, atrophe Narben, narbige Alopezie und NagelDazu kommen eine Alopezie (vom männlichen Typ), Naverlust von Geburt an. Zudem erschweren kutane und extrageldystrophie beziehungsweise Nagelverlust, Zahnschmelzkutane Komplikationen, welche bei der REBD-Hallopeauhypoplasie und sogenannte Epidermolysis bullosa-Nävi. DieSiemens am häufigsten auftreten, den Krankheitsverlauf. se hell- bis dunkelbraunen, bis handtellergroßen Nävuszellnävi entstehen im Bereich von Blasen und formen deren Kutane Komplikationen Grenzen nach. Mit zunehmendem Alter werden sie papilloBei 75 Prozent der Patienten mit REBD-HS treten bis matöser und heller. Klinisch und teilweise auch histopathozum sechsten Lebensjahr Mutilationen an Händen und Fülogisch weisen sie Kriterien auf, die denen von Melanomen ßen mit Pseudosyndaktylien sowie Kontrakturen auf. Zuweitgehend gleichen. Bisher wurde von uns aber noch keine dem weisen diese Patienten auch ein erhöhtes Risiko für die maligne Entartung beobachtet. Lebensbedrohliche ExtrakuEntstehung von aggressiven Plattenepithelkarzinomen auf, tanmanifestationen sind bei der EBJ-non-HERLITZ selten, die oft multipel vorkommen, rasch metastasieren und kaum wodurch die Lebenserwartung dieser Patienten in der Regel chemo- oder radiosensibel sind. Die kumulative Häufigkeit nicht eingeschränkt ist. der Plattenepithelkarzinome steigt für Patienten mit REBDHS von 22 Prozent im 25. Lebensjahr bis zu 53 Prozent im Eine weitere, sehr seltene Untergruppe ist die EBJ mit Py35. Lebensjahr. lorusatresie (EBJ-PA). Den Betroffenen fehlt mutationsbedingt ein funktionstüchtiges α6β4-Integrin in Hemidesmosomen von Epithelien sowie Schwann-Zellen, Thymozyten Extrakutane Komplikationen und perineuronalen Fibroblasten peripherer Nerven. Durch Zähne: den schweren Verlauf der Hauterkrankung und SystembeteiZahnschmelzhypoplasie und Zahndysplasie bereiten geligung (Pylorusatresie) gekennzeichnet, versterben Kinder meinsam mit der erschwerten Mundhygiene und Nahrungsmit EBJ-PA meist innerhalb der ersten Lebensmonate. Es aufnahme aufgrund schmerzhafter Blasenbildung und Erowurden jedoch auch nicht letale Varianten, welche durch sionen an Gingiva, Zunge und Mundschleimhaut die compound-heterozygote Mutationen hervorgerufen wurden, Grundlage für das Auftreten von exzessiver Karies. beschrieben. 3 ❯ österreichische ärztezeitung ❮ 7 ❮ 10. april 2005 7_state_fweb 02.05.2005 11:27 Uhr Seite 30 Gastrointestinaltrakt: Stoffwechsel und Allgemeinsymptome: Häufige Erosionsbildung an der Schleimhaut des Gastrointestinaltraktes führen zu Mikrostomie, Dysphagie, Strikturen und Pseudo-Divertikelbildung im Darmbereich, Obstipation und schmerzhafter Defäkation bis hin zur Stuhlverhaltung. Chronische Anämie (49 Prozent) und Wachstumsretardierung (42 Prozent) sind häufige Aspekte der EBD. Die Anämie reflektiert meist einen chronischen Eisenmangel, die Wachstumsretardierung fortwährende Mangelernährung. Über denudierte Areale der Haut und Schleimhäute gehen, wie bei Verbrennungen II. Grades, permanent Proteine und andere Nährstoffe verloren; außerdem liegt bei Patienten mit angeborener Epidermolysis bullosa durchgehend eine katabole Stoffwechsellage mit gesteigertem Kalorienbedarf vor. Respirationstrakt: Schleimhautveränderungen des Respirationstraktes finden sich am häufigsten bei der EBJ. Diese können zu chronischer Heiserkeit, inspiratorischem Stridor, laryngealen Stenosen und Obstruktionen führen. Das Endstadium einer ausgeprägten Beteiligung des Respirationstraktes stellt die tracheotomiepflichtige Atemwegsobstruktion dar, eine lebensbedrohliche Komplikation, die hauptsächlich in den ersten Lebensjahren beobachtet wird. Urogenitaltrakt: Urologische Veränderungen sind mit etwa 3,5 Prozent der EBD-Patienten relativ selten. Aber aufgrund schwerwiegender Komplikationen wie Dysurie, Hämaturie, Stenosen, Reflux, Hydronephrose, Urosepsis und Amyloidose sollten bei allen Patienten regelmäßige urologische Kontrolluntersuchungen durchgeführt werden. Augen: Eine Beteiligung der Augen ist bei der REBD mit 51 Prozent sehr häufig. Korneale und konjunktivale Erosionen können zu Narbenbildungen, Auftreten von Symblephara und Lidfehlstellungen führen. Völlige Erblindung tritt bei 2,5 Prozent der EBD-Patienten auf. Diagnose und Differenzialdiagnosen Die besondere Bedeutung der Diagnostik der Epidermolysis bullosa-Erkrankungen beruht darauf, dass die Veränderungen auf molekularer Ebene mit Klinik, Verlauf, Prognose und damit der entsprechenden Therapie korrelieren. Erst die exakte Diagnose erlaubt eine genaue Aussage bezüglich des individuellen Schicksals und ermöglicht eine adaptive Behandlungsstrategie für eine bestmögliche Lebensqualität. Ein wichtiges diagnostisches Verfahren bei der Diagnosestellung von hereditären bullösen Dermatosen ist neben der Routinehistologie (intraepidermale Zytolyse bei EBS versus subepidermale Spaltbildung bei EBJ und EBD) und Elektronenmikroskopie (Spalt in Lamina lucida versus unter Lamina densa, Fehlen oder Reduktion von Ankerfibrillen) das „AntigenMapping“. Dabei lassen sich mit Hilfe der Immunperoxidase- beziehungsweise Immunfluoreszenztechnik die Lokalisation beziehungsweise Expression von Strukturproteinen in der dermo-epidermalen Basalmembranzone darstellen. So kann nicht nur sehr rasch und vergleichsweise billig die Höhe der Spaltbildung definiert werden, sondern es lassen sich auch semiquantitative Aussagen (fehlend-reduziert-normal) über den Proteindefekt treffen, die letztendlich die Basis für die Mutationsanalysen darstellen. Allerdings ergeben rein funktionelle Ausfälle von BMZ-Proteinen nicht selten ein normales Färbemuster. Zusätzliche, oft sehr aufwändige molekularbiologische Techniken wie die Mutationsanalyse bieten verfeinerte diagnostische und investigative Detektionsmöglichkeiten. Diese Verfahren haben angesichts der genetischen Heterogenität der Epidermolysis bullosa und der großen Zahl an familienspezifischen Mutationen weitreichende Implikationen und sind letztendlich die Grundlage für eine umfassende genetische Beratung und Prognosestellung für betroffene und gegebenenfalls zukünftige Kinder. Abb. 4 Symblepharonbildung im temporalen Lidwinkel bei EBD. 4 Beim Vorliegen von schweren Epidermolysis bullosa-Formen wie EBJ-H oder REBD-HS in einer Familie besteht bei einer neuerlichen Schwangerschaft die Möglichkeit einer pränatalen Diagnostik. Ab der elften Gestationswoche ❯ österreichische ärztezeitung ❮ 7 ❮ 10. april 2005 7_state_fweb 02.05.2005 11:27 Uhr Seite 32 Abb. 5 Unter professioneller Anleitung von den Eltern selbst angefertigte straffe Verbände, die das Zusammenwachsen der Finger vermeiden sollen. kann mit Hilfe der PCR-Amplifikation von DNA aus Chorionzottenbiopsien oder Amniozenteseproben eine Mutationsanalyse durchgeführt werden. Zwischen der 17. und 21. Gestationswoche besteht die Möglichkeit, fetale Hautbiopsien elektronenmikroskopisch oder mit immunhistochemischen Methoden zu analysieren. Differenzialdiagnostisch kommen bei neonataler Blasenbildung nur wenige andere Erkrankungen in Betracht: Sowohl die Streptokokken- als auch die Staphylokokken-bedingte Impetigo können mit einer Blasenbildung einhergehen. Aufgrund anamnestischer (sehr ansteckend, oft kleine Epidemien) und klinischer Merkmale (deutliche Entzündungszeichen, Pusteln, honiggelbe Krusten) kann man sie jedoch - besonders bei Erregernachweis - von einer Epidermolysis bullosa unterscheiden. Neben diesen wichtigen konservativen Maßnahmen sind manchmal auch chirurgische Eingriffe notwendig, wie die Lösung von Pseudosyndaktylien und Kontrakturen der Finger mit nachfolgender Deckung der Wunden mit Spalthaut, Vollhaut oder künstlicher Haut. Auch die Langzeiternährung über eine Magensonde nach Gastrostomie ist bei einigen Patienten notwendig und hilfreich, um eine ausreichende Nahrungs- und Kalorienzufuhr zu gewährleisten. Unverzichtbar ist die interdisziplinäre Zusammenarbeit mit anderen Fachrichtungen, um mögliche Komplikationen frühzeitig erkennen und behandeln zu können. Ein möglicher Ansatz zur kurativen Behandlung ist in Zukunft die Gentherapie. Damit könnte es künftig gelingen, das fehlende Gen bei den rezessiv vererbten Epidermolysis bullosa-Formen zu ersetzen und das mutierte Allel bei den dominant vererbten Formen zu inaktivieren oder zu reparieren. Aufgrund der leichten Zugänglichkeit der Keratinozyten und Fibroblasten der Haut und wegen deren einfacher Kultivierbarkeit sind hereditäre bullöse Dermatosen als Kandidaten für gentherapeutische Ansätze sehr gut geeignet. Bis zur Entwicklung brauchbarer gentherapeutischer Behandlungen wird jedoch noch einige Zeit vergehen. Literatur bei den Verfassern Therapie Für Epidermolysis bullosa-Erkrankungen steht zur Zeit keine kausale Behandlung zur Verfügung. So ist die derzeitige Therapie eine rein symptomatische, die sich auf fünf wichtige Pfeiler stützt: Verhinderung oder Verminderung der Blasenbildung durch gepolsterte Schutzkleidung. Bei der Nahrungsaufnahme verhindert flüssige oder breiige Kost eine schmerzhafte Traumatisierung im Gastrointestinaltrakt. Vermeidung von sekundären Infektionen von Erosionen durch Behandlung mit sterilen Verbänden beziehungsweise antimikrobiellen Externa. Rasche und, wenn möglich, erregerspezifische systemische Antibiose zur Behandlung ausgeprägter bakterieller Infektionen. Förderung der Wundheilung durch gepolsterte, sterile Verbände. Sicherstellung einer ausreichenden Ernährung. 5 *) Univ. Prof. Dr. Helmut Hintner, Dr. Elke Sadler im Namen des Epidermolysis bullosa-Teams Salzburg: J.W. Bauer, M. Burger-Rafael, P. Buttenhauser, A. Diem, J. Hachleitner, A. Klausegger, C. Krenkel, M. Laimer, M. Langthaler, C. Lanschuetzer, B. Ludwikowski, W. Muss, G. Pohla-Gubo, R. Puttinger, R. Riedl, J. Ruecker, J. Ruckhofer, W. Sperl, R. Stadlhuber, A. Steiner, H. Steiner, J. Stoiber, V. Wally, I. Walser, H. Weiss, D. Wurzenrainer; Universitätsklinik für Dermatologie/Paracelsus Medizinische Privatuniversität Salzburg; Müllner Hauptstraße 48, 5020 Salzburg, Tel.: 0662/44 82/58 827; Fax-DW 30 03; E-mail: [email protected] Lecture Board: Univ. Prof. Dr. Klemens Rappersberger, Krankenanstalt der Stadt Wien Rudolfstiftung; Univ. Prof. Dr. Josef Smolle, Universitätsklinik für Dermatologie und Venerologie Graz; Univ. Prof. Dr. Matthias Schmuth, Universitätsklinik für Dermatologie und Venerologie Innsbruck Herausgeber: Abteilung: Universitätsklinik für Dermatologie, Paracelsus Medizinische Privatuniversität Salzburg Diesen Artikel finden sie auch im Web unter www.arztakademie.at ❯ österreichische ärztezeitung ❮ 7 ❮ 10. april 2005 7_state_fweb 02.05.2005 11:27 Uhr Seite 35 DFP - Literaturstudium eb-Haus A ufgrund des seltenen Vorkommens dieser Genodermatosen (rare oder „orphan“ diseases) hält sich – auch die fachärztliche – Erfahrung in engen Grenzen. Bei unterschiedlichem klinischen Bild beeinträchtigen die Folgeerscheinungen das individuelle Leben im Großen (Schulbildung, Berufswahl, familiäre und finanzielle Belastung, Kosmetik), aber auch bei den täglichen Abläufen (Essen, Gehen, Hygiene, regelmäßige Verbandwechsel, Arztbesuche). Die Vielschichtigkeit der Grundkrankheit als Multiorganerkrankung und der (in)direkt assoziierten Belastungen verpflichtet zu einer fachüberschreitenden Betreuung (medizinisch, psychologisch, sozial) und umfassenden Koordination (zeitlich und örtlich) aller Beteiligten, also von Patient, Familie, Selbsthilfegruppen und ärztlichem, Pflege- sowie wissenschaftlichem Personal. Um diesen Anspruch besser erfüllen zu können, vorhandene Ressourcen besser auszuschöpfen und eine optimale Infrastruktur für die Betreuung der Patienten zu schaffen, hat man sich in Salzburg die Errichtung eines medizinischen Spezialzentrums zum Ziel gesetzt. Am 04. Oktober 2004 erfolgte der Spatenstich zum Bau des eb-hauses, eines „Centers of Excellence“ für Behandlung, Beratung und Erforschung der Epidermolysis bullosa. Finanziert wird dieses Vorhaben aus Spendengeldern, für deren Rekrutierung sich die „debra-austria“, eine EB-Selbsthilfegruppe, besonders engagiert. Zentrale Aktivität der „debra-austria“, einer Organisation mit international organisiertem Dachverband, ist neben einer engagierten Öffentlichkeitsarbeit (mit fundraising) der Informations- und Erfahrungsaustausch auf Patientenebene. Als medizinisches Kompetenzzentrum soll das eb-haus Salzburg durch eine vorrangig ambulante Versorgung, in die eine auf Epidermolysis bullosa spezialisierte Ärztin und eine speziell dafür ausgebildete Krankenschwester eingebunden sind, die bedürftnisgerechte Betreuung der meist jungen Patienten sicherstellen. Um die Komplikationen der Erkrankung effizient behandeln zu können, komplettieren Ärzte mit Epidermolysis bullosa-Erfahrung aus verschiedenen Fachgebieten der Medizin (Dermatologie, Kinder- und Jungendheilkunde, Kinderchirurgie, Mund- Kiefer- und Gesichtschirurgie, Gynäkologie, Urologie, HNO, Orthopädie, Augenheilkunde sowie physikalische Medizin und Rehabilitation) mit wertvollem Spezialwissen den klinischen Betreuerstab. Eine Kooperation mit den Instituten für Pathologie und klinische Genetik sowie der ernährungsmedizinischen und psychologischen Beratung ergänzt das Angebot. Der zweite Teilbereich, die Epidermolysis bullosa-Akademie, dient auf mehreren Ebenen dem vielfältigen Wissens- und Erfahrungsaustausch zwischen allen, die eingebunden sind. Ein umfangreicher bibliographischer Fundus, kontinuierliche Aus- und Fortbildungsprogramme mit der Organisation von Seminaren und internationalen Kongressen sollen - ebenso wie Schulungen und Beratung der Betroffenen sowie deren Angehörigen - permanent Gelegenheit zur praktischen und theoretischen Qualifizierung und Spezialisierung bieten. Die Teledermatologie für Diagnose, second-opinion Konsultation und Lehre ist eine weitere zentrale Komponente des Akademiebereichs, die zum Teil im Rahmen des TIGA („Tele-Immunofluorescence Microscopy in a Global Alliance“)-Projekts, einer internationalen Zusammenarbeit mehrerer Kliniken und Labors auf dem Gebiet der Befundung und Diskussion von Immunfluoreszenz-Untersuchungen, bereits realisiert werden konnte (J Telemed Telecare 2004; 10:39-43). Die wissenschaftliche Auseinandersetzung mit der Epidermolysis bullosa im Rahmen klinischer, basiswissenschaftlicher und gentherapeutischer Forschung ist ein Kernbereich im eb-haus. Denn das bessere Verstehen der pathologischen Mechanismen bildet die Grundlage, um Lösungsansätze zu entwickeln. Durch die Zusammenarbeit mit renommierten Institutionen der Epidermolysis bullosa-Forschung und durch den Aufbau weltweiter Netzwerke bietet sich die Möglichkeit, wissenschaftlich auf international hohem Niveau mitzuarbeiten. „debra-austria” Spendenkonto PSK 90.000.096 (BLZ 60.000) oder „debra-austria, Verein zur Förderung der Epidermolysis Forschung“ PSK 90.033.300 (BLZ 60.000); Spenden für den Verein sind steuerlich absetzbar. IMPRESSUM Medieninhaber (Verleger), Herausgeber und Redaktion: Österreichische Ärztekammer, Verlagshaus der Ärzte GmbH Gesellschaft für Medienproduktion und Kommunikationsberatung GmbH, 1010 Wien, Nibelungeng. 13 Mit der Herausgabe beauftragt: Mag. Martin Stickler, Tel. 512 44 86, Fax 512 44 86-24, E-Mail: [email protected] Chefredaktion: Mag. Reinhard Hampel, Dr. Agnes M. Mühlgassner Redaktion: Dr. Monika Berthold, Mag. (FH) Silvia Hecher MAS, Birgit Merz Sekretariat, Fotos, Kongresse: Beatrice Ostermann, DW 13 Verlagsleitung ÖÄZ, Anzeigenleitung: Ulrich P. Pachernegg DW 18 Kleinanzeiger, Abos: Anna Hisch DW 41 Layout: Irene Guberner Hersteller: Druckerei Berger, Ferdinand Berger & Söhne Ges.m.b.H. A-3580 Horn, Wienerstrasse 80, Tel. 02982/461-0, DVR 0506664. Die namentlich gezeichneten Beiträge sind als persönliche Meinung des jeweiligen Autors aufzufassen. Beiträge im Produktreport sind bezahlt. Die Zeitung erscheint jeden Monat am 10. und 25., die Folgen 1/2 (Jän.), 13/14 (Juli), 15/16 (Aug.) und 23/24 (Dezember) erscheinen als Doppelnummer. Verbreitete Auflage: 38.562 Stk. (geprüft durch ÖAK Österr. Auflagenkontrolle 3/04). Derzeit gilt der Inseratentarif Nr. 53. *) In den Rubriken "Produktreport" und "Supplementum" erscheinen Beiträge, die über Präparate oder andere Produkte informieren. Diese Beiträge sind gesponsert. ❯ österreichische ärztezeitung ❮ 7 ❮ 10. april 2005 6











