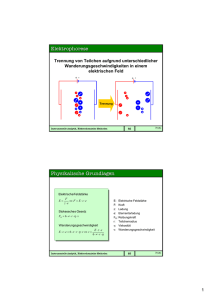
Einführung in die Elektrochemie Definitionen (1)
Werbung

Einführung in die Elektrochemie > Grundlagen, Methoden > Leitfähigkeit von Elektrolytlösungen, Konduktometrie > Elektroden – Metall-Elektroden 1. und 2. Art – Redox-Elektroden – Membran-Elektroden > Potentiometrie > Elektrogravimetrie > Coulometrie > Voltammetrie – Polarographie – Amperometrie – Voltametrie > Elektrophorese – Gelelektrophorese – Kapillarelektrophorese Instrumentelle Analytik, Elektrochemische Methoden 1 MAH Definitionen (1) > Elektrochemische Analysenmethoden beruhen auf physikalischen oder chemischen Vorgängen, die in elektrochemischen Zellen unter Ladungsaustausch an den Elektroden ablaufen. > Elektrochemische Zellen bestehen meist aus zwei Elektroden, die in den Elektrolyten hineinragen. Instrumentelle Analytik, Elektrochemische Methoden 2 MAH 1 Definitionen (2) > Elektroden sind sich berührende Phasen, bei denen neben elektronenleitenden Phasen in mindestens einer Phase Ionenleitung möglich ist. > Als Elektrodenreaktionen bezeichnet man heterogene Reaktionen zwischen Bestandteilen zweier sich berührender Phasen, in deren Verlauf ein Durchtritt von Ionen oder Elektronen und damit Stromfluß durch die Phasengrenzfläche stattfindet. Instrumentelle Analytik, Elektrochemische Methoden 3 MAH Elektrochemische Messmethoden > Direktverfahren – zur qualitativen Bestimmung (selten, z. B. Polarographie) – zur quantitativen Bestimmung (häufiger, z. B. Elektrogravimetrie, Polarographie, Coulometrie) > Indizierung von Äquivalenzpunkten – bei fast allen klassischen Titrationsverfahren z. B. potentiometrisch, konduktometrisch, voltametrisch, coulometrisch u. a. Instrumentelle Analytik, Elektrochemische Methoden 4 MAH 2 Meßgrößen in der Elektrochemie > Spannung der elektrochemischen Zelle (Potentiometrie) > durch die Zelle fließende Stromstärke (Amperometrie) > durch die Zelle transportierte elektrische Ladung (Coulometrie) > Stoffmenge bzw. Masse einer durch Stromfluß abgeschiedenen Substanz (Elektrogravimetrie) > elektrischer Widerstand bzw. Leitwert (Leitfähigkeit) (Konduktometrie) > Wanderungsgeschwindigkeit von Ionen im elektrischen Feld (Elektrophorese) Instrumentelle Analytik, Elektrochemische Methoden 5 MAH Elektrische Leiter > Metalle (Leiter 1. Klasse, Elektronenleiter) – Stromfluß durch Elektronen – geringer elektrischer Widerstand – Widerstand abhängig u. a. von Länge, Querschnitt und Beschaffenheit des Metalls (Temperatur, Element) > Elektrolytlösungen (Leiter 2. Klasse, Ionenleiter) – Stromfluß durch Ionen – hoher elektrischer Widerstand – Widerstand abhängig u. a. von Länge, Querschnitt, Beschaffenheit der Lösung (Temperatur, Ionenart, Lösungsmittel, Konzentration; Ionenladung, Ionenradius, Ionenbeweglichkeit) Instrumentelle Analytik, Elektrochemische Methoden 6 MAH 3 Mechanismen der Ionenleitung > Migration – Wanderung im elektrischen Feld (Feldgradient) > Konvektion – thermische Ionenwanderung (Temperaturgradient) – mechanische Ionenwanderung (Rühren) > Diffusion – Ionenwanderung zum Ausgleich von Konzentrationsunterschieden Instrumentelle Analytik, Elektrochemische Methoden 7 MAH Elektrische Meßgrößen, Einheiten & Gesetze > Stromstärke I= > Q t W Q U: W: Spannung in Volt [V] Arbeit / Energie in Joule [J = N·m] E: F: Feldstärke [V·m-1] Kraft in Newton [N] R: Widerstand in Ohm [Ω] Feldstärke E= > Stromstärke in Ampere [A] Ladung in Coulomb [C = A·s] Faraday-Konstante: 96 487 C·mol -1 Spannung U= > I: Q: F: F Q E= U l Ohmsches Gesetz I= U R Instrumentelle Analytik, Elektrochemische Methoden 8 MAH 4 Widerstand bzw. Leitfähigkeit (Leiter 1. & 2. Ord.) > Spezifischer Widerstand ρ = R⋅ A l > spezifischer Widerstand [Ω·cm] Querschnitt des Leiters [cm2] Länge des Leiters [cm] L, (G): Leitwert in Siemens [S, Ω-1] κ: Leitfähigkeit [Ω-1·cm -1, S·cm -1] Leitwert L(G) = > ρ: A: l: 1 R Leitfähigkeit κ=1= l ρ R⋅ A Instrumentelle Analytik, Elektrochemische Methoden 9 MAH Leitfähigkeit (Leiter 2. Ordnung) > Molare Leitfähigkeit Λ = κ ⋅ 1000 c > molare Leitfähigkeit [S·cm2·mol-1] Λ*: Äquivalentleitfähigkeit [S·cm2·mol-1] Ladung(en) der Kationen bzw. Anionen Zahl der Anionen bzw. Kationen Äquivalentleitfähigkeit Λ* = κ ⋅ 1000 c⋅z⋅n > Λ: z: n: Äquivalentleitfähigkeit bei unendlicher Verdünnung Λ = Λ∞ − k ⋅ c Λ∞: Λ* bei unendlicher Verd. (c → 0) k: substanzspez. Proportionalitätsfaktor „Kohlrauschsches Quadratwurzelgesetz“ Instrumentelle Analytik, Elektrochemische Methoden 10 MAH 5 Leitfähigkeit HCl HCl NaOH NaOH NaCl NaCl NaOAc NaOAc AcOH AcOH Äquivalentleitfähigkeit Konzentrationsabhängigkeit von Λ c lg c MAH 11 Instrumentelle Analytik, Elektrochemische Methoden Molare Ionenleitfähigkeit λ Λ∞ = ν + ⋅ λ+ ,∞ + ν − ⋅ λ−,∞ λ+ , ∞ S ⋅ cm ⋅ mol 350 74 2 H 3O K+ + Na+ H H O + H + Na λ− , ∞ −1 50 OH Cl- S ⋅ cm 2 ⋅ mol −1 200 76 - AcO- 41 H H H H H H H O O O O O O O H H H H H H H H H H H H O O O O O O H H H Instrumentelle Analytik, Elektrochemische Methoden H H 12 H + H + Na H MAH 6 Konduktometrie > Meßgröße elektrische Leitfähigkeit einer Elektrolytlösung > unspezifisch es wird die Leitfähigkeit der gesamten Lösung erfaßt ⇒ Direktmessung: Gesamtelektrolytgehalt > hohe Empfindlichkeit Leitfähigkeit ändert sich, – wenn sich die Zahl der gelösten Ionen ändert. – wenn sich die Ionenleitfähigkeiten ändern (Ionen werden ersetzt). ⇒ Konduktometrische Titrationen Instrumentelle Analytik, Elektrochemische Methoden MAH 13 Konduktometrische Titrationen (1) > Fällungstitrationen, Komplexometrische Titrationen Na+ + Cl- + Ag+ + NO3- → Na+ + NO3- + AgCl↓ κ HH3OO++ 3OH OHCl Cl+ Na Na+ gesamt gesamt > Säure-Base-Titrationen H3O+ + Cl- + Na+ + OH- → 2 H2O + Cl- + Na+ > Redoxtitrationen ÄP Instrumentelle Analytik, Elektrochemische Methoden 14 τ MAH 7 Konduktometrische Titrationen (2) > Vorteile – sehr schwache Säuren sind titrierbar – sehr verdünnte Lösungen sind titrierbar (besser als konzentrierte) – hohe Empfindlichkeit > Nachteile – konzentrierte Lösungen weniger genau titrierbar (Abweichung gemäß Kohlrauschschem Quadratwurzelgesetz) – hohe Fremdionenkonzentration stört – Redoxtitrationen meist nicht durchführbar MAH 15 Instrumentelle Analytik, Elektrochemische Methoden Konduktometrische Titrationen (3) κ κ Natriumacetat Natriumacetat Ammoniak Ammoniak Salzsäure Salzsäure Essigsäure Essigsäure mit mitHCl HCl mit mitNaOH NaOH (simultan) (simultan) ➊ ➌ ➋ ÄP τ Instrumentelle Analytik, Elektrochemische Methoden 1. ÄP 16 2. ÄP τ MAH 8 Meßtechnik > platinierte Platinbleche – Oberflächenvergrößerung, Vermeidung von Polarisation > thermostatierbare Tauchzellen A – mit bekannter Zellkonstante für Direktbestimmungen l > Wechselspannung Zellkonstante l/A – Senkung des Wechselstromwiderstandes – Vermeidung von Konzentrationspolarisation – 50 Hz bis 20 kHz > Oszillometrie – 100 kHz bis 10 MHz – geringer Wechselstromwiderstand – Elektroden an der Gefäßaußenwand 17 Instrumentelle Analytik, Elektrochemische Methoden MAH Leitfähigkeitsmessung > Direktmessung – konstante Spannung wird angelegt – Strom wird gemessen – aus R = U/I ergibt sich zusammen mit der Zellkonstanten κ > Wheatstonesche Brückenschaltung Rv R1 ∼ I R2 Rx R1 R ⋅R = ⇔ Rx = 1 2 R2 Rv Rv Rx Instrumentelle Analytik, Elektrochemische Methoden 18 MAH 9