Pembrolizumab
Werbung
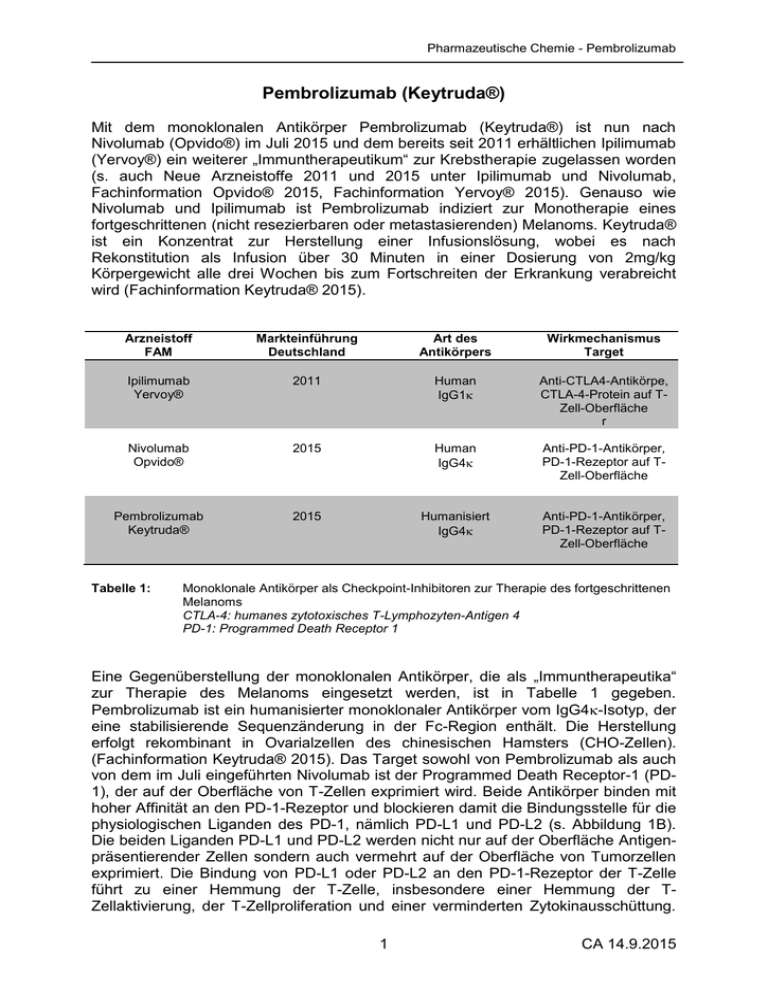
Pharmazeutische Chemie - Pembrolizumab Pembrolizumab (Keytruda®) Mit dem monoklonalen Antikörper Pembrolizumab (Keytruda®) ist nun nach Nivolumab (Opvido®) im Juli 2015 und dem bereits seit 2011 erhältlichen Ipilimumab (Yervoy®) ein weiterer „Immuntherapeutikum“ zur Krebstherapie zugelassen worden (s. auch Neue Arzneistoffe 2011 und 2015 unter Ipilimumab und Nivolumab, Fachinformation Opvido® 2015, Fachinformation Yervoy® 2015). Genauso wie Nivolumab und Ipilimumab ist Pembrolizumab indiziert zur Monotherapie eines fortgeschrittenen (nicht resezierbaren oder metastasierenden) Melanoms. Keytruda® ist ein Konzentrat zur Herstellung einer Infusionslösung, wobei es nach Rekonstitution als Infusion über 30 Minuten in einer Dosierung von 2mg/kg Körpergewicht alle drei Wochen bis zum Fortschreiten der Erkrankung verabreicht wird (Fachinformation Keytruda® 2015). Arzneistoff FAM Markteinführung Deutschland Art des Antikörpers Wirkmechanismus Target Ipilimumab Yervoy® 2011 Human IgG1 Anti-CTLA4-Antikörpe, CTLA-4-Protein auf TZell-Oberfläche r Nivolumab Opvido® 2015 Human IgG4 Anti-PD-1-Antikörper, PD-1-Rezeptor auf TZell-Oberfläche Pembrolizumab Keytruda® 2015 Humanisiert IgG4 Anti-PD-1-Antikörper, PD-1-Rezeptor auf TZell-Oberfläche Tabelle 1: Monoklonale Antikörper als Checkpoint-Inhibitoren zur Therapie des fortgeschrittenen Melanoms CTLA-4: humanes zytotoxisches T-Lymphozyten-Antigen 4 PD-1: Programmed Death Receptor 1 Eine Gegenüberstellung der monoklonalen Antikörper, die als „Immuntherapeutika“ zur Therapie des Melanoms eingesetzt werden, ist in Tabelle 1 gegeben. Pembrolizumab ist ein humanisierter monoklonaler Antikörper vom IgG4-Isotyp, der eine stabilisierende Sequenzänderung in der Fc-Region enthält. Die Herstellung erfolgt rekombinant in Ovarialzellen des chinesischen Hamsters (CHO-Zellen). (Fachinformation Keytruda® 2015). Das Target sowohl von Pembrolizumab als auch von dem im Juli eingeführten Nivolumab ist der Programmed Death Receptor-1 (PD1), der auf der Oberfläche von T-Zellen exprimiert wird. Beide Antikörper binden mit hoher Affinität an den PD-1-Rezeptor und blockieren damit die Bindungsstelle für die physiologischen Liganden des PD-1, nämlich PD-L1 und PD-L2 (s. Abbildung 1B). Die beiden Liganden PD-L1 und PD-L2 werden nicht nur auf der Oberfläche Antigenpräsentierender Zellen sondern auch vermehrt auf der Oberfläche von Tumorzellen exprimiert. Die Bindung von PD-L1 oder PD-L2 an den PD-1-Rezeptor der T-Zelle führt zu einer Hemmung der T-Zelle, insbesondere einer Hemmung der TZellaktivierung, der T-Zellproliferation und einer verminderten Zytokinausschüttung. 1 CA 14.9.2015 Pharmazeutische Chemie - Pembrolizumab Somit besitzt PD-1 quasi die Eigenschaften eines „physiologischen Immunsuppressivums“. Wird nun durch Pembrolizumab bzw. Nivolumab der PD-1Rezeptor blockiert, unterbleibt das inhibitorische Signal an die T-Zelle (s. Abbildung 1A), die Hemmung der Immunantwort findet nicht statt, vielmehr kommt es zu einer Potenzierung der T-Zellreaktion inklusive einer Tumorabwehrreaktion (Mamalis et al. 2014, Momtaz und Postow 2014, Kyi und Postow 2014). Abbildung 1: Wirkmechanismus der anti-PD-1-Antikörper Pembrolizumab und Nivolumab Literatur: Fachinformation Keytruda® 2015, Merck Sharp & Dohme Limited Fachinformation Opvido® 2015, Bristol-Myers Squibb Pharma EEIG Fachinformation YERVOY® 2015, Bristol-Myers Squibb Pharma EEIG Kyi, C. und Postow, M.A. FEBS Letters 2014, 588, 368 Mamalis, A. et al. Arch Dermatol Res 2014, 306, 511 Momtaz, P. und Postow, M.A. Pharmgenomics Pers Med. 2014, 7, 357 2 CA 14.9.2015











