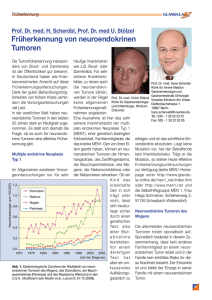
Was sind neuroendokrine Tumoren?
Werbung

Netzwerk Neuroendokrine Tumoren (NeT) e.V. Heft 7-2006 www.karzinoid.info www.neuroendokrine-tumoren.de Aus dem Inhalt Publik ● Gründungsversammlung des Netzwerks Neuroendokrine Tumoren (NeT) e.V. ● Einladung zum 3. Überregionalen Neuroendokrinen Tumor-Tag in Mainz ● Gründung der Regionalgruppen Rhein-Main und Lübeck ● Bericht vom Patiententreffen in Erlangen ● Die Regionalgruppe München informiert Übersicht ● Was sind neuroendokrine Tumoren? Übersicht zur Klassifikation, Diagnostik und Therapie Veranstaltungen ● Treffen der MEN-1-Gruppe in Heidelberg ● 2. Jahrestagung der ENETS in Krakau ● 2. Überregionaler Neuroendokriner Tumor-Tag in Nürnberg Diagnostik ● Diagnostik bei neuroendokrinen Tumoren ● Nuklearmedizinische Bildgebung bei neuroendokrinen Tumoren ● Die Nuklearmedizinische Klinik des Universitätsklinikums Erlangen stellt sich vor Behandlungsmöglichkeiten ● Medikamentöse Therapie bei neuroendokrinen Tumoren ● Lokale Therapieverfahren bei Lebermetastasen neuroendokriner Tumoren ● Angiogenese-Inhibitoren, neue Somatostatinanaloga und andere neue Behandlungsoptionen Verlaufsbeurteilung ● Bedeutung von Chromogranin A als Tumormarker NET-Zentren stellen sich vor ● Schwerpunkt Endokrinologie und Stoffwechselerkrankungen im Klinikum der Johannes Gutenberg Universität Mainz ● Insulinom & GEP-Tumor-Zentrum Neuss – Düsseldorf (GEP-TuZ) Leserbriefe Editorial Liebe Leserinnen, liebe Leser, vor Ihnen liegt die 7. Ausgabe der Glandula NeT für Patienten mit neuroendokrinen Tumoren (Karzinoiden). Wir sind recht froh, dass es uns nach einer kleinen schöpferischen Pause und einer Vereinsgründung wieder gelungen ist, ein neues Heft in guter Qualität und mit vielen wichtigen Informationen zusammenzustellen. Wir bedanken uns insbesondere bei den Referenten aus verschiedenen NeT-Zentren in Deutschland, die uns bei der Erstellung dieser Glandula NeT unterstützt haben. Natürlich kann und soll die Glandula NeT eine kompetente ärztliche Beratung vor Ort nicht ersetzen, aber sie kann Betroffenen eine Orientierung und Anhaltspunkte geben für das ärztliche Beratungsgespräch und Ausgangspunkt für eine intensivere Beschäftigung mit dem Thema sein. Auch den Dialog unter Betroffenen kann die Glandula NeT nicht ersetzen. Vor allem Gespräche untereinander in der Selbsthilfegruppe geben moralische Unterstützung und liefern Hintergrundinformationen über die verschiedenen Behandlungsmöglichkeiten und individuelle Erfolge. Viele auf den ersten Blick neu, innovativ und erfolgreich erscheinende Therapien entpuppen sich auf den zweiten Blick als wenig untersucht und erweisen sich manchmal auch als Schnellschuss. Der Vorstand des Netzwerks Neuroendokrine Tumoren wünscht Ihnen bei der Lektüre dieser Zeitschrift viele neue Erkenntnisse und Hilfen bei der Einschätzung der Verfahren. Bitte nutzen Sie auch die persönliche Arbeit in den Regionalgruppen und merken Sie sich in Ihrem Kalender den nächsten Neuro­endokrinen Tumor-Tag vor, der dieses Mal im November in Mainz stattfinden wird. Wir möchten Sie ermuntern, uns Beiträge für die nächste Ausgabe der Glandula NeT zukommen zu lassen, und würden uns sehr freuen, weitere Mitglieder für das Netzwerk Neuroendokrine Tumoren e.V. mit Sitz in Erlangen zu gewinnen! Prof. Dr. Johannes Hensen, Hannover Herausgeber und Vorsitzender des wiss. Beirats Ingeborg Schäfer, Vorstandsmitglied Netzwerk Neuroendokrine Tumoren e.V. Priv.-Doz. Dr. Marianne Pavel, Erlangen Vorstandsmitglied und Mitglied des wiss. Beirats Rosemarie Oehme, Vorstandsmitglied Netzwerk Neuroendokrine Tumoren e.V. Martin Michael, Vorstandsmitglied Netzwerk Neuroendokrine Tumoren e.V. Publik Bericht von der Gründungsversammlung: Netzwerk Neuroendokrine Tumoren (NeT) e.V. Am 6. Juli 2005 wurde ein für die Netzwerkmitglieder, die unter neuroendokrinen Tumoren leiden, wichtiger Schritt vollzogen: Das bis dahin im Netzwerk Hypophysen-und Nebennierenerkrankungen e.V. integrierte Netzwerk Neuroendokrine Tumoren wurde zum eigenen Verein „Netzwerk Neuroendokrine Tumoren (NeT) e.V.“. Der Einladung zur Gründungsversammlung waren 24 Personen (Mitglieder, Angehörige, Gäste) gefolgt. Herr Allmendinger, Vorstand der NeT-Gruppe, schilderte einleitend die Entwicklung des Netzwerks NeT unter dem Dach des Vereins Netzwerk Hypophysen- und Nebennierenerkrankungen e.V. Anfangs waren es nur einige wenige, 2005 waren es bereits 143 Patienten mit neuroendokrinen Tumoren, die Mitglieder des Netzwerks sind. Um sie angemessen betreuen und ihren Interessen und Problemen besser gerecht werden zu können, sollte nun ein eigenständiger Verein gegründet werden. Das sind sie, die 16 Gründungsmitglieder des Vereins Netzwerk Neuroendokrine Tumoren (NeT). Abstimmung der Vereinssatzung Grundlage für diesen Verein ist eine eigene Satzung, deren insgesamt 20 Paragraphen vor ihrer „Absegnung“ durch die Gründungsmitglieder diskutiert und abgestimmt wurden. Im Paragraph 2 beispielsweise werden Zweck, Aufgaben und Gemeinnützigkeit des Vereins definiert (vgl. In- sert auf S. 3). Weitere Paragraphen regeln den Beginn und das Ende der Mitgliedschaft, die Mitgliedsbeiträge, die Wahl, Aufgaben, Zuständigkeiten und Amtszeit der Vereinsorgane (Vorstand, Mitgliederversammlung, medizinisch-wissenschaftlicher Beirat und Regionalgruppen) sowie die Zusammenarbeit mit anderen Vereinen. Mitglieder des Netzwerks NeT, die sich für Einzelheiten der Vereins- Der Vorstand des Netzwerks Neuroendokrine Tumoren (NeT) e.V. Ingeborg Schäfer, München Martin Michael, Fürth Rosemarie Oehme, Auerswalde Prof. Dr. med. Johannes Hensen, Klinikum Hannover Nordstadt Priv.-Doz. Dr. med. Marianne Pavel, Medizinische Klinik I, Universitätsklinikum Erlangen Publik Auszug aus der Satzung des Netzwerks Neuroendokrine Tumoren (NeT) e.V. § 2: Zweck, Aufgaben, Gemeinnützigkeit Abs. 1 Zweck des Vereins ist es, Abs. 1.a die medizinische Versorgung von Patienten mit Neuroendokrinen Tumoren (NeT) zu verbessern. Abs. 1.b Hilfe zur Selbsthilfe für Patienten mit Neuroendokrinen Tumoren (Karzinoiden) zu ermöglichen. Dabei sollen der Erfahrungsaustausch unter den Betroffenen und der Kontakt von Betroffenen, Ärzten und anderem medizinischem Fachpersonal sowohl bundesweit, international als auch regional gefördert werden. Abs. 1.c die Forschung auf dem Gebiet von Neuroendokrinen Tumoren (NeT) in tensiv zu unterstützen und, falls möglich, finanziell zu fördern. Abs. 1.d Informationsmaterial für Patienten, für deren Familien, für betroffene Institutionen (z.B. Krankenkassen, Ministerien), für die Öffentlichkeit, sowie für die behandelnden Ärzte und anderes medizinisches Fach personal zu sammeln, herzustellen und zu verbreiten. Hierbei sollen insbesondere Informationen über frühe Erkennung der Erkrankungen, Symptome der Erkrankungen, moderne therapeutische Möglichkeiten und neue Entwicklungen dargestellt werden. Abs. 1.e die Zusammenarbeit mit fachbezogenen Institutionen z.B. Kliniken, Ärzten, anderen Selbsthilfegruppen, Krankenkassen oder ähnlichen Einrichtungen zu pflegen und zu fördern, um die Situation von Betroffenen sowie behandelnden und forschenden Institutionen zu verbessern. Abs. 1.f Vorhaben zur Erforschung und besseren Behandlung von Patienten mit Neuroendokrinen Tumoren (NeT) zu fördern. Abs. 1.g Seminare und Weiterbildungsmaßnahmen für Betroffene und Ärzte zu fördern. Abs. 1.h Tätigkeit als überregionaler und bundesweit tätiger Verein (Dachver band) von „vor Ort“ aktiven Regionalgruppen. Abs. 2 Der Verein verfolgt ausschließlich und unmittelbar gemeinnützige Zwecke im Sinne des Abschnitts „Steuerbegünstigte Zwecke“ der Abgabenordnung. Abs. 3 Der Verein ist selbstlos tätig; er verfolgt nicht in erster Linie eigenwirtschaftliche Zwecke. Abs. 4 Die Mittel des Vereins dürfen nur für satzungsgemäße Zwecke verwendet werden. Die Mitglieder erhalten keine Zuwendungen aus den Mitteln des Vereins, ausgenommen übliche Erstattungen für Auslagen. Es darf keine Person durch Ausgaben, die dem Zweck des Vereins fremd sind, oder durch unverhältnismäßig hohe Vergütungen begünstigt werden. Abs. 5 Bei Auflösung oder Aufhebung des Vereins oder bei Wegfall seines bisherigen Zwecks fällt das Vermögen des Vereins an das Netzwerk Hypophysen- und Nebennierenerkrankungen e.V., der es unmittelbar und ausschließlich für gemeinnützige Zwecke zu verwenden hat. satzung interessieren, können die Satzung in der Geschäftsstelle in Erlangen anfordern. Bei der Festlegung der Satzung wurde außerdem vereinbart, dass die enge logistische und personelle Zusammenarbeit mit dem Netzwerk Hypophysen- und Nebennierenerkrankungen e.V. beibehalten wird und die Kostenaufteilung der beiden Vereine vertraglich geregelt werden soll. Für die MEN-1-Patienten gilt auf deren Wunsch folgende Vereinbarung: Sie bleiben vorläufig im Netzwerk Hypophysen- und Nebennierenerkrankungen e.V., erhalten aber alle Informationen des Netzwerks Neuroendokrine Tumoren (NeT) e.V. 16 Gründungsmitglieder wählen ihren Vorstand Schließlich war es dann so weit: Aus den Anwesenden erklärten sich 16 Personen bereit, Gründungsmitglieder des Vereins Netzwerk Neuroendokrine Tumoren (NeT) zu werden. Sie billigten einstimmig den Wortlaut der Satzung und beschlossen ebenso einstimmig, den Verein Netzwerk Neuroendokrine Tumoren zu gründen. In einer offenen Wahl wurden folgende Personen in den Vorstand gewählt: Von Seiten der Betroffenen: • Rosemarie Oehme • Ingeborg Schäfer • Martin Michael Von Seiten der Ärzte: • PD Dr. med. Marianne Pavel • Prof. Dr. med. J. Hensen Erste Aufgabe des neu gewählten Vorstands war es, Vorschläge für Publik den wissenschaftlichen Beirat zu sammeln. Von den Anwesenden stellten sich neben den Vorstandsmitgliedern Professor Hensen und Frau Dr. Pavel spontan auch Herr Prof. Dr. med. Matthias Weber und Herr PD Dr. med. Christoph Auernhammer zur Verfügung. Überregionaler Neuroendokriner Tumor-Tag Auf der Gründungsversammlung fasste der Vorstand den Beschluss, am 19. und 20. November 2005 in Nürnberg den 2. überregionalen Neuroendokrinen Tumor-Tag abzuhalten (Bericht auf Seite 20ff.). Prof. Dr. med. Matthias Weber wird die NeT-Veranstaltung 2006 in Mainz organisieren und Herr PD Dr. med. Christoph Auernhammer 2007 in München. Brigitte Söllner, Erlangen Mitgliederentwicklung im Netzwerk Neuroendokrine Tumoren (NeT) e.V. • 143 Mitglieder mit neuroendokrinen Tumoren sowie 48 Mitglieder mit MEN 1 waren bereits als Untergruppen im Netzwerk Hypophy sen- und Nebennierenerkrankungen e.V. ingegriert. • Davon sind 128 Mitglieder mit NET in den neuen Verein übergetreten, die MEN-1-Patienten sind dagegen im Netzwerk Hypophysen- und Nebennierenerkrankungen e.V. geblieben, 15 Mitglieder sind ausgeschieden. • Seit Vereinsgründung kamen bereits 40 neue Mitglieder dazu. • Insgesamt hat das Netzwerk Neuroendokrine Tumoren (NeT) e.V. derzeit 168 Mitglieder. Mit Rat und Tat für Sie da: Netzwerk-Geschäftsstelle in Erlangen Liebe Mitglieder und solche, die es werden wollen, Sie haben Fragen zur Mitgliedschaft oder zu Veranstaltungen? Sie suchen einen Ansprechpartner, mit dem Sie sich über Ihre Erkrankung austauschen können? Sie benötigen eine Broschüre über Ihre Erkrankung? Oder Sie haben eine wichtige Information, die Sie – z.B. über die Glandula NeT – auch den anderen Mitgliedern zukommen lassen wollen? Dann wenden Sie sich einfach an unsere Geschäftsstelle in Erlangen. Dort helfen Ihnen Frau Hummel und Frau Jalowski gerne weiter. Das Netzwerk-Büro ist besetzt: • Montag bis Freitag von 8.30 bis 11.45 Uhr • Dienstag und Donnerstag 13.00 bis 16.30 Uhr. In dieser Zeit sind wir telefonisch für Sie da unter der Nummer: 09131/81 50 46. Elisabeth Hummel Andrea Jalowski Wenn Sie uns außerhalb der Bürozeiten anrufen, können Sie uns eine Nachricht auf dem Anrufbeantworter hinterlassen. Wir rufen Sie dann gerne zurück. Sie können uns aber auch ein Fax oder eine E-Mail senden: • Fax: 09131/81 50 47 • E-Mail: [email protected] Unsere Postanschrift lautet: Netzwerk Neuroendokrine Tumoren (NeT) e.V. Waldstraße 34, 91054 Erlangen Publik ++ wichtiger termin +++ wichtiger termin +++ wichtiger termin +++ wichtiger termin +++ wichtiger termin +++ Liebe Leserinnen und Leser, bitte merken Sie sich schon heute den folgenden Termin vor: Von Freitag, den 24. bis Sonntag, den 26. November 2006 findet in Mainz der 3. Überregionale Neuroendokrine Tumor-Tag statt. Im Namen von Professor Mathias M. Weber und seinen Mitarbeiterinnen und Mitarbeitern vom Klinikum der Johannes Gutenberg Universität Mainz, die diese Veranstaltung für Sie organisieren und bereits mitten in den Vorbereitungen stecken, laden wir Sie ganz herzlich dazu ein. Viele interessante Vorträge und Gruppenaktivitäten warten auf Sie, außerdem besteht wie immer die Möglichkeit, sich mit Fragen direkt an die Kapazitäten auf dem Gebiet der neuroendokrinen Tumoren zu wenden und mit Betroffenen Erfahrungen auszutauschen. Nutzen Sie die Möglichkeit, mehr über Ihre – in der Regel sehr seltene – Erkrankung sowie die neuesten Behandlungsmöglichkeiten zu erfahren, gute Bekannte vom Netzwerk NeT zu treffen und neue Kontakte zu knüpfen! Alle Mitglieder des Netzwerks Neuroendokrine Tumoren (NeT) e.V. erhalten rechtzeitig per Post eine Einladung sowie das ausführliche Programm der Veranstaltung. Wie immer werden wir Ihnen auch Tipps zur Unterbringung geben. Für weitere Fragen wenden Sie sich bitte an die Netzwerk-Geschäftsstelle in Erlangen, Tel. 09131/ 81 50 46. Ihr Netzwerk-Team ++ wichtiger termin +++ wichtiger termin +++ wichtiger termin +++ wichtiger termin +++ wichtiger termin +++ Gründung der Regionalgruppe Rhein-Main des Netzwerks NeT e.V. Im Rahmen des 3. Überregionalen Neuroendokrinen Tumor-Tages, der vom 24. bis 26. November 2006 in Mainz stattfinden wird, soll eine „Regionalgruppe Rhein-Main“ des Netzwerks NeT e.V. gegründet werden. Mit der Regionalgruppe soll für Patienten und Angehörige ein lokales Forum zum Gedanken- und Informationsaustausch geschaffen werden, um die Belange der Betroffenen wirksamer vertreten zu können. Bereits jetzt sind alle Interessierten herzlich eingeladen, sich aktiv an den Vorbereitungen und Planungen der Regionalgruppe Rhein-Main zu beteiligen! Als Ansprechpartner stehen Ihnen von ärztlicher Seite Herr Prof. Dr. med. M. M. Weber und Herr Dr. med. Christian Fottner gerne zur Verfügung, Kontaktadressen von Patienten können Sie bei der Netzwerk-Geschäfts­stelle erfragen. Über ein reges Inte­resse würden wir uns freuen. Ansprechpartner Netzwerk NeT e.V. – Regionalgruppe Rhein-Main Netzwerk NeT e.V. Prof. Dr. med. Matthias M. Weber Waldstraße 34 Dr. med. Christian Fottner 91054 Erlangen Schwerpunkt Endokrinologie und Stoffwechselerkrankungen Tel.: 09131/81 50 46 I. Medizinische Klinik und Poliklinik Klinikum der Johannes Gutenberg Universität Mainz Langenbeckstraße 1 55101 Mainz Tel.: 06131/17-7260 E-Mail.: [email protected] Publik Aufruf zur Gründung einer Regionalgruppe in Lübeck Nach unseren guten Erfahrungen mit der Gründung der lokalen Selbsthilfegruppe „Lebenshaus e. V.“ für GIST-Patienten im Juni 2005 möchten wir dieses unseren Patienten mit neuroendokrinen Tumoren ebenfalls anbieten. Die bisherige Arbeit und Vernetzung, die das Netzwerk Neuroendokrine Tumoren geleistet hat, sind sehr überzeugend. Die Klinik für Chirurgie am Universitätsklinikum Schleswig-Holstein (UKSH), Campus Lübeck, Chefarzt Prof. Dr. med. Hans-Peter Bruch, ruft daher auf zur Gründung einer Regionalgruppe des Netzwerks NeT. Seit Februar 2006 bieten wir eine Sondersprechstunde für Patienten mit neuroendokrinen Tumoren an. Alle Patienten, die in unserer Klinik mit dieser Diagnose operiert wurden und werden, werden systematisch erfasst und zur Nachsorge einbestellt. Über die chirurgische Poliklinik wird die Nachsorge koordiniert und in enger Zusammenarbeit mit der Gastroenterologie (Prof. Ludwig), der Onkologie (Prof. Wagner) und Endokrinologie (Prof. Kern) durchgeführt. Besondere Fälle werden im interdisziplinären Tumorkolloquium gemeinsam mit den Radiologen (Prof. Helmberger), Nuklearmedizinern (Prof. Bähre) und Pathologen (Prof. Feller) besprochen. Seit 2005 ist unsere Klinik dem nationalen NET-Register angeschlossen. Das heißt, die Daten unserer Patienten werden, falls das Einverständnis vorliegt, in anonymisierter Form zentral ausgewertet. Wir erhoffen uns darüber baldigst neue Erkenntnisse zu dieser seltenen und vielseitigen Erkrankung. Mit der Gründung einer Selbsthilfegruppe möchten wir den Dialog und Diskurs unter Medizinern in dieser Region anregen und die Betreuung unserer Patienten verbessern. Voraussichtlich wird im November das Erste Lübecker NET-Symposium für Ärzte und Pflegepersonal angeboten werden. Die Gründung der Selbsthilfegruppe soll in ein Arzt-Patienten-Seminar am Klinikum eingebettet werden. Der Termin dafür wird noch festgelegt und kann telefonisch erfragt werden. Patienten und Angehörige, die in der Regionalgruppe mitarbeiten möchten, erhalten weitere Informationen bei: Dr. med. Nehara Begum Assistenzärztin Klinik für Chirurgie UKSH, Campus Lübeck Ratzeburger Allee 160 23538 Lübeck Sekretariat Prof. Bruch: Tel. 0451/5 00 20 01 Chirurgische Poliklinik: Tel. 0451/5 00 20 88 Kennen Sie schon unsere Jubiläums-CD? 10 Jahre Netzwerk Hypophysen- und Nebennierenerkrankungen e.V. waren Anlass für uns, eine Sammlung unserer Zeitschriften und Broschüren, die bis August 2004 erschienen sind, in Form einer CD herauszugeben. Auf dieser CD finden auch Patienten mit neuroendokrinen Tumoren wichtige Informationen: • Ausgaben 1 bis 5 der Glandula NeT • Broschüre „Karzinoid – Diagnose und Therapie“ • Broschüre „GEP-Tumoren“ • Broschüren „MEN 1“ und „MEN 2“ Die CD können Sie bei der Netzwerk-Geschäftsstelle in Erlangen bestellen. Für Mitglieder kostet sie 5,00 e, für Nichtmitglieder 10,00 e. Das Wichtigste in Kürze ... ...finden Sie in unserem Flyer Sie suchen Informationen über den neuen Verein Netzwerk Neuroendokrine Tumoren e.V.? Oder Sie haben anderen Betroffenen von diesem Verein erzählt und würden ihnen gerne eine „Gedächtnisstütze” mit auf den Weg geben? Kein Problem, denn für solche Zwecke haben wir einen Flyer, den Sie (in begrenzter Menge) in unserer Geschäftsstelle anfordern können. Publik Bericht vom Patiententreffen am 27.10.2005 in Erlangen Der Leiter der Regionalgruppe, Herr Allmendinger, machte nach der Begrüßung der wie immer zahlreich erschienenen Teilnehmer auf einige wichtige Termine aufmerksam, insbesondere auf den 2. Überregionalen Neuroendokrinen Tumor-Tag für Patienten, Angehörige, Interessierte und Ärzte, der vom 18. bis 20. November 2005 in Nürnberg stattfindet. Die dreitägige Veranstaltung hat folgende Schwerpunkte: • 18.11. Mitgliederversammlung für Netzwerkmitglieder, • 19.11. Fortbildungsveranstaltung einschließlich Workshops, • 20.11. Erfahrungsaustausch unter Patienten. Die Glandula NeT erscheint im Frühjahr 2006 und wird u. a. auch über den Neuroendokrinen TumorTag berichten. Antworten auf dringende Fragen Bis zum Eintreffen von Frau Dr. Pavel wurden Gepräche unter den Patienten geführt. Dabei stellte sich ein neuer Patient aus Hof vor und berichtete von seiner Erkrankung. Von Frau Dr. Pavel wollte er gern Näheres zur Höhe des Tumormarkers Chromogranin A wissen und erfuhr, dass der Chromogranin-AWert ziemlich schwankt, vor allem während der Chemotherapie, und dass dieser Tumormarker immer unter Kontrolle bleiben muss. (Die Frage nach Chromogranin A haben wir aufgenommen und bringen einen Beitrag dazu in dieser Glandula NeT; Sie finden ihn auf Seite 47f.; Anm. der Redaktion). Eine andere Frage betraf das Prostatakarzinom, bei dem auch Kar- zinoide auftreten können. Diese Diagnose bedeutet in der Regel eine schlechtere Prognose als beim „normalen” Prostatakarzinom. Da die Veranlagung für die Entwicklung von Tumoren anscheinend vererbt werden kann, besteht ein erhöhtes Risiko, an neuroendo­ krinen Tumoren zu erkranken, wenn in der Familie bereits vermehrt Tu­­morerkrankungen aufgetreten sind. Daher sollten die Angehörigen von Betroffenen unbedingt die üblichen Vorsorgeuntersuchun­ gen wahrnehmen: Darmuntersuchung und Mammographie alle 2 Jahre. Wenig differenzierte Karzinoide kommen nur bei 5–10 % der Patienten mit neuroendokrinen Tumoren vor und es gibt kaum einen Austausch zwischen den Betroffenen. Daher soll ein Aufruf in der Glandula NeT abgedruckt werden, um eine Gesprächsgruppe zu bilden (siehe Rubrik Leserbriefe, Seite 55). Studienergebnisse aus den USA Abschließend berichtete Frau Dr. Pavel über Studien zu neuroendokrinen Tumoren aus Amerika (Einzelheiten dazu erfahren Sie im Beitrag von Frau Dr. Pavel auf Seite 43ff.). In den USA können aufgrund des großen Patientenpotenzials größere Studien durchgeführt werden und die Ergebnisse liegen nach kürzerer Zeit vor als in Deutschland. Während in den USA jetzt schon eine Datenbank über neuroendokrine Tumoren existiert, gibt es in Deutschland bislang nur ein Register zu diesen Erkrankungen. Zum Schluss bedankt sich Herr Allmendinger bei Frau Dr. Pavel für die wertvollen Ausführungen sowie bei Frau Hummel und bei Frau Jalowski für die gute Betreuung. Rosemarie Oehme, Auerswalde Termine der Regionalgruppe Erlangen Wir laden Sie herzlich ein, an unseren Patiententreffen in Erlangen teilzunehmen. Bitte merken Sie sich die folgenden Termine vor: • Donnerstag, 13.07.2006 • Donnerstag, 26.10.2006 • Donnerstag, 15.03.2007 • Donnerstag, 21.06.2007 • Donnerstag, 25.10.2007 Beginn ist jeweils 18.00 Uhr. Veranstaltungsort: Nichtopera­ tives Zentrum der Universitätsklinik Erlangen, Ulmenweg 18. Den Besprechungsraum können Sie an der Information erfragen. Wie immer wird Frau PD Dr. med. Marianne Pavel an unseren Treffen teilnehmen und Ihre Fragen beantworten. Wir freuen uns auf Ihr Kommen! H.-D. Allmendinger, Hemmhofen Treffen der Regionalgruppe Erlangen am 30.3.2006 Publik Auf den wichtigsten Kongressen präsent ... ... ist das Netzwerk Neuroendokrine Tumoren e.V. mit seinem InfoStand, um unseren Verein bei Ärzten, medizinischem Fachpersonal und Patienten bekannt zu machen. Herr Allmendinger bedankte sich im Namen der Erlanger Gruppe bei Frau Dr. Pavel ganz herzlich für ihr Engagement. Unser Treffen in der Uniklinik in Erlangen war mit über 30 Teilnehmern sehr gut besucht, insbesondere hatten einige neu Betroffene den zum Teil weiten Weg nach Erlangen nicht gescheut. Herr Allmendinger gab zunächst organisatorische Dinge bekannt und gab dann weiter an Frau Priv.-Doz. Dr. Pavel, die unsere Fragen beantwortete. Von besonderem Interesse waren diesmal die folgenden Themen: • Radiorezeptor-Tumortherapie mit 90Yttrium-Somatostatinana loga • Wachstumshemmung der Ge fäßzellen als neue Therapie­ möglichkeit bei neuroendo krinen Tumoren • Misteltherapie • Ergebnisse aktueller Studien Die Erläuterungen waren sehr gut verständlich und aufschlussreich und wurden durch Diskussionen innerhalb der Gruppe noch vertieft. Abschließend regte Herr Allmendinger an, dass die Gruppenmitglieder ihre Erfahrungen in einem Beitrag für die Glandula NeT niederschreiben und die sie bewegenden Fragen oder Probleme in einem Leserbrief an alle Netzwerk-NeT-Mitglieder richten sollten. Rosemarie Oehme, Auerswalde Professor Hensen (links) nutzte die Vortragspause auf dem DGEKongress für eine Visite am Info-Stand des Netzwerks NeT, an dem unser Vorstandsmitglied Frau Schäfer den interessierten Besuchern unermüdlich Rede und Antwort stand. Unterstützt wurde sie dabei von ihrem Mann (Mitte). So auch auf dem 50. Symposion der Deutschen Gesellschaft für Endokrinologie, das vom 1. bis 4. März 2006 in Essen stattfand. Das Interesse der Ärzte und Endokrinologie-Assistentinnen an unserem Verein, den Informationsbroschüren und der Glandula NeT war sehr groß. Es fanden zahlreiche Kontakte und gute Gespräche statt, in denen klar wurde, wie wichtig das Netzwerk NeT auch für die Zusammenarbeit zwischen Ärzten und Patienten ist. Schon 3 Wochen später baute Frau Schäfer den Info-Stand in Berlin auf, denn dort fand vom 22. bis 26. März 2006 der 27. Deutsche Krebskongress statt. Unterstützt wurde sie diesmal vom Vorstandsmitglied Herrn Martin Michael. Auch in Berlin ergab sich So präsentierte sich unser Netzwerkeine Vielzahl interessanter Ge- NeT-Stand auf dem Krebskongress in spräche und wichtiger Kontakte, Berlin. zum einen zu Ärzten, die auf neuroendokrine Tumoren spezialisiert sind, und zum anderen zu anderen Patientenorganisationen, mit denen wertvolle Tipps zur Vereinsarbeit ausgetauscht wurden. Vom 22. bis 26. April wird Frau Schäfer das Netzwerk NeT auf dem 112. Kongress der Deutschen Gesellschaft für Innere Medizin in Wiesbaden vertreten und nach einer kleinen Verschnaufpause vom 13. bis 16. September auf der 61. Jahrestagung der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten (DGVS). B. S. Publik Die Regionalgruppe München informiert Seit ihrer Gründung im Jahr 2003 trifft sich die Regionalgruppe München regelmäßig im Klinikum der Universität München – Großhadern. Ärztlicherseits wird die Gruppe von Frau PD Dr. Spitzweg und Herrn PD Dr. Auernhammer betreut. Auf dem letzten Treffen am 24.11.2005 berichtete Herr Dr. Auernhammer ausführlich über den 2. überregionalen Neuroendokrinen Tumor-Tag vom 19. bis 20.11.2005 in Nürnberg, so dass auch die Patienten und Angehörigen, die nicht an dieser Veranstaltung teilnehmen konnten, gut über die referierten Themen informiert sind. Anschließend gab es – wie immer – ausreichend Gelegenheit zum Erfahrungsaustausch und zur Diskussion. Auch für 2006 sind wieder zwei Treffen der Regionalgruppe München geplant. Sie finden statt am: • Donnerstag, den 11.05.2006, 19.00 Uhr • Thema: Neues vom Jahrestreffen 2006 der European Neuroendocrine Tumor Society (ENETS) Donnerstag, den 09.11.2006, 19.00 Uhr Thema: Vorstellung der Interdisziplinären Tumor- sprechstunde und Fallkonferenz für Neuroendokrine Tumoren am Klinikum Großhadern Veranstaltungsort: Klinikum der Universität München – Großhadern, Marchioninistraße 15, 81377 München, Konferenzraum G12 (1. Stock bis FG, dann bei FG rechts Aufzug zum 12. Stock). Wir bitten um zahlreiche Teilnahme und freuen uns auf Ihr Kommen! Ansprechpartner aus dem Patientenkreis der Region, die Ihnen weitergehende Informationen geben können, erfragen Sie bitte im Netzwerkbüro in Erlangen. Ingeborg Schäfer Was ist eigentlich Hyperthermie? Am 7. Oktober 2005 war die Regionalgruppe Erlangen der Einladung von Herrn Dr. Birkenhaken nach Nürnberg ins Klinikum Nord gefolgt, um sich über das Thema „Hyperthermie” zu informieren. Wir haben die wichtigsten Aspekte für Sie notiert. Bei der Hyperthermie (= Überwärmung) wird in bestimmten Kärperarealen durch Energiezufuhr eine Temperatur von 40–44°C herbeigeführt, die je nach Indikation 1–2 Stunden aufrechterhalten wird. Das Verfahren beruht auf einer Beobachtung aus dem Jahr 1866: Ein Patient hatte einen Weichteiltumor und litt unter einem hochfieberhaften Infekt. Nach Abklingen der Infektion ist auch der Tumor verschwunden. Methodik Heute wird die Temperaturerhöhung nicht mehr durch Erzeugung von Fieber, sondern durch Ultraschall, elektromagnetische Wellen oder Infusion einer erwärmten Flüssigkeit erreicht. Man unterscheidet verschiedene Therapieformen: • Bei der lokalen Hyperthermie werden dicht unter der Haut liegende Tumoren gezielt mit Ultraschall, Radio- oder Mikrowellen bestrahlt. • Bei der regionalen Hyperthermie werden größere Körperregionen durch elektromagnetische Wellen erwärmt, die von einer ringförmigen Strahlungsquellen ausgehen. • Bei der Ganzkörperhyperthermie wird die Körpertemperatur z.B. mit Infrarotstrahlen auf 41–42°C erhöht. Meist werden 1–2 Behandlungen pro Woche über einen Zeitraum von 10 Wochen durchgeführt. bilisierender Effekt ein. Die zelleigene Reparatur der Strahlenschäden wird vermindert und es kann eine geringere Strahlendosis gewählt werden. Bei Überwärmung ist eine bis zu fünffach gesteigerte Wirksamkeit der Strahlen zu erreichen. Erwärmte Zellen reagieren auch sensibler auf Chemotherapeutika. Außerdem steigert die Überwärmung die Durchblutung der Tumoren, so dass eine größere Menge der Medikamente ihr Ziel erreicht. Die erhöhte Durchblutung führt ebenfalls zu einer besseren Sauerstoffversorgung im Tumor, was wiederum den Effekt einer Strahlentherapie verstärkt. Wirkungsweise Die Hyperthermie wird ergänzend zu Chirurgie, Chemotherapie und Immuntherapie sowie Strahlentherapie eingesetzt, um den Therapieeffekt zu verstärken. Als alleinige Therapiemaßnahme ist sie nicht geeignet. Ihre Wirkung hängt von der erreichten Temperatur ab: Ab 42,5 °C wirkt sie direkt zellabtötend. Bei Temperaturen von 40–41,2 °C tritt ein strahlensensi- Anwendung bei neuroendokrinen Tumoren? Bei Lebermetastasen kann die Hyperthermie in Kombination mit der Chemotherapie angewendet werden, die Kombination mit der Strahlentherapie ist nicht ratsam. Die Hyperthermie ist keine Standardmethode und es handelt sich immer um einen individuellen Heilversuch, weil auch die Belastungsgrenze individuell ist. Übersicht Was sind neuroendokrine Tumoren? Übersicht zur Klassifikation, Diagnostik und Therapie Neuroendokrine Tumoren (NET) sind selten: Pro Jahr beträgt die Zahl der Neuerkrankungsfälle (Inzidenz) nur 0,5–2,0 pro 100.000 Einwohner. NET haben ihren Ursprung im diffusen neuroendokrinen Zellsystem. Diese Zellen haben die Veranlagung zur Amin- und Peptidhormonsynthese. Im Tumorgewebe lassen sich verschiedene Peptidhormone und Amine (wie Serotonin) nachweisen. Jedoch schütten nicht alle dieser Tumoren diese Botenstoffe in die Blutbahn aus, so dass wir funktionell aktive NET von funktionell inaktiven NET unterscheiden. Wichtig für die Diagnose von funktionell aktiven NET ist, dass die Ausschüttung eines speziellen Botenstoffs zu einem bestimmten klinischen Beschwerdebild (Syndrom) führt. Die Tumoren sind insgesamt sehr unterschiedlich, nicht nur was ihre Lokalisation im Körper und die Fähigkeit zur Ausschüttung von Botenstoffen in die Blutbahn angeht, sondern auch ihr Wachstumsverhalten und die damit verbundene Prognose der Erkrankung. Statt „Karzinoid“ jetzt „neuroendokriner Tumor“ Es existiert eine begriffliche Vielfalt, diese Tumoren zu benennen. Auch hat es einen Wandel in der Begriffsbestimmung in den letzten Jahren gegeben. Früher wurden neuroendokrine Tumoren als „Karzinoide“ bezeichnet. Diesen Begriff findet man auch heute noch in der Literatur. Er wurde geprägt von dem Pathologen Oberndorfer im Jahr 1907 10 für Tumoren des Darms mit sehr langsamem Wachstum, die sich weniger aggressiv als die gewöhnlichen Karzinome verhalten. Nachdem „Karzinoide“ nicht nur im Dünndarm, sondern auch an anderen Stellen im Körper beschrieben wurden, wurden diese nach embryogenetischen Gesichtspunkten eingeteilt in „Vorderdarmkarzinoide“ (Lunge, Magen, Zwölffingerdarm [Duodenum], oberer Leerdarm [Jejunum], Bauchspeicheldrüse), „Mitteldarmkarzinoide“ (hinteres Jeju­num, Krummdarm [Ileum], Blind­ darm [Appendix], Anfangsteil des Dickdarms [Zökum]) und „Hinterdarmkarzinoide“ (Grimmdarm [Kolon] und Enddarm [Rektum]). Diese Einteilung erwies sich als zu ungenau für die Unterscheidung biologisch relevanter Tumorentitäten. Neuroendokrine Tumoren wurden jahrzehntelang als relativ homogene Gruppe betrachtet. Wir wissen jedoch heute, dass diese Tumoren sich sehr unterschiedlich verhalten je nach ihrem Ursprung in verschiedenen Organen (z.B. Lunge, Magen, Pankreas oder Dünndarm), ihrer feingeweblichen Struktur und ihrer Veranlagung, Hormone in die Blutbahn auszuschütten. Der Begriff des „Karzinoids“ reicht nicht mehr aus, um dem gesamten morphologischen und biologischen Spektrum dieser Tumoren gerecht zu werden. In der Klassifikation der WHO von 2000 wird daher statt des Begriffs des „Karzinoids“ der übergeordnete Begriff des „neuroendokrinen Tumors“ und „neuroendokrinen Karzinoms“ benutzt. Priv.-Doz. Dr. med. Marianne Pavel, Medizinische Klinik 1, Universitätsklinikum Erlangen Heute verbindlich – die NETKlassifikation der WHO In der NET-Klassifikation der WHO werden je nach Lage sowie basierend auf morphologischen und biologischen Kriterien folgende Tumoren unterschieden: • NET mit benignem (gutartigem) Verhalten, • NET mit fraglicher Dignität (gutoder bösartig), • NET mit niedrig-malignem Verhalten und • NET mit hoch-malignem (bösartigem) Verhalten. Dabei sind die Tumorgröße, die Tumorausdehnung und das Wachstum in die Umgebung, das Vorhandensein von Metastasen sowie die Anzahl der sich teilenden Zellen im Tumorgewebe (Proliferationsindex) von großer Bedeutung. Wenn die Tumoren eine bestimmte Größe überschreiten, führen sie mit wenigen Ausnahmen zu Absiedlungen, vor allem in der Leber. Oft ist die Leber von vielen Metastasen durchsetzt. Das Wachstum der Metastasen kann, wie oben beschrieben, sehr unterschiedlich sein. Die Prognose der Erkrankung wird vor allem vom Wachstum der Lebermetastasen bestimmt (Abb. 1). Übersicht Einteilung in funktionell aktive und inaktive Tumoren Die Einteilung in funktionell aktive und inaktive Tumoren hat unverändert Bedeutung, da diese Tumoren sich klinisch unterscheiden und zum Teil unterschiedliche Therapien erfordern. Bronchopulmonales System andere Funktionell inaktive Tumoren Leber Etwa 50 % der NET verhalten sich funktionell inaktiv. Sie fallen durch unspezifische Beschwerden wie Bauchschmerzen, Gewichtsverlust oder Gelbsucht auf oder werden zufällig bei einer bildgebenden Untersuchung aus anderem Grund entdeckt. Pankreas Magen Dünndarm Kolon Rektum 75 – 80% Abbildung 1: Lokalisationen von neuroendokrinen Tumoren. In der Leber finden sich häufig Absiedlungen (Metastasen) der Primärtumoren. Neuroendokrine Tumoren: Funktionelle Aktivität Funktionell aktive Tumoren Die funktionell aktiven Tumoren gehen mit charakteristischen Beschwerden einher. Je nachdem, ob sie in der Bauchspeicheldrüse lokalisiert sind oder im Darm, rufen sie unterschiedliche Krankheitsbilder hervor (Abb. 2). Von den funktionell aktiven Bauchspeicheldrüsentumoren sind das Insulinom und das Gastrinom die häufigsten Tumoren. Alle anderen Tumoren sind äußerst selten. • Führendes Symptom beim Insulinom sind die durch die Unterzuckerung hervorgerufenen vegetativen Symptome, verbunden mit Heißhungergefühl und prompter Besserung auf Glukosegabe. Im Vordergrund stehen oft Störungen des zentralen Nervensystems (Kopfschmerzen, Sehstörungen, Koordinationsstörungen bis hin zu Persönlichkeitsveränderungen). • Beim Gastrinom, auch ZollingerEllison-Syndrom genannt, treten NET des GI-Traktes (Karzinoide) funktionell aktiv Endokrine Pankreastumoren (EPT) funktionell aktiv nicht funktionell aktiv Karzinoid-Syndrom: Serotonin nicht funktionell aktiv Insulinom Gastrinom VIPom Glukagonom Somatostatinom Magen Dünndarm Pankreas Dickdarm Abbildung 2: Funktionell aktive Tumoren führen je nachdem, ob sie in der Bauch­ speicheldrüse lokalisiert sind oder im Darm, zu unterschiedlichen Krankheitsbildern. wiederholt Magen- und Zwölffingerdarmgeschwüre auf, verbunden mit Bauchschmerzen, und häufig auch wässrigen Durchfällen. • Das VIPom ist gekennzeichnet durch massive wässrige Durchfälle, mit Flüssigkeitsverlusten bis 8 Liter pro Tag, körperlicher Schwäche, Kaliummangel und 11 Übersicht Muskelkrämpfen. Ursache ist die Bildung von vasoaktivem intestinalem Peptid (VIP) im Tumor. • Das Glukagonom fällt durch einen wandernden charakteristischen Hautausschlag auf (migratorisches Erythem), oft verbunden mit einem Diabetes mellitus. • Kennzeichen des Somatostatinoms sind Gallensteine, Diabe-­ tes mellitus und breiige Durch­ fälle. Die Bestimmung des entsprechenden Hormons in der Blutbahn bestätigt die Diagnose. Serotonin-produzierende Tumoren des Dünndarms, die Serotonin in relevanten Mengen in die Blutbahn ausschütten, rufen das Karzinoid-Syndrom hervor. Überwiegend sitzen diese Tumoren im Dünndarm, seltener im Dickdarm oder Magen. Das Karzinoid-Syndrom umfasst die Beschwerden Flush und Durchfälle, die bei 85–90 % der Patienten auftreten, und Asthmaanfälle bei bis zu 20 % der Patienten. Als Flush wird die anfallsartige Gesichtsrötung bezeichnet. Sie betrifft das Gesicht und die Halsregion und erstreckt sich gelegentlich auch auf den Oberkörper. Herzklopfen und Schweißausbrüche begleiten öfter einen Flush-Anfall, sehr selten sind ausgeprägte Kreislaufreaktionen bis zum Kollaps. Der Flush dauert in der Regel nur Sekunden bis wenige Minuten, kann jedoch zu bleibenden Gesichtsrötungen (Erythem/Teleangiektasien) führen. In der Regel tritt er erst bei Leberbeteiligung auf. Auslösende Faktoren sind Nahrungszufuhr, Alkohol, psychische Belastung, Untersuchung bzw. Druck im Bereich der Leber. Die Durchfälle sind öfter von krampfartigen Bauchschmerzen begleitet. 12 Karzinoid-Herzerkrankung Endokardfibrose - Herzklappen - Herzinnenwände Lokalisation - rechtes Herz / linkes Herz (40 / 13%) - links v.a. bei bronchialem Tumor z.B. Trikuspidalklappeninsuffizienz Pulmonalklappenstenose Klinisches Bild - Herzrhythmusstörungen - Herzinsuffizienz Abbildung 3: Als Spätfolge eines Karzinoid-Syndroms kann eine KarzinoidHerzerkrankung auftreten. Das klinische Bild ist sehr variabel und reicht von einigen breiigen Stühlen bis zu mehrfachen wässrigen Entleerungen pro Tag. Relativ selten sind Asthmaanfälle, zum Teil werden diese durch Belastung hervorgerufen. Eine genaue Dokumentation der Beschwerden ist sinnvoll zur Verlaufsbeurteilung, da die Beschwerden durch intermittierende Hormonausschüttung oft von wechselndem Charakter sind. Nach heutiger Auffassung, die jedoch nicht als sicher gilt, wird der Flush durch gefäßaktive Stoffe, wie Kallikrein, Substanz P und Neuropeptid K verursacht. Die gleichen Hormone scheinen auch für die Atembeschwerden verantwortlich zu sein. Durchfälle werden auf Serotonin zurückgeführt. Serotonin scheint auch Ursache für die Schädigung der Herzklappen zu sein. Bauchschmerzen treten auf durch Darmverlegung, aber auch Sklerose der Darmgefäße, die durch Mediatoren (Botenstoffe) der Tumoren hervorgerufen wird. Eine Spätfolge des Karzinoid-Syndroms stellt die Karzinoid-Herz­ erkrankung dar. Etwa 25–50 % der Patienten mit Karzinoid-Syndrom weisen Veränderungen am Herzen auf (Abb. 3). Bei 90 % der Patienten führen plaqueartige Bindegewebsablagerungen zu einer verminderten Schlussfähigkeit der Trikuspidalklappe (Trikuspidalklappeninsuffizienz), bei 50 % der Patienten zu einer Verengung der Pulmonalklappe (Pulmonalklappenstenose) und bei 80 % zu einer leicht verminderten Schlussfähigkeit der Pulmonalklappe (Pulmonalklappeninsuffizienz). Ursächlich wird hier eine durch Serotonin induzierte Bindegewebsvermehrung (Fibrose) angesehen. Die Karzinoid-Herzerkrankung tritt spät im Verlauf der Erkrankung auf, ist dann jedoch häufig entscheidend für die Prognose. Eine akute Komplikation des Karzinoid-Syndroms stellt die krisenhafte Entwicklung der Symptome des Karzinoid-Syndroms (Karzinoid-Krise) durch massive Ausschüttung Übersicht von Botenstoffen aus dem Tumor dar. Es handelt sich um eine potenziell lebensbedrohliche Situation, die durch Blutdruckabfall, Kreislauf­ insuffizienz, Schwellungen von Gesicht und allgemeine Ödembildung, mitunter auch Asthmaanfälle oder anhaltende Engstellung der Atemwege gekennzeichnet ist. Auslösende Faktoren sind die Mobilisation des Tumors bei einer Operation und Druck auf den Tumor (bei der Untersuchung), daher muss immer eine entsprechende Vorbehandlung vor einer Anästhesie/OP erfolgen. Diagnose von neuroendokrinen Tumoren Die Diagnostik umfasst die Bestimmung von Hormonen und Mediatoren im Blut bzw. Urin, eine bildgebende Diagnostik zur Bestimmung der Tumorausdehnung und die histologische (feingewebliche) Aufarbeitung des Tumors nach erfolgter Operation oder nach Probenentnahme aus einer Lebermetastase. Laboruntersuchungen Zur Labordiagnostik von funktionell aktiven Tumoren gehören die Bestimmung des spezifischen Peptidhormons bei endokrin aktiven Pankreastumoren, wie Insulin, Gastrin, Glukagon oder anderen, und die Bestimmung der 5-Hydroxy­ indolessigsäure im 24-StundenUrin beim Karzinoid-Syndrom. Der bedeutendste allgemeine Tumormarker ist Chromogranin A, ein Glykoprotein, das in neuroendokrinen Tumorzellen synthetisiert, in sekretorischen Granula gespeichert und in die Blutbahn ausgeschüttet wird. Die Bestimmung von Chromogranin A hat insbesondere bei • Endokrine Pankreastumoren <1cm • Endosonographie • Ganzkörperscreening und Staging • “Octreoscan”(111Indium-DTPA-Octreotid): Verfahren der ersten Wahl • Routinebildgebung/Tumornachsorge • Sonographie der Leber • CT (+ Angiographie), MRT • Primariussuche und Staging (optional) • • • Positronemissionstomographie (PET) mit 11C-5 HTP oder 11C-L-dopa oder 18F-FDG SMS-R-PET: 68Gallium-DOTANOC-PET PET/CT • Skelettszintigraphie Tabelle 1: Bildgebende Diagnostik zum Nachweis von Primärtumor und Metastasen. Tumoren ohne funktionelle Aktivität Bedeutung. Chromogranin A wird bei mehr als 80 % der Patienten im Plasma erhöht gemessen und dient auch der Verlaufsbeurteilung der Tumorerkrankung. Die Höhe des Chromogranin-A-Spiegels variiert interindividuell stark, es besteht eine Korrelation zur Tumormasse. Nähere Informationen zur Bedeutung dieses Markers finden Sie im Beitrag auf Seite 47f. Sollte Chromogranin A nicht erhöht gemessen werden, so kann alternativ bei Tumoren der Bauchspeicheldrüse Pankreatisches Polypeptid (PP) oder Calcitonin und bei Tumoren des Bronchialsystems auch die Neuronspezifische Enolase (NSE) bestimmt werden. Bildgebende Untersuchungen Die Bildgebung vereint verschiedene Disziplinen: Radiologie (CT/ MRT), Endoskopie (endoskopischer Ultraschall) und Nuklearmedizin (So­ matostatin-Rezeptor-Szintigraphie, Positronenemissionstomographie (PET). Das bildgebende Verfahren der ersten Wahl zum Nachweis von Primärtumor und Metastasen ist die Somatostatin-Rezeptor-Szintigraphie (111In-Octreotid-Szintigraphie, Octreoscan) (Tab. 1). Das Verfahren stellt die in der Regel auf neuroendokrinen Tumoren in hoher Dichte vorhandene SomatostatinRezeptorsubtypen 2 und 5 dar und hat eine hohe Nachweisquote von 80–90 % (Ausnahme Insulinom). Die Untersuchung ermöglicht durch Ganzkörperdarstellung den gleichzeitigen Nachweis von Tumorabsiedlungen an unterschiedlichen Stellen im Körper, verbunden mit einer Aussage zu Therapiemöglichkeiten, wie dem Einsatz von Radionuklid-gekoppelten Somatostatinabkömmlingen. Bei positivem Octreotid-Szintigramm dienen MRT und CT der genaueren morphologischen Erfassung von Primärtumor und Lebermetastasen, die auch im Verlauf mit konventioneller Bildgebung beurteilt werden. Nur bei steigendem Tumormarker und stabilem Tumorbefund im Bereich der Leber oder Auftreten anderer Beschwerden, die eine Tumor­ absiedlung an Orten außerhalb der Leber wahrscheinlich machen, ist eine erneute Somatostatin-Rezep13 Übersicht tor-Szintigraphie in der Verlaufsbeurteilung des Tumors angemessen. Bei kleinen Tumoren der Bauchspeicheldrüse, z.B. Insulinomen und Pankreastumoren im Rahmen einer Multiplen Endokrinen Neoplasie Typ 1 (MEN 1), ist der endoskopische Ultraschall das Verfahren der ersten Wahl. Die Bildgebung wird erweitert und zum Teil verbessert durch den Einsatz der Positronenemissionstomographie unter Verwendung von verschiedenen Substanzen, die in der Tumorzelle verstoffwechselt wer­ den (z.B. 11C-5-Hydroxytryptophan, 18 F-L-dopa, 18F-FDG), auch in Kombination mit CT (PET-CT). Bei speziellen Fragestellungen kann der zusätzliche Einsatz dieser Methoden hilfreich sein (z.B. vor Operation mit dem Ziel der Tumorfreiheit). Histologische Untersuchung Die Diagnose wird letztendlich histologisch am Operationspräparat oder durch Untersuchung einer Probe aus einer Lebermetastase gesichert. Ein erfahrener Pathologe kann das lichtmikroskopische Bild bereits zuordnen, in der Regel werden Spezialfärbungen im Tumormaterial mit Nachweis von Chromogranin A und Synaptophysin (Membranbestandteil von kleinen Vesikeln in neuroendokrinen Tumorzellen) durchgeführt (siehe Abbildung auf S. 25). Bei Pankreastumoren mit funktioneller Aktivität erfolgt auch der Nachweis des spezifischen Peptids (z.B. Insulin oder Gastrin) im Tumormaterial. Therapeutische Möglichkeiten Das Ziel der Therapie ist zunächst die möglichst komplette chirur14 systemisch lokal Somatostatinanaloga Chemoembolisation Interferon-a Hochfrequenz-Thermotherapie Chemotherapie Laser-induzierte Thermotherapie Nuklearmedizinische Verfahren (Alkoholinjektion) (Kryokoagulation) Tabelle 2: Therapieverfahren bei neuroendokrinen Tumoren. gische Tumorentfernung mit dem Ziel einer Heilung des Tumorleidens. In vielen Fällen ist dies nicht möglich, da der Tumor sich bereits in die Lymphknoten oder die Leber ausgebreitet hat. Auch in diesen Fällen ist insbesondere bei funktionell aktiven Tumoren zu prüfen, ob ein Teil der Tumormasse, z.B. durch Leberteilresektion, entfernt werden kann, um das Ansprechen auf eine medikamentöse Behandlung zu verbessern. Die medikamentöse Behandlung hat bei funktionell aktiven Tumoren das Ziel, die durch Hormonausschüttung bedingten Beschwerden zu reduzieren, z.B. Flush, Durchfälle und Asthmaanfälle beim KarzinoidSyndrom, und möglichen Komplikationen vorzubeugen, wie Karzinoid-Krise und Karzinoid-Herzerkrankung. Das weitere Ziel der Behandlung ist die Hemmung des Tumorwachstums bei allen NET. Dazu stehen verschiedene Therapieansätze zur Verfügung (Tab. 2). Die längsten Erfahrungen bestehen zum Einsatz von Somatostatinanaloga (Octreotid, Lanreotid) und Interferon-a beim Karzinoid-Syndrom. Ergänzend werden lokale Therapieverfahren, wie Chemoembolisation, Hochfrequenzthermotherapie (HFTT) oder Laser-induzierte Thermotherapie (LITT) eingesetzt. Die systemische Chemotherapie hat Bedeutung bei wachsenden Pankreastumoren und schlecht differenzierten, schnell wachsenden Tumoren jeglicher Lokalisation. Die medikamentösen Therapieverfahren sind in den Beiträgen auf Seite 35ff. und 43ff. näher beschrieben. Das Spektrum der Therapie wird erweitert durch die Anwendung der Radiorezeptortherapie (Radionu­klid­ therapie) unter Verwendung von Radionukliden, die an Somatostatinanaloga gekoppelt sind, z.B. 90YDOTATOC oder 177Lu-DOTA-Tyr3octreotate. Voraussetzung für diese Therapie ist ein hoher Besatz von Somatostatin-Rezeptorsubtypen im Tumor. Tumorrückbildungen werden in ca. 30 % der Fälle, eine Wachstumsstabilisierung in ca. 40–50 % der Fälle erzielt. Es liegen jedoch bisher keine umfangreichen Daten zum Langzeitansprechen vor. Ebenso fehlt ein Vergleich dieser Methode mit anderen bereits etablierten Methoden. Die Therapie ist nach wie vor nicht zugelassen und liegt in der Verantwortung der einzelnen Zentren, die sie anbieten. Mit wenigen Ausnahmen stellt sie keine Erstlinientherapie dar. Eine Vereinheitlichung der Radionuklidtherapie in Deutschland wird angestrebt. Vorgehensweise Die Auswahl der Therapie ist individuell sehr verschieden. In der Regel Übersicht Verschiedene Therapiekonzepte Keine Hormonbildung Kein Wachstum Karzinoid-Syndrom Wachsender EPT Hochmaligner Tumor Operation Operation Chemotherapie Resttumor stabil Regress Somatostatinanaloga ggf. Operation anschließen Keine Therapie Interferon-alpha stabil Progress Embolisation/ Radionuklidtherapie Neue Therapieverfahren Keine Therapie Neue Therapieverfahren Abbildung 4: Das therapeutische Vorgehen richtet sich nach der individuellen Situation des Patienten. Patienten mit neuroendokrinen Tumoren Interdisziplinäre Betreuung Chirurgie Endokrinologie Gastroenterologie Radiologie Nuklearmedizin Individuelle Therapieoptimierung werden Patienten mit NET im Lauf ihrer Erkrankung verschiedenen Behandlungen zugeführt. Das Spektrum der Vorgehensweisen reicht von „Zuwarten ohne spezifische Therapie“ bei funktionell inaktiven Tumoren, die keine Wachstumstendenz zeigen, über Einsatz der Biotherapie, Somatostatinanaloga und/ oder Interferon-a beim KarzinoidSyndrom und ergänzende Chemoembolisation oder Radionuklidtherapie bei Tumorwachstum oder unzureichender Symptomkontrolle, bis zum Einsatz der systemischen Chemotherapie beim wachsenden Bauchspeicheldrüsentumor oder bei aggressivem Wachstum schlecht differenzierter neuroendokriner Karzinome (Abb. 4). Sollten diese Therapieverfahren ausgeschöpft sein, ergibt sich die Möglichkeit des Einsatzes neuer Therapiestrategien, die im Rahmen von klinischen Studien erfolgen oder als individueller Heilversuch unter Nutzung bereits für andere Tumorentitäten zugelassener Therapien (siehe Beitrag auf S. 43ff.). Interdisziplinäre Zusammenarbeit Wichtig ist die interdisziplinäre Betreuung der Patienten unter Einbeziehung eines erfahrenen Chirurgen, der Nuklearmedizin und Radiologie unter Führung des Patienten durch einen auf diesem Gebiet versierten Internisten, der dem Gebiet der Endokrinologie, Gastroenterologie oder Onkologie angehören kann. Diese interdisziplinäre Versorgung des Patienten ermöglicht eine optimierte individuelle Therapieplanung, die alle Facetten der Erkrankung berücksichtigt (Abb. 5). Verbesserung von Lebensqualität und Prognose Abbildung 5 Priv.-Doz. Dr. med. Marianne Pavel, Universitätsklinikum Erlangen 15 Veranstaltungen Treffen der MEN-1-Gruppe in Heidelberg Die Selbsthilfegruppe der Patienten mit multipler endokriner Neoplasie Typ 1 (MEN 1) traf sich parallel zum 9. überregionalen Hypophysenund Nebennieren-Tag in Heidelberg am 19. 9. 2005 zu einer eigenen Veranstaltung. 7 Betroffene bzw. An­ ge­hörige waren gekommen, um an der Fortbildung und dem anschließenden Gedankenaustausch teilzunehmen. Frau PD Dr. Karin Frank-Raue (endokrinologische und humangene­ tische Praxis, Heidelberg) und Herr PD Dr. Tobias Schilling (Med. Klinik I, Endokrinologie, Universität Heidelberg) erörterten die medizinischen Aspekte der Erkrankung: Grundlagen der Krankheitsentstehung, mögliche Organbeteiligung sowie Interventions- und Behandlungsmöglichkeiten. Im Folgenden soll nicht auf einzelnen Aspekte eingegangen werden, vielmehr sollen stichpunktartig einige markante Punkte und Fragengenannt werden, über die sich ein weiteres Nachdenken bzw. Besprechen mit den jeweiligen medizinischen Experten vor Ort lohnt. Entfernung von Nebenschilddrüsen und Thymus Wann ist der richtige Zeitpunkt für eine Nebenschilddrüsenoperation? Sollte eine Operation bereits bei einer leichten Kalziumerhöhung oder erst bei einem deutlich erhöhten Kalziumwert erfolgen? Wie ausgedehnt sollte der Eingriff vorgenommen werden? 16 Die Überfunktion der Nebenschilddrüse ist häufig das erste Krankheitszeichen im jungen Erwachsenenalter. Bei bekannter MEN1-Diagnose werden 3 1/2 der 4 Nebenschilddrüsen (Abb. 1) entfernt und nur ein kleiner Drüsenrest belassen (subtotale Nebenschilddrüsenentfernung). Oder alle Drüsen werden entnommen und ein ausreichendes Restdrüsengewebe in den Arm verpflanzt (Autotransplantation). Bei beiden Varianten wird außerdem eine so genannte zervikale Thymek- Rachen untere Schilddrüsenschlagader gemeinsame Halsschlagader Schilddrüse rechte Nebenschilddrüse rückläufiger Kehlkopfnerv Speiseröhre Susanne Werkmeister, Erlangen tomie durchgeführt. Dabei wird der Großteil der Thymusdrüse vom Hals aus entfernt, weil sich darin manchmal eine weitere Nebenschilddrüse befinden kann. Oft sind nach Jahren Wiederholungseingriffe wegen einer erneuten Nebenschildddrüsenüberfunktion notwendig. Diskussionspunkt in Heidelberg war, ob gerade im Hinblick auf mögliche bösartige neuroendokrine Tumoren des Thymus (Abb. 2), die sich manchmal entwickeln können, nicht sofort die gesamte Thymusdrüse entfernt werden sollte. Bei einigen der Teilnehmer war die Thymusdrüse bereits wegen bösartiger Veränderungen (Karzinoiden) komplett entfernt worden. Abbildung 1: Typische Lage der vier Nebenschilddrüsen an der Rückseite der Schilddrüse. Luftröhre Lunge Thymus Abbildung 2: Der Thymus, auch Bries genannt, liegt unmittelbar hinter dem Brustbein. Er wächst bis zur Pubertät, in der er seine größte Ausdehnung erreicht, und bildet sich danach kontinuierlich zurück.Beim alten Menschen ist er nur noch als kleiner Geweberest vorhanden. Der Thymus ist wesentlich am Aufbau und an der Prägung des Immunsystems beteiligt, indem er bestimmte weiße Blutkörperchen produziert. Später übernehmen die Lymphknoten, das Knochenmark und die Milz diese Funktion. Veranstaltungen Was tun bei Hyperprolaktinämie? Ab wann soll ein zu hoher Prolaktinspiegel (Hyperprolaktinämie) behandelt werden, insbesondere wenn kein Hypophysenadenom nachweisbar ist? Eine medikamentöse Therapie sollte hier erfolgen, wenn Beschwerden vorliegen. Eine leichte Prolaktinerhöhung ohne Tumor­nachweis muss nicht unbedingt behandelt werden. Prolaktinome können häufig gut medikamentös mit Prolaktinhemmern behandelt werden. Operationen kommen eher in Betracht bei Hypophysenade­nomen, die eine gewisse Größe überschreiten (>1 cm) und zu mechanischen Komplikationen führen. Beteiligung von Bauch­ speicheldrüse und Thymus Die Beteiligung der Bauchspeicheldrüse bzw. des Thymus ist nach Einschätzung der Referenten am schwierigsten zu „handhaben“, da Knoten in diesen Organen im Gegensatz zur Nebenschilddrüse und Hypophyse bösartig sein können oder eine unvorhersagbare bösartige Entwicklung nehmen können. Hinzu kommt, dass in Fachkreisen noch darüber diskutiert wird, wann bzw. ob operative Eingriffe beim Vorliegen von Tumoren in der Bauchspeicheldrüse oder im Verdauungstrakt sinnvoll sind und in welchem Fall bzw. wie lange eine beobachtende Haltung angebracht ist. Diesbezüglich liegen derzeit zu wenige und uneinheitliche Daten vor. Insbesondere darüber, ob frühzeitige operative Eingriffe bei bösartigen Tumoren wirklich zu einer Lebensverlängerung führen. Hier sollten Fragen nach der Buchtipp Die Multiple Endokrine Neoplasie Typ 1 4 ge fla u .A Ein Ratgeber für Patienten von der Deutschen MEN 1Datenbank Die Deutsche MEN 1-Datenbank hat zum Ziel, Daten zum Krankheitsbild der multiplen endokrinen Neoplasie Typ 1 (MEN 1) zu sammeln und auszuwerten. Die aus den anonym erhobenen Einzeldaten gewonnenen Erkenntnisse über den Verlauf dieser seltenen Erbkrankheit ermöglichen es, neue Konzepte für die Behandlung zu entwickeln. Die Informationsbroschüre der Datenbank gibt einen Überblick über den momentanen Erkenntnisstand und ist als Ratgeber für die Betroffenen und ihre Familien gedacht. Einleitend werden die typischen Beschwerden erläutert, die sich in Abhängigkeit vom jeweils erkrankten Organ entwickeln können. Ein ausführliches Kapitel ist der Diagnose und dem Gentest gewidmet, ein weiteres den therapeutischen Möglichkeiten. Außerdem werden häufige Fragen beantwortet und in einem kleinen Wörterbuch die im Zusammenhang mit der Erkrankung verwendeten Fachbegriffe erklärt. Den Ratgeber können Mitglieder des Netzwerks kostenlos über die Geschäftsstelle in Erlangen beziehen. B. S. Lebensqualität, die durch große Eingriffe beeinträchtigt werden kann, sorgfältig abgewogen werden. insbesondere Untersuchungs- und Behandlungsmaßnahmen betreffen, selbstverantwortlich in die Hand nehmen. Früherkennung und Verlauf Interna Einen großen Stellenwert zur Früherkennung der MEN 1 hat die molekulare Gendiagnostik. Denn durch eine Genuntersuchung können die betroffenen Familienangehörigen identifiziert und frühzeitig behandelt werden. Eine Vorhersage über die Ausprägung der Erkrankung beim einzelnen Patienten sowie zum individuellen Krankheitsverlauf ist jedoch nicht möglich. MEN 1 tritt selbst bei Familienmitgliedern, die alle die gleiche Veränderung im Erbmaterial aufweisen, in sehr unterschiedlicher Ausprägung und unterschiedlichem Schweregrad auf. Aufgrund der Komplexität der Erkrankung erscheint es ganz besonders wichtig, dass Patienten mit MEN 1 über ihre Erkrankung gut Bescheid wissen und die aktive Kommunikation mit ihren Ärzten suchen. Denn nur wenn sie ausreichend informiert sind, können sie notwendige Entscheidungen, die Über die rein medizinischen Informationen hinaus gab es einige organisatorische Dinge zu besprechen. Parallel zum Netzwerk Hypophysenund Nebennieren-Erkrankungen e.V. hat sich jetzt das Netzwerk Neuroendokrine Tumoren (NeT) e.V. als eigenständiger Verein gegründet. Da MEN-1-Betroffene von beiden Krankheitsgruppen betroffen sein können, steht nun die Entscheidung an, zu welchem Verein sich die MEN-1-Gruppe organisatorisch zuordnen möchte. Einigung bestand darüber, dass Mitglieder mit MEN 1 Informationen beider Vereine (z.B. Glandula und Glandula NeT) erhalten möchten. Die Treffen der MEN-1-Gruppe sollen auch in Zukunft einmal im Jahr erfolgen. Wann das nächste Treffen stattfindet, können Sie im Netzwerk-Büro erfragen. Susanne Werkmeister, Erlangen 17 Veranstaltungen 2. Jahrestagung der ENETS vom 20.–22.4.2005 in Krakau Neuroendokrine Tumoren zwischen Leitlinien und klinischer Praxis Unter der Schirmherrschaft des polnischen Staatspräsidenten Aleksander Kwasniewski tagte die European Neuroendocrine Tumor Society (ENETS) im vergangenen Jahr in Krakau. Rund 400 Ärztinnen und Ärzte diskutierten unter dem Vorsitz von Prof. Dr. Bertram Wiedenmann (Berlin) über den aktuellen Stand der Diagnostik und Therapie neuroendokriner Tumoren. Wir haben die wichtigsten Ergebnisse für Sie zusammengefasst. Entwicklung strukturierter Therapiestrategien Eine ENETS-Arbeitsgruppe hat im vergangenen Jahr, basierend auf internationalen Publikationen, „Leitlinien zur Diagnostik und Behandlung von neuroendokrinen gastrointestinalen Tumoren“ erarbeitet und in der Zeitschrift Neuroendocrinology veröffentlicht. Gegliedert sind die Leitlinien nach der Tumorlokalisation, wobei jedes Kapitel diagnostische Empfehlungen zum klinisch-pathologischen Staging, zur Bildgebung, biochemischen und histologischen Diagnostik sowie therapeutische Empfehlungen enthält, die alle in Frage kommenden Therapiemodalitäten einschließlich operativer Verfahren, biologischer Therapie, Chemoembolisation, Radiotherapie und Chemotherapie berücksichtigen. Tumormarker – wertvolle NETVerlaufsparameter Über Tumormarker, die bei NET zur Verlaufsbeobachtung herangezogen 18 werden, berichtete Prof. Kjell Öberg (Uppsala). Einer der wichtigsten ist das Chromogranin A (CgA). Bei den meisten NET ist die Serumkonzen­ tration von CgA erhöht. Bei Typ-3NET des Magens ist CgA der sensitivste biochemische Marker. Hochgradige CgA-Wert-Erhöhungen auf das 100- bis 1000fache gegenüber Normalwerten (<60 mg/l) findet man bei NET im Mitteldarmbereich. Exzessiv hohe Konzentrationen über 1000 mg/l sind mit einer ungünstigen Prognose assoziiert. Eine Behandlung mit Somatostatinanaloga senkt die CgA-Konzen­ trationen im Plasma, was aber nach Ansicht des Experten eher auf einer Hemmung der Hormonsynthese und -freisetzung als auf einem Rückgang der Tumormasse beruht. Deswegen sollten Veränderungen des Plasma-CgA mit Vorsicht interpretiert werden. Mit Fortschreiten der Tumorerkrankung unter Somatostatinanaloga können erhöhte CgA-Spiegel auf einen Verlust der sekretorischen Kontrolle oder auch auf erneutes Tumorwachstum hindeuten, unter Umständen zu einem Zeitpunkt, zu dem in der Bildgebung noch keine Progressionszeichen sichtbar sind. Ein weiterer wichtiger Marker ist das Serotonin (5-HT), wobei in der Praxis aber nur die Bestimmung des Serotonin-Metaboliten 5-Hydroxyindolessigsäure (5-HIES) im Urin brauchbar ist. Bei Patienten mit Pankreas-NET ist außerdem die Bestimmung von Peptidhormonspiegeln in Erwägung zu ziehen. NET des Magens und Zwölffingerdarms sind meist gutartig Gastrinome des Zwölffingerdarms sind viel seltener maligne, als viele Ärzte denken, darauf machte Prof. Robert Jensen (Maryland, USA) aufmerksam. Generell sind die meisten NET im oberen Magen-Darm-Trakt hoch differenziert, funktionell nicht aktiv und wachsen langsam. Viel seltener sind niedrig differenzierte und schnell wachsende kleinzellige endokrine Karzinome mit ungünstiger Prognose. Man unterscheidet bei NET des Magens zwischen den hoch differenzierten Typen 1 (etwa 80 % aller Fälle, kleine, meist benigne Tumoren), 2 (selten, meist gutartig) und 3 (etwa 15 % aller Fälle, >2 cm, infil­ tratives Wachstum, metastasierend) sowie niedrig differenzierten Tumoren. „Eine ablative Therapie ist bei Typ1-NET des Magens in der Regel nicht erforderlich und einmal jährliche endoskopische Kontrollen sind ausreichend“, erklärte PD Dr. Ursula Plöckinger (Berlin). Bei mehr als 6 Polypen >1 cm, Ausdehnung in die Muskularis oder Tumorrezidiven wird eine chirurgische Resektion oder Antrektomie Typ 1 empfohlen. „Bei maligner Entwicklung nach lokaler Resektion, bei Tumoren vom Typ 3 und niedrig differenzierten Tumoren ist eine partielle oder totale Gastrektomie (Magenentfernung) mit Lymphknotendissektion angezeigt“, empfahl Philippe Ruszniewski (Clichy/Frankreich). Eine zytoreduktive Veranstaltungen Therapie von Lebermetastasen mittels Radiofrequenz- oder Kryoablation kommt bei Typ-3-Tumoren und niedrig differenzierten NET in Frage. Die medikamentöse Therapie sollte bei Gastrin-produzierenden Tumoren Protonenpumpenhemmer einschließen. „Unter Somatostatinana­ loga wurden bei gastralen NET vom Typ 1 und 2 zwar Regressionen beobachtet, allerdings ist der Effekt begrenzt und bei asymptomatischen Tumoren sind die Substanzen nicht zu empfehlen,“ erklärte Ruszniewski. Der Nutzen von Interferon-a ist ungewiss, ein Therapieversuch ist bei streuenden Typ-2- und Typ-3Tumoren gerechtfertigt. Eine systemische Chemotherapie kommt nur bei metastasierenden Tumorerkrankungen in Frage. NET des Pankreas: Diagnose mittels Endosonographie und Biopsie Die Mehrzahl aller Pankreas-NET ist gut differenziert. Die beiden größten Fraktionen machen die Insulinome (40 % aller Pankreas-NET) und die funktionell inaktiven Tumoren aus (30–35 %). Die Lokalisations­ diagnostik insbesondere kleinerer Tumoren des Pankreas kann eine Herausforderung darstellen, wie Frau Professor Babro Eriksson (Uppsala) darlegte. Folgende diagnostische Verfahren kommen dafür in Frage: • Kontrastmittelverstärkte CT/MR/ Sonographie • Octreotidszintigraphie + SPECT • Endoskopische Sonographie • Intraoperative Sonographie • PET mit 11C-5-HTP, 18F-L-DOPA, 68 Ga-DOTA-Octreotid • In seltenen Fällen Angiographie oder Portalvenen-Sampling Verfahren Primärtumoren Metastasen Sonographie Computertomographie (CT) Magnetresonanztomographie (MRT) Somatostatin-Rezeptor-Szintigraphie (SRS) SRS (Insulinome) Endoskopische Sonographie Portalvenen-Sampling (Gastrinome) Sekretin, Kalzium (Insulinome) Intraoperative Sonographie <20 % 0 % (1 cm) 30 % (1–3 cm) 95 % (>3 cm) 50 % >60 % <50 % 75 % (auch kleine Tumoren) <70 % >80 % >75 % <50 % <50 % <50 % <50 % 80 % >90 % <50% Tabelle 1: Sensitivität verschiedener diagnostischer Verfahren in der Lokalisationsdiagnostik von endokrinen Pankreastumoren (nach Eriksson 2005). In Übereinstimmung mit den aktuellen ENETS-Leitlinien empfahl Professor Eriksson die Kombination aus endoskopischer Sonographie und Biopsie, die in erfahrenen Händen die sensitivste diagnostische Vorgehensweise ist. Die Vorteile der Octreotidszintigraphie bestehen darin, dass es sich dabei um eine nichtinvasive Ganzkörperuntersuchung handelt, die besonders auch für das Staging eines bereits identifizierten endokrinen Primärtumors geeignet ist und in 40 % der Fälle zu einer Anpassung des Behandlungsmanagements führt. Außerdem hat diese Methode einen prädiktiven Wert bezüglich einer Therapie mit Somatostatinanaloga. Die Sensitivität der Methode liegt in Bezug auf die Erkennung primärer Gastrinome bei 58 % und ist damit höher als die von Angiographie (28 %), MRT (30 %), CT (31 %) und Sonographie (9 %). Auch bezogen auf die Lokalisationsdiagnostik endokriner Pankreasprimärtumoren und -Metastasen besitzt die Somatostatin-RezeptorSzintigraphie (SRS) eine hohe Sensitivität (Tab. 1). Bei kleinen Tumoren allerdings und auch bei Tumoren, die keine Somatostatin-Rezeptoren exprimieren, ist sie von begrenztem Nutzen. Sorgfältiges Staging ist essenziell für die Therapieplanung PD Dr. Ursula Plöckinger (Berlin) zeigte am Beispiel der „MitteldarmNET“ (= im mittleren Bereich des Magen-Darm-Trakts, d.h. im Jejunum oder Ileum lokalisierte NET), wie essenziell die Früherkennung und im Anschluss daran ein sorgfältiges histologisches und morphologisches Staging (Stadieneinteilung) dieser sehr heterogenen Tumorerkrankungen für die Einschätzung der Prognose und damit für die Vermeidung einer Über- oder Untertherapie ist. Bei Patienten mit metastasierenden NET kann man nach heutiger Datenlage von einer 10-Jahres-Überlebensrate von 60 % ausgehen. Von den Patienten, bei denen bereits Lebermetastasen vorliegen, überleben 25 % innerhalb von 10 Jahren. Die 5-Jahres-Überlebensrate liegt bei Patienten mit lokaler Erkrankung bei 65 %, bei Patienten mit Fernmetastasen bei 39 %. Dr. Plöckinger nennt abschließend folgende Faktoren, die nachweislich mit der Überlebensrate korrelieren: • gute Differenzierung des Tumors, • niedrige Konzentration des Proliferationsmarkers Ki67, • primäre Resektion. B. S. 19 Veranstaltungen 2. Überregionaler Neuroendokriner Tumor-Tag 18.–20. November 2005 in Nürnberg Diese Veranstaltung, die das Netzwerk Neuroendokrine Tumoren (NeT) e.V. für Patienten, Angehörige, Interessierte und Ärzte durchführte, war das erste Highlight in der Geschichte des noch jungen Vereins. 126 Betroffene und Angehörige waren ins Le Méridien Grand Hotel nach Nürnberg gekommen, um sich die Ausführungen der 9 Referenten anzuhören, miteinander zu diskutieren, Fragen zu stellen und Erfahrungen auszutauschen. Auch einige Ärzte aus dem Raum Erlangen Nürnberg nutzten die Gelegenheit, den Vorträgen beizuwohnen und mit den Spezialisten Fragen der Diagnostik und Therapie zu erörtern. Das Programm hatte an jedem der 3 Tage einen eigenen Schwerpunkt: • 18.11.05: Mitgliederversammlung • 19.11.05: Vorträge und Workshops • 20.11.05: Erfahrungsaustausch unter Patienten Freitag Abend: Mitgliederversammlung Am Abend vor den Vorträgen trafen sich die NeT-Mitglieder zu ihrer ersten Mitgliederversammlung. Frau Oehme, unsere Schriftführerin, hat die wichtigsten Tagungsordnungspunkte für Sie festgehalten: TOP 1: Bericht des Vorstands Herr Professor Hensen begrüßte die Anwesenden und stellte die Vorstandsmitglieder vor. Er legte die Gründe dar, die zur Gründung eines eigenständigen Vereins Netzwerk NeT e.V. ge­führt hatten, und 20 berichtete von der Gründungsversammlung am 6. Juli 2005. Bereits am 21. Juli 2005 wurde der Verein ins Vereinsregister des Amtsgerichtes Erlangen eingetragen. Alle Patienten mit neuroendokrinen Tumoren, die bis dahin Mitglied des Netzwerks Hypophysenund Nebennierenerkrankungen e.V. waren, werden nach schriftlichem Antrag in den neuen Verein übernommen. Der Mitgliedsbeitrag bleibt mit 15,00 m pro Jahr gleich, auch die Ansprechpartnerinnen in der Geschäftsstelle in Erlangen bleiben dieselben. Für Mitglieder mit MEN 1 gilt folgende Regelung: Diese Gruppe ist in beiden Vereinen gleich gut aufgehoben und erhält daher Informationsmaterial von beiden Vereinen. Professor Hensen ist auch Vorsitzender des wissenschaftlichen Beirats. Auf der Gründungsversammlung konnten Herr PD Dr. C. Auernhammer (München) sowie Herr Prof. Dr. M. Weber (Mainz) als wissenschaftliche Beiräte gewonnen werden. Dieser Kreis soll noch erweitert werden um Spezialisten aus den verschiedenen Disziplinen, die bei der Betreuung von Patienten mit neuroendokrinen Tumoren eng zusammenarbeiten. Vor allen Dingen sollte die Bereitschaft zur Mitarbeit (Vorträge, Workshops, Beiträge für die Glandula NeT usw.) vorhanden sein. TOP 2: Sonstiges Frau Dr. Pavel gab einen kurzen Überblick über die Vorträge und Workshops, die am nächsten Tag stattfinden sollten, und wies dar- auf hin, dass nach jedem Vortrag genügend Zeit für Fragen und Diskussion eingeplant wäre. Außerdem könnten auch in der Expertenrunde und in den 3 Workshops noch Fragen an die Referenten gestellt werden. Abschließend wurde darüber diskutiert, wie man Betroffene ans Netzwerk NeT heranführen könnte. Genannt wurden folgende Möglichkeiten: durch eigene Veranstaltungen, durch Info-Stände auf Kongressen, über die Glandula NeT, die Pharmazie und die Apotheken (Apotheken Umschau) sowie nicht zuletzt über die InternetSeite des Netzwerks. Da die Hilfe zur Selbsthilfe eines der Hauptanliegen des Vereins ist, erging an die Mitglieder die Bitte, sich als Ansprechpartner im Netzwerk NeT zur Verfügung zu stellen. (Adressen und Telefonnummern der Ansprechpartner werden auf Wunsch nur über die Geschäftsstelle an Interessierte weitergegeben und nicht in der Glandula veröffentlicht, Anm. der Redak­ tion). Samstag: Vorträge und Workshops Am Samstag früh breitete sich Kongress-Atmosphäre im Grand Hotel aus: Ab 9.15 Uhr standen 6 medizinische Vorträge auf dem Programm. Spezialisten aus den Fachbereichen Endokrinologie, Radiologie, Nuklearmedizin und Chirurgie waren angereist, um neben bewährten Verfahren in Diagnostik und Therapie auch neue Ansätze Veranstaltungen Kongress-Splitter „Es ist gut, dass es den NET-Tag gab! Die Fülle an Informationen hätte mir kein Arzt im persönlichen Gespräch vermitteln können.” 21 Veranstaltungen zu erläutern und Einblicke in die aktuelle Forschung zu geben. Wir freuen uns sehr, dass sich die meisten Referenten dazu bereit erklärt haben, uns eine Zusammenfassung ihres Vortrags für die Glandula NeT zu überlassen. Daher können sich auch diejenigen unter Ihnen, die nicht auf der Veranstaltung dabei sein konnten, über die Möglichkeiten der Diagnostik und Therapie informieren. Ab Seite 23 finden Sie die folgenden Beiträge: • Diagnostik bei neuroendokrinen Tumoren (Prof. Dr. med. M. We ber, Mainz) • Nuklearmedizinische Bildgebung bei neuroendokrinen Tumoren (Dr. med. A. Nömayr, Erlangen) • Die Nuklearmedizinische Klinik des Universitätsklinkums Erlan gen stellt sich vor (Prof. Dr. med. T. Kuwert, Erlangen) • Medikamentöse Therapie bei neuroendokrinen Tumoren (PD Dr. med. C. J. Auernhammer, München) • Lokale Therapieverfahren bei Lebermetastasen neuroendokri ner Tumoren (Prof. Dr. med. H.-J. Wagner, Marburg) • Neue Ansätze in der medika mentösen Therapie: Angiogene se-Inhibitoren, neue Somatosta tinanaloga und andere neue Be handlungsoptionen (PD Dr. med. M. Pavel, Erlangen) An dieser Stelle danken wir allen Referenten nochmals ganz herzlich für die gut verständlichen und aufschlussreichen Vorträge, die für die Patienten und ihre Angehörigen eine ungemein wichtige Informationsquelle sind und daher wesentlich dazu beitragen, mit der doch sehr bedrückenden Diagnose „neuroen22 Der Vorstand des Netzwerks NeT e.V., von links: PD Dr. Marianne Pavel, Prof. Dr. Hensen, Ingeborg Schäfer, Martin Michael, Rosemarie Oehme. dokriner Tumor” besser umgehen zu können. Krankheitsbewältigung – dieses überaus wichtige Thema hatte auch einer der drei angebotenen Workshops zum Inhalt. In kleiner Runde erarbeiteten die Teilnehmer unter der Leitung von Frau Dr. med. Jutta Hensen Strategien, wie sie am besten mit der Krankheit leben können. Frau PD Dr. med Marianne Pavel erläuterte in ihrer Arbeitsgruppe, wie therapeutische Konzepte richtig eingesetzt werden, und Herr Prof. Dr. med. Johannes Hensen gab Antworten auf die Frage: Verlaufsuntersuchungen: Was ist sinnvoll und wie oft? Sonntag Vormittag: Erfahrungsaustausch unter Patienten Wo kann ich Hilfe finden? Was kann ich selbst tun? Als Mitglied des Netzwerks NeT werden Sie mit solchen Fragen nicht alleine gelassen. Auf dem Neuroendokrinen TumorTag konnten die Teilnehmer viel voneinender erfahren, neue Kontakte knüpfen und dank neuer An- und Einsichten auch wieder Hoffnung schöpfen. Wann findet der nächste Neuroendokrine Tumor-Tag statt? Das war die häufigste Frage nach dieser gelungenen Veranstaltung, 26 Mitglieder (inklusive Vorstand) nahmen an der Mitgliederversammlung teil. die bei allen – den Betroffenen, ihren Angehörigen, aber auch den Ärzten – sehr großen Anklang gefunden hat. Maßgeblich zum Gelingen beigetragen haben die wissenschaftlichen Leiter Frau Dr. Pavel und Herr Professor Hensen sowie unsere Mitarbeiterinnen im Netzwerk-Büro, Frau Hummel und Frau Jalowski. Ihnen allen ein herzliches Dankeschön! Last but not least bedanken wir uns vielmals bei Frau Gyde Haeseler und Frau Dr. Karin Grassmann, Novartis Pharma GmbH, Nürnberg, durch deren großzügige Unterstützung die Veranstaltung erst möglich wurde. Halt, fast hätten wir es vergessen: Der diesjährige Neuroendokrine Tumor-Tag findet vom 24. bis 26. November unter der Leitung von Herrn Professor Weber in Mainz statt – wir freuen uns auf Ihr Kommen! Brigitte Söllner, Erlangen Diagnostik Diagnostik bei neuroendokrinen Tumoren Definition und Einteilung Klinisches Bild Unter dem Begriff der neuroendokrinen Tumoren (NET) werden seltene Tumoren zusammengefasst, die von neuroendokrinen Zellen ausgehen. Entsprechend ihrer Herkunft weisen diese sowohl nervenähnliche (neuronale) als auch hormonbildende (endokrine) Eigenschaften auf. Sie können überall im Körper vorkommen und wachsen meist sehr langsam. Daher ist es oft schwierig zu entscheiden, ob ein NET gutartig oder bösartig (mit der Fähigkeit zur Ausbildung von Tochtergeschwülsten) ist. Früher wurden die NET auch als Karzinoide oder APUDome bezeichnet. Die aktuelle Einteilung der NET zeigt Tabelle 1. Sie berücksichtigt nicht nur den feingeweblichen (histologischen) Aufbau des Tumors, sondern auch eine mögliche hormonelle Aktivität (Hormonsekretion) und die Lokalisation des Tumors. Aufgrund der entwicklungsgeschichtlichen Herkunft der Organe werden hinsichtlich der Lokalisation unterschieden: • Vorderdarm-Tumoren in 20 % (Lunge, Thymus [Bries], Pankreas [Bauchspeicheldrüse], Duo­ denum [Zwölffingerdarm], Magen), • Mitteldarm-Tumoren in 70 % (Jejunum, Ileum [Dünndarm]), Appendix [Blinddarm], Coecum [erster Teil des Dickdarms]) und • Enddarm-Tumoren in 10 % (Kolon, Sigma, Rektum [übriger Dickdarm]). Häufig ist die klinische Symptomatik wegweisend für die Diagnostik neuroendokriner Tumoren. Allerdings werden die ersten klinischen Beschwerden oft lange Zeit nicht richtig zugeordnet, da die Tumoren anfangs nur uncharakteristische oder geringe Beschwerden verursachen. Dabei können NET entweder über ihre Hormonaktivität oder über das Tumorwachstum zu klinischen Symptomen führen. Nicht selten werden sie aber als Zufallsbefund entdeckt (zum Beispiel bei einer Blinddarmentfernung). Werden keine klinisch aktiven Hormone sezerniert, bleiben die NET aufgrund ihres langsamen Wachstums und ihrer anfangs geringen Größe häufig lange unentdeckt. Typische klinische Befunde, die durch das Tumorwachstum verursacht werden können, sind Lebervergrößerung (bei Lebermetastasen), Gelbsucht (durch GalleabflussStörung), Darmverschluss, Bauchschmerzen oder eine Blutung. Univ.-Prof. Dr. med. Matthias M. Weber, Schwerpunkt Endokrinologie und Stoffwechselerkrankungen, Klinikum der Johannes Gutenberg Universität Mainz Etwas weniger als die Hälfte aller NET sind klinisch hormonaktiv und können durch die Sekretion von Hormonen zu sehr charakteristischen klinischen Krankheitsbildern führen. Die häufigsten klinischen Krankheitsbilder sind dabei: • das Insulinom (Insulin-produzierender Tumor mit plötzlichen Phasen von Verwirrtheit bis Bewusstlosigkeit bei Unterzuckerungen), • das Gastrinom (Zollinger-EllisonSyndrom mit therapieresistenten Magen- und Zwölffingerdarmgeschwüren durch Gastrinsekretion des Tumors) sowie Histologische Merkmale (Gewebsuntersuchung) 1.Hoch differenzierter neuroendokriner Tumor gutartig, fraglich gutartig 2.Hoch differenziertes neuroendokrines Karzinom niedriggradig bösartig 3.Niedrig differenziertes neuroendokrines Karzinom hochgradig bösartig Biologische Merkmale 1.Klinisches Bild, hormonelle Aktivität 2.Tumorlokalisation Tabelle 1: Einteilung neuroendokriner Tumoren (NET), WHO Klassifikation (2000). 23 Diagnostik • das Karzinoid-Syndrom, das durch die Sekretion von Serotonin und anderen Hormonen zu der charakteristischen Flushsymptomatik (plötzliche Hautrötung, Durchfall, Schwitzen) führen kann. Wesentlich seltener sind das VIPom (Sekretion von vasoaktivem intestinalem Polypeptid), das im Rahmen des Werner-Morrison-Syndroms zu massiven wässrigen Durchfällen führen kann, das Glukagonom, das Somatostatinom, das CushingSyndrom (ACTH-Sekretion) und die Akromegalie (GHRH-Sekretion). Labordiagnostik Laboruntersuchungen spielen eine wichtige Rolle bei der diagnostischen Abklärung und Verlaufskontrolle von neuroendokrinen Tumoren. Insbesondere bei Tumoren, die Hormone produzieren, können diese oft in erhöhter Konzentration im Blut oder im Urin gefunden werden. Da es in manchen Fällen schwierig sein kann, zwischen einem normalen Hormonspiegel und einer krankhaften Hormonse­ kretion zu unterscheiden, werden bei bestimmten Fragestellungen zudem Stimulations- oder Hemmtests durchgeführt. Die Interpretation und die Durchführung dieser Tests sind oft sehr kompliziert und die Bestimmungsmethoden meist sehr anspruchsvoll, so dass diese Untersuchungen nur von Ärzten durchgeführt werden sollten, die damit Erfahrung haben, wie zum Beispiel Endokrinologen. Bis heute sind über 15 hormonelle Marker der neuroendokrinen Tumoren bekannt. Die wichtigsten sind: • Insulin • Gastrin 24 • Serotonin und sein Abbauprodukt 5-Hydroxyindolessigsäure (5-HIES) • pankreatisches Polypeptid. Seltener findet sich eine erhöhte Konzentration von Glukagon, VIP, Somatostatin, Calcitonin, ACTH, GHRH, PTH related peptide etc. Die wichtigsten Tumormarker, die auf die Abstammung des NET von Nervenzellen hinweisen und die auch im Blut von Patienten in erhöhter Konzentration gefunden werden können, sind die neuronspezifische Enolase (NSE) sowie das Chromogranin A. Chromogranin A ist ein Bestandteil der Speicherbläschen von Nervenzellen und kann von neuroendokrinem Tumorgewebe gebildet werden. Eine stark erhöhte Chromogranin-A-Konzentration im Blut spricht für das Vorliegen eines neuroendokrinen Tumors und kann auch als ein Verlaufsparameter unter der Therapie herangezogen werden (siehe dazu Beitrag auf Seite 47f.). Leicht erhöhte ChromograninA-Konzentrationen findet man aber auch bei eingeschränkter Nierenfunktion und ausgeprägten Resorptionsstörungen des Darms. Die Konzentration von Gastrin im Blut wird bei Verdacht auf ein Gastrinom gemessen. Bei extrem erhöhten Werten und dem Auftreten von therapieresistenten wiederholten Magen- und Zwölffingerdarmgeschwüren mit saurem Magensaft ist die Diagnose gesichert. Allerdings können die Werte auch bei einer chronischen Magenschleimhautentzündung (Gastritis) mit einer autoimmun bedingten Zerstörung der säurebildenden Schleimhautzellen, bei Helicobacter-pylori-Befall sowie bei eingeschränkter Nierenfunktion erhöht sein. In vielen Fällen muss daher zusätzlich der Säure- wert des Magensaftes bestimmt oder ein Stimulationstest (SekretinTest) durchgeführt werden. Vor der Gastrin-Bestimmung müssen Medikamente, die die Säureproduktion des Magens hemmen, für 5 Tage (Protonen-Pumpen-Hemmer, z.B. Omeprazol) bzw. 24 Stunden (H2Rezeptor-Antagonisten, z.B. Ranitidin) abgesetzt werden. Ein wichtiger Laborwert bei Verdacht auf das Vorliegen eines Karzinoid-Syndroms bei Tumoren des Mitteldarms ist die Bestimmung von 5-HIES im angesäuerten 24-Stunden-Sammelurin. 5-HIES ist das Abbauprodukt des körpereigenen Hormons Serotonin, welches bei der Bestimmung nur sehr ungenaue und störanfällige Ergebnisse liefert. Vor der 5-HIES-Bestimmung müssen tryptophanhaltige (Tryptophan = ein Eiweißbaustein) Nahrungsmittel wie z. B. Bananen, Nüsse, Avocado, Tomaten oder bestimmte Medikamente vermieden werden. Die Bestimmung von Insulin kann insbesondere im Zusammenhang mit einem erniedrigten Blutzuckerspiegel wegweisend für die Diag­ nose eines Insulin-produzierenden Tumors (Insulinom) sein. Für die Diagnosesicherung eines Insulinoms ist meist die Durchführung eines 72-Stunden-Hungerversuchs notwendig. Immunhistochemische Untersuchung des Tumorgewebes Nach der operativen Entfernung des Tumors oder bei einer Probeentnahme (Biopsie) wird das Tumorgewebe durch bestimmte Färbetechniken auf die Produktion von spezifischen Botenstoffen hin untersucht (immunhistochemische Untersuchung). Diagnostik So erlaubt der Nachweis von hormonellen oder neuronalen Markern im Tumor wie etwa Chromogranin und Synaptophysin die Einordnung des NET und dient zusammen mit der Bestimmung von Faktoren, die die Geschwindigkeit des Zellwachstums erfassen (Ki 67, MIB-1), auch der prognostischen Einordnung des Tumors (Abb. 1.). Bildgebende Untersuchungen Um den Tumor oder Tochtergeschwülste (Metastasen) sowie vergrößerte, vom Tumor befallene Lymphknoten darzustellen, werden die unterschiedlichsten bildgebenden Verfahren eingesetzt. A Sonographie Das am wenigsten belastendende Verfahren ist die Ultraschalluntersuchung (Sonographie), mit deren Hilfe erfahrene Untersucher insbesondere im Bauch- und Beckenraum (Leber, Nebennierenregion, Bauchspeicheldrüse, Lymphknoten, Blasenregion) sowie im Halsbereich auch kleine Strukturen darstellen können. Der Vorteil der Sonographie liegt im geringen Aufwand der Untersuchung, die bei fehlender Strahlenbelastung auch kurzfristig mehrmals hintereinander – zum Beispiel zur Kontrolle eines Therapieerfolges – durchgeführt werden kann. Werden spezielle Geräte eingesetzt, kann mit Hilfe der so genannten Farbdopplersonographie auch die Durchblutung von Tumoren (z. B. bei Lebermetastasen) erfasst oder im Rahmen der Echokardiographie die Funktion des Herzens untersucht werden. Letzteres ist insbesondere zum Nachweis einer Endokardfibrose oder Klappenschädi- B Abbildung 1: Feingewebliche (histologische) Untersuchung von neuroendokrinem Tumorgewebe. Durch bestimmte Färbetechniken (Immunhistochemie) lassen sich neuroendokrine Marker selektiv anfärben. Im vorliegenden Fall sind die stark Synaptophysin-positiven (A) und vereinzelt Chromogranin-positiven Zellstrukturen (B) braun angefärbt. gung beim Karzinoid-Syndrom von klinischer Bedeutung. Endoskopie Mit Hilfe der Endoskopie gelingt nicht nur der direkte Nachweis (Videoaufnahme) von Tumoren oder Schleimhautveränderungen, wie zum Beispiel Geschwüren (Ulzera) im Magen-Darm-Trakt (Magen- oder Darmspiegelung), im Bronchialsystem (Lungenspiegelung) oder in der Blase (Blasenspiegelung), sondern auch die Gewinnung von Gewebsproben (Biopsie) zur Gewebsunter25 Diagnostik Abbildung 2: Endosonographie der Bauchspeicheldrüse mit Darstellung eines ca. 1 cm messenden neuroendokrinen Tumors (Insulinom). Der Tumor stellt sich als echoarme (dunkle), glatt begrenzte Struktur im umliegenden Bauchpeicheldrüsen­ gewebe dar. suchung und sogar kleine therapeutische Eingriffe wie zum Beispiel eine Polypenentfernung oder eine Blutungsstillung. Eine endoskopische Gewebsuntersuchung ist bei neuroendokrinen Tumoren des Magens zur Festlegung des therapeutischen Vorgehens nötig, da die NET des Magens eine sehr heterogene Gruppe darstellen und eine genaue Klassifikation für die Planung der weiteren Therapie und Kontrolluntersuchungen von großer Bedeutung ist. Spezielle endoskopische Anwendungen sind die ERCP (endoskopisch retrograde Cholangiopankreatikographie), bei der im Rahmen einer Endoskopie die Gallenwege und der Pankreasgang mit Röntgenkontrastmittel dargestellt werden, sowie die Kapselendoskopie oder der Doppelballonkatheter zum Nachweis von Dünndarmtumoren. Eine sehr wichtige Untersuchungsmethode bei NET des Magen-DarmTrakts ist die Endosonographie, eine 26 Kombination der beiden Untersuchungsverfahren Magenspiegelung (Gastroskopie) und Sonographie. Hierbei befindet sich an der Spitze des flexiblen Endoskops ein Ultraschallkopf, welcher ein hochauflösendes Bild der Darmwand und der benachbarten Organe liefert. Diese Untersuchungstechnik besitzt eine sehr hohe Sensitivität für den Nachweis von Tumoren im Bereich der Magen- und Duodenalwand, der Bauchspeicheldrüse und der Nebennieren, so dass auch kleine, nur wenige Millimeter große Tumore in einem frühen Stadium erfasst werden können (Abb. 2). Neben der ­exakten Bestimmung der Tumorgröße und -ausbreitung ist auch die endoskopische ultraschall-gesteuerte Punktion von unklaren Strukturen möglich. Computertomographie Die Standardmethode zur Tumorlokalisation, Therapieplanung und Verlaufsbeobachtung insbesondere bei fortgeschrittenen NET mit der möglichen Ausbildung von Tochtergeschwülsten ist die Computertomographie (CT). Hierbei werden die Patienten in einem bogenförmigen Gerät durch Röntgenstrahlen kreisoder spiralförmige abgetastet und die Daten anschließend im Computer ausgewertet. Mit modernen Geräten und durch den Einsatz von Kontrastmitteln können so in relativ kurzer Zeit dünne Querschnitte von 1–10 mm Schichtdicke des gesamten Körpers erzeugt werden und auf diese Weise sehr genaue Aussagen zu einer möglichen Tumorausbreitung und zur Gefäßversorgung getroffen werden (Abb. 3). Kernspintomographie Bei der Kernspintomographie oder auch Magnetresonanz-Tomographie (MRT) werden die Patienten in einem röhrenförmigen Gerät mit Hilfe eines sehr starken Magnetfeldes untersucht. Auch hier können wie beim CT nicht nur sehr enge Längsoder Querschnitte durch den Körper angelegt werden, sondern durch den Einsatz von bestimmten Kontrastmitteln auch die Gefäßversorgung bestimmter Bereiche (MR-Angiographie) oder Galleabflusshindernisse (MRCP) dargestellt werden. Vorteil dieser Untersuchung ist die fehlende Strahlenbelastung, Nachteil die häufig sehr enge Röhre, die für Patienten mit Angst vor engen Räumen als unangenehm empfunden werden kann. Nicht möglich ist diese Untersuchung bei Patienten mit Schrittmacher oder anderen Metallteilen im Körper. Diagnostik Somatostatin-RezeptorSzintigraphie Eine zentrale Bedeutung bei der Diagnostik von NET haben in den letzten Jahren nuklearmedizinische Verfahren gewonnen. An erster Stelle steht hierbei die Somatostatin-Rezeptor-Szintigraphie (Octreo­ scan), bei der man sich zu Nutze macht, dass viele NET eine erhöhte Dichte an Bindungsstellen für das Hormon Somatostatin aufweisen. Verabreicht man dem Patienten einen radioaktiv markierten Abkömmling von Somatostatin (Octreotid), so reichert sich dieser auf der Zell­ oberfläche dieser Tumoren an (Abb. 3). Mit Hilfe spezieller Kameras können auf diese Weise auch weit verstreute NET im ganzen Körper sehr spezifisch nachgewiesen werden. Eine Besonderheit ist, dass sich bei einer guten Anreicherung hieraus auch die Möglichkeit zu einer späteren Radionuklid-Strahlentherapie ergeben kann. Weitere nuklearmedizinische Verfahren, die häufiger bei NET angewandt werden, sind das 18F-FDG-PET bei undifferenzierten schnell wachsenden NET, die Knochenszintigraphie zum Nachweis von Knochenmetastasen sowie die MIBG-Szintigraphie und das Dopa-PET bei Verdacht auf das Vorliegen eines Phäochromozytoms oder Paraganglioms (siehe auch Beitrag „Nuklearmedizinische Bildgebung auf Seite 28ff.). Fazit Zusammenfassend spiegelt sich die Vielfalt der neuroendokrinen Tumoren auch in einer Vielzahl von diagnostischen Möglichkeiten wider. Welche der jeweiligen diagnostischen Verfahren bei einem Abbildung 3: Bildgebende radiologische und nuklearmedizinische Verfahren zum Nachweis neuroendokriner Tumoren. Die hier dargestellte Computertomographie (CT) und Somatostatin-Rezeptor-Szintigraphie (Octreotid-Szintigraphie) zeigen Lebermetastasen eines neuroendokrinen Karzinoms des Dünndarms. Mehrere im CT nachweisbare größere Leberraumforderungen stellen sich in der OctreotidSzintigraphie als mehrspeichernde schwarze Herde dar. Die szintigraphische Abbildung links zeigt eine Ganzkörperaufnahme, die Darstellung rechts zeigt ein szintigraphisches Querschnittsbild (SPECT) analog zum dargestellten Querschnittsbild der Computertomographie. Patienten eingesetzt werden, hängt sehr stark von der Fragestellung und von individuellen Besonderheiten des Patienten ab und sollte immer von einem in der Behandlung neuroendokriner Tumoren erfahrenen interdisziplinären Ärzteteam entschieden werden. Aufgrund des enormen technischen und wissenschaftlichen Fortschritts haben sich in den letzten Jahren insbesondere auf dem Gebiet der neuroendokrinen Tumoren große Fortschritte im diagnostischen Bereich ergeben, die sich auch in einer deutlich effektiveren Behandlungsmöglichkeit für Patienten mit NET niederschlagen. Univ.-Prof. Dr. med. Matthias M. Weber, Leiter des Schwerpunktes Endokrinologie und Stoffwechsel­ erkrankungen, I. Medizinische Klinik und Poliklinik, Klinikum der Johannes Gutenberg Universität Mainz 27 Diagnostik Nuklearmedizinische Bildgebung bei neuroendokrinen Tumoren Bei nuklearmedizinischen Verfahren werden radioaktiv markierte Moleküle zum Aufspüren von Krankheiten eingesetzt. Die hiermit verbundene Strahlenbelastung der Patienten ist in der Regel sehr gering und mit derjenigen durch radiologische Verfahren vergleichbar. Positronenemissionstomographie (PET) und des radioaktiv markierten Zuckers F-18-Deoxyglukose (FDG). Dieses Verfahren hat bei vielen Krebsarten einen festen diagnostischen Stellenwert. Gut differenzierte neuroendokrine Tumoren nehmen in der Regel wenig FDG auf, lassen sich mit diesem Verfah- Dr. med. Anton Nömayr, Nuklearmedizinische Klinik und Poliklinik, Universitätsklinikum Erlangen Somatostatin-RezeptorSzintigraphie Ein Vorteil der nuklearmedizinischen Verfahren gerade in der Diagnostik neuroendokriner Tumoren besteht darin, dass sich mit dem radioaktiven Pharmakon Indium-111-Octre­ otid Tumorzellen sichtbar machen lassen, die Somatostatin-Rezeptoren tragen (Abb. 1). Neben so genannten planaren Aufnahmen kann hierzu auch die nuklearmedizinische Computertomographie SPECT verwendet werden. Durch dieses besondere Prinzip der Bildgebung ist die Somatostatin-Rezeptor-Szintigraphie radiologischen Verfahren wie der Magnetresonanztomographie oder der Röntgencomputertomographie hinsichtlich der Empfindlichkeit für die Entdeckung von Absiedlungen neuroendokriner Tumoren überlegen. Positronenemissionstomographie (PET) Ein weiteres nuklearmedizinisches Verfahren zur Untersuchung von Patienten mit Krebserkrankungen ist die Darstellung des Zuckerstoffwechsels unter Verwendung der 28 Abbildung 1: Indium-111-Octreotid-Ganzkörperszintigraphie. Eine physiologische Traceranreicherung findet sich in Leber, Nieren und Milz. Der Pfeil markiert die Tracerbindung an die Somatostatin-Rezeptoren eines Lungentumors. L = Leber, M = Milz, N = Niere. Diagnostik zur Indium-111-Szintigraphie oder Indium-111-SPECT eine verbesserte Detektion von Tumorherden. Hierzu ist eine Vielzahl von Tracern in Entwicklung. Am häufigsten wird Gallium-68-DOTATOC verwendet, allerdings sind diese Tracer noch nicht kommerziell erhältlich. Fusionsbildgebung Abbildung 2: Lebermetastase eines entdifferenzierten neuroendokrinen Tumors. FDG-PET: Deutliche Anreicherung in der Lebermetastase (Pfeil) bei erhöhtem Zuckerstoffwechsel. In111-SPECT: Keine Traceranreicherung bei stark reduzierten oder fehlenden Somatostatin-Rezeptoren. ren also nicht erfassen. Tritt jedoch eine Entdifferenzierung des Tumors ein, lässt sich auch die FDG-PET bei Patienten mit neuroendokrinen Tumoren einsetzen (Abb. 2). Weiterhin kann auch mittels der PET eine Rezeptoren-basierte Untersuchung erfolgen. Die PET bietet im Vergleich Nuklearmedizinische Verfahren sind zum Aufspüren von Krankheitsherden sehr empfindlich. Ihre Schwäche liegt jedoch in ihrer vergleichsweise schlechten Darstellung der normalen Körperanatomie. Dies führt dazu, dass sich die mit nuklearmedizinischen Verfahren „angefärbten“ Krebsabsiedlungen auf den nuklearmedizinischen Bildern nur Positronenemissionstomographie (PET) Im Computertomogramm (CT) sehen Krebszellen nicht immer anders aus als gesunde Zellen; sie fallen nur durch Anhäufung auf. Mit der Positronenemis­ sionstomographie, die Stoffwechselvorgänge in leben­ den Organismen sichtbar macht, können Tumorzellen dagegen an ihrem beschleunigten Stoffwechsel erkannt werden. Da Tumorzellen im Vergleich zu gesunden Zellen ein Mehrfaches an Zucker (Glukose) verbrauchen, lassen sich mit Hilfe radioaktiv markierter Zuckermoleküle krankhaft veränderte Zellen auch in geringer Zahl auffinden. Bei der PET-Untersuchung wird dem Patienten ein mit einem Positronenstrahler markierter Stoff (Radio­ pharmakon, z.B. Fluordeoxyglukose, FDG) injiziert. Das Radiopharmakon zerfällt im Körpergewebe und sendet Strahlen aus, die von Kristallen im PET-Scanner aufgefangen werden und dort Lichtblitze erzeugen. Bei Verwendung von Lutetium-Silicium-OxidKristallen, die extrem empfänglich für den Einfall der Teilchen sind, erhält man ein besonders helles und damit deutliches, aussagekräftiges Bild. Tumor-PET • Indikation: Staging (Lymphknoten und Fernmetastasen) maligner Tumoren, Restaging/Therapiekon­ trolle, Rezidivsuche, Abklärung unklarer pulmo­naler Rundherde • Radiopharmakon: F-18 FDG • Aktivität: 7 MBq/kg • Untersuchungsablauf: Nach einer kurzen Ruhephase und Gabe von Buscopan wird FDG injiziert, eine Stunde später wird die Aufnahme mit dem PET-Scanner angefertigt (Dauer ca.1–2 Stunden). Bei Fragestellungen in Blasennähe (z. B. Lokalrezidiv eines Rektumkarzinoms) ist ein Blasenkatheter erforderlich, ebenso wie bei inkontinenten Patienten oder bei Blasenentleerungsstörung. Auf eine ausreichende Schmerztherapie ist bei einer reinen Aufnahmedauer von 60–90 Minuten zu achten. B. S. 29 Diagnostik Hybridgerät SPECT/Spiral-CT Das SPECT/Spiral-CT wurde zur exakteren Diagnose von Krebs- und Herzerkrankungen entwickelt. Das über 1 Million Euro teure Diagnosegerät „Symbia True ­Point SPECT CT“ von Siemens Medical Solutions, das seit März 2005 in der Universitätskinik Erlangen in Betrieb ist, vereint die Vorteile der etablierten und sicheren Diagnose-Systeme SPECT (Single-Photon Emission Computertomographie) und Spiral-Computertomographie (CT). SPECT: Funktionsorientierte Diagnostik SPECT ist ein bewährtes nuklearmedizinisches Verfahren, bei dem im menschlichen Organismus ablaufende Stoffwechselvorgänge gezielt untersucht und in Form von Funktionsbildern dargestellt werden können. Dazu wird dem Patienten eine am Stoffwechselgeschehen beteiligte Substanz gespritzt, die mit einem radioaktiven Isotop markiert wurde. Dieses Radiopharmakon reichert sich entsprechend seiner pharmakologischen Eigenschaften in verschiedenen Körpergeweben an und sendet beim Zerfall Gammastrahlung aus, die von der um den Patienten rotierenden Gamma-Kamera erfasst wird. Die Messung der vom Radioliganden emittierten Gammastrahlung sowie die mathematische Berechnung der Lokalisation des Isotops zum Zeitpunkt der Emission liefern Informationen über den Ort und den Umsatz der Substrate. Auf diese Weise sind krankhafte Veränderungen schon im Molekularbereich erkennbar, bevor eine Änderung der anatomischen Struktur im Submillimeterbereich mit der Computertomographie sichtbar wäre. Aufgrund der hohen Spezifität der verwendeten radioaktiven Testsubstanzen für bestimmte Gewebe/ Organe werden die übrigen Körperstrukturen jedoch nur verschwommen oder gar nicht dargestell. Daher ist die ebenfalls nötige anatomische Detailinforma­tion bei der SPECT-Untersuchung eingeschränkt und eine genaue räumliche Zuordnung des Befundes sehr schwierig. Spiral-CT: Strukturorientierte Diagnostik Diese „Systemschwäche“ des SPECT gleicht der Computertomograph aus, mit dem sich zwei- oder dreidimensionale Aufnahmen des Körpers anfertigen 30 lassen. Dazu wird mit einer Röntgenröhre ein fächerförmiger Strahl erzeugt und durch den Körper des Patienten geleitet. Die Röntgenstrahlung wird von den verschiedenen Körpergeweben verschieden stark geschwächt und beim Austritt aus dem Körper von Detektoren aufgefangen. Das Signal wird anschließend elektronisch aufbereitet und an einen Rechner weitergeleitet. Da sich das System aus Röhre und Detektoren ständig spiralförmig um das Messfeld dreht, werden viele verschiedene Projektionen derselben Schicht erzeugt. Im Rechner werden die Datensätze zu einem Bild verarbeitet, das die Körperstrukturen sehr detailliert darstellt. Hybridgerät: Diagnostischer Sprung vom cmin den mm-Bereich SPECT und Spiral-CT konnten bislang nicht in diagnostischer Güte miteinander kombiniert werden. Die Patienten wurden in der Regel an zwei Tagen an zwei verschiedenen Geräten untersucht und erhielten am dritten Tag das Untersuchungsergebnis. Mit dem neuen SPECT/Spiral-CT liegt der Befund nun innerhalb einer Stunde vor. Die flächigen SPECT-Bilder können mit den CT-Schichtbildern überlagert werden, so dass der Arzt submillimetergenau erkennen kann, an welchen Stellen im Körper Erkrankungen vorliegen. B. S. Diagnostik sehr schlecht lokalisieren lassen. Hier führt die Kombination der nuklearmedizinischen Bilder mit denjenigen der CT oder MRT in der Regel weiter (Abb. 3). Allerdings muss dabei gewährleistet sein, dass die nuklearmedizinischen und radiologischen Bilder exakt überlagert sind. Zu diesem Zweck lässt sich Software einsetzen, die jedoch bisher noch vergleichsweise ungenaue Ergebnisse liefert. Der beste Weg für die Bildüberlagerung sind die so genannten Hybridgeräte. Bisher verfügbare Hybridgeräte kombinieren die PET oder SPECT mit der Röntgencomputertomographie. Dadurch, dass beide Untersuchungen kurz hintereinander an einem auf derselben Liege positionierten Patienten durchgeführt werden, sind Ungenauigkeiten der Überlagerung in der Regel minimal, wodurch die diagnostische Genauigkeit steigt. Als Nebenprodukt des Einsatzes der Hybridgeräte kommt es zu einer Verkürzung der Zeit, die für die Diagnostik benötigt wird. Hierdurch sind im Krankenhaus Kosteneinsparungen zu erwarten, für den Patienten wird die Zeit der oft quälenden Ungewissheit beim Warten auf die endgültige Diagnose ebenfalls deutlich verkürzt. Bedeutung der Hybrid­ bildgebung für die Planung der nuklear­ medizinischen Therapie Ein weiteres Einsatzgebiet von Hybridkameras ist die Planung einer Therapie mit offenen radioaktiven Stoffen, wie z. B. mit Yttrium-90DOTATOC. Ideal für die Planung solcher Therapien wäre die prätherapeutische Bestimmung der Strahlendosis innerhalb des Tumors. Abbildung 3: Bauchfellmetastasen eines neuroendokrinen Tumors. Genaue Lokalisation der Metastasen (Pfeile) in der Computertomographie (Mitte) durch exakte Fusion der Indium-111-SPECT-Untersuchung mit einem Hybrid-SPECT/CT-Scanner. Abbildung 4: SPECT/CT: Schwächungskorrektur durch die Computertomographie. Die Phantommessung (= Zy­linder, gefüllt mit radioaktivem Tracer) zeigt den Effekt der so genannten Schwächung: Die Strahlung, die aus den zentralen Arealen des Phantoms stammt, wird auf ihrem Weg nach außen durch die Dicke des Phantomkörpers (= „weiterer Weg“) mehr abgeschwächt als die Strahlung der äußeren Phantomregionen. Das heißt, die Strahlung der inneren Phantomregionen wird durch die SPECT-Untersuchung falsch bewertet (zu niedrig). Dadurch entsteht der „schwarze Ring“ im Phantombild links. Die Schwächungskorrektur der SPECT/CT korrigiert diesen Effekt und liefert nun Bilder mit der „wahren“ Intensitätsverteilung der Tracer-Anreicherung im Körper. Dadurch lassen sich zentral im Körper gelegene Tumoren besser entdecken, die sich nach erfolgter Schwächungskorrektur intensiver abbilden (siehe Bild oben, L = Leber). Außerdem wird dadurch eine exakte Quantifizierung der Tracer-Anreicherung im Tumor und den Organen möglich, was bei der Dosimetrie (= Kalkulation der notwendigen bzw. möglichen Dosis) vor einer geplanten Radiopeptidtherapie (z.B. Yttrium-90-DOTATOC) notwendig ist. Für die Ermittlung der Strahlendosen müssen sowohl die Radioaktivitätskonzentration im Zielorgan als auch dessen Größe exakt bestimmt werden. Unter Einsatz konventioneller nuklearmedizinischer Messgeräte ist die Bestimmung der Radioaktivitätskonzentration im Zielorgan schwierig, da die erhaltenen Messwerte durch die Abschwächung der Strahlung aus dem Körperinneren deutlich zu niedrig sind, also auch die Tumordosis unterschätzt würde (Abb. 4). Mit Hilfe der SPECT/CT-Hybrid-Kamera lassen sich diese so genannten Schwächungsartefakte korrigieren, da das CT-Bild zur Berechnung dieser Größe herangezogen werden kann. Gleichzeitig besteht auch die Möglichkeit, im CT die Größe einzelner Tumorherde oder auch anderer Organe des Körpers wie etwa der Niere zu bestimmen. Dr. med. Anton Nömayr, Nuklearmedizinische Klinik und Poliklinik, Universitätsklinikum Erlangen 31 Diagnostik Die Nuklearmedizinische Klinik des Universitätsklinikums Erlangen stellt sich vor Unter Nuklearmedizin versteht man die Anwendung offener radio­ aktiver oder radioaktiv markierter, d. h. Strahlung aussendender Sub­ stanzen (Radiopharmaka) für die Diagnostik und Therapie von Krankheiten. Modernste Verfahren für Diagnostik und Therapie Die Nuklearmedizinische Klinik in Erlangen wurde 1973 als eine der ersten eigenständigen Kliniken ihres Fachgebietes in Deutschland gegründet und wird seit 1999 von Herrn Prof. Dr. med. Torsten Kuwert geleitet. In ihren beiden Standorten bietet sie das komplette Spektrum nuklearmedizinischer Verfahren mit den jeweils modernsten Geräten an. Dazu gehören die Szintigraphie mit modernen Gammakameras, ferner Schichtaufnahmetechniken wie die Einzelphotonenemissions-Computertomographie (SPECT) und die Positronenemissionstomographie (PET). Ein besonderer Schwerpunkt der Klinik ist die vergleichende Bildgebung zwischen PET/SPECT einerseits und den radiologischen Schnittbildverfahren CT/MRT (Röntgencomputertomographie/Mag­ netresonanztomographie) andererseits. Der zweite wissenschaftliche Fokus ist die Neuentwicklung nuklearmedizinischer Methoden. Hierzu zählen die Entwicklung neuer Radiopharmaka und die Verbesserung von Verfahren für die Dosime­trie 32 von Therapien mit offenen Radio­ nukliden. Nuklearmedizinische In-vivo-Diagnostik Eine wichtige Aufgabe der Nuklearmedizinischen Klinik ist die Versorgung innerhalb des Uniklinikums mit diagnostischen Leistungen. Etwa 5.000 Patienten jährlich werden so untersucht. Das Spektrum der durchgeführten Untersuchungen reicht von verhältnismäßig einfachen, technisch weniger anspruchsvollen Untersuchungen wie der Schilddrüsenszintigraphie bis hin zu den nuklearmedizinischen Computertomographien SPECT und PET. Mit diesen Schnittbildver- Prof. Dr. med. Torsten Kuwert, Direktor der Nuklearmedizinischen Klinik des Universitätsklinikums Erlangen fahren lässt sich die Radioaktivitätsverteilung im Körper von Patienten dreidimensional darstellen. Als Weltneuheit wurde im Stammbereich der Klinik in der Krankenhausstraße 12 im März 2005 im Rahmen einer Forschungsleihe der Prototyp einer so genannten Hybridkamera aus SPECT und Spiral-CT aufgestellt (Abb. 1). Dieses Gerät wird kooperativ von der Nuklearmedizinischen Klinik und dem Abbildung 1: Ein besonderes Highlight: Im März 2005 wurde der europaweit erste Hybrid-SPECT/CT-Scanner im Universitätsklinikum Erlangen installiert. Nuklearmedizin Abbildung 2: Jod-131-SPECT/CT eines Patienten mit hoch differenziertem Schilddrüsenkarzinom. In der SPECT-Untersuchung zeigen sich zwei fokale, metastasenverdächtige Jod-131-Anreicherungen im Halsbereich (linkes Bild) – eine anatomische Zuordnung ist erst durch die exakte Fusion (mittleres Bild) mit der Computertomographie (rechtes Bild) möglich. Es handelt sich hier um verkalkte Lymphknotenmetastasen (rechtes Bild). T = Trachea (Luftröhre) Radiologischen Institut betrieben. Erste klinische Ergebnisse zeigen einen Qualitätssprung in der diagnostischen Genauigkeit im Vergleich zu alleinigen SPECT-Geräten (Abb. 2). Unter anderem durch die Möglichkeit zur so genannten Schwächungskorrektur verbessert dieses Gerät auch die Dosisfindung bei Therapien mit offenen Radionukliden, so etwa bei der Therapie des Schilddrüsen-Karzinoms mit Radiojod oder neuroendokriner Tumoren mit den DOTATOC-Derivaten (siehe dazu auch den Beitrag von Herrn Dr. Nömayr auf S. 28ff.). gen gut etabliert sind die Radio­ jodtherapien von Patienten mit Schilddrüsenkrebs und Schilddrüsenüberfunktion, die Behandlung der rheumatoiden Arthritis mit offenen radioaktiven Isotopen (Radio­ synoviorthesen) und die palliative Schmerztherapie. Neu eingeführt ist die Therapie maligner Bauchhöhlenergüsse mit Y-90-Silikat, die Behandlung des M. Bechterew mit Ra-224 und die Radioimmuntherapie von Lymphomen. Als einzige nuklearmedizinische Klinik Nordbayerns werden in Erlangen auch Behandlungen eines bösartigen kindlichen Tumors des Nebennierenmarkes, des Neuroblastoms, mit I-131-MIBG durchgeführt. Zusätzlich besteht seit kurzem in Erlangen Nuklearmedizinische Therapiestation Aus strahlenschutzrechtlichen Gründen müssen die meisten nuklearmedizinischen Therapieformen in Deutschland stationär durchgeführt werden. Die mit sechs Betten ausgestattete nuklearmedizinische Therapiestation ist im Südflügel des Altbaus der Medizin untergebracht. Hier werden jährlich knapp über 400 Patienten betreut. Das Spektrum der durchgeführten Behandlungen ist ausgesprochen breit: Seit Jahrzehnten in Erlan- Abbildung 3: Hybrid-PET/CT-Scanner der neuesten Generation: Hochauflösende Positronenemissionstomographie kombiniert mit Hochleistungs-Spiral-Computer­ tomographie (64-Zeilen-Scanner).­ 33 Nuklearmedizin auch die Möglichkeit, neuroendokrine Tumoren mit Y-90-DOTATOC zu behandeln. Die therapeutische Vorgehensweise wird hierbei einem gemeinsam mit weiteren deutschen Universitätskliniken unter Führung des Ausschusses „Therapie“ der Deutschen Gesellschaft für Nuklearmedizin erarbeitetem Protokoll entsprechen. Ausblick Im Laufe des Jahres 2006 wird der Ausbau der Klinik weiterge- hen. Das im März 2005 aufgestellte SPECT/CT-Gerät beinhaltet eine SPECT-Kamera mit einem Zweidetektor-Spiral-CT und wird im Mai 2006 durch eine Hybridkamera mit einem Sechsdetektor-CT ersetzt. Die Nuklearmedizinische Klinik wird dann voraussichtlich die erste Klinik in Deutschland sein, in der eine SPECT-Untersuchung mit einer kontrastmittelgestützten CT in ausreichender diagnostischer Qualität durchgeführt werden kann. Im Herbst dieses Jahres wird der Klinik ein weiteres Highend-HybridGerät durch Fortsetzung der Koo- peration mit der Firma Siemens Medical Solutions im Imaging Sciences Institute (ISI) zur Verfügung stehen, eine Hybridkamera aus PET und einem 64-Zeilen-Spiral-CT (Abb. 3). Auch von dieser Kamera, die derzeit kommerziell noch nicht verfügbar ist, ist ein weiterer Sprung in der diagnostischen Genauigkeit zu erwarten. Prof. Dr. med. Torsten Kuwert, Direktor der Nuklearmedizinischen Klinik des Universitätsklinikums Erlangen Kontakt: Nuklearmedizinische Klinik Direktor Prof. Dr. med. Torsten Kuwert Stammbereich Medizin: • • • • • • Zuständig für alle Untersuchungen außer Hirn-SPECT und PET, zu finden im 3. Stock der Medizinischen Klinik Hausanschrift: Krankenhausstr. 12, 91054 Erlangen Pforte: Tel. 09131/85-3 34 34, -3 34 35 Sekretariat: Tel. 09131/85-3 34 11 E-Mail: [email protected] Terminvergabe zur Schilddrüsenuntersuchung : 09131/85-3 34 16 Alle anderen Untersuchungen anmelden unter : 09131/85-3 34 22 Teilbereich Kopfklinikum: • Zuständig für alle PET-Untersuchungen, alle Gehirn-SPECTUntersuchungen, Kinderonkologie, zu finden im Erdgeschoß des Kopfklinikums, neben der Röntgen-Abteilung • Hausanschrift: Schwabachanlage 6, 91054 Erlangen • Pforte: 09131/85-3 30 01, -3 30 02 • Terminvergabe: 09131/85-3 45 27 Weitere Informationen finden Sie im Internet unter: http://www.nuklearmedizin.klinikum.uni-erlangen.de Radioaktive Strahlung Radioaktive Strahlung entsteht beim Zerfall von nicht stabilen Atomkernen. Atomkerne enthalten praktisch die gesamte Masse eines Atoms und sind positiv geladen. Sie sind nur dann stabil, wenn die Zahl ihrer Bausteine (Protonen und Neutronen) nicht zu groß wird und wenn das Verhältnis von Protonen zu Neutronen bei den leichten Atomkernen etwa 1:1 und bei den schweren etwa 1:1,5 beträgt. Sind diese Bedingungen nicht erfüllt, ist der Atomkern bestrebt, sich in eine günstigere Konfiguration umzuwandeln. Bei dieser Umwandlung werden Teilchen und Energie frei – die radioaktive Strahlung. Zu große Kerne setzen meist einen Teil des Atomkerns in Form eines Heliumkerns (2 Protonen und 2 Neutronen) frei, was als Alpha-Strahlung bezeichnet wird. Kerne mit einer zu großen Neutronenzahl im Verhältnis zur Protonenzahl senden ein Elektron und ein Antineu­trino aus. Diese schnellen, energiereichen Elektronen werden Beta-Strahlung genannt. Kerne mit einem zu hohen Energieinhalt geben das Zuviel als Wellenstrahlung ab, die sog. Gamma-Strahlung. Die Durchdringungsfähigkeit dieser Wellenstrahlung ist sehr viel größer als die der Teilchenstrahlung. 34 Bei einer nuklearmedizinischen Untersuchung wird dem Patienten eine radio­ aktive Substanz injiziert, die je sich je nach Verstoffwechselung in bestimmten Organen anreichert. Die von diesem Radiopharmakon ausgesandte Strahlung lässt sich vor allem für diagnostische Zwecke nutzen. Da radioaktive Strahlen Zellen und Gewebe schädigen, muss die Strahlendosis möglichst niedrig gehalten werden. Sie ist abhängig von: •der Menge des radioaktiven Stoffes, •dem verwendeten Isotop (möglichst kurze physikalische Halbwertszeit), •der Art des Zerfalls (möglichst nur Gamma-Strahlung), •der Verteilung im Körper (möglichst nicht in strahlensen-­ siblen Organen), •den Körperfunktionen, z.B. der Nierenfunktion bei renal ausgeschiedenen Substanzen. B. S. Behandlungsmöglichkeiten Medikamentöse Therapie bei neuroendokrinen Tumoren Allgemeines Therapiekonzept Neuroendokrine Tumoren des Magen-Darm-Trakts und der Bauchspeicheldrüse werden häufig pauschal unter dem Begriff „neuroendokrine Tumoren“ zusammengefasst. Dabei bilden diese Tumoren keine als Einheit zu betrachtende Tumorgruppe, sondern es handelt sich hierbei um Tumoren mit unterschiedlichem Ursprungsort (Magen, Dünndarm, Dickdarm, Pankreas), unterschiedlicher Aktivität (hormonaktive Tumoren, die das Karzinoid-Syndrom verursachen, nicht hormonaktive Tumoren), individuell unterschiedlicher Tumorbiologie (benigne, niedrig maligne, hoch maligne) und unterschiedlichem Wachstumsverhalten (kein Wachstum, langsames Wachstum, rasches Wachstum). Angesichts der Heterogenität der neuroendokrinen Tumorerkrankungen und der Vielfalt der Therapieoptionen ist ein individuell auf die jeweilige Tumorerkrankung abgestimmtes Therapiekonzept sinnvoll und notwendig. Hierfür ist die Zusammenarbeit und gemeinsame Therapieplanung von betroffenem Patient und Ärzten verschiedener Fachdisziplinen erforderlich (Abb. 1). Individuelle Therapieziele erfordern maßgeschneiderte Therapiestrategien Das primär angestrebte Therapieziel bei neuroendokrinen Tumoren ist immer die vollständige operative Entfernung des Tumors. Häufig sind zum Zeitpunkt der Diagnosestellung jedoch bereits Tumorabsiedelungen in der Leber (= hepatische Metastasen) oder außerhalb der Leber (= extrahepatische Metastasen) bekannt. Falls diese nicht ebenfalls durch eine Operation komplett entfernt werden können (= nicht operabler Tumor bzw. nicht operable Tumormetastasen), müssen anschließend weitere Therapieschritte folgen. Im Einzelfall kann bei engmaschiger Verlaufsbeobachtung der Tumorgröße eine zunächst rein abwartende Haltung (= „Wait and See“-Strategie) bis zum Nachweis einer Tumorgrößenzunahme (= Tumorprogression) gerechtfertigt sein. Medikamentöse Therapiekonzepte, die nachfolgend genauer dargestellt werden, umfassen die Biotherapie und die Chemotherapie. Weitere Priv.-Doz. Dr. med. C. J. Auernhammer, Medizinische Klinik II, Standort Großhadern, Klinikum der Ludwig-MaximiliansUniversität München ergänzende Therapiekonzepte sind verschiedene lokal-ablative Maßnahmen bei hepatischen Metastasen und die Radiorezeptortherapie bei hepatischen und extrahepatischen Metastasen. Das Therapieziel und die im Einzelfall anzuwendende Therapiestrategie müssen jeweils individuell festgelegt werden (Abb. 2). Heterogenität der NET Unterschiedliches Wachstumsverhalten Vielfältige Therapieoptionen Patient/in Enge Zusammenarbeit Chirurgie Endokrinologie Gastroendokrinologie Onkologie Nuklearmedizin Radiologie Individuelle Therapieoptimierung multimodaler und interdisziplinärer Ansatz Verbesserung des Langzeitüberlebens Verbesserung / Erhaltung der Lebensqualität Abbildung 1: Voraussetzung für die Entwicklung des optimalen Therapiekonzepts ist die enge Zusammenarbeit zwischen Patient und allen behandelnden Ärzten. 35 Behandlungsmöglichkeiten Lokal-ablative Methoden l Chemoembolisation (TACE) l Radiofrequenzablation (RFA) l Selektive intraarterielle Radionuklidtherapie (SIRT) l andere Chirurgische Therapie l vollständige Tumorentfernung l Tumorverkleinerung l Inoperabilität Radiorezeptortherapie l 111 Indium l 90 Yttrium l 177 Lutetium l andere „Wait and See” Biotherapie l Somatostatinanaloga l Interferon Chemotherapie l Streptozotocin / Doxorubicin l Streptozotocin / 5-Fluoruracil l Cisplatin / Etoposid l „neue” Substanzen Abbildung 2: Welche der heute für die Behandlung neuroendokriner Tumoren zur Verfügung stehenden Verfahren eingesetzt werden, hängt von den spezifischen Eigenschaften des Tumors und dem Stadium der Erkrankung ab. Prinzipielle Therapiestrategien bei nicht kurativ operablen NET endokrin aktiver NET Symptome hoch differenziert langsames Tumorwachstum gering differenziert, kleinzellig rasches Tumorwachstum Symptomatische Therapie Antiproliferative Therapie Antiproliferative Therapie Chemotherapie* Biotherapie *für alle NET unabhängig von der Primärlokalisation Biotherapie l Somatostatinanaloga Somatostatin INF-α l Interferon-α spezielle Pharmakotherapie Chemotherapie* *nur für NET des Pankreas Loko-regionale ablative Therapie Radio-Rezeptortherapie Abbildung 3: Vorgehensweise bei nicht operablem Tumor bzw. nicht operablen Tumormetastasen. Beispiele für Therapiestrategien bei nicht kurativ operablen Tumoren Bei hormonaktiven Tumoren, die das Karzinoid-Syndrom mit chronischen Durchfällen und Flush-Symptomatik verursachen, besteht das Therapieziel häufig in einer symptomatischen Therapie (= Therapie zur Kontrolle der Beschwerdesymptomatik des 36 betroffenen Patienten durch Hemmung der Hormonproduktion und -freisetzung). Hierzu wird eine so genannte Biotherapie mit Somatostatinanaloga oder Interferon-α erfolgreich eingesetzt (Abb. 3). Eine antiproliferative (= wachstumshemmende) Therapie ist dagegen bei allen nicht operablen Tumoren mit in der Verlaufskontrolle nachweisbarem Tumorwachstum in- diziert. Bei den häufiger vorkommenden neuroendokrinen Karzinomen, die vom Pathologen als hoch differenzierte Tumoren mit meist niedrigen Proliferationsmarkern (= niedrig maligne Karzinome) beschrieben werden und die in den regelmäßig durchgeführten Verlaufskontrollen ein nur langsames Tumorwachstum aufweisen, steht eine Reihe verschiedener Therapieoptionen (Biotherapie, Chemotherapie, lokal-ablative Therapieverfahren, Radiorezeptortherapie) zur Verfügung (Abb. 3). Bei den seltener vorkommenden neuroendokrinen Karzinomen die vom Pathologen als gering differenzierte Tumoren mit hohen Proliferationsmarkern (= hoch maligne Karzinome) beschrieben werden und die in den regelmäßig durchgeführten Verlaufskontrollen ein sehr rasches Tumorwachstum aufweisen, ist meist eine systemische Chemotherapie notwendig (Abb. 3). Medikamentöse Therapieoptionen Biotherapie Die Biotherapie beinhaltet die Behandlung mit den Somatostatinanaloga Octreotid oder Lanreotid sowie die Behandlung mit Interferon-α. Die meisten hoch differenzierten neuroendokrinen Tumorzellen weisen auf ihrer Zelloberfläche Rezeptoren (= Bindungsstellen) für die körpereigenen Substanzen Somatostatin oder Interferon-α auf (Abb. 4). Durch die Bindung der jeweiligen Wirkstoffe an die Rezeptoren kommt es in den Tumorzellen: 1. zur Hemmung der Hormonausschüttung und damit zur Kontrolle der Beschwerdesymptomatik Behandlungsmöglichkeiten (= symptomatische Therapie bei Patienten mit Karzinoid-Syndrom) und 2. zur Vermittlung von wachstumshemmenden Effekten auf die Tumorzellen ( = antiproliferative Therapie). Durch Somatostatinanloga kann bei Patienten mit Karzinoid-Syndrom eine Kontrolle der Beschwerde­ symptomatik in 70–80 % der Fälle erreicht werden. Keine weitere Tumorprogression (= Hemmung des weiteren Tumorwachstums) lässt sich durch Somatostatinanlaoga in 55–75 % erreichen; eine partielle Tumorregression (= teilweise Verkleinerung der bestehenden Tumormasse) kann dagegen nur in maximal 10 % erwartet werden. In Deutschland ist zurzeit (Stand 04/2006) ausschließlich das Somatostatinanalogon Octreotid zur Therapie von Patienten mit neuroendokrinen Tumoren zugelassen; das Somatostatinanalogon Lanreotid ist in anderen europäischen Ländern für diese Indikation ebenfalls zugelassen. Die beiden Somatostatinanaloga werden meist als ähnlich effektiv beschrieben. Als Therapiestandard wird Octreotid als langwirksames Depotpräparat „Octreotid LAR“ alle 4 Wochen in einer Dosis von 20 oder 30 mg in den Gesäßmuskel injiziert. Zur Therapieeinleitung oder gelegentlich als Zusatzmedikation kann kurzwirksames Octreotid in einer Dosis von 100 bis 500 µg dreimal täglich subkutan (= unter die Haut) injiziert werden. Typische mögliche Nebenwirkungen aller Somatostatinanaloga sind Übelkeit, Blähungen, Bachschmerzen, Durchfälle, Ausbildung von in der Mehrzahl der Fälle asymptomatischen (= nicht Beschwerden verursachenden) Gal- Somatostatin-Rezeptor Interferon-Rezeptor IFN-α Somatostatinanalogon neuroendokrine Tumorzelle Hemmung der Hormonsekretion der Tumorzellen Antiproliferative Effekte Symptomkontrolle Abildung 4: Prinzip der Biotherapie: Durch die Bindung der Wirkstoffe Somatostatinanalogon und Interferon-α an den spezifischen Rezeptoren auf der Zelloberfläche wird die Hormonsekretion bzw. das Tumorwachstum gehemmt. lensteinen. Falls Nebenwirkungen auftreten, sind diese meist mild und nehmen häufig im Verlauf der Therapie ab; eine Beendigung der Therapie ist nur selten notwendig. Durch Interferon-α lässt sich bei Patienten mit Karzinoid-Syndrom eine Kontrolle der Beschwerdesymptomatik in 40–70 % der Fälle erreichen. Keine weitere Tumorprogression (= Hemmung des weiteren Tumorwachstums) kann durch Interferon-α in 65–75 % erreicht werden; eine partielle Tumorregression (= teilweise Verkleinerung der bestehenden Tumormasse) kann nur in etwa 10 % erwartet werden. Zur Therapie werden 3 bis 5 Millionen Einheiten Interferon-α jeweils 3bis 5-mal pro Woche vom Patienten selbst subkutan (= unter die Haut) injiziert. Akute Nebenwirkungen von Interferon-α, die unmittelbar nach der Injektion auftreten, sind ein „grippeähnliches“ Beschwerdebild mit Fieber, Gliederschmerzen, Kopfschmerzen, Übelkeit und Abgeschlagenheit. Die möglichen Langzeitnebenwirkungen von Interferon-α sind vielfältig und zwingen in 15–20 % der Fälle zum Abbruch der Therapie. Von einigen Behandlungszentren wird in letzter Zeit wegen der besseren Verträglichkeit so genanntes „pegyliertes Interferon-α” als länger wirksames Depotpräparat gegeben. Pegyliertes Interferon-α ist jedoch für die Therapie bei neuro­ endokrinen Tumoren bisher nur wenig untersucht und nicht zugelassen. Aufgrund der besseren Verträglichkeit der Somatostatin­ analoga gegenüber Interferon-α wird eine Therapie mit Interferon-α hauptsächlich bei fehlendem Erfolg einer Therapie mit Somatostatin­ analoga in Erwägung gezogen. Chemotherapie Eine Chemotherapie von neuroendokrinen Karzinomen ist nur bei nachgewiesenem Tumorprogress (= Tumorwachstum) und durch andere Therapiemaßnahmen nicht kontrollierbarem Tumorwachstum 37 Behandlungsmöglichkeiten indiziert. Bei hoch differenzierten neuroendokrinen Tumoren des Pankreas kann eine Chemotherapie mit z.B. Streptozotocin/Doxorubicin mit relativ guter Ansprechwahrscheinlichkeit durchgeführt werden. Im Gegensatz dazu ist bei hoch differenzierten Tumoren des Darms eine Chemotherapie wegen der geringen Ansprechwahrscheinlichkeit im Allgemeinen nicht indiziert und es werden andere Therapieoptionen bevorzugt. Bei allen gering differenzierten, kleinzelligen, hochmalignen neuroendokrinen Tumoren kann eine Chemotherapie beispielsweise mit Cisplatin/Etoposid mit relativ guter initialer Ansprechwahrscheinlichkeit durchgeführt werden. Verschiedene neue Substanzen werden bei Pati- enten mit neuroendokrinen Karzinomen derzeit in klinischen Studien untersucht. Die so genannte adjuvante Chemotherapie (= Chemotherapie direkt nach einer Operation zur Verhinderung des Auftretens von Rezidiven oder Metastasen) oder neoadjuvante Chemotherapie (= Chemotherapie vor einer geplanten Operation zur Verkleinerung des Tumors vor der Operation) hat bei anderen Tumorarten zum Teil einen festen Stellenwert in der Therapie. Bei neuroendokrinen Karzinomen sind dagegen adjuvante oder neoadjuvante Chemotherapien bisher nicht untersucht und haben keinen etablierten Stellenwert. Ausblick Ein individuell auf die jeweilige Tumorerkrankung abgestimmtes Therapiekonzept ist angesichts der Heterogenität der neuroendokrinen Tumorerkrankungen und der Vielfalt der Therapieoptionen sinnvoll und notwendig. Durch interdisziplinäre Therapiekonzepte und eine individuelle Therapieplanung können eine Verbesserung des Langzeit­ überlebens und eine Verbesserung bzw. Erhaltung der Lebensqualität der betroffenen Patienten erreicht werden. PD Dr. med. C. J. Auernhammer, Medizinische Klinik II, Standort Großhadern, Klinikum der Ludwig-MaximiliansUniversität München Buchtipp Neu in der Reihe „Manuale des Tumorzentrums München”: Endokrine Tumoren Das Tumorzentrum München (TZM) ist eine Einrichtung an den Medizinischen Fakultäten der beiden Münchner Universitäten, der Ludwig-Maximilians-Universität und der Technischen Universität München. Seit 1983 publiziert das TZM in regelmäßiger Folge Empfehlungen zur Diagnostik, Therapie und Nachsorge in Form der „Blauen Manuale“. Bislang sind 17 Manuale erschienen, die von den verschiedenen Projektgruppen des TZM erarbeitet wurden. Zielsetzung ist, Ärzte kompakt und umfassend über die jeweils wissenschaftlich gesicherten Standards der Betreuung krebskranker Patienten zu informieren. Die Manuale sind nach den Prinzipien der „Evidence Based Medicine (EBM)“ ausgerichtet und die Empfehlungen stehen in Übereinstimmung mit den vom Informationszentrum für Standards in der Onkologie (ISTO) der Deutschen Krebsgesellschaft (DKG) herausgegeben Leitlinien. Herausgeber des Manuals „Endokrine Tumoren” sind Prof. Dr. B. Göke (Med. Klinik II, Klinikum der Universität MünchenGroßhadern) und Prof. Dr. H. Fürst (Chirurgische Klinik, Krankenhaus Matha-Maria, München). Die darin beschriebenen Standards zur Diagnostik und Therapie wurden von fünf interdisziplinären Projektgruppen erarbeitet, die auf eine umfangreiche klinische Erfahrung zurückgreifen können. Daher enthalten die Therapiestrategien auch sehr detaillierte Vorschläge, die dem behandelnden Ärzt die oftmals komplizierte und folgenschwere Entscheidung erleichtern können. 38 Die 6 großen Kapitel sind nach dem Auftreten der Tumoren in verschiedenen Organsystemen gegliedert: • Maligne Tumoren der Schilddrüse • Nebenschilddrüsenkarzinom • Hypophysentumoren und andere selläre Raumforderungen • Tumoren der Nebenniere • Neuroendokrine Tumoren des Gastrointestinaltraktes • Multiple endokrine Neoplasien Für NET-Patienten von Interesse ist das Kapitel „Neuroendokrine Tumoren des Gastrointestinaltraktes”, das ausführlich über Klassifikation, Diagnostik sowie chirurgische und nicht-operative Therapie informiert. Allerdings ist, da es sich um ein Manual für Ärzte handelt, zum Verständnis medizinisches Grundwissen erforderlich. Das Manual können Sie über den Buchhandel bestellen. Es ist im Zuckschwerdt Verlag (München) erschienen und hat die ISBN-Nr. 3-88603-881-5. Der Umfang liegt bei 188 Seiten, der Preis beträgt 19,90 m. Noch ein Tipp: Auf der Internet-Seite des TZM finden Sie weitere Manuale zum Herunterladen: http://tzm.web.med.uni-muenchen.de. B. S. Behandlungsmöglichkeiten Lokale Therapieverfahren bei Lebermetastasen neuroendokriner Tumoren Neuroendokrine Tumoren werden oft erst dann symptomatisch, wenn sie Tochtergeschwülste (Metastasen) in der Leber gebildet haben. Die Patienten leiden dann unter der hormonellen Symptomatik (z.B. „Flush“ bei Karzinoiden mit Serotoninproduktion) oder unter dem Massenaspekt der Metastasen, der zu einer Vergrößerung der Leber und zur Verdrängung des gesunden Lebergewebes führt. Lebermetastasen neuroendokriner Tumoren sollten behandelt werden, da sie einen ungünstigen Faktor für das Überleben darstellen. Lebermetastasen, die nur eine langsame Wachstums­tendenz zeigen, können mit bildgebenden Verfahren (Ultraschall, Computertomographie, Kernspintomographie und Szintigraphie) beobachtet werden. Zeigt sich allerdings ein rasches Wachstum – das heißt, einzelne Herde nehmen innerhalb von 6 Monaten um mehr als 25% an Größe zu oder es treten neue Herde in der Leber auf –, so sollte eine Therapie zur Wachstumshemmung oder zur Zerstörung der Metastasen eingeleitet werden. Ein weiterer Grund für eine lokale Therapie der Lebermetastasen stellen zunehmende hormonelle Symptome dar, die durch die Basisbehandlung mit Somatostatinanaloga (Octreotid) oder a-Interferon nicht ausreichend beherrscht werden können. Operative Resektion, RF-Ablation und Lasertherapie nur bei vereinzelten Lebermetastasen sinnvoll Traditionell werden Lebermetastasen durch eine Operation chirurgisch entfernt. Vorteil der Methode ist, dass der Operateur den Leberherd komplett mit einem Saum von gesundem Gewebe herausschneidet und so eine vollständige Entfernung des jeweiligen Herdes möglich ist. Das Verfahren kann aber nur sinnvoll eingesetzt werden, wenn die Anzahl der Lebermetastasen begrenzt ist. Man geht heutzutage von maximal 5 Lebermetastasen aus, die aus der Leber „herausgeschält“ werden können. Gleiches gilt auch für moderne alternative Verfahren zur Zerstörung von Lebermetastasen, die Hitze verwenden, um die Leberherde thermisch zu vernichten. Sowohl die Radiofrequenzablation (RF-Ablation) als auch die Lasertherapie (LITT) kann sinnvoll nur beim Vorliegen von bis zu 5 Metastasen angewendet werden. Zusätzlich lassen sich diese beiden neueren Verfahren auch nur bei Metastasen bis zu maximal 5 cm Durchmesser erfolgreich anwenden. Gegenüber der chirurgischen Metastasenresektion besitzen die beiden genannten Verfahren den Vorteil, dass das Tumorgewebe durch einen Einstich in der Haut (perkutan) und ohne das Eröffnen des Bauchraumes durch einen Schnitt zerstört werden kann. Prof. Dr. Hans-Joachim Wagner, Klinik für Strahlendiagnostik, Philips-Universität Marburg Neue Verfahren zur selektiven Tumorzerstörung bei zahlreichen Lebermetastasen Leider findet sich bei neuroendokrinen Tumoren sehr häufig eine Metastasierung der Leber, die durch viele (in der Regel deutlich mehr als fünf) und unterschiedlich große Herde gekennzeichnet ist. Abbildung 1 zeigt eine typische Lebermetastasierung eines neuroendokrinen Tumors. In der Kernspintomographie finden sich viele Herde in beiden Leberlappen (links und rechts). Für Patienten mit einem derartigen Befund kommen die oben genannten lokal ablativen (zerstörendes) Verfahren – chirurgische Entfernung (Resektion), RF-Ablation, LITT – nicht in Frage. Liegen zahlreiche Lebermetastasen vor, sollte die Leber als ganzes Organ behandelt werden. Da die Tochtergeschwülste neuroendokriner Tumoren häufig auf die Leber begrenzt bleiben und die Lebenserwartung der Patienten vor allem durch die Lebermetastasen bestimmt wird, ist es sinnvoll, die Leber gezielt zu therapieren. Damit kann der restliche Körper geschont und die gesamte Dosis der tumorzerstörenden Substanz kann di39 Behandlungsmöglichkeiten Abbildung 1: Kernspintomographie der Leber. In beiden Leberlappen findet sich eine Vielzahl von Metastasen ( ). * rekt in die Leber gegeben werden (lokoregionäre Therapie). So lässt sich eine hohe Dosis in der Leber erreichen und gleichzeitig können systemische Nebenwirkungen der tumorzerstörenden Substanz minimiert werden. In diesem Sinne kommen zwei Therapierverfahren zur Anwendung, die im Weiteren kurz besprochen werden sollen: die transarterielle Chemoembolisation (TACE) und die selektive interne Radiotherapie (SIRT). Beide Techniken machen sich zu Nutze, dass die Lebermetastasen fast zu 100% aus dem Blut der Leberarterie versorgt werden, während das normale Lebergewebe nur zu ca. 25% aus der Leberarterie und zu 75% aus der Pfortader (dem zweiten Gefäßsystem der Leber) Sauerstoff und Nährstoffe erhält. Wählt man also eine Therapie über die Leberarterie, kann man selektiv die Metastasen schädigen, während man das gesunde Lebergewebe schont. 40 Transarterielle Chemoembolisation (TACE) Bei der TACE sondiert man von der Leiste aus die Leberarterie mit einem kleinen Kunststoffschlauch (Katheter; Durchmesser weniger als 2 mm). Sobald man die Spitze des Katheters in der rechten oder linken Leberarterie positioniert hat, kann man über den Katheter ein Zellgift (Zytostatikum) in die Arterie leiten. Dieses wird gemischt mit einem ölhaltigen Kontrastmittel (Lipiodol), um das Zytostatikum besser an die bösartigen Zellen zu transportieren und es dort festzuhalten. Vorteil der Technik ist, dass man die gesamte Menge des Zytostatikums direkt in die Leber gibt, während bei der üblichen Einspritzung in eine Vene am Arm (systemische Chemotherapie) nur ein Bruchteil der Gesamtmenge tatsächlich in die Leber kommt. Nach der Einspritzung des Zytostatikums/Kontrastmittelgemischs wird die Leberarterie verschlossen, indem man rundliche Partikel eines Kunststoffes (meist Polyvinylalkohol) mit einem Durchmesser von ca. 0,2–0,7 mm in die Arterie spritzt. Diese Partikel verstopfen die Arterie und führen dazu, dass kein Blut mehr über die Leberarterienäste zur Metastase fließen kann. Da diese, wie oben gesagt, zu fast 100% von der Arterie versorgt wird, geht die Metastase zusätzlich zur Schädigung durch das Zytostatikum auch wegen Blut- und Sauerstoffmangel zugrunde (Nekrose). Weil man nicht die ganze Leber in einer einzigen Sitzung behandeln kann, wird jeweils nur ein Teil der Leber mit TACE behandelt und die Therapie in sechs- bis achtwöchigen Abständen wiederholt, bis alle Metastasen therapiert wurden. Abbildung 2 zeigt ein Computertomogramm vor der TACE-Behandlung (Abb. 2a) und die Behandlung selbst (Abb. 2 b und c). Das Computertomogramm nach TACE (Abb. 2d) belegt, dass die Lebermetastasen gut getroffen wurden, das übrige Lebergewebe aber geschont werden konnte. Selektive interne Radiotherapie (SIRT) Auch bei der zweiten transarteriellen Behandlungsform, der selektiven internen Radiotherapie (SIRT), wird ein Katheter von der Leiste aus in die Leberarterie gelegt. Durch diesen werden dann winzige Kügelchen, die als radioaktiven Strahler Yttrium-90, enthalten, in die Leber eingespritzt. Die Kügelchen bleiben in den tumorversorgenden feinen Ästen der Leberarterien hängen. Von dort aus wirkt der radioaktive Strahler auf die Tumorzellen. Yttrium-90 hat nur eine sehr kurze Reichweite von maximal 1 cm. Behandlungsmöglichkeiten Abbildung 2: Transarterielle Chemoembolisation (TACE). a) Computertomographie der Leber mit Kontrastmittel. In der Leber finden sich mehrere Metastasen ( ) eines * neuroendokrinen Tumors. b) Angiographie. Die Spitze (Pfeil) des Katheters liegt in der Leberarterie. Beim Einspritzen des Kontrastmittels zeigt sich eine kräftige Durchblutung der Metastasen. c) Mit einem sehr kleinen Katheter (Pfeil) wird die linke Leberarterie selektiv sondiert. Nun kann das Gemisch aus Zytostatikum und Lipiodol verabreicht werden. Danach erfolgt der Verschluss der Leberarterie durch die Kunststoffpartikel. d) Das Computertomogramm etwa 3 Tage nach der TACE zeigt das ölhaltige Kontrastmittel vorwiegend in den Lebermetastasen des linken Lappens ( ). * Das umliegende Lebergewebe wird geschont, behandelt wird vor allem der Tumor. 41 Behandlungsmöglichkeiten Abbildung 3: Selektive interne Radiotherapie (SIRT). a) Computertomographie der Leber. Man erkennt zahlreiche Metastasen ( ) eines neuroendokrinen Tumors in der Leber. * b) Computertomographie 9 Monate nach SIRT. Alle Lebermetastasen wurden durch die Bestrahlung erfolgreich zerstört. Dadurch werden ausschließlich die Metastasen und die Leber bestrahlt. Der Strahler zerfällt mit der Zeit zu einem nicht mehr radioaktiven, ungefährlichen Stoff. Nach etwa 14–21 Tagen ist mit keiner Strahlung mehr zu rechnen. Aufgrund der extrem kurzen Reichweite dringt keine wesentliche Strahlung nach außen, so dass die Behandlung keine besonderen Strahlenschutzmaßnahmen erfordert und auf einer normalen Station erfolgen kann. Der Patient kann nach wenigen Tagen wieder nach Hause entlassen werden. Abbildung 3 zeigt einen Behandlungserfolg nach einmaliger SIRT. Die zahlreichen Lebermetastasen konnten durch die Bestrahlung vollständig zerstört werden. Alle in diesem Beitrag genannten Behandlungsmethoden haben natürlich, wie jede medizinische Therapie, auch Nebenwirkungen und Komplikationen. Die Darstellung der unerwünschten Wirkungen und spezifischer Komplikationen der TACE und SIRT würde den Rahmen dieses Artikels sprengen. Deshalb sollen sowohl diese Aspekte als auch die Ergebnisse, die sich mit den beiden therapeutischen Möglichkeiten erzielen lassen, in einem separaten Artikel in Glandula NeT 8 beschrieben werden. Prof. Dr. Hans-Joachim Wagner, Klinik für Strahlendiagnostik, Universitätsklinikum Marburg und Gießen GmbH, Marburg Selektive interne Radiotherapie mit SIR-Spheres® SIR-Spheres sind winzige Plastikkügelchen (Durchmesser 0,032 mm), die Yttrium-90 enthalten und daher Betastrahlen aussenden. Sie werden über einen Katheter von der Leiste aus in die Leberarterie injiziert (Bild ) und wandern mit dem Blutstrom in die tumorversorgenden Gefäße. Dort bleiben die Kügelchen in den feinen Arterien hängen (Bild ). Der darin enthaltene radioaktive Strahler wirkt aufgrund seiner geringen Reichweite selektiv auf die Tumorzellen, das heißt, das weiter entfernte gesunde Gewebe bleibt weitgehend unbeschädigt. Die Injektion der SIR-Spheres dauert 15 bis 20 Minuten, die gesamte Prozedur etwa 1 Stunde. 42 Weitere Informationen finden Sie auf der Internetseite der Firma Sirtex: www.sirtex.com. Dort gibt es auch eine Patientenbroschüre zum Herunterladen (allerdings nur in englischer Sprache). B. S. Behandlungsmöglichkeiten Neue Ansätze in der medikamentösen Therapie: Angiogenese-Inhibitoren, neue Somatostatinanaloga und andere neue Behandlungsoptionen Zur medikamentösen Therapie von metastasierten neuroendokrinen Tumoren stehen Somatostatinanaloga und Interferon-a, auch Biotherapie genannt, zur Verfügung. In nicht kontrollierten Untersuchungen konnte damit in etwa 40–50 % der Fälle ein wachstumshemmender Effekt erzielt werden. Nach neueren Studien wird ein wachstumshemmender Effekt in etwa 30 % der Fälle erreicht, wobei Tumorverkleinerungen eine Seltenheit darstellen. Die systemische Chemotherapie hat ihren Stellenwert bei wachsenden Bauchspeicheldrüsentumoren und schlecht differenzierten, aggressiv wachsenden Tumoren jeglicher Lokalisation. Die Radiorezeptortherapie (Yttrium-90-DOTATOC- bzw. Lutetium-177-DOTATATE-Therapie) kommt bei ausreichendem bzw. kräftigem Somatostatin-Rezeptorbesatz im Bereich der Tumorabsiedlungen zum Einsatz, in der Regel nach Versagen einer Biotherapie. Das Therapiespektrum wird erweitert durch lokale Maßnahmen, die gezielt die Leberabsiedlungen behandeln. Die meisten und längsten Erfahrungen liegen zum Einsatz der Chemoembolisation vor. Weitere Therapieverfahren stellen die Hochfrequenz-Thermotherapie (HFTT) und die Laser-induzierte Thermotherapie (LITT) dar. Dagegen spielen die Alkoholinjektion und Kryokoagulation heutzutage eine untergeordnete Rolle. Neue Therapieansätze haben Bedeutung bei Tumorwachstum, nach Versagen einer Therapie mit Somatostatinanaloga und/oder Interferona, bei fehlender Option einer Radionuklidtherapie (negatives Somatostatin-Rezeptor-Szintigramm) und bei Versagen einer systemischen Chemotherapie. Neue Therapieoptionen umfassen: • neue Somatostatinanaloga (z.B. Pasireotid, auch SOM230 genannt), • pegyliertes Interferon-a, • Hemmstoffe der Gefäßneubildung (Angiogenese-Inhibitoren) sowie • Hemmstoffe von Gefäßzellen und Tumorzellen. Somatostatinanaloga Natürliches Somatostatin vermittelt durch Bindung an Somatostatin-Rezeptoren SSTR-1 bis -5 hemmende Priv.-Doz. Dr. med. Marianne Pavel, Medizinische Klinik 1, Universitätsklinikum Erlangen Signale im Bereich von Gehirn, Magen-Darm-Trakt, Bauchspeichel­ drüse und Hirnanhangsdrüse. Das Somatostatinanalogon Octreotid bewirkt durch präferenzielle Bindung an die Somatostatin-Rezeptoren SSTR-2 und -5 hemmende Signale und damit eine Hemmung der Hormonausschüttung und des Tumorwachstums bei neuroendokrinen Tumoren. Der neue Somatostatinabkömmling Pasireotid (SOM230) vermittelt hemmende Signale über zwei weitere Somatostatin-Rezeptor-Subtypen, neben SSTR-2 und -5 auch über SSTR-1 und -3 (Abb. 1). Neue Somatostatinanaloga: SOM230 SOM230 SSTR-1 SSTR-2 SSTR-3 SSTR-4 SSTR-5 Hemmende Signale: } Hemmung der Hormonausschüttung bei NET Hemmung des Tumorwachstums ? Abbildung 1: SOM230 vermittelt hemmende Signale über 4 Somatostatin-RezeptorSubtypen (SSTR). 43 Behandlungsmöglichkeiten In einer ersten internationalen klinischen Studie konnte bei 28 Patienten mit Restbeschwerden unter Octreotid LAR (≥4 flüssige Stühle oder 2 Flush-Anfälle pro Tag) unter Einsatz von 2-mal täglich SOM230 eine Besserung der Beschwerden Flush und/oder Durchfall in etwa 30 % der Fälle erzielt werden. Hauptsächliche Nebenwirkungen waren Übelkeit (bei 28,6 % der Patienten), Bauchbeschwerden (bei 20,6 %) und Gewichtsverlust (bei 34 %). Durchfall und Blähungen waren mit 5,7 % selten. Ein Abbruch der Therapie aufgrund von Nebenwirkungen erfolgte bei 18 % der Patienten. Die Ergebnisse dieser Studie wurden im vergangenen Jahr von Larry Kvols (Tampa, Florida) auf dem amerikanischen Kongress für klinische Onkologie (ASCO) präsentiert. Ob durch Pasireotid eine stärkere Wachstumshemmung des Tumors im Vergleich zu Octreotid erzielt werden kann, muss in zuküftigen Studien untersucht werden. Die bisherigen Ergebnisse weisen darauf hin, dass das neue Somatostatinanalogon bei einem Drittel der Patienten Bedeutung hat, wenn Octreotid nicht mehr ausreichend wirksam ist. Interferon-a Bereits seit den 80er Jahren bestehen Erfahrungen zum Einsatz von Interferon-a bei der Behandlung von neuroendokrinen Tumoren. Eine Hemmung der Hormonsekretion und eine Besserung der Symptome Flush und Diarrhoe bei hormonell aktiven Tumoren werden in 40–70 % der Fälle erzielt. Eine Hemmung des Tumorwachstums wird bei 30–40 % der Patienten beobachtet. Die mittlere Dosierung liegt bei 3-mal 5 Mil44 Wirkspiegel des pegylierten Interferon-alpha im Vergleich zu nicht verändertem Interferon-alpha pegyliert nicht pegyliert Gleich bleibend hoher Wirkspiegel über 7 Tage Schneller Abfall des Wirkspiegels bereits am 2. Tag nach der Injektion Die Tumorabwehr bleibt gleichmäßig erhalten ➔immer wieder Verschnaufpause für Viren bzw. Tumorzellen Abbildung 2: Einer der Vorteile von Pegyliertem Interferon-a ist sein gleich bleibender Wirkspiegel. lionen IE pro Woche subkutan. Problematisch bei der konventionellen Interferon-a-Therapie sind grippeähnliche Symptome in 90 % der Fälle, Müdigkeit bei 70 % der Patienten und ein Gewichtsverlust in 50 % der Fälle. Duch Pegylierung von Interferon-a kann Interferon vor frühzeitigem Abbau geschützt werden. Dabei wird Interferon-a von einer Polyethylenglykol-(PEG-)Kette umgeben, die sich wie ein Schutzmantel um das Interferon-Molekül legt. Dadurch bleibt der Interferon-Spiegel im Körper über einen längeren Zeitraum gleichmäßig hoch (Abb. 2). Bei der bisherigen Interferon-a-Therapie dagegen fällt der Wirkstoffspiegel bereits am 2. Tag nach der Injektion wieder ab, so dass mindesten 3-mal wöchentliche Injektionen erforderlich sind, wobei keine kon­ stant hohen Wirkspiegel vorliegen. Im Gegensatz zum nicht pegylierten Interferon-a wird pegyliertes Interferon-a nur einmal wöchentlich subkutan injiziert. In der Universitätsklinik Erlangen wurde eine offene Studie an bisher mehr als 17 Patienten im Alter von 52–76 Jahren durchgeführt, davon hatten 10 Patienten einen hormonaktiven und 7 Patienten einen inaktiven Tumor. Bei allen Patienten lag vor Einleitung der Therapie ein Tumorwachstum vor. Alle Patienten wurden im Vorfeld mit Octreotid behandelt. Bei 6 Patienten war eine 3-mal wöchentliche Interferon-aTherapie nach dem konventionellen Schema durchgeführt worden, diese wurde jedoch bei allen Patienten aufgrund der genannten Nebenwirkungen abgebrochen. Bei den Patienten mit hormonell aktiven Tumoren konnten durch pegyliertes Interferon-a in 70 % der Fälle eine Verbesserung der Beschwerden Flush und Durchfall sowie ein Absenken der hormonellen Sekretion (Abnahme der 5-Hydroxyindolessigsäure-Exkretion im 24-StundenUrin) erzielt werden. Bei 11 von 17 Patienten wurde ein Wachstumsstillstand erreicht, bei 2 Patienten eine Tumorverkleinerung. Lediglich 2 von Behandlungsmöglichkeiten 17 Patienten beendeten die Therapie aufgrund von Nebenwirkungen nach 3 Monaten. Zu grippeähnlichen Beschwerden kam es bei 24 % der Patienten, zu leichtgradiger (nicht beeinträchtigender) Müdigkeit bei 47 % und zu einer Appetitminderung bei 18 %. Schwerwiegende Nebenwirkungen traten über einen mittleren Beobachtungszeitraum von 30 Monaten nicht auf. Fazit: Insgesamt erscheint pegyliertes Interferon-a eine gute Therapiealternative bei Patienten zu sein, die die konventionelle Interferon-aTherapie mit 3-mal wöchentlichen Injektionen nicht vertragen. Gefäßaussprossung Gefäßreicher Tumor Tumorzelleinbruch in Gefäß Metastasierung Stadien der Tumorentwicklung, bei denen die Blutgefäßneubildung eine Rolle spielt Abbildung 3: Bedeutung der Tumorgefäßneubildung bei Entstehung, Wachstum und Aussaat eines Tumors. VEGF und Rezeptoren Angiogenese-Inhibitoren (Hemmstoffe der Gefäßneubildung) Die Blutgefäßneubildung spielt eine Rolle bei verschiedenen Stadien der Tumorentwicklung. Sie hat Bedeutung bei Entstehung, Wachstum und Aussaat eines Tumors (Abb. 3). In neuroendokrinen Tumoren kann zu einem hohen Prozentsatz (nach eigenen Untersuchungen in 83 % der Fälle) ein Gefäßwachstumsfaktor (Vascular Endothelial Growth Factor, VEGF) nachgewiesen werden. Bei der feingeweblichen Untersuchung wird dieser durch entsprechende Färbemethoden im Tumormaterial nachgewiesen. Es gibt verschiedene Möglichkeiten, die Wirkung des Gefäßwachstumsfaktors VEGF an der Gefäßzelle zu hemmen. Zum einen lässt sich das im Körper zirkulierende VEGF durch einen Antikörper „wegfangen”, so dass eine Bindung an der Gefäßzelle nicht erfolgen kann. Zum anderen kann durch einen Antikörper gegen die Andockungsstelle eine Bindung des Gefäßwachstumsfak- Außenseite der Gefäßzelle VEGF-A VEGF-B Innenseite der VEGFR-1 Gefäßzelle Gefäßneubildung VEGF-A VEGF-C VEGF-E VEGF-C VEGF-D Antikörper gegen VEGF VEGFR-2 Gefäßneubildung Hemmstoffe der Rezeptoraktivierung Antikörper gegen Rezeptor VEGFR-3 Lymphgefäßneubildung Metastasierung Abbildung 4: Hemmung der Wirkung des Gefäßwachstumsfaktors VEGF (Vascular Endothelial Growth Factor) an der Gefäßwand: „Wegfangen” von VEGF durch Antikörper (Mitte) und Blockade der Bindungsstelle durch einen Antikörper gegen den Rezeptor in der Gefäßwand (rechts). tors an den Rezeptor (Andockstelle) verhindert oder die Vermittlung des Wachstumssignals in der Gefäßzelle unterbunden werden (Abb. 4). Auf diese verschiedenen Weisen lässt sich die Gefäßneubildung, die für die Ernährung und das Wachstum des Tumors essenziell ist, bremsen bzw. unterbinden. 45 Behandlungsmöglichkeiten Ein Antikörper gegen zirkulierendes VEGF (Bevacizumab/Avastin) ist bereits zur Behandlung des Dickdarmkrebses im Einsatz. In einer ersten amerikanischen Studie wurden günstige Effekte auch bei neuroendokrinen Tumoren beobachtet. Im Rahmen einer europaweiten Studie mit Bestimmung der Verstoffwechselung eines neuen Hemmstoffs der Gefäßneubildung, kurz PTK genannt, wurden erste Erfahrungen bei Patienten mit neuroendokrinen Tumoren an der Universitätsklinik in Erlangen gesammelt. Bei 9 Patienten im Alter von 34–69 Jahren mit neuroendokrinen Tumoren unterschiedlicher Lokali­ sation ohne hormonelle Aktivität wurde ein Tumoransprechen bei 4 Patienten für einen gewissen Zeitraum beobachtet, davon eine geringe Tumorrückbildung bei 2 Patienten und ein Wachstumsstillstand bei 2 weiteren Patienten. Ein Drittel der Patienten brach die Therapie aufgrund von Nebenwirkungen (vor allem Übelkeit, Erbrechen und Schwindel) ab, die allgemeine Verträglichkeit war gut. Hemmstoffe der Tumorund Gefäßzelle Viel versprechende neue Therapieentwicklungen stellen die Hemmstoffe dar, die sowohl an der Tumorzelle als auch an der Gefäßzelle wirksam sind. Diese Hemmstoffe richten sich gegen Wachstumsfaktor-Rezeptoren an der Tumor- oder Gefäßzelle und gegen relevante Strukturen in der Zelle, die für die Zellteilung verantwortlich sind bzw. Schaltstellen des Tumorwachstums darstellen (Abb. 5). Hemmstoffe dieser Art werden auch mit dem Begriff „multiples Targeting” umschrieben. 46 Gefäße Tumor Hemmstoffe PDGFR VEGFR c-kit Tumorzelle Gefäßzelle Abbildung 5: Multiples Targeting: Angriff an mehreren Zielstellen, die an der Tumorzelle und der Gefäßzelle Wachstum vermitteln. PDGFR und VEGFR = Rezeptoren („Andockstellen”) für Wachstumsfaktoren. In den USA wurde von März 2003 bis März 2006 bereits an 100 Patienten mit neuroendokrinen Tumoren (60 % Pankreas-Tumoren, 40 % Karzinoid-Tumoren) eine Behandlung mit einem derartigen Hemmstoff (Sunitinib) durchgeführt. Erste Ergebnisse dieser Studie wurden auf dem europäischen Kongress für klinische Onkologie (ECCO) im November 2005 in Paris vorgestellt. Unter der früh begonnenen Behandlung war in 81 % der Fälle die Tumorerkrankung stabil, eine Tumorverkleinerung wurde bei 10 % der Betroffenen beobachtet. Weitere Studien zu Substanzen, die sich gegen relevante Schaltstellen in Tumor- und Gefäßzellen richten, werden in Zukunft folgen. Priv.-Doz. Dr. med. Marianne Pavel, Universitätsklinikum Erlangen Bei Fragen zu neuen Therapieoptionen können Sie sich gerne an Frau Priv.-Doz. Dr. med. Marianne Pavel wenden. Sie erreichen Sie unter folgender Adresse: Universitätsklinikum Erlangen Medizinische Klinik I Ulmenweg 18 91054 Erlangen E-Mail: [email protected] Verlaufsberurteilung Bedeutung von Chromogranin A als Tumormarker Tumormarker im Serum oder Plasma dienen bis auf wenige Ausnahmen in aller Regel nicht der Frühdiagnostik einer Tumorerkrankung, sondern der Beurteilung des individuellen Verlaufs. Beispiele sind das „Prostata-Spezifische-Antigen“ (PSA), das sich sowohl zur Frühdiagnostik als auch zur Beurteilung des Verlaufs eines Prostatakarzinoms eignet. Das „Carcino-Embryonale-Antigen“(CEA) ist dagegen ein Beispiel für einen Tumormarker, der zur Verlaufsbeurteilung eines bösartigen Dickdarmtumors oder eines medullären Schilddrüsenkarzinoms herangezogen wird. Das „Alpha-1-Foetoprotein“(AFP) dient zur Verlaufsbeurteilung eines primären Leberkarzinoms und das „CA19-9“ zur Verlaufsbeurteilung eines Pankreaskarzinoms. Ähnliche Tumormarker gibt es auch zur Beurteilung des Verlaufs von gynäkologischen Tumoren wie dem Ovarialkarzinom und des Brustkrebses oder des Hodenkrebses bzw. des kleinzelligen Bronchialkarzinoms. Wie ist es bei den neuroendokrinen Tumoren? Verlaufsbeurteilung bei funktionell aktiven neuroendokrinen Tumoren anhand der freigesetzten Hormone Bei dieser seltenen Tumorerkrankung unterscheidet man funktionell aktive und funktionell inaktive Tumoren. Die funktionell aktiven Tumoren sind durch Krankheitsbilder gekennzeichnet, die weniger durch das Tumorwachstum als vielmehr durch die vom Tumor freigesetzten Hormone geprägt sind. Beispiele sind das Insulinom, das durch Unterzuckerungszustände bis hin zum Koma als Folge der ungebremsten Insulinfreisetzung aus den Tumorzellen charakterisiert ist. Beim Zollinger-Ellison-Syndrom (ZES oder Gastrinom) produzieren die Tumorzellen Gastrin. Gastrin wiederum stimuliert die Säuresekretion des Magens. So entstehen gefährliche Geschwüre im Magen und Zwölffingerdarm, die bluten oder sogar durchbrechen können. Auch die für das ZES typischen Durchfälle sind Folge der ungezügelten Gastrinfreisetzung aus dem Tumor. Weitere Beispiele sind das Karzinoid-Syndrom mit seinen FlushAnfällen und Durchfällen, die durch vasoaktive Hormone (Flush) und Serotonin (Durchfall) ausgelöst werden. Beim Glukagonom-Syndrom werden der typische Hautausschlag durch die Überproduktion von Glukagon, beim Verner-Morrison-Syndrom die Durchfälle durch vasoaktives intestinales Polypeptid (VIP) bedingt. In diesen Fällen eignet sich die Bestimmung des jeweiligen Hormons nicht nur zur Diagnose des Krankheitsbildes, sondern auch zur Verlaufsbeurteilung der Tumor­ erkrankung. Unter Verlaufsbeurteilung ist zu verstehen: Normalisierung des Tumormarkerwertes nach kurativer Operation, Anstieg des Markers als Folge eines zunehmenden Tumorwachstums oder bei Wiederauftreten des Tumors nach vorausgegangener Operation oder anderen therapeutischen Maßnahmen. Prof. Dr. med. R. Arnold, München Besonderheiten von Chromogranin A Etwa die Hälfte aller neuroendokrinen Tumoren sind funktionell inaktiv, weil die Tumorzellen zwar Hormone produzieren und auch ins Blut freisetzen, diese Hormone aber zu keinen Symptomen oder Beschwerden führen. Funktionell inaktive neuroendokrine Tumoren werden daher entweder zufällig anlässlich einer routinemäßig durchgeführten Ultraschalluntersuchung entdeckt oder sie fallen auf, weil sie Beschwerden verursachen wie Oberbauchschmerzen, Krämpfe im Unterbauch oder weil sie infolge einer Verlegung der Gallenwege zur Gelbsucht führen. Funktionell aktive und funktionell inaktive Tumoren setzen ein besonderes Hormon frei, das zu keinen Beschwerden führt, sich aber hervorragend als Tumormarker eignet, das Chromogranin A. Chromogranin A gehört zu einer Gruppe von Eiweißstoffen, die in fast allen menschlichen Zellen vorkommen, die Hormone bilden. Es handelt sich um wasserlösliche Eiweißstoffe, die Hormone und Kalzium binden. Chromogranin A trägt dazu bei, dass die Hormone in einer Zelle 47 Der Krebsschmerz-Informationsdienst KSID im Deutschen Krebsforschungszentrum Wie können Tumorpatienten mit Schmerzen umgehen? Was können Angehörige tun? Ausführliche Antworten zu diesen und weiteren Fragen zum Thema Schmerz bei Krebs gibt der Krebsschmerz-Informationsdienst des Deutschen Krebsforschungszentrums in Heidelberg telefonisch, per E-Mail oder im Internet. Telefonische Anfragen werden von Mitarbeiterinnen beantwortet, die in der Schmerz- und Palliativmedizin geschult wurden und meist eine ärztliche Ausbildung haben oder aus Berufen des Gesundheitswesens kommen. Da die Nutzer von KSID auf Wunsch anonym bleiben, können sie sich auch in schwierigen Situationen an den KSID wenden. Meist gelingt es, mögliche Bewältigungsstrategien im persönlichen Gespräch am Telefon aufzuzeigen. an die richtigen Stellen gelangen, von wo sie dann in das Blut freigesetzt werden. Chromogranin A wurde zuerst in Zellen des Nebennierenmarks, später in fast allen anderen hormonproduzierenden Zellen nachgewiesen. Die Pathologen können Chromogranin A histologisch mittels bestimmter Färbeverfahren ganz leicht nachweisen. Chromogranin A kommt, weil es nicht tumorspezifisch ist, bei jedem Menschen vor. Nur dann, wenn ein neuroendokriner Tumor vorliegt, wird Chromogranin A besonders stark freigesetzt und kann durch Bestimmung mittels eines spezifischen Laborverfahrens (ELISA) im Blut nachgewiesen werden. Chromogranin A ist also ein Tumormarker für alle hormonproduzierenden Tumoren. Es eignet sich ganz besonders zur Beurteilung des Verlaufs einer Tumorerkrankung. Wann wird Chromogranin A bestimmt und wann nicht? Die Indikationen für eine Chromogranin-A-Bestimmung sind im Einzelnen: 48 Verlaufsbeurteilung Der KSID möchte den Betroffenen Orientierungshilfe innehalb des Gesundheitswesens geben, indem er Wege zur Nutzung der vorhandenen Ressourcen aufzeigt. Dies können zum einen Adressen von niedergelassenen Schmerztherapeuten oder Schmerzambulanzen, aber auch Anlaufstellen für schwerstkranke Menschen wie ambulante und stationäre Pflege, Palliativeinrichtungen und Hospize sein. B. S. So erreichen Sie uns •Telefon: 06221/42-2000, Montag-Freitag, 12–16 Uhr •E-Mail: [email protected] •Internet: www.KSID.de • ein neu entdeckter neuroendokriner Tumor; hier sagt die Höhe des Chromogranin-A-Spiegels etwas über die Tumorlast, d.h. über die Anzahl der Lebermetastasen aus. Des Weiteren spiegelt der Chromogranin-A-Wert die Tumorprogression wider. • ein bereits bekannter metastasierter neuroendokriner Tumor; der Wert sagt etwas über die Metastasenlast aus. • eine Verlaufsbeurteilung; erfolgt die Bestimmung von Chromogranin A im Abstand von 3–6 Monaten, so kann aus dem jeweiligen Wert geschlossen werden, ob eine Tumorprogression stattfand oder nicht. Keine Indikation für die Chromogranin-A-Bestimmung sind folgende Situationen: • Suche nach einem neuroendokrinen Tumor ohne morphologischen Hinweis auf ein Tumorgeschehen mittels Ultraschall oder CT bzw. MRT. • Suche nach einem Neuauftreten von Metastasen nach vorheriger kurativer Tumoroperation und keinem Hinweis auf ein neues Tumorgeschehen mittels moderner Bildgebung. Was muss man bei der Interpretation der Werte beachten? Erhöhte Chromogranin-A-Werte können fälschlich auf ein Tumorgeschehen hindeuten: • bei einer Niereninsuffizienz • bei einer fortgeschrittenen Herzinsuffizienz • bei einer verminderten Leberfunktion • bei einer Typ-A-Gastritis • unter lang andauernder Einnahme potenter Säurehemmer (Protonenpumpeninhibitoren). Fazit Die Bestimmung von Chromogranin A eignet sich hervorragend zur Verlaufsbeurteilung bei einem bekannten metastasierten neuroendokrinen Tumor. Die Bestimmung sollte allerdings unterbleiben, wenn ein neuroendokriner Tumor vermutet wird, die bildgebenden Verfahren aber keinen Hinweis auf ein Tumorgeschehen ergeben. In solchen Fällen wird der Patient oftmals völlig unbegründet verunsichert. Prof. Dr. med. R. Arnold, München NET-Zentren stellen sich vor Schwerpunkt Endokrinologie und Stoffwechse­l­ erkrankungen der I. Medizinischen Klinik und Poliklinik des Klinikums der Johannes Gutenberg Universität in Mainz Der Schwerpunkt Endokrinologie und Stoffwechselerkrankungen der I. Medizinischen Klinik und Poliklinik des Klinikums der Johannes Gutenberg Universität Mainz umfasst die ambulante und stationäre Versorgung von Patienten mit Hormonerkrankungen, Diabetes mellitus, Stoffwechselerkrankungen sowie endokrinen und neuroendokrinen Tumoren auf höchstem medizinischem Niveau. Der Schwerpunkt Endokrinologie und Diabetologie der Universitätsklinik Mainz ist im Landeskrankenhausplan von Rheinland Pfalz als diabetologisches Zentrum der maximalen Versorgungsstufe ausgewiesen und ist ein diabetisches Fußzentrum der AG Fuß nach den Richtlinien der DDG. Im Bereich der Endokrinologie werden Erkrankungen der Schilddrüse, Nebenniere und Hypophyse, des Knochenstoffwechsels sowie Hormon­ störungen des Mannes und der Frau behandelt. Insgesamt wurden im letzten Jahr über 3000 Patienten ambulant und fast 800 Patienten stationär versorgt. Für die stationäre Therapie stehen 2 endokrinologische/diabetologische Schwerpunktstationen mit insgesamt 37 Betten zur Verfügung. Neben der allgemeinen Endokrinologischen Ambulanz und weiteren Spezialambulanzen wird eine Spezialambulanz für Patienten mit neuroendokrinen und endokrinen Tumoren angeboten, die von Herrn Dr. Fottner geleitet wird. Das Team besteht neben dem Schwerpunkt- leiter, Herrn Univ.-Prof. Dr. med. Matthias M. Weber, aus zwei Oberärzten und sechs Assistenzärzten sowie aus vier Diabetes- und ErnährungsbeDr. med. Christian Fottner, Univ.-Prof. Dr. med. Matthias raterinnen, drei Spezialambulanz M. Weber, Schwerpunkt Diabetes-Fuß- für endokrine und Endokrinologie und Stoffwechselerkrankungen, schwestern und neuroendokrine Tumoren, Universitätsklinik Mainz Universitätsklinik Mainz drei Funktionsschwestern, die für die Durchführung der endokri- Universitätsklinik Mainz traditionell nologischen Untersuchungen und eine sehr große Bedeutung. Im Funktionstests mitverantwortlich Schwerpunkt Endokrinologie wird sind. seit vielen Jahren eine große Anzahl von Patienten mit hormonaktiven und hormoninaktiven neuroendoBehandlungsschwerpunkt krinen Tumoren des Magen-Darmendokrine und neuroendokrine Traktes und der Bauchspeichel­Tumoren drüse (Gastro-entero-pankreatische [GEP] Tumoren), mit Tumoren der Die interdisziplinäre Behandlung Schilddrüse und Nebenniere sowie von Patienten mit neuroendokrinen mit familiären endokrinen Tumorund endokrinen Tumoren hat in der syndromen betreut. Das Behand- Gebäude 303, Schwerpunkt Endokrinologie und Stoffwechselerkrankungen 49 NET-Zentren stellen sich vor Station 303 EG Poliklinik Patientenzimmer Funktionsbereiche des Schwerpunktes lungsspektrum des Schwerpunktes umfasst die Diagnosestellung und Therapie aller endokrinen und neuroendokrinen Tumoren. Umfassende Funktionsunter­ suchungen und Lokalisations­ diagnostik Neben speziellen klinischen und laborchemischen Funktionsuntersuchungen, die durch besonders ausgebildetes Personal in unserer endokrinologischen Funktionsabteilung durchgeführt werden, kommen zur Lokalisationsdiagnostik sämtliche endoskopische Verfahren (Magenspiegelung, Dickdarmspiegelung, Dünndarmspiegelung sowie insebsondere die Endosonographie) einschließlich der ultraschallgesteuerten Biopsie sowie die Minilaparoskopie zum Einsatz. Darüber hinaus werden in Zusammenarbeit mit den anderen Abteilungen des Klinikums der Universität Mainz modernste radiologische (Mehrzeilen-CT, MRT mit 1,5 Tesla) und nuklearmedizinische Verfahren (So50 Funktionslabor Gruppenschulungsraum matostatin-Rezeptor-Szintigraphie, DOPA-PET, FDG-PET) eingesetzt. Komplettes Spektrum der onkologischen Therapie In unserer Spezialambulanz und auf den endokrinologischen Stationen werden die Patienten in enger Kooperation mit den anderen beteiligten Fachdisziplinen des Klinikums behandelt, wobei das gesamte Spektrum der onkologischen Therapie endokriner und neuroendokriner Tumoren (Operation, endoskopische Nebennierenentfernung, lokale tu­morreduzierende Verfahren wie Chemoembolisation oder Radiofrequenzablation, Radiojodtherapie, Radionuklidtherpie, Strahlentherapie sowie Chemo- und Biotherapie) angeboten wird. Einen klinischen Schwerpunkt bilden Patienten mit Schilddrüsenund Nebenschilddrüsenkarzinomen. Sie werden interdisziplinär in enger Zusammenarbeit mit dem renommierten Schilddrüsenchirurgen Prof. Dr. T. Musholt (Leiter der endokri- nen Chirurgie der Universitätsklinik Mainz) und Frau Dr. Eichhorn (Oberärztin der Nuklearmedizinischen Klinik) betreut. Ein weiterer Schwerpunkt ist die Versorgung von Patienten mit Tumoren der Nebenniere (Phäochromozytome, Nebennierenrindenkarzinome), die im Rahmen des deutschen Nebennierenkarzinomregisters nach neuesten wissenschaftlichen Studienprotokollen behandelt. Als eines der wenigen Zentren in Deutschland bietet der Schwerpunkt in Zusammenarbeit mit der Klinik für Nuklearmedizin darüber hinaus seit 1 ½ Jahren die Radio­ peptid-Therapie neuroendokriner Tumoren mit 90Y-DOTATOC an (Ansprechpartner Dr. C. Fottner, Schwerpunkt Endokrinologie, oder Dr. A. Helisch, Oberarzt der Nuklearmedizinischen Klinik). Des Weiteren erfolgt eine Zusammenarbeit mit internationalen Arbeitsgruppen (AG Neuroendokrine Tumoren der Deutschen Gesellschaft für Endokrinologie [DGE], Deutsche Gesellschaft für NET-Zentren stellen sich vor Verdauungs- und Stoffwechselerkankungen [DGVS], European Neuroendocrine Tumor Network [ENET], Nebennierenkarzinomregister) im Rahmen klinisch-wissenschaftlicher Studien zur Entwicklung neuester Therapiemöglichkeiten für diese seltenen Tumorerkrankungen. Erbliche Tumorerkrankungen mit Beteiligung endokriner Organe Im Schwerpunkt Endokrinologie besteht eine große Erfahrung in der Betreuung von Familien mit seltenen vererbbaren endokrinen Tumorerkrankungen. Hier sind insbesondere die Multiple Endokrine Neoplasie Typ 1 und 2 (MEN 1 und 2) zu nennen, das von Hippel-Lindau-Syndrom (VHL), das familiäre Phäochromozytom-ParagangliomSyndrom (PGL, bedingt durch Mutationen des SDHD- bzw. SDHBoder SDHC-Gens) sowie – seltener – die Neurofibromatose Typ I (NF I), familiäre Formen des Schilddrüsenkarzinoms und der so genannte Carney-Complex. Neben dem gesamten Spektrum der anspruchsvollen laborchemischen und technischen Untersuchungen sind auch die molekularbiologische Diagnosesicherung und eine humangenetische Beratung für diese seltenen erblichen Tumorerkrankungen im Universitätsklini­kum etabliert. Die Behandlung in unseren Spezialambulanzen erfolgt nach den neuesten wissenschaftlichen Erkenntnissen und in enger Kooperation mit nationalen und internationalen Arbeitsgruppen (z. B. der American-German Paraganglioma Study Group). Interdisziplinäre Zusammenarbeit und Qualitätssicherung Die enge Kooperation mit den benachbarten Fachdisziplinen stellt ein wesentliches Qualitätsmerkmerkmal für einen optimalen Behandlungserfolg bei neuroendokrinen und endokrinen Tumorerkrankungen dar. Der Schwerpunkt Endokrinologie legt großen Wert auf eine enge interdisziplinäre Zusammenarbeit mit den anderen Kliniken der Universität und ist ständig bestrebt, einen für die Patienten bestmöglichen Qualitätsstandard aufrechtzuerhalten. Die eigenen Ergebnisse werden regelmäßig in nationalen und inter- nationalen Fachzeitschriften veröffentlicht und es findet ein reger nationaler und internationaler wissenschaftlicher Austausch statt. Auf diese Weise werden unsere diagnostischen und therapeutischen Strategien ständig überprüft und an den neuesten Stand der Erkenntnis angepasst, so dass jederzeit eine optimale Behandlung sichergestellt werden kann. Dies findet seinen Niederschlag auch in der Organisation und Leitung des interdisziplinären endokrinen und neuroendokrinen Tumorforums (IENET, vgl. Insert), das im Rahmen des Comprehensive Cancer Center (CCC) der Uniklinik Mainz von Herrn Prof. Dr. M. M. Interdisziplinäres Endokrines und Neuroendokrines Tumorforum (IENET) des Universitätsklinikums Mainz Sprecher: Univ.-Prof. Dr. med. Matthias M. Weber Schwerpunktmäßig beteiligte Zentren und Ansprechpartner: • Schwerpunkt Endokrinologie und Stoffwechselerkrankungen I. Medizinische Klinik und Poliklinik Leiter: Univ.-Prof. Dr. med. Matthias M. Weber Dr. med. Christian Fottner • Klinik und Poliklinik für Nuklearmedizin Univ.-Prof. Dr. med. Peter Bartenstein Dr. med. Andreas Helisch Dr. med. W. Eichhorn • Klinik und Poliklinik für Allgemein- und Viszeralchirurgie Univ.-Prof. Dr. med. Th. Junginger Endokrine Chirurgie Leiter: Univ.-Prof. Dr. med. Thomas J. Musholt • Klinik für Diagnostische Radiologie Univ.-Prof. Dr. med. Christoph Düber Dr. med. Simin Schadmannd-Fischer • Klinik für Transplantationschirurgie und Chirurgie von Leber, Gallenwegen und Pankreas Univ.-Prof. Dr. med. Gerd Otto • Klinik und Poliklinik für Radioonkologie und Strahlentherapie Univ.-Prof. Dr. med. H. Schmidberger • Urologische Klinik und Poliklinik Univ.-Prof. Dr. med. J. W. Thüroff • Hals-, Nasen-, Ohren- Klinik und Poliklinik Univ.-Prof. Dr. med. Dr. h.c. mult. W. Mann • III. Medizinische Klinik und Poliklinik Univ.-Prof. Dr. med. Th. Wölfel E-Mail: [email protected] oder E-Mail.: [email protected] 51 NET-Zentren stellen sich vor Weber als Sprecher vertreten wird. Regelmäßig werden hier im Rahmen einer fachübergreifenden Konferenz Patienten mit endokrinen und neuroendokrinen Tumorerkrankungen besprochen und in einem Protokoll das diagnostische und therapeutische Vorgehen festgelegt. Neben den aktuell stationär und ambulant am Klinikum behandelten Patienten können hier auch externe Patienten von ihrem behandelnden Arzt vorgestellt werden. Für eine Kontaktaufnahme interessierter Patienten oder Ärzte stehen ihnen die Mitarbeiter des Schwerpunktes Endokrinologie gerne zur Verfügung. Die Kontaktadressen sowie weitere Informationen über den Schwerpunkt finden Sie auch im Internet. Dr. med. Christian Fottner, Spezialambulanz für endokrine und neuroendokrine Tumoren, Schwerpunkt Endokrinologie und Stoffwechselerkrankungen, I. Medizinische Klinik und Poliklinik, Klinikum der Johannes Gutenberg Universität Mainz Kontakt: Schwerpunkt Endokrinologie und Stoffwechselerkrankungen I. Medizinische Klinik und Poliklinik Klinikum der Johannes Gutenberg Universität Mainz Langenbeckstraße 1 55101 Mainz www.endokrinologie.klinik.uni-mainz.de Sekretariat Prof. Weber Frau E. Kroehle-Diehl Tel.: 06131/17-7260 Fax.: 06131/17-5608 E-Mail: [email protected] Spezialambulanz endokrine und neuroendokrine Tumoren Dr. med. C. Fottner Tel.: 06131/17-2831 Fax.: 06131/17-5615 E-Mail: [email protected] Buchtipp Die „Blauen Ratgeber“ – Broschüren der Deutschen Krebshilfe Verlaufsbeurteilung Umfangreiche Informationen, Hinweise und Anregungen zu verschiedenen Themen rund um die Krebskrankheiten erhalten Betroffene, Angehörige und Interessierte in den „Blauen Ratgebern“ der Deutschen Krebshilfe. Hier zwei Beispiele: Wegweiser zu Sozialleistungen Krebs-Patienten belasten nicht nur physische und psychische, sondern oft auch finanzielle Probleme. Der Staat bietet hier zahlreiche Hilfen. Doch die wenigsten Betroffenen sind über diese Angebote gut informiert. In der Broschüre „Wegweiser zu Sozialleistungen“ stellt die Deutsche Krebshilfe staatliche Hilfsangebote vor und klärt die Patienten über ihre Ansprüche auf soziale Leistungen auf. TEAMWORK Krebspatienten und Ärzte als Partner Wichtigste Voraussetzung dafür, dass ein Krebspatient bald wieder gesund wird, ist die gute Zusammenarbeit zwischen dem Betroffenen, seinen Ärzten und Pflegern sowie den Angehörigen. Doch die Realität sieht oft anders aus: Patienten und Ärzte verstehen einander nicht, der Kranke fühlt sich als „Fall“, die Ärzte sind überlastet und haben wenig Zeit. Die Broschüre gibt konkrete Hilfen für eine gute Teamarbeit. Sie können diese Broschüren online lesen unter www.Krebshilfe.de oder kostenlos bestellen bei: Deutsche Krebshilfe e.V., Postfach 1467, 53004 Bonn. 52 B. S. NET-Zentren stellen sich vor Insulinom & GEP-Tumor-Zentrum Neuss – Düsseldorf (GEP-TuZ) haus) wurden die Voraussetzungen für eine engagierte, fachübergreifende interdisziplinäre Kooperation schnell gefunden. Von der Diagnostik bis zur Therapie – der behandelnde Arzt ist immer dabei Das Lukaskrankenhaus in Neuss: Hier finden Patienten mit GEP-Tumoren alle kompetenten Ansprechpartner unter einem Dach. Das Insulinom & GEP-Tumor-Zentrum Neuss-Düsseldorf wurde 2002 auf Initiative von Prof. Dr. Achim Starke von der Medizinischen Klinik am Universitätsklinikum Düsseldorf und Prof. Dr. Peter Goretzki nach seiner Ernennung zum Chefarzt der Klinik für Allgemeine und Viszerale Chirurgie am Lukaskrankenhaus (Akademisches Lehrkrankenhaus der Heinrich-Heine-Universität Düsseldorf) in Neuss gegründet. Interdisziplinäre Zusammenarbeit ist das A und O Eine jahrzehntelange Kooperation auf dem Gebiet der Insulinom- Diagnostik und -Therapie sowie der selteneren neuroendokrinen Tumoren des Magen-Darm-Traktes am Universitätsklinikum in Düsseldorf bewog die beiden Ärzte, am Lukaskrankenhaus unter einem Dach für die Patienten mit Insulinomen, Karzinoiden, nicht-funktionellen NET und weiteren selteneren GEP-NET inklusive der Patienten mit MEN 1 und MEN 2 kompetente Ansprechpartner zu bleiben. Mit Prof. Dr. Peter Czygan, Ärztlicher Direktor und Leiter der Klinik für Gastroenterologie und Onkologie, Prof. Dr. Rainer Köster (Leiter des Instituts für Radiologie und Nuklearmedizin) sowie Prof. Dr. Cyrus Tschahargane (Leiter des Instituts für Pathologie am Lukaskranken- Nach Abschluss umfassender Renovierungsarbeiten stehen heute im Lukaskrankenhaus Neuss freundliche und geräumige Stationen mit zumeist 2-Bettzimmern inkl. Telefonund Fernseh-Anschluss sowohl in der Medizinischen als auch in der Chirurgischen Klinik zur Verfügung. Sämtliche z. T. komplexe diagnos­ tischen Maßnahmen, wie z. B. oraler Glukosebelastungs- (oGTT) und Fastentest, Sekretin-Test, intra­ arterieller Kalzium-Stimulationstest (sog. Imamura-Test) werden ebenso durchgeführt wie der gesamte Umfang erforderlicher Operationen auf dem Gebiet der endokrinen Chirurgie, insbesondere der Pankreasund Schilddrüsenchirurgie. In der modern umgestalteten Endo­ skopie-Abteilung der Klinik für Gastroenterologie stehen die üblichen apparativen diagnostischen Prozeduren wie Endosonographie und ggf. Radiofrequenzablation (RFTA), in der Radiologie modernste CT, 53 NET-Zentren stellen sich vor MRT- und Angiographie-Technik so­wie die Octreotid-Szintigraphie mit 111Indium zur Verfügung. Große Erfahrung besteht in der arteriel­len Leber-Chemoembolisation von Lebermetastasen sowie der Chemoperfusion. Lediglich zur DOTATOC bzw. DOTANOC-Therapie müssen die Patienten an entsprechend ermächtigte nuklearmedizinische Abteilungen weitergeleitet werden. Es war uns immer selbstverständlich im Rahmen der interdiszipli­ nären Kooperation, dass der Internist (Prof. Starke) den Patienten nicht nur in den Operationssaal begleitet und dem Eingriff beiwohnt, sondern auch bei den invasiven Manipulationen an der Leber (Chemoembolisation) dem Radiologen zur Entscheidungshilfe zur Verfügung steht. Das GEP-TuZ bietet folgende Leistungen an: • Abklärung von Hypoglykämien (Unterzuckerungen) jedweder Art, insbesondere beim benignen und malignen Insulinom, sowie von post prandialen Hypoglykämien (NIPHS) • Betreuung und differentielle Behandlung von Patienten mit gutartigen und bösartigen neuroendokrinen Tumoren (GEP-NET) • Diagnostik, chirurgische Therapie und Langzeitüberwachung/ Therapie bei: Im Lukaskrankenhaus werden regelmäßig sog. Tumorboards abgehalten. Auf Wunsch können alle Patienten an ausführlichen Besprechungen mit den beteiligten Disziplinen teilnehmen, um auch neuere Therapiekonzepte fachkundig zu erörtern. Bereits dreimal haben wir in Neuss in den letzten Jahren an Samstagen (zuletzt im November 2003 und März 2004) Patiententage unter Beteiligung der Selbsthilfegruppe (NET-SHG) abgehalten und standen den Patienten und ihren Angehörigen Rede und Antwort. Prof. Dr. med. Achim Starke, GEP-TuZ Neuss 54 Insulinom Karzinoid Gastrinom Glukagonom Vipom Somatostatinom (u.a.) sowie sog. „nicht-funktionellen“ neuroendokrinen Tumoren (vor allem des Pankreas) abdominellen und thorakalen Tumoren bei MEN 1, MEN 2 • Spezielle therapeutische Verfahren: Tumorboards und Patiententage − − − − − − − − − − − − − − − − komplette Nebenschilddrüsen- und Schilddrüsen-Chirurgie Verfahren bei malignen Tumoren sog. „biologische Therapie“ mit Somatostatin/Sandostatin®/Interferon Leber-Embolisation mit verschiedenen Materialien Chemo-Embolisation (TACE der Leber, u.a. Streptozotozin) Chemo-Perfusion (TACP; u.a. Streptozotozin) Streptozotozin-Chemotherapie und erweiterte Chemotherapie (nach Port-Implantation) Radiofrequenzablation (RFTA/RITA) bei Indikation in Zusammenarbeit mit der Radiologie • Hilfe/Kontakte bei Vermittlung einer DOTATOC-Therapie Kontakt Ambulante Kontakte sind in den entsprechenden Büros des Zentrums sowohl in Neuss • Tel.: 02131/888 3001 oder 888 2711, Sekretariat Prof. Goretzki und Onkologische Ambulanz als auch auf dem Gelände des Universitätsklinikums • Tel.: 0211/811 6327, Prof. Starke möglich, wobei keinerlei Beschränkungen hinsichtlich der Kranken­ kassen bestehen. Detaillierte Informationen sowohl für betroffene Patienten als auch deren Hausärzte und die beteiligten Klinikärzte stehen auf unseren Internetseiten unter www.gep-net.com und www.insulinoma.net zur Verfügung. Leserbriefe Aus Briefen an das Netzwerk Neuroendokrine Tumoren e.V. Waldstraße 34 91054 Erlangen Schnell wachsende Tumoren Im 1. Quartal 2005 traten bei mir ständig Durchfälle auf, wodurch ich 10 kg Gewicht verlor. Im März kamen Schmerzen an den linken Rippenbögen hinzu. Nach mehreren unzutreffenden Diagnosen durch einen Internisten wurde im April am Universitätsklinikum Regensburg festgestellt, dass die Ursache der Beschwerden ein schnell wachsendes, malignes neuroendokrines Karzinom (Proliferationsgrad ca. 50 %) ist. Der Primärtumor und zwei Metastasen lagen zwischen Magen und Pankreas, eine Metastase saß am rechten Sitzbeinast und eine weitere hatte den Brustwirbelkörper 11 durchsetzt. Gute Therapieerfolge Die letztgenannte Absiedlung verschwand durch Bestrahlung bis Juni. Eine Chemotherapie mit Etoposid und Carboplatin beseitigte bis November die Metastase am Sitzbeinast und verkleinerte die anderen drei Tumoren deutlich. Mitte Dezember wurden diese Reste mit Pankreasschwanz und Milz erfolgreich operativ entfernt. Viele Leserbriefe und die Korrespondenz mit dem Netzwerk NeT e.V. enthalten Schilderungen sehr persön­licher Probleme und medizinischer Situationen. Zur Wahrung der Vertraulichkeit wird aus diesen Briefen deshalb grundsätzlich nur anonym zitiert – es sei denn, der Schreiber oder die Schreiberin wünscht die Namensnennung. Im Übrigen gilt in der Glandula-­Redaktion wie bei allen Zeitschriften: Anonym zugesandte Briefe werden gar nicht veröffentlicht, Kürzungen und redaktionelle Korrekturen bleiben vorbe­ halten. Baldiger Rückfall Leider endet meine Krankheitsgeschichte damit nicht. Bereits Mitte Januar 2006 trat ein Rückfall am Bauchfell rechts mit einzelnen Lymphknotenabsiedlungen auf. Da der Tumor einen Nervenstrang erfasst hat, verursacht er auch starke Schmerzen. Die daraufhin wiederholte Chemotherapie mit Etoposid und Carboplatin bewirkte nichts. Deshalb ersetzten wir sie durch die Gabe von Topotecan, die zumindest das Voranschreiten abbremst. Um die Schmerzen zu lindern, wird einerseits der Herd am Bauchfell bestrahlt und andererseits werden hohe Dosen von Schmerzmitteln verabreicht. Die Einnahme von Saroten soll ebenfalls die Schmerzbelastung vermindern. Kontaktwunsch Mich freut es, dass es mit dem Netzwerk Neuroendokrine Tumoren e. V. eine Basis für Information und Erfahrungsaustausch unserer seltenen Krebserkrankungen gibt. Vor allem in der Regionalgruppe Erlangen und beim Neuroendokrinen Tumor-Tag des Netzwerks NeT in Nürnberg ergaben sich schon viele gute Begegnungen. Darüber hinaus wünsche ich mir jetzt Kontakt zu Betroffenen. Bitte schreiben Sie mir, wenn Sie unter einem ähnlichen Krankheitsbild leiden. R. F.* Viele Fragen bleiben offen ... Im Heft 6 habe ich auf Seite 41 über meine Erkrankung (Karzinoidmetastasen am Bauchfell) berichtet. Nach nun fast 2 Jahren hat sich keine Verschlimmerung meiner Beschwerden ergeben. Es waren pro Jahr 2–3 Anfälle von Bauchschmerzen zu überstehen (mit Schmerzmitteln erträglich). Im Dezember 04 und November 05 wurden Octreotid-Szintigraphien durchgeführt. Befund: Flaue Mehranreicherung in Mittelund Unterbauch. Kein Nachweis pathologischer Mehranreicherung in Leber, Lunge oder Skelettsystem. Die 5-HIES-Urinuntersuchung ergab 2004 einen Wert von 7,1 im Jahr 05 von 34,9. Eine Kontrolluntersuchung erfolgt demnächst. Dieses eigentlich erfreuliche Ergebnis (keine Verschlechterung) hinter* Name und Anschrift sind der Redaktion bekannt. Zuschriften richten Sie bitte an die Netzwerk-Geschäftsstelle, wir leiten sie gerne weiter. 55 Leserbriefe lässt trotzdem ein ungutes Gefühl. Worauf warte ich eigentlich? Warte ich auf eine Verschlechterung? Warten die Ärzte auf eine Verschlechterung, um mit irgendeiner Maßnahme zu beginnen? Wobei ich den Eindruck habe, dass sie recht ratlos sind und evtl. eintretende Beschwerden nur durch Chemotherapie oder Notoperationen für kurze Zeit beheben können. Oder wird es heißen: „Ja, wenn Sie früher damit gekommen wären?“ Was mich jedoch am meisten wundert, ist, dass auf meinen Bericht keinerlei Reaktion erfolgte. Bin ich der Einzige mit einer solchen Erkrankung? Liest der „Ärztliche Beirat“ die Patientenbeiträge überhaupt? Es ist mir auch bei der Durchsicht verschiedener Krebs-Foren im Internet nicht gelungen, einen 2. Fall aufzuspüren. Bei den meisten Bauchfell-Krebserkrankungen handelt es sich um Pseudomyoma peritonei (Bericht von Joachim Eden). Dieser Krebs ist mit einer starken Aszites (Flüssigkeitsanreicherung im Bauch) verbunden und anscheinend nur durch eine OP nach Dr. Sugarbaker zu behandeln (große OP und sehr umstritten). Da diese Diagnose für mich nicht zutrifft und mein Leidensdruck derzeit nicht groß ist, werde ich mich keiner großen Behandlung aussetzen. Es bleiben jedoch noch einige Fragen offen wie: Wie viele Menschen leider unter der gleichen Erkrankung? Erscheinen die in irgendeiner Statistik? Wo erhalten diese Menschen Auskunft und welche Ärzte kennen sich mit dieser Krankheit aus? G. W.* Der obige Leserbrief berührt einige für Betroffene mit Karzinoid wichtige Themen. Der Betroffene berichtet zunächst, dass er nahezu beschwerdefrei ist und dass die Ergebnisse der Untersuchungen eine Befundkonstanz über 2 Jahre zeigen. Dennoch ist er unzufrieden. Das eigentlich erfreuliche Ergebnis, nämlich da der Krebs nicht wächst, auch ohne Therapie, hinterlässt für ihn ein ungutes Gefühl, weil er nicht weiß, wie es weitergeht. Natürlich würden wir alle gern in die Zukunft blicken können. Aber wer weiß schon, wie unser aller Zukunft aussieht? Wer soll dem Patienten Kraft und Zuversicht geben? Der Arzt, die Familie, Freunde, die Selbsthilfegruppe, ein Seelsorger, die Kirche, ein Psychologe, er selbst? Am besten alle zusammen. Der Patient fragt, warum sich nie- mand bei ihm gemeldet hat, warum er keinen Brief erhalten hat und ob er vielleicht der Einzige mit einer solchen Erkrankung ist. Letztere Frage kann man klar beantworten. Obwohl neuroendokrine Tumoren insgesamt eher selten sind, gibt es viele Patienten mit einer ähnlichen Erkrankung und ähnlich erfreulichem Verlauf. Viele dieser Betroffene arbeiten auch im Netzwerk mit und treffen sich in Regionalgruppen oder auf den Netzwerk-Veranstaltungen. Der Betroffene surft im Internet in verschiedenen Krebsforen. Offensichtlich ist er dabei in eine Krebskategorie gesurft, die mit der seinen wenig zu tun hat. Er ist auf Abwege geraten. Dies zeigt, dass Betroffene in medizinischen Dingen insbesondere auf professionellen Rat und valide Informationen angewiesen sind. Das Netzwerk Neuroendokrine Tumoren e.V. ist eine partnerschaftliche Organisation, neben Betroffenen arbeiten auch Ärzte aktiv mit. Was kann man dem Leserbriefschreiber raten? Vielleicht dies: Er sollte in einer Selbsthilfegruppe aktiv mitarbeiten, an Tagungen der Selbsthilfegruppe teilnehmen, in einer Regionalgruppe mitarbeiten und versuchen, anderen zu helfen. Dann wird er Antworten finden – auf seine Fragen und auf Fragen, die er bisher noch nicht gestellt hat. Prof. Dr. J. Hensen Interessiert an „Wohnzimmer-Gesprächen”? Sie sind – wie ich – an einem neuroendokrinen Tumor erkrankt? Sie sind interessiert an einem Austausch? Sie möchten sich gerne im kleinen Kreis treffen? Setzen wir uns doch einfach zusammen: zu zweit, zu dritt, zu viert, gemütlich im Wohnzimmer oder in einem Café! Nehmen Sie einfach Kontakt mit mir auf: Katharina Mellar, Nürnberg, Tel. 0911/48 39 66 56 * Name und Anschrift sind der Redaktion bekannt. Zuschriften richten Sie bitte an die Netzwerk-Geschäftsstelle, wir leiten sie gerne weiter. Wissenschaftlicher Beirat des Netzwerks NeT e.V. Unserem wissenschaftlichen Beirat gehören zahlreiche Experten aus verschiedenen Fachdisziplinen an: • Prof. Dr. Arnold, Marburg (Internist/Gastroenterologie) • PD Dr. Auernhammer, München (Internist/Endokrinologie) • Prof. Dr. Becker, Göttingen (Nuklearmedizin) • PD Dr. Breidert, Baden-Baden (Internist) • Prof. Dr. Goretzki, Neuss (Chirurg) • Prof. Dr. Hensen, Hannover (Internist/Endokrinologie) • Prof. Dr. Mann, Essen (Internist/Endokrinologie) • Frau PD Dr. Pavel, Erlangen (Internistin/Endokrinologie) • Prof. Dr. Ramadori, Göttingen (Internist/Gastroenterologie) • Prof. Dr. Rothmund, Marburg (Chirurg) • PD Dr. Schaaf, München (Internist/Endokrinologie) • Prof. Dr. Scherübl, Berlin (Internist/Gastroenterologie) • Prof. Dr. Schmolle, Halle (Chirurg) • Prof. Dr. Weber, Mainz (Internist/Endokrinologie) • Prof. Dr. Wiedenmann, Berlin (Internist/Gastroenterologie) Internetseiten für NeT-Patienten Neben unserer Homepage www.karzinoid.info bzw. www. neuroendokrine-tumoren.de empfehlen wir Ihnen auch die Seite www.netumoradvisor.org, auf der Sie viele Hintergrundinformationen zu Karzinoiden, endokrinen Pankreastumoren sowie MEN 1 und 2 finden. Die Originalseite ist auf Englisch, kann aber in einer deutschen Version aufgerufen werden. Liebe Leserinnen und Leser, damit wir Ihren Brief oder Beitrag in der nächsten Glandula NeT abdrucken können, beachten Sie bitte: Redaktionsschluss für Ausgabe 8/2006 ist der 15. Oktober 2006 Impressum: GLANDULA NeT ist die Mitgliederzeitschrift der bundesweiten Selbsthilfe-Organisation „Netzwerk Neuroendokrine Tumoren (NeT) e.V.“, Sitz Erlangen. Die Zeitschrift erscheint zweimal jährlich. Internet-Adresse: http://www.karzinoid.info oder http://www.neuroendokrine-tumoren.de Herausgeber: Prof. Dr. med. Johannes Hensen, Medizinische Klinik, Klinikum Hannover Nordstadt, Hannover, E-Mail: [email protected] Redaktion: Brigitte Söllner, Erlangen ([email protected]) Fotos: privat Layout und Gestaltung: Klaus Dursch, Fürth Druck: Druckerei Raum, Oberasbach Redaktionsanschrift: Redaktion GLANDULA NeT, Netzwerk Neuroendokrine Tumoren (NeT) e.V., Waldstraße 34, 91054 Erlangen, Tel. 09131/815046, Fax 09131/815047, E-Mail: [email protected] Diese Zeitschrift und alle in ihr enthaltenen Beiträge sind urheberrechtlich geschützt, Nachdruck nur mit Genehmigung und Quellenangabe. Jede beruflich (gewerblich) genutzte Fotokopie verpflichtet zur Gebührenzahlung an die VG Wort, 80336 München, Goethestraße 49. Keine Haftung für unverlangt eingesandte Manuskripte. Namentlich gekennzeichnete Beiträge geben nicht in jedem Fall die Meinung von Redaktion und Herausgeber wieder. Wichtiger Hinweis: Medizin und Wissenschaft unterliegen ständigen Entwicklungen. Autoren, Herausgeber und Redaktion verwenden größ­tmögliche Sorgfalt, daß vor allem die Angaben zu Behandlung und medikamentöser Therapie dem aktuellen Wissensstand entsprechen. Eine Gewähr für die Richtigkeit der Angaben ist jedoch ausdrücklich ausgeschlossen. Jeder Benutzer muss im Zuge seiner Sorgfaltspflicht die Angaben anhand der Beipackzettel verwendeter Präparate und ggf. auch durch Hinzuziehung eines Spezialisten überprüfen und ggf. korrigieren. Jede Medikamentenangabe und/oder Dosierung erfolgt ausschließlich auf Gefahr des Anwenders. Mit Namen gekennzeichnete Beiträge geben nicht unbedingt die Meinung des wissenschaftlichen Beirats des Netzwerks oder der Redaktion wieder.