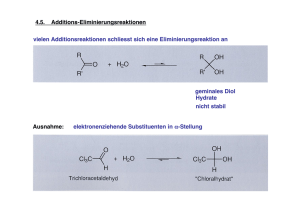
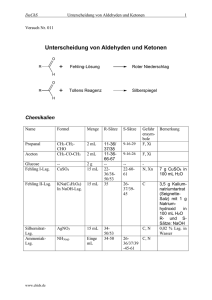
1 Moderne Methoden der Organischen Chemie – Prof. Dr. Stefan
Werbung

1 Moderne Methoden der Organischen Chemie – Prof. Dr. Stefan Bräse Institut für Organische Chemie, KIT, Tel.: 0721 / 608 4 2903 Inhalt 0 1 2 2.1 2.2 2.3 2.4 2.4.1 2.4.2 2.4.3 2.4.4 2.5 2.6 2.7 3 3.1 3.2 3.2.1 3.2.2 3.3 3.3.1 3.3.2 3.3.3 3.3.4 4 4.1 4.1.1 4.1.2 4.1.3 4.1.4 4.1.5 4.1.6 4.1.7 5 5.1 5.2 5.2.1 5.2.2 5.2.3 5.2.4 5.3 5.4 Literatur und Vorbemerkungen Metall-Organische Chemie: Einführung Chemie der Enolate Allgemeines Regiokontrolle bei der Bildung von Li-Enolaten aus Ketonen Stereokontrolle bei der Bildung von Li-Enolaten Diastereoselektive Aldol-Reaktionen Der Zimmerman-Traxler-Übergangszustand Auxiliarkontrolle nach Evans Auxiliarkontrolle nach Enders Auxiliarkontrolle nach Myers Di-Enolate von Acylessigester-Derivaten Die Synthese von -Funktionalisierten Carbonyl-Verbindungen über Enolate Chirale Glycin-Enolat-Äquivalente 1,2- und 1,4-Addition an Carbonyle Allgemeines Stereoselektive 1,2-Additionen Substrat-Kontrolle Reagens-Kontrolle – Katalysierte Reaktionen 1,4-Additionen Allgemeines Cuprate Addition von Schwefel-Yliden Umpolung der Carbonyl-Reaktivität Funktionalisierung von Doppelbindungen Epoxidierungen Allgemeines Sharpless – Enantioselektive Epoxidierung von Allylalkoholen Jacobsen – Epoxidierung von Alkenen Sharpless – Enantioselektive Dihydroxylierung von Alkenen Sharpless – Enantioselektive Aminohydroxylierung von Alkenen Cuprat-Additionen Hydroborierung Olefinierungen Allgemeines Phosphor-Ylide (Wittig, Wadsworth-HornerEmmons, Wittig-Schlosser) Allgemeines Die Wittig-Reaktion Die Schlosser-Variante Die Horner-Wadsworth-Emmons-Reaktion Sulfone (Julia) Silizium (Petersen) 5.5 5.6 6 6.1 6.2 6.3 6.4 6.5 6.6 6.7 6.7 7 7.1 7.1.1 7.1.2 7.2 7.3 8 9 10 10.1 10.2 10.2.1 10.2.2 10.2.3 10.2.4 10.3 10.3.1 10.3.2 10.3.3 10.4 10.5 10.5.1 10.5.2 10.6 10.7 11 11.1 11.2 11.2.1 11.2.2 11.2.3 11.2.4 11.2.5 11.2.6 12 Tebbe Olefin-Metathese Kreuzkupplungen Allgemeines Heck-Kupplung (Pd) Suzuki-Kupplung (B) Stille-Kupplung (Sn) Kumada-Kupplung (Ni) Negishi-Kupplung Sonogashira Die Hartwig-Buchwald Aryl-Aminierung Oxidationen / Reduktionen Oxidationen Oxidation von Alkoholen zu Aldehyden und Ketonen Oxidation von Aldehyden zu Carbonsäuren Redox-Reaktionen unter Beteiligung von Phosphanen (außer Wittig) Reduktionen Stereoelektronische Effekte, Baldwin-Rules Bor-Chemie Übergangsmetall-Chemie Chrom Cobalt Cobalt als Schutzgruppe (2 + 2 + 2)-Cycloadditionen Die Pauson-Khand-Reaktion Isomerisierungen Rhodium Das Monsanto-Verfahren Der Oxoprozess (Hydroformylierung) Hydrierung Nickel Palladium Der Wacker-Prozess Nucleophile Substitution an Allylverbindungen Zirkonium Eisen Peptidchemie Schutzgruppen Kupplungsmethoden Allgemeines Die Carbodiimid-Methode Aktivierung über Anhydride Phosphoniumsalze Uronium/Guanidinium-Salze Aktivester Synthesebeispiele