Slide 1
Werbung
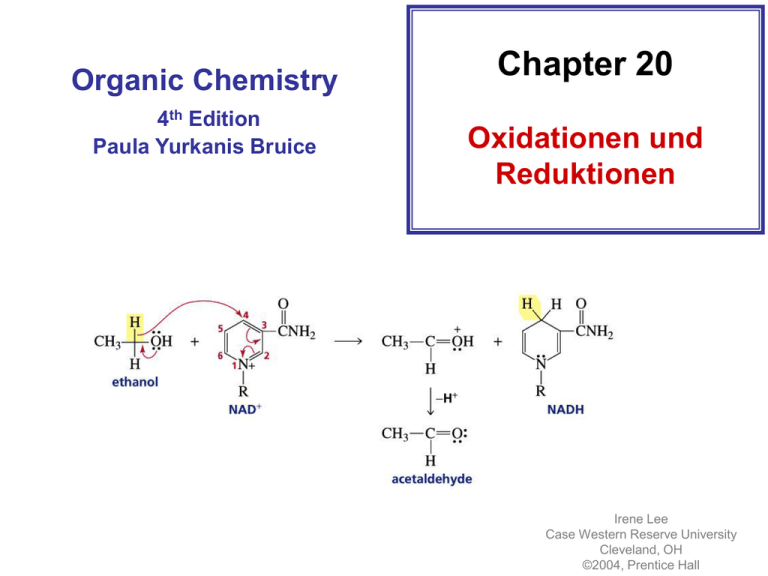
Organic Chemistry 4th Edition Paula Yurkanis Bruice Chapter 20 Oxidationen und Reduktionen Irene Lee Case Western Reserve University Cleveland, OH ©2004, Prentice Hall • Oxidation und Reduktion sind immer gekoppelt • Elektronenabgabe = Oxidation • Elektronenaufnahme = Reduktion • The oxidation state of a carbon atom equals the total number of its C–O, C–N, and C–X bonds NEIN!!!!!!! NEIN!!!!!!! NEIN!!!!!!! Wasserstoff, Hydrid und Hydrazin sind Reduktionsmittel! Brom und Chromsäure sind Oxidationsmittel! Reduktion durch katalytische Hydrierung Reduktionen mit Hydriden LiAlH4 ist stärker reduzierend als NaBH4 LiAlH4 wird eingesetzt um Verbindungen zu reduzieren, die mit NaBH4 nicht umgesetzt werden können. Keine Reaktion mit NaBH4 NaBH4 selektiv für Aldehyde und Ketone in Gegenwart von Estern Amine durch Reduktion von Amiden Oxidation von Alkoholen Oxidation eines primären Alkohols Wenn die Reaktion im basischen Medium durchgeführt wird (z. B. in Pyridin) erfolgt die Oxidation nur bis zum Aldehyd! Mechanismus der Chromoxidation Oxidation von Aldehyden Das Tollens Reagenz oxidiert nur Aldehyde, keine Alkohole Erinnern Sie sich an den Versuch “verspiegelte Colaflasche”, wo Glucose mit dem Tollens Reagenz umgesetzt wurde! Oxidation von Alkenen mit Persäuren Mechanismus der Epoxidation eines Alkens Die Epoxidierung ist stereospezifisch! Hydroxylierung von Alkenen Mechanismus der cis-Glykol Bildung Analog, aber besere Ausbeuten, werden mit Osmiumtetroxid erzielt Spaltung von Alkenen durch Ozonolyse Mechanismus: Cycloaddition im ersten Schritt Prim. Ozonid Sek. Ozonid Das primäre Ozonid ist instabil (2 O-O Bindungen) Sekundäre Ozonid ist stabil Ozonide können zu Carbonylverbindungen gespalten werden Beispiele für Ozonolysen Table 20.1 Summary of the Methods Used to Oxidize an Alkene Umwandlung von Aldehyden in andere funktionelle Gruppen Oxidation-Reduktion in der Biologie NAD+ oxidiert Ethanol durch Aufnahme eines Hydridions NADH reduziert durch Abgabe eines Hydridions