PowerPoint-Präsentation
Werbung

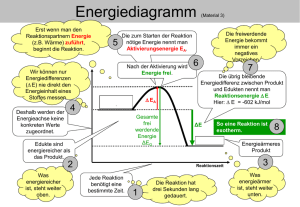
Energiediagramm (Material 2) Energie . . Reaktionszeit Energiediagramm Wir können nur Energiedifferenzen ( E) jedoch nie direkt den Energieinhalt Ei eines Stoffes messen. Deshalb werden der Energieachse keine konkreten Werte zugeordnet. Erst wenn man den Reaktionspartnern Energie (z.B. Wärme) zuführt, beginnt die Reaktion. Die zum Starten der Reaktion nötige Energie nennt man Aktivierungsenergie EA. Die übrig bleibende Energiedifferenz zwischen Produkt und Edukten nennt man Reaktionsenergie E. Energieärmeres Produkt Energiereiche Edukte. Was energiereicher ist, steht weiter oben. Die freiwerdende Energie bekommt immer ein negatives Vorzeichen. Jede Reaktion benötigt eine bestimmte Zeit. Die Reaktion hat drei Sekunden lang gedauert. Was energieärmer ist, steht weiter unten. Energiediagramm Nach der Aktivierung wird Energie frei. Da Energie frei wird (Pfeil nach unten), ist E < 0. Hier: E = -602 kJ/mol Reaktionszeiten können sehr unterschiedlich sein (Pikosekunden bis Stunden); Werte interessieren in der Regel nicht. Deshalb werden der Zeitachse keine konkreten Werte zugeordnet.