Übung zur Komplexnomenklatur: Chemie-Praxis
Werbung
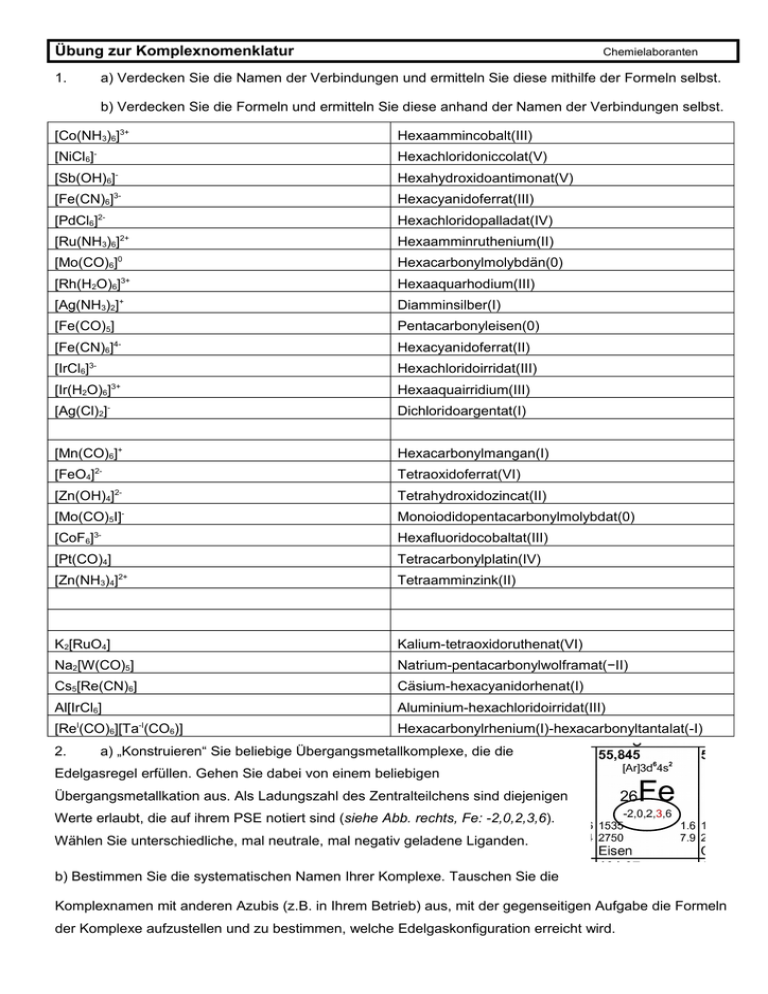
Übung zur Komplexnomenklatur 1. Chemielaboranten a) Verdecken Sie die Namen der Verbindungen und ermitteln Sie diese mithilfe der Formeln selbst. b) Verdecken Sie die Formeln und ermitteln Sie diese anhand der Namen der Verbindungen selbst. [Co(NH3)6]3+ Hexaammincobalt(III) [NiCl6]- Hexachloridoniccolat(V) [Sb(OH)6] - Hexahydroxidoantimonat(V) [Fe(CN)6]32- [PdCl6] Hexacyanidoferrat(III) Hexachloridopalladat(IV) [Ru(NH3)6]2+ 0 [Mo(CO)6] [Rh(H2O)6]3+ [Ag(NH3)2] + [Fe(CO)5] Hexaamminruthenium(II) Hexacarbonylmolybdän(0) Hexaaquarhodium(III) Diamminsilber(I) Pentacarbonyleisen(0) 4- [Fe(CN)6] Hexacyanidoferrat(II) [IrCl6]3- Hexachloridoirridat(III) 3+ [Ir(H2O)6] [Ag(Cl)2] - Dichloridoargentat(I) [Mn(CO)6]+ [FeO4] 2- [Zn(OH)4] Hexacarbonylmangan(I) Tetraoxidoferrat(VI) 2- [Mo(CO)5I][CoF6] Hexaaquairridium(III) 3- Monoiodidopentacarbonylmolybdat(0) Hexafluoridocobaltat(III) [Pt(CO)4] [Zn(NH3)4] Tetrahydroxidozincat(II) Tetracarbonylplatin(IV) 2+ Tetraamminzink(II) K2[RuO4] Kalium-tetraoxidoruthenat(VI) Na2[W(CO)5] Natrium-pentacarbonylwolframat(−II) Cs5[Re(CN)6] Cäsium-hexacyanidorhenat(I) Al[IrCl6] Aluminium-hexachloridoirridat(III) [ReI(CO)6][Ta-I(CO6)] Hexacarbonylrhenium(I)-hexacarbonyltantalat(-I) 2. a) „Konstruieren“ Sie beliebige Übergangsmetallkomplexe, die die Edelgasregel erfüllen. Gehen Sie dabei von einem beliebigen Übergangsmetallkation aus. Als Ladungszahl des Zentralteilchens sind diejenigen Werte erlaubt, die auf ihrem PSE notiert sind (siehe Abb. rechts, Fe: -2,0,2,3,6). Wählen Sie unterschiedliche, mal neutrale, mal negativ geladene Liganden. b) Bestimmen Sie die systematischen Namen Ihrer Komplexe. Tauschen Sie die Komplexnamen mit anderen Azubis (z.B. in Ihrem Betrieb) aus, mit der gegenseitigen Aufgabe die Formeln der Komplexe aufzustellen und zu bestimmen, welche Edelgaskonfiguration erreicht wird.











