Quantenmechanik - Institut für Experimentelle Kernphysik
Werbung

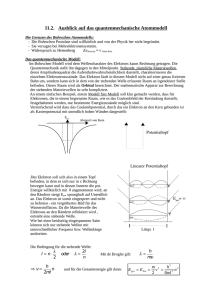
9. Übungsblatt Universität Karlsruhe Institut für Experimentelle Kernphysik Ausgewählte Kapitel der Physik SS 2007 Prof. Dr. G. Quast Ausgabe: 27.06.2007 Besprechung: 05.07.2007 Dr. T. Kuhr [email protected] Quantenmechanik Aufgabe 1: Potentialstufe Ein Teilchenstrom der Stärke von N0 Teilchen pro Sekunde und cm2 in x-Richtung, bestehend aus Teilchen der Energie E und Masse m, trifft bei der Position x = 0 auf eine Potentialstufe der Höhe V0 < E. a) Ein solcher Teilchenstrahl kann in guter Näherung als ebene Welle beschrieben werden. Geben Sie die Gleichung für die ensprechende ebene Welle an. Wie ist die Normierungskonstante zu wählen? Hilfe: Ein Strom ist gegeben durch das Produkt aus Teilchendichte und Teilchengeschwindigkeit. j = ρ · v. b) Was passiert in der klassischen Physik mit dem Teilchenstrahl, d.h. was sind die Teilchengeschwindigkeiten und Ströme rechts und links von der Potentialstufe? c) Um das korrekte, quantenmechanisch bestimmte Verhalten des Teilchenstrahls zu berechnen, kann man die eindimensionale, stationäre Schrödingergleichung benutzen. Berechnen Sie zunächst den Reflexionskoeffizienten, d.h. den Quotienten aus einlaufendem und reflektiertem Teilchenstrom. Hilfe: Formulieren Sie einen geeigneten Lösungsansatz für die Wellenfunktion für die Gebiete rechts und links der Potentialstufe. Welche Bedingungen sind an die Wellenfunktion bei x = 0 zu stellen, um die freien Koeffizienten im Lösungsansatz zu bestimmen? d) Bestimmen Sie den Transmissions-Koeffizienten, d.h. den Quotienten der Teilchenströme vor und hinter der Potentialstufe. e) Vergleichen Sie die quantenmechanische Lösung mit der klassischen! Unter welchen Grenzbedingungen stimmen klassische und quantenmechanische Lösung überein? Aufgabe 2: Potentialbarriere und Tunneleffekt Ein Elektron befindet sich in einem Potentialkasten, der bei x = 0 durch eine unendlich hohe Wand begrenzt ist, und bei x > 1.0 · 10−10 m durch eine Potentialbarriere mit der Dicke a = 0.1 nm und der Höhe V0 = 1000 eV (siehe Skizze). V= 8 V(x) V0 a 0 1 −10 10 x a) Skizzieren Sie den Verlauf der Wellenfunktion, wenn sich das Elektron im Potentialkasten im Grudzustand befindet. Nehmen Sie hierfür an, dass die Potentialbarriere so hoch ist, dass sich Wellenfunktion und Energie des Elektrons nur wenig von denen im Kastenpotential (Blatt 8, Aufg. 4) unterscheidet. b) Berechnen Sie näherungsweise den Transmissionskoeffizienten T für die Transmission eines Elektrons im Grundzustand durch die Potentialbarriere. Hinweis: Nehmen Sie an, daß man die Wellenfunktion des Elektrons als Überlagerung einer nach links und nach rechts laufenden Welle auffassen kann, die durch die Barriere tunnelt. c) Das Elektron wird nach einer gewissen Zeit aus dem Potentialkasten wegtunneln. Man kannn das folgendermassen verstehen: Das Elektron bewegt sich mit einer der Grundzustandsenergie entsprechenden Geschwindigkeit zwischen der rechten und der linken Seite periodisch hin und her. Berechnen Sie die dafür benötigte Zeit tu . Wie groß ist die Transmissionsrate pro Umlauf, d.h. T /tu ? Wie groß ist deren Kehrwert, d.h. tu /T ? Hinweis: tu /T ist die “Zerfallszeit” des Elektrons im Potentialtopf. Die Änderung der Wahrscheinlichkeit Pe , das Elektron nach einer Zeit ∆t noch im Kasten zu finden, ist gegeben durch ∆Pe = −∆t tTu · P (t), oder, als Differentialgleichung geschrieben: dPe dt = T tu t · P ; diese hat die Lösung P (t) = e− τ mit τ = tu T . Aufgabe 3: Bohr’sches Atommodell und Wasserstoff (alte Klausuraufgabe) Im Bohr’schen Modell des Wasserstoffatoms wird angenommen, dass sich ein Elektron auf einer Kreisbahn (strahlungslos) im Coulomb-Potential des Protons bewegt. a) Geben Sie die kinetische und potentielle Energie des Elektrons als Funktion des Abstands r vom Proton an. Wie groß ist der Drehimpuls des Elektrons als Funktion von r? b) Nach dem 3. Bohr’schen Postulat soll der Drehimpuls “gequantelt” sein und nur Werte von L = nh̄, n = 1, 2, ... annehmen dürfen. Welche Werte für die möglichen Radien rn und die Gesamtenergie En des Elektrons ergeben sich? c) Die exakten quantenmechanischen Lösungen für das Wasserstoffatom werden durch die Quantenzahlen n, l und m charakterisiert. Welche Werte können diese Quantenzahlen jeweils annehmen und was ist hier der größtmögliche Wert des Drehimpulses für einen Zustand n? d) Diskutieren Sie kurz die Unzulänglichkeiten des Bohr‘schen Modells im Vergleich zur korrekten quantenmechanischen Behandlung des Wasserstoffproblems. (mindestens drei) Aufgabe 4: Ionisationsenergie Die Ionisationsenergie ist die Energie, die man benötigt, um ein Elektron aus einem Atom zu entfernen. Bestimmen Sie die Ionisationsenergien von a) einem Wasserstoffatom, dessen Elektron sich im angeregten Zustand mit n = 3 befindet. b) He+ im n = 2-Zustand (Heliumkern, einfach ionisiert, d.h. nur ein Elektron, das sich im n = 2-Zustand befindet) c) Li++ im n = 4-Zustand. Hinweis: Der He-Kern enthält 2 Protonen, der Lithium-Kern 3 Protonen. Rydberg-Energie: E0 = 13, 6 eV 2 Aufgabe 5: Drehimpuls ~ für die Bahn eines Elektrons im a) Berechnen Sie die Länge der Drehimpulsvektoren L Zustand mit den Drehimpulsquantenzahlen l = 0, l = 1 und l = 2. b) Bestimmen Sie für diese drei Fälle die möglichen z-Komponenten des Bahndrehim~ durch geeignete graphische Konstruktion. pulsvektors L c) Wie sehen für das Beispiel l = 1 die magnetischen Momente aus? —————————————————————————————————————————– Die Übungsaufgaben finden Sie auch im Internet unter der URL: http://www-ekp.physik.uni-karlsruhe.de/~tkuhr/AKdPh 3