Das Elektron und das Atom
Werbung

Kapitel 2
Teilchenphysik
35
Bei der Kathodenstrahlröhre wird ein Glasrohr mit Hilfe einer
Vakuumpumpe (solche Pumpen wurden am Ende des 19. Jahrhunderts entwickelt) evakuiert. Siehe Abb. 1.
2.1.1 Die Kathodenstrahlröhre
Eine wichtige Rolle am Anfang der Teilchenphysik spielte die
Kathodenstrahlröhre.
Man kannte die atomaren Absorptions- und Emissionspektren der Atome, aber es gab nur empirische Regeln dafür.
Man sagt oft, dass die Entdeckung des Elektrons im Jahr 1897 der
Geburt der Teilchenphysik entspricht. Vor 1897 existierte die
moderne atomare Beschreibung der Materie nicht:
2.1 Der Ursprung der Teilchenphysik
Das Elektron und das
Atom
36
Die Kathodenstrahlröhre.
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Man beobachtete auch Licht am Ende des Rohrs, als man dort einen
Fluoreszenzschirm aufstellte.
Man weiss auch, dass bestimmte Arten von Gasen Licht erzeugen
können, wenn ein elektrischer Strom fliesst.
Ein niedriger Druck genügt, um einen Strom zu beobachten. Man studierte die Eigenschaften der erzeugten Ströme als Funktion des Gasdrucks, der Art von Gas, der elektrischen Spannung, usw...
ein elektrischer Strom durch den elektrischen Kreis kann
erzeugt werden, wenn man das Rohr langsam mit Gas füllt.
Man beobachtete experimentell:
Figur 1.
Zwei elektrische Platten werden im Glasrohr eingebaut. Eine elektrische Spannung wird mit Hilfe von Batterien zwischen der Kathode
und der Anode erzeugt.
Das Elektron und das Atom
Physik
37
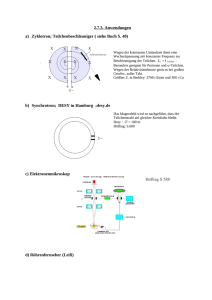
Die Strahlen von verschiedenen radioaktiven Elementen wurden in
eine bestimmte Flugrichtung gezwungen. Man erzeugte ein zur
Ebene senkrechtes magnetisches Feld in einem Gehäuse, das evakuiert wird. Die Strahlen werden mit Hilfe einer photographischen
Platte nachgewiesen.
Am Ende des 19. Jahrhunderts wusste man, dass es in der Natur drei
Arten von radioaktiven Strahlen gibt. Diese Formen von Strahlen
wurden mit Hilfe eines magnetischen Feldes charakterisiert. Siehe
Abb. 2.
Im Jahr 1898 entdeckten Marie und Pierre Curie, dass verschiedene
Elemente existieren, die auch radioaktiv sind: das Polonium und
Radium. Diese Elemente schwärzten auch photographische Filme.
Im Jahr 1896 entdeckte Becquerel die natürliche Radioaktivität,
d.h., es gibt in der Natur ein radioaktives Element, das spontan
Strahlen emittiert: das Uran. Uran schwärzte photographische Filme.
2.1.3 Drei Arten von Strahlen
Diese Strahlen werden in der Kathodenstrahlröhre erzeugt. Er beobachtete, dass sie durchdringend und unsichtbar waren. Sie konnten
mit Hilfe von photographischen Filmen nachgewiesen werden,
indem die Strahlen den Film schwärzten.
Im Jahr 1895 entdeckte Röngten “zufällig” die sogenannten Röntgenstrahlen (“X-rays”).
2.1.2 Röntgenstrahlen (1895)
Der Ursprung der Teilchenphysik
38
Die Alpha-Strahlen verschwinden wenn das Gehäuse nicht evakuiert ist. Die Alpha-Stahlen fliegen nur einige Zentimeter durch Luft
mit normalem Druck.
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
1.
Man beobachtete auch, dass die Strahlen mehr oder weniger durchdringend durch Materie sind:
Man schloss daraus, dass Alpha- und Beta-Strahlen elektrisch geladen sind, weil sie durch ein magnetisches Feld abgelenkt werden. Die
Gamma-Strahlen sind elektrisch ungeladen.
Es gab drei unterschiedliche Zonen auf dem Film, die
geschwärtz wurden. Diese drei Zonen entsprechen den drei
Arten von Strahlen: die sogenannten Alpha-, Gamma- und
Beta-Strahlen.
Man beobachtete experimentell:
Ein Apparat, um die verschiedenen Arten von Strahlen zu
studieren.
Figur 2.
Das Elektron und das Atom
Einige Millimeter von dichter Materie sind genügend, um die
Beta-Strahlen zu stoppen.
Die Gamma-Strahlen, die mit Röntgen-Strahlen identifiziert wurden, sind die durchdringendsten: man braucht einige Zentimeter
Blei, um die Intensität der Strahlen zu reduzieren.
Physik
Figur 3.
39
Die experimentelle Anordnung, um das Verhältnis e/m zu messen.
Seine experimentelle Anordnung ist in Abb. 3 gezeigt.
Er hat eine Kathodenstrahlröhre benutzt und hat eine genaue
Messung des Verhältnisses e/m der Teilchen durchgeführt, die
in der Kathodenstrahlröhre emittiert wurden, wobei e die
elektrische Ladung und m die Masse der Teilchen bedeutet.
J.J. Thompson hat das Elektron 1897 entdeckt:
2.2 Die Entdeckung des Elektrons
3.
2.
Die Entdeckung des Elektrons
40
Die emittierten Teilchen mussten elektrisch geladen sein, weil die
Position des Flecks mit der Intensität des E- oder B-Feldes zusammenhängt.
Aus der Richtung der Krümmung sind die Strahlen negativ geladen.
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Die Felder sind so gerichtet, dass die magnetischen und elektrischen
Kräfte entgegengerichtet sind. Man kann die Stärke der Felder so
wobei v die Geschwindigkeit des Teilchens ist.
B-Feld: senkrecht zum E-Feld und in guter Näherung auch zur
Geschwindigkeit
r
r r
r r
Kraft FB = qv ¥ B = -ev ¥ B = evB
E-Feld: zwei parallele metallische Platten der Länge l und Abstand d
mit Spannung V
r V
r
r eV
Feldstärke: E =
fi Kraft FE = -eE =
d
d
Quantitativ können wir sagen:
2.
1.
Er beobachtete die Lage des Flecks auf dem Fluoreszenz-Schirm und
bemerkte:
Um das Verhältnis e/m der von der Kathode emittierten Teilchen zu
messen, hat J.J. Thompson ein elektrisches und ein magnetisches
Feld im Rohr erzeugt. Das E- und B-Feld wurden senkrecht zu einander gerichtet.
Am Ende des Glasrohrs wurde ein Fluoreszenzschirm aufgestellt.
Damit konnte man die Bahnkurve der Teilchen bestimmen.
Das Elektron und das Atom
fi
v=
V
dB
2
2
Physik
41
Das Verhältnis (e/m)Ionen für Ionen war aus elektrolytischen Experimenten bekannt, wobei e die gesamte elektrische Ladung (Q=I.Dt)
J.J. Thompson beobachtete, dass das gemessene Verhältnis unabhängig von der Art des Gases ist. Er schloss daraus, dass das Verhältnis
eine Eigenschaft der Strahlen, die von der Kathode emittiert wurden,
darstellt. Wie konnte man sicher sein, dass er ein neues Teilchen entdeckt hatte?
Weil die Geschwindigkeit v mit eingeschaltenem E- und B-Feld
gemessen wurde, konnte J.J. Thompson das Verhältnis e/m berechnen.
2
1 Ê e ˆ Ê V ˆ Ê 1ˆ
Ê dd ( l) ˆ
Ê eˆ 1
S1S2 ª Á
˜ L = Á ˜ Á ˜ Á ˜ 2 lL µ Á ˜ 2
Ë dl ¯
Ë m¯ v
2 Ë m¯ Ë d ¯ Ë v ¯
und die Ablenkung auf dem Schirm ist gleich
1
1 Ê eV ˆ Ê l ˆ
1 Ê e ˆÊV ˆÊ lˆ
d ( l) = at 2 ª Á ˜ Á ˜ = Á ˜ Á ˜ Á ˜
2
2 Ë md ¯ Ë v ¯
2 Ë m¯ Ë d ¯ Ë v ¯
Es gilt (Siehe Abb. 3),
Nun wird das magnetische Feld ausgeschaltet und die Ablenkung
S1S2 des Lichtflecks auf dem Schirm gemessen.
und so wird die Geschwindigkeit des Teilchens gemessen.
eV
= evB
d
wählen, dass die Teilchen nicht abgelenkt werden, d.h., beide Kräfte
kompensieren einander
Die Entdeckung des Elektrons
42
m << mIonen
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Er hatte das Elektron entdeckt.
Er schloss daraus, dass die Strahlen, die von der Kathode der Kathodenstrahlröhre emittiert wurden, Teilchen mit sehr niedriger Masse
entsprechen.
Ê eˆ
Ê eˆ
Á ˜ ª 1836Á ˜
Ë m¯
Ë m¯ H +
Der grösste Wert für (e/m)Ionen erhält man für Wasserstoff. J.J.
Thompson fand, dass
d.h., die Masse des unbekannten Teilchens musste viel kleiner sein
als die Masse eines Ions.
e = eIonen
und
entweder e >> eIonen oder m << mIonen
J.J. Thompson nahm an, dass
und deshalb
Ê eˆ
Ê eˆ
>> Á ˜
Á ˜
Ë m ¯ J.J.Thompson
Ë m ¯ Ionen
Experimentell wurde gefunden, dass gilt,
und m die gesamte Masse bedeutet, die auf der Elektrode abgeschieden wird.
Das Elektron und das Atom
das Elektron ist negativ geladen: was kompensiert diese Ladung?
das Elektron ist sehr leicht: woher kommt die Masse der Atome?
Physik
1. H. Geiger (1882-1945), E. Marsden (1889-1970), E. Rutherford (1871-1937)
43
Wegen der elektromagnetischen Welchselwirkung wird ein Stoss zwischen den a-Teilchen und den Goldatomen stattfinden. Während des
Stosses wird Impuls zwischen den a-Teilchen und den Atomen übertragen. Die a-Teilchen werden abgelenkt.
Ein paralleler Strahl von a-Teilchen wurde senkrecht auf eine 0,4µm
dünne Goldfolie gerichtet. Siehe Abb. 4.
a-Teilchen: doppelt ionisiertes Heliumatom
Rutherford hatte die Identität von a-Strahlen mit einer ähnlichen
Messung wie J.J. Thompson gefunden: er hatte das Verhältnis (e/m)
für a-Strahlen gemessen.
Streuexperiment: eine der wichtigsten experimentellen Entwicklungen der Teilchenphysik
Im Jahr 1911 hat Rutherford die Resultate seines wichtigen Streuexperiments1 mit a-Teilchen veröffentlicht.
2.3.1 Das Streuexperiment von Rutherford
2.
1.
J.J. Thompson verstand, dass das Elektron, das er entdeckt hatte, eine
fundamentale Rolle in der Struktur der Materie spielen muss. Es gab
trotzdem mindenstens zwei Probleme:
2.3 Die Entdeckung der Struktur der
Atome
Die Entdeckung der Struktur der Atome
44
Die Anordnung des Streuexperiments von Rutherford et. al.
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Figur 4.
Rutherford schloss aus seinen Experimenten, dass eine Rückwärtsstreuung von a-Teilchen nicht von den Elektronen verursacht werden
kann, da die Masse der Elektronen viel zu gering ist, um die schweren
a-Teilchen so stark ablenken zu können.
Die meisten a-Teilchen werden in Vorwärtsrichtung gestreut.
Eine geringe Anzahl wird nach rückwärts gestreut.
Experimentell beobachtete man:
Das Elektron und das Atom
Physik
Figur 5.
Die Definition der Grössen für das Streuexperiment.
45
und die Bahnkurve des a-Teilchens wurde mit Hilfe der klassischen
Mechanik vorausgesagt.
Streuwinkel: q
Stossparameter b: (vor dem Stoss)
Um sein Modell mit der Theorie zu vergleichen, wurden der Streuwinkel und der Stossparameter eingeführt (Siehe Abb. 5)
Mit diesen Experimenten bewies Rutherford, dass ein Atom aus
einem positiv geladenen Kern mit einer äusseren Elektronenhülle
besteht. Der Kern des leichtesten bekannten Atoms (Wasserstoff)
wurde von Rutherford als Proton bezeichnet.
Nach der Impulserhaltung muss die Masse des Stosspartners
viel grösser als die des a-Teilchens sein. Rutherford stellte
daraufhin sein Atommodell vor, bei dem ein positiv geladener
massereicher Kern von einer fast masselosen Hülle von negativ geladenen Elektronen umgeben ist.
Die Entdeckung der Struktur der Atome
46
1 zZe 2
4pe 0 r 2
D
(cosa - 1) = 0
2b
fi
zZe 2
p -q
q 2b
q
cot
= cot =
fi b(q ) =
2
2 D
2( 4pe 0 ) E
2
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
wenn das a-Teilchen mit einem Stossparameter zwischen b
und b+db auf den Kern trifft, wird es nach dem Stoss einen
Streuwinkel zwischen q und q+dq besitzen.
Wir definieren nun, dass
tan
Mit q=p–a erhalten wir eine Beziehung zwischen dem Streuwinkel q
und dem Stossparameter b:
sin a +
zZe 2
1
und E = mv 2
2
(4pe 0 ) E
2b 1 - cosa
a
=
= tan
2
D
sin a
wobei D =
Wenn r nach unendlich geht, dann gilt
1 1
D
= sin a + 2 (cosa - 1)
2b
r b
findet man die folgende Bahnkurve
r
F =
Durch die Lösung des Newtonschen Bewegungsgesetzes für eine
Kraft der Form
Die Coulombsche Kraft ist zentral (der gesamte Drehimpuls wird
erhalten) und wir nehmen an, dass der Kern sich während des Stosses
nicht bewegt.
Das Elektron und das Atom
und
dW ∫ d cosqdf
Physik
db
b db
ds
∫b
=d cosq
sin q dq
dW
b Ê zZe 2 ˆ d Ê q ˆ
=Á cot ˜
sin q ÁË 2( 4pe 0 ) E ˜¯ dq Ë
2¯
Wir bestimmen das Verhältnis
Figur 6.
s auf den Kern trifft, wird
Ein Teilchen, das durch die Fläche ds
W streuen.
nach dem Stoss in den Raumwinkel dW
wenn das a-Teilchen durch die Fläche ds auf den Kern trifft,
wird es nach dem Stoss in den Raumwinkel dW streuen.
d.h.
ds ∫ bdbdf
47
Wenn wir die Fläche ds und den Ramwinkel dW betrachten (Siehe
Abb. 6), erhalten wir
Die Entdeckung der Struktur der Atome
48
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Dass diese starke Abhängigkeit gilt, bewies Geiger 1911 experimentell in den Grenzen 5° und 150°. In diesem Bereich ändert sich der
Wirkungsquerschnitt um einen Faktor ª105 !
Wir bemerken die charakteristische 1/sin4q/2 Form des Wirkungsquerschnitts, die zu einer sehr starken Abhängigkeit von q führt. Man
spricht von einem vorwärts-“peaked” Wirkungsquerschnitt.
wobei q der Streuwinkel und E die Energie des Teilchens ist. Dieses
Resultat wird in Abb. 7 als Funktion des Streuwinkels geplottet.
Ê zZe 2 ˆ
1
Ê ds ˆ
=Á
Á ˜
q
Ë dW¯ Rutherford Ë ( 4pe 0 ) 4 E ˜¯
sin 4
2
2
Zusammenfassend haben wir die folgende Beziehung gefunden
Dieses Verhältnis wird als differentieller Wirkungsquerschnitt
bezeichnet.
Ê zZe 2 ˆ
1
=Á
˜
Ë ( 4pe 0 ) 4 E ¯ sin 4 q
2
2
q
q
q
2
2
1 Ê zZe 2 ˆ 1 cos 2
1 Ê zZe 2 ˆ 1 2 sin 2 cos 2
=
= Á
8 Ë ( 4pe 0 ) E ˜¯ sin q sin 3 q 16 ÁË ( 4pe 0 ) E ˜¯ sin q sin 4 q
2
2
qÊ
ˆ
2
Ê zZe 2 ˆ cot 2 Á
1 ˜1
= -Á
˜
Ë 2( 4pe 0 ) E ¯ sin q ÁÁ sin 2 q ˜˜ 2
Ë
2¯
Das Elektron und das Atom
Physik
Figur 7.
Der Rutherford-Wechselwirkungsquerschnitt als Funktion des
Streuwinkels.
49
50
2.4 Deutung des Wirkungsquerschnitts
Falls q nach Null geht, beobachten wir eine Divergenz. Ihr Ursprung
liegt in der Form der Coulombschen Kraft, deren Reichweite unendlich ist. In Wirklichkeit werden die Elektronen um den Kern die Kernladung abschirmen.
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Ê ds ˆ 1 dN (q,f )
Á ˜=
Ë dW¯ f dW
Der Wirkungsquerschnitt ist proportional zur Anzahl der Teilchen pro Zeiteinheit, die in den Raumwinkel dW gestreut werden:
und es folgt:
Ê ds
ˆ
Ê ds ˆ
dW˜ = f Á ˜ dW
dN ∫ fds = f Á
Ë dW ¯
Ë dW¯
Diese Teilchen werden in dem Raumwinkel dW gestreut, d.h. die
Anzahl der Teilchen, die in den Raumwinkel dW gestreut werden, ist
gleich
dN ∫ fds
Wir betrachten die Anzahl der Teilchen dN, die eine Fläche ds pro
Zeiteinheit durchqueren
f=Anzahl der Teilchen pro Zeiteinheit und pro Flächeneinheit
(z.B. Teilchen/m2/s)
Wir betrachten im Allgemeinen einen Strahl von Teilchen. Wir nehmen an, dass die Teilchen gleichförmig in einer Fläche senkrecht zur
Bewegungsrichtung verteilt sind, d.h., wir definieren den Fluss f der
Teilchen als
2.4.1 Differentieller und totaler Querschnitt
Das Elektron und das Atom
Die Entdeckung der Struktur der Atome
s
dx
Physik
Figur 8.
Skizze einer Reaktion eines Teilchenstrahls mit einem dünnen
Target der Dicke dx.
Fluss f
Fläche A
51
Wir bemerken, dass der Wirkungsquerschnitt die Einheit einer Fläche
besitzt. Man kann ihn daher geometrisch deuten. Wir betrachten ein
dünnes Target der Fläche A und der Dicke dx (Siehe Abb. 8). Die
schwarzen Punkte entsprechen den Streuzentren und jedes Streuzentrum hat eine Streufläche s. Die Dichte der Streuzentren sei r
(Anzahl der Streuzentren pro Volumeneinheit) Der Fluss der (senkrecht zur Fläche des Targets) einfallenden Teilchen wird als f
bezeichnet.
Im Fall des Rutherford-Wechselwirkungsquerschnitts ist der totale
Wirkungsquerschnitt divergent, wegen des Verhältnisses wenn q nach
Null geht.
Ê ds ˆ
s tot = Ú Á ˜ dW
Ë dW¯
Der totale Wirkungsquerschnitt wird definiert als:
Deutung des Wirkungsquerschnitts
52
A
(rAdx )s
= rdxs
( Einheit: L-3 LL2 = 1)
R sin a = b
b = R sin a = R sin((p - q ) / 2) = R cos(q / 2)
wobei
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Wir berechnen nun (Siehe Kap. 2.3.1):
D.h.,
2a + q = p
Dass der Wirkungsquerschnitt mit der geometrischen Fläche der
Streuzentren verwandt ist, kann mit Hilfe der elastischen Streuung an
einer harten Kugel veranschaulicht werden. Siehe Abb. 9. Der Radius
der Kugel ist R. Die Bedingung für einen harten elastischen Aufprall
ist:
wobei NA die Avogadro-Zahl ist, und M ist die Gesamtmasse des Targets.
N WW = (Vr)fs = N Nukleonfs = ( N A M )fs
wobei V das Volumen des Targets ist. Wenn wir z.B. Nukleonen als
Streuzentren betrachten, wäre die Rate
N WW = fArdxs = ( Adx ) rfs = (Vr)fs
Die Wechselwirkungsrate (Anzahl pro Zeiteinheit) ist daher
Wahrscheinlichtkeit =
Wenn die einfallenden Teilchen gleichförmig verteilt sind, ist die
Wahrscheinlichkeit, dass ein Teilchen mit einem Streuzentrum des
Targets wechselwirkt, gleich dem Verhältnis der Fläche der Streuzentren zur Targetfläche:
Das Elektron und das Atom
2
R2
Êqˆ Êqˆ R
cosÁ ˜ sinÁ ˜ =
Ë 2¯ Ë 2¯ 4
2 sin q
=
Physik
Figur 9.
a
Streuung an einer harten Kugel.
b
a
a
q
R
53
Er entspricht der Querschnittsfläche der Kugel. Teilchen innerhalb
der Fläche werden gestreut. Die Teilchen ausserhalb der Fläche sind
unbeeinflusst.
s tot
R2
Ê ds ˆ
= Ú Á ˜ dW =
dW = pR 2
Ë dW¯
4 Ú
Der totale Wechselwirkungsquerschnitt ist daher, wie erwartet,
gleich:
b R Êqˆ
sinÁ ˜
sin q 2 Ë 2 ¯
=
db
b db
ds
∫b
=
d cosq sin q dq
dW
Deutung des Wirkungsquerschnitts
54
fnN1N 2
4ps xs y
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
wobei f die Umlaufsfrequenz ist, n ist die Anzahl der “Teilchenpakete” im Ring, N1, N2 sind die Anzahlen von Teilchen pro Paket für
die Strahlen 1 und 2, und sx, sy sind die transversalen Dimensionen
der Teilchenpakete am Kollisionspunkt (unter der Annahme einer
Gaussverteilung im Raum).
L=
Die Luminosität kann als Funktion der Parameter des Kolliders
bestimmt werden:
Die Einheit der Luminosität ist eine inverse Fläche pro Zeiteinheit.
Die geplante Luminosität beim CERN LHC ist z.B. 1034 cm–2 s–1.
Der gesamte Proton-Proton Wirkungsquerschnitt ist bei einer SPEnergie von 14 TeV ungefähr sª0,1 barn=10–25 cm2. Man erwartet
somit R=109 Ereignisse pro Sekunde.
R = Ls
Die Reaktionsrate R bei Kollidern wird als das Produkt des Wirkungsquerschnitts und der Luminosität L definiert:
Bei Kollidern kollidieren zwei Strahlen von Teilchen. Z.B. beim LEP
am CERN wurden Elektronen-Antielektronen(Positronen)-Kollisionen studiert. Weil Teilchen und Antiteilchen entgegesetzte elektrische
Ladungen besitzen, werden sie im gleichen Ring beschleunigt. Bei
Kollidern kann offensichtlich nur die Wechselwirkung zwischen stabilen Teilchen wie Ionen, Protonen-Antiprotonen oder ElektronenPositronen studiert werden.
2.4.2 Die Luminosität
Das Elektron und das Atom
Physik
ÏM + E = E ¢ + E ¢
g
p
g
Ô p
Ìr
r ¢ r¢
ÔÓ pg = p p + pg
55
Im Jahr 1932 schliesst Chadwick mit Hilfe einer kinematischen
Analyse, dass die X-Strahlen keine elektromagnetische Strahlung
sein konnten. D.h., er bewies, dass wenn die X-Strahlen Protonen
durch einen Vorgang herausschlagen, der ähnlich zum Compton-Vorgang ist, dann muss wegen der Erhaltung der Energie und des Impulses gelten (Siehe Abb. 10):
Im Jahr 1932 entdeckten Irène Curie-Joliot und Joliot, dass die XStrahlen Protonen herausschlagen konnten.
Sie dachten zuerst, dass X elektromagnetische Strahlen (d.h. g-Strahlen) waren.
Strahl
a + Be Æ C + {
X
Im Jahr 1930 beobachteten Bothe und Becker neutrale durchdringende Strahlen, die erzeugt wurden, wenn a-Teilchen auf ein Beryllium-Target aufprallen:
Rutherford sagte die Existenz eines neuen Teilchens voraus,
das ähnliche Eigenschaften wie das Proton hat, aber elektrisch ungeladen sein musste: das sogenannte Neutron.
Nach der Entdeckung des Protons und des Elektrons war das Verständnis der Atomstruktur nicht vollständig. Man konnte die Masse
und den Spin von Isotopen und von Elementen schwerer als Wasserstoff nicht erklären.
2.5 Die Entdeckung des Neutrons
Die Entdeckung des Neutrons
56
θ
(E'γ,p'γ)
(E'p,p'p)
2
2
2
Eg =
M p - E p ¢ + p p ¢ cosq
M p ÊË E p ¢ - M p ˆ¯
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
Es folgt,
Ê M + E - E ¢ ˆ = Ê E ¢ ˆ = E 2 + Ê p ¢ ˆ - 2 p ¢ E cosq
g
p ¯
g
p
g
Ë p¯
Ë g ¯
Ë p
2
Mit der Gleichung für die Energie finden wir
Entdeckung des Neutrons: Compton-Streuung an einem Proton.
2
Eg2 + ÊË p p ¢ ˆ¯ - 2 p p ¢ Eg cosq = ÊË Eg ¢ ˆ¯
(Eγ,pγ)
Figur 10.
oder
2
r
r
r
r 2
pg - p p ¢ = pg ¢ fi pg2 + ÊË p p ¢ ˆ¯ - 2 p p ¢ pg cosq = ÊË pg ¢ ˆ¯
Wenn wir den Streuwinkel q des Protons einführen, erhalten wir
Das Elektron und das Atom
M p - E p¢ + p p¢
M p ÊË E p ¢ - M p ˆ¯
=
p p¢ - T ¢
M pT ¢
Physik
a + Be Æ C + n
und
n+ pÆn+ p
57
Die X-Teilchen können nicht g-Strahlen sein. Was beobachtet wurde,
waren Protonen, die durch die Reaktionen
Chadwick schloss daraus, dass diese grosse Energie mit den bekannten radioaktiven Energien nicht kompatibel war.
Eg min ª 50 MeV
2
1
M Ê v ¢ ˆ ª 5 MeV und p p ¢ c ª M p v p ¢ c ª 100 MeV
2 pË p ¯
und deshalb
T¢ ª
Numerisch findet man, dass für diesen Wert das einfallende Photon
mindenstens eine Energie gleich 50 MeV besitzen muss, um Protonen
mit der beobachteten Geschwindigkeit herauszuschlagen, d.h.:
v p ¢ ª 3 ¥ 10 9 cm / s ª 0.1c
Curie und Joliot hatten die Geschwindigkeit des herausgeschlagenen
Protons gemessen:
wobei T’ die kinetische Energie des herausgeschlagenen Protons ist.
Eg min =
Der minimale Wert der Photonenergie erhält man für cosq=1. In diesem Fall gilt
Die Entdeckung des Neutrons
58
Teilchenphysik II&III, WS 03/04-SS04, Prof. André Rubbia (ETHZ)
herausgeschlagen wurden. In diesem Fall ist die kinematische Situation ganz anders, weil das Neutron eine ähnliche Masse wie das Proton besitzt.
Das Elektron und das Atom