Zunehmende Probleme mit Health-Claims Health-Claims sind
Werbung

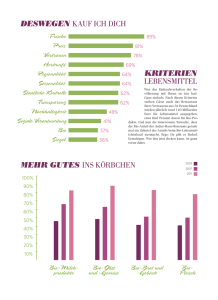
Zunehmende Probleme mit Health-Claims Health-Claims sind gesundheitsbezogene Angaben auf Lebensmitteln. Sie charakterisieren eine Grenzlinie zwischen Lebensmitteln und Arzneimitteln. Grundsätzlich gilt, dass für Lebensmittel nicht mit krankheitsbezogenen Angaben geworben werden darf. Zulässig waren schon immer so genannte gesundheitsbezogene Angaben, wobei naturgemäß die Abgrenzung zwischen krankheitsbezogenen und gesundheitsbezogenen Informationen sehr schwierig war. Hier sollen nunmehr die so genannten Health-Claims Abhilfe schaffen. Allerdings ist es für die Verwendung dieser Health-Claims, also gesundheitsbezogener Angaben, notwendig, dass die genauen Formulierungen von der Europäischen Behörde für Lebensmittelsicherheit (EFSA) in Parma geprüft und freigegeben werden. Die Lebensmittelwirtschaft geht davon aus, dass eine gut fünfstellige Zahl von Anträgen auf Zulassung bestimmter gesundheitsbezogener Formulierungen bereits bei der Behörde vorliegt. Ende vergangenen Jahres wurden nun die ersten Health-Claims geprüft – mit niederschmetterndem Ergebnis: Die überwiegende Zahl der Anträge wurde zurückgewiesen, da die jeweilige Aussage wissenschaftlich nicht ausreichend belegt sei. Besonders problematisch war dabei, dass die Behörde offensichtlich noch nicht einmal Standardwissen aus Lehrbüchern als Beweis für bestimmte Wirksamkeitsaussagen anerkannt hat. Vielmehr wurden umfangreiche so genannte Interventionsstudien gefordert, die Wirksamkeitsaussagen auf Testreihen mit großer Teilnehmerzahl stützen. Solche Studien sind natürlich mit einem erheblichen Zeitaufwand und Kosten verbunden. Es besteht daher die Befürchtung, dass eine Fortführung dieser Prüfungspraxis insbesondere kleinere Unternehmen benachteiligt und einen entsprechenden Markteintritt erschwert. Nach Ansicht von Beobachtern waren die bislang zurückgewiesenen Anträge überwiegend gut begründet und keinesfalls „Grenzfälle“. Dieses Ergebnis verwundert umso mehr, als die nationalen Länderbehörden bereits eine Vorauswahl bei den Anträgen zur Zulassung von Health-Claims übernommen hatten: Formale Fehler oder offensichtlich unbegründete Anträge wurden schon aussortiert, bevor die Unterlagen nach Brüssel geschickt wurden. In diesen Zusammenhang passt eine Entscheidung des Landgerichts Frankfurt, wonach ein Bier mit der Bezeichnung „Anti-Aging“ gegen die Health-Claims-Verordnung verstoße. Verwunderlich ist, dass dieses Bier mit der entsprechenden Bezeichnung als Marke eingetragen ist. Damit platzt wohl ein Traum deutscher Biergenießer, wonach Bier, in ausreichenden Ma- -2- ßen genossen, eine Alterung verhindere. Dafür würde allerdings die Erkenntnis sprechen, dass Alkohol konserviert (LG Frankfurt, 4 K 455/04). Abgrenzung Lebensmittel/Arzneimittel in der aktuellen Rechtsprechung Zwei aktuelle Entscheidungen des Bundesgerichtshofs befassen sich ebenfalls mit der Abgrenzung zwischen Arzneimitteln und Lebensmitteln, und zwar anhand des Beispiels der bereits seit Jahrzehnten streitigen „Knoblauchkapseln“: Leider lassen die beiden neuen Entscheidungen noch immer keine klare und eindeutige Abgrenzung auch für andere Fälle zu. Es fehlen nachvollziehbare und in der Praxis handhabbare Abgrenzungskriterien. Der BGH orientiert sich vielmehr an der jüngeren Rechtsprechung, wonach die konkret empfohlene Tagesdosis keine pharmakologische Wirkung haben darf. Diese Frage wurde in den beiden genannten Fällen verneint. Fraglich ist aber, was eine pharmakologische Wirkung in diesem Zusammenhang ist: Stoffe, die zwar auf den menschlichen Körper einwirken, jedoch keine oder zumindest keine nennenswerte Auswirkung auf den körperlichen Stoffwechsel haben, sollen keine pharmakologische Wirkung haben und gelten danach als Lebensmittel. Ein Erzeugnis, dass einen Stoff enthalte, der auch mit der normalen Nahrung aufgenommen wird, sei danach nicht als Arzneimittel anzusehen, wenn durch das Erzeugnis keine gegenüber den Wirkungen bei normaler Nahrungsaufnahme nennenswerte Einflussnahme auf den Stoffwechsel erzielt wird. Der BGH orientiert sich insoweit an einer Entscheidung des Europäischen Gerichtshofs vom 15. November 2007 (Rechtssache C 319/05). Nicht zulässig sind damit auch sogenannte „Funktionsarzneimittel, deren pharmakologische Eigenschaften wissenschaftlich festgestellt worden und die dazu bestimmt sind, eine ärztliche Diagnose zu erstellen oder physiologische Funktionen wiederherzustellen, zu bessern oder zu beeinflussen. Der Bundesgerichtshof hat seine frühere Rechtsprechung nach eigener Definition an den durch Artikel 1 Nummer 1 der Richtlinie 2004/27/EG neu definierten Arzneimittelbegriff angepasst. Eine Anpassung von „Arzneimitteln nach Bezeichnung“, das heißt sogenannten Funktionsarzneimitteln hat sich aber insoweit nichts geändert. -3- Daher hat der BGH ein L-Carnitin-Produkt nicht als Arzneimittel, sondern als Lebensmittel eingestuft (Urteil vom 26. Juni 2008; I ZR 61/05). Solche Produkte würden, zumindest in der entschiedenen Darreichungsform und Menge, keine ernährungsphysiologische Wirkung erzielen, die über die eines Lebensmittels hinausgehe. Auch bei einer L-Carnitin-Dosierung bis zu 1000 mg ergebe sich nur insoweit eine physiologische Wirkung, als der Stoff als Nährstoff aufgenommen werde, nicht aber eine darüber hinausgehende pharmakologische Wirkung. Der BGH hat sich auch noch ausführlich damit auseinandergesetzt, ob nach der Verbrauchererwartung L-Carnitin-Produkte als Arzneimittel einzustufen sind und hat dies verneint. Dabei hat er, wie seit einigen Jahren, auf den durchschnittlich informierten, insbesondere auch informationsbreiten Verbraucher abgestellt. In eine ähnliche Richtung geht eine weitere Entscheidung des Bundesgerichtshofs vom 26. Juni 2008 (I ZR 112/05): Auch insoweit hat der BGH seine vorstehend beschriebene Definition unterstrichen. In dem hier entschiedenen Fall ging es um ein Präparat, das im Wesentlichen aus Hydroxymethylbutyrat („HMB“) besteht. Hier handle es sich um einen ambivalenten Stoff, der jedenfalls auch Ernährungszwecken dienen könne. Bei der im entschiedenen Fall maßgeblichen empfohlenen Dosierung fehle es jedoch jedenfalls an einer pharmakologischen Wirkung. Das Produkt „HMB“ habe vielmehr die Wirkung, einen Muskelabbau infolge intensiven sportlichen Trainings zu verhindern. Darin liege die Befriedigung eines besonderen Ernährungsbedürfnisses in einer besonderen Ernährungssituation für eine bestimmte Personengruppe, nämlich von Sportlern. Diese Personengruppe habe das Ziel, durch Training Muskelgewebe zu erhalten und aufzubauen. Daraus ergebe sich keine arzneiliche Zweckbestimmung. Das Produkt deckt lediglich einen sportspezifischen Bedarf. Auch wenn aufgrund besonderer persönlicher Lebensgestaltung, zum Beispiel aufgrund eines speziellen Sporttrainings, besondere physiologische Bedürfnisse und sich daraus ergebende Ernährungserfordernisse bestehen, führt dies nicht dazu, dass entsprechend hierauf speziell ausgerichtete Produkte automatisch zum Arzneimittel werden. Als Zweck der Ernährung kommt auch eine Steigerung der körperlichen Leistungsfähigkeit in Betracht. Auch eine Sportlernahrung, die nicht Mangelzustände nach Hochleistung auffüllen soll, sondern die Fähigkeit fördern soll, Höchstleistungen erst zu erreichen, ist immer noch Sportlernahrung und damit Lebensmittel. Der BGH hat darauf abgestellt, dass die Tatsache, das „HMB“ auch in „natürlichen“ Lebensmittel wie gereiftem Käse oder fermentiertem Gemüse vorkommt und auch in entsprechender Menge durch diese Lebensmittel aufgenommen werden kann, zeigt, dass es sich bei dem fraglichen Produkt um ein Lebensmittel und nicht um ein Arzneimittel gehandelt hat. -4- Gestützt auf ein Gutachten haben das Gericht und das untergeordnete Oberlandesgericht festgestellt, dass die empfohlene Tagesdosis von 1500 mg keine pharmakologische Wirkung entfaltet. Es ist insoweit auch keine Gesundheitsgefährdung gegeben. Daher war das Produkt als Lebensmittel und nicht als Arzneimittel einzustufen. Daneben hat sich die genannte Entscheidung auch wiederum mit L-Carnitin-Produkten auseinandergesetzt und hierzu die gleichen Feststellungen getroffen, wie sie auch in dem zuerst berichteten Urteil enthalten sind. Neuregelungen für die Bezeichnung von Lebensmitteln als „gluten-frei“ Die EU hat neue Regelungen für Lebensmittel erlassen, die als gluten-frei bezeichnet werden und die insbesondere auf die Backwarenindustrie erhebliche Auswirkungen haben werden: Danach dürfen nur noch solche Lebensmittel als „gluten-frei“ bezeichnet werden, die weniger als 20 ppm (parts per million) Gluten aufweisen. Diese Regelung stellt insoweit eine erhebliche Änderung dar, als die bisherigen internationalen Standards davon ausgingen, als gluten-Frei könnten auch Lebensmittel mit weniger als 200 ppm Gluten bezeichnet werden. Neuregelung für Nährwertkennzeichnung Am 18. November 2008 trat die Richtlinie 2008/100/EG der Europäischen Kommission in Kraft. Sie befasst sich mit der Nährwertkennzeichnung von Mineralstoffen und Vitaminen. Allerdings gelten derzeit noch recht großzügige Übergangsfristen. Spätestens zum 31. Oktober 2012 müssen jedoch alle dann im Verkehr befindlichen Lebensmittel den neuen Bestimmungen entsprechen. Daher ist es insbesondere für langlebige Produkte, das heißt beispielsweise für Nahrungsergänzungen, Konserven o.ä. bereits heute wichtig, die Produktion entsprechend auszurichten bzw. die Kennzeichnung anzupassen. Nahrungsmittel dürfen nach den neuen Regeln nur dann mit Inhaltsstoffen wie beispielsweise Chlorid, Kalium oder Vitamin C beworben werden, wenn Sie eine sogenannte „signifikante Menge“ des jeweiligen Stoffes enthalten. Als signifikant wird üblicherweise ein Mindestsatz von 15 % der empfohlenen Tagesdosis (RDA) angesehen. Insgesamt werden für 27 Vitamine und Mineralstoffe empfohlene Tagesdosen festgelegt, darunter befinden sich neun „neue“ Inhaltsstoffe, so beispielsweise Chlorid (RDA: 800 mg) und Kalium (RDA: 2 g). Die Abkürzung RDA steht für Recommended Daily Allowance. -5- Traurige Vernichtung Aktuell hat der deutsche Zoll wieder 1200 Flaschen besten ukrainischen Schaumweins vernichtet. Der Hintergrund sind unterschiedliche Bezeichnungen: In Osteuropa wird als Champagne jeder Schaumwein bezeichnet, hier handelt es sich praktisch um eine geläufige Gattungsbezeichnung. In der EU ist Champagne jedoch als Herkunftsbezeichnung für das gleichnamige französische Weinanbaugebiet geschützt. Daher kommt es immer wieder vor, dass entsprechend falsch bezeichnete Flaschen vernichtet werden müssen. Hier ist vor allem Importeuren zu großer Vorsicht und zur Prüfung aller Bestandteile einer Etikettierung geraten. Erneut Gen-Produkt genehmigt Die EU-Kommission hat der gentechnisch veränderten Sojasorte MON 89788 die Genehmigung erteilt. Diese Sorte kann nunmehr eingeführt und innerhalb der EU verwendet werden. Die sorgfältige Prüfung hat ergeben, dass weder für die menschliche noch für die tierische Gesundheit irgendein Risiko bestünde. Auch Umweltaspekte wurden hierbei berücksichtigt. In Zukunft ist damit zu rechnen, dass diese Sojasorte bei der Lebensmittelherstellung oder auch bei der Futtermittelherstellung verwendet wird. Pflicht ist allerdings ein entsprechender Hinweis auf den Gehalt gentechnisch veränderter Bestandteile. Gefahr für die bayrische Brezel? Nachdem die bayrische Brezel in der vergangen Jahrzehnten einen Siegeszug nicht nur durch ganz Deutschland angetreten hat, sondern inzwischen sogar in New York an jeder Straßenecke zu kaufen ist, droht nun eine Gefahr aus ungeahnter Richtung: aus Brüssel. Im Rahmen der sogenannten Health Claims-Verordnung werden Nährwertprofile von der EU-Kommission veröffentlich, aus denen sich ergibt, wie bestimmte Lebensmittel hergestellt werden sollen, wenn Nährwert- und gesundheitsbezogene Aussagen gemacht werden. Mit solchen Profilen wird insbesondere festgelegt, welche Menge an Fett, gesättigten Fettsäuren, Zucker und Salz in den jeweiligen Produkten als „noch gesund“ anzusehen sind. Lebensmittel, die diesen Profilen nicht entsprechen, dürfen daher nicht als „gesund“ beworben werden oder müssen einen Warnhinweis enthalten. Gegenwärtig wird bei der Herstellung von Brot in Deutschland ca. 1,8 bis 2,4 % Salz verwendet. Die EU möchte den Salzgehalt jedoch auf rund 1 % zurückschrauben. Dies ist teil- -6- weise mehr als eine Halbierung. Ganz besonders betroffen sind Laugenbrezeln, da diese im Verhältnis zum Gesamtgewicht einen relativ hohen Salzanteil im Mehl und insbesondere auf der Oberfläche enthalten. Dem Vernehmen nach hat sich nicht nur in Bayern erheblicher Widerstand formiert! Ich werde hierüber weiter berichten. Die Zahl derer, die sich auf EU-Ebene generell gegen die geplanten Nährwertprofile wenden, wird immer größer.