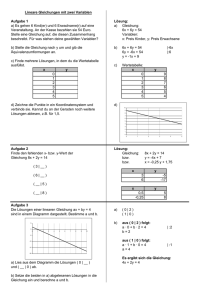
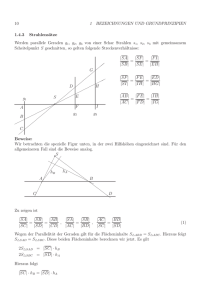
1.8.8 Das NAVIER-STOKES Gesetz Zur viskosen Reibung fähige
Werbung

1.8.8 Das NAVIER -STOKES Gesetz Zur viskosen Reibung fähige Fluide werden gerne durch das NAVIER-STOKES Gesetz beschrieben. In einer kartesischen Basis x lautet es: σ ij = − p δ ij + λ (x) (x) (x) ∂υ ∂υ i ∂ υ j (x) (x) δ ij + µ + ∂xk ( x ) ∂x j ∂xi . (x) k (1.8.27) Die skalaren, eventuell temperatur- und dichteabhängigen Größen λ und µ nennt man auch (x) (x) die Volumen- bzw. die Scherviskosität. Mithin ist das NAVIER-STOKES Gesetz dem HOOKEschen Gesetz für isotrope Festkörper mathematisch sehr ähnlich (vgl. Gleichungen (1.8.6) im Zusammenhang mit der Definition der Dehnung aus Gleichung (1.8.2)). Das ist nicht allzu verwunderlich, denn Flüssigkeiten verhalten sich typischerweise isotrop, an die Stelle der Verschiebung tritt bei der Beschreibung ihrer „Deformation“ sinnvollerweise die Geschwindigkeit und in erster Näherung werden Reibungseffekte durch lineare Ausdrücke in den Geschwindigkeitsgradienten beschrieben. In der Tat folgt bei „Abschaltung“ der Reibung aus Gleichung (1.8.27): σ ij = − p δ ij . (x) (1.8.28) (x) Die skalare Materialgröße p nennt man auch den Druck, der wie man nicht anders vermuten (x) würde in alle Richtungen gleich wirkt, was man mathematisch auch an dem „Kugeltensor“ δ ij erkennt und zwar sowohl in Gleichung (1.8.27) als auch in (1.8.28). Auch der Druck ist im allgemeinen von der Dichte und der Temperatur abhängig. Weiter unten werden wir eine einfache Materialgleichung für ihn angeben und ihn so in Verbindung mit diesen, primär interessierenden Feldgrößen bringen. Den Zusammenhang (1.8.28) bezeichnet man in Verbindung mit reibungsfreien Strömungen auch gerne als den Spannungszusammenhang für ein EULERsches Fluid. Im Zusammenhang mit Gleichung (1.8.27) notieren wir nun die folgenden Transformationsgleichung für Skalare und Tensoren: ∂z k ∂z l ∂z k ∂z l σ ij= σ kl , δ ij = g kl , (x) ∂xi ∂x j ( z ) ∂xi ∂x j ∂υ ∂υ k ∂z k ∂z l = υ k ;l , ( x ) = υ k ;k , (z ) ∂x j ∂xi ∂x j (z ) ∂xk (x) i p= p , λ =λ , µ =µ. (x) (z ) (x) (z ) (x) (z ) 73 (1.8.29) Nach Einsetzen dieser Beziehungen in Gleichung (1.8.27) kann man den gemeinsamen Faktor ∂z k ∂z l herausziehen, und es entsteht das NAVIER-STOKES sche Gesetz in einer beliebigen ∂xi ∂x j Basis z in Bezug auf die Indizes k und l vollständig kovariant geschrieben: σ kl = − p g kl + λ υ r ;r g kl + µ υ k ;l + υ l ;k . (z ) (z ) (z ) (z ) (z ) (z ) ( z ) (1.8.30) 1.8.9 Übung: Das NAVIER-STOKES Gesetz alternativ geschrieben Erinnere an die Möglichkeit, mit Hilfe des Metriktensors Indizes in Tensoren hoch bzw. runter zu ziehen und unter kovariante Ableitungen zu schieben: Übung 1.6.13. Erläutere damit die Gültigkeit der folgenden Alternativformen zu Gleichung (1.8.30): σ kl = − p g kl + λ υ r;r g kl + µ υ k ;r g rl + υ l ;r g rk , (z ) ( z ) ( z) (z ) (z ) ( z ) ( z) σ k (z ) l σ l (z ) k = − p δ lk + λ υ r ;r δ lk + µ υ k ;l + υ l;r g rk , ( z )( z ) (z ) (z ) (z ) (z ) (1.8.31) = − p δ kl + λ υ r;r δ kl + µ υ k ;r g rl + υ l ;k . ( z )( z ) (z ) (z ) (z ) (z ) 1.8.10 Übung: NAVIER-S TOKES Gesetz und Verzerrungstensor in physikalischen Zylinder- und Kugelkoordinaten Begründe mit Hilfe der Ergebnisse aus den Übungen 1.8.6/7 die Gültigkeit der folgenden Darstellungen für das NAVIER-STOKES Gesetz: σ < ij >= λ D < ll > δ < ij > + 2 µ D < ij > , i, j ∈ (r , ϑ , z ) , (1.8.32) wobei i , j ∈ (r ,ϑ , z ) für Zylinderkoordinaten und i , j ∈ (r , ϕ,ϑ ) zu setzen ist und der symmetrisierte Geschwindigkeitsgradient wie folgt definiert wurde: 1 Dkl = υ k ;l + υ l;k . (z ) 2 (z ) (1.8.33) Erläutere ferner anhand der Ergebnisse aus den Übungen 1.8.6/7, warum für Zylinder- bzw. für Kugelkoordinaten die folgenden Darstellungen für den symmetrisierten Geschwindigkeitsgradienten gelten müssen: 74 ∂υ < r > 1 ∂υ < ϑ > υ < r > ∂υ < z > , D < ϑϑ > = + , D < zz > = , ∂r r ∂ϑ r ∂z 1 1 ∂υ < r > ∂υ < ϑ > υ < ϑ > (1.8.34) D < rϑ > = + − , 2 r ∂ϑ ∂r r 1 ∂υ < z > ∂υ < r > 1 ∂υ < ϑ > 1 ∂υ < z > D < rz > = + + , D < ϑz > = , 2 ∂r ∂z 2 ∂r r ∂ϑ D < rr > = bzw.: ∂υ < r > 1 ∂υ < ϑ > υ < r > , D < ϑϑ > = + , ∂r r ∂ϑ r 1 ∂υ < ϕ > υ < r > cot (ϑ ) D < ϕϕ > = + +υ < ϑ > , r sin (ϑ ) ∂ϕ r r D < rr > = 1 1 ∂υ < r > υ < ϕ > ∂υ < ϑ > − + , 2 r sin (ϑ ) ∂ϕ r ∂r 1 1 ∂υ < r > υ < ϑ > ∂υ < ϑ > D < rϑ > = − + , 2 r ∂ϑ r ∂r 1 1 ∂υ < ϕ > cot (ϑ ) 1 ∂υ < ϑ > D < ϕϑ > = −υ < ϕ > + . 2 r ∂ϑ r r sin (ϑ ) ∂ϕ D < rϕ > = (1.8.35) Notiere schließlich für beide Fälle die physikalischen Komponenten der Geschwindigkeit ausgedrückt durch die Zeitableitungen der jeweiligen Koordinaten z i . 1.8.11 Das ideale Gasgesetz Der in den Gleichungen (1.8.27/28) auftretende Druck ist i.a. eine nicht analytische Funktion der Elementarfelder Dichte ρ und Temperatur T (einzusetzen in Einheiten von Kelvin) sowie eventuell deren Ableitungen nach Ort und Zeit. Es gibt jedoch ein „Material“, für welches sich ein analytischer Zusammenhang angeben lässt, nämlich das ideale Gas. Hierfür gilt (in jedem Koordinatensystem): p=ρ R T. M (1.8.36) Dabei bezeichnen R = 8,314 kJ (kgK ) die sogenannte ideale Gaskonstante und M das der Periodentafel der Element zu entnehmende (dimensionslose) Molekulargewicht des betreffenden Stoffes also etwa 44 für CO2 . Gleichung (1.8.36) mag dem ungeübten Auge auf den ersten Blick etwas verfremdet erscheinen, kennt man aus der Schulchemie doch zumeist den Zusammenhang: ~ pV = ν RT . (1.8.37) 75 Dabei ist die Anzahl der Mole ν an Substanz in einer Kammer mit Volumen V eingeführt worden. Multipliziert man ν mit der sogenannten Avogadroschen Zahl N Avo = 6,021⋅ 1023 , so erhält man die Gesamtzahl an Molekeln in der Kammer. Die Gesamtmasse der Substanz (in kg) zu errechnen gelingt, wenn man nun noch die Masse eines Zwölftels des Kohlenstoffatoms kennt. Diese beträgt ungefähr µ = 1,66 ⋅10 −27 kg . Also gilt: m = ν N Avoµ M , (1.8.38) wobei vorausgesetzt wurde, dass das Molekulargewicht im Periodensystem der Elemente auf der Basis eines Vielfachen des Zwölftels eines Kohlenstoffatoms angegeben wird. Indem wir nun die Anzahl der Mole mit dieser Gleichung in (1.8.37) ersetzen, entsteht: p= ~ m R T. V NAvoµ M (1.8.39) Beachten wir nun noch, dass für homogen gefüllte Behälter gilt, dass: ρ= m V (1.8.40) und dass ferner: N Avoµ = 10− 3 kg , (1.8.41) so folgt aus Gleichung (1.8.39) die Beziehung (1.8.37), wenn man nur setzt: ~ J R = R ⋅10 −3 kg = 8,314 , K (1.8.42) und wie man die Gaskonstante aus der Schule auch kennt. Gleichung (1.8.36) ist in dem Sinne allgemeiner als die Beziehung (1.8.37), dass sie lokal gilt, also auch für einen Behälter, in dem die Verhältnisse nicht homogen sind, es also einen Dichte- und Temperaturgradienten geben mag. Die ideale Gasgleichung hat auch nichts mit dem Phänomen der Reibung zu schaffen, denn diese geht an einer ganz anderen Stelle ein, wie Gleichung (1.8.27) lehrt. Sie ist also u.a. einsetzbar bei der Beschreibung reibungsbehafteter Gasströmungen, jedenfalls in erster Näherung als analytische Materialbeziehung für den Druck. 76 1.8.12 Die innere Energie des ide alen Gases und des DULONG-PETITschen Festkörpers Wir wenden uns nun der Materialgleichung für das Skalarfeld der inneren Energie zu. Wie der Druck ist sie i.a. eine nichtanalytische Funktion der Dichte und der Temperatur. Für ein ideales Gas jedoch kann man einen analytischen Zusammenhang angeben und darf schreiben: u=z R T + u0 . M (1.8.43) Darin ist u0 eine Konstante, die jedoch für unsere Zwecke irrelevant ist, da sie in die Bilanzgleichungen eingesetzt bei Differentiation nach Ort und Zeit rausfällt. Ferner ist z eine Zahl und zwar gleich 3/2, 5/2 bzw. 3 je nachdem, ob es sich um ein ein-, zwei- oder mehratomiges Gas handelt. Für praktische Anwendungen wie beispielsweise die Auslegung von Turbinen, in denen man während des Betriebes ein Gemisch aus Luft (Sauerstoff) und Treibstoff verbrennt, ist Gleichung (1.8.43) unzureichend und man „verbessert“ diese Gleichung, indem man schreibt: u = cV (T ) T + u0 . (1.8.44) Es bezeichnet cV (T ) die nunmehr temperaturabhängige spezifische Wärme bei konstantem Volumen (typischerweise in kJ (kgK ) ), die für viele (Elementar-) Gase in tabellierter Form als Funktion der Temperatur vorliegt und je nach Temperatur mehr oder weniger von dem konstanten Wert z R M des idealen Gases abweicht. Für ideale Festkörper gilt eine zu (1.8.43) analoge Gleichung. Man darf sagen, bei einem Gas 1 R dass pro molekularem Freiheitsgrad die innere Energie um T zunimmt. Ist das Gas 2M einatomig, so gibt es drei translative Freiheitsgrade, also ist z = 3 2 . Handelt es sich um zweiatomige Gasmolekeln, so treten noch zwei rotative Freiheitsgrade jeweils senkrecht zur Bindungsachse hinzu. Also ist dann z = 5 2 . Handelt es sich schließlich um Molekeln mit drei und mehr Atomen, so gibt es drei Freiheitsgrade der Translation und auch drei Freiheitsgrade der Rotation, und folglich ist z = 6 2 = 3 . Dieses trifft mit etwas Phantasie auch für einen Festkörper zu und folglich gilt in idealer Weise: u=3 R T + u0 . M (1.8.45) Das ist die Regel von DULONG-PETIT, die man meist so schreibt: u = cV T + u0 mit cV = 3 R = const. T . M (1.8.46) 77 Man begründet sie auch etwas eloquenter, indem man sich den Festkörper als ein Ensemble von mit Federn verbundenen Atomen vorstellt. Der Festkörper hat dann drei Freiheitsgrade der Translation und (wegen der 3D Federkonstruktion) auch drei Freiheitsgrade an potentieller Energie, was den Faktor 3 in Gleichung (1.8.45) erklärt. Für viele Anwendungen ist eine von der Temperatur unabhängige spezifische Wärme bei konstantem Volumen jedoch nicht genau genug. Man hilft sich dann wieder mit Gleichung (1.8.44), wobei für viele (Element) Festkörper cV (T ) tabelliert ist. 1.8.13 Übung: Spezifische Wärme eines Festkörpers Betrachte einen Eisenklotz der Masse mFe der Ausgangstemperatur TFe . Dieser wird in ein Wasserbad (Masse m H 2 O , Ausgangstemperatur TH 2 O .) geworfen. Die beiden Substanzen tauschen intern Wärme aus und die Temperatur des Eisens sinkt, bzw. die Temperatur des Wassers steigt auf einen gemeinsamen Wert Tend . Wie groß ist diese Temperatur ? Starte zur Lösung mit dem globalen Energiesatz. Wende ihn auf ein geeignetes materielles Volumen an. Setze voraus, dass ein Wärmeaustausch nur zwischen dem Wasser und dem Eisenklotz erfolgt und der Wasserbehälter ansonsten keine Wärme durchlässt. Integriere nun die Energiebilanz über die Zeit vom Anfang bis zum Ende des internen Wärmeaustausches, verwende für die innere Energie des Wassers die Gleichung (1.8.39) mit der konstanten spezifischen Wärmekapazität cυ , H 2 O = 4,18 ⋅10 3 J (kgK ) bei konstantem Volumen. Verwende ferner für die innere Energie des Eisens die Regel von DULONG-PETIT gemäß der Gleichung (1.8.41). Hätte man zur Lösung auch von der globalen Bilanz der inneren Energie also vom 1. Hauptsatz ausgehen können? 1.8.14 Übung: Versagen der Halterung zwischen zwei Gaskammern Betrachte die in der Abbildung 1.8.2 dargestellte Situation. Das Gas in der rechten Kammer (Volumen V2st , Masse m2 , Molekulargewicht M 2 ) steht eingangs unter einem viel höheren Druck p2St , als das Gas in der linken Kammer (Volumen V1st , Masse m1 , Molekulargewicht M 1 , Druck p1St ,). Beide Gase haben die gleiche Temperatur T st . Nach Versagen der Sicherungshalterung beginnt sich der beide Kammern trennende Kolben zu bewegen. Die Gase werden turbulent verwirbelt und zwar solange bis aufgrund von Reibung die kinetische Energie vernichtet wurde und wieder stationär, homogene Verhältnisse vorliegen. Nimm an, dass der Kolben wärmeleitend ist, die äußeren Kammerwände jedoch adiabat (= wärmeundurchlässig) versiegelt sind, so dass die Temperatur am Ende des Prozesses in beiden Kammern wie- 78 der gleich ist: T1end = T2end = T end . Beide Gase sollen ferner einatomig und (im Ruhezustand) mit der idealen Gasgleichung beschreibbar sein. Zeige, dass gilt: m1 R M 1 + m 2 R M 2 st T , V tot m1 M 1 m2 M 2 = V tot , V2end = V tot , V tot = V1st + V2st . m1 M1 + m2 M 2 m1 M1 + m2 M 2 T end = T st , p1end = p2end = p end = V1end (1.8.47) V V2(t) V1(t) p1<<p2 p2 Abb. 1.8.3: Zwei Gaskammern. 1.8.15 Übung: Die Adiabatengleichung Erinnere an die Bilanz für die innere Energie in regulären Punkten nach Gleichung (1.7.41), allerdings geschrieben mit materieller Zeitableitung für kartesische Koordinaten (Begründung!): ρ du ∂q ∂υ = − i + σ ji i + ρr . dt ∂ xi ∂ xj (1.8.48) Unter welchen Annahmen folgt hieraus die sog. Adiabatengleichung in der Form: pυ κ = const. t , κ = z +1 ? z (1.8.49) Wie ergeben sich folgende Alternativversionen zu dieser Gleichung: υ κ −1T = const. t , pT − κ κ −1 = const. t ? (1.8.50) 79 1.8.16 Übung: Grenzen der Anwendbarkeit der Adiabatengleichung Betrachte einen adiabaten zylindrischen Behälter mit vorgegebener Querschnittsfläche A , in dem sich ein reibungsfrei beweglicher, völlig dicht schließender Kolben der Masse mK befinR det, und der darunter ein ideales Gas der Masse mG , spezifische Wärme cυG = z enthält. M Der Kolben wird zunächst auf der Höhe z A festgehalten, die Temperatur des Gases und des Kolbens beträgt eingangs T A , der mit Hilfe der idealen Gasgleichung aus den bisherigen Daten berechenbare Druck wird mit p A bezeichnet. Dann wird der Kolben losgelassen, er sinkt herab, induziert Strömungsprozesse im Gas, beginnt eine Schwingung und kommt schließlich durch Reibungswirkung im Gas auf der Höhe z E zur Ruhe. Begründe zunächst anschaulich, ob sich die Luft bei diesem Prozeß erwärmt oder abkühlt und berechne dann die Höhe z E (die spezifische Wärme des Kolbens cυK soll als Konstante berücksichtigt werden) sowie die Endtemperatur TE des Gases und zwar zunächst unter Umgehung der Adiabatengleichung (1.8.49) (warum?). Verwende dabei ein geeignetes Kontrollvolumen in Verbindung mit dem globalen Energiesatz sowie geeigneter Materialgleichungen und zeige, dass gilt: m m cK A mK + G g + zAp 1 + K υG 2 mG cυ z . zE = A K mK cυ mG m + z + 1 + z g G K m c 2 G υ (1.8.51) Verwende bei der Herleitung die folgende Hilfsformel für den Schwerpunkt (anzuwenden auf das Gas), die es ebenfalls zu beweisen gilt: d xiS 1 = ∫∫∫ ρυ i dV . dt m V (t ) (1.8.52) Setze nun die Adiabatengleichung an und generiere folgende Alternativlösung: 1 Ap A κ z A . z E = mK g (1.8.53) Gebe dem Praktiker eine Empfehlung, unter welchen Umständen und in welchem Parameterbereich diese verwendet werden kann. 80 1.8.17 Die FOURIERsche Wärmegleichung Bereits FOURIER hat festgestellt, dass der Wärmefluss dem Temperaturgradienten entgegen gerichtet ist. Wir schreiben in einem kartesischen System: q i= −κ (x) (x) ∂T (x ) ∂xi . (1.8.54) Darin bezeichnet die Größe κ eine skalare, eventuell von den Skalaren Dichte und Temperatur abhängige Materialfunktion, auch bekannt als die Wärmeleitfähigkeit. Um diese Gleichung in ein beliebiges z -System umzuschreiben, multiplizieren wir sie mit ∂xi ∂z k und beachten, dass: q k= (z ) ∂xi q i , T =T , κ =κ, (z ) (x) (z ) (x) ∂z k ( x ) (1.8.55) so folgt mit der Kettenregel die folgende kovariant geschriebene Beziehung: (z ) ∂T (z ) . ( z ) ∂z k q k= − κ (1.8.56) Möchte man eine entsprechende, kontravariante Gleichung generieren, so ist mit der Metrik durchzumultiplizieren wie folgt: q r = − κ g rk (z ) (z ) ∂T (z ) ∂z k ∂z r ∂z k ∂ T ∂z r ∂ T (z ) (z ) = − κ . ( z ) ∂x ∂x ∂z k ( z ) ∂x ∂x j j j j = −κ (1.8.57) 1.8.18 Übung: Wärmeleitung durch Wand Eine Wand der Gesamtfläche A und der Dicke d trennt ein Zimmer der Temperatur TZ von kalter Außenluft TL . Zeige, dass für den Temperaturverlauf innerhalb der Wand gilt: T ( x1 ) = (TZ − TL ) x1 + TL . d (1.8.58) Starte beim Beweis mit dem 1. Hauptsatz der Thermodynamik und argumentiere zunächst, dass im vorliegenden Fall gelten muß: 81 ∂q (x ) ∂xi i = 0. (1.8.59) Begründe und verwende nun den Ansatz: q i = q 1( x1 ) , 0 , 0 . (x) (x ) (1.8.60) in Kombination mit der FOURIERschen Wärmeleitungsgleichung (1.8.51) zur Erstellung einer Differentialgleichung für T ( x1 ) . Integriere und passe die Lösung geeignet an. Berechne nun noch q 1( x1 ) . Zeichne q in ein Schemabild der Situation (Richtung !). Wie groß ist der ge(x) samte Wärmeverlust des Zimmers pro Zeiteinheit ? 1.8.19 Übung: Temperaturverteilung um einen Hitzdraht Betrachte einen sehr langen, geraden, stromführenden Draht, in dem durch Dissipation JOULEsche Wärme entsteht. Der Draht gibt dadurch über seine Oberfläche bei r = r0 den Wärmestrom q0 an die umgebende Luft weiter. Zur Ableitung der Wärme und zur Aufrechterhaltung stationärer Verhältnisse ist im Abstand r = ra ein Metallzylinder axialsymmetrisch um den Hitzdraht gestellt, der auf konstanter Temperatur Ta gehalten wird. Nimm stationäre Verhältnisse an und berechne mit Hilfe der lokalen Bilanz für die innere Energie in Zylinderkoordinaten und einem geeigneten semiinversen Ansatz den Wärmeflußbektor (erinnere in diesem Zusammenhang auch die Gleichungen für die Divergenz eines Vektorfeldes, (1.6.18) und (1.7.6)). Schreibe dann das F OURIERsche Gesetz nach Gleichung (1.8.56) in physikalische Zylinderkoordinaten um und berechne die Temperaturverteilung um den Draht im Bereich r0 ≤ r ≤ ra . Wie verhält sich die Lösung für ra → ∞ und wie ist das Ergebnis zu interpretieren ? Wie sieht die Lösung aus, wenn man anstelle des Wärmestromes an der Hitzdrahtoberfläche eine Oberflächentemperatur T0 vorgibt ? Was haben beide Probleme miteinander zu schaffen, wie lassen sie sich ineinander überführen ? 82