Zuverlässigkeit von Antikörpernachweisen
Werbung

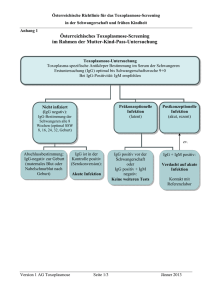
Zuverlässigkeit von Antikörpernachweisen Jeder der sich näher mit der Zuverlässigkeit der serologischen Antikörpertests beschäftigt stößt schnell auf die Problematik mit unterschiedlichen, widersprüchlichen und zum Teil sogar eindeutig falschen Angaben. Hier einmal eine kurze Darstellung wie sich die „Experten“ selbst widersprechen. Das RKI schreibt z.B. im Epidemiologisches Bulletin 22/98 Empfehlungen zur Diagnostik-Therapie der Lyme-Borreliose folgendes: Zu erwartende positive Ergebnisse beim Antikörpernachweis: Stadium; seropositiv IgM versus IgG II (lokalisierte Infektion); 20-50% vorwiegend IgM-Antikörper bei kurzer Krankheitsdauer III (disseminierte Infektion); 70-90% vorwiegend IgG-Antikörper bei langer Krankheitsdauer IIII (chronische Infektion); 99-100% in der Regel nur IgG Zum einfacheren Verständnis beschränke ich mich bei der weiteren Betrachtung zuerst nur auf das Stadium III, da in den meisten Veröffentlichungen geschrieben wird, dass ein negatives Ergebnis eine Spätborreliose praktisch ausschließt. Die Problematik dürfte aber analog für die Stadien I-II gleichermaßen gelten. Das RKI gibt also als erwartende positive Ergebnisse (Sensitivität) für Stadium III 99-100% an und schreibt weiter: „Ein negativer serologischer Befund schließt das Vorliegen einer Spätmanifestation weitgehend aus.“ Die utopisch hohe Zahl von 99-100% positiven Testergebnissen ist bei den bekannten Problemen der Serologie schon sehr verwunderlich zumal das RKI darin ebenfalls schreibt: “Ein großes Problem der serologischen Diagnostik ist in der bislang fehlenden Standardisierung der Testverfahren zu sehen. Als Hauptgründe für die häufig differenten Testergebnisse sind vor allem anzuführen: unterschiedliche serologische Techniken, unterschiedliche Borrelienstämme als Testantigen, unterschiedliche Vorbehandlung der Seren und unterschiedliche Cut-off Definitionen. Insbesondere der Immunoblot wird dem hohen Anspruch als Bestätigungstest in der Praxis vielfach nicht gerecht. Die kommerziell erhältlichen Testkits erlauben selten die zuverlässige Identifikation spezifischer Banden. Es fehlen auch allgemein- verbindliche Auswertekriterien.“ Wie können also zu 99-100% positive Ergebnisse zustande kommen, wenn es „häufig“ differente Testergebnisse gibt und die Tests nur „selten“ die zuverlässige Identifikation spezifischer Banden erlauben. Nach deren eigenen Aussage dürfen diese doch nur zu maximal 1% falsch negativ sein.? Schauen wir einmal weiter in den offiziellen Qualitätsrichtlinen zur mikrobiologischen Diagnostik der Lyme-Borreliose MIQ 12 2000 welche unter Federführung des nationalen Referenzzentrums für Borrelien NRZ von Frau Prof. Wilske et. al. herausgegeben wurde. Dort steht in Tabelle 7. Sensitivität von Antikörpernachweismethoden zur Diagnose der Lyme-Borreliose folgendes: „Stadium III, Sensitivität 90-100%, in der Regel nur IgG“. Auch diese Zahl verwundert sehr, da sich das NRZ mit Fr. Wilske in einer neuen Veröffentlichung 2005 damit rühmt die Sensitivität „exzellent“ durch einen neuen rekombinanten Immunoblot mit VlsE and DbpA im IgG von 70.6% (Westernblot) auf 84.7% (Lineblot) und im IgM von 40.0% auf 73.8% verbessert zu haben. Wie kann das sein, dass in den MIQ in 2000 eine Sensitivität von 90-100% angegeben wurde, da nach eigener Darstellung die Sensitivität damals bestenfalls 70.6% im IgG und 40% im IgM betrug und dieses bei den hervorragenden Tests des NRZ ? Wie sieht es erst dann bei den handelsüblichen einfacheren billigen Tests aus ? 1 J Clin Microbiol. 2005 Aug;43(8):3602-9. Improvement of Lyme borreliosis serodiagnosis by a newly developed recombinant immunoglobulin G (IgG) and IgM line immunoblot assay and addition of VlsE and DbpA homologues. Goettner G, Schulte-Spechtel U, Hillermann R, Liegl G, Wilske B, Fingerle V. Max von Pettenkofer-Institut fur Hygiene und Medizinische Mikrobiologie, Ludwig-Maximilians-Universitat Munchen, Pettenkoferstr. 9a, D-80336 Munich, Germany. We developed and evaluated a recombinant Borrelia line immunoblot assay based on 18 homologues of seven different antigens, i.e., p100, p58, p41i, BmpA, VlsE, OspC, and DbpA. Each recombinant antigen can be detected separately and is distinct even from homologues with identical molecular weights. This blot was compared to the recently described recombinant Borrelia Western immunoblot assay (U. Schulte-Spechtel, G. Lehnert, G. Liegl, V. Fingerle, C. Heimerl, B. J. Johnson, and B. Wilske, J. Clin. Microbiol. 41:1299-1303, 2003). To verify sensitivity and specificity, both blots were evaluated for reactivity with Borrelia-specific immunoglobulin G (IgG) and IgM antibodies with 85 sera from patients with different manifestations of Lyme borreliosis and 110 controls. According to European interpretation criteria for Borrelia Western blots, which define a serum as positive when it recognizes at least two bands, sensitivity increased significantly from 70.6% (Western blot) to 84.7% (line blot) for IgG (P = 0.042) and from 40.0% (Western blot) to 73.8% (line blot) for IgM (P < 0.005). The increased sensitivity for IgG detection is due to the new line blot technique, whereas the improvement in detection of IgM is mainly achieved through incorporation of the additional antigens. Notably, the recombinant VlsE of Borrelia garinii strain PBi displayed the highest sensitivity of all antigens tested for IgG detection and is also one of the most useful antigens for IgM. Due to its excellent sensitivity and specificity combined with ease of evaluation, this line immunoblot assay offers a useful improvement in serodiagnosis of Lyme borreliosis. PMID: 16081885 Hier ein aktuelles Beispiel zur Zuverlässigkeit im Vergleich von fünf verschiedenen Tests.: Clin Microbiol Infect. 2006 Jul;12(7):648-55. Comparison of five different immunoassays for the detection of Borrelia burgdorferi IgM and IgG antibodies. Smismans A, Goossens VJ, Nulens E, Bruggeman CA. Department of Medical Microbiology, University Hospital Maastricht, Maastricht, The Netherlands. The performances of five commercially available enzyme immunoassays were compared for the detection of Borrelia burgdorferi IgM and IgG antibodies. Sensitivity was assessed with European serum samples collected from 45 patients with clinically defined Lyme disease in conjunction with a positive immunoblot (n = 44) or other serological test (n = 1). Sensitivities for the detection of IgM and IgG with each test were: Dako IgM 64%; Dako IgG 53%; Serion IgM 89%; and Serion IgG 88%. The Immunetics assay makes no distinction between IgM and IgG antibodies and had a sensitivity of 91%. Specificity was calculated by testing a control group comprising 40 patients with acute Epstein-Barr virus infection, cytomegalovirus infection, syphilis or rheumatoid factor positivity. The specificities achieved for each test were: Dako IgM 78%; Dako IgG 100%; Serion IgM 52%; Serion IgG 92%; and Immunetics 92%. The discriminatory power between control and patient samples appeared highest for the Immunetics assay. Between-run variation was comparable for the five tests and did not exceed 13%. When the Immunetics assay was used as an initial screening test, with low-titre positive results confirmed by an immunoblot, a sensitivity of 91% and a specificity of 100% were achieved. To attain maximal sensitivity, the Serion IgM and IgG tests were also performed on samples with negative Immunetics results. All positive Serion IgM and IgG results were also confirmed by immunoblot. In conclusion, the Immunetics assay, based on a synthetic C6 peptide, can be used reliably as an initial screening test for the serodiagnosis of Lyme disease. PMID: 16774561 Grobe Übersetzung: Vergleich von fünf verschiedenen Immunoassays zur Ermittlung von Borrelia burgdorferi IgM and IgG Antikörpern. Die Leistungen von fünf handelsüblichen Enzym Immunoassays (ELISA) wurden zum Nachweis von Borrelia burgdorferi IgM und von IgG Antikörpern verglichen. Die Sensitivität wurde mit europäischen Serumproben bewertet, gesammelt von 45 Patienten mit klinisch definierter Lyme Krankheit in Verbindung mit einem positiven Immunoblot (n = 44) oder anderer serologischem Test (n = 1). Die Sensitivität zum Nachweis von IgM und von IgG mit jedem Test war: Dako IgM 64%; Dako IgG 53%; Serion IgM 89%; und Serion IgG 88%. Der Immunetics Test trifft keine Unterscheidung zwischen IgM und IgG Antikörpern und hatte eine Sensitivität von 91%. Die Spezifität wurde durch die Untersuchung einer Kontrollgruppe von 40 Patienten mit akuter Epstein-Barr Virusinfektion, Cytomegalovirusinfektion, Syphilis oder positivem Rheumafaktor ermittelt. Die erzielte Spezifität für jeden Test war: Dako IgM 78%; Dako IgG 100%; Serion IgM 52%; Serion IgG 92%; und Immunetics 92%. Die charakteristische Leistung zwischen Kontroll- und Patientenproben zeigte sich bei den Immunetics Test am höchsten. Zwischenlauf Variationen waren für die fünf Prüfungen vergleichbar und überstiegen nicht 13%. Wenn der Immunetics Test als initialer Suchtest mit niedrigem positiven Titer bestätigt durch einen Immunoblot verwendet wurde, wurde eine Sensitivität von 91% und eine Spezifität von 100% erzielt. Zur Erzielung maximaler Sensitivität, die Serion IgM und IgG Tests wurden auch an Proben mit negativen Immunetics Ergebnissen durchgeführt. Alle positiven Serion IgM und IgG Ergebnissen wurden auch durch den Immunoblot bestätigt. In der Zusammenfassung kann der Immunetics Test, basierend auf einem synthetischen Peptid C6, als initialer Suchtest zuverlässig für die Serodiagnostik der Lyme-Krankheit verwendet werden. 2 Dieses Ergebnis zeigt sehr deutlich wie abhängig die Sicherheit der Diagnostik von dem jeweiligen Test / Labor ist. So werden durch die erschreckend schlechte Sensitivität beim Dako-Test 47% der Infizierten im IgG bzw. 36% im IgM durch falsch negative Ergebnisse überhaupt nicht erkannt und vermutlich als „gesund“ einem ungewissem chronischem Krankheitsschicksal entgegen sehen. Ebenso zeigt diese Studie wieder einmal wie unsinnig und gesundheitsgefährdend die offiziell empfohlene Stufendiagnostik ist. Bei der nach einem (all zu oft falsch) negativen Ergebnis des ELISA Suchtests eine mögliche Borreliose abgehakt ist und nur bei einem positiven Ergebnis ein wesentlich spezifischerer Westernblot (Immunoblot) zur Bestätigung durchgeführt werden soll. In der Selbsthilfe sind unzählige Fälle bekannt bei denen trotz negativen Suchtest ein anschließender Immunoblot (Westernblot) eindeutig positive Ergebnisse zeigte. Hier noch ein anderes Beispiel: Limitation of serological testing for Lyme borreliosis: evaluation of ELISA and western blot in comparison with PCR and culture methods. Wien Klin Wochenschr 2002 Jul 31;114(13-14):601-5 (ISSN: 0043-5325) Tylewska-Wierzbanowska S; Chmielewski T Department of Bacteriology, National Institute of Hygiene, Warsaw, Poland. [email protected]. The aim of the study was to evaluate a one-step procedure using an ELISA test of high specificity and a two-step procedure using immunoblot as a confirmation test, and to compare the results of serological testing with detection of bacterial DNA and living spirochetes. Sera, synovial (SF) and cerebro-spinal fluids (CSF) were obtained from 90 patients with clinical symptoms of Lyme borreliosis. Serum samples were tested with recombinant ELISA and Western blot assay. Citrated blood, cerebrospinal and synovial fluids samples were cultured in cell line and tested by PCR to detect spirochetes. No correlation was found between levels of specific B. burgdorferi antibodies detected with a recombinant antigen ELISA and the number of protein fractions developed with these antibodies by immunoblot. Moreover, Lyme borreliosis patients who have live spirochetes in body fluids have low or negative levels of borrelial antibodies in their sera. This indicates that an efficient diagnosis of Lyme borreliosis has to be based on a combination of various techniques such as serology, PCR and culture, not solely on serology. Grobe Übersetzung: (ohne Gewähr) Grenzen der serologischen Tests für Lyme-Borreliose: Auswertung von ELISA und Western Blot im Vergleich mit PCR und Kultivierungs-Methoden. Wien Klin Wochenschr 2002 Jul 31;114(13-14):601-5 (ISSN: 0043-5325) Tylewska-Wierzbanowska S; Chmielewski T Department of Bacteriology, National Institute of Hygiene, Warsaw, Poland. [email protected]. Das Ziel der Studie war, die Auswertung von einstufigen Verfahren mittels hochspezifischen ELISA Tests und von zweistufigen Verfahren mittels Immunoblot als Bestätigungstest und der Vergleich dieser Ergebnisse der serologischen Tests mit dem Nachweis von Bakterien DNA und lebenden Spirochäten. Serum, Synovial- (SF) und Cerebrospinalflüssigkeit (CSF)(=Liquor) wurde von 90 Patienten mit klinischen Symptomen einer Lyme-Borreliose erhalten. Die Serumproben wurden mit recombinanten ELISA und Western Blot Tests getestet. Citratblut, Liquor und Synovialflüssigkeitsproben wurden in Zellinien kultiviert und mittels PCR zur Ermittlung von Spirochäten getestet. Es wurde kein Zusammenhang gefunden zwischen der Höhe der spezifischen B. burgdorferi Antikörper, ermittelt mit recombinanten Antigen ELISA und der Anzahl von Proteinbestandteilen entdeckt mit diesen Antikörpern durch den Immunoblot. Außerdem, Lyme-Borreliose Patienten welche lebende Spirochäten in Körperflüssigkeiten hatten, hatten niedrige oder negative Borrelienantikörper-Titer in ihrem Serum. Das zeigt an, dass eine effiziente Diagnose der Lyme Borreliose auf eine Kombination von verschieden Techniken wie Serologie, PCR und Kultur und nicht ausschließlich auf die Serologie gestützt werden soll. 3 Oder ein weiteres interessantes Beispiel: Evaluation of fifteen commercially available serological tests for diagnosis of Lyme borreliosis. Eur J Clin Microbiol Infect Dis 1999 Aug;18(8):551-60 (ISSN: 0934-9723) Goossens HA; van den Bogaard AE; Nohlmans MK Department of Medical Microbiology, University of Maastricht, The Netherlands. The performance of 11 commercially available enzyme immunoassays (EIA) and four Western blot (WB) tests for the detection of IgM and IgG antibodies against Borrelia burgdorferi were compared. A total of 229 serum specimens were used: 26 from patients with early Lyme borreliosis, 13 from patients with late Lyme borreliosis, 62 from healthy controls and 128 from patients with disorders clinically mimicking Lyme borreliosis and/or known to cause cross-reactivity in Lyme borreliosis serological tests (patient control group). In specimens from patients with early Lyme borreliosis, the sensitivity of the individual tests ranged from 35 to 81% for detection of IgM. In late Lyme borreliosis, sensitivity of the tests ranged from 46 to 92%. In healthy controls the specificity of the tests ranged from 89 to 100% and from 82 to 97% for IgM and IgG tests, respectively. In the patient control group, specificity of the tests ranged from 75 to 90% for IgM and from 84 to 100% for IgG tests. The Behring (Germany) and Genzyme Virotech (Germany) IgM EIA tests showed the best performance in detecting early Lyme borreliosis. For the detection of late Lyme borreliosis, the Dako (Denmark) IgG test was the best despite its low sensitivity. The maximum sensitivity of Western blotting for detecting IgM in patients with early Lyme borreliosis and IgG in patients with late Lyme borreliosis was 50 and 46%, respectively. The use of an EIA-WB two-test protocol improved the specificity and positive predictive values of the EIA results but caused a significant loss in sensitivity. Patients with Epstein-Barr virus or cytomegalovirus infection who had a positive reaction in the IgM EIA could not be discriminated from patients with early Lyme borreliosis with the help of Western blotting. Hence, positive and negative predictive values in combination with sensitivity and specificity values indicated that the exclusion of these infections was more relevant than the confirmation of a positive IgM EIA with Western blot. Übersetzung ohne Gewähr. Auswertung von fünfzehn im Handel erhältlichen serologischen Tests zur Diagnose der Lyme-Borreliose. Eur J Clin Microbiol Infect Dis 1999 Aug;18(8):551-60 (ISSN: 0934-9723) Goossens HA; van den Bogaard AE; Nohlmans MK Department of Medical Microbiology, University of Maastricht, The Netherlands Die Leistung von 11 im Handel erhältlichen Enzymimmunoassays (EIA) und vier Westernblot (WB) zur Ermittlung von IgM und IgG Antikörper gegen burgdorferi Borrelia wurden verglichen. Eine Gesamtmenge von 229 Serumproben wurden verwendet: 26 von Patienten mit früher Lyme-Borreliose, 13 von Patienten mit später Lyme-Borreliose, 62 von gesunden Kontrollpersonen und 128 von den Patienten mit Beschwerden einer klinisch nachahmender Lyme-Borreliose und/oder bekannt eine Kreuz-Reaktivität in den serologischen Tests der Lyme-Borreliose zu verursachen (Patienten Kontrollgruppe). In den Proben von den Patienten mit frühem Lyme-Borreliose, reichte die Sensitivität der einzelnen Tests von 35 bis 81% zur Erkennung des IgM. Bei später Lyme-Borreliose reichte die Sensitivität der Tests von 46 bis 92%. Bei den gesunden Kontrollpersonen reichte die Spezifität der Tests von 89 bis 100% und von 82 bis 97% für Tests IgM beziehungsweise IgG. Bei der Patienten Kontrollgruppe reichte die Spezifität der Tests von 75 bis 90% für IgM und von 84 bis 100% für IgG Tests. Die Behring (Deutschland) und Genzyme Virotech (Deutschland) IgM EIA Tests zeigten die beste Leistung zur Erkennung der frühen Lyme-Borreliose. Für die Erkennung der späten Lyme-Borreliose, war der Dako (Dänemark) IgG Test trotz seiner niedrigen Sensitivität der beste. Die maximale Sensitivität des Westernblot zur Ermittlung von IgM bei Patienten mit früher Lyme-Borreliose und IgG bei Patienten mit später Lyme-Borreliose war 50 beziehungsweise 46%. Der Gebrauch von einem Zweitestprotokoll EIA-WB verbesserte die Spezifität und positive prädiktive Werte der EIA-Resultate aber verursachte einen bedeutenden Verlust in der Sensitivität. Patienten mit Epstein-Barr Virus oder Cytomegalovirusinfektion, die eine positive Reaktion im IgM EIA hatten, konnten nicht von den Patienten mit frühem Lyme-Borreliose mit Hilfe des Westernblot unterschieden werden. Folglich zeigten positive und negative prädiktive Werte im Verbindung mit Sensitivitäts- und Spezifitätswerten an, dass der Ausschluss dieser Infektion relevanter als die Bestätigung von einem positiven IgM EIA mit Westernblot war. Noch schwieriger wird es im Stadium I, hier ist die serologische Trefferquote teilweise katastrophal PRÄVALENZ UND INZIDENZ DER LYME-BORRELIOSE IN SÜD- UND OSTBAYERN (Abteilung für Infektions- und Tropenmedizin, Max-von-Pettenkofer Institut für Mikrobiologie, Universität München) (B. Reimer, A. Marschang, V. Fingerle, B. Wilske, F. v. Sonnenburg) Auszug: "Im Zeitraum Juni 1996 bis November 1998 wurden durch die niedergelassenen Ärzte im Studiengebiet 118 Probanden mit Verdacht auf eine Lyme-Erkrankung gemeldet. Sie zeigten überwiegend Hauterscheinungen, die als Erythema migrans gedeutet wurden. Die Infektion konnte nur bei zwei dieser Probanden auch serologisch als Serokonversion nachgewiesen werden. Das Einverständnis der Probanden zu einer Hautbiopsie für den direkten Erregernachweis war lediglich in drei Fällen erhältlich. Der Borreliennachweis (Kultur und PCR) war in keinem dieser drei Fälle positiv gewesen. Bei genauer Befragung der zuständigen Ärzte waren bei ungefähr 2/3 der gemeldeten Verdachtsfälle die klinischen Kriterien der Lyme-Borreliose (Größe und Aussehen des Erythems, z.T. photographisch dokumentiert) erfüllt." 4 Demnach konnte nur bei "zwei" der 118 Probanden (1,7%) mit einem Erythema migrans die Infektion serologisch nachgewiesen werden. Auch wenn man wie angegeben annimmt, dass es sich nur bei 2/3 der Verdachtsfälle um eine klinisch nachgewiesene Lyme-Borreliose gehandelt hat, wäre die serologische Trefferquote nur 2,5% ! Überhaupt sind die Angaben zur Sensitivität mit Vorsicht zu genießen. Man muss dabei nur näher überlegen wie denn diese bestimmt wird? Man nimmt z.B. 100 Patienten mit einer „eindeutig“ nachgewiesener Borreliose und testet diese mit dem jeweiligen Test. Wenn nun bei 90 dieser Patienten der Test positiv ausfällt beträgt die Sensitivität 90% oder anders betrachtet sind 10% falsch negativ und können mit diesem Test nicht erfasst werden. Doch hierbei kommt der springende Punkt, wie wählt man eigentlich die 100 Patienten aus und wie wurde die Borreliose bei diesen nachgewiesen ? Die Experten schweigen sich zu diesen wichtigen Details meistens aus. Praktisch kann man doch bei dem diagnostischen Dilemma nur diejenigen Patienten auswählen welche durch andere Tests „eindeutig“ positiv bezüglich Borreliose sind. Alle zweifelhaften Fälle sind hierbei ungeeignet. Da jedoch dafür nur die wirklich eindeutig nachweisbaren Fälle tauglich sind, fallen wohl schon einmal bei dieser Vorauswahl alle schwieriger zu diagnostizierenden, zweifelhaften und möglicherweise sogar seronegativen Patienten aus dem Raster da bei diesen die Borreliose letztendlich nicht „eindeutig“ nachgewiesen werden kann. Da deswegen nur die wirklich „eindeutig“ nachweisbaren Fälle verwendet werden können, dürfte das Ergebnis zur Sensitivität wesentlich besser ausfallen als bei einem Patentenkollektiv inklusive den schwierig und unsicher zu diagnostizierenden Problemfällen. Aber gerade bei diesen „Problemfällen“ wären hoch sensitive und spezifische Tests erforderlich. In der Praxis zeigt sich, dass im Stadium I die Tests noch weitgehend negativ sind und deshalb auch von den Experten normal nicht empfohlen werden. Da jedoch das typische Erythem nur bei ca. 50 % auftritt fällt schon mall ein großer Teil aus diesem Grund durch das diagnostische Raster. In den fortgeschrittenen Stadien fällt ein weiterer Teil der Patienten wegen der schlechten Sensitivität der Tests heraus. Ist jedoch der Test positiv, wird dieses wiederum des öfteren einfach unkritisch als „Seronarbe“ abgetan, da die Tests nicht zwischen aktiver Infektion und Seronarbe unterscheiden können und in diesem Stadium in der Regel nur noch IgG vorhanden ist. Diejenigen Patienten die endlich eine Diagnose erhalten werden üblicherweise mit einer 2-3 wöchigen antibiotischen Standardtherapie behandelt und da nach Meinung der Experten eine serologische Verlaufkontrolle mit diesen Tests nicht möglich ist, einfach entsprechend dem Lehrbuch für geheilt erklärt. Falls dennoch typische Beschwerden vorhanden sind bzw. anschließend erneut auftreten werden diese, ebenso wie bei den durch das diagnostische Raster Gefallenen, allen anderen möglichen Ursachen zugeschrieben, im Zweifel rein psychosomatischen nur nicht einer möglichen weiterhin persistierenden Borreliose. Anstatt auf das bekannte diagnostische Dilemma der Borreliose durch völlig unzureichende Tests hinzuweisen beschränken sich die „Experten“ zum Nachteil unzähliger Patienten überwiegend nur auf ihre Forschungsergebnisse mit exzellenten Labortests. So sieht leider immer noch in weiten Bereichen die real existierende Borreliosewelt aus. Die Borreliose ist entgegen den offiziellen Verlautbarungen aufgrund der völlig unzureichenden Labortests sowie einem sehr vielfältigen, bizarren meist unspezifischen Beschwerdebild vielfach nicht so einfach zu diagnostizieren und zu therapieren sondern stellt eine sehr große Herausforderung an die ärztliche Kunst bei der auch unbedingt eine sehr sorgfältige Differentialdiagnostik erforderlich ist. © Dietmar Seifert, Juni 2006 5