Clostridium difficile @ KSA
Werbung

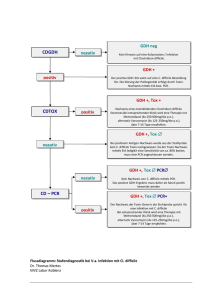
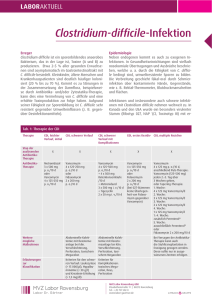
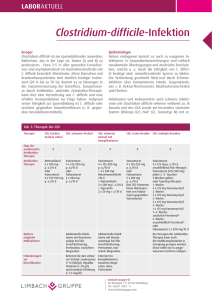
Clostridium difficile @ KSA Surveillance 2014 – 2016: Epidemiologie und Risikofaktoren Sebastian Haubitz, Nicole Bartlomé, Constanze Spelters, Christoph Fux Klinik für Infektiologie und Spitalhygiene, KSA Einleitung Clostridium difficile - Sporenbildendes grampositives anaerobes Stäbchen (Akkumulation im health care setting, relativ magensäureresistent) - Virulenzfaktor: Toxine (TcdA, TcdB, binary toxin CDT) - Zumeist nach Antibiotika (aber nicht ausschliesslich). - Ribotyp 027 (NAP1/BI Strain) mit Outbreaks und hoher Mortalität (1623x mehr Toxin) [McDonald, NEJM 2005; Loo, NEJM 2005] - Historisch: 1974 Suche nach Clindamycin-assoz. Colitis [Tedesco. Ann Int Med 1974]. 1977/78 Identifikation von C.difficile 2 Einleitung Clostridium difficile - Unterschiedliche Schweregrade: Asympt. Kolonisation < C.diff.-assoz. Diarrhoe < C.diff.-assoz. Colitis < Pseudomembranöse Colitis < toxisches Megacolon (Perforation/Schock) - Kolonisationsraten: Säuglinge (40%), Erwachsen/gesund (2-5%), Erw/Spital (20-50%), Langzeitpflege (5-51%) - Häufig Rezidive, 28% nach Metronidazol [Musher et al. CID 2005] - Neue (=teure) Therapien: Fidaxomicin, FMT, (Rifaximin), (Actoxumab, Bezlotoxumab) - Prävention: Schutz vor Sporen (Isolation, Hände waschen, Alkohol nicht effektiv gegen Sporen, Umgebungsdesinfektion), Antimicrobial Stewardship (weniger Antibiotika), (Probiotika?) 3 Risikofaktoren für Kolonisation und Infektion 4143 Patienten 6 kanadische Spitäler 15 Mt. prospektiv Loo et al. N Engl J Med 2011. Risikofaktoren für CDI-Rezidiv 5 ESCMID Guidelines. Debast et al. Clin Microbiol Infect 2014; 20 (Suppl. 2): 1–26 Strategie im KSA - Suchtests: - Klinischer Case GDH? (Sens, Spez) Toxin-PCR (Sens, Spez, teuer!) - Isolation: bei Inkontinenz Schürzenpflege, Kontaktisolation (falls mobil) - Behandlung: - Metronidazol 3x500mg/d p.o. 10 Tage, verlängert bei fortgeführten ABx - Schwere CDI: Vancomycin 4x125(-250)mg/d p.o. 10-14 Tage, ev. kombiniert - 1. Rezidiv: dito (Metronidazol) - ab 2. Rezidiv individuell gemäss Infektiologie-Konsil (Fidaxomicin, Vancomycin im Tapering-Schema) 6 Studiendesign - Einschlusskriterien: - alle Erwachsenen mit C.difficile Infektion im KSA 2014 – 2016 - Methodik: - Retrospektive Erhebung als Qualitätskontrolle bis mind. 2 Mt nach Therapie - Risikofaktoren (Antibiotika vor und während CDI-Therapie, Vor-Hosp/IPS, PPI, IBD, solide und hämatologische Neoplasien, Neutropenie <1G/L, PDN >20mg/d, Nierenfunktion, chron. Infektionen, Transplantation, DM, Albumin, CRP und Leukozytose) - CDI-Therapieverlauf (non-response < 7 Tage; Therapiedauer) - Endpunkte: alle Rezidive (<2 Monate); Tod; neue CDI (>2 Monate). 7 Baseline characteristics (198 Patienten) 8 Therapieverlauf 9 Therapieverlauf 10 Therapieverlauf 11 Rezidive und Risikofaktoren 12 20% Erstrezidivrate (36/183 Patienten) 13 17% Gesamtmortalität über die ersten 60 Tage (33/198 Patienten) 14 Diskussion und Schlussfolgerungen - Gute Therapieerfolgsrate unter zumeist Metronidazol bei Erstbehandlung (78%) auch bei erster Rezidivbehandlung (85%, meist erneut Metronidazol 74%, sonst Fidaxomicin) - Rezidivrate ähnlich der Literatur (20%) - PPI, Alter>70 und hämatologische Neoplasie als Risikofaktoren für Rezidiv, Ribotyp 027 bei uns (noch) selten - Hohe Gesamtmortalität (17% innert 2 Monaten), CDI somit Marker für schwer kranke Patienten 15 Zukunftsaussichten, Strategieanpassung - Patienten mit hohem Rezidivrisiko definieren: - Alter > 70 Jahre - PPI - Hämatologische Neoplasie - (schwere Niereninsuffizienz und Hämodialyse) - (Hypalbuminämie) - (Nicht-CDI-Antibiotika können nicht gestoppt werden) - Bei hohem Rezidivrisiko Therapie anpassen: - PPI möglichst stoppen - Vancomycin p.o. mit Tapering? - Fidaxomicin, Tapering? (teuer!) - Probiotika? (limitierte Evidenz) - FMT (sehr teuer! aufwändig!) Risikoscore? 16