Tagungsbericht der Gesellschaft für Innere - Thüringen
Werbung

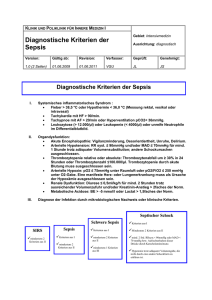
Tagungsbericht Entzündung: Mehr als Bakterien oder Viren Frühjahrstagung der Gesellschaft für Innere Medizin Thüringens e. V. im Rahmen des Internistenkongresses in Wiesbaden Andreas Stallmach, Paul La Rosée In der Differentialdiagnose entzündlicher Erkrankungen denken wir rasch an Bakterien und Viren. Doch die unspezifischen klassischen Symptome „Rubor, Calor, Dolor, Tumor“ treten natürlich nicht nur bei Infektionskrankheiten auf, sondern sind auch Zeichen von autoimmunologischen Erkrankungen. Diese betreffen etwa fünf Prozent der Menschen in den Industrieländern, ihre Häufigkeit nimmt zu. Die Differentialdiagnose zwischen klassischen Infektionskrankheiten und Autoimmunerkrankungen ist schwierig. Vor diesem Hintergrund fand am Sonntag, den 7. April 2013 auf dem 119. Jahreskongreß der Deutschen Gesellschaft für Innere Medizin (DGIM) in Wiesbaden unter diesem Titel „Entzündung: Mehr als Bakterien oder Viren“ das traditionelle Regionalsymposium der Gesellschaft für Innere Medizin Thüringens e. V. statt. Trotz der frühen Stunden hörten mehr als 50 Interessierte, wie zunächst Professor Dr. Frank Brunkhorst (Jena, Paul-Martini-For- schergruppe für Klinische Sepsisforschung, Universitätsklinikum Jena, Integriertes Forschungs- und Behandlungszentrum (IFB) „Sepsis und Sepsisfolgen“) zu der klassischen Infektionskrankheit, der „Sepsis“, neue Aspekte vorstellte. Er führte aus, daß das bisherige Scheitern neuer Ansätze zur Behandlung der schweren Sepsis und des septischen Schocks eng mit den Defiziten einer differenzierten Diagnosemöglichkeit verbunden ist. Der Zeitpunkt der Diagnose und damit die frühzeitige Initiierung therapeutischer Maßnahmen sind jedoch die entscheidende Determinante der Mortalität. Sowohl im prähospitalen als auch im intrahospitalen Verlauf der Erkrankung vergehen häufig Stunden bis Tage bis zur Diagnose und adäquaten Behandlung auf der Intensivstation. Gerade bei Intensivpatienten ist die Differentialdiagnose einer infektiösen Ätiologie des akuten inflammatorischen Organversagens (schwere Sepsis) angesichts der geringen Spezifität klinischer Symptome (Fieber, Leukozytose, Tachykardie und Tachypnoe, CRP-Anstieg) von anderen nichtinfektiösen Ursachen (SIRS) extrem schwierig. Zudem ist der mikrobiologische Nachweis einer Infektion gerade bei antibiotisch vorbehandelten Patienten problematisch. Procalcitonin (PCT) gilt gegenwärtig als einer der vielversprechendsten Biomarker in der Differentialdiagnostik der Sepsis. Procalcitonin ist ein Protein, das als Vorstufe des Hormons Calcitonin in der Schilddrüse gebildet wird. Bei bakteriellen und mykotischen Infektionen jedoch bilden auch Zellen in anderen Organen dieses Prohormon, dessen Konzentrationen im Blut dann schnell um ein Vielfaches ansteigen. In einer kürzlich publizierten Metaanalyse wurde die diagnostische Wertigkeit dieses Biomarkers erstmals systematisch untersucht (Wacker C, Prkno A, Brunkhorst FM, Schlattmann S., Procalcitonin as a diagnostic marker for sepsis: a systematic review and meta-analysis. Lancet Infectious Diseases. May;13(5):426-35). Hierbei wurden hohe Anforderungen bezüglich der methodischen Qualität gestellt, insbesondere mußte der gegenwärtige Goldstandard der Sepsisdefinition einschließlich mikrobiologischer Kriterien berichtet sein. Die bivariate Analyse der Daten ergab für Calcitonin eine mittlere Sensitivität und Spezifität von 0,77 (95 Prozent Konfidenzintervall [CI], 0,72-0,81) und 0,79 (95 Prozent CI, 0,74-0,84). Die Fläche unter der ROC-Kurve (AUC) betrug 0,85 (95 Prozent CI, 0,81-0,88). Die Heterogenität zwischen den Studien war jeAnzeige Ausgabe 6/2013 24. Jahrgang 343 Tagungsbericht doch erheblich (I2 = 96 Prozent). Procalcitonin ist der derzeit beste verfügbare Biomarker für die frühe Diagnose einer bakteriellen Sepsis. Allerdings reicht er als alleiniger Test für eine sichere Therapieentscheidung nicht aus, dazu müssen die Vorgeschichte des Patienten, das klinische Bild und immer auch mikrobiologische Untersuchungen mitbetrachtet werden. Procalcitonin ist der derzeit beste verfügbare Biomarker für die frühe Diagnose einer bakteriellen Sepsis. Professor Dr. Peter C. Konturek, Klinik Innere Medizin II (Thüringen-Kliniken GmbH, Standort Saalfeld) zeigte, daß eine immunsupprimierende Therapie (Chemotherapeutika, monoklonale Antikörper, Immunsuppressiva nach Transplantation, prolongierte Kortikoidtherapie, im Verlauf von hämatologischonkologischen beziehungsweise rheumatologischen Erkrankungen) eine Reaktivierung von verschiedenen viralen Infektionen begünstigen kann. Bestimmte Viren verbleiben im Organismus nach der Primärinfektion in nichtinfektiöser Form und werden infolge der Immunsuppression wieder reaktiviert. Klinisch relevant sind in erster Linie Reaktivierungen von Herpesinfektionen (α-Herpesviren wie Herpes-simplex-Virus-1, Herpes-simplex-Virus-2 und Varicella-Zoster-Virus, β-Herpesviren wie CMV, HHV-6 und -7-Viren und γ-Herpesviren wie Epstein-Barr-Virus, Kaposi-Sarcoma-Herpesvirus – HHV-8 (KSHV)). Infolge der Immunsuppression findet eine erhöhte Virusreplikation statt, die bei einem betroffenen Patienten zur progressiven Ausweitung der Infektion mit Befall der Haut (insbesondere HSV-1, HSV-2, VZV), innerer Organe (Pneumonie, Hepatitis, Nephritis, Enzephalomyelitis) und diversen Manifestationen im Gastrointestinaltrakt (breites Spektrum an Läsionen von Erosionen bis zu tiefen Ulzerationen) führt. Die Zytomegalievirusinfektion gilt als eine der am häufigsten reaktivierten Virusinfektionen unter Immunsuppression. Die CMV-Reaktivierung führt zu einer Reihe von klinischen Krankheits- 344 bildern wie Mononukleosesyndrom, Hepatitis, Chorioretinitis beziehungsweise Retinitis, Enterokolitis, Meningoenzephalitis, Guillain-Barré-Syndrom, interstitielle Pneumonie, Myokarditis, Thrombozythämie, hämolytische Anämie und in seltenen Fällen sogar akute Nebenniereninsuffizienz. CMV zeigt darüber hinaus eine hohe Affinität zu dem Gastrointestinaltrakt und verursacht im Rahmen einer Reaktivierung multiple Schleimhautulzerationen. Differentialdiagnostisch muß an die CMVReaktivierung bei Patienten mit Colitis ulcerosa (viel seltener mit Morbus Crohn) gedacht werden, falls die immunsuppressive Therapie mit einem Anstieg der entzündlichen Aktivität in der Kolonschleimhaut und Kortikoidrefraktärität assoziiert ist. Ohne eine spezifische Behandlung der CMV-Infektion (z.B. mit Gancyclovir) droht den Patienten oft die Notwendigkeit einer Kolektomie. Die Reaktivierungen der γ-Herpesviren (EBV, KSHV) sind nicht nur mit systemischer entzündlicher Reaktion, sondern auch mit erhöhtem onkogenem Potential verbunden. Die Folge der Reaktivierung von EBV sind unter anderem Posttransplantationslymphoproliferatives Syndrom (PTLS), BurkittLymphom, Morbus Hodgkin, Nasopharyngealkarzinom, Haarzelleukoplakie und ganz selten X-chromosomale lymphoproliferative Erkrankung. Die Reaktivierung der KSHV (HHV-8) kann in seltenen Fällen die Entwicklung eines Kaposi-Sarkoms mit der Manifestation an der Haut oder im Darm auslösen. Die Reaktivierung einer Hepatitis B unter Immunsuppression stellt in der Praxis ein besonders wichtiges, aber leider oft unterschätztes klinisches Problem dar. Das Risiko einer Hepatitis-B-Reaktivierung ist abhängig vom serologischen Status, von der Intensität der Immunsuppression sowie von der Art der Grunderkrankung. Das größte Risiko, unabhängig von der zu Grunde liegenden Erkrankung, findet sich bei HBsAg-positiven Patienten. Grundsätzlich können Reaktivierungen auch bei HBsAg-negativen Individuen (aber AntiHBc-AK-positiv) auftreten. Das Risiko einer Hepatitis-B-Reaktivierung ist insbesondere hoch bei Therapie mit mono- klonalen Antikörpern, Chemotherapie (insbesondere Anthrazykline) beziehungsweise Therapie mit Rituximab (Anti-CD20). Vor diesem Hintergrund ist es klinisch relevant, immer vor Einleitung einer immunsuppressiven Therapie den serologischen Hepatitis-Bund -C-Status zu erheben. Schließlich kann die Therapie mit monoklonalen Antikörpern (Rituximab, Natalizumab oder Efalizumab) in sehr seltenen Fällen eine gefährliche, mit hoher Mortalität assoziierte Manifestation im ZNS – die progressive multifokale Leukoenzephalopathie (PML) – als Folge haben. Die überlebenden Patienten sind infolge der schweren neurologischen Symptome (kognitive Störungen, motorische Dysfunktionen und Sehstörungen) stark behindert. Die Reaktivierung der Polyomaviren (JC-Viren) wird pathogenetisch für die Entstehung dieser Erkrankung verantwortlich gemacht. Eine umgehende Therapieeinleitung mit Mefloquine und Mirtazapin ist derzeit die empfohlene Behandlung. Die Reaktivierung einer Hepatitis B unter Immunsuppression stellt in der Praxis ein besonders wichtiges, aber leider oft unterschätztes klinisches Problem dar. Professor Dr. Peter Oelzner (Funktionsbereich Rheumatologie/Osteologie, Klinik für Innere Medizin III, Universitätsklinikum Jena) referierte zum Thema „Infektionsgetriggerte Autoimmunerkrankungen/Kollagenosen“. Neuere Untersuchungen liefern begründete Hinweise für die Bedeutung einer Infekt­ triggerung in der Pathogenese von Kollagenosen, insbesondere des Systemischen Lupus erythematodes (SLE) und des Sjögren-Syndroms. Virale Infekte spielen einerseits eine bedeutende Rolle bei der Induktion von programmiertem Zelltod (Apoptose). Auf genetischer Basis sind beim SLE physiologische Mechanismen der Beseitigung von apoptotischem Material gestört. Diese Störung bedingt eine Präsentation von Auto-Antigenen durch dendritische Zellen an TZellen sowie die Bildung von Auto-Antikörpern. Andererseits gibt es Hinweise Ärzteblatt Thüringen Tagungsbericht für eine gestörte Viruselimination. Für die Amplifikation der Entzündung sind Dysfunktionen der in die Abwehr von Virusinfektionen eingebundenen molekularen Systeme bedeutsam. Eine genetisch bedingte Überreaktivität des Tolllike-Rezeptor-abhängigen Interferon-αSystems, welches unter anderem durch Erkennung viraler DNA stimuliert wird, scheint in diesem Zusammenhang eine zentrale Rolle zu spielen. Auf Basis dieser Erkenntnisse sind neue molekularbasierte Therapien (z.B. mit Antikörpern gegen Interferon-α) in Entwicklung, welche Ansätze für eine Differentialtherapie auf Basis genetischer Marker bieten. In der Pathogenese des Systemischen Lupus erythematodes (SLE) und des Sjögren-Syndroms besitzt die Infekttriggerung eine hohe Bedeutung. Eine zwar seltene, aber sehr wichtige Differentialdiagnose bei inflammatorischen Krankheitsbildern ist die hämophagozytische Lymphohistiozytose (HLH). Dr. Thomas Schenk aus der Klinik für Innere Medizin II (Direktor: Prof. A. Hochhaus) stellte in einer sehr informativen Übersicht zum Thema „Ungebremste Inflammation: Die hämophagozytische Lymphohistiozytose (HLH)“ Daten vor, die belegen, daß die hämophagozytische Lymphohistiozytose (HLH) ein oft lebensbedrohliches Hyperinflammationssyndrom ist, das klinisch durch persistierendes Fieber und Splenomegalie gekennzeichnet ist (Abb. 1). Des weiteren findet man eine typische Laborkonstellation mit mindestens Bizytopenie, Hypertriglyzeridämie (≥ 3 mmol/l), erniedrigtem Fibrinogen (< 1,5 g/l), Ferritinerhöhung (≥ 500 µg/l, oft massiv erhöht), erhöhtem löslichen IL-2 Rezeptor (≥ 2400 U/ml), verminderter NK-Zell-Aktivität sowie eine Hämophagozytose (in Knochenmark, Liquor oder Lymphknoten), die jedoch kein zwingendes Diagnosekriterium darstellt. Für die Diagnose müssen fünf der genannten Kriterien oder ein bekannter genetischer Defekt vorliegen. Pathophysiologisch liegt diesen Veränderungen eine massive Zytokinaktivierung zugrunde. Trigger für die Entwicklung einer HLH sind vor allem (virale) Infektionen, aber auch maligne oder rheumatische Erkrankungen (Synonym: Makrophagenaktivierungs-Syndrom). Während bei der primären, vorwiegend im Kindesalter auftretenden HLH zunehmend definierte genetische Immundefekte als Ursache entdeckt wurden und eine standardisierte Therapie zur deutlichen Überlebensverbesserung geführt hat, ist die Genese bei der im Erwachsenenalter auftretenden sekundären HLH zum Großteil ungeklärt und die Mortalität mit ca. 50 – 60 Prozent hoch (Mitursache: Diagnose- und Therapieverzögerung!). Eine rasch eingeleitete intensive Chemoimmuntherapie stellt bei schwerer HLH einen deutlichen Überlebensvorteil für den Patienten dar. Im Rahmen einer Registerstudie am Klinikum Jena sollen offene Fragen zu Epidemiologie, Risikofaktoren und Therapie bei der Erwachsenen-HLH untersucht werden ([email protected]. de). Eine Registerstudie am Klinikum Jena soll offene Fragen zu Epidemiologie, Risikofaktoren und Therapie bei der Erwachsenen-HLH untersuchen (HLH. [email protected]). Insgesamt zeigte die sehr intensive Diskussion, daß bei dem Thema der Frühjahrstagung viele interessierte und zahlreiche, auch schwierige Fragen im Gespräch mit den Referenten beantwortet werden konnten. Vielleicht haben wir damit einen kleinen Beitrag zum Gelingen des in diesem Jahr sehr gelungenen Internistenkongresses liefern können. Abb. 1. Nachweis deutlicher Makrophagenvermehrung mit Hämophagozytose im Knochenmark eines Patienten mit Myelodysplastischem Syndrom. Phagozytierter Zelldetritus ist als dunkles Pigment deutlich in der Pappenheim-Färbung zu erkennen. Als ursächlich für die HLH ist die maligne hämatologische Systemerkrankung zu betrachten. Nach Einleitung einer spezifischen Therapie (5-Azacytidine) war die systemische Inflammation mit dem klinischen Bild eines hochfieberhaften sepsis-ähnlichen Geschehens deutlich rückläufig, zeigte jedoch im therapiefreien Intervall HLH-Rezidiv-Episoden. Aktuell erhält der Patient eine konsolidierende allogene Stammzelltransplantation. Hämophagozytose ist eines von 8 Diagnosekriterien der HLH, wird jedoch nur in ca. 60% der Fälle beobachtet. Bild: Dr. T. Schenk, Jena Ausgabe 6/2013 24. Jahrgang Prof. Dr. med. Andreas Stallmach Klinik für Innere Medizin IV Universitätsklinikum Jena e-mail: [email protected] PD Dr. med. Paul La Rosée Klinik für Innere Medizin II Universitätsklinikum Jena Erlanger Allee 1101 07747 Jena e-mail: [email protected] 345