8 Seiten
Werbung

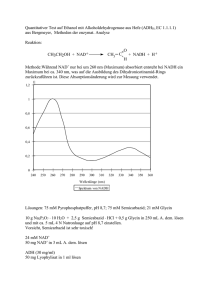
100 BIOCHEMIEPRAKTIKUM I: ANALYSE VON BIOMOLEKÜLEN PLATZ 1: MESSUNG VON ENZYMAKTIVITÄTEN UND METABOLITKONZENTRATIONEN Die Messung von Enzymaktivitäten und Metabolitkonzentrationen mit Hilfe des optischen Tests nach Warburg ist eine Routinemethode im biochemischen und klinisch-chemischen Labor. Auch Enzymreaktionen, an denen NADH und NAD+ bzw. NADPH und NADP+ nicht direkt beteiligt sind, können via Hilfsreaktionen mit den photometrisch messbaren Redoxreaktionen gekoppelt werden (gekoppelter Enzymassay im Exp. 1.8). Auf diese Weise wird der Anwendungsbereich des optischen Tests wesentlich vergrössert. Aktivitätsbestimmungen von Enzymen, die in Zellen vorhanden sind und die normalerweise im Serum nur in geringer Menge vorkommen, spielen in der Medizin bei der sogenannten Enzymdiagnostik eine bedeutende Rolle. Das Auftreten organspezifischer Enzyme im Serum kann eine Schädigung dieser Organe anzeigen. Bei leichten, reversiblen Zellschädigungen kommt es bevorzugt zu einem Austritt von Enzymen des cytoplasmatischen Raumes. Mitochondriale Enzyme in grösserer Menge im Serum findet man bei absterbenden Zellen (Zellnekrosen). Durch sorgfältige Interpretation von sogenannten "Enzymmustern", bei denen das Verhältnis der Aktivitäten verschiedener Enzyme zueinander beachtet wird, kann man in gewissen Fällen den Grad der Einzelzellschädigung, die Ausdehnung des Schadens und die Geschwindigkeit des ablaufenden Krankheitsprozesses (fulminant, akut, chronisch) beurteilen. Die Aufnahme der UV-Spektren von NAD+ und NADH soll die Grundlage für den sog. optischen Test zur Bestimmung von Enzymaktivitäten und Metabolitkonzentrationen aufzeigen. Die Bestimmung der Geschwindigkeiten des Umsatzes verschiedener Alkohole durch die Alkoholdehydrogenase in Exp. 1.6 soll die Substratspezifität der Enzyme demonstrieren. Theoretische Grundlagen: Photometrie (S. 31) UV-Spektren von Pyridinnucleotiden (S. 20) Optischer Test nach Warburg (S. 43) Enzymreaktionen (S. 34) Kenntnisse über Glykolyse und alkoholische Gärung Bezug zu anderen Plätzen: Substratspezifität von Trypsin und Chymotrypsin, Exp. 10.4 Messung von Enzymaktivität, Exp. 9.1 101 Experiment 1.6: UV-Spektren von NAD+ UND NADH In je eine Quarzküvette (teuer, sorgfältig zu behandeln!) NAD+ und NADH (50 µM in 50 mM Phosphatpuffer) sowie 50 mM Phosphatpuffer pH 7 (Blindwert) füllen. Die Extinktion der NAD+und NADH-Lösungen gegen den Blindwert zwischen 230 nm und 400 nm in 10 nm-Intervallen ablesen (5 nm-Intervalle im Bereich der Absorptionsmaxima) und tabellarisch festhalten. Die Extinktion des Blindwertes, definitionsgemäss Null, muss nach jeder Änderung der Wellenlänge kontrolliert und wenn nötig wieder auf Null abgeglichen werden (warum? siehe Theorieteil). Die gemessenen Extinktionswerte als Funktion der Wellenlänge auf Millimeterpapier aufzeichnen (Abszisse: Wellenlänge in nm, Ordinate: Extinktion) und millimolaren Extinktionskoeffizienten von NAD+ und NADH bei 260 und 340 nm berechnen. S Welche praktische Bedeutung haben die unterschiedlichen Spektren von NAD+ und NADH? Experiment 1.7: Aktivität und Substratspezifität der Alkoholdehydrogenase Prinzip: Alkoholdehydrogenase katalysiert die Reaktion: Ethanol + NAD+ º Acetaldehyd + NADH + H+ In diesem Versuch wird die Geschwindigkeit der Oxidation des Alkohols bei Substratsättigung gemessen. Damit die Reaktion vollständig nach rechts abläuft, wird der entstehende Acetaldehyd durch das Carbonylreagens Semikarbazid abgefangen. Die Enzymaktivität wird aus der Bildungsgeschwindigkeit von NADH ermittelt. Zur Illustration der Substratspezifität wird ferner die Enzymaktivität mit n-Propylalkohol und Isopropylalkohol bestimmt. Lösungen: 1 2 2a 2b 3 NAD+, 0.04 M Ethanol (0.21 M) und Semikarbazid (0.053 M) in Glycin/Natriumpyrophosphatpuffer, pH 8.7 n-Propylalkohol (0.21 M), sonst wie 2 Isopropylalkohol (0.21 M), sonst wie 2 Alkoholdehydrogenase (60 µg/ml) aus Hefe Ausführung: 1. In eine Küvette zuerst 0.1 ml Lösung 1, dann 1.89 ml Lösung 2 pipettieren, sorgfältig mischen durch Eintauchen des Rührstäbchens. 2. Küvette in den Lichtweg des Photometers bringen; Lichtweg öffnen und Extinktionsanzeige auf E = 0.0 einstellen. 3. 10 µ1 verdünnte Enzymlösung (Lösung 3) auf Rührstäbchen aufpipettieren und Reaktion durch 3-maliges sorgfältiges Eintauchen des Rührstäbchens in die Küvette auslösen. 102 4. Registrierschreiber (Papiergeschwindigkeit: 2mm/Sekunde; der Skalabereich der Ordinate von 0 bis 100 entspricht einer Extinktion von 1.0) starten und die Extinktion gegen die Zeit aufzeichnen bis die Extinktion ca. 0.7 oder der Papiervorschub 20-25 cm erreicht hat, dann Schreiber stoppen. Test mit n-Propylalkohol und Isopropylalkohol wiederholen. Auswertung: Extinktionsänderungen pro Minute ()E/min) aus der Anfangssteigung bestimmen. Aktivitätskonzentrationen, spezifische Aktivität und molekulare Aktivität berechnen (siehe Theorieteil, Einheiten der Enzymaktivität). Der millimolare Extinktionskoeffizient von NADH bei 340 nm beträgt 6.22 mM-1 cm-1. Alkoholdehydrogenase hat eine Molekularmasse von 150'000 Da. Ethanol n-Propyl alkohol*) Isopropylalkohol*) )E/min ........ ........ ........ Aktivitätskonz. in der Messküvette (U/ml) ........ ........ ........ Aktivitätskonz. der Enzymlösung (U/ml) ........ ........ ........ Spezifische Aktivität (U/mg) ........ ........ ........ Molekulare Aktivität (min-1) ........ ........ ........ *) Falls nicht beide Substrate untersucht werden, Resultate zwischen den Kursteilnehmern austauschen. S Wie liesse sich feststellen, ob die geringere Aktivität mit den C3-Alkoholen auf schlechtere Bindung der Substrate ans Enzym oder auf langsamere Oxidation zum Aldehyd zurückzuführen ist? S Wovon hängt die Enzymaktivität bei gegebener Substratkonzentration ab? S Wie lange dauert ein Reaktionszyklus der Alkoholdehydrogenase mit Ethanol als Substrat? S Welche praktische Bedeutung hat die Bestimmung der spezifischen Aktivität? 103 Experiment 1.8: Messung der Aktivität von Kreatinkinase im Plasma mit "Trockenchemie" Der folgende Versuch soll eine wichtige Entwicklung der klinischen Chemie demonstrieren. Mit "Trockenchemie" können in jeder Arztpraxis ohne Aufwand einige wichtige Substanzen und Enzymaktivitäten im Blut gemessen werden. Trockenchemie: Die Weiterentwicklung der Teststreifenmethodik (Exp. 5.7 spezifischer Nachweis von Glucose mit Diabur-Test) hat zu neuen Reagenzträgern mit mehrschichtigem Aufbau geführt. Die Reagenzien sind in haltbarem Zustand in verschiedenen Schichten enthalten. Aufeinanderfolgende Reaktionsschritte können durch die Diffusion der Probe und der dabei aufgelösten Hilfsreagenzien auf dem Weg in tiefere Schichten getrennt stattfinden. Der Begriff "Trockenchemie" hat sich zur Bezeichnung durchgesetzt, da im Testträger die Reagenzien in getrocknetem Zustand vorhanden sind. Blut Transparente Folie Schutznetz Reaktionschicht Trennvlies Trgerfolie Glasfasertransportvlies Magnetcode Querschnitt durch einen Reagenzträger, der mit Vollblut funktionsfähig ist. Die Erythrozyten der auf dem Schutznetz aufgetragenen Vollblutprobe werden im Trennvlies vollständig und ohne Hämolyse zurückbehalten. Durch Diffusion erreicht das Plasma ein Glasfasertransportvlies, das als Plasmareservoir dient und Plasma unter die Reaktionszone bringt. Bei Reaktionsstart wird die Reaktionszone ins Plasmaresevoir gedrückt und entnimmt die benötigte Menge Plasma. Die spezifische Reaktionskette führt zur Bildung eines Farbstoffs, der in die transparente Folie diffundiert. Die Konzentration des Farbstoffs wird durch Reflexion von Licht geeigneter Wellenlänge an der transparenten Folie photometrisch gemessen. Je mehr Farbstoff gebildet wird, desto mehr wird vom auffallenden Licht absobiert und desto weniger Licht wird von der Folie reflektiert und kann im Reflexionsphotometer gemessen werden. Der Magnetstreifen enthält alle testund methodenspezifischen Informationen, die zur Durchführung des Tests und zur Berechnung der gesuchten Konzentration durch den Mikroprozessor des Photometers notwendig sind. Enzymaktivitäten werden aus dem zeitlichen Verlauf der Farbintensität automatisch berechnet. 104 Prinzip: Kreatinkinase kommt in Skelettmuskeln, im Herz, Gehirn und in glatten Muskelzellen vor. Drei dimere Isoenzyme kommen vor: CK-MM (Skelettmuskeltyp), CK-MB (Herzmuskeltyp) und CK-BB (Gehirntyp). In glatten Muskelzellen findet sich hauptsächlich CK-BB. Diagnostische Bedeutung hat nur die Bestimmung der Herzmuskel- und Skeletmuskelenzyme. Die Kreatinkinase katalysiert die Reaktion Kreatin + ATP º Kreatinphosphat + ADP (1) Die Reaktion von rechts nach links dient der raschen Bereitstellung von ATP für die Muskelkontraktion. Die Kreatinkinase kommt im Herz- und Skelettmuskel in hoher Konzentration vor. Werden Muskelfasern geschädigt (z.B. bei 02-Mangelversorgung des Myocards infolge Verschlusses einer Coronararterie), so gelangt Kreatinkinase ins Blut. Die Bestimmung der Kreatinkinase-Aktivität im Serum ist darum von grosser klinisch-diagnostischer Bedeutung. In diesem Experiment wird die Aktivität der Kreatinkinase aus der Geschwindigkeit der Bildung von ATP gemessen (Reaktion (1) von rechts nach links). Da die Geschwindigkeit der Bildung von Kreatin und ATP nicht direkt mit einer optischen Methode bestimmt werden kann, wird die Reaktion (l) mit den Hilfsreaktionen (2), (3) und (4) gekoppelt: Kreatinphosphat + ADP º Kreatin + ATP (l) ATP + Glycerin 6 Glycerin-3-phosphat + ADP (2) Glycerin-3-phosphat + O2 6 Dihydroxyacetonphosphat + H2O2 (3) H2O2 + Chromogen 6 Farbstoff + H2O (4) Kreatin + Dihydroxyacetonphosphat + Farbstoff + H2O (1-4) Kreatinphosphat + Glycerin + O2 + Chromogen 6 Reaktion (2) wird durch Glycerokinase, Reaktion (3) durch Glycerinphosphatoxidase und Reaktion (4) durch eine Peroxidase katalysiert. Die gesuchte Geschwindigkeit der Reaktion (1) ist gleich der gemessenen Geschwindigkeit der Reaktion (4), sofern die gekoppelten Hilfsreaktionen (2)-(4) viel schneller als die Reaktion (1) ablaufen und ihre Gleichgewichte rechts liegen. Alle Enzyme sowie die im System nicht erzeugten Substrate müssen in trockenem Zustand in der Reaktionszone des Reagenzträgers enthalten sein (siehe vorne). S Nennen Sie die Substrate, die im Reagenzträger enthalten sein müssen. 105 Lösungen und Angaben zu den Blutproben: 1. Puffer für Verdünnung (falls notwendig) 2. Proben 1-3: Kreatinkinase enthaltendes Plasma eines Schweins mit Enzymaktivitäten, wie sie im Verlauf eines Herzinfarkts (= Nekrose eines Teils des Herzmuskels infolge eines akuten Sauerstoffmangels durch den plötzlichen Gefässverschluss im Bereich einer Herzkranzarterie) beim Mensch gemessen werden. Ausführung: An Stelle von Vollblut wird hier Plasma verwendet, weil Plasma zur Aufbewahrung eingefroren werden kann. Die Messbereitschaft des Geräts wird auf der Anzeige angegeben. Alle hundert Messungen muss das Reflexionsphotometer geeicht werden und es erscheint "CHEK" auf der Anzeige. - In diesem Fall den Teststreifen aus dem CHEK-Behälter nehmen und flach so halten, dass der Magnetstreifen auf der Unterseite liegt und das Graufeld gegen das Gerät hin weist. - Messkammer öffnen und den Streifen waagrecht auf der Mitte der Lade bis zum Einrasten einführen. Die drei Messwerte auf der Anzeige sollen innerhalb der Grenzen, die auf dem CHEKBehälter angegeben sind,liegen. Sonst der Kurslaborantin (via Assistierende) melden. - Teststreifen durch vorsichtiges Ziehen entfernen und in den CHEK-Behälter zurücklegen. Messkammer schliessen. Messung der Proben: 1. Testträger aus dem CK-Behälter entnehmen und die Schutzfolie vom nicht gelochten Ende abziehen und verwerfen. 2. Das vordere Ende mit der Reaktionszone des Reagenzträgers flach in den Halteschlitz der Pipettenhalterung einführen. 3. Mit der bereitgestellten Pipette 32 µl der Plasmaprobe in die Plastikspitze aufziehen und überschüssige Probe mit einem Papiertüchlein wegwischen. 4. Probe auf das Zentrum des roten Netzes auftragen ohne das Netz zu berühren. Wichtig: unter keinen Umständen darf mehr als das vorgegebene Volumen aufgetragen werden, da sonst überschüssiges Plasma aus dem Reagenzträger gepresst wird und das Messgerät beschädigt wird. 5. Innerhalb von 15 Sekunden muss der Teststreifen mit der Reaktionszone voran waagrecht auf der Mitte der Lade in die Messkammer bis zum Einrasten eingeführt werden. Messkammer schliessen. 6. Anzeige verfolgen und warten bis das Resultat auf der Anzeige erscheint und ausgedruckt wird. Papiervorschub betätigen, Papierstreifen mit Resultat abreissen und beschriften. Das Resultat ist bereits in U/Liter ausgerechnet. Falls die Enzymaktivität den Messbereich überschreitet, 0.1 ml der Probe mit 2.9 ml Puffer verdünnen und erneut messen. Resultat mit dem Verdünnungsfaktor multiplizieren. 7. Testträger durch vorsichtiges Ziehen aus der Messkammer entfernen und kontrollieren, ob eine Farbveränderung auf dem oberen Teil des Testträgers stattgefunden hat. 8. Messkammer schliessen. Resultate tabellarisch unten festhalten. 106 Es wird angenommen, dass die Blutproben von einem 61-jährigen Patienten stammen, der mit Verdacht auf Herzinfarkt als Notfall ins Spital eingewiesen wird (siehe Lösungen). Blutentnahmen *) Kreatinkinaseaktivität (U/Liter) ca. 1 Stunde ......... ca. 7 Stunden ......... 24 Stunden ......... 5 Tage 59 U/l *) Zeitpunkt nach Spitaleinlieferung des Patienten Der Normalwert der Kreatinkinaseaktivität ist mit der hier verwendeten Messmethode 10-80 U/Liter. Der zeitliche Verlauf der gemessenen Enzymaktivität ist beispielhaft für den Verlauf eines (komplikationslosen) Herzinfarkts. Die Aktivität der Kreatinkinase im Blut steigt spätestens 6 Stunden nach dem Infarktereignis im Blut an, erreicht nach ca. 24 Stunden ein Maximum und kehrt meist nach 5-6 Tagen in den Bereich der Norm zurück. S In einer Blutprobe wird ein erhöhter Gehalt an Kreatinkinase gemessen. Aus welchen Organen/Geweben kann die Kreatinkinase stammen? Welche Ursache für einen solchen Befund könnten Sie sich vorstellen? S Nennen Sie die Vorteile eines "Trockenchemie-Tests". S Wie könnte man einen Testträger zur Messung der Blutglucose entwickeln? Welche Reaktionskette schlagen Sie vor? (siehe Exp. 5.6) 107 Experiment 1.9 Messung der Pyruvatkonzentration mit Lactatdehydrogenase Prinzip: Lactatdehydrogenase katalysiert die Reaktion Pyruvat + NADH + H+ º Lactat + NAD+ Unter den gewählten Bedingungen liegt das Gleichgewicht stark rechts, d.h. nach Zugabe des Enzyms werden Pyruvat und NADH nahezu vollständig in Lactat und NAD+ umgewandelt. Die Abnahme von im Überschuss vorhandenem NADH ist deshalb ein Mass für die Menge des vorhandenen Pyruvats. Lösungen: NADH (3.75 mM); Tris-HCl-Puffer (0.06 M), pH 7.6; Natriumpyruvat, unbekannte Konzentration; Lactatdehydrogenase (ca. 100 µg/ml). Ausführung: In die Küvette werden in untenstehender Reihenfolge einpipettiert und durch Eintauchen des Rührstäbchens sorgfältig gemischt: NADH Puffer Substrat 0.1 ml 2.29 ml 0.1 ml 1. Photometeranzeige ohne Küvette im Lichtweg auf E340 nm = 0.0 einstellen. Registrierschreiber ebenfalls mit "Zero-Knopf" auf 0-Linie einstellen (rechte Grundlinie). 2. Testküvette in den Lichtweg schieben und Extinktion ablesen. 3. 10 µl Enzymlösung auf Rührstäbchen pipettieren und Reaktion durch 3maliges Eintauchen des Stäbchens in die Küvette auslösen. 4. Registrierschreiber starten (Papiergeschwindigkeit: 1 cm/Minute; der Skalabereich der Ordinate von 0 bis 100 entspricht einer Extinktion von 1.0) und die Extinktion gegen die Zeit aufzeichnen bis die Extinktion konstant bleibt, d.h. für ca. 10-15 Minuten. Schreiber stoppen. 5. Extinktion ablesen und Extinktionsabnahme, )E340, aus Anfangs- und Endwert bestimmen. Berechnung der Pyruvatkonzentration: Aus )E340 die umgesetzte Pyruvat-Konzentration in der Messküvette berechnen (g340nm = 6.22 mM-1 cm-1), dann die millimolare Pyruvatkonzentration in der untersuchten Lösung berechnen und in mg/ml umrechnen (Mr 88). S Welche Voraussetzungen müssen erfüllt sein, damit der optische Test zur Konzentrationsbestimmung von Substraten verwendet werden kann? S In welcher Weise beeinflusst der pH-Wert das Gleichgewicht der Lactatdehydrogenase-Reaktion? S Wie beeinflusst die zugegebene Enzymmenge den Verlauf der Kurve? S Können Lactatkonzentrationen mit Hilfe dieser Reaktion bestimmt werden?