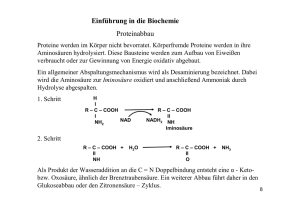
Pitavastatin (Livazo®) Pitavastatin (Livazo®) ist ein weiteres Statin
Werbung

Pitavastatin - Pharmazeutische Chemie Pitavastatin (Livazo ) Pitavastatin (Livazo) ist ein weiteres Statin, das nun in Deutschland auf dem Markt ist. Die Substanz ist schon längere Zeit bekannt und in Japan bereits seit 2003, in Korea seit 2005, in China seit 2009 und in den USA seit 2010 zugelassen. Es wird in Form des stabilen Calciumsalzes eingesetzt und ist indiziert zur Senkung erhöhter Gesamtcholesterol- und LDL-Cholesterolwerte bei primärer Hypercholesterinämie und gemischter Dyslipidämie, sofern nichtmedikamentöse und diätetische Maßnahmen versagen. HO COOH OH F N Pitavastatin Abbildung 1 Das erste Statin überhaupt - Mevastatin (ML-236B, Compactin) - wurde bereits 1973 entdeckt, wird aber nicht in der Klinik eingesetzt (Endo 2010). Neben Pitavastatin sind zahlreiche weitere Statine in der Klinik etabliert: Lovastatin (u.a. Mevinacor), Atorvastatin (Sortis), Fluvastatin (u.a. Cranoc, Locol), Simvastatin (u.a. ZOCOR), Pravastatin (u.a. Mevalotin protect) und Rosuvastatin (Crestor). Cerivastatin (Lipobay) wurde 2001 vom Markt zurückgenommen. Allen Statinen ist der Wirkmechanismus gemeinsam. Sie hemmen die endogene Cholesterol-Biosynthese, indem sie kompetitiv die HMG-CoA-Reduktase - das Schrittmacherenzym zur Bildung von körpereigenem Cholesterol - blockieren. Dieses Enzym katalysiert unter Verbrauch von zwei Molekülen NADPH die 4Elektronen-Reduktion von 3-Hydroxy-3-methyl-glutaryl-CoA (HMG-CoA) zu Mevalonsäure (Abbildung 2) (u.a. Istvan 2002, Friesen und Rodwell). Mevalonsäure ist die Ausgangsverbindung für alle Isoprenoide und Sterole und demnach auch für Cholesterol im menschlichen Körper. 1 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie Als Kompensation zur verminderten, hepatischen Cholesterolsynthese durch die HMG-CoA-Reduktase-Hemmung kommt es u.a. zu einer vermehrten Expression von LDL-Rezeptoren, wodurch vermehrt LDL aus dem Plasma in die Zellen aufgenommen wird und demzufolge der Plasma-LDL-Spiegel absinkt. Statine (u.a. Pitavastatin) HO COOH HMG-CoA-Reduktase HO O SCoA OH 2 NADP+ CoA-SH 2 NADPH 2 H+ (R)-Mevalonsäure (S)--3-Hydroxy-3-methyl-glutaryl-CoA (HMG-CoA) Abbildung 2: COOH Wirkmechanismus der Statine nach Istvan 2002 Statine werden unterteilt in die nichtsynthetischen Typ 1-Statine natürlichen oder zumindest teilweise natürlichen Ursprungs und die vollsynthetischen Typ 2-Statine (Istvan 2002) (Strukturformeln s. Abbildungen 4 und 5). Zu den Typ 1-Statinen zählen das erste entdeckte Statin überhaupt, das Mevastatin, sowie Lovastatin, Pravastatin und Simvastatin. Pravastatin wird durch mikrobielle Hydroxylierung aus Mevastatin gewonnen, Simvastatin wird partialsynthetisch aus Lovastatin hergestellt (s. Steinhilber, Schubert-Zsilavecz, Roth 2010). Alle anderen Statine, darunter auch Pitavastatin, gehören zu den Typ 2-Statinen und werden vollsynthetisch hergestellt. Die Statine zeigen hinsichtlich ihrer chemischen Struktur einen einheitlichen, immer wiederkehrende Bauplan. Sie können als 7-substituierte 3,5Dihydroxyheptansäuren aufgefasst werden (s. Abbildung 3). Als Pharmakophor fungiert dabei die 3,5-Dihydroxycarbonsäurekette mit den C-Atomen 1 bis 5, die strukturell sehr ähnlich der Hydroxymethylglutaryl-Einheit von HMG-CoA ist und diese am Enzym imitiert. Insbesondere die Konfigurationen an den beiden chiralen und OH-tragenden Kohlenstoffatomen sind für die Wirksamkeit von Bedeutung. Diese HMG-imitierende Gruppe der Statine bindet mit hoher 2 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie Affinität an die HMG-CoA-Bindungsstelle des Enzyms. Die NADPHBindungsstelle wird von den Statinen nicht besetzt. 2 HO 1 COOH 3 4 OH 5 7 6 Ringsystem 7-substituierte 3,5-Dihydroxyheptansäure Abbildung 3: Einheitlicher Bauplan der Statine Mevastatin, Lovastatin und Simvastatin sind Prodrugs. Die inaktiven Lactonstrukturen dieser Verbindungen werden in Darmmukosa und Leber schnell zu den entsprechenden wirksamen, offenkettigen Hydroxycarbonsäuren hydrolisiert. Pravastatin ist das einzige Typ 1-Statin, das in seiner ringoffenen Form vorliegt und damit keiner Bioaktivierung bedarf. Die Ethylgruppe (CAtome 6 und 7) als Spacer ist für die Aktivität optimal. Als Ringsystem besitzen alle Typ 1-Statine ein teilweise ungesättigtes Decalin mit charakteristischen Substitutionen. Auch bei den Typ 2-Statinen ist die 3,5-Dihydroxycarbonsäurestruktur vorhanden. Alle liegen in der ringoffenen, aktiven Form vor. In der Klinik werden die stabilen Salze - vorwiegend die Calciumsalze - verwendet. Zwischen der HMG-imitierenden Einheit (= Dihydroxycarbonsäure) und dem Ringsystem ist ein Abstand von zwei C-Atomen optimal. Außer Atorvastatin besitzen alle anderen Typ 2-Statine innerhalb der Kohlenstoffbrücke eine (E)-konfigurierte Doppelbindung. Das Ringsystem kann stark variiert werden. Hier sind sowohl 5als auch 6-gliedrige (stickstoffhaltige) Aromaten und auch bizyklische Systeme möglich. Die Affinität zur HMG-CoA-Reduktase wird durch p-Fluorophenyl- sowie verzweigte, kurze, aliphatische Substituenten wie zum Beispiel einem Isopropylrest in ortho-Position des Ringsystems erhöht. Auch beim Pitavastatin wurde das Rad nicht neu erfunden. Hier liegt ein Chinolinring vor, der an der 3 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie einen ortho-Position den typischen p-Fluorophenyl-Substituenten trägt, an der anderen anstelle des Isopropylrestes einen Cyclopropylrest. Typ 1-Statine inaktives Lacton, Prodrug HO H ringoffene Hydroxycarbonsäure Wirkform HO O Buttersäureester O + H 2O COOH Hydrolyse OH O 2 C-Atome Abstand O H vgl. H HO COOH Decalin-Ringsystem, teilweise ungesättigt O S Lovastatin CoA HMG-CoA HO H O HO H COOH O OH O O O O H H H HO Simvastatin Abbildung 4: Pravastatin Typ 1-Statine nach Istvan 2002 4 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie Typ 2-Statine HM G-imitierende Gruppe: 3,5-Dihydroxycarbonsäure M ethylgruppe des HM G -CoA fehlt HO COO H HO H vgl. O COO H Pitavastatin OH S CoA F HM G-CoA imm er p-FluorophenylSubstituent bei Pitavastatin Cyclopropylgruppe, ansonsten immer Isopropylgruppe N zentrales Ringsystem, 5- oder 6-gliedrige H eteroarom aten, auch Bizyklen möglich, bei Pitavastatin: Chinolin H HO HO H COO H COO H OH OH F F (E) N O Fluvastatin H HO N C erivastatin HO H COOH CO OH OH OH F F N N N O N S O HN O Atorvastatin R osuvastatin Abbildung 5: Typ 2-Statine nach Istvan 2002 5 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie Die Bindungsverhältnisse im aktiven Zentrum der HMG-CoA-Reduktase sind durch Kristallstrukturanalysen sowie Molecular-Modelling-Untersuchungen aufgeklärt worden (Istvan und Deisenhofer 2001, Istvan 2002, Saito 2009). Alle Statine zeigen wie erwähnt ein ähnliches Bindungsverhalten - allerdings mit einer unterschiedlichen Anzahl von Wechselwirkungen zwischen Enzym und Inhibitor. Daraus resultieren dann unterschiedliche Wechselwirkungsenergien und letztlich unterschiedliche Hemmkonstanten (s. Tabelle 1). Statin Fluvastatin Cerivastatin Rosuvastatin Atorvastatin Pitavastatin IC50 28 nM 10 nM 5 nM 8 nM 6,8* nM Tabelle 1: IC50-Werte für Typ 2-Statine nach Istvan 2002 * nach Saito 2009 Der Pharmakophor - die 3,5-Dihydroxycarbonsäureeinheit - besetzt das aktive Zentrum genau da, wo das natürliche Substrat HMG-CoA gebunden wird. Die Carboxylatgruppe des Pharmakophors wird über H-Brücken mit den terminalen Aminogruppen zweier Lysinreste (K692 und K735) sowie mit der Hydroxylgruppe eines Serins (S684) fixiert. Zusätzlich stabilisiert wird die Bindung des Pharmakophors im aktiven Zentrum durch H-Brücken seiner beiden Hydroxylgruppen mit weiteren Aminosäuren (Glutaminsäure E559, Asparaginsäure D690 und Asparagin N755). Die variable, hydrophobe Partialstruktur der Statine positioniert sich in einer Tasche des Enzyms, die sich erst nach Bindung des Pharmakophors durch Neuausrichtung von Aminosäuren am C-terimalen Ende ausbildet. Für die Typ 2-Statine ergibt sich durch die p-Fluorophenylgruppe eine zusätzliche Bindung mit einem Argininrest (R590). Die Cyclopropylgruppe des Pitavastatins genauso wie auch die Isopropylgruppen der übrigen Typ 2-Inhibitoren ersetzen funktionell den Decalinring der Typ 1-Inhibitoren. Für Rosuvastatin und Atorvastatin ergeben sich durch ihre zusätzlichen funktionellen Gruppen am Heterozyklus weitere Wechselwirkungen mit Aminosäureresten des Enzyms. In Abbildung 6 sind die vermeintlichen polaren Bindungen von Pitavastatin im aktiven Zentrum der HMG-CoA-Reduktase wiedergegeben (nach Istvan 2002, Saito 2009 und in Anlehnung an Steinhilber, Schubert-Zsilavecz, Roth 2010). So sehr sich die Statine in ihrem Wirkmechanismus ähneln, so unterschiedlich ist deren Pharmakokinetik (s. dazu u.a. Steinhilber, Schubert-Zsilavecz, Roth 2010, Saito 2009 und Kawai et al. 2011). 6 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie D690 E559 K692 O O H N O O H H H N755 O O H K735 O 1 N 3 H N 5 H H O H 7 O S684 F R590 N H N H H Abbildung 6: N N H H Postulierte Bindung von Pitavastatin im aktiven Zentrum der HMG-CoA-Reduktase nach Istvan 2002 und Saito 2009. Pitavastatin wird nach peroraler Einnahme schnell und gut aus den oberen Abschnitten des Magen-Darm-Traktes resorbiert, wobei die unveränderte Substanz einem enterohepatischen Kreislauf unterliegt. Die Absorptionsrate beträgt 80 % (Fujino et al. 2003). Interessant ist die Metabolisierung des Pitavastatins (s. Fujino et al. 2003, Saito 2009, Fachinformation Livazo 2011) (Abbildung 7). Statine sind bekannt dafür, sich selektiv in der Leber anzureichern und dort über CYP-vermittelte Reaktionen metabolisiert zu werden. Beispielsweise werden die lipophilen Statine Lovastatin, Simvastatin und Atorvastatin über das CYP3A4-Isoenzym verstoffwechselt. Pitavastatin ist ebenfalls lipophil, ähnelt bezüglich der Biotransformation aber eher dem hydrophilen Pravastatin, das nur minimal über CYP3A4 abgebaut wird und dessen Hauptbiotransformationsreaktion eine Sulfatierung ist. 7 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie HO COOH Pitavastatin OH F N sehr wenig! CYP2C9 Hydroxylierung UDP-Glucuronyl Transferasen HO COOH OH O HO HO OH OH COOH O F O Esterglucuronid OH F N OH N M-13 Pitavastatinglucuronid Elimination der Glucuronsäure Ringschluss HO O O F Hydrolyse Pitavastatin N Pitavastatinlacton Hauptmetabolit Abbildung 7: Pitavastatin-Metabolismus nach Saito 2009 8 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie Im Plasma liegt Pitavastatin überwiegend in unveränderter Form vor. Im Vordergrund beim Pitavastatinmetabolismus steht die Konjugation mit Glucuronsäure in der Leber durch verschiedene UDP-Glucuronyltransferasen (UGT1A1, UGT1A3, UGT2B7). Die Konjugation erfolgt an der freien Carboxylgruppe, so dass das resultierende Pitavastatinglucuronid als Estertypglucuronid (Acylal) bezeichnet werden kann. Anschließend kommt es unter Elimination der Glucuronsäure zur Bildung des inaktiven Pitavastatinlactons, das der Hauptmetabolit ist. Interessanterweise wird der Lipidregulator Gemfibrozil auch über UGT1A1 und UGT1A3 metabolisiert und hemmt dadurch gleichzeitig stark die Glucuronidierung von Statinen wie z.B. der Wirkform von Simvastatin, der Simvastatinsäure (Vaughan und Gotto 2003). Dementsprechend ist die gleichzeitge Anwendung von Pitavastatin und Gemfibrozil natürlich kontraindiziert. Die Metabolisierung des Pitavastatins über Cytochrom P450 spielt nur eine untergeordnete Rolle. Ein Nebenmetabolit ist zum Beispiel das hydroxylierte M13, dessen Bildung u.a. durch CYP2C9 vermittelt wird, in vivo aber kaum detektierbar ist (Fujino et al 1999). Dementsprechend sollte das Interaktionspotenzial zum Beispiel bei gleichzeitiger Einnahme von CYP3A4Inhibitoren deutlich geringer ausgeprägt sein als beispielsweise beim Simvastatin. Eine Studie zum Einfluss von Grapefriutsaft (CYP3A4!) auf die Pharmakokinetik von Pitavastatin bestätigt diese Annahme (Ando et al. 2005). Die selektive Anreicherung der Statine wird auf ihre Affinität zu einem leberspezifischen Anionentransporter, dem OATP2, zurückgeführt, wodurch die unter physiologischen Bedingungen vorwiegend als Carboxylat-Anionen vorliegenden Statine aktiv in das Lebergewebe aufgenommen werden. Auch für Pitavastatin wird ein solcher Mechanismus angenommen, da die gleichzeitige Applikation von Ciclosporin, einem OATP2-Inhibitor, zu einem 4,6-fachen Anstieg der Plasmakonzentration des Statins führte. Demzufolge ist Pitavastatin bei denjenigen Patienten, die mit Ciclosporin behandelt werden, kontraindiziert (Hirano et al. 2004, Saito 2009). Literatur: Ando, H. et al. Br J Clin Pharmacol 2005, 60, 494 Endo, A. Proc Jpn Acad Ser B Phys Biol Sci 2010, 86, 484 Fachinformation Livazo 2011 Friesen, J.A. und Rodwell, V.W. Genome Biology 2004, 5, 248 Fujimo, H. et al. Xenobio Metabol Dispos 1999, 14, 415 Fujino, H. et al. Xenobiotica 2003, 33, 27 Hirano, M. et al. J Pharmacol Exp Ther 2004, 311, 139 Istvan, E.S. und Deisenhofer, J. Science 2001, 292, 1160 9 CA 17.7.2011 Pitavastatin - Pharmazeutische Chemie Istvan, E.S. Am Heart J 2002, 144(6 Suppl), S27 Kawai, Y.K et al. Drug Des Devel Ther 2011, 5, 283 Saito, Y. Vasc Health Risk Manag 2009, 5, 921 Steinhilber, D., Schubert-Zsilavecz, M. und Roth, H.J. in: Medizinische Chemie, Deutscher Apotheker Verlag 2010, 2. Aufl., 429 Vaughan, C.J. und Gotto, A.M. Circulation 2004, 110, 886 10 CA 17.7.2011