B17 - Institut für Kernchemie - Johannes Gutenberg
Werbung
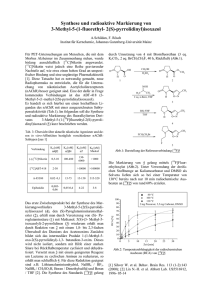
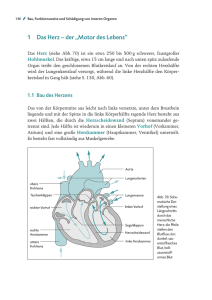
Ex vivo-Biodistributionen des D2-Antagonisten Fallypride 1 M. Piel1, S. Höhnemann1, D. Stark, U. Schmitt2, F. Rösch1 Institut für Kernchemie, 2Klinik für Psychiatrie, Johannes Gutenberg-Universität Mainz In Zusammenarbeit mit der Klinik für Psychiatrie wurden die Synthese, die Markierung [1] und die in vitroAffinität [2] des selektiven D2-Antagonisten Fallypride evaluiert, Abb.1: O O O N H sungsmittel wurde im Vakuum entfernt und das Produkt in isotonischer Kochsalzlösung aufgenommen. 100 µl dieser Lösung wurden in Sprague-Dawley Ratten (250350 g, n = 12) injiziert, diese nach festgelegten Zeitpunkten t (5, 10, 30 60 und 90 Minuten) getötet und die Verteilung der Verbindung in den verschiedenen Organen untersucht, Abb. 3 & 4: 1,75 Hirn Niere Leber Blut N 1,50 F Abb.1: N-(((S)-1-Allylpyrrolidin-2-yl)methyl)-5-(3[18F]fluorpropyl)-2,3-dimethoxybenzamid ([18F]Fallypride, [18F]FP) 1,00 0,75 0,50 18 18 F-Aktivität [% iD/g] 1,25 0,25 0,00 Im Rahmen dieser ex vivo-Biodistributionsstudie sollte die Organverteilung des Liganden für verschiedene, für die PET relevante Organe untersucht werden. 18 Experimentelles: Zur Darstellung von [ F]FP wurde der Markierungsvorläufer (5 mg, 10 µmol) in 1 mL MeCN gelöst und für 5 Minuten mit 5 mg K2CO3 behandelt. Anschließend wurde diese Lösung bei 85°C für 20 Minuten mit [18F]Fluorid umgesetzt: O O O N H N 0 10 20 30 40 50 60 70 80 90 Zeit p.i. [min] Abb.3: Biodistribution von [18F]FP in Hirn, Niere, Leber und Blut Dabei zeigte sich für Leber und Niere eine ähnliche Anreicherungskinetik mit einer maximalen Aktivität von 1,0 - 1,5 %ID/g. Die Anreicherung der Verbindung im Gehirn ergab eine hohe Hirnaufnahme von ca. 0,7 %ID/g, die für einen hirngängigen PET-Liganden gut ist. Die Aktivitätsanreicherung im Blut dagegen betrug maximal 0,2 %ID/g, was ein gutes Aktivitätsverhältnis Hirn/Blut erwarten lässt. Knochen 6 4 3 2 18 [K+⊂2.2.2]18F MeCN; 85 °C; 20 min F-Aktivität [% iD/g] 5 OTs 1 0 0 O O O 20 30 40 50 60 70 80 90 Zeit p.i. [min] N H 18 10 Abb.4: Biodistribution von [18F]FP im Knochen N F Abb.2: Reaktionsschema der 18F-Fluorierung des Markierungsvorläufers des [18F]FP Die Reaktionslösung wurde anschließend in Wasser aufgenommen, mittels HPLC gereinigt, auf einer Strata X Kartusche fixiert und mit wenig Ethanol eluiert. Das Lö- Die Aktivitätsanreicherung im Knochen dagegen stieg stetig an bis auf ein Maximum von 6 %ID/g, was auf eine teilweise Freisetzung des 18F-Fluors in Form von [18F]Fluorid hindeutet: Literatur: [1] Diplomarbeit A. Gleich, Institut für Kernchemie, 2000 [2] D. Stark et al., Jahresbericht 2003, Artikel B5