Synthese und Evaluierung von neuen Derivaten als potentielle
Werbung

Synthese und Evaluierung von neuen Derivaten als potentielle Kandidadaten
zur molekularen Bildgebung des NMDA-Rezeptors mit Fluor-18
T. Betzel1, M. Piel1, T. Capito1, C. Edinger2, G. Dannhardt2, F. Rösch1
Institut für Kernchemie1, Institut für Pharmazie2, Johannes Gutenberg-Universität, 55128 Mainz
Einleitung: Der N-Methyl-D-aspartat (NMDA)Rezeptor ist an einer Vielzahl von neuroexzitatorischen
Vorgängen beteiligt und spielt eine wichtige Rolle bei
neurologischen Fragestellungen.
Experimentelles: Angelehnt an Leitstrukturen, die eine
hohe Affinität zur Strychnin-insensitiven Bindungsstelle
zeigen, wurden zwei potentielle Referenz-Liganden
dargestellt, die auf ihre Eignung zur Visualisierung des
NMDA Rezeptors getestet werden sollen. In einer 8stufigen Synthese wurde eine Imidazolidin-substituierte
Indol-carbonsäure dargestellt1, bei der an einer phenolischen Hydroxygruppe ein Fluorethylrest mit Hilfe von
1,2-Brom-fluorethan eingeführt wurde. Parallel dazu
wurde in einer 7-stufigen Synthese ein Chinolin-2-onDerivat aufgebaut2, welches ebenfalls an einer phenolischen Hydroxyfunktion fluorethyliert wurde.
Ihre Fluor-18 markierten Analoga [18F]4,6-Dichloro-3{3-[4-(2-fluor-ethoxy)-phenyl]-2-oxo-imidazolidin-1ylmethyl}-1H-indol-2-carbonsäure ([18F]TBI-1) und
[18F]7-Chlor-3-{3-[4-(2-fluor-ethoxy)-phenoxy]phenyl}-4-hydroxy-1H-chinolin-2-on ([18F]TBC-1), vgl.
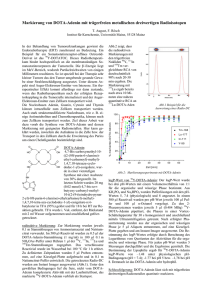
Abb. 1, sind vielversprechende Kandidaten, um den
NMDA-Rezeptor mittels PET zu visualisieren. Von
beiden inaktiven Referenzverbindungen wurde der
logP-Wert mit der HPLC-Methode bei einem pH von
7,3 unter physiologischen Bedingungen (SörensenPuffer) als Maß für die Lipophilie der Substanz bestimmt, um eine Aussage über das Passieren der BlutHirn-Schranke zu treffen.
Ergebnisse: Es wurde der logP-Wert von TBI-1E, TBI1 und TBC-1 zu 3,45, 1,31 und 0,34 bestimmt. Auffällig
ist der der niedrige logP-Wert für TBC-1. Er deutet darauf hin, dass die Substanz recht hydrophil ist. Der logPWert von TBI-1E wurde bestimmt, falls die freie Säure,
welche essentiell für die Bindung ist, nicht die BlutHirn-Schranke passieren sollte. Hierzu sollte der entsprechende Ethylester in der Lage sein und durch Esterasen im Hirn sollte die Carbonsäure freigelegt werden.
Parallel dazu gibt es auch andere Transportvorgänge in
das Gehirn, so dass der logP-Wert nur ein Richtwert ist.
Ausblick: Im nächsten Zug sollen die in vitroAffinitäten der inaktiven Referenzverbindungen über
die Verdrängung des tritiierten Liganden [3H]MDL105,519 an präparierten Ratten- oder Schweinehirnmembranen erfolgen. Zeitgleich soll eine Variation des
Fluorethylrests im aromatischen Teil von TBI erfolgen,
siehe Abb. 1. Auf Grund der niedrigen logP-Werte wird
angestrebt, die Struktur durch die Einführung eines alternativen Strukturelements dahingehend zu modifizieren (TBV-1).3
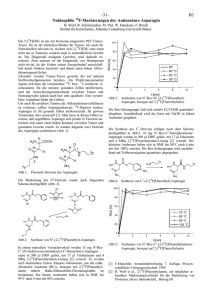
Abb. 1: Überblick der Referenzverbindungen
Struktur
R
Name
O
Cl
N
N
R
O
TBI-1E
COOEt
F
N
H
Cl
O
TBI-1
F
O
Cl
N
N
TBI-2
R
O
F
COOH
N
H
Cl
TBI-3
O
F
O
OH
F
O
Cl
N
H
TBC-1
O
O
H
N
Cl
TBV-4
O
COOH
Cl
F
N
H
Literatur
1
M. Jansen et. al.; Hydantoin-Substituted 4,6Dichloroindole-2-carboxylic Acids as Ligands with High
Affinity for the Glycine Binding Site of the NMDA Receptor; J. Med. Chem. 2003, 46, 64-73
2
A. Kreimeyer et. al.; Evaluation and Biological Properties
of Reactive Ligands for the Mapping of the Glycine Site
on the N-Methyl-D-aspartarte (NMDA) Receptor; J. Med.
Chem. 1999, 42, 4394 – 4404
3
Romano Di Fabio et al.; Substituted Indole-2-carboxylates
as in Vivo Potent Antagonists Acting as the StrychnineInsensitive Glycine Binding Site, J. Med. Chem. 1997, 40,
841-850