Neue Technologie zum raschen Nachweis aller therapierelevanten
Werbung

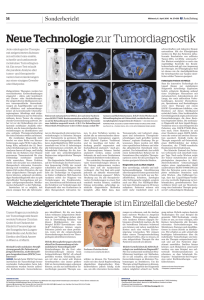
Pharma Report Molekulare Diagnostik beim nicht-kleinzelligen Bronchialkarzinom Neue Technologie zum raschen Nachweis aller therapierelevanten Genanomalien © Springer-Verlag GmbH Grundlage jeder zielgerichteten Tumortherapie ist eine exakte, schnelle und umfassende molekulare Tumordiagnostik. Da immer mehr therapeutisch relevante Genveränderungen im nicht-kleinzelligen Lungenkarzinom (NSCLC) entdeckt werden, steigen auch die Anforderungen an die molekulare Tumordiagnostik. Dank einer neuen Technologie ist jetzt ein diagnostischer Test verfügbar, der parallel alle therapierelevanten genomischen Veränderungen an kleinsten Gewebemengen oder an einer einzigen Blutprobe nachweist. Impressum „Neue Technologie zum raschen Nachweis aller therapierelevanten Genanomalien“ Literaturarbeit Redaktionelle Mitarbeit: Dr. Katharina Arnheim, Freiburg i. Br. Corporate Publishing (verantwortlich): Ulrike Hafner, Dr. Michael Brysch, Dr. Katharina Finis, Dr. Friederike Holthausen, Sabine Jost, Ann Köbler, Dr. Claudia Krekeler, Inge Kunzenbacher, Dr. Christine Leist, Dr. Sabine Lohrengel, Dr. Ulrike Maronde, Dr. Monika Prinoth, Dr. Annette Schilling, Yvonne Schönfelder, Dr. Petra Stawinski, François Werner, Teresa Windelen Report in „Der Pneumologe“ Band 12, Heft 6, November 2015 Mit freundlicher Unterstützung der NEO New Oncology AG, Köln Die Herausgeber der Zeitschrift übernehmen keine Verantwortung für diese Rubrik. Springer Medizin Springer-Verlag GmbH Tiergartenstraße 17, 69121 Heidelberg Springer ist Teil der Fachverlagsgruppe Springer Science + Business Media © Springer-Verlag Berlin Heidelberg 2015 Die Wiedergabe von Gebrauchsnamen, Handelsnamen, Warenbezeichnungen usw. in dieser Zeitschrift berechtigt auch ohne besondere Kennzeichnung nicht zu der Annahme, dass solche Namen im Sinne der Warenzeichen- und Markenschutz-Gesetzgebung als frei zu betrachten wären und daher von jedermann benutzt werden dürfen. Für Angaben über Dosierungsanweisungen und Applikationsformen kann vom Verlag keine Gewähr übernommen werden. Derartige Angaben müssen vom jeweiligen Anwender im Einzelfall anhand anderer Literaturstellen auf ihre Richtigkeit überprüft werden. Derzeit erkranken in Deutschland jährlich mehr als 50.000 Menschen an Lungenkrebs [1] die meisten davon (80–85 %) am nicht-kleinzelligen Lungenkarzinom (NSCLC). Durch zielgerichtete Medikamente hat sich die Prognose für viele dieser Patienten in den letzten Jahren deutlich verbessert. Die Behandlung ist dann besonders effektiv, wenn die Wahl der zielgerichteten Therapie auf Basis genetischer Tumormerkmale erfolgt [2]. So zeigen Patienten mit einer aktivierenden EGFR (Epidermal growth factor receptor)-Mutation unter der Behandlung mit einem Tyrosinkinaseinhibitor (TKI) ein deutlich verlängertes progressionsfreies Überleben im Vergleich zur Chemotherapie [3]. Eine aktivierende KRAS-Mutation hingegen ist äußerst selten vergesellschaftet mit einer „druggable“ Mutation [3, 4]. Patienten mit nachgewiesener ALK (Anaplastic lymphoma kinase)-Translokation profitieren von der Behandlung mit dem ALK-TKI Crizotinib, der in klinischen Studien erfolgreich auch zur Therapie von Patienten mit ROS1-Translokation oder MET-Amplifikation eingesetzt wird [5–7]. Patienten mit einer Amplifikation des HER2-Rezeptors sprechen hingegen in bis zu 50 % aller Fälle auf die Behandlung mit HER2-Inhibitoren wie Trastuzumab an [8]. Zahlreiche weitere zielgerichtete Wirkstoffe sind in der fortgeschrittenen klinischen Testung [9–12]. Zudem gewinnen Immuncheckpoint-Inhibitoren wie Nivolumab (monoklonaler Antikörper gegen PD-1) an Bedeutung in der Behandlung des NSCLC [13, 14], wobei diese Inhibitoren bei Tumoren mit hoher Mutationslast besonders wirksam zu sein scheinen [15]. Um Patienten mit histologisch gesicherter NSCLC-Diagnose eine optimierte Therapie bieten zu können, ist es angesichts der vielen verfügbaren Wirkstoffe notwendig, den Tumor molekularpathologisch auf individuelle Genveränderungen zu untersuchen. Eine exakte, schnelle und umfassende molekulare Tumordiagnostik ist auch dann erforderlich, wenn Resistenzen unter einer Therapie auftreten, die eine neue Therapiestrategie erfordern. So sind die Punktmutation T790M im EGFR-Gen oder die Amplifikation des MET-Gens mit einer Resistenz gegen bestimmte EGFR-TKI assoziiert [16]. Diese Resistenzmutationen wiederum können mit neueren zielgerichteten Wirkstoffen erfolgreich behandelt werden [17]. In den nächsten Jahren ist mit der Identifizierung weiterer Genveränderungen und Resistenzme- chanismen beim Lungenkarzinom zu rechnen, die mit neuen zielgerichteten Medikamenten behandelbar sind. Damit werden auch die Anforderungen an die molekulare Diagnostik steigen. Bisherige Diagnosemethoden auf Dauer unzureichend Gerade beim Lungenkarzinom stößt die molekulare Diagnostik bei begrenztem Probenmaterial an ihre Grenzen. Die Einzelgen­ analytik mittels FISH (Fluoreszenz-in-situ-Hybridisierung)-Analyse und IHC (Immunhistochemie) benötigt Tumormaterial, das mit Nadel- oder Stanzbiopsien oftmals nicht in ausreichender Menge gewonnen werden kann. In etwa 30 % aller Fälle kann die molekulare Diagnostik beim Lungenkarzinom daher nicht erfolgreich für alle molekularen Marker abgeschlossen werden [2]. Da dem Patienten eine erneute belastende Biopsie selten zugemutet werden kann, wird in diesen Fällen kein diagnostischer Befund er- NOWEL: heimatnahe Versorgung von Patienten mit Lungenkrebs Im Netzwerk Nord-Ost-West-Lunge (NOWEL) haben sich regionale Experten aus den Bereichen Onkologie, Pneumologie und Pathologie zusammengeschlossen, um im norddeutschen Raum eine flächen­ deckend zugängliche optimale Versorgung von Lungenkrebspatienten ­sicherzustellen. Ziel ist es, dem Patienten die Neuerungen der evidenzbasierten, personalisierten Tumortherapie auf wissenschaftlich hohem Niveau durch eine interdisziplinäre und sektorenübergreifende Zusammenarbeit anzubieten. Ein Schwerpunkt von NOWEL liegt in der Versorgungsforschung: Durch eine umfassende qualitätsgesicherte Nutzenanalyse soll dazu beigetragen werden, diagnostische und therapeutische Versorgungskonzepte zu verbessern. Pharma Report stellt, wodurch dem Patienten womöglich die Chance auf eine effektive zielgerichtete Therapie verwehrt wird. Dieses Problem wird sich durch die Zunahme der therapierelevanten genetischen Alterationen noch verschärfen: Zwar können in der Routinediagnostik Punktmutationen mit schnellen und zuverlässigen PCR-basierten Methoden nachgewiesen werden, viele der neu entdeckten therapierelevanten Veränderungen sind jedoch Translokationen (z. B. RET, ROS1) und Kopienzahlveränderungen (z. B. HER2, MET), die sich derzeit nur mit zeit- und materialintensiven FISH- und IHC-Analysen nachweisen lassen. „Hybrid Capture“-basierte ­Tumordiagnostik Mit der NEO-Plattform steht seit Kurzem ein molekulardiagnostischer Test zur Verfügung, mit dem sich das gesamte Spektrum klinisch relevanter genomischer Veränderungen – Mutationen, Insertionen, Deletionen, Kopienzahlveränderung und Translokationen – zuverlässig und schnell nachweisen lässt [18]. Als Ausgangsmaterial eignen sich kleinste Mengen von paraffineingebettetem oder zytologischem Material und sogar Blutproben. Der Test basiert auf der Technologie des „Hybrid Capture-based Next Generation Sequencing“: Zunächst werden alle therapierelevanten Genregionen mithilfe von komplementären Sonden aus dem Gesamtgenom des Tumors angereichert. Anschließend werden die Zielregionen klonal amplifiziert und mittels „Next Generation Sequencing (NGS)“ ausgelesen. Die klonale Amplifikation ermöglicht es, auch niedrigfrequente Genvarianten verlässlich zu detektieren und die Allelfrequenz festzustellen. Der Mutationsstatus wird quantitativ erfasst und mutierte Allele werden auch vor einem hohen Hintergrund sensitiv detektiert. Da auch intronische Regionen mit bekannten genomischen Bruchpunkten angereichert werden, können auch Trans- NEOlung-Studie: Gewebesparende Diagnostik und breiterer Einsatz zielgerichteter Therapien Kommentar von Prof. Dr. Frank Griesinger, Direktor der Klinik für Hämatologie und Onkologie am Pius Hospital Oldenburg und Leiter der Studie „Die Behandlung von Patienten mit Lungenkarzinom ist mit der Entdeckung molekularer Alterationen und der Verfügbarkeit von zielgerichteten Therapien wie EGFR-, ALK-, ROS1- und weiteren Tyrosinkinaseinhibitoren komplexer und effektiver geworden. Eine umfassende, gewebesparende Diagnostik, die alle genetischen Alterationen inklusive Amplifikationen (relevant u. a. bei HER2, c-MET) und Translokationen (relevant u. a. bei ALK und ROS1) in einem Ansatz erfasst, bietet die Möglichkeit, bei mehr Patienten eine zielgerichtete Therapie durchzuführen. Diese Chance sehen wir in der innovativen ‚Hybrid Capture‘-basierten NGS-Technologie. Besonders interessant sind die Ansätze der ‚Liquid Biopsy‘, die bei einer gesicherten Tumorerkrankung gewebesparend und nicht invasiv genetische Charakteristika detektieren und auch die ggf. therapeutisch relevante genetische Heterogenität von unterschied­lichen Tumormanifestationen in einem Patienten adressieren kann. Daher freuen wir uns, im Netzwerk NOWEL diese Methodik bei mehreren Registerprojekten einsetzen zu können, unabhängig von noch bestehenden Hürden der Diagnostik im stationären Bereich. Weitere Registerprojekte zur molekularen Diagnostik, die die bestehenden Netzwerke einbinden und Synergien schaffen werden, sind im Rahmen von CRISP, einem deutschlandweiten Register mit Beginn 4. Quartal 2015, geplant.“ lokationen zuverlässig nachgewiesen werden. Die gewonnenen Sequenzierdaten werden bioinformatisch ausgewertet, um die Treibermutationen von klinisch irrelevanten Passenger-Mutationen abzugrenzen. Das Verfahren hat den Vorteil, dass alle therapierelevanten genomischen Veränderungen in einem einzigen Test gemessen werden können. FISH- bzw. IHC-Analysen oder PCR-basierte Sequenzierungen sind damit nicht mehr erforderlich. Zudem können neu identifizierte diagnostisch relevante Genveränderungen jederzeit problemlos aufgenommen werden, um der aktuellen klinischen Forschung Rechnung zu tragen. Flüssigbiopsie: Diagnostik aus dem Blut Mit dem NEOliquid-Test gibt es inzwischen auch ein „Hybrid Capture“-basiertes Verfahren, mit dem klinisch relevante genomische Veränderungen an der zell- freien, zirkulierenden Tumor-DNA (ctDNA) aus dem Blut von Krebspatienten analysiert werden können. Belastende Biopsien oder Bronchoskopien lassen sich somit teilweise vermeiden. Die Flüssigbiopsie ermöglicht darüber hinaus eine regelmäßige Kontrolle des Krankheitsverlaufs, sodass die Tumorentwicklung unter Therapie beobachtet, mögliche Resistenzen frühzeitig erkannt und die Behandlung gegebenenfalls angepasst werden können. Registerstudie zur Molekulardiagnostik Vor Kurzem wurde die prospektive nicht-interventionelle Registerstudie NEOlung (Molecular NEO diagnostics in patients with lung cancer) zum molekularen Screen­ing von Lungenkrebs-Patienten begonnen. Etwa 1.500 Patienten mit fortgeschrittenem oder metastasiertem NSCLC sowie nicht kurativ zu behandelndem kleinzelligem Lungenkarzinom (SCLC) er- halten im Rahmen des Netzwerks ­NOWEL direkten und schnellen Zugang zu einer umfassenden molekularen Diagnostik. Das Registerprojekt soll FFdas Spektrum der therapeutisch nutzbaren genetischen Veränderungen erfassen, FFdie Effektivität der Therapie mit zielgerichteten Substanzen in verschiedenen Therapie­ linien dokumentieren sowie FFden Verlauf der Tumorerkrankung und das Auftreten von Resistenzen im klinischen Alltag prospektiv erfassen. Die Studie beinhaltet außerdem den Vergleich mit diagnostischen Standardmethoden und den Abgleich zwischen diagnostisch verwertbaren Daten aus Gewebe und aus Blut. Literatur 1. World Health Organisation, International Agency for Research on Cancer, EUCAN, http://eco.iarc.fr/eucan/ Cancer.aspx?Cancer=18 (Zugriff: 09.10.2015) 2. The Clincal Lung Cancer Genome Project (CLCGP) and Network Genomic Medicine (NGM), Science Translational Medicine 2013, 5:209ra153 3. Mok TS et al., N Engl J Med 2009, 361:947–957 4. Pao W et al., PLoS Medicine 2005, 2:57–61 5. Shaw AT et al., N Engl J Med 2013, 368:2385–2394 6. Mazières J et al., J Clin Oncol 2015, 33:992-999 7. Schwab R et al., Lung Cancer 2014, 83:109–111 8. Mazières J et al., J Clin Oncol 2013, 31:1997–2003 9. Sánchez-Torres JM et al., Transl Lung Cancer Res 2013, 2:244–250 10. Drilon A et al., Cancer Discov 2013, 3:630–635 11. Xu C et al., Mol Cancer Ther 2015, 14:2382–2389 12. Vansteenkiste JF et al., J Thorac Oncol. 2015, 10:1319–1327 13. Spigel DR et al., ASCO 2015, Abstr. 8009 14. Paz-Ares L et al., ASCO 2015, Abstr. LBA109 15. Rizvi NA et al., Science 2015, 348:124– 128 16. Godin-Heymann N et al., Mol Cancer Ther 2008, 7:874–879 17. Gautschi O et al., J Thorac Oncol 2015, Epub ahead of print 18. Heuckmann JM, Thomas RK, Ann Oncol 2015, 26:1830–1837