Transkriptlevel-Bestimmung in der Buche
Werbung

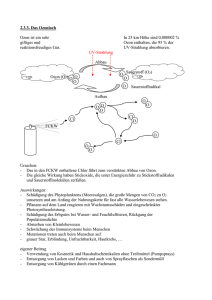
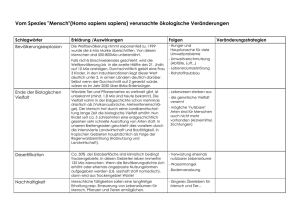
709_761_BIOsp_0709.qxd 30.10.2009 9:58 Uhr Seite 747 747 Mikroarrays Transkriptlevel-Bestimmung in der Buche MAREN OLBRICH 1 , GERHARD WELZL 2 , JANA BARBRO WINKLER 3 , KARL -HEINZ HÄBERLE 4 , DIETER ERNST 1 1 INSTITUT FÜR BIOCHEMISCHE PFLANZENPATHOLOGIE, HELMHOLTZ ZENTRUM MÜNCHEN 2 INSTITUT FÜR ENTWICKLUNGSGENETIK, HELMHOLTZ ZENTRUM MÜNCHEN 3 INSTITUT FÜR BODENÖKOLOGIE, HELMHOLTZ ZENTRUM MÜNCHEN 4 LEHRSTUHL FÜR ÖKOPHYSIOLOGIE DER PFLANZEN, TECHNISCHE UNIVERSITÄT MÜNCHEN Ozonstress verändert die Transkriptebene von Pflanzen. Mit einem cDNA-Array wurden für die Europäische Buche (Fagus sylvatica L.) die Interaktion Pflanze-Stressor und die Gen-Reprogrammierung untersucht und die Ergebnisse durch quantitative Real-Time-PCR verifiziert. Ozone stress leads to changes upon transcriptional level of plants. For European beech (Fagus sylvatica L.), DNA array technology detects interaction between plant stress and gene changes. Results were verified with quantitative real-time PCR. Pflanzliche Reaktion auf Ozon ó Ozon ist als abiotischer Elizitor bei krautigen Pflanzen bekannt und löst die Induktion Abwehr-verwandter Gene aus [1]. Bei holzigen Pflanzen wurde ein Ozon-induzierter „Memory-Effekt“ mit verspäteten Symptomentwicklungen und persistenten biochemischen Antworten beobachtet [2]. Je nach Dauer, Intensität und Konzentration der Ozongabe sowie Empfindlichkeit und Entwicklungsstadium der Pflanzen werden sie entweder anfälliger oder resistenter gegen weitere Stressoren wie Pathogene [2]. So verfrühte die Exposition von jungen Buchen im Freiland mit zweifach ambienten Ozonkonzentrationen deren Seneszenz [3, 4], adulte Buchen im Waldbestand unter denselben Ozonbedingungen zeigten hingegen kaum veränderte Transkripte [5]. Ozon dringt über die Stomata in das Blatt ein, im interzellularen Raum zersetzt es sich relativ schnell. In wässriger Lösung führt es zur Bildung von reaktiven Sauerstoffspezies (ROS) (Abb. 1). Sekundär entstehen durch die Reaktion von Ozon mit Zellwand-gebundenen phenolischen Gruppen äußerst reaktive Hydrogenradikale. Bei der Reaktion mit Plasmamembranlipiden und -proteinen kommt es BIOspektrum | 07.09 | 15. Jahrgang zur Bildung organischer Peroxide. Innerhalb weniger Stunden nach subakuter Ozonexposition bilden sich Signalmoleküle (Ethylen, Zellwand Salicylsäure und Jasmonsäure), ROS, Pathogen-verwandte (PR)-Proteine und antioxidative Verbindungen. Ferner kommt es zur Aktivierung des Polyaminmetabolismus, der Polyphenol- und der Ligninbiosynthese [6]. Bestimmung von Transkriptkonzentrationen über einen cDNA-Mikroarray und Ergebnisverifizierung mittels quantitativer Real-Time-PCR (qRT-PCR) Über eine suppressive subtraktive Hybridisierung (SSH) wurden Ozon-regulierte ESTs (expressed sequence tags) isoliert, daraus wurde eine cDNA-Bank erstellt [7]. Die ESTs wurden mittels PCR amplifiziert, gereinigt und auf einen Aldehyd-beschichteten Objektträger (Slide) gebracht (Abb. 2). Nur qualitativ hochwertige RNA sollte für Mikroarray-Analysen sowie für die qRT-PCR zur Erstellung der cDNA verwendet werden. Mithilfe von Superscript III Reverse Transkriptase wurde die RNA bei 42 °C in cDNA umgeschrieben. Für die Mikroarray-Analysen Ozon Stomata Ozon und sekundäre Produkte Phenolische Gruppen, ungesättigte Komponenten, Amide Ethylen, ACC ROSJasmonat Salicylsäure, Methylsalicylate ROS Antioxidative Stoffe Signalkette Lipidperoxidation Rezeptoren Plasmamembran „oxidative burst“ Signalkette Hemmung der Photosynthese Pigmentverlust Chloroplast Kinasekaskade Proteinaktivierung Spezifische mRNA Bildung Geninduktion/ -repression Zytoplasma Zellkern Abwehrantwort Anitoxidative Verbindungen, Polyamine, Polyphenole, Ligninbiosynthese, PR-Proteine Veränderter metabolischer Status Erhöhte Anfälligkeit oder Resistenz für nachfolgenden Stress Wachstumshemmung, Sichtbare Symptome ˚ Abb. 1: Ozon-induzierte Abwehrantwort im Gewebe einer Pflanzenzelle (modifiziert nach [2]). 709_761_BIOsp_0709.qxd 748 30.10.2009 9:58 Uhr Seite 748 W I S S E N SCH AFT · S P E C I A L : P C R Referenzgene und Primer-Effizienz Herstellung der SS H-Bank Buchenblätter Sequenzierung der Klone RNA isolieren Einteilung der ESTs in funktionelle Gruppen cDNA-Herstellung durch RT-PCR Klonausw ahl und Plasm idpräparation Labeln mit Cy-3 und C y-5 Amplifizierungs-PCR m it modifizierten M 13-Primern Reinigung des Ansatzes Reinigung und Kontrolle der PC R-Produkte (cDNA) Auf Array auftragen Spotten Blocken Prähybridisieren und w aschen Hybridisierung für mindes tens 18 h W aschen der Slides Scannen Ausw ertung über GenePixPro und Acuity ˚ Abb. 2: Arbeitsablauf zur Erstellung des Buchen-cDNA-Mikroarrays. wurden Oligo-dT-Primer und für die qRT-PCR Random-Hexamerprimer eingesetzt. Die qRT-PCR-Spezifität wurde über die Anwendung spezifischer Primer erreicht, deren Sequenzen aus Datenbanken entnommen wurden. Für den Mikroarray wurden die cDNAs der Kontrollbuchen mit grün- und die der Ozonbehandelten Buchen mit rot-fluoreszierendem Farbstoff markiert. Die markierte cDNA der zusammengehörigen Kontroll- und Testbuchen wurde auf einen Slide gegeben, wobei gleiche cDNA an das entsprechende PCRFragment des Slides hybridisierte. Das von einem Scanner ermittelte Farbsignal des Fluoreszenzfarbstoffs erlaubte die Bestimmung der Transkriptgehalte der Test- relativ zu den Kontrollbuchen (Abb. 2). Die Transkriptmenge der qRT-PCR wurde mittels Comparativer Ct-Methode, unter Benutzung der Formel 2–CtBehandlung –CtKontrolle , errechnet. Dabei werden die Ct-Werte von Kontroll- und Testmaterial durch ein Referenzgen normalisiert, welches während der qRT-PCR-Reaktion mitgeführt wird. Die Software Primer Express 2.0 (Applied Biosystems, Darmstadt) erlaubte das Primerdesign unter Beachtung der folgenden Faktoren: (1) Primerlänge von 10 bis 30 bp; (2) Länge des Amplifikates von 50 bis 100 bp; (3) keine Anhäufung der Base Guanin in den Primern; (4) weniger als zwei Guaninund/oder Cytosin-Basen am 3’-Ende des Nukleotids. Am Blattmaterial der Buche wurden verschiedene allgemein benutzte Referenzgene getestet und die Buchen verschiedenen Stressoren wie erhöhtem Ozon, erhöhtem CO2, Pathogeninfektion mit dem Wurzelpathogen Phytophthora citricola ausgesetzt sowie der Einfluss der Blattmorphologien (Sonnen- versus Schattenblatt) untersucht (Tab. 1). Die Probennahme erfolgte zu zwei Zeitpunkten, für jeden Zeitpunkt wurde ein neues Referenzgen zur Normalisierung ermittelt [8]. Ob die jeweilige Behandlung den Transkriptgehalt des Referenzgens beeinflusst, wurde mittels Varianzanalyse geprüft. Bei Buchen unterschiedlichen Alters und Genotyps, die unter verschiedenen Umweltbedingungen standen, können die Transkriptgehalte sehr unterschiedlich ausfallen. Deswegen wurde der Faktor „Baum“ in die statistische Analyse einbezogen und ein lineares Modell mit gemischten Effekten angewendet [9, 10]. Bei der Anwendung der Comparativen CtMethode ist die annähernd gleiche PrimerEffizienz von Ziel- und Referenzgen wichtig. Dafür wurde eine Templateverdünnung erstellt und die Regressionskoeffizienten für die verschiedenen Gene errechnet. Die Proben stammten aus den Versuchen und wurden unter denselben Bedingungen gemessen wie die Versuchsproben. Ergebnisse Die 18S rRNA, die oft als Referenzgen für die qRT-PCR von Pflanzenmaterial eingesetzt wird, zeigte in unserer Studie allerdings 12 Tage nach der Infektion mit P. citricola einen veränderten Transkriptgehalt. Die mRNAKonzentrationen von GAPDH1 (31 Stunden nach der Infektion mit P. citricola, Sonnenund Schattenblätter am 19.09.05), GAPDH2 (CO2-Behandlung am 01.05.05 und am Tab. 1: Beeinflussung der getesteten Referenzgene durch die verschiedenen Behandlungen bzw. der Einfluss der unterschiedlichen Blattmorphologien. Gen CO2 n=6 P. citricola n=6 31 Stunden 12 Tage 01.05.05 10.5.05 18S rRNA 0,1079 0,1019 0,0822 Aktin 0,3812 0,1974 GAPDH1 0,5582 GAPDH2 Ozon n=5 Sonnen-/Schattenblätter n=5 12.05.05 19.09.05 27.07.05 29.08.05 0,0458 0,7768 0,1819 0,2565 0,3977 0,2752 0,6422 0,1038 0,3249 0,1295 0,9942 0,3464 0,0398 0,8910 0,3686 0,6691 0,4078 0,0255 <0,0001 <0,0001 1,0000 0,5685 0,0082 0,5062 0,5164 0,9726 α -Tubulin 0,0203 0,0572 1,0000 0,7995 0,7976 0,8549 0,2947 0,4366 ubiquitin-like protein 0,0304 0,0024 0,9841 0,3675 0,8896 0,7622 0,3897 0,9440 Aufgetragen ist der jeweilige p-Wert, der unter Anwendung des linearen Modells mit gemischten Effekten aus der ANOVA-Tabelle entnommen wurde (rot = signifikante Beeinflussung) [8]. BIOspektrum | 07.09 | 15. Jahrgang 709_761_BIOsp_0709.qxd 30.10.2009 9:58 Uhr Tab. 2: Bestimmung der Primer-Effizienz durch Ermittlung des Regressionskoeffizienten [8]. Gene Regressionskoeffizient 18S rRNA 0,9968 Aktin 0,9975 GAPDH1 0,9999 GAPDH2 0,3975 α -Tubulin 0,9999 ubiquitin-like protein 0,0122 Die Regression wurde aus den gemessenen CtWerten und der jweiligen Verdünnungsstufe (1:128 bis 1:4) ermittelt. 10.05.05), α-Tubulin (CO2-Behandlung am 01.05.05) und ubiquitin-like protein (CO2Behandlung an beiden Probenahmetagen) waren durch die jeweiligen Behandlungen beeinflusst (Tab. 1). Aktin war das einzige unbeeinflusste Gen. Gute Effizienz wurde für 18S rRNA, Aktin, GAPDH1 und α-Tubulin ermittelt, wohingegen GAPDH2 und ubiquitin-like protein über keine gute Effizienz verfügten (Tab. 2). Seite 749 [4] Winkler JB, Lang H, Graf W et al. (2009) Experimental setup on field lysimeters for studying effects of elevated ozone and below-ground pathogen infection on a plant-soil-system of juvenile beech (Fagus sylvatica L.). Plant Soil DOI 10.1007/ s11104-009-9936-x [5] Olbrich M, Gerstner E, Welzl G et al. (2009) Transcriptional signatures in leaves of adult European beech trees (Fagus sylvatica L.) in an experimentally enhanced free air ozone setting. Environ Pollut DOI:10.1016/j.envpol.2009. 08.001 [6] Sandermann H, Ernst D, Heller W et al. (1998) Ozone: an abiotic elicitor of plant defence reactions. Trends Plant Sci 3:47–50 [7] Olbrich M, Betz G, Gerstner E et al. (2005) Transcriptome analysis of ozone-responsive genes in leaves of European beech (Fagus sylvatica L.). Plant Biol 7:670–667 [8] Olbrich M, Gerstner E, Welzl G et al. (2008) Quantification of mRNAs and housekeeping gene selection for quantitative real-time RT-PCR normalization in European beech (Fagus sylvatica L.) during abiotic and biotic stress. Naturforsch C 63:574–582 [9] Pinheiro J, Bates D, DebRoy S et al. (2005) nlme: Linear and nonlinear mixed effects models. R package version 3.1-66 [10] RDevelopmentCoreTeam (2005) R Foundation for Statistical Computing. Wien, Österreich Korrespondenzadresse: Dr. Maren Olbrich Helmholtz Zentrum München Institut für Biochemische Pflanzenpathologie Arbeitsgruppe für Pflanzlichen abiotischen Stress Ingolstädter Landstraße 1 D-85674 Neuherberg Tel.: 089-3187-2719 Fax: 089-3187-3383 [email protected] Fazit Abhängig vom Gewebetyp und appliziertem Stress eignen sich mehrere Gene als Referenzgen für die qRT-PCR. Für die Buche kann das Aktin-Gen das Referenzgen der Wahl sein, da es durch keine Behandlung in dieser Studie beeinflusst war und eine gute Effizienz besaß. Allerdings wird die Transkriptkonzentration von Pflanzengenen durch viele Faktoren beeinflusst. Deswegen sollte für jedes Experiment ein geeignetes Referenzgen ermittelt werden. AUTOREN 1 2 3 4 Dr. Maren Olbrich3 ist wissenschaftliche Mitarbeiterin am Helmholtz Zentrum München im Institut für Biochemische Pflanzenpathologie in der Arbeitsgruppe für Pflanzlichen Abiotischen Stress von Dr. Ernst. Dr. Jana Barbro Winkler4 ist wissenschaftliche Mitarbeiterin am Helmholtz Zentrum München in der Abteilung für Experimentelle Umweltsimulation und stellvertretende Abteilungsleiterin. Dr. Gerhard Welzl1 ist Teamleiter Biostatistik am Institut für Entwicklungsgenetik. Dr. KarlHeinz Häberle5 ist wissenschaftlicher Mitarbeiter am Lehrstuhl für Ökophysiologie der Pflanzen der TU München. Dr. Dieter Ernst2 ist Leiter der Arbeitsgruppe für Pflanzlichen Abiotischen Stress am Helmholtz Zentrum München und stellvertretender Institutsleiter am Institut für Biochemische Pflanzenpathologie. 5 Danksagung Dank gilt der Deutschen Forschungsgesellschaft, die den Sonderforschungsbereich 607 „Wachstum und Parasitenabwehr“ unterstützt. ó Literatur [1] Langebartels C, Schraudner M, Heller W et al. (2002) Oxidative stress and defense reactions in plants exposed to air pollutants and UV-B radiation. In: Inzé D, Van Montagu (eds) Oxidative Stress in Plants. Taylor & Francis, London, 105–135 [2] Sandermann H (2000) Ozone/biotic disease interactions: molecular biomarkers as a new experimental tool. Environ Pollut 108:327–332 [3] Olbrich M, Gerstner E, Welzl G et al. (2009) Transcript responses in leaves of ozone-treated beech saplings at an outdoor free air fumigation site over two growing seasons. Plant Soil 323:61–74 BIOspektrum | 07.09 | 15. Jahrgang Darmstadt hat eine weitere Topadresse: AppliChem GmbH Ottoweg 4 64291 Darmstadt Fon 0049 6151/93 57-0 Fax 0049 6151/93 57-11 [email protected] www.applichem.com