Berechnung von Kraftkonstanten an Thio
Werbung
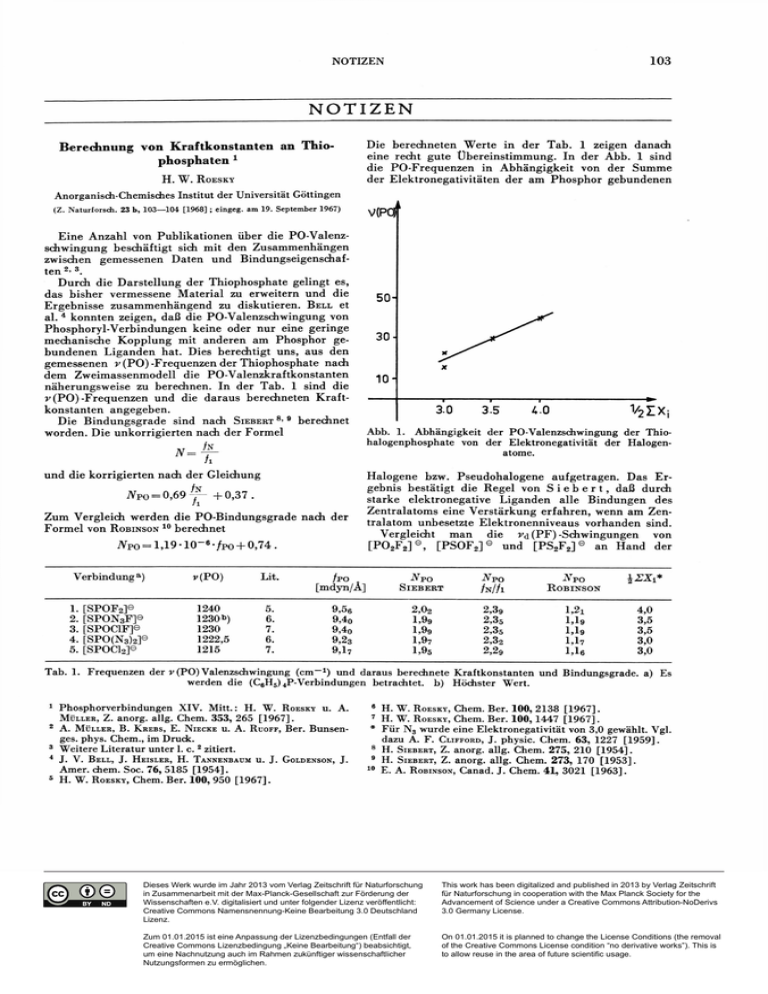
NOTIZEN Die berechneten Werte in der Tab. 1 zeigen danach eine recht gute Ubereinstimmung. In der Abb. 1 sind die PO-Frequenzen in Abhängigkeit von der Summe der Elektronegativitäten der am Phosphor gebundenen Berechnung von Kraftkonstanten an Thiophosphaten 1 H. W. ROESKY Anorganisch-Chemisches Institut der Universität Göttingen ( Z . N a t u r f o r s c h . 2 3 b , 1 0 3 — 1 0 4 [ 1 9 6 8 ] ; e i n g e g . a m 19. S e p t e m b e r 1967) VtPOf Eine Anzahl von Publikationen über die PO-Valenzschwingung beschäftigt sich mit den Zusammenhängen zwischen gemessenen Daten und Bindungseigenschaften 2- 3 . Durch die Darstellung der Thiophosphate gelingt es, das bisher vermessene Material zu erweitern und die Ergebnisse zusammenhängend zu diskutieren. B E L L et al. 4 konnten zeigen, daß die PO-Valenzschwingung von Phosphoryl-Verbindungen keine oder nur eine geringe mechanische Kopplung mit anderen am Phosphor gebundenen Liganden hat. Dies berechtigt uns, aus den gemessenen v (PO) -Frequenzen der Thiophosphate nach dem Zweimassenmodell die PO-Valenzkraftkonstanten näherungsweise zu berechnen. In der Tab. 1 sind die v (PO) -Frequenzen und die daraus berechneten Kraftkonstanten angegeben. Die Bindungsgrade sind nach S I E B E R T 8 ' 9 berechnet worden. Die unkorrigierten nach der Formel N-. /N_ h und die korrigierten nach der Gleichung iVpo = 0 , 6 9 ^ - + 0 , 3 7 . Ji Zum Vergleich werden die PO-Bindungsgrade nach der Formel von R O B I N S O N 10 berechnet iVpo = 1,19 • 10~ 6 -/PO + 0,74 . Verbindung a ) ] E 1. [SPOF 2. [ S P O N 3 F P 2 I>(PO) 3. [SPOC1F]© 4. [SPO(N3)2] 5. [SPOCI2P E 1240 1230b) 1230 1222,5 1215 Lit. 5. 6. 7. 6. 7. 50 30- 103.0 3.5 v2ix 4.0 Abb. 1. Abhängigkeit der PO-Valenzschwingung der Thiohalogenphosphate von der Elektronegativität der Halogenatome. Halogene bzw. Pseudohalogene aufgetragen. Das Ergebnis bestätigt die Regel von S i e b e r t , daß durch starke elektronegative Liganden alle Bindungen des Zentralatoms eine Verstärkung erfahren, wenn am Zentralatom unbesetzte Elektronenniveaus vorhanden sind. Vergleicht man die vn (PF) -Schwingungen von [ P 0 F ] , [ P S O F ] und [ P S F ] an Hand der 2 G 2 N fpo [mdyn/A] PO SIEBERT 9,56 9,40 9,40 9,23 9,17 2,02 1,99 1,99 1,97 1,95 2 q 2 2 9 NFO ATpo h/h ROBINSON 2,3g 2,35 2,35 2,32 2,29 L2I 1,1® 1,19 Llv 1,16 J R X I * 4,0 3,5 3,5 3,0 3,0 Tab. 1. Frequenzen der v (PO) Valenzschwingung ( c m - 1 ) und daraus berechnete Kraftkonstanten und Bindungsgrade, a) Es werden die (C6H5) 4 P-Verbindungen betrachtet, b) Höchster Wert. 1 Phosphorverbindungen X I V . Mitt.: H . W . ROESKY U . A . anorg. allg. Chem. 3 5 3 , 2 6 5 [ 1 9 6 7 ] . A . M Ü L L E R , B. K R E B S , E . N I E C K E U. A . R U O F F , Ber. Bunsenges. phys. Chem., im Druck. Weitere Literatur unter 1. c. 2 zitiert. MÜLLER, Z . 2 3 4 5 J . V . B E L L , J . H E I S L E R , H . TANNENBAUM U . J . GOLDENSON, Amer. ehem. Soc. 76, 5185 [1954]. H . W . ROESKY, Chem. Ber. 100, 9 5 0 J. 6 H. W . ROESKY, Chem. Ber. 100, 2 1 3 8 [ 1 9 6 7 ] . H. W . ROESKY, Chem. Ber. 1 0 0 , 1 4 4 7 [ 1 9 6 7 ] . * Für N 3 wurde eine Elektronegativität von 3,0 gewählt. Vgl. dazu A . F. C L I F F O R D , J . physic. Chem. 6 3 , 1 2 2 7 [ 1 9 5 9 ] . 8 H. S I E B E R T , Z . anorg. allg. Chem. 275, 2 1 0 [ 1 9 5 4 ] . 9 H. S I E B E R T , Z . anorg. allg. Chem. 273, 1 7 0 [ 1 9 5 3 ] . 10 E . A . ROBINSON, Canad. J . Chem. 4L, 3 0 2 1 [ 1 9 6 3 ] . 7 [1967]. Dieses Werk wurde im Jahr 2013 vom Verlag Zeitschrift für Naturforschung in Zusammenarbeit mit der Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. digitalisiert und unter folgender Lizenz veröffentlicht: Creative Commons Namensnennung-Keine Bearbeitung 3.0 Deutschland Lizenz. This work has been digitalized and published in 2013 by Verlag Zeitschrift für Naturforschung in cooperation with the Max Planck Society for the Advancement of Science under a Creative Commons Attribution-NoDerivs 3.0 Germany License. Zum 01.01.2015 ist eine Anpassung der Lizenzbedingungen (Entfall der Creative Commons Lizenzbedingung „Keine Bearbeitung“) beabsichtigt, um eine Nachnutzung auch im Rahmen zukünftiger wissenschaftlicher Nutzungsformen zu ermöglichen. On 01.01.2015 it is planned to change the License Conditions (the removal of the Creative Commons License condition “no derivative works”). This is to allow reuse in the area of future scientific usage. Verbindung K©]P02F2e (C )4N®]PSOF2 Cs®]PS 2 F 2 e 3 H 7 Vas(PF) [cm-1] fs(PF) [cm-1] Lit. vd(PF) [cm-1] 857 822 818 834 805 804 11. 5. 12. 846 814 811 V4 3,75 3,5 3,25 Tab. 2. PF-Schwingungen von substituierten Phosphaten. Tab. 2, so beobachtet man in der angegebenen Reihe eine Verschiebung zu größeren Wellenlängen. In der Abb. 2 ist Vd(PF) Durchschnittsfrequenz gegen die Summe der Elektronegativitäten der Liganden auf- s>d(pF) 850" getragen. Hier beobachtet man keinen linearen Zusammenhang. Wie M Ü L L E R et al. 2 zeigen konnten, wird die PS-Frequenz hauptsächlich durch mechanische Kopplung beeinflußt. Die Änderung des SP-Bindungsgrades spielt eine untergeordnete Rolle. Die Verhältnisse zwischen v(PO)- und v (PS)-Valenzschwingungen sind somit nur bedingt vergleichbar. In der Reihe SPF 3 2, [S 2 PF 2 ] 0 und [PS 4 ] 3 0 ist infolge von Kopplung und Entartung der Schwingungen (PS 4 3 9 ) * eine Berechnung von PS-Valenzkraftkonstanten nach dem Zweimassenmodell wenig sinnvoll. Für das CsS2PF2-Salz wurden folgende Absorptionen gemessen 818 sst, 804 sst, 735 st, 710 sst, 384 m, 360 m, 319 s [ c m - 1 ] . Sie werden versuchsweise folgenden Schwingungen zugeordnet: r a s (PF) 818, vs (PF) 804, v(PS) 735, 710 und Deformationsschwingungen. 840830- Experimentelles 820 Die Darstellung der Thio- und Dithiophosphate wurde an anderer Stelle mitgeteilt 5 - 7 ' 1 2 . Die Aufnahme der Infrarotspektren erfolgte mit einem Gerät der Firma Leitz. 810800- 790 3.25 3.50 3.75 Abb. 2. Abhängigkeit der rd (PF) -Durchschnittsfrequenz von der Elektronegativität der Liganden. 11 12 K. B Ü H L E R U . W. B U E S , Z. anorg. allg. Chem. 308, 62 [1961]. H. W. R O E S K Y , F . N. T E B B E U . E . L . M U E T T E R T I E S , J. Amer. chem. Soc. 89, 1272 [1967]. Herrn Dr. A. M Ü L L E R danke ich für wertvolle Diskussionen. Dem Direktor des Anorganisch-Chemischen Instituts, Herrn Professor Dr. O . G L E M S E R , danke ich für großzügige Unterstützung. Der D e u t s c h e n Forschungsgemeins c h a f t danke ich für die Gewährung von Sachmitteln. Uber die vollständige Messung der Schwingungsspektren sowie die Berechnung von Kraftkonstanten wird in einer weiteren Arbeit publiziert.— A. M Ü L L E R U. H. W. R O E S K Y (in Vorbereitung); B. G. T R I D O T U . P. T R I B O D E T , L'indust. Chim.1965,369.