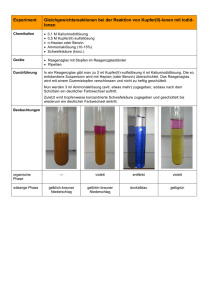
Qualitative Analyse – Allgemeiner Teil A
Werbung

Institut für Anorganische Chemie/Materialchemie, der Universität Wien Chemisches Grundpraktikum /2012 Qualitative Analyse, Grundlagen Qualitative Analyse – Allgemeiner Teil A. Theoretische Grundlagen 1. Einleitung Die qualitative Analyse behandelt die Trennung von Ionengemischen, sowie die Nachweise von Ionen und Elementen. Trennoperationen beruhen im allgemeinen auf einer Verteilung der einzelnen Stoffe auf verschiedene Phasen. Bei der qualitativen Analyse handelt es sich meistens darum, dass bestimmte Stoffe als Niederschläge abgeschieden werden, während andere in Lösung bleiben. Durch Nachweisreaktionen soll das Vorhandensein eines Stoffes (Elements, Ions) angezeigt werden. Es geht dabei insbesondere um das Ausfallen eines Niederschlages, um eine Gasentwicklung oder um eine Farbänderung durch Komplexbildung. Die als Trennoperationen und Nachweise verwendeten chemischen Reaktionen kann man auf vier Grundtypen zurückführen: Niederschlagsbildung Komplexbildung Säure-Basen-Reaktionen Redoxreaktionen Die meisten in der qualitativen Analyse verwendeten Reaktionen gehören zu diesen Grundtypen oder können als Kombinationen mehrerer Grundtypen beschrieben werden. Für jeden Reaktionstyp werden im Text einige für die qualitative Analyse wichtige Beispiele behandelt, wobei die Diskussion der zugrunde liegenden Gleichgewichte und deren Beschreibung durch das Massenwirkungsgesetz im Vordergrund steht. 2. Niederschlagsbildung Die Trennung eines Systems in Niederschlag und Lösung ist die wichtigste Trennmethode der klassischen Analyse. Wir beschränken uns hier auf ionische Verbindungen, wobei angenommen wird, dass die Ionen des gelösten Salzes lediglich unter Hydratisierung reagieren (diese tritt prinzipiell bei allen Ionen ein, wird aber in der Regel in den Formeln nicht mit angegeben). Komplexbildung oder Redoxreaktionen mit etwa vorhandenen Fremdionen sollen ausgeschlossen sein. Es wird angenommen, dass der aus der Lösung ausfallende Niederschlag eine reine Phase ist. Wir wollen nun den Vorgang der Niederschlagsbildung bei Zugabe eines Fällungsmittels betrachten, also das Ausfällen eines schwerlöslichen Salzes AB aus einer Lösung eines seiner Ionen. Bei Zugabe von B--Ionen (in Form eines gelösten, in Ionen dissoziierten gut löslichen Salzes XB) zu einer Lösung von A+-Ionen (in Form eines gelösten, in Ionen dissoziierten Salzes AY) läuft folgende Reaktion ab: A+ + B- ⇌ AB(s) Es genügt, die an der Niederschlagsbildung beteiligten Ionen anzuschreiben. Die Gleichgewichtskonstante des in umgekehrter Richtung verlaufenden Vorganges ist das Löslichkeitsprodukt. Die Ausgangskonzentration von A+, [A+]o, ist vorgegeben. Chemisches Grundpraktikum - 44 - Qualitative Analyse / 2012 Es lassen sich verschiedene Bereiche unterscheiden: a) Bei der Zugabe von B- zur Lösung tritt zunächst kein Niederschlag auf, solange das Produkte der Konzentrationen [A+]0·[B-] kleiner als das Löslichkeitsprodukt von AB ist. Die Lösung ist „ungesättigt“. b) Erst wenn die Lösung gesättigt ist, ist der Punkt erreicht, an dem bei weiterer Zugabe die Fällung beginnt. Die hierzu nötige Konzentration [B-] ergibt sich zu [B − ] = L [A + ] 0 d.h. sie ist umso kleiner, je kleiner L und je größer die Ausgangskonzentration [A+]o ist. Wird der schwerlösliche Niederschlag zum Nachweis des Ions A+ erzeugt, so ist die Fällung also am empfindlichsten in konzentrierteren Lösungen und für möglichst schwerlösliche Salze. c) Bei fortgesetzter Zugabe von B- fällt zunehmend festes AB aus (heterogenes Gleichgewicht), wodurch die Konzentration [A+] sinkt und die im Gleichgewicht befindliche Konzentration [B-] ansteigt. Entsprechend dem Zusammenhang L [ A+ ] = − [B ] wird die im Gleichgewicht vorliegende Konzentration [A+] umso kleiner sein, je größer die zugesetzte Menge an B- ist. Dieser Löslichkeitserniedrigung, die ja im Allgemeinen gewünscht wird, sind jedoch aus praktischen Gründen Grenzen gesetzt, weil Ionenkonzentrationen wegen eintretender Sättigung grundsätzlich nicht beliebig gesteigert werden können. Bei sehr hoher Konzentration [B-] kann unter Umständen Komplexbildung mit entsprechender Löslichkeitserhöhung eintreten. Da Gleichgewichte von beiden Seiten her erreicht werden können, gilt das oben Gesagte sinngemäß auch für die Auflösung eines Niederschlages. Wird das Produkt der Konzentration [A+] · [B-], die mit dem schwerlöslichen Niederschlag AB im Gleichgewicht stehen, unterschritten, so tritt Auflösung des Niederschlages ein, bis diese Gleichgewichtskonzentrationen wiederhergestellt sind. Können sie nicht erreicht werden, so löst sich der gesamte Niederschlag auf. Das kann zum Beispiel geschehen, wenn reines Lösungsmittel zugesetzt wird, ist aber bei schwerlöslichen Salzen wenig wirksam (für ein Salz, dessen Löslichkeit 10-5 mol·l-1 beträgt, würde man 105 Liter Wasser benötigen, um 1 mol Niederschlag in Lösung zu bringen). Viel effektiver können die Konzentrationen vermindert werden, wenn Stoffe zugesetzt werden, die mit A+ oder B- unter Bildung wenig dissoziierter Verbindungen zusammentreten können (z.B. Zugabe von H+ oder Komplexbildnern), oder wenn die Konzentration eines der beiden Stoffe durch eine Redoxreaktion herabgesetzt wird. Daraus ergeben sich für die Ausführung einer möglichst quantitativen Fällung folgende Gesichtspunkte: Die zu fällende Lösung soll, wenn möglich, nicht allzu verdünnt, aber auch nicht zu konzentriert sein, um Mitreißen oder Einschließen von Fremdionen (bei Trennungen) zu vermeiden. Die Fällungslösung wird tropfenweise in der Wärme und unter gutem Rühren zugesetzt, bis der Niederschlag auszufallen beginnt. Sodann wird langsam weiter Fällungsmittel zugesetzt bis die Fällung offenbar beendet ist, und ein kleiner Überschuss des Fällungsmittels zugegeben, um die Löslichkeit weiter zu erniedrigen. Chemisches Grundpraktikum - 45 - Qualitative Analyse / 2012 Zusammenfassung: Ein schwerlöslicher Niederschlag fällt bei allmählichem Zusatz der Fällungslösung aus, sobald das Löslichkeitsprodukt überschritten wird. Ein Salz ist daher umso schwerer löslich, je kleiner sein L ist. Sind mehrere Ionenarten vorhanden, die mit dem zugesetzten Ion schwerlösliche Niederschläge bilden können, so fällt zunächst derjenige Niederschlag aus, dessen L zuerst überschritten wird, also bei gleichen Ausgangskonzentrationen und gleichen Salztypen der Niederschläge (1:1, 2:1, usw.) der mit dem kleineren L. Es gilt auch die Umkehrung, dass sich ein Niederschlag auflöst, sobald in der darüber befindlichen Lösung das L unterschritten wird, z.B. durch Verdünnung, Komplexbildung oder Redoxreaktion. 3. Niederschlagsbildung, gekoppelt mit anderen Reaktionen Ist ein Reaktand gleichzeitig an verschiedenen Reaktionen beteiligt, so sind diese Reaktionen gekoppelt und ihre durch das MWG beschriebenen Gleichgewichte sind über die Konzentration des gemeinsamen Reaktanden verknüpft. Lässt sich eine chemische Reaktion durch Addition anderer Reaktionsgleichungen erhalten, so berechnet man die Gleichgewichtskonstante der Gesamtreaktion durch Multiplikation der Konstanten der einzelnen Teilgleichungen. Wurden die Teilgleichungen vor der Addition mit einem Faktor multipliziert, so sind ihre Konstanten vor der Multiplikation mit demselben Faktor zu potenzieren. Als Spezialfall ist hier auch die Umkehrreaktion enthalten: Man erhält die Gleichung der Umkehrreaktion durch Multiplikation mit -1; die Gleichgewichtskonstante der Umkehrreaktion ist gleich dem reziproken Wert der Gleichgewichtskonstante der ursprünglichen Reaktion. 4. Löslichkeitsgleichgewichte, gekoppelt mit Komplexbildung Komplexbildung besteht in der aufeinanderfolgenden Anlagerung von Liganden an ein Zentralatom (bei Kationen in wässrigen Lösungen handelt es sich meist um Ersatz von H2OMolekülen der ersten Hydratationssphäre durch Liganden-Ionen oder -Moleküle). Es gilt z.B. für drei Neutralliganden (siehe Beispiel Komplexbildungsreaktionen): A2+ + L ⇌ [AL]2+ K1 [AL]2+ + L ⇌ [AL2]2+ 2+ [AL2] + L ⇌ [AL3] K2 2+ K3 A2+ + 3 L ⇌ [AL3]2+ β3 = ß3 = K1 · K2 · K3 [[AL 3 ] 2 + ] [A 2 + ] ⋅ [L] 3 Entsprechendes gilt für mehr Liganden. K1, K2, K3 sind die Bildungskonstanten der einzelnen Komplexe, ß3 wird als Bruttobildungskonstante bezeichnet. Reaktionen, bei denen die Komplexbildung mit Löslichkeitsgleichgewichten gekoppelt ist, sind für die Analyse sehr wichtig; es kann durch Zusatz eines Komplexbildners ein in Wasser sehr schwerlöslicher Niederschlag in Lösung gebracht werden, bzw. wird die Bildung eines solchen Niederschlages durch den Komplexbildner verhindert. Chemisches Grundpraktikum - 46 - Qualitative Analyse / 2012 Beispiel: Auflösung von AgCl in NH3 : AgCl(s) ⇌ Ag+ + Cl- L ß2 Ag+ + 2 NH3 ⇌ [Ag(NH3)2]+ AgCl(s) + 2 NH3 ⇌ [Ag(NH3)2]+ + ClK = L · ß2 K= [[Ag(NH 3 ) 2 ] + ] ⋅ [Cl − ] [NH 3 ] 2 (L = 1·10-10) (ß2 = 1,6 ·107) = L ⋅ β 2 = 1,6 ⋅ 10 −3 Man kann nun die Löslichkeit c von AgCl in einer NH3-Lösung der Ausgangskonzentration co berechnen, wobei folgende Gleichgewichtskonzentrationen eingehen: c ([Ag(NH3)2]+) = c (Cl-) = c; c (NH3) = (co - 2c); K= c2 ; (c 0 − 2c) 2 Nimmt man z.B. an co = 2,0 mol·l-1 , so ergibt sich c = 0,074 mol·l-1. 5. Fällung von Hydroxiden Die Ausfällung von Hydroxiden durch Zusatz von OH--haltigen oder H+-aufnehmenden Stoffen wird in der qualitativen Analyse häufig durchgeführt; so fallen z.B. in der Eisengruppe Cr(OH)3 und Al(OH)3 durch das zugesetzte NH3 trotz der Gegenwart von Sulfiden aus, da die Hydroxide dieser Elemente schwerer löslich sind als ihre Sulfide und daher zuerst ausfallen. Die Fällung von Hydroxiden unterscheidet sich nicht grundsätzlich von der anderer schwer löslicher Salze. Für die Löslichkeitsprodukte gilt z.B.: L (A(OH)2) = [A2+] · [OH-]2 L (A(OH)3) = [A3+] · [OH-]3 Die Niederschlagsbildung wird aber hier mit dem Gleichgewicht für die Eigendissoziation des Wassers sowie mit anderen in der Lösung ablaufenden Protonierungs- und Deprotonierungsreaktionen gekoppelt sein. 6. Hydroxokomplexe Eine Anzahl von Hydroxiden bildet mit überschüssigen OH--Ionen wasserlösliche Hydroxokomplexe: Al(OH)3 + OH- ⇌ [Al(OH)4]Zn(OH)2 + 2 OH- ⇌ [Zn(OH)4]2Es treten auch Zwischenstufen wie [Zn(OH)3]- auf. Für die Auflösung von Zn(OH)2 in starker Lauge (NaOH) kann man - bei Nichtberücksichtigung von [Zn(OH)3]- - formulieren: Chemisches Grundpraktikum - 47 - Qualitative Analyse / 2012 Zn(OH)2(s) ⇌ Zn2+ + 2 OHL ß4 Zn2+ + 4 OH- ⇌ [Zn(OH)4]2 Zn(OH)2(s) + 2 OH- ⇌ [Zn(OH)4]2K = L·ß4 K= (L = 10-17) (ß4 = 1016) [[ Zn (OH ) 4 ] 2− ] = L·ß4 = 10-1 [OH − ] 2 Derartige Hydroxide vermögen daher sowohl mit Säuren als auch mit Basen zu reagieren, sie sind amphoter. Zu diesen gehören die Hydroxide von Al, Zn, Sn(II), Sn(IV) und Pb(II). Aus den Komplexsalzlösungen kann durch Verschiebung des Komplexgleichgewichtes infolge Verringerung der OH-Konzentration wieder das Hydroxid ausgefällt werden; hierzu sind alle Stoffe imstande, die H+-Ionen abgeben können (Säuren nach Brönstedt), z.B. das Ion NH4+. Für die Ausfällung von Al(OH)3 aus einer Lösung von [Al(OH)4]-, z.B. durch Zugabe von NH4+-Ionen, kann man - wieder unter Nichtberücksichtigung von Zwischenstufen - formulieren: ·10-5) Al3+ + 3 OH[Al(OH)4]NH4+ + OH- ⇌ Al(OH)3(s) ⇌ Al3+ + 4 OH⇌ NH3 + H2O 1/L 1/β4 1/KB (L = 10-33) (ß4 = 1032) (KB = 2 [Al(OH)4]- + NH4+ ⇌ Al(OH)3(s) + NH3 + H2O K= [NH 3 ] − + [[Al(OH)4 ] ] ⋅ [NH 4 ] = 1 = 5 ⋅ 10 5 β4 ⋅ L ⋅ K B 7. Fällung von Sulfiden Die Sulfide der meisten Elemente unterscheiden sich hinsichtlich ihrer Löslichkeitsprodukte in charakteristischer Weise voneinander, sodass durch zweckmäßige Wahl des pH-Wertes (siehe unten) zahlreiche Trennungen ausgeführt werden können. a) In 1-2 M HCl fallen mit H2S die Sulfide von As, Sb, Sn, Hg, Bi, Pb, Cu und Cd aus (kleines Löslichkeitsprodukt). b) Aus ammoniakalischer Lösung fallen die Sulfide von Fe, Zn, Mn, Co und Ni aus (größeres Löslichkeitsprodukt). Die Sulfide von Cr und Al (die unter diesen Bedingungen ebenfalls ausfallen sollten) haben eine größere Löslichkeit als die Hydroxide dieser Elemente, sodass bei der eintretenden Konkurrenz der Ionen OH- und S2- um das Kation zuerst die Hydroxide ausfallen. Eine interessante Besonderheit tritt bei den Sulfiden von Co und Ni auf: Obwohl sie in saurer Lösung wegen ihres verhältnismäßig hohen Löslichkeitsproduktes nicht ausfallen und daher erst in ammoniakalischer Lösung durch H2S gefällt werden, lösen sie sich, im Gegensatz zu den Sulfiden von Fe, Mn und Zn, bei nachfolgender Behandlung mit 2 M HCl nicht mehr auf. Dieses Verhalten wird bei einigen Analysengängen zu ihrer Abtrennung benützt. Der Grund für dieses Verhalten liegt in einer irreversiblen Veränderung dieser Sulfide beim Stehen an Luft. Chemisches Grundpraktikum - 48 - Qualitative Analyse / 2012 Die Fällung von Sulfiden kann sowohl aus saurer (Fall a) als auch aus alkalischer Lösung (Fall b) mit H2S erfolgen. (Zur Problematik der Ausfällung von Hydroxiden im Alkalischen siehe Punkt 5.) Dabei reagiert H2S als zweiprotonige (tweibasige, zweiwertige) Säure: H2S ⇌ H+ + HSK1 = 10-7 + 2HS ⇌ H + S K2 = 10-13 H2S ⇌ 2 H+ + S2KS = K1·K2 = 10-20 − KS = [H + ] 2 ⋅ [S2 ] = K1 ⋅ K 2 = 10 −20 [H 2 S] Drückt man aus dieser Beziehung die Sulfidionenkonzentration [S2-] aus, so erhält man − [S 2 ] = K S ⋅ [H 2 S] [H + ] 2 Da bei Sättigung einer wässrigen Lösung mit H2S (p(H2S) = 1,013 bar) die H2S-Konzentration c (H2S, 25°C) = 0,1 mol·l-1 beträgt, so erhält man für [S2-]: [S 2− ] = 10 −21 [H + ] 2 Diese Beziehung drückt die Abhängigkeit der Sulfidionenkonzentration von der H+-Ionenkonzentration bzw. vom pH-Wert aus. Die hier beschriebene Überlegung beruht ausschließlich auf dieser einfachen Beziehung. Unsicherheiten hinsichtlich des Zahlenwertes von K2 sowie Protolyse-Gleichgewichte des S2--Ions, vor allem in alkalischen Lösungen, werden nicht berücksichtigt. Für die Löslichkeit eines Sulfids AS in H2S-gesättigter saurer Lösung werden folgende Gleichgewichte herangezogen: ⇌ A2+ + S2L AS(s) 2+ S + 2 H ⇌ H2S 1/Ks AS(s) + 2 H+ ⇌ A2+ + H2S K = L/KS K= [ A 2 + ] ⋅ [ H 2 S] + 2 [H ] (Ks = 10-20) = L ⋅ 10 20 Mit [H2S] = 0,1 mol·l-1 (siehe oben), L = [A2+] · [S2-] und c = [A2+] erhält man aus der Beziehung c ⋅ 10 -1 [H + ] 2 für die Löslichkeit des Sulfids AS (entspricht in diesem Fall zahlenmäßig gleichzeitig der Stoffmengenkonzentration des Metallkations): L ⋅ 10 20 = c = 1021 · L · [H+]2 Chemisches Grundpraktikum - 49 - Qualitative Analyse / 2012 Für saure Lösungen (z.B. pH = 0 oder [H+] = 1 mol·l-1) ist c für L < 10-21 klein; das Gleichgewicht der oben genannten Reaktion liegt auf der linken Seite, d.h. das Sulfid ist schwer löslich. Sulfide mit L > 10-21 sind dagegen bei diesen Bedingungen löslich. In alkalischen Lösungen (z.B. pH = 8 oder [H+] = 10-8 mol·l-1) sind auch Sulfide mit L > 10-21 schwer löslich. Ein Beispiel aus dem Analysengang soll aufgrund der unterschiedlichen Löslichkeitsprodukte die Fällung von Sulfiden aus saurer bzw. alkalischer Lösung zeigen: in saurer Lösung fallen aus: ¦ in alkalischer Lösung fallen aus: HgS: L = 10-52 ¦ FeS: L = 10-17 CuS: L = 10-36 ¦ MnS: L = 10-14 CdS: L = 10-26 ZnS: L = 10-23 Enthält die saure Lösung, aus der HgS und CuS ausgefällt wurden auch Cd oder Zn, so müsste die saure Lösung nach dem Einleiten von H2S auf das etwa Vierfache ihres Volumens mit H2O verdünnt werden (um den pH-Wert zu erhöhen), damit CdS ausfällt. Bei einer größeren Verdünnung könnte auch ZnS ausfallen. 8. Auflösung von Sulfiden durch Komplexbildung mit Sulfidionen Einige Metalle (As, Sb, Sn), die schwerlösliche Sulfide bilden, geben mit einem Überschuss von Sulfidionen lösliche Komplexe (Thiokomplexe, Thiosalze). Im Folgenden soll die Auflösung von SnS2 durch solche Komplexbildungsprozesse in einfacher Weise betrachtet werden, d.h. es wird angenommen, dass nur die in den Reaktionsgleichungen angeführten Spezies eine Rolle spielen. SnS2(s) ⇌ Sn4+ + 2 S2L 4+ 2Sn + 3 S ⇌ [SnS3]2 ß4 SnS2(s) + S2- ⇌ [SnS3]2K = L · ß3 K= [[SnS 3 ] 2 − ] [S 2 − ] = L ⋅ β3 Aus dieser Gleichgewichtskonstante folgt daher für die Auflösung eines Sulfids unter Thiosalzbildung, dass die Reaktion bei genügend großer Sulfidionenkonzentration von links nach rechts ablaufen muss, vorausgesetzt β3 ist hinreichend groß. Fügt man H+-Ionen zu (starke Säure) so sinkt [S2-] gemäß [S 2− ] = 10 21 [ H + ]2 Dadurch wird die Reaktion rückläufig; die Thiosalze zersetzen sich beim Ansäuern, d.h. Sulfid fällt aus und H2S wird freigesetzt. Die Bruttogleichung lautet: [SnS3]2- + 2 H+ ⇌ H2S + SnS2↓ Chemisches Grundpraktikum - 50 - Qualitative Analyse / 2012 Wegen der Löslichkeit ihrer Sulfide in S2--Lösungen hoher Konzentration können die zur Thiosalzbildung befähigten Elemente As, Sb und Sn(IV) von Hg, Pb, Bi, Cu und Cd getrennt werden. Da auch das HgS eine gewisse Tendenz zur Thiosalzbildung zeigt, darf zum Abtrennen nur die weniger basische Ammoniumsulfidlösung verwendet werden; eine Natriumsulfidlösung würde eine zu hohe OH--Konzentration und damit auch eine zu hohe S2--Konzentration besitzen. Um die Oxidation von Sn(II), das keine Thiosalze bildet, zum Sn(IV) zu sichern, wird gelbes Ammoniumpolysulfid, (NH4)2Sx, verwendet. Hierdurch werden gleichzeitig As(III) zu As(V) und Sb(III) zu Sb(V) oxidiert, wobei Schwefel der Oxidationszahl 0 in solchen der Oxidationszahl -II übergeht. (siehe auch Beispiel 14: Kupfergruppe) 9. Redoxreaktionen In diesem Abschnitt werden die Beziehung zwischen den Gleichgewichtskonstanten von Redoxreaktionen und den elektrochemischen Potentialen sowie einige Anwendungen dieser Beziehung behandelt. Oxidation und Reduktion Redoxreaktionen sind Prozesse, bei denen Elektronenübertragung zwischen Ionen bzw. Atomen oder Molekülen stattfindet. In jeder Redoxreaktion sind ein Reduktions- und ein Oxidationsprozess miteinander gekoppelt, d.h. es nehmen zwei „Redoxpaare“ an einem solchen Prozess teil. Als Redoxpaar bezeichnet man die reduzierte und oxidierte Form eines Stoffes, die durch Elektronenabgabe bzw. -aufnahme ineinander überführt werden. (Siehe Beispiel 5: Redoxreaktionen). Daraus wird ersichtlich, dass bei einem chemischen Vorgang keine Oxidation ohne gleichzeitige Reduktion und umgekehrt stattfinden kann. Es sei daran erinnert, dass sich ein Zinkblech, welches in eine CuSO4- oder Cu(NO3)2-Lösung taucht, mit metallischem Kupfer überzieht. Allgemein ist die Abscheidung von Metallen aus ihren Lösungen durch Zugabe weniger edler Metalle möglich. Einige Nachweise in der qualitativen Analyse können mit solchen Redoxreaktionen im Reagenzglas durchgeführt werden. z.B. wird Antimon auf einem Eisennagel oder Quecksilber und Silber auf einem Kupferblech abgeschieden. B. Praktische Hinweise Trennungsgang In der Qualitativen Analyse benutzt man die Fällung mit H2S zur Trennung der Metalle in Gruppen. Die Bezeichnungen der einzelnen Ionengruppen leiten sich von einem charakteristischen Element der Gruppe oder von einem Fällungsmittel ab. Der auch heute noch am häufigsten angewendete, in seinen Grundzügen bereits 1840 von C. R. Fresenius aufgestellte Kationentrennungsgang beruht auf der unterschiedlichen Löslichkeit der Metallsulfide im sauren und basischen Medium. Bei Durchführung eines Trennungsganges im Rahmen des Praktikums werden zunächst aus der salzsauren Lösung die schwerlöslichen Chloride von Ag, Hg(I) und Pb gefällt (Silbergruppe, HCl-Gruppe). Aus der verbleibenden sauren Lösung werden durch Einleiten von H2S die Sulfide der H2S-Gruppe gefällt (As, Sb, Sn, Hg, Bi, Cu und Cd), die anschließend mittels selektiver Komplexbildung (s. Punkt 8) als Arsengruppe (As, Sb, Sn) und Kupfergruppe (Hg, Bi, Cu, Cd) getrennt werden können. Chemisches Grundpraktikum - 51 - Qualitative Analyse / 2012 Durch Zugabe von H2S im ammoniakalischen Bereich können sowohl die Hydroxide von Al, Cr, Fe, Mn (Hydroxidgruppe) als auch die Sulfide von Zn, Fe, Co, Ni, Mn (Sulfidgruppe) gleichzeitig als „Fe-Gruppe“ (bezugnehmend auf (NH4)2S als Fällungsmittel auch als Ammoniumsufidgruppe) gefällt werden. Die Sulfide der Alkalimetalle sind wasserlöslich (lösliche Gruppe), ebenso jene der Erdalkalimetalle, wobei jedoch die Elemente Ca, Sr und Ba als schwerlösliche Sulfate (Sulfatgruppe) oder alternativ als Carbonate gefällt werden könnten. Mit Ausnahme des Beispiels „Feste Probe“ werden im Praktikum die Kationen nur gruppenweise ausgegeben. Dadurch kommt die in manchen Fällen nur teilweise mögliche Trennung (s. die Zuordnung von Mn zu den beiden Untergruppen der Fe-Gruppe) nicht zum Tragen. Mengen. Die ausgegebenen Analytikproben sind vor den Versuchen auf das 3-4-fache ihres Volumens zu verdünnen — Ausnahme: der Carbonatnachweis (Anionen I) muß mit der konzentrierten Probe durchgeführt werden. Die angegebenen Mengen an Probe und Reagenzien sind für den Anfänger gedacht, sehr Geübte können sämtliche Mengen vermindern. Die erforderlichen Konzentrationen der Reagenslösungen sind durch Verdünnen der konzentrierten („konz.“ abgekürzt) Lösungen von den Studierenden selbst herzustellen. Zugabe von Reagenzien. Die Zugabe von Reagenslösungen erfolgt tropfenweise, insgesamt, wenn nicht anders angegeben, 1-2 ml. Danach ist die Lösung gut durchzumischen (Glasstab), um die Ausbildung von Schichten infolge unterschiedlicher Dichten zu verhindern. Mischungen von Reagens- und Waschlösungen werden im Text durch „+“ bzw. „/“ gekennzeichnet (z.B. „2 ml Ethanol + 2 Tropfen H2SO4“, „Ether/Ethanol“). Feste Reagenzien werden mit dem Spatel zugefügt und durch Umrühren mit einem Glasstab in der Probelösung aufgelöst (keinesfalls mit dem Spatel umrühren, weil sonst dessen Bestandteile in der Probe nachgewiesen werden könnten). Ansäuern, ammoniakalisch machen. Nach der Zugabe der Reagenzien und dem Durchmischen der Probe muß der pH-Wert überprüft werden. Niederschlagsbildung. Fällt nach Zugabe eines Fällungsreagens kein Niederschlag aus, so kann man versuchen, die Niederschlagsbildung durch leichtes Kratzen mit einem Glasstab an der Gefäßinnenwand auszulösen. Niederschläge sind oft erst nach dem Zentrifugieren erkennbar. Unerwartet auftretende Niederschläge werden abzentrifugiert und gegebenenfalls identifiziert. Trennoperationen. Alle Trennungen müssen möglichst quantitativ durchgeführt werden, weil sonst Ionen verschleppt werden und dann Nachweise stören können. Prüfen auf Vollständigkeit der Fällung. Bei Fällungsreaktionen prüfe man stets auf Vollständigkeit der Fällung. Dies erfolgt, wenn nicht anders angegeben, folgendermaßen: Man zentrifugiert und fügt der Lösung anschließend nochmals einige Tropfen Fällungsmittel zu. Fällt dabei ein Niederschlag aus, wird erneut abzentrifugiert. Diesen Vorgang wiederholt man solange, bis kein Niederschlag mehr ausfällt. Unterbrechen der Arbeit. Niederschläge und alkalische Lösungen sollten möglichst rasch weiterverarbeitet werden. Saure Lösungen können längere Zeit aufbewahrt werden. Zentrifugieren. Bei den Versuchen werden Niederschläge von Lösungen durch Zentrifugieren abgetrennt. Dazu stehen im Praktikum Zentrifugen mit Ausschwingrotoren für jeweils vier oder acht 15 ml-Zentrifugen-röhrchen (je nach Bauart) zur Verfügung, deren Deckel aus Sicherheitsgründen erst geöffnet werden kann, wenn der Rotorstillstand angezeigt wird. Drehzahl (ca. 4000 U/min) und Zentrifugierdauer (1-2 min) können mit den entsprechenden Drehknöpfen oder digital eingestellt werden. Chemisches Grundpraktikum - 52 - Qualitative Analyse / 2012 Vor dem Zentrifugieren ist es notwendig, ein weiteres Zentrifugenröhrchen (möglichst gleiche Röhrchen verwenden) als Gegengewicht so weit mit Wasser zu füllen, dass in beiden Röhrchen der Flüssigkeitsspiegel gleich hoch steht. Es ist ratsam, stets dasselbe, entsprechend gekennzeichnete Zentrifugenröhrchen als Gegengewicht zu verwenden, um sich Reinigungsarbeit (= Zeit) und Ärger wegen verwechselter Zentrifugenröhrchen - oft müssen auch scheinbar klare Lösungen abzentrifugiert werden! - zu ersparen. WICHTIG! Die Zentrifugenröhrchen dürfen beim Zentrifugieren nicht randvoll sein! Füllhöhe nur etwa 3/4 bis 4/5 des Fassungsvermögens! Bevor die beiden Zentrifugenröhrchen in einander gegenüberliegende Rotorgefäße gestellt werden, müssen sie außen gesäubert und getrocknet werden! Pflege und Wartung der Zentrifugen: Zum Schutz vor Korrosion müssen Rotorkammer, Rotor und Rotorzubehör stets sauber gehalten werden. Zur Reinigung ist ein möglichst neutrales Reinigungsmittel zu verwenden. Das Gehäuse darf nur mit von organischen Lösungsmitteln freien Reinigungsmitteln gesäubert werden. Kommt es während des Zentrifugierens zu Glasbruch, so muss sofort die Zentrifuge unverzüglich abgestellt werden! Diensthabende verständigen! Schleuderraum und Arbeitskopf auf Schäden untersuchen und reinigen! Auch der Tragbecher muss frei von Glassplittern sein, da Splitter im Gummipolster erneut zu Glasbruch führen! Bei Betriebsstörungen der Zentrifuge sind die Diensthabenden zu verständigen! Fein verteilte Niederschläge. Sehr fein verteilte und gelatinöse Niederschläge benötigen etwas länger zum Absitzen, doch kann dieser Vorgang durch Zugeben von etwas Papierbrei in die Lösung und nochmaliges Zentrifugieren beschleunigt werden. Der Papierbrei wirkt mechanisch sammelnd und reißt den fein suspendierten (aufgeschlemmten) Niederschlag mit. Farbe von Niederschlägen: Farbangaben beziehen sich auf reine Niederschläge, Spuren von Beimengungen können die Farbe stark verändern. Suspendierte Niederschläge sind mitunter anders gefärbt als abzentrifugierte. Waschen von Niederschlägen. Der Niederschlag wird nach Entfernen (Abpipettieren oder Dekantieren) der überstehenden Lösung im Zentrifugenröhrchen mit der jeweiligen Waschlösung übergossen und mit einem Glasstab gründlich aufgewirbelt. Danach zentrifugiert man den Niederschlag wieder ab und verwirft, wenn nicht anders angegeben, die Waschflüssigkeit. In manchen Fällen ist der Waschvorgang zu wiederholen, entsprechende Hinweise finden sich an den betreffenden Stellen des Textes. Überführen von Niederschlägen in andere Gefäße: Dies erfolgt durch Suspendieren des Niederschlages in einer geeigneten Flüssigkeit. Wird nur ein Teil des Niederschlages benötigt, so transferiert man den entsprechenden Anteil der Suspension mit einer Tropfpipette in das gewünschte Gefäß. Lösen von Niederschlägen. Man gibt etwas Lösungsmittel ins Zentrifugenröhrchen und rührt mit einem Glasstab um, bis sich der Niederschlag gelöst hat. Gegebenenfalls fügt man noch einige Tropfen Lösungsmittel zu. Eindampfen. Flüssigkeiten werden in einem Becherglas oder einer Porzellanschale auf dem Sandbad eingeengt. Das Gefäß ist mit einem Uhrglas zu bedecken, das auf Glashäkchen oder Ähnlichem ruht. Alle Operationen, bei denen giftige, ätzende oder belästigende Dämpfe entstehen (z.B. Säuren, NH3, Ammoniumsalze, H2S, ...), sind unter einem gut ziehenden Abzug durchzuführen. Chemisches Grundpraktikum - 53 - Qualitative Analyse / 2012 Abrauchen. Falls Chlorid-, Nitrat- oder Ammonium-Ionen bei nachfolgenden Reaktionen störend wirken, können sie durch Abrauchen in einer Porzellanschale oder einem Porzellantiegel entfernt werden: Man übergießt dazu den noch feuchten oder trockenen Rückstand der eingeengten oder eingedampften Lösung mit dem entsprechenden Reagens und dampft neuerlich ein; den Rückstand nimmt man dann im gewünschten Lösungsmittel auf. Chloride werden durch Abrauchen mit konz. HNO3 in Nitrate, Nitrate durch Abrauchen mit konz. HCl in Chloride umgewandelt. Ammoniumsalze werden abgeraucht, indem man die eingeengte Lösung im Porzellantiegel mit 1 ml konz. HCl und 2 ml konz. HNO3 eindampft und anschließend mit dem Brenner glüht (Dreifuß, Tondreieck; vor weiterer Lösungsmittelzugabe den Tiegel auskühlen lassen!). Einsatz von H2S: H2S, Na2S liefern Sulfid- bzw. SH--Ionen, pH-Wert-Änderung gegebenenfalls beachten! Nachweisreaktionen. Die meisten der im folgenden beschriebenen Nachweisreaktionen werden von anderen Ionen gestört, deshalb müssen vorher immer entsprechende Trennoperationen durchgeführt werden. Alkali- und Erdalkali-Ionen – außer Mg2+ – können durch ihre Flammenfärbung bzw. ihre charakteristischen Spektrallinien identifiziert werden. Bei der Formulierung der Reaktionsgleichungen werden u.a. folgende Symbole verwendet: ↓ Niederschlag fällt aus ↑ Gas entweicht (s) solidus: Substanz liegt als Feststoff vor (aq) aqua: Substanz liegt in wässriger Lösung vor In manchen Fällen werden zwecks Übersichtlichkeit vereinfachte Formelschreibweisen angewandt. Die Hydratisierung eines Stoffes wird im allgemeinen nicht angegeben. Vergleichs- und Blindproben. Es wird empfohlen, vorher die Reaktionen mit reinen Lösungen des betreffenden Ions oder mit entsprechenden Ionengemischen (ohne das gesuchte Ion) als Blindprobe auszuführen, insbesondere wenn bei der Durchführung der Nachweisreaktionen Schwierigkeiten oder Unklarheiten auftreten. Tropfengröße. Das Volumen ist direkt proportional zum Öffnungsradius und zur Oberflächenspannung, indirekt proportional zur Dichte. Für Wasser und r = 1 mm gilt: V ≈ 0,04 ml. Empfindlichkeit. Die bei Durchführung der qualitativen Analyse anwesenden Fremdsalze verändern im allgemeinen die Empfindlichkeit eines Nachweises. Sie wird meist verringert, kann aber auch erhöht werden