ppt - Userpage
Werbung
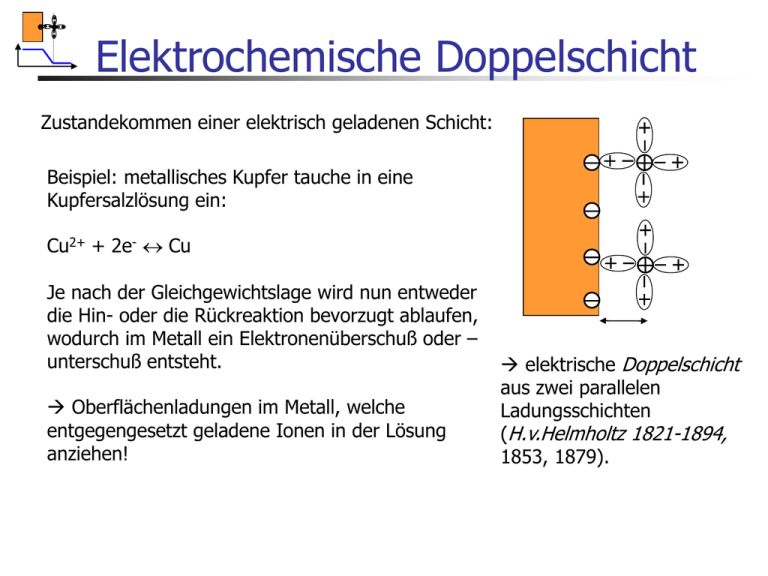
Elektrochemische Doppelschicht Zustandekommen einer elektrisch geladenen Schicht: Beispiel: metallisches Kupfer tauche in eine Kupfersalzlösung ein: Cu2+ + 2e- Cu Je nach der Gleichgewichtslage wird nun entweder die Hin- oder die Rückreaktion bevorzugt ablaufen, wodurch im Metall ein Elektronenüberschuß oder – unterschuß entsteht. Oberflächenladungen im Metall, welche entgegengesetzt geladene Ionen in der Lösung anziehen! elektrische Doppelschicht aus zwei parallelen Ladungsschichten (H.v.Helmholtz 1821-1894, 1853, 1879). Elektrochemische Doppelschicht Zustandekommen einer elektrisch geladenen Schicht: Doppelschichten bilden sich aber auch durch Adsorption von Dipolen und nichtabgesättigten Bindungen Das gesamte System ist elektroneutral; Jedoch an der Grenzfläche gibt es eine Ladungstrennung!!! qm + qs = 0 elektrische Doppelschicht aus zwei parallelen Ladungsschichten (H.v.Helmholtz 1821-1894, 1853, 1879). Elektrochemische Doppelschicht Elektrochemische Doppelschicht Findet keine elektrochemische Reaktion statt, d, h, kein eTransfer kann man eine äussere Zellspannung an das System anlegen und verändert damit die elektrochemische Doppelschicht: - + - + - + FU Berlin Constanze Donner / Ludwig Pohlmann 2010 + 3 Elektrochemische Doppelschicht Elektrochemische Zelle Elektrochemische Doppelschicht Elektrochemische Zelle Helmholtz Helmholtz war der erste , welcher versuchte, die Doppelschicht zu erklären FU Berlin Constanze Donner / Ludwig Pohlmann 2010 7 Elektrochemische Doppelschicht Näherungen: man betrachtet zwei planparallele Ladungsschichten man betrachtet nur Punktladungen Ionen nähern sich der Doppelschicht bis auf Hydrathüllenabstand Es wird keine thermische Bewegung betrachtet Kapazität eines Plattenkondensators C = - e / 4pd - + r FU Berlin Constanze Donner / Ludwig Pohlmann 2010 8 Elektrochemische Doppelschicht Füllt man einen elektrisch nichtleitenden Stoff zwischen zwei Platten, Polarisierung wirkt dem Feld entgegen wird er polarisiert Elektrische Verschiebung: D = eo E ( Abschwächung) Die Feldstärke sinkt er = Eo / E Kapazität eines Plattenkondensators C = - e / 4pd - + r FU Berlin Constanze Donner / Ludwig Pohlmann 2010 9 Plattenkondensator-Modell starre Doppelschicht von solvatisierten Ionen und Elektronen auf der Metallseite „Plattenabstand“: einige Moleküldurchmesser Metall FU Berlin äußere HH-Schicht Ladungsfreier Raum zwischen den Schichten: Linearer Potentialabfall Poisson Gleichung d 2 mit 0 dx2 e re 0 Constanze Donner / Ludwig Pohlmann : Raumladungsdichte 2010 10 Plattenkondensator-Modell d kons tan t dx konstante Feldstärke Metall FU Berlin äußere HH-Schicht Ladungsfreier Raum zwischen den Schichten: Linearer Potentialabfall Poisson Gleichung d 2 mit 0 dx2 e re 0 Constanze Donner / Ludwig Pohlmann : Raumladungsdichte 2010 11 Konsequenzen I „Plattenkondensator“ mit kleinstmöglichem Plattenabstand! Extrem hohe Feldstärke: = 500 mV, d = 0.5 nm Feldstärke E = 109 V/m ! Zum Vergleich: Durchschlagsfeldstärke: Luft: 106, Quarz: 108 V/m Diese enormen Feldstärken sind notwendig (und hinreichend), um chemische Bindungen brechen bzw. neu formen zu können! Elektrochemische Reaktionen können nur in der Helmholtzschicht stattfinden! EC ist Surface Science! FU Berlin Constanze Donner / Ludwig Pohlmann 2010 12 Konsequenzen II „Plattenkondensator“ mit kleinstmöglichem Plattenabstand! Riesige Kapazität: e re 0 A Kapazität pro Fläche beim Plattenkondensator: C d Wasser: er = 78,5 C = 350 F/cm2 e0= 8 x 10-12 C / V m in Wirklichkeit kleiner, ca. 10-50 F/cm2, da er in der starren Doppelschicht kleiner ist Anwendung für Kondensatoren! FU Berlin Constanze Donner / Ludwig Pohlmann 2010 13 Doppelschichtkondensatoren Kapazität: 10-40 F/cm2 Goldcaps, Boostcaps, Supercaps Seit 1971 (1957 Patent) FU Berlin Constanze Donner / Ludwig Pohlmann 2010 14 Superkondensatoren Prinzip: poröse Kohlenstoffelektroden mit einer sehr großen inneren Oberfläche! (Aktivkohle, Aerogele) Kapazitäten bis zu 100 F / g ! 1 W CU 2 2 Energiedichte: 4 Wh / kg bis zu 60 Wh / kg Forschung: neue Elektrodenmaterialien, geeignetere Elektrolyte Anwendung: kleinste Ströme, bzw. Schnelle Ströme FU Berlin Constanze Donner / Ludwig Pohlmann 2010 15 Anwendungsperspektiven FU Berlin Constanze Donner / Ludwig Pohlmann 2010 16 Plattenkondensator-Modell d kons tan t dx C e re 0 d A konstante Feldstärke dq C d W 0.5C 2 q 0 Konstante Kapazität Metall FU Berlin äußere HH-Schicht Constanze Donner / Ludwig Pohlmann 2010 17 Plattenkondensator-Modell Widerspruch zum Experiment Konstante Kapazität nur für sehr hohe Elektrolytkonzentrationen im negativen Bereich gültig! Sie ist abhängig vom Potential. C q Ursache ist die Orientierung der Wasserdipole und Adsorption von Ionen 0 Konstante Kapazität FU Berlin Constanze Donner / Ludwig Pohlmann 2010 18 Plattenkondensator-Modell Obwohl die Ladung metallseitig nur auf die Oberfläche konzentriert ist, Muss dies nicht notwendigerweise für die Lösung gelten. Besonders für niedrige Konzentrationen bekommt die Schicht lösungsseitig mehr Ausdehnung, es entsteht eine Diffuse Doppelschicht FU Berlin Constanze Donner / Ludwig Pohlmann 2010 19 Gouy (1910) –Chapman( 1913) -Modell Grundidee: zwei gegenläufig Prozesse Das elektrostatische Feld der Elektrode zieht entgegengesetzt geladene Ionen an Die thermische Molekularbewegung zerstört immer wieder jede Ordnung Analogie: Debye Hückel FU Berlin Constanze Donner / Ludwig Pohlmann 2010 20 Gouy-Chapman-Modell Analogie: Debye Hückel FU Berlin Radialsymmetrische vs ebene Geometrie Ionenwolke vs. Raumladungszone Constanze Donner / Ludwig Pohlmann 2010 21 Gouy ( 1910) –Chapman (1913) Sie verwendeten ähnliche Näherungen: Die größte Konzentration an Ionen befindet sich nahe der Metallseite und sinkt mit zunehmendem Abstand von der Elektrode - - - - - - - - Elektrostatische / thermische Energie abstandsabhängig Die Schicht wird schmäler, wenn: die Ladungsdichte steigt die Konzentration des Elektrolyten größer wird FU Berlin Constanze Donner / Ludwig Pohlmann 2010 23 Gouy ( 1910) –Chapman (1913) + - - - - - - nahe der Elektrode gilt: Elektrostatische > thermische Energie - - Im Abstand x0 besitzt die Ionenkonzentration den Wert im Volumen: Referenzzustand n0 x0 Die Anzahl der Ionen in der Doppelschicht wird durch die Boltzmann-Verteilung beschrieben: zF ( x) n( x) n0 exp( ) RT (x) = – (s) (s) = 0 Elektroneutralität FU Berlin Constanze Donner / Ludwig Pohlmann 2010 24 Gouy ( 1910) –Chapman (1913) Die Anzahl der Ionen in der Doppelschicht wird durch die Boltzmann-Verteilung beschrieben: zF ( x) n( x) n0 exp( ) RT (x) = – (s) (s) = 0 Elektroneutralität Summiert über alle Arten von Ionen gilt für die Ladungsdichte pro Volumen: ( x) FU Berlin zi F ( x) zi n0i F exp( ) RT Constanze Donner / Ludwig Pohlmann 2010 25 Gouy ( 1910) –Chapman (1913) Die Poisson Gleichung verknüpft die Raumladungsdichte mit dem Potential ( Analogie zur Debye – Hückel Theorie) d 2 (x (x e re 0 dx2 Kombination der Boltzmann- Gleichung mit der Poisson- Gleichung führt zu d 2 2 dx F e 0e r zi F ( x) zi n0i exp( ) RT Diese Gleichung enthält nur noch das Potential FU Berlin Constanze Donner / Ludwig Pohlmann 2010 26 Gouy ( 1910) –Chapman (1913) Kombination der Boltzmann- Gleichung mit der Poisson- Gleichung d 2 dx2 F e 0e r z F ( x) zi n0i exp( i ) RT Lösung unter folgenden Annahme möglich: er ist unabhängig von x ( grobe Näherung, sie gilt streng genommen nur weit weg von der Elektrode) zF << RT, dann gilt auch : zi F ( x) << 1 RT Elektrostatische Energie < thermische Energie !!! Achtung: gilt nur für kleine Potentialdifferenzen!!! FU Berlin Constanze Donner / Ludwig Pohlmann 2010 27 Gouy ( 1910) –Chapman (1913) Lösungsweg in Analogie zur Debye - Hückeltheorie d 2 dx2 F e 0e r z F ( x) zi n0i exp( i ) RT Linearisierte Form nach Taylor- Reihenentwicklung 1 d 2 dx2 praktikabel FU Berlin 2FF I e 0e r RT I 0.5 zi 2ci zi co 0 aus Elektroneutralitätsbedingungen Ionenstärke Constanze Donner / Ludwig Pohlmann 2010 28 Gouy ( 1910) –Chapman (1913) d 2 2FF I 2 e 0e r RT dx 2 d 2 2 dx 1 2 ( ) I 0.5 mit 1 : Debyelänge FU Berlin Constanze Donner / Ludwig Pohlmann 1 zi 2ci Ionenstärke 2F 2I e 0e r RT [ 1 m 2010 2 ] 29 Gouy ( 1910) –Chapman (1913) d 2 dx2 1 2 ( ) : Debyelänge mit 1 1 2F 2I e 0e r RT [ 1 m 2 ] Gibt an in welchem Abstand das Potential auf den e- ten Teil abgefallen ist. bzw. Dicke der diffusen Doppelschicht FU Berlin Constanze Donner / Ludwig Pohlmann 2010 30 Gouy-Chapman Wie verhält sich der Potentialabfall? Lösung der Differentialgleichung für x = x (x M exp s 0 Gibt an, wann M auf den e-ten Teil abgefallen ist 1 2 N Ae2 I e r e0 kT x FU Berlin Constanze Donner / Ludwig Pohlmann 2010 31 Gouy-Chapman Was gilt dann für die Raumladungsdichte in der Doppelschicht? Zur Erinnerung d 2 (x (x e re 0 dx2 e re 0 d 2 (x d 2 1 2 eoer ( ) M exp( x / ) dx2 dx2 ( x) 1 2 ( ) x (x M exp Unterschied Helmholtzschicht FU Berlin Constanze Donner / Ludwig Pohlmann 2010 32 Nullladungspotential Folgerungen: Potentialdifferenz = 0 Überschußladung = 0 =PZC Schichtdicke „Plattenkondensator“: Debye-Länge! Minimum der differentiellen Kapazität im Nulladungspotential: d 2z 2 e 2 e r e 0 n 0 ze 0 C cosh d0 kT 2kT FU Berlin Constanze Donner / Ludwig Pohlmann 2010 33 Nullladungspotential Folgerungen: Potentialdifferenz = 0 Überschußladung = 0 =PZC !!! Achtung: Keine 0V, kein open circuit potential OCP Q Schichtdicke „Plattenkondensator“: Debye-Länge! Minimum der differentiellen Kapazität im Nulladungspotential: 2 z 2e 2e r e 0 n 0 d ze 0 C cosh d 0 kTC 2kT FU Berlin Constanze Donner / Ludwig Pohlmann PZC 2010 34 Exkurs: Adsorption von Zusätzen Das Nullladungspotential steuert die potentialabhängige Adsorption von polaren und unpolaren Molekülen, welche selbst an der Reaktion nicht teilnehmen (Additive): Konzentration Polare Moleküle, positive Seite negativ Polare Moleküle, negative Seite unpolare Moleküle PZC positiv Das Nullladungspotential hat nichts mit dem Nernst-Potential zu tun, welches das elektrochemisch Gleichgewicht definiert! Und nichts mit 0 V FU Berlin Constanze Donner / Ludwig Pohlmann 2010 35 Synthese: GC + HH = Stern-Modell Limits des GC Modells: e ist nicht unabhängig von x H2O ca 78 und 6-8 am Metall Die Kapazitätswerte sind viel zu hoch in der Berechnung C ~ e Bei größereren Potentialdifferenzen versagt das Modell Bei großen Elektrolytkonzentrationen versagt das Modell Ionen sind keine Punktladungen FU Berlin Constanze Donner / Ludwig Pohlmann 2010 36 Synthese: HH + GC = Stern-Modell 1924 Limits GC und HH Das GC-Modell ist geeignet für die Nähe des Nullladungspotentials, das HH-Modell für größere Entfernungen davon Synthese HH-Schicht und die diffuse GC-Schicht sind geometrisch hintereinander angeordnet Logisch ist eine Synthese: Reihenschaltung beider Kondensatoren Modell von Stern 1888-1969 (1924): 1 1 1 H GC Cd Cd Cd (0 FU Berlin Constanze Donner / Ludwig Pohlmann 2010 37 Synthese: HH + GC = Stern-Modell 1924 Logisch ist eine Synthese: Reihenschaltung beider Kondensatoren Modell von Stern 1888-1969 (1924): Zetapotential M s (M H ) (H s ) Outer Helmholtz Plane Linearer Potentialabfall FU Berlin Exponentieller Abfall Constanze Donner / Ludwig Pohlmann 2010 38 Synthese: HH + GC = Stern-Modell 1924 Modell von Stern 1888-1969 (1924): M s (M H ) (H s ) Differentiation d (M s ) d (M H ) d (H s ) dqM dqM dqM 1 1 1 H GC Cd Cd Cd (0 FU Berlin Constanze Donner / Ludwig Pohlmann 2010 39 Stern-Modell 1924 Potential Entfernung von d. Grenzfläche qm = - qs = -( qH+qGC) FU Berlin Constanze Donner / Ludwig Pohlmann 2010 40 Stern-Modell FU Berlin Constanze Donner / Ludwig Pohlmann 2010 41 Stern-Modell Der kleinste Kondensator bestimmt, welche Kapazität im Experiment gemessen wird: 1 1 1 H GC Cd Cd Cd (0 CGC wird größer mit der Ionenstärke I, da die Ausdehnung der Doppelschicht kleiner wird; CHH gewinnt an Einfluss FU Berlin Constanze Donner / Ludwig Pohlmann 2010 42 Kapazitätsverlauf FU Berlin Constanze Donner / Ludwig Pohlmann 2010 43 Reale Doppelschicht FU Berlin Constanze Donner / Ludwig Pohlmann 2010 44 Portraits FU Berlin Constanze Donner / Ludwig Pohlmann 2010 45 Doppelschichten In allen Theorien wird nicht die spezifische (chemische) Wechselwirkung von Ionen mit der Elektrodenoberfläche betrachtet Elektrostatische WW: für NaF, NaClO4 etc- gute Übereinstimmung mit Theorie für Br-, J-, SO42-, Cl– - schlechte Übereinstimmung Weitere Einflüsse: Anionen und Kationen sind unterschiedlich hydratisiert Oberfläche ist hydratisiert an der Oberfläche wird die Wasserstruktur gebrochen Wasser ist ein Dipol mit chem. WW des Sauerstoffes LM FU Berlin Constanze Donner / Ludwig Pohlmann 2010 46 Doppelschichten Einige Abschätzungen und Betrachtungen: Immobilisierte Wasserdipole an der negativ geladenen Oberfläche führen durch Kompression kleine Kapazität, weil kleines e zur Elektrostriktion Stokes Radien der Ionen im Durchschnitt: 0.2-0.3 nm Wasser hat einen Radius von ca. 0.27 nm OHP ~ 0.47 -0.57 nm e 7; CM 12 F/cm2 Positive Oberfläche: Dicke der Schicht ist schmal (spez. Ad) = C wird größer FU Berlin Constanze Donner / Ludwig Pohlmann 2010 47 Doppelschichten Einige Abschätzungen und Betrachtungen: Elektrische Feldstärke E d dx U: extern angelegtes Potential FHH 0.8 M 0.1 M 0.01M PZC=0V FU Berlin 0 PZC Constanze Donner / Ludwig Pohlmann U vs NHE 2010 48 Doppelschichten- spezifische Adsorption ( Skizze: GC =Linear) Chemische WW – 3 Grenzfälle F Lösungspotential Evs NHE FU Berlin Constanze Donner / Ludwig Pohlmann 2010 49 Doppelschichten- Messmethoden Wechselspannungsmethoden – siehe auch Impedanzmethoden Messungen mit Gleichspannung – Strom- Spannungskurve im Doppelschichtbereich dq (CE) C E E C dt dt dt t Scan rate Kinetik Doppelschicht Elektrolyt FU Berlin Constanze Donner / Ludwig Pohlmann 2010 50 Doppelschichten- Messmethoden dq (CE) C E E C dt dt dt t Scan rate Kinetik Der capazitive Strom hängt linear von der Scanrate ab Er ist in der Regel viel kleiner als der Faradaysche Strom I q E FU Berlin Constanze Donner / Ludwig Pohlmann E 2010 51