4.21 Peptide und Proteine
Werbung
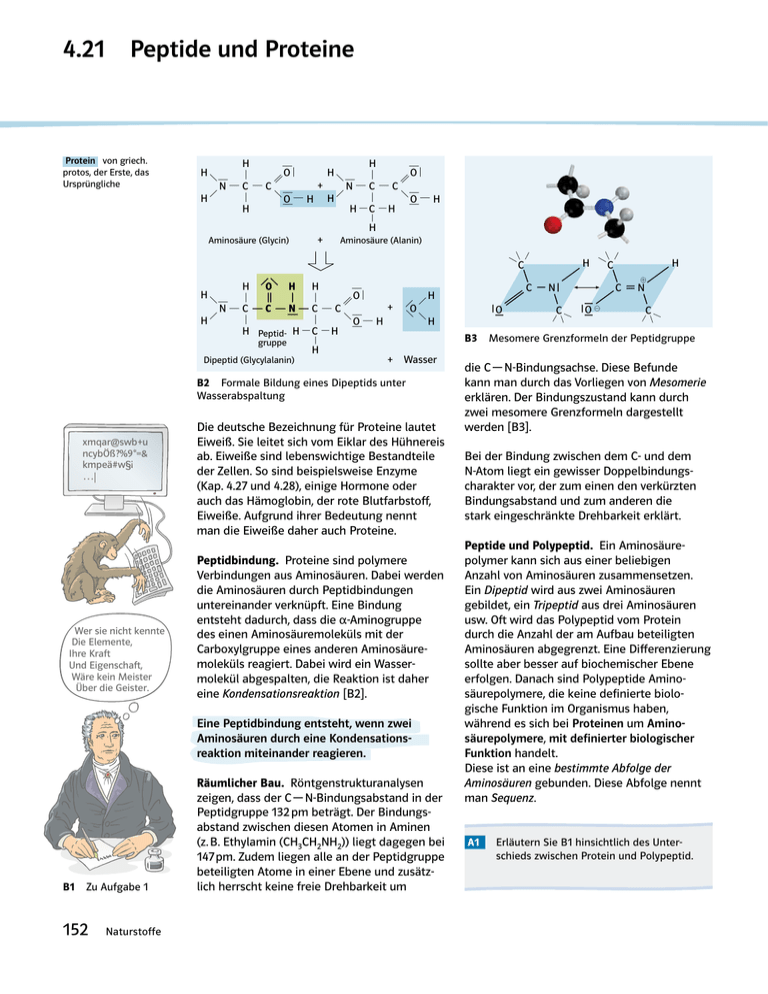
4.21 Peptide und Proteine 2 2 2 5 2 2 2 2 5 2 2 2 2 2 H H 2 2 H O O 2 2 + N2C 2C N2C 2C 2 2 H O2H H O2H 2 H H 2C 2H 2 H 2 Protein von griech. protos, der Erste, das Ursprüngliche H Aminosäure (Alanin) H + Wasser B2 Formale Bildung eines Dipeptids unter Wasserabspaltung xmqar@swb+u ncybÖß?%9*=& kmpeä#w§¡ … Wer sie nicht kennte Die Elemente, Ihre Kraft Und Eigenschaft, Wäre kein Meister Über die Geister. Die deutsche Bezeichnung für Proteine lautet Eiweiß. Sie leitet sich vom Eiklar des Hühnereis ab. Eiweiße sind lebenswichtige Bestandteile der Zellen. So sind beispielsweise Enzyme (Kap. 4.27 und 4.28), einige Hormone oder auch das Hämoglobin, der rote Blutfarbstoff, Eiweiße. Aufgrund ihrer Bedeutung nennt man die Eiweiße daher auch Proteine. Peptidbindung. Proteine sind polymere Verbindungen aus Aminosäuren. Dabei werden die Aminosäuren durch Peptidbindungen untereinander verknüpft. Eine Bindung entsteht dadurch, dass die a-Aminogruppe des einen Aminosäuremoleküls mit der Carboxylgruppe eines anderen Aminosäure­ moleküls reagiert. Dabei wird ein Wasser­ molekül abgespalten, die Reaktion ist daher eine Kondensationsreaktion [B2]. Eine Peptidbindung entsteht, wenn zwei Aminosäuren durch eine Kondensations­ reaktion miteinander reagieren. B1 Zu Aufgabe 1 152 Naturstoffe Räumlicher Bau. Röntgenstrukturanalysen zeigen, dass der C — N-Bindungsabstand in der Peptidgruppe 132 pm beträgt. Der Bindungs­ abstand zwischen diesen Atomen in Aminen (z. B. Ethylamin (CH3CH2NH2)) liegt dagegen bei 147 pm. Zudem liegen alle an der Peptidgruppe beteiligten Atome in einer Ebene und zusätzlich herrscht keine freie Drehbarkeit um 2 2 2 5 2 2 2 2 2 5 2 2 2 H ! 2 Dipeptid (Glycylalanin) H O H C 2 C 2N C 5 N2 2 O5 O @2 C C 2 2 2 2 Peptidgruppe H 2 22 2 2 2 H O H H 2 O 2 + N2C 2C 2N2C 2C 2 2 2H H O H H 2C 2H 2 H 2 C 2 + 2 Aminosäure (Glycin) B3 Mesomere Grenzformeln der Peptidgruppe die C — N-Bindungsachse. Diese Befunde kann man durch das Vorliegen von Mesomerie erklären. Der Bindungszustand kann durch zwei mesomere Grenzformeln dargestellt werden [B3]. Bei der Bindung zwischen dem C- und dem N-Atom liegt ein gewisser Doppelbindungs­ charakter vor, der zum einen den verkürzten Bindungsabstand und zum anderen die stark eingeschränkte Drehbarkeit erklärt. Peptide und Polypeptid. Ein Aminosäure­ polymer kann sich aus einer beliebigen Anzahl von Aminosäuren zusammensetzen. Ein Dipeptid wird aus zwei Aminosäuren gebildet, ein Tripeptid aus drei Aminosäuren usw. Oft wird das Polypeptid vom Protein durch die Anzahl der am Aufbau beteiligten Amino­säuren abgegrenzt. Eine Differenzierung sollte aber besser auf biochemischer Ebene erfolgen. Danach sind Polypeptide Amino­ säurepolymere, die keine definierte biologische Funktion im Organismus haben, während es sich bei Proteinen um Amino­ säurepolymere, mit definierter biologischer Funktion handelt. Diese ist an eine bestimmte Abfolge der Aminosäuren gebunden. Diese Abfolge nennt man Sequenz. A1 Erläutern Sie B1 hinsichtlich des Unterschieds zwischen Protein und Polypeptid. 4.22 Eigenschaften und Nachweis von Proteinen Bezeichnung Eigenschaften Vorkommen Albumine in Wasser löslich, gerinnen bei 65 °C im Eiklar, Blut, Fleischsaft, in Milch, Kartoffeln Globuline löslich in Salzlösungen, nicht löslich in Wasser im Eiklar, Blutplasma (Fibrinogen), in Muskeln, Milch Pflanzen­samen Skleroproteine (Gerüsteiweiß) unlöslich in Wasser und in Salzlösungen Bindegewebe, Knorpel, Knochen, Federn, Haare, Nägel, Naturseide B1 Vorkommen und Eigenschaften einiger wichtiger Proteine Überall im Organismus kommen Proteine vor. Sie erfüllen verschiedene Funktionen und müssen daher verschiedene Eigenschaften besitzen. Dennoch können sie mit den gleichen Reaktionen nachgewiesen werden, da sie alle Aminosäurepolymere sind und aufgrund der Peptidgruppen grundsätzlich einen gleichen Aufbau besitzen [B2]. Wegen ihrer unterschiedlichen Eigenschaften werden Proteine in drei verschiedene Gruppen eingeteilt [B1]. Der Tyndall-Effekt. Bestrahlt man eine klare Proteinlösung im abgedunkelten Raum mit einem dünnen Lichtstrahl [V1], erkennt man in der Proteinlösung einen deutlich abgegrenzten „Lichtstreifen“ (Kap. 8.9). Der Tyndall-Effekt zeigt, dass Proteinlösungen kolloidale Lösungen sind. O H ... N R1 C H C N H R2 O H H C N C O R3 C H ... C N H Farbreaktionen. Proteine können durch bestimmte Farbreaktionen erkannt werden. Die bekannteste Reaktion ist die Biuretreak­ tion [B3]. Dabei erhält man im Alkalischen nach Zugabe von Kupfer(II)-sulfat-Lösung zu einer Eiweißlösung eine violette Lösung [V2]. B3 Biuretreaktion. Violettfärbung von Kupfer(II)-sulfat-Lösung weist Eiweiß nach Für die Xanthoproteinreaktion benötigt man als Nachweisreagenz konzentrierte Salpetersäure. Es kommt zu einer charakteristischen Gelb­färbung [B4, V3]. V1 Man löst 0,5 g Gelatine in 200 ml warmem Wasser auf. Auf eine Taschenlampe wird eine Lochmaske aus Pappe (Lochdurchmesser ca. 0,5 cm) geklebt. Nach dem Verdunkeln des Raums wird die Lösung mit dem gebündelten Strahl von der Seite aus bestrahlt. V2 10 ml einer möglichst klaren Proteinlösung werden mit 10 ml Natronlauge versetzt. Anschließend gibt man einige Tropfen einer verdünnten Kupfer(II)-sulfat-Lösung (Fehling-I-Lösung) dazu. V3 Auf ein Stück eines hartgekochten Eies gibt man wenig konzentrierte Salpetersäure. B4 Xanthoprotein­ reaktion. Mit Salpetersäure ergibt sich eine Gelb­färbung B2 Allgemeiner Aufbau von Proteinen Naturstoffe 153 4.23 Struktur der Proteine — — H2N COOH … Asp—Pro—Ala—Arg—Ser—Tyr—Val—His—Glu—Phe—Lys—Gly—Asn—Ile… B1 Aminosäuresequenz mit Kürzeln dargestellt Bei Proteinen unterscheidet man bis zu vier Ebenen der Molekülstruktur: Die Primär-, die Sekundär-, die Tertiär- und die Quartärstruktur. Primärstruktur. Proteine sind Aminosäure­ polymere. Die Reihenfolge der einzelnen – durch Peptidbindung verknüpften – Aminosäuren, die das Protein aufbauen, bezeichnet man als Primärstruktur. Die Primärstruktur ist somit identisch mit der Aminosäuresequenz des Proteins. Um lange Namen für Proteine zu vermeiden, verwendet man für die am Aufbau beteiligten Aminosäuren die aus drei Buch­staben bestehenden Kürzel (Kap. 4.18). Per definitionem wird die Aminosäuresequenz so dargestellt, dass die freie Aminogruppe (N-terminales Ende) links steht und die Aminosäure mit der freien Carboxylgruppe (C-terminales Ende) rechts ist [B1]. Sekundärstruktur. Die Sekundärstruktur eines Proteins beschreibt räumliche Struktur­ elemente, die sich regelmäßig wiederholen. Die molekularen Ursachen für diese Regel­ mäßigkeit sind die Wasserstoffbrücken, die zwischen der C O- und der N — H-Gruppe einer anderen Peptidgruppe auftreten. Da in Proteinen sehr viele Wasserstoffbrücken auftreten, führt dies zu einem sehr starken Zusammenhalt im Molekül. a-Helix. Bei sehr großen Aminosäureresten ordnet sich die Polymerkette bevorzugt als a-Helix an. Dabei windet sich das Molekül schraubenförmig um seine Längsachse. Diese Wendel wird durch intramolekulare Wasser­ stoffbrücken zusammengehalten. Die a-Helix ist rechtsgängig, d. h. die Windungen der Proteinkette sind wie bei einem Korkenzieher angeordnet, die Aminosäurereste weisen nach außen [B2]. b-Faltblatt. Diese Variante der Sekundär­ struktur beruht auf intermolekularen Wasser­ stoffbrücken zwischen nebeneinander­ liegenden Proteinketten. Die Aminosäure­- reste stehen dabei abwechselnd oberhalb und unterhalb der Peptidgruppenebene [B3]. Oft treten in einem Proteinmolekül mehrere a-Helices und b-Faltblattstrukturen neben­einander auf [B4]. Der Rest des Protein­ moleküls bildet strukturell vielgestaltige Be­reiche mit Schlaufen oder spiraligen Struk­- turen. N-terminal R CH C H N HC O C N R CH C H N HC HC O H N C R R CH N H O C HC O H N C R R CH C-terminal B2 Die a-Helix wird durch Wasserstoffbrücken zwischen den Peptidbindungen stabilisiert (links), Schrägeinblick in Richtung der Längsachse der a-Helix (rechts) 154 Naturstoffe C-terminal R O H R O N-terminal B3 b-Faltblatt, eine Sekundärstruktur – unterschiedliche Darstellungsmöglichkeiten: Formel­ darstellung (links), Bändermodell (rechts) S t r u kt u r d e r P rot e i n e Exkurs BSE a-Helix und ß-Faltblatt (Pfeil weist in N ¥ CRichtung) innerhalb eines Moleküls B4 Proteinmolekül mit a-Helices und b-Faltblattstrukturen Unter der Primärstruktur eines Proteins ver­ steht man seine Aminosäuresequenz. Die Sekundärstruktur beruht auf dem Vorhanden­ sein von Wasserstoffbrücken. Die beiden Hauptformen dabei sind die a-Helix und die ß-Faltblattstruktur. Ende des 20. Jahrhunderts beunruhigte eine rätsel­ hafte Krankheit bei Rindern die Bevölkerung. Die Krankheit hatte den Namen BSE (Bovine Spongiforme Encephalopathie). Die Namens­ gebung beruhte auf der klinischen Symptomatik, da bei infizierten Rindern die Gehirnmasse schwammartig perforiert war. Medizinische Untersuchungen ergaben, dass die Ursache für diese Krankheit, die auch auf den Menschen übertragbar war, Proteine waren. Daher fasste man BSE mit vergleichbaren Krankheiten wie Scrapie (Schaf) oder nvCJD (Mensch) unter dem Begriff Prionen­ erkrankungen zusammen. Prion leitet sich aus dem Englischen ab (Protein­aceous Infectious particle) und bedeutet soviel wie infektiöses Protein. Das Protein existiert in einer normalen, gesunden Konformation und in einer krankheitsauslösenden. Der Unterschied liegt lediglich in der Sekundärstruktur. Während bei der gesunden Konformation der a-Helix-Anteil überwiegt, ist bei der krankheitsauslösenden Konformation der b-Faltblattanteil abnormal hoch [B5]. A1 Zeichnen Sie die Formel des Tetrapeptids mit folgender Primärstruktur: Ala — Ser — Arg — Trp. A2 Zeichen Sie die Formeln aller möglichen Dipeptide, die aus den Aminosäuren Alanin und Glycin gebildet werden können. A3 Ein Dipeptid ist aus den Aminosäuren Lysin und Valin (Lys — Val) aufgebaut. Begründen Sie, an welchem Stickstoffatom bevorzugt eine Protonierung stattfinden wird. A4 Recherchieren Sie im Internet, welche Proteine einen besonders hohen a-Helixbzw. b-Faltblattanteil haben. A5 Informieren Sie sich über die Krankheit Kuru. Beschreiben Sie die Ursache und Symptome der Krankheit. B5 Protein mit normaler Konformation (links), krankheitsauslösende Konformation (rechts) Solche Übergänge bei der Sekundärstruktur treten aber auch bei natürlichen Vorgängen auf. So wird z. B. aus der Helixstruktur der Moleküle von tierischer Wolle in feuchter Wärme unter Ein­ wirkung von Zugkraft eine glatte Faltblattstruktur, da Wasserstoffbrücken neu ausgebildet werden. Diesen Vorgang macht man sich u. a. beim Bügeln zunutze. Naturstoffe 155 Str u ktur der Proteine Exkurs Haarformung und Proteinstruktur Asn Viele Vorgänge, die beim Umformen von Haaren ab­laufen, lassen sich durch die Veränderung der Proteinstruktur erklären. Föhnfrisur. Haare sind sehr elastisch, besonders in feuchtem Zustand. Unter Zugbelastung wandelt sich die a-Helixstruktur des Keratins in eine b-Faltblattstruktur um. Dabei werden z. B. Bindungen zwischen Ammoniumund Carboxylatgruppen durch Hydratisierung gelöst und Wasserstoff­brücken geöffnet. Wird das Haar getrocknet, werden neue Bindungen und Wasserstoffbrücken zwischen benachbarten Proteinfäden ausgebildet. Die Veränderung bleibt bestehen, auch wenn die Zugbelastung nachlässt. Durch Einwirkung von Feuchtigkeit wird sie jedoch wieder rückgängig gemacht, die ursprüngliche a-Helixstruktur entsteht wieder. Föhnfrisuren sind nicht wetter­beständig. Dauerwelle. Die Verformung der Haare nach dem Dauerwellverfahren beruht darauf, dass Disulfid­brücken zwischen zwei Cysteinmolekülen von demselben oder von zwei verschiedenen Peptidsträngen geöffnet und nach gewünschter Form­gebung der Haare wieder geschlossen werden. Davon sind etwa 20 % der im Haar vorhandenen Disulfid­brücken betroffen. Im Gegensatz zur Föhn­ welle werden Elektronenpaarbindungen verändert. Die so erzielten Frisuren sind wetterfest und einige Monate haltbar. Beim Dauerwellverfahren laufen Redoxprozesse ab. Als Reduktionsmittel („Wellmittel“) wird in den meisten Fällen eine alkalische Lösung von Ammo­ niumthioglykolat (HS — CH2 — COO–NH4+ ) mit einem pH-Wert zwischen 7,5 und 8,5 eingesetzt. Als Oxidationsmittel („Fixiermittel“) wird Wasserstoffperoxid­ lösung (w = 1 bis 2 %) verwendet. Die Prozesse bei der Erzeugung einer Dauerwelle lassen sich in folgende Abschnitte gliedern: a) Öffnen der Disulfidbrücken: – NH4 + OOC — CH2 — SH + Disulfidbrücke Haar Reduktionsmittel („Wellmittel“): Cys — S — S — Cys + HS — CH2 — COO– NH4+ Ammoniumthioglykolat – – Cys — SH + HS — Cys + NH4 + OOC — CH2 — S — S — CH2 — COO NH4+ b) Legen der neuen Frisur und Ausspülen von überschüssigem Wellmittel. c) Schließen der Disulfidbrücken unter Verknüpfung von Cysteineinheiten, die durch das Legen der Frisur in die gewünschte Position gebracht werden: Oxidationsmittel („Fixiermittel“): CH2 C O N H H H H N O C CH2 CH2 Lys a-Helix CH2 CH2 CH2 CH2 N H H H O O C CH2 CH2 S S CH2 Phe Asp Ionenbindung Vander-WaalsKräfte Echte Bindungen 1. Disulfidbrücken: Sie entstehen, wenn zwei Cysteinreste miteinander reagieren. 2. Ionenbindung zwischen funktionellen Gruppen. Zwischenmolekulare Kräfte 3. Wasserstoffbrücken 4. Van-der-Waals-Kräfte Quartärstruktur. Bilden mehrere Proteinmoleküle eine gemeinsame Funktionseinheit, spricht man von einer Quartärstruktur. Dabei werden die einzelnen Proteinketten durch die gleichen Bindungskräfte zusammengehalten wie bei einer Tertiärstruktur. Das bekannteste Beispiel für ein Molekül mit Quartärstruktur ist das Hämoglobin [B7]. b1-Globulin + 2 H2O b2-Globulin Häm a1-Globulin Das Hämoglobin besteht aus vier Protein-Untereinheiten, an die zusätzlich je eine Hämgruppe gebunden ist. Nur diese Struktur kann Sauerstoff binden. a2-Globulin B7 Hämoglobin, Quartärstruktur Naturstoffe Disulfidbrücke Tertiärstruktur. Um die räumliche Anordnung aller Atome eines Proteins zu erklären, muss man die Wechselwirkungen zwischen den Amino­- säureresten berücksichtigen [B6]. Es ergibt sich die Tertiärstruktur. Ein Beispiel für eine Ter­tiär­- struktur ist in B4 abgebildet. Für die Aus­­- bildung der Tertiärstruktur sind von Bedeutung: Wasserstoffperoxid 156 Cys B6 Tertiärstruktur einer a-Helix. Verschiedene Wechselwirkungen können daran beteiligt sein Cys — SH + HS — Cys + H2O2 Cys — S — S — Cys Cys CH2 CH2 Gln Wasserstoffbrücken Phe 4.24 Denaturierung Die Veränderung der räumlichen Struktur eines Proteins bezeichnet man als Denaturierung. Häufig geht dabei auch die biologische Funktion des Proteins verloren. Dabei sind die Sekundär-, Tertiär- und damit eventuell auch die Quartärstruktur betroffen. Die Primär­ struktur ändert sich dabei in der Regel nicht. Eine Proteindenaturierung ist meistens ein nicht umkehrbarer Vorgang. Verschiedene Bedingungen führen zur Denaturierung von Proteinen: B1 Käseherstellung Hitze. Disulfidbrücken, Ionenbindungen, Wasserstoffbrücken und Van-der-Waals-Kräfte werden „aufgebrochen“ und es bilden sich an neuen bzw. anderen Stellen Bindungen bzw. zwischenmolekulare Kräfte aus. Dadurch ändern sich sowohl die räumlichen Verhältnisse innerhalb eines Proteinmoleküls als auch zwischen den Molekülen. Dadurch kommt es beispielsweise beim Braten eines Eies zu den bekannten Ergebnissen [B2]. pH-Wert. Durch die Protonierungen der Seitenketten ändern sich schlagartig die elektrischen Ladungsverhältnisse, sodass viele Bindungen auseinanderbrechen. Ein bekanntes Phänomen dafür ist das Koagulieren (flockig werden) des Milchproteins, wenn Milch sauer wird. Reduktionsmittel. Sie können Disulfidbrücken spalten. Dieser Vorgang kann umgekehrt werden, z. B. beim Dauerwellverfahren [Exkurs Haarformung und Proteinstruktur]. Salze bewirken das Aussalzen, einen Verlust der Hydrathülle. Viele Gemüsesorten werden vor der Zubereitung gesalzen, um Wasser zu entziehen und die Geschmacksintensität zu steigern. Dabei werden Proteine denaturiert. Schwermetallionen binden an Amino­ säurereste, stören so die elektrostatischen Wechselwirkungen und verändern die Tertiärstruktur. Darauf beruht die hohe Giftigkeit von Blei- und Quecksilbersalzen. Auch radioaktive Strahlung führt zur Denaturierung von Proteinen. B2 Braten eines Spiegeleis Als Denaturierung bezeichnet man die meist nicht umkehrbare Veränderung der räumlichen Struktur von Proteinen. Positive Aspekte der Denaturierung. Die Denaturierung von Proteinen hat nicht nur Nachteile, sie kann auch von Vorteil sein, z. B. wenn man in diesem Zusammenhang die Bereiche Ernährungsphysiologie und Lebensmitteltechnologie betrachtet. Proteine, die mit der Nahrung aufgenommen wurden, können nur dann von Enzymen (Kap. 4.27 und 4.28) abgebaut werden, wenn sie zuvor durch Hitze (Kochen, Braten) oder Säure (Salzsäure des Magens) denaturiert wurden. Bei der Käse­ herstellung [B1] werden die Caseine der Milch ent­weder durch Säure oder Lab (ein Enzym) ausgefällt. V1 Verrühren Sie das Eiklar eines Hühnereiweißes mit 200 ml Wasser. Geben Sie in Einzelversuchen zu je 5 ml des Filtrats a) 3 ml Salzsäure (c = 1 mol · l–1), b) 10 ml Ethanol, c) 2 g Ammoniumsulfat. A1 Informieren Sie sich, worum es sich beim „Autoklavieren“ handelt und welche Dinge bei diesem Vorgang beachtet werden müssen. Stellen Sie den Zusammenhang zwischen Autoklavieren und Denaturierung her. A2 a) Recherchieren Sie, welche Schutzfunktion Fieber für den Menschen hat. b) Begründen Sie, weshalb hohes Fieber über eine längere Zeitspanne lebens­ gefährlich sein kann. Naturstoffe 157











