Die Institute Institut für Molekulare Immunologie
Werbung

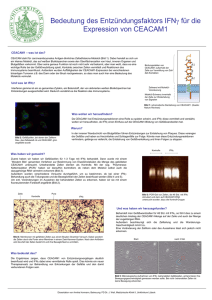
20.05.2005 9:37 Uhr Seite 165 Institut für Molekulare Immunologie Institute of Molecular Immunology München / Munich (Direktor / Director: Prof. Dr. Dolores J. Schendel) D ie Forschungsaktivitäten des Instituts bewegen sich im Grenzgebiet zwischen Hämatologie, Immunologie, Onkologie und Transplantationsbiologie. Hier werden Konzepte zur Modulation des Immunsystems mittels zell- und molekularbiologischer Methoden entwickelt. Untersucht werden neue Strategien der Immuntherapie und Gentherapie bei Krebs sowie bei Autoimmunerkrankungen und Transplantat-Abstoßungsreaktionen. Dabei kommen Tiermodelle und In-vitro-Studien mit isolierten Zellen des menschlichen Immunsystems zum Einsatz. Auf der Grundlage dieser Strategien werden in enger Kooperation mit medizinischen Fakultäten sowohl innerhalb als auch außerhalb Münchens klinische Studien entworfen und umgesetzt. Das Institut beteiligt sich am Programm Infektion und Immunität der HelmholtzGemeinschaft. Die Arbeiten werden federführend von Prof. Dr. D. J. Schendel, PD Dr. E. Nößner, PD Dr. C. S. Falk, Prof. Dr. R. Mocikat und Dr. E. Kremmer geleitet. Im Institut für Molekulare Immunologie arbeiten zum Jahresende 9 Wissenschaftler/ innen, 8 Nachwuchswissenschaftler/innen, davon 4 sonderfinanziert, und 10 Technische Assistenten/innen (3 sonderfinanziert) an immunologischen Projekten der Grundlagenforschung bzw. der anwendungsorientierten Forschung. 2 Doktoranden promovierten 2004 zum Dr. rer. nat. Als Beispiel unserer Forschungsaktivitäten im Jahr 2004 stellen wir jeweils ein Projekt aus der Arbeitsgruppe Monoklonale Antikörper sowie aus der Klinischen Kooperationsgruppe „Urologische Tumoren“ vor. Die Institute 165_170_imi_inst.qxd R esearch in the institute is focused on the intersecting field between haematology, immunology, oncology, and transplantation biology. Concepts are developed for modulating the immune system by means of cellular and molecular methods. New strategies are investigated for the immunotherapy and gene therapy of cancer, and the treatment of autoimmune diseases and transplant rejection reactions. The research uses both animal models and in vitro studies with isolated cells from the human immune system. Clinical studies based on these strategies are designed and carried out in close cooperation with medical faculties both in Munich and elsewhere. The Institute participates in the programme on ‘Infection and Immunity’ of the Helmholtz-Gemeinschaft. The research is coordinated by Prof. D. J. Schendel, PD Dr. E. Nößner, PD Dr. C. S. Falk, Prof. R. Mocikat, and Dr. E. Kremmer. At the Institute there are currently 9 scientists and 8 junior scientists, 4 of them supported by research grants, and 10 technicians (3 supported by grant funds) involved in basic and applied immunological research. In 2004, 2 students were awarded their doctorates (Dr. rer. nat.). As an example of our activities in 2004 we present projects from our ‘Monoclonal Antibodies’ Group and the Clinical Cooperation Group ‘Urological Tumours’. GSF 165 165_170_imi_inst.qxd 20.05.2005 9:37 Uhr Seite 166 Untersuchungen zur Genexpression in neuronalen Geweben mittels monoklonaler Antikörper Elisabeth Kremmer, Christine Hennard, Anna Malamid und Ralph Mocikat Eine der bedeutendsten Herausforderungen für die biomedizinische Forschung in den nächsten Jahren besteht darin, den im Rahmen des Humangenomprojektes identifizierten und sequenzierten menschlichen Genen Funktionen zuzuweisen. Im Allgemeinen geschieht dies durch Methoden der Proteomik, durch transgene Tiermodelle sowie durch Suche nach homologen Genen, deren Funktion bekannt ist, in anderen Spezies. Ein wichtiger Modellorganismus ist dabei der Zebrafisch, da er leicht handhabbar ist, eine kurze Generationszeit aufweist und durchsichtig ist, so dass Entwicklungsvorgänge am lebenden Tier beobachtet werden können. Wir interessierten uns für Gene und die zugehörigen Genprodukte, die in neuronalen Geweben des Zebrafisches exprimiert werden, für deren Expressionsmuster während der Embryonalentwicklung sowie für die Frage, ob es homologe Genprodukte in anderen Spezies gibt. Zu diesem Zweck wurden monoklonale Antikörper hergestellt, mit deren Hilfe die entsprechenden Proteine in Gewebeschnitten, im Western-Blot, in der Immunpräzipitation sowie in Expressionsgenbanken detektiert werden konnten. Nach Immunisierung von Ratten mit Gehirngewebe des Zebrafisches wurden aus den Milzen der immunisierten Tiere Antikörper-produzierende Hybridom-Zelllinien etabliert. Für weitere Untersuchungen wurden nur die Antikörper ausgewählt, die in histologischen Schnitten mit neuronalen Strukturen des adulten oder embryonalen Zebrafisches reagierten. Um herauszufinden, um welche Moleküle es sich bei den im Nervengewebe exprimierten, von den Antikörpern spezifisch erkannten Proteinen handelte, wurden zwei Methoden angewandt: Einerseits wurde mit den Antikörpern eine Phagen-Expressionsgenbank abgesucht, welche aus Zellen von drei Tage alten Zebrafischen generiert worden war. Die Gene, deren Produkte von den Antikörpern 166 GSF erkannt wurden, wurden isoliert und sequenziert. Andererseits wurden die Proteine mit Hilfe der Antikörper aus Zelllysaten des Fischgehirns immunpräzipitiert oder nach Western-Blot-Analysen aus präparativen Proteingelen isoliert. Die isolierten Proteine wurden dann der Massenspektrometrie zugeführt. Die dabei gefundenen Peptide wurden mit Datenbanken verglichen, so dass die zugehörigen Proteine identifiziert werden konnten. Um Hinweise auf die phylogenetische Konservierung der im Zebrafisch erkannten Zielstrukturen zu gewinnen, wurden die in den beiden Ansätzen verwendeten monoklonalen Antikörper an Geweben anderer Spezies immunhistologisch getestet. Tatsächlich zeigten sich Kreuzreaktionen zwischen neuronalen Strukturen des Zebrafisches und solchen des Menschen, der Ratte oder der Maus. Ein Protein, das im Laufe unserer Arbeiten mit Hilfe von Immunpräzipitation und Massenspektrometrie identifiziert werden konnte, stellte sich als Tenascin-R heraus. Tenascin-R ist Bestandteil der extrazellulären Matrix. Es interagiert mit Proteoglykanen und wird vor allem während früher Stadien der Entwicklung exprimiert. Es wird mit Prozessen der Zellmigration, der Axonentwicklung und der Synapsenbildung in Verbindung gebracht. Der dagegen gerichtete Antikörper färbt im Zebrafisch Strukturen des zentralen Nervensystems an. Abbildung 1 zeigt die Färbung an einem elf Tage alten Rattenembryo. Untersuchungen an anderen Spezies ergaben, dass der Antikörper z.B. auch das entsprechende Protein von Maus, Ratte und Mensch detektiert. Mittels der Phagen-Expressionsgenbank konnte das Protein VAT-1 identifiziert werden. Dieses Protein wurde erstmals im Zitterrochen beschrieben und soll dort eine Rolle bei der Nerven-Signalübertragung spielen. Dementsprechend färbt der Antikörper, der dieses Protein erkennt, beim zwölf Tage alten Fisch Gehirn, Rückenmark und Retina an (Abb. 2). Obwohl homologe Proteine auch in Säugetieren gefunden wurden, konnte eine Kreuzreaktion des Antikörpers mit anderen Spezies nicht beobachtet werden. Die Funktion der zu VAT-1 homologen Säugerproteine ist noch unbekannt. Der Genort beim Men- 20.05.2005 9:37 Uhr Seite 167 Die Institute 165_170_imi_inst.qxd Abb. 1. Anfärbung von Tenascin-R in den Gehirnstrukturen eines elf Tage alten Rattenembryos mit Hilfe eines monoklonalen Antikörpers, der durch Immunisierung mit Gehirnzellen des Zebrafisches generiert wurde. Vergrößerung 2,5 x. Abb. 2. Anfärbung von VAT-1 in Gehirn, Rückenmark und Retina eines zwölf Tage alten Zebrafisches. schen liegt interessanterweise im Bereich des BRCA-1-Gens, das mit der neoplastischen Entartung von Mamma und Ovar in Verbindung gebracht wurde. Unsere Arbeiten leisten einen Beitrag zur Genom- und Proteomforschung. Wir konnten zeigen, dass monoklonale Antikörper ein wichtiges Werkzeug sind, mit deren Hilfe die Funktion menschlicher Gene aufgeklärt werden kann. ron-α) mit Ansprechraten von 30 %. Die relativ hohe Ansprechrate auf eine unspezifische Immuntherapie wird als Hinweis gewertet, dass das Nierenzellkarzinom, ähnlich dem Melanom, ein immunogener Tumor ist. Folgerichtig wird in vielen Arbeitsgruppen an einer Verbesserung von Immuntherapien für das Nierenzellkarzinom gearbeitet. Im Rahmen unserer Klinischen Kooperationsgruppe arbeiten wir vorwiegend an der Etablierung und klinischen Umsetzung von aktiven Vakzinierungsstrategien. So befindet sich momentan die gentechnisch optimierte Vakzine RCC-26 IL2/CD80 in der klinischen Erprobung. Ferner wird auch die Nutzung von dendritischen Zellen zur aktiven Vakzinierung von Tumorpatienten im Labor intensiv untersucht. Unabhängig von der Verbesserung der Immuntherapie wäre es äußerst wünschenswert, tumorbezogene prognostische Parameter zu haben, die eine individuelle Abschätzung des Ansprechens eines Patienten auf eine adjuvante Immuntherapie erlauben. Mit hoher Wahrscheinlichkeit sind Immunevasions-Mechanismen der Tumoren für das Scheitern von adjuvanten Immuntherapien bei RCC-Patienten verantwortlich; eine bessere Kenntnis dieser Toleranzmechanismen wäre daher von hoher klinischer Relevanz. Ein Molekül, das in diesem Zusammenhang in den letzten Jahren eine stetig wachsende Bedeutung erlangt hat, ist das Klinische Kooperationsgruppe „Immuntherapien bei urologischen Tumoren“ Transiente Expression des Tumorsuppressors CEACAM1 als ImmunevasionsMechanismus beim Nierenzellkarzinom Robert Kammerer, Julia Schleypen und Heike Pohla Das Nierenzellkarzinom (RCC) führt in Deutschland zu ca. 12 000 Neuerkrankungen jährlich. Etwa 30 % der Patienten haben zum Diagnosezeitpunkt bereits Metastasen, weitere 30 % entwickeln sie im weiteren Verlauf. Wegen weitgehender Strahlen- und Chemoresistenz existiert als einzige etablierte systemische Therapieoption eine kostenintensive und nebenwirkungsreiche unspezifische Immuntherapie auf der Basis von Zytokinen (meist Interleukin-2 und Interfe- GSF 167 165_170_imi_inst.qxd 20.05.2005 9:38 Uhr Seite 168 g a 200 µm 100 µm A B t 200 µm C D 50 µm Abb. 3: Immunhistologische Färbung von Normalnierengewebe (A), papillärem Adenom (B), klarzelligem Nierenzellkarzinom (C) und einer Lungenmetastase (D) mit CEACAM1-spezifischen Antikörpern. Für die Detektion wurden Peroxidase-konjugierter anti-Maus-Ig-Antikörper und 3-Amino-9-EthylCarbazol verwendet, gegengefärbt wurde mit Mayer’s Hämalaun. Das Normalgewebe zeigt CEACAM1Expression in den Glomeruli (g), endothelialen Zellen () und proximalen Tubuli (). Tumorgewebe (t) zeigt CEACAM1-Expression nur in den Endothelzellen und infiltrierenden Granulozyten (Kontrollfärbungen mit Markern für Endothelzellen und Granulozyten hier nicht gezeigt). CEACAM1-negativ sind die distalen Tubuli () und die Epithelzellen des Adenoms (a). CEACAM1, ein Zelladhäsionsmolekül aus der Familie der karzinoembryonalen Antigene (CEA). CEACAM1 wird u.a. auf Epithelzellen, T-Zellen, natürlichen Killer(NK)-Zellen sowie dendritischen Zellen exprimiert. CEACAM1 spielt eine Rolle bei der Zell/ZellKommunikation, da es nach Ligandenkontakt der Zelle regulatorische Signale vermittelt. Als zelluläre Liganden wurden CEACAM1 selbst und CEA/CEACAM5 identifiziert. Auf Tumorzellen scheint es interessanterweise eine Zelltyp-spezifische Funktion auszuüben. So ist bekannt, dass CEACAM1 in verschiedenen Karzinomen eine Tumorsuppressorfunktion ausübt und dementsprechend in diesen Tumoren herunterreguliert ist. Überraschenderweise 168 GSF konnte jedoch kürzlich gezeigt werden, dass beispielsweise beim malignen Melanom die De-novo-Expression von CEACAM1 mit einer deutlich schlechteren Prognose korreliert. Vermutlich beruht dies darauf, dass CEACAM1-exprimierende Melanomzellen in der Lage sind, die zytotoxische Aktivität von NK-Zellen zu inhibieren und so der Überwachung durch das Immunsystem zu entkommen. Die Expression von CEACAM1 im RCC wurde bisher noch nicht untersucht. Da die meisten monoklonalen Antikörper gegen CEACAM1 mit anderen CEA-Familienmitgliedern kreuzreagieren, haben wir mittels genetischer Immunisierung einen neuen CEACAM1-spezifischen monoklonalen Antikörper (8G5) hergestellt. Mit diesem 20.05.2005 9:38 Uhr Seite 169 Antikörper konnten wir die CEACAM1Expression im Normalgewebe der tumortragenden Niere immunhistochemisch bestimmen. Es zeigte sich, dass CEACAM1 in vereinzelt angetroffenen Granulozyten, den Endothelzellen der Nierenkapillaren und den epithelialen Zellen der proximalen Tubuli, von denen sich das klarzellige RCC ableitet, exprimiert wird (Abb. 3). Völlig überraschend war deshalb der Befund, dass in keinem der 35 untersuchten RCC eine CEACAM1Expression in den Tumorzellen nachweisbar war. Im Tumor war CEACAM1 ausschließlich auf Endothelzellen und tumorinfiltrierenden Granulozyten zu finden. Ebenso wie im Primärtumor zeigten die Tumorzellen in Metastasen oder in Nierenzellthromben der Vena Cava kein CEACAM1-Protein. Da wir selbst in Adenomen der Niere einen kompletten Verlust der CEACAM1-Expression beobachteten, muss man davon ausgehen, dass die Herunterregulation von CEACAM1 ein äußerst frühes Ereignis während der Tumorgenese darstellt. (Abb. 4). RT-PCR-Analysen zeigten, dass die CEACAM1-Expression auf Transkriptionsebene reguliert wird, jedoch nur transient ist und nach Entzug von IFN-γ innerhalb von 6 Tagen wieder vollständig eingestellt wird. Da auch in frisch isolierten Tumorzellen durch IFN-γ eine CEACAM1-Expression induziert werden kann, muss man davon ausgehen, dass diese Hochregulation auch in vivo während einer gegen den Tumor gerichteten Immunreaktion stattfindet. Expression von CEACAM1 auf tumorinfiltrierenden Lymphozyten Die Institute 165_170_imi_inst.qxd Die vorübergehende Expression von CEACAM1 in RCC-Zellen könnte zu einer A CaKi 2 bp – A498 + – RCC26 + – IFN-γ CEACAM1-4L + 600 CEACAM1-4S 300 CEACAM1-3L CEACAM1-3S 900 GAPDH Regulation der CEACAM1-Expression B In Übereinstimmung mit den immunhistologischen Ergebnissen an Tumorschnitten zeigen auch RCC-Zelllinien einen Verlust der CEACAM1-Expression. Eine Rolle des CEACAM1 bei der Interaktion der Tumorzellen mit Zellen des Immunsystems erscheint daher eher unwahrscheinlich. Um dies zu verifizieren, haben wir einen Angriff aktivierter zytotoxischer T-Zellen gegen die Tumorzellen in vitro simuliert und die CEACAM1Expression zu verschiedenen Zeitpunkten der Interaktion bestimmt. Dabei stellte sich heraus, dass die Herunterregulation des CEACAM1 auf den Tumorzellen reversibel ist, da nach einer dreitägigen Kokultur von allogenen CD8+-T-Zellen mit den RCC-Zelllinien A498 und RCC26 diese eine deutliche CEACAM1-Expression zeigten. In gleicher Weise konnte eine Hochregulation von CEACAM1 auf den zytotoxischen T-Zellen (CTL) beobachtet werden, was auf einer Allo-Aktivierung dieser Zellen beruht. Die Hochregulation auf den Tumorzellen könnte durch das von den aktivierten CTL sezernierte IFN-γ induziert werden. In der Tat ist die Stimulation der RCC-Zelllinien mit IFN-γ ausreichend, um CEACAM1 zu induzieren 64 88 – IFN-γ 0 100 101 102 + IFN-γ 103 0 100 CEACAM1 101 102 103 C 265 0 0 10 0d 101 265 102 0 0 10 3d 101 102 CEACAM1 265 0 0 10 6d 101 102 Abb. 4: CEACAM1-Expression ist durch IFN-γ in RCC-Linien und primären RCC-Zellen induzierbar. (A) RT-PCR-Analyse der vier wichtigsten CEACAM1Spleißvarianten von mRNA aus 106 Zellen +/500 U/ml IFN-γ. Insbesondere die Spleißvarianten für den langen zytoplasmatischen Anteil sind induzierbar. Gezeigt ist zur quantitativen Abschätzung auch die GAPDH-Kontrollamplifikation. (B) Durchflusszytometrische Analyse primärer RCC-Zellen nach 3 Tagen +/- 500 U/ml IFN-γ. (C) Analyse der transienten CEACAM1-Expression auf einer RCC-Zelllinie an Tag 0, Tag 3 und Tag 6 nach 3-tägiger Kultivierung mit IFN-γ (= 0 d). GSF 169 165_170_imi_inst.qxd 20.05.2005 9:38 Uhr Seite 170 Inhibition von zytotoxischen tumorinfiltrierenden Lymphozyten (TIL) führen und so einen Immunevasions-Mechanismus für das RCC darstellen. Dieser Mechanismus kann jedoch nur dann wirksam sein, wenn auch die TIL CEACAM1 exprimieren. Eine solche Expression konnten wir bei den immunhistochemischen Untersuchungen jedoch nicht beobachten. Dies könnte darauf beruhen, dass die TIL im Tumor in Anergie verharren. Durchflusszytometrische Analysen ergaben, dass etwa 90 % der TIL T- oder NK-Zellen waren, wobei die NK-Zellen einen Anteil von 7– 40 % ausmachten. Auch diese Analysen ergaben, dass nur wenige TIL minimale Mengen CEACAM1 exprimieren; die NKZellen waren vollständig negativ für CEACAM1. Allerdings führte die Stimulation mit IL-2 zu einer Expression von CEACAM1 auf der Mehrheit der T- und NK-Zellen. Zusammenarbeit Bedeutung der Ergebnisse Die Hoffnung, die Erfolgsaussichten einer Immuntherapie anhand der CEACAM1Expression im RCC individuell abschätzen zu können, hat sich nicht erfüllt. Dagegen haben diese Untersuchungen gezeigt, wie wichtig für die erfolgreiche Anwendung von Tumorimmuntherapien eine genaue Kenntnis von Immunevasions-Mechanismen ist. In erster Linie sollte der Dynamik der TumorImmunzell-Interaktion deutlich mehr Beachtung geschenkt werden. So könnte man sich z.B. vorstellen, dass nicht die bestehende CEACAM1-Expression im Tumorgewebe, wohl aber das Maß der CEACAM1-Induzierbarkeit ein prognostischer Faktor für den Erfolg einer Immuntherapie beim RCC ist. Im Hinblick auf die Therapie legen die Ergebnisse dieser und weiterer Untersuchungen nahe, die Immunantwort gegen Tumorzellen durch Blockierung der CEACAM1Funktion (z. B. durch inhibierende Antikörper) zu verbessern. Experimente, in denen solche Ansätze überprüft werden sollen, werden gegenwärtig durchgeführt. Ausgewählte Veröffentlichungen Sieben Mitarbeiter/innen sind am Lehrbetrieb der Ludwig-Maximilians-Universität beteiligt. Die Institutsleiterin ist Koordinatorin des HGF-Programms „Infektion und Immunität“ für die GSF und stellvertretende Sprecherin eines DFG-Sonderforschungsbereichs (SFB 455). Arbeitsgruppen des Instituts sind an insgesamt vier Sonderforschungsbereichen beteiligt. Kolb, H.J., Schmid, C., Barrett, A.J., Schendel, D.J.: Graftversus-leukemia reactions in allogeneic chimeras. Blood, 103, 767-776 (2004) Fünf Klinische Kooperationsgruppen, die Abteilung Genexpression sowie ein GMP-Labor sind dem Institut angeschlossen. Roth, W., Sustmann, C., Kieslinger, M., Gilmozzi, A., Irmer, D., Kremmer, E., Turck, C., Grosschedl, R.: PIASyDeficient Mice Display Modest Defects in IFN and Wnt Signaling. J. Immunol., 173, 6189-6199 (2004) Die Arbeiten des Instituts werden mit Drittmitteln der EU, der DFG, der Wilhelm-Sander-Stiftung, der MildredScheel-Stiftung für Krebsforschung und der Else-KrönerFresenius-Stiftung gefördert. Es bestehen direkte Kooperationen mit verschiedenen HGF-Zentren (DKFZ Heidelberg, MDC Berlin). Daneben bestehen intensive Kooperationen mit der Urologischen Klinik und Poliklinik und der III. Medizinischen Klinik der Ludwig-Maximilians-Universität, mit dem Institut für Experimentelle Onkologie und Therapieforschung der Technischen Universität München sowie mit der Hautklinik bzw. dem Institut für Zellbiologie, Abt. Immunologie, der Eberhard-Karls-Universität Tübingen. 170 GSF Misslitz, A., Pabst, O., Hintzen, G., Ohl, L., Kremmer, E., Petrie, H.T., Forster, R.: Thymic T cell development and progenitor localization depend on CCR7. J. Exp. Med. 200, 481-491 (2004) Schleypen, J.S., von Geldern, M., Weiss, E.H., Kotzias, N., Rohrmann, K., Schendel, D.J., Falk, C.S.*, Pohla, H*.: Renal cell carcinoma-infiltrating natural killer cells express differential repertoires of activating and inhibitory receptors and are inhibited by specific HLA class I allotypes. (* gleicher Beitrag) Int. J. Cancer. 106, 905-912 (2003) Ulbrecht, M., Maier, S., Hofmeister, V., Falk, C.S., Brooks, A.G., McMaster, M.T., Weiß, E.H.: Truncated HLA-G isoferms are retaiend in endoplasmatic reticulum and insufficient provide HLA-E ligands. Hum. Immunol. 65, 200-2008 (2004)