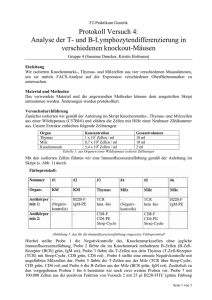
Zytotoxische Funktion von T-Lymphozyten gegen Melanomzellen
Werbung

Zytotoxische Funktion von T-Lymphozyten gegen Melanomzellen nach in vitro Stimulation mit einem Melanoma chondroitin sulfate proteoglycan (MCSP)xCD3 bispezifischen Antikörper Der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg zur Erlangung des Doktorgrades Dr. med. vorgelegt von Stefan Heinrich aus München Als Dissertation genehmigt von der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg Tag der mündlichen Prüfung: 14.10.2013 Vorsitzender des Promotionsorgans: Prof. Dr.med. Jürgen Schüttler Gutachter: Prof. Dr. med. Andreas Mackensen Prof. Dr. med. Armin Gerbitz Meinen Eltern Meinem Bruder Meiner Freundin Inhaltsverzeichnis 1 Zusammenfassung und Abstract ..................................................................... 6 1.1 Zusammenfassung ............................................................................................... 6 1.1.1 Hintergrund und Ziele ....................................................................................................... 6 1.1.2 Methoden............................................................................................................................. 6 1.1.3 Ergebnisse und Beobachtungen....................................................................................... 6 1.1.4 Praktische Schlussfolgerungen ......................................................................................... 7 1.2 2 1.2.1 Background and Objectives .............................................................................................. 7 1.2.2 Methods ............................................................................................................................... 8 1.2.3 Results .................................................................................................................................. 8 1.2.4 Conclusions ......................................................................................................................... 8 Einleitung ......................................................................................................... 9 2.1 Immunsystem ....................................................................................................... 9 2.2 Malignes Melanom .............................................................................................. 13 2.2.1 Klinische Bedeutung und Epidemiologie ..................................................................... 13 2.2.2 Standardtherapieverfahren und Prognose .................................................................... 16 2.2.3 Experimentelle Therapieansätze .................................................................................... 18 2.2.4 Tumorimmunologie ......................................................................................................... 20 2.2.5 Antikörpertherapie ........................................................................................................... 23 2.3 3 Abstract ................................................................................................................. 7 Zielsetzung der Arbeit .........................................................................................28 Material und Methoden ..................................................................................29 3.1 Material ................................................................................................................29 3.1.1 Medien, Puffer und Lösungen........................................................................................ 29 3.1.2 Peptid-MHC-Tetramere .................................................................................................. 30 3.1.3 Antikörper ......................................................................................................................... 30 3.1.4 Bispecific T Cell Engagers (BiTEs) ............................................................................... 31 3.1.6 Oligonukleotide ................................................................................................................ 32 3.1.7 Zellkulturflaschen, -platten und -röhrchen .................................................................. 32 3.1.8 Zelllinien ............................................................................................................................ 33 3.1.9 Software ............................................................................................................................. 33 3.2 Methoden .............................................................................................................34 3.2.1 Ermittlung der Zellzahl durch Trypanblaufärbung..................................................... 34 3.2.2 Kryokonservierung von Zellen ...................................................................................... 34 3.2.3 Auftauen von Zellen ........................................................................................................ 34 3.2.4 Kultivieren von Zelllinien ............................................................................................... 35 4 3.2.5 Durchflusszytometrie und Zellsortierung .................................................................... 36 3.2.6 Antikörperfärbung ........................................................................................................... 36 3.2.7 Dichtegradientenzentrifugation ..................................................................................... 37 3.2.8 Isolierung von Gesamt-RNA ......................................................................................... 38 3.2.9 Reverse Transkription ..................................................................................................... 38 3.2.10 Quantitative Polymerase-Kettenreaktion (qPCR) .................................................... 38 3.2.11 Enzyme Linked Immunosorbent Assay (ELISA) .................................................... 39 3.2.12 51Chrom-Zytotoxizitätstest ........................................................................................... 40 Ergebnisse ....................................................................................................... 41 4.1 Charakterisierung der Melanomzelllinien .......................................................... 41 4.1.1 Expression von LMP-2/-7 und TAP-1/-2 in Melanomzelllinien ............................ 42 4.1.2 Expression von immunologisch relevanten Proteinen in Melanomzelllinien ........ 43 4.1.3 Sekretion von IL-10 in Melanomzelllinien ................................................................... 44 4.2 T-Zell vermittelte Immunantwort mit und ohne BiTEs.....................................45 4.2.1 Charakterisierung spezifischer CD8+-T-Zell-Klone ................................................... 45 4.2.2 Zytotoxizität von klonalen T-Zellen gegen Melanomzellen ...................................... 45 4.3 Tumor-Immune-Escape durch eine BiTE induzierte Immunantwort ..............48 4.3.1 Effekt auf die Melanomzelllinie Mel ImSi .................................................................... 49 4.3.2 Effekt auf die Melanomzelllinie A2058 ........................................................................ 50 4.3.3 Effekt auf die Melanomzelllinie Mel624 ....................................................................... 52 4.4 Zytotoxisches Potential verschiedener T-Zell-Subpopulationen nach BiTE induzierter Stimulation .................................................................................................59 5 Diskussion .......................................................................................................60 6 Literaturverzeichnis ........................................................................................75 7 Abkürzungsverzeichnis ...................................................................................93 8 Danksagung ....................................................................................................96 6 1 Zusammenfassung und Abstract 1.1 1.1.1 Zusammenfassung Hintergrund und Ziele Das maligne Melanom der Haut gehört zu den Tumoren, dessen Inzidenz in den letzten Jahren am stärksten zugenommen hat. 80% aller Todesfälle durch Hautkrebs sind auf ein malignes Melanom zurückzuführen. Die mediane Überlebenszeit von Patienten im Stadium IV beträgt derzeit nur vier bis sechs Monate und kein Therapeutikum, mit Ausnahme von Ipilimumab, konnte diese bis dato effektiv verlängern. Einen neuartigen Therapieansatz für die Behandlung des malignen Melanoms stellen Bispecific T Cell Engagers (BiTEs) dar. Hierbei handelt es sich um ein bispezifisches Antikörperkonstrukt, das sowohl CD3 als auch das gewünschte TAA bindet. T-Zellen können so vorübergehend an die Zielzelle binden und nach Aktivierung diese lysieren. In der vorliegenden Arbeit soll die zytotoxische Funktion von T-Lymphozyten gegen Melanomzellen nach Stimulation mit einem MCSPxCD3 BiTE in vitro untersucht werden. 1.1.2 Methoden Melanomzelllinien wurden in vitro kultiviert und mittels PCR, FACS und ELISA auf Mutationen der APM, die Expression immunologisch relevanter Proteine bzw. die Sekretion immunsuppressiver Faktoren untersucht. Mittels 51Chrom-Release wurde die zytotoxische Funktion von drei CD8+-T-Zell-Klonen gegen Melanomzellen ohne BiTE, mit Kontroll-BiTE oder mit MCSP-BiTE bestimmt. Des Weiteren wurden Melanomzelllinien mit klonalen CD8+-T-Zellen in An- bzw. Abwesenheit von KontrollBiTE oder MCSP-BiTE inkubiert. Die überlebenden Melanomzellen wurden anschließend erneut charakterisiert und ihre Sensitivität gegenüber einem T-Zell mediierten Kill im 51Chrom Release bestimmt. Außerdem wurden verschiedene CD3+-TZell-Subpopulationen von gesunden Spendern mittels Zellsorting isoliert und im 51 Chrom Release auf ihr Potential getestet, eine BiTE induzierte Immunantwort gegen Melanomzellen zu vermitteln. 1.1.3 Ergebnisse und Beobachtungen Alle untersuchten Melanomzelllinien exprimierten MCSP und ließen sich von klonalen T-Zellen in Anwesenheit von MCSP-BiTE lysieren. Mutationen der APM, die 7 Expression bekannter immunologisch relevanter Proteine wie PD-L1 und lösliche, immunsuppressive Faktoren wie IL-10 hatten hierauf keinen Einfluss. In Kokulturexperimenten, in denen Melanomzellen über antigenspezifische T-Zellen lysiert wurden, konnte durch die Zugabe von MCSP-BiTE keine Steigerung der Zytotoxizität erzielt werden. Für eine Melanomzelllinie konnte exemplarisch gezeigt werden, dass Melanomzellen, die eine MCSP-BiTE vermittelte Immunreaktion überlebt hatten, in der Folge eine verminderte Expression von MCSP aufwiesen. Diese Zellen waren gegenüber einem MCSP-BiTE mediierten Kill weniger sensitiv als die entsprechende Kontrolle. Alle aus MNCs isolierten CD3+-T-Zell-Subpopulationen waren in der Lage, eine MCSP-BiTE mediierte Immunantwort gegen Melanomzellen zu vermitteln. 1.1.4 Praktische Schlussfolgerungen Die vorliegenden Daten lassen darauf schließen, dass MCSP-BiTEs eine wirkungsvolle Lyse von MCSP positiven Melanomzellen durch T-Zellen, unabhängig von verschiedenen immunologischen Faktoren, induzieren können. BiTEs stellen somit ein neuartiges, wirkungsvolles Therapeutikum für die Behandlung von Patienten mit malignem Melanom dar. Von Bedeutung sind die Ergebnisse zu den Melanomzellen, die einer BiTE vermittelten Lyse entkommen sind und in der Folge das MCSP Antigen herunterreguliert haben. Hierbei handelt es sich um einen bisher in der Literatur noch nicht beschriebenen Tumor-Immune-Escape-Mechanismus. 1.2 Abstract 1.2.1 Background and Objectives The incidence of malignant melanoma of the skin has increased rapidly within the last years. 80% of skin cancer related deaths are caused by malignant melanomas. The median survival time of stage IV patients ranges between four to six months and no drug except Ipilimumab has ever shown to effectively prolong overall survival. A novel therapeutic approach for the treatment of patients with malignant melanoma could be BiTEs. This class of bispecific antibodies is specific for CD3 and a selected tumour associated antigen, enabling T cells to bind to the target cell and induce target cell lysis. This study aims to analyse the functional activity of T lymphocytes against melanoma cells after stimulation with a MCSPxCD3 BiTE in vitro. 8 1.2.2 Methods Melanoma cell lines were cultured in vitro and analysed for mutations of the APM, the expression of relevant immunological proteins as well as the secretion of immunosuppressive molecules using PCR, FACS and ELISA techniques. Furthermore, three antigen-specific cytotoxic T cell clones were incubated with melanoma cells without any BiTE, with a control BiTE or with MCSP-BiTE. Using a 51chromiumrelease assay, the efficacy of the T cell induced lysis was determined. Moreover, out of co-cultures of melanoma cells and T cells with and without MCSP-BiTE, surviving melanoma cells were isolated. These cells were then tested for their sensitivity towards a T cell mediated killing. In addition, different CD3 positive T cell subpopulations were isolated out of healthy donors’ blood using cell sorting. These cells were then tested in a 51 chromium-release for their ability to induce a BiTE mediated cytotoxic immune response against melanoma cells. 1.2.3 Results All melanoma cell lines analysed expressed MCSP and could be killed by clonal T cells in the presence of MCSP-BiTE. The capacity of T cells to kill melanoma cells upon BiTE stimulation was independent on different immunological factors. Melanoma cell lines sensitive to an antigen-specific killing showed no increased cytotoxicity after addition of MCSP-BiTEs. For one melanoma cell line, it could be shown that cells having survived a MCSP-BiTE mediated immune response subsequently revealed a decreased MCSP expression. These cells were also less sensitive against a MCSP-BiTE mediated kill than control cells not having been exposed to MCSP-BiTE before. All CD3 positive T cell subpopulations isolated out of healthy donors’ blood were effective to induce a BiTE mediated cytotoxic immune response against melanoma cells. 1.2.4 Conclusions These data clearly demonstrate that MCSP-BiTEs are able to induce a T cell mediated cytotoxic activity against MCSP positive melanoma cells regardless of the expression of different immunological factors. BiTEs might thus present an effective novel therapeutic approach for the treatment of patients with malignant melanoma. Of interest, melanoma cells, having survived BiTE mediated lysis, revealed a downregulation of MCSP. Downregulation of MCSP is a new tumour immune escape mechanism not having been described before in literature. 9 2 Einleitung 2.1 Immunsystem Das menschliche Immunsystem stellt ein hochkomplexes und fein reguliertes System dar, das den menschlichen Organismus vor Gefahr schützen soll. Es ist kein starres, in sich geschlossenes System, sondern muss als dynamisches Bindeglied zwischen dem menschlichen Organismus und seiner Umwelt angesehen werden (156). Das menschliche Immunsystem ist gezwungen, sich aufgrund ändernder Umweltbedingungen ständig neu anzupassen und seine Abwehrmechanismen zu trainieren und zu verfeinern. Nur so kann es neuen Erregern wirksam entgegentreten. Seiner Aufgabe kann das Immunsystem nur nachkommen, indem es zwischen „selbst“ und „fremd“ zu unterscheiden vermag (156). Autoimmunerkrankungen auf der einen und Allergien auf der anderen Seite bezeugen die essentielle Bedeutung dieser Unterscheidungsfähigkeit. Indem es „fremde“ Ags (Antigene) als solche erkennt, schützt das menschliche Immunsystem den Körper vor Infektionen durch Bakterien, Viren, Pilze und Parasiten. Wird es im Rahmen einer angeborenen Dysfunktion wie z.B. dem Di-George-Syndrom, einer erworbenen Erkrankung wie z.B. AIDS (Acquired Immune Deficiency Syndrome) oder durch immunsuppressive Behandlungen in seiner Funktion gestört, kann es zu schwerwiegenden Infektionen kommen, die selbst bei adäquater Behandlung zum Teil letal verlaufen (115, 170). In den letzten Jahrzehnten wurde außerdem die wichtige Rolle des Immunsystems bei der Kontrolle und Bekämpfung entarteter Zellen erkannt (151). So gehen Störungen des Immunsystems wie z.B. im Rahmen von AIDS häufig mit einer erhöhten Tumorinzidenz einher (2, 18). Ein zentraler Bestandteil des Immunsystems für seine Fähigkeit zwischen „selbst“ und „fremd“ zu unterscheiden, ist das sogenannte HaupthistokompatibilitätskomplexSystem (MHC- bzw. HLA-System). Diesem kommt auch in der Transplantationsmedizin eine wichtige Rolle zu: Um Abstoßungsreaktionen zu vermeiden, müssen Spender und Empfänger gematcht werden (105). Das MHC-System besteht aus mehreren Komplexen. Auf dem MHC-I-Komplex, der von den meisten kernhaltigen Zellen exprimiert wird, werden in der Regel intrazelluläre Peptide präsentiert (156, 180). Hierfür werden im Cytosol zunächst Proteine durch multikatalytische Proteasome bestehend aus mehreren Untereinheiten (unter anderem LMP-2 und -7) in Peptide gespalten und sodann mit Hilfe verschiedener Transporter (z.B. TAP-1 und -2) in das endoplasmatische Retikulum befördert (180, 181). Im 10 endoplasmatischen Retikulum entsteht dann im Zusammenspiel mit verschiedenen Faktoren wie z.B. Tapasin, Calnexin und Calreticulin ein Komplex aus MHC-I, ß2Mikroglobulin und Peptid (181). Dieser Komplex wird anschließend mit Hilfe des Golgi-Apparates an die Zelloberfläche befördert und dort präsentiert (180). Die an dem beschriebenen Vorgang beteiligten Faktoren bezeichnet man in ihrer Gesamtheit als Antigen-Prozessierungs-Maschinerie (APM) (vgl. Abbildung 1). Abbildung 1: Antigen-Prozessierungs-Maschinerie (180) Die Abbildung zeigt wichtige Bestandteile der APM. Die in Proteasomen entstandenen Peptide werden mittels TAP-1 und -2 in das endoplasmatische Retikulum transportiert und bilden dort mit MHC-I und ß 2-Mikroglobulin einen Proteinkomplex. Dieser wird dann auf der Zelloberfläche präsentiert. Durch Kreuzpräsentation ist es jedoch auch möglich, dass extrazelluläre Peptide auf MHC-I präsentiert werden (204, 208). Dieser Mechanismus spielt unter anderem bei der Tumorabwehr eine wichtige Rolle (179). Auf dem MHC-II-Komplex, der von den sogenannten antigenpräsentierenden Zellen (APCs) exprimiert wird, werden hingegen von extrazellulär aufgenommene Peptide präsentiert (156). APCs haben damit MHC-Iund MHC-II-Komplexe. Das Abwehrsystem kann in eine angeborene, unspezifische und eine erworbene bzw. adaptive, spezifische Immunantwort untergliedert werden. Dennoch gibt es zahlreiche Verbindungs- und Regulationsmechanismen zwischen den beiden Immunantworten und nur deren enges Zusammenspiel führt zu einer zielgerichteten und adäquaten Immunreaktion (156). Beide Teile lassen sich wiederum in humorale und zelluläre Bestandteile gliedern (vgl. Abbildung 2). 11 Abbildung 2: Vereinfachte Übersicht über das Immunsystem (156) Die Abbildung zeigt in stark vereinfachter Form die verschiedenen Bestandteile des Immunsystems. Die dargestellten Pfeile sollen verdeutlichen, dass die einzelnen Bestandteile nicht isoliert agieren, sondern im ständigen Wechselspiel mit den anderen Faktoren gesehen werden müssen. Nicht aufgeführt in der Grafik sind die physikalischen und chemischen Barrieren. Die angeborene Immunabwehr stellt die erste Verteidigungslinie des menschlichen Körpers gegen Erreger dar. Es handelt sich hierbei um ein relativ unspezifisches System, das jedoch sehr schnell und ohne vorhergehende Antigenpräsentation reagieren kann. Es ist in der Lage, ein breites Spektrum an Erregern wirksam zu bekämpfen (156). Zur unspezifischen Immunabwehr zählen neben physikalischen (wie z.B. Haut und Schleimhäute) und chemischen Barrieren (wie z.B. Säuren und Enzyme) zelluläre Bestandteile (Makrophagen/Monozyten, Mastzellen, Granulozyten, DCs (Dendritische Zellen) und Natürliche Killer-Zellen) sowie verschiedene humorale Faktoren (Komplementfaktoren, Zytokine, Defensine und Akute-Phase-Proteine) (81, 156). Das adaptive Immunsystem stellt die zweite Verteidigungslinie dar. Zu ihm gehören die Tund B-Lymphozyten (156). T-Lymphozyten agieren vorwiegend durch direkte ZellZellkontakte. Sie vermögen so virusbefallene oder entartete Zellen zu eliminieren (156). Außerdem spielen sie eine wichtige Rolle bei der Koordination der Immunabwehr (CD4+-T-Zellen, T-Helferzellen) (179). B-Lymphozyten zeichnen sich insbesondere durch ihre Fähigkeit aus, Antikörper zu produzieren und so z.B. bakterielle Infektionen zu bekämpfen (81). Das erworbene Immunsystems muss erst durch komplexe Mechanismen aktiviert werden und ist daher nicht sofort zur Erregerabwehr fähig (81). Dafür arbeitet es hochspezifisch und ist im Gegensatz zum unspezifischen Immunsystem in der Lage, sogenannte Gedächtniszellen zu bilden und damit eine langfristige Immunität aufzubauen (156). Gelingt es Erregern, die physikalischen und chemischen Barrieren zu durchdringen, so treffen sie zunächst auf phagozytäre Zellen. Zu ihnen zählen insbesondere Makrophagen/Monozyten, neutrophile Granulozyten und DCs, die durch die Sezernierung von Botenstoffen wie z.B. Chemokine und Zytokine weitere Immunzellen 12 anlocken und stimulieren können (156). Daneben zeichnen sich Makrophagen/Monozyten und DCs dadurch aus, dass sie zur Gruppe der APCs gehören (156). Sollten die Mechanismen der angeborenen Immunantwort nicht ausreichen, um den Erreger erfolgreich zu eliminieren, so präsentieren APCs Peptidsequenzen des Erregers über den MHC-I-Komplex an native CD8+-T-Zellen und über den MHC-II-Komplex an native CD4+-T-Zellen (81, 156). Es werden nur jeweils diejenigen T-Lymphozyten aktiviert, die das präsentierte Ag über ihren TCR (T cell receptor) spezifisch erkennen und binden (132). Dieser Prozess bestehend aus Aktivierung und klonaler Expansion von T-Lymphozyten wird als Priming bezeichnet (132). Er findet in den sekundären lymphatischen Organen, vor allem in den Lymphknoten, statt. Für die Aktivierung von T-Lymphozyten ist jedoch die alleinige Interaktion des TCR mit dem MHC-Antigenkomplex der APC nicht ausreichend. Erst durch zusätzliche kostimulatorische Signale, wie z.B. dem Wechselspiel zwischen dem CD28-Komplex des T-Lymphozyten und dem B7-Komplex der APC, kommt es zu einer antigenspezifischen Aktivierung (vgl. Abbildung 3) (81). Abbildung 3: Antigenspezifische Aktivierung von CD8+-T-Lymphozyten (81) Für die Aktivierung von CD8 +-T-Lymphozyten sind prinzipiell zwei Signale erforderlich. Neben der Interaktion des TCR mit dem MHC-I-Antigenkomplex ist ein weiteres kostimulatorisches Signal wie z.B. über CD28/B7 nötig. Dieses zweite Signal kann durch eine weitere Interaktion der DC mit einem CD4 +-T-Lymphozyten über den CD40/CD40L-Komplex noch verstärkt werden, da dieses Wechselspiel zu einer Hochregulation von B7 führt, von der letztendlich auch der CD8+-TLymphozyt profitiert. CD8+-T-Lymphozyten können nun, wenn ihnen das entsprechende Peptid im MHCKontext präsentiert wird, durch Ausschüttung von zytotoxischen Molekülen (Perforine, Granzyme und Granulysine) sowie mittels FAS-L(CD95-L)/FAS(CD95)-Interaktion in der Zielzelle Apoptose induzieren (35). CD4+-T-Lymphozyten interagieren nach Aktivierung insbesondere antikörperproduzierenden mit Plasmazellen B-Lymphozyten, differenzieren wodurch (156). diese Innerhalb zu dieses 13 komplexen Zusammenspiels kommt den Tregs (Regulatorische T-Zelle) (CD4+CD25+Foxp3+) eine wichtige modulatorische Rolle zu (132). Am Ende der Immunantwort werden die meisten Lymphozyten durch Apoptose und Phagozytose eliminiert (81). Einige Lymphozyten differenzieren jedoch zu sogenannten Gedächtniszellen, wodurch es bei erneuter Exposition mit dem gleichen Erreger zu einer beschleunigten Immunabwehr kommt. Auf diesem Phänomen basiert z.B. die Wirksamkeit von Impfungen (81). 2.2 Malignes Melanom 2.2.1 Klinische Bedeutung und Epidemiologie Das maligne Melanom (C43 nach ICD-10) ist ein von Melanozyten ausgehender bösartiger Tumor (69). In Bezug auf die Gesamtzahl aller bösartiger Tumore der Haut macht das maligne Melanom nur etwa 4% der Fälle aus (129). Dagegen sind etwa 80% aller Todesfälle durch Hautkrebs auf maligne Melanome zurückzuführen (129). Dies lässt sich dadurch erklären, dass andere Formen des Hautkrebses wie z.B. das Basaliom und das Plattenepithelkarzinom zwar bei weitem häufiger sind, dafür aber eine bessere Prognose haben (154). Das maligne Melanom der Haut stellt keinen einheitlichen Tumor dar sondern kann anhand unterschiedlicher Kriterien klassifiziert werden (154). Klinisch werden das Lentigo-maligna-Melanom, das Superfiziell spreitende Melanom, das Noduläre Melanom und das Akrolentiginöse Melanom unterschieden (19). Im klinischen Alltag hat sich zur Unterscheidung Melanom-verdächtiger Läsionen von anderen dermalen Effloreszenzen die sogenannte ABCD-Regel als hilfreich erwiesen (154). Sie berücksichtigt die Merkmale Asymmetrie, Begrenzung, Color und Durchmesser. Wird anhand der genannten Kriterien die klinische Verdachtsdiagnose eines malignen Melanoms gestellt, so muss diese histologisch gesichert werden (20). In den letzten Jahren konnten verschiedene Risikofaktoren für das Auftreten eines malignen Melanoms identifiziert werden. An erste Stelle steht eine erhöhte UV-LichtExposition, vor allem im Kindes- und Jugendalter bei Personen mit hellem Hauttyp (19, 63). Wie Abbildung 4 zeigt, unterscheidet sich die Inzidenzrate des malignen Melanoms in verschiedenen geographischen Gebieten. Die hohe Melanominzidenz in Australien und Neuseeland wird unter anderem auf die erhöhte Sonnenexposition und den hohen Anteil an Einwohnern keltischer Herkunft zurückgeführt (20). 14 Abbildung 4: Inzidenzrate des malignen Melanoms in verschiedenen geographischen Gebieten (148) Die Abbildung zeigt für Männer (schwarz) und Frauen (weiß) Inzidenzrate des die altersstandardisierte malignen Melanoms in unterschiedlichen geographischen Gebieten der Welt bezogen auf 100.000 Menschen. Auf dem ersten Platz befinden sich mit großem Abstand Australien und Neuseeland. Die Inzidenzrate für Westeuropa und damit auch für Deutschland liegt zwischen 7,3 (Männer) und 10,3 (Frauen). Zu den Risikofaktoren zählen weiterhin familiäre Vorbelastung, multiple benigne oder atypische Naevi und Immunsuppression (129). Außerdem haben Personen nach Exzision eines Melanoms eine erhöhte Wahrscheinlichkeit für die Bildung eines weiteren primären Melanoms (19). In Deutschland wird für das Jahr 2000 für das maligne Melanom eine Inzidenz von etwa zwölf Fällen/100.000 Einwohner angegeben (20). Bemerkenswert ist, dass das maligne Melanom zu den Tumoren gehört, deren Neuerkrankungsrate in Deutschland in den letzten 30 Jahren mit am stärksten gestiegen ist, wohingegen sich die Sterberate auf gleichem Niveau hält (220). Dies spricht dafür, dass immer mehr maligne Melanome in einem prognostisch günstigen Stadium entdeckt werden und wirksamere Therapien zur Verfügung stehen (vgl. Abbildung 5) (20). Abbildung 5: Altersstandardisierte Neuerkrankungs- und Sterberate (83) Gezeigt ist die altersstandardisierte Neuerkrankungs- und Sterberate des malignen Melanoms in Deutschland getrennt nach Geschlecht im Zeitraum von 1980-2006 bezogen auf je 100.000 Einwohner. Zu dieser Entwicklung haben verschiedene Faktoren beigetragen. Zum einen kam es durch ein geändertes Freizeitverhalten und die Nutzung von Solarien zu einer erhöhten 15 Exposition gegenüber UV-Strahlung und damit zu einer realen Zunahme der Erkrankungszahlen (20, 220). Zum anderen führte die Aufklärung breiter Bevölkerungsschichten und eine Sensibilisierung der Ärzteschaft zu einer erhöhten Diagnosehäufigkeit, vor allem auch von Melanomen in einem frühen Tumorstadium (220). Außerdem haben seit 2008 alle gesetzlich Versicherten ab dem Alter von 35 Jahren im Rahmen eines speziell eingerichteten Früherkennungsprogrammes (Hautkrebs-Screening) alle zwei Jahre Anspruch auf eine Inspektion der Haut durch einen Arzt (4). Früherkennungsmaßnahmen sind deshalb von so großer Bedeutung, weil maligne Melanome in einem frühen Stadium nahezu immer heilbar sind (20). Der Anteil an malignen Melanomen der Haut verglichen mit allen aufgetretenen bösartigen Neubildungen betrug in Deutschland 2008 für Frauen 4,0% und für Männer 3,6% (jeweils etwa 8.900 Fälle) (90). Das maligne Melanom stellt damit in Bezug auf die Häufigkeit seines Neuauftretens verglichen mit allen anderen bösartigen Tumorerkrankungen bei Frauen die fünft- und bei Männern die acht-häufigste Tumorentität in Deutschland dar (vgl. Abbildung 6). Abbildung 6: Anteil ausgewählter Tumorlokalisationen an allen Krebsneuerkrankungen (90) Die Abbildung zeigt die Tumorinzidenz der häufigsten Tumore des Mannes (blau) und der Frau (rot) in Prozent. Gezeigt sind die Daten für Deutschland für das Jahr 2008. Nicht-melanotische Formen des Hautkrebses sind in der Statistik nicht aufgeführt. Weltweit starben 2002 etwa 41.000 Menschen an einem malignen Melanom (148). In Deutschland verursachte das maligne Melanom 2008 circa 1% aller Krebstodesfälle (etwa 2.500 Fälle) und liegt bei Männern auf dem 15. und bei Frauen auf dem 19. Platz der Krebssterbefälle (vgl. Abbildung 7) (90). 16 Abbildung 7: Anteil ausgewählter Tumorlokalisationen an allen Krebssterbefällen (90) Die Abbildung zeigt die Häufigkeit einzelner Tumore an allen Krebssterbefällen für Männer (blau) und Frauen (rot) in Prozent. Gezeigt sind die Daten für Deutschland für das Jahr 2008. 2.2.2 Standardtherapieverfahren und Prognose Die Therapie des malignen Melanoms ist komplex und sollte von erfahrenen Ärzten unter Berücksichtigung aktueller Leitlinien (z.B. S3 AWMF Leitlinie: „Diagnostik, Therapie und Nachsorge des Melanoms" und „Deutsche Leitlinie: Malignes Melanom“) durchgeführt werden (64, 110). Sie richtet sich neben individuellen Faktoren des Patienten insbesondere nach dem Stadium der Erkrankung und dem damit verbundenen Metastasierungspotenzial (20). So ist die Therapie in frühen Tumorstadien in der Regel kurativ ausgelegt, in den späteren Stadien hingegen meist palliativ orientiert (154). Die wichtigste Therapiemaßnahme besteht in einer möglichst frühzeitigen Exzision des Primärtumors (19). Wenn bereits Metastasen aufgetreten sind, stehen neben deren chirurgischen Exzision auch die hypertherme Zytostatikaperfusion und strahlentherapeutische Maßnahmen zur Verfügung (65). Für die adjuvante Behandlung stellt Interferon-α ein wichtiges Therapeutikum dar. Hierbei gibt es verschiedene Therapie-Schemata, wobei bis dato für kein Interferon Schema eine klare Überlegenheit gegenüber einem anderen nachgewiesen werden konnte (65, 110). Die Indikation für eine Strahlentherapie besteht meist dann, wenn ein operativer Eingriff nicht möglich ist und bzw. oder bereits eine palliative Situation eingetreten ist (z.B. bei Auftreten von Hirnmetastasen) (65). In einer palliativen Situation (i.d.R. Stadium IV) kann des Weiteren die Indikation für eine Chemotherapie z.B. mit Dacarbazin bzw. eine Chemoimmuntherapie bestehen (65, 110). Nach erfolgter Behandlung wird außerdem je nach Rezidivrisiko in bestimmten 17 zeitlichen Intervallen eine Melanomnachsorge über den Zeitraum von zehn bis 20 Jahren empfohlen (20, 154). Die Prognose des malignen Melanoms hängt von verschiedenen Faktoren ab. Die tumorspezifische 10-Jahres-Überlebensrate für das Gesamtkollektiv beträgt etwa 7580% (65). Einzeln betrachtet ist die Tumordicke nach Breslow zum Zeitpunkt der Exzision der wichtigste prognostische Faktor (20, 21) (vgl. Abbildung 8). Abbildung 8: Tumordicke und Überlebensrate (19) Die Tabelle zeigt die 10-Jahres-Überlebensrate in Abhängigkeit von der Tumordicke nach Breslow. Sind bereits Metastasen vorhanden, so spielt die Tumordicke keine prognostische Rolle mehr. TD: Tumordicke Wie aus Abbildung 8 hervorgeht, haben maligne Melanome mit einer geringen Tumordicke eine exzellente Prognose, wohingegen dickere Tumore mit einer eher schlechten Prognose einhergehen. Dies lässt sich dadurch erklären, dass mit zunehmender Tumordicke auch die Wahrscheinlichkeit für die Ausbildung von Metastasen steigt (19). Sind bereits Metastasen aufgetreten, so sinkt die Überlebenswahrscheinlichkeit unabhängig von der Dicke des Primärtumors (19). Weitere prognostische Faktoren sind Ulzerationen des Tumors, Nachweis einer Lymphoder Blutgefäßinvasion durch Tumorzellen, ein hoher mitotischer Index und bedingt der Invasionslevel nach Clark (8, 19, 65). Aussagekräftiger als die Betrachtung eines einzelnen Faktors allein, ist deren Kombination: das Tumorstadium (vgl. Abbildung 9). Abbildung 9: Überlebenskurve (7) Dargestellt ist die Überlebenskurve von Patienten mit malignem Melanom in Abhängigkeit vom Stadium der Erkrankung nach der Kaplan-Meier-Methode. Zu beachten ist, dass dem Graphen die AJCC Stagingkriterien von 2001 zu Grunde liegen. 18 2.2.3 Experimentelle Therapieansätze Wie Abbildung 9 zu entnehmen ist, geht das maligne Melanom, Stadium IV, mit einer infausten Prognose einher. Die mediane Überlebenszeit von Patienten im Stadium IV beträgt vier bis sechs Monate und bisher konnte in nur einer Studie ein verlängertes Überleben in diesem Stadium erreicht werden (20, 80, 173). Die Entwicklung und Erforschung neuer Therapieansätze für die Behandlung der betroffenen Patienten aber auch von Patienten in anderen Stadien ist daher dringend geboten. Diese Therapieansätze werden, da sie bislang noch nicht in prospektiv kontrollierten randomisierten Studien überprüft wurden, als experimentelle Therapieansätze bezeichnet (64). Abbildung 10 zeigt aktuelle Strategien experimenteller Therapieansätze unter besonderer Beachtung der T-Zell-Immuntherapie auf. Abbildung 10: T-Zellen in der Tumortherapie (5) Die vorliegende Grafik zeigt die Rolle von T-Zellen in der Tumortherapie und mögliche Ansatzpunkte für Therapeutika. APCs wie z.B. DCs präsentieren nativen T-Zellen in Lymphknoten die von Tumorzellen freigesetzten Ags. Erkennt eine T-Zelle dieses Ag mittels seines TCRs und erhält weitere kostimulatorische Signale, so differenziert sie zu einer CTL (Cytotoxischer TLymphozyt), expandiert und entfaltet ihre antitumorale Wirkung. Verschiedene Therapieansätze wie z.B. Immunisierung bzw. Vakzination in Kombination mit bestimmten Adjuvantien, Blockade von CTLA-4 durch mAbs (Monoclonal Antibody), adoptiver T-Zell-Transfer und bispezifische Antikörper versuchen diesen Prozess zu verbessern. Im Folgenden soll insbesondere auf diejenigen Therapiestrategien näher eingegangen werden, die in der „Deutsche Leitlinie: Malignes Melanom“ aufgeführt sind: PeptidImmunisierung, Vakzination mit DCs, Adoptiver T-Zell-Transfer und Immunisierung mit DNA (64). 19 Bei der Peptid-Immunisierung werden MHC-I-bindende Peptidsequenzen aus Melanom-assoziierten Proteinen zunächst synthetisch hergestellt und dann, ggf. zusammen mit einem oder mehreren Adjuvantien (z.B. GM-CSF, KLH, IL-2 oder IL12), verabreicht (64, 174). Die Peptidsequenz kann, ohne vorher prozessiert zu werden, direkt an die MHC-I-Moleküle von DCs binden und so zu einer Aktivierung von zytotoxischen T-Lymphozyten führen (64, 174). Ein Problem der Peptidimmunisierung ist die HLA-Restriktion der Peptide (172). In einer ersten von Marchand et al. durchgeführten Studie konnte nach wiederholter Injektion des MAGE-3.A1 Peptids eine Tumorregression bei sieben von 39 Patienten mit malignem Melanom, Stadium III oder IV, beobachtet werden (123). Weitere Studien wie z.B. von Wang et al., Hersey et al., Roberts et al. und Bins et al. mit unterschiedlichen Ansprechraten und Ergebnissen folgten (14, 75, 162, 212). Die ECOG Phase II Studie E1696, welche die erste große randomisierte Studie zu den Effekten einer Peptidimmunisierung bei Patienten mit malignem Melanom, Stadium IV, darstellt, zeigte ein objektives klinisches Ansprechen bei sechs von 120 Patienten (97). Die Zugabe immunmodulatorischer Zytokine hatte keinen nachweisbaren Effekt. Eine Modifikation der alleinigen Peptid-Immunisierung besteht in der gleichzeitigen Aktivierung von CD4+-Lymphozyten (186). In einer Studie von Phan et al. an 41 Patienten mit metastasierten malignem Melanom konnte jedoch durch die gleichzeitige Immunisierung mit einem MHC-Klasse-II restringierten Peptid keine Verbesserung der Immunantwort festgestellt werden (149). Bei der DC Vakzination werden zumeist aus Monozyten differenzierte DCs ex vivo mit TAA (Tumorassoziiertes Antigen) beladen und dann dem Patienten in Form eines Impfstoffes appliziert (112, 195, 202). In diesem Zusammenhang ist es möglich, DCs entweder mit einem oder mehreren definierten TAAs zu beladen (peptide pulsing) oder sie mit Tumorzelllysaten zu inkubieren (193). Eine alternative Beladungsmethode stellt die Transfektion von DCs mit Tumor-RNA dar (64, 107-109). In einer Pilotstudie von Nestle et al. konnte durch DC Vakzinierung ein Ansprechen bei fünf von 16 Patienten mit malignem Melanom, Stadium IV, beobachtet werden (139). Thurner et al. konnten bei sechs von elf Patienten mit malignem Melanom, Stadium IV, mittels DC Vakzinierung eine Rückbildung von Fernmetastasen erreichen (194). Schuler-Thurner et al. konnten außerdem zeigen, dass es mit Hilfe dieser Technik nicht nur möglich ist, CD8+-Lymphozyten zu aktivieren, sondern auch CD4+Th1-Lymphozyten (178). Zahlreiche Folgestudien bestätigten die prinzipielle Wirksamkeit der DC Vakzinierung (10, 55, 76, 111, 133, 137, 167, 187, 201, 207). In einer von Schadendorf et al. 2006 veröffentlichten randomisierten Phase III Studie an 108 Patienten mit malignem 20 Melanom, Stadium IV, konnte jedoch eine Überlegenheit der DC Vakzinierung verglichen mit einer Standardchemotherapie mit Dacarbazin nicht nachgewiesen werden (173). In jüngeren Studien wird daher insbesondere die Wirksamkeit der DC Vakzinierung in Kombination mit anderen Therapeutika wie z.B. bestimmten Antikörpern oder der Effekt von modifizierten Ags auf das peptide pulsing untersucht (87, 113, 158). Ein weiteres therapeutisches Einsatzgebiet von DCs bei der Therapie des malignen Melanoms ist die Hybridzellvakzination. Hierbei werden DCs ex vivo mit Tumorzellen kombiniert und dann dem Patienten appliziert. Erste Studien von Trefzer et al. und Wei et al. bestätigten das Wirkprinzip und zeigten vereinzelt sogar komplette Remissionen (199, 214). Beim adoptiven T-Zell-Transfer werden tumorspezifische T-Lymphozyten des Patienten wie z.B. TILs (Tumorinfiltrating Lymphocyte) ex vivo expandiert und aktiviert und diesem dann zurückgegeben (77). In einer ersten Studie von Rosenberg et al. konnte mit diesem Therapieansatz und der zusätzlichen Gabe von IL-2 bei elf von 20 Patienten mit malignem Melanom, Stadium IV, eine Regression beobachtet werden (164). Weitere Studien unterstrichen das Potential des adoptiven T-Zell-Transfers (46-48, 95, 121, 165, 205). Die objektive Ansprechrate liegt, je nach Studie, bei etwa 50-70% (163). Eine Abwandlung des klassischen T-Zell-Transfers stellt die Verwendung von genetisch modifizierten T-Lymphozyten dar (28, 77). Bei der Immunisierung mit DNA wird diese entweder nackt oder im Komplex mit anderen Molekülen appliziert (152). Damit das betreffende TAA anschließend richtig exprimiert werden kann, enthalten DNA-Vakzine alle hierfür nötigen regulatorischen und kodierenden Sequenzen (171). Verschiedene kleinere Phase I und II Studien belegen die Wirksamkeit dieser Methode (38, 68, 190, 219). Hingegen wiesen zwei Phase I Studien von Triozzi et al. und Tagawa et al. zwar laborchemisch verschiedene Lymphozytenaktivierungsmarker nach, ein klinisches Ansprechen war indes nicht zu beobachten (191, 200). Des Weiteren wird versucht, durch Kombination unterschiedlicher immunmodulierender Therapien bessere Ansprechraten zu erzielen (177). 2.2.4 Tumorimmunologie Die genaue Pathogenese des malignen Melanoms ist nicht abschließend geklärt (19, 128). Alle bisher gewonnenen Ergebnisse deuten auf ein komplexes Wechselspiel verschiedener Umwelteinflüsse, insbesondere des UV-Lichts, mit bestimmten molekulargenetischen, immunologischen Faktoren hin (89, 147). UV-Licht induziert in 21 der Haut Genmutationen, eine Veränderung der Immunfunktion, die Produktion von lokalen Wachstumsfaktoren und die Bildung reaktiver Sauerstoffverbindungen mit DNA schädigender Wirkung (129). Des Weiteren regt es in Melanozyten die Synthese von Melanin an (67). Eine abnormale Pigmentierung der Haut kann daher auf eine erhöhte UV-Licht-Exposition hindeuten. Auf molekularer Ebene scheint UV-Licht möglicherweise Mutationen in den MC1R- und RAS-/BRAF-Genen zu induzieren, die eine wichtige Rolle bei der Regulation und Kontrolle des Zellzyklus spielen (105, 147). Anhand molekulargenetischer Untersuchungen an Familien mit gehäuftem Auftreten von malignen Melanomen war es außerdem möglich, bestimmte Risikogene für dessen Entstehung zu identifizieren. Neben Mutationen von BRAF, CDK4, NRAS und PTEN konnten bei etwa 25-40% der untersuchten Personen Mutationen des Tumorsuppressorgens CDKN2A, das für p16Ink4A kodiert, nachgewiesen werden (105, 129). p16Ink4A ist ebenfalls an der Regulation des Zellzyklus beteiligt (105). Mutationen von CDKN2A und der anderen genannten Gene vermögen folglich zu einem unkontrollierten Zellwachstum zu führen. Derzeit wird jedoch davon ausgegangen, dass das maligne Melanom nicht durch eine bestimmte genetische Veränderung entsteht, sondern hierfür verschiedene Mutationen erforderlich sind (147). Damit entwickelt sich das maligne Melanom, wie andere Tumoren auch, durch die schrittweise Transformation von Zellen, in diesem Fall von Melanozyten, verbunden mit der Aktivierung von Protoonkogenen und dem Verlust von Tumorsuppressorgenen (105). Diese stufenweise Entstehung des malignen Melanoms wird in Clarks histopathologischem Modell dargestellt. Danach entwickelt sich das maligne Melanom schrittweise auf der Basis eines benignen Naevus (36). Zu beachten ist jedoch, dass sich neueren Ergebnissen zufolge nur etwa 30-40% aller Melanome in Assoziation mit einem melanozytären Naevus bilden (19). Nach Ansicht einiger Autoren lassen sich den einzelnen von Clark beschriebenen Stadien auch bestimmte genetische Mutationen zuordnen (vgl. Abbildung 11) (129). 22 Abbildung 11: Pathogenese des malignen Melanoms, Modell nach Clark (129) Die Abbildung zeigt die schrittweise Entstehung des malignen Melanoms auf der Basis eines benignen Naevus mit den damit verbundenen molekularen Veränderungen. Zu erkennen ist weiterhin, dass das Melanom zwei verschiedene Wachstumsphasen aufweist. Erfolgt das Wachstum in einem ersten Schritt primär horizontal, so geht es in einem zweiten Schritt in ein vertikales Wachstum über. Die Rolle des Immunsystems bei der Tumorentstehung wird kontrovers diskutiert: Spontanremissionen auf der einen, als auch aggressive Verläufe bei Immunsupprimierten auf der anderen Seite, belegen seine komplexe Rolle (40, 65). Dem Immunsystem kommt im Rahmen der Immunosurveillance eine wichtige Funktion bei der Kontrolle und Abwehr entarteter Zellen zu (50). Dieses ursprünglich von Burnet und Thomas entwickelte Konzept konnte jedoch erst in den letzten Jahren, unter anderem durch Versuche von Shankaran et al., tierexperimentell bestätigt werden (27, 51, 183, 192). Andererseits gibt es Hinweise, dass das Immunsystem das Tumorwachstum fördert (51). Makrophagen können z.B. durch Freisetzung von bestimmten Wachstumsfaktoren, Enzymen und Zytokinen zur Tumorprogression beitragen (185). Einige Autoren verwenden daher für die gegenseitigen Wechselwirkungen des Immunsystems mit dem Tumor den Begriff des Immunoediting (50). Hierbei spielen CD8+-T-Lymphozyten aufgrund ihrer Fähigkeit entartete Zellen anhand bestimmter Peptide, sogenannter TAA, zu erkennen und zu lysieren, eine Schlüsselrolle (35). Dazu 23 muss ihnen aber zuvor von APCs das entsprechende Peptid auf MHC-I präsentiert worden sein (177). Wird eine Immunantwort gegen einen Tumor induziert, so gibt es dennoch zahlreiche Möglichkeiten, wie dieser dem Angriff des Immunsystems entgehen kann: Neben der Produktion von immunsuppressiven Faktoren wie z.B. IL-10 und antiapoptotischen Molekülen wie z.B. Proteinase Inhibitor-9 sind hierbei insbesondere Veränderungen der APM zu nennen (126, 177). So ist in Tumoren im Allgemeinen und in Melanomen im Speziellen häufig eine verminderte Expression von MHC-I, LMP-2 und -7 sowie TAP-1 und -2 zu detektieren (59, 78, 180). Kageshita et al. konnten für primäre Melanome nachweisen, dass eine Herunterregulation von MHC-I sowie TAP-1 und -2 mit der Tumordicke, dem Tumorstadium und dem Überleben korreliert (91). Ihre Ergebnisse zeigen außerdem, dass in Metastasen eines malignen Melanoms die Expression von HLA-I sowie TAP-1 und -2 signifikant häufiger herunterreguliert ist als in Primärtumoren. Dissemond et al. konnten nachweisen, dass primäre maligne Melanome, die histologische Zeichen der Regression zeigen, verglichen mit solchen, die dies nicht tun, eine erhöhte Expression von LMP-2 und -7 aufweisen (42). Zusammengefasst deuten diese Daten darauf hin, dass Melanomzellen mit Mutationen der APM der Kontrolle durch T-Zellen entgehen, selektiert werden, proliferieren und einen soliden Tumor bilden können (91). Das unmittelbare Umfeld eines solchen soliden Tumors wird mit dem Begriff des Tumormicroenvironment beschrieben (1, 61). Einige der dort lokalisierten Lymphozyten infiltrieren den Tumor und werden als TILs bezeichnet (142). Diese sind zwar prinzipiell dazu in der Lage, Tumorzellen zu lysieren, jedoch scheint ihr Aktivitätszustand für die Mediierung einer effektiven Immunantwort nicht auszureichend zu sein (43). Derzeit wird davon ausgegangen, dass hierauf verschiedene Faktoren einen Einfluss haben: Tregs, die Expression inhibitorischer Liganden wie z.B. PD-L1 oder auch bestimmte Enzyme wie z.B. die Indolamin-2,3Dioxygenase (15, 44, 60-62, 70, 206). In zahlreichen klinischen Studien zum malignen Melanom wird derzeit der Effekt verschiedener Substanzen untersucht, die mit bestimmten Bestandteilen des Tumormicroenvironment interagieren (209). 2.2.5 Antikörpertherapie Durch die 1975 von Köhler und Milstein entwickelte Hybridomtechnik und der damit verbundenen Möglichkeit mAbs zu produzieren und später auch klinisch zu nutzen, konnten in der Vergangenheit entscheidende Durchbrüche in der Behandlung von bestimmten Krankheiten, insbesondere bei der Therapie von Neoplasien, erzielt werden (96, 99). Dank mAbs ist es möglich, bestimmte Immunzellen zur Abwehr und 24 Eliminierung maligner Zellen zu gewinnen (102). Das Potential von mAbs bleibt jedoch hauptsächlich auf diejenigen Zellpopulationen beschränkt, die mittels ihrer FcγRezeptoren mAbs auch binden können: Makrophagen, neutrophile Granulozyten und Natürliche Killer-Zellen (102). In Studien wird derzeit insbesondere der Stellenwert von zwei verschiedenen anti-CTLA-4 mAbs (Ipilimumab und Tremelimumab) in der Behandlung des malignen Melanoms evaluiert (vgl. auch Abbildung 10) (80, 157, 160, 161, 213). Bei CTLA-4 handelt es sich um ein Oberflächenprotein, das von T-Zellen exprimiert wird und auf diese einen inhibitorischen Effekt vermittelt. Die Blockade von CTLA-4 durch Antikörpern verhindert somit die Herunterregulation der T-Zell Aktivität und könnte damit zu einer verbesserten anti-tumoralen Immunantwort führen (160). In einer Phase III Studie an Patienten mit metastasiertem Melanom konnten Hodi et al. erstmals eine signifikante Verlängerung des medianen Gesamtüberlebens verglichen mit der Kontrollgruppe durch die Gabe des CTLA-4 Antikörpers Ipilimumab erzielen (80). Die Autoren führen jedoch an, dass es zum Teil zu schweren Nebenwirkungen unter der Therapie kam. Mithilfe normaler, unveränderter mAbs ist es jedoch nicht möglich, T-Zellen zu rekrutieren, da diese keine Fcγ-Rezeptoren besitzen. T-Zellen spielen aber als hochspezialisierte Immunzellen eine wichtige Rolle in der Tumor-Kontrolle (5). Vor diesem Hintergrund gelang es 1985 Staerz et al. erstmals, mithilfe eines bispezifischen Antikörperkonstruktes eine T-Zell-Antwort gegen ein bestimmtes Ag hervorzurufen (189). Bei bispezifischen Antikörpern handelt es sich um künstlich hergestellt Proteinkomplexe, die zwei verschiedene Epitope spezifisch binden können (102). Bispezifische Antikörper stellen keine in sich geschlossene, homogene Gruppe dar, sondern lassen sich verschiedenen Typen zuordnen: Quadromas, F(ab’)2s, Heterodimeric scFvs, Heterodimeric Fabs, Diabodies und Tandem scFvs wie z.B. Bispecific T Cell Engagers (BiTEs) (103). 1995 entwickelten Mack et al. den ersten Antikörper nach dem heutigen BiTE-Prinzip (119). Bei BiTEs handelt es sich um ein rekombinant hergestelltes Antikörperkonstrukt, das durch die Verbindung zweier scFvAntikörperfragmente zu Stande kommt: Ein scFv-Fragment ist spezifisch für CD3, das andere für das gewünschte TAA (5). T-Zellen können so vorübergehend an die entsprechende Zielzelle binden und in dieser Apoptose induzieren (vgl. Abbildung 10 und Abbildung 12) (6). 25 Abbildung 12: Grundidee von BiTE-Antikörperkonstrukten (6) Die Abbildung zeigt die Grundidee von BiTE-Antikörpern: Sie entstehen aus der Kombination von gegen CD3 und gegen das entsprechende TAA gerichteten Antikörperfragmenten. Durch die Bindung der T-Zelle an die Zielzelle werden diese aktiviert und induzieren einen Zelltod der Zielzelle. Das Konzept von BiTEs ist, dass ihre Wirksamkeit nicht länger auf der Generierung spezifischer T-Zell-Klone oder der Antigenpräsentierung durch APCs beruht, sondern prinzipiell jede T-Zelle (z.B. auch TILs) ohne vorherige Stimulation rekrutiert werden kann (6, 175). Die Expression von MHC-I ist hierbei nicht notwendig, so dass BiTEs das Potential haben, ihre Wirksamkeit unabhängig von Mutationen der APM zu entfalten (5, 32, 143). BiTEs zeichnen sich des Weiteren insbesondere durch folgende Charakteristika aus: mittlere effektive Konzentration (EC50) zwischen 0,1-50pmol/L (21.000pg/mL), serielle Eliminierung von Zielzellen, niedriges E:T-Verhältnis (Effektor:Target-Verhältnis) und Aktivierung von T-Zellen nur in Anwesenheit der Zielzelle (5, 6, 22, 31, 82, 100). BiTEs binden zwar auch in Abwesenheit der Zielzelle mit geringer Affinität an T-Zellen, führen jedoch erst nach Erkennung des TAA zu deren Aktivierung (22, 45). T-Zellen können dann durch Freisetzung von Perforinen und Granzyme-B in der Zielzelle Apoptose auslösen (6, 71). Kostimulatorische Signale wie bei der herkömmlichen T-Zell-Antwort sind dabei nicht notwendig (vgl. Abbildung 13) (5, 215). 26 Herkömmliche T-Zell-Antwort BiTE induzierte T-Zell-Antwort Abbildung 13: Vergleich einer herkömmlichen mit einer BiTE induzierten T-Zell-Antwort (5) Die Abbildung zeigt wichtige Charakteristika einer herkömmlichen T-Zell-Antwort (links) verglichen mit einer BiTE induzierten T-Zell-Antwort (rechts). Für das Zustandekommen einer herkömmlichen T-Zell-Antwort sind neben der korrekten Funktion des TCR/CD3-Komplexes eine vorangegangene Präsentation des Ags durch eine APC, die ungestörte Präsentierung dieses Ags auf dem MHC-I-Komplex der Zielzelle sowie verschiedene kostimulatorische Signale (z.B. CD28/B7 Interaktion) nötig. Eine effektive BiTE induzierte T-Zell-Antwort setzt sowohl eine ausreichende Expression von CD3 auf der T-Zelle als auch des TAA auf der Tumorzelle voraus. Bisher wurden für mehr als zehn verschiedene Zielantigene spezifische BiTEs entwickelt, wovon sich drei in klinischer Erprobung befinden: MT110, MT111 (MEDI565) und MT103 (Blinatumomab) (6, 136). In neueren Forschungsprojekten wird außerdem versucht, BiTE-Antikörperkonstrukte für nicht tumorale Erkrankungen wie z.B. Asthma zu entwickeln (5). Die Wirkung von MT110, das mit seinen Bindungsarmen spezifisch CD3 und EpCAM (Epithelial cell adhesion molecule) bindet, wird derzeit 1 in einer Phase 1 Studie (ClinicalTrials.gov Identifier: NCT00635596) an Patienten mit soliden Tumoren untersucht, die EpCAM exprimieren (z.B. Lungenkrebs und gastrointestinalen Tumoren) (6, 23, 71, 74).2 Ebenfalls in einer Phase 1 Studie befindet sich MT111, das spezifisch für CD3 und CEA (Carcinoembryonic antigen) ist (ClinicalTrials.gov Identifier: NCT01284231) (146).3 Blinatumomab stellt das derzeit am weitesten entwickelte BiTE dar. Es handelt sich hierbei um ein CD3xCD19 bispezifisches Antikörperkonstrukt, das für die Behandlung von Erkrankungen entarteter B-Zellen ausgelegt ist (135). In einer Phase 1 Studie wurden 38 Patienten mit therapierrefraktärem Non–Hodgkin-Lymphom über vier bis acht Wochen mit Blinatumomab in Konzentrationen zwischen 0,0005 und 0,06mg/m2/24h behandelt (9). Stand März 2013 Siehe http://clinicaltrial.gov/ aufgerufen am 03.03.2013 3 Siehe http://clinicaltrial.gov/ aufgerufen am 03.03.2013 1 2 27 Es konnten vier komplette Remission und sieben Teilremissionen bei Dosen über 0,015mg/m2/24h beobachtet werden. Zum Vergleich: Bei der Standardtherapie des Non-Hodgkin-Lymphoms mit dem anti-CD20 mAb Rituximab wird eine Dosis von 375mg/m2/24h (etwa 25.000x höher) verabreicht (134). Außerdem zeigten alle sieben Patienten, die mit einer Dosis von 0,06mg/m2/24h behandelt wurden, ein objektives Ansprechen auf die Therapie. Zu den häufigsten Nebenwirkungen zählten Fieber, Lympho- und Leukopenie, Schüttelfrost und ein Anstieg des C-reaktives Proteins. Außerdem wurden komplett reversible ZNS-Nebenwirkungen wie z.B. Tremor, Enzephalopathie, Aphasie und Krampfanfall beobachtet (134). In einer Phase 2 Studie wurden 21 Patienten mit MRD-positiver B-ALL (Akute lymphatische Leukämie), die sich in kompletter hämatologischer Remission befanden, über vier Wochen mit 0,015mg/m2/24h Blinatumomab behandelt (197). 16 von 20 Patienten wurden MRD negativ (ein Studienabbrecher). Nach einem medianen Überwachungszeitraum von 405 Tagen war es bei vier von 20 Patienten zu einem hämatologischen Rezidiv gekommen und 16 von 20 Patienten befanden sich weiterhin in Remission, wobei hiervon acht Patienten eine allogene Stammzelltransplantation erhalten hatten. Nebenwirkungen der Therapie bestanden hauptsächlich in Fieber, Schüttelfrost, Abfall der ImmunglobulinWerte, Hypokaliämie und Lymphopenie. Die meisten davon waren komplett reversibel. Ein Patient zeigte Synkopen mit Krampfanfällen. Aktuell4 wird Blinatumomab in zwei klinischen Phase 2 Studien getestet: Eine Studie an Patienten mit MRD-positiver B-ALL (ClinicalTrials.gov Identifier: NCT00560794) und eine andere an Patienten mit refraktärer B-ALL bzw. einem Rezidiv (ClinicalTrials.gov Identifier: NCT01209286). Vier weitere Studien sind angemeldet (ClinicalTrials.gov Identifier: NCT01207388, NCT01471782, NCT01466179 und NCT01741792).5 Für die Behandlung des malignen Melanoms befindet sich derzeit ein Melanoma chondroitin sulfate proteoglycan (MCSP)-BiTE in der präklinischen Entwicklung (5, 17). MCSP ist ein Oberflächenantigen, das zu einem hohen Prozentsatz von Melanomzellen exprimiert wird und daher ein geeignetes TAA für eine BiTE induzierte T-Zell Lyse darstellt (17). Erste Daten wurden 2007 von Kischel et al. im Rahmen der Poster-Session des AACR Annual Meetings, San Francisco, vorgestellt (98). Die erste Publikation zu den MCSP-BiTEs stammt aus dem Jahre 2011. In dieser Veröffentlichung beschreiben Torisu-Itakura et al., dass aus PBMCs (Peripheral Blood Mononuclear Cell) über Negativselektion gewonnene CD8+-T-Zellen in der Lage sind, 4 5 Stand März 2013 Siehe http://clinicaltrial.gov/, aufgerufen am 03.03.2013 28 eine MCSP-BiTE induzierte Immunantwort gegen MCSP positive Melanomzelllinien zu vermitteln (198). Ein Jahr zuvor hatten Bluemel et al. die Wirksamkeit von MCSPBiTEs gegen MCSP positive CHO-Zellen belegen können (17). Klinische Studien wurden mit dem MCSP-BiTE bisher noch nicht durchgeführt. 2.3 Zielsetzung der Arbeit Ziel der vorliegenden Arbeit ist es, die zytotoxische Funktion von T-Lymphozyten gegen Melanomzellen nach in vitro Stimulation mit einem MCSPxCD3 bispezifischen Antikörper (BiTE) zu bestimmen. Hierfür wurden neun primäre Melanomzelllinien kultiviert und mittels FACS, PCR und ELISA auf die Expression verschiedener immunologisch relevanter Faktoren hin untersucht. Anschließend wurde mithilfe eines Zytotoxizitätsassays (51Chrom-Release) die anti-tumorale Immunreaktion von klonalen T-Lymphozyten gegen Melanomzellen bestimmt und des Weiteren untersucht, ob und falls ja welchen Effekt die Zugabe von MCSP-BiTEs hat. In einem nächsten Schritt wurde ermittelt, ob es durch die Zugabe von MCSP-BiTEs zu Tumor-Immune-EscapeMechanismen kommen kann. Abschließend sollte geklärt werden, welche CD3+Effektorzellpopulationen eine effektive MCSP-BiTE mediierte Immunantwort gegen Melanomzellen vermitteln können. 29 3 Material und Methoden 3.1 Material 3.1.1 Medien, Puffer und Lösungen Medium/Puffer/Lösung Humanserum-haltiges Hersteller/Zusammensetzung Medium Standardmedium mit 10% humanem AB-Serum (A’) und TCGF (isoliert aus Zellüberständen, vgl. (120)) AB-Serum, human Biotech, Aidenbach Cytofix/Cytoperm BD, Heidelberg Dimethylsulfoxid (DMSO) Sigma, München Einfriermedium 90% Fötales Kälberserum (FCS) mit 10% Dimethylsulfoxid FACS Clean BD, Heidelberg FACS Flow BD, Heidelberg FACS Rinse BD, Heidelberg FCS PAA, Linz, Österreich FCS-haltiges Medium (B’) Standardmedium mit 10% FCS Fixierungs-/Permeabilisierungs- BD, Heidelberg Lösung Lymphozytenseparations-Lösung PAN Biotech, Aidenbach PBS Biochrom, Berlin Perchlorsäure Merck, Darmstadt Perm/Wash BD, Heidelberg Standardmedium (serumfrei) insgesamt 500ml RPMI Medium mit Phenolrot (PAN Biotech, Aidenbach) mit folgenden Zusätzen: -­‐ -­‐ -­‐ T-Zell-Medium (A’) 1x L-Glutamin (Gibco, Darmstadt) 2ml Vitamine (PAN Biotech, Aidenbach) 5ml nicht-essentielle Aminosäuren (PAN Biotech, Aidenbach) -­‐ 100mM Natriumpyruvat (PAN Biotech, Aidenbach) -­‐ 40U/ml Penicillin (Gibco, Darmstadt) -­‐ 40µg/ml Streptomycin (Gibco, Darmstadt) -­‐ 50µM ß-Mercaptoethanol (Gibco, Darmstadt) Standardmedium mit 10% humanem AB-Serum 30 und TCGF (isoliert aus Zellüberstand) T-Zell-Stimulationsmedium T-Zell-Medium mit PHA-L Tetracyclin-Hydrochlorid Sigma-Aldrich, Steinheim Trypanblau Gibco, Darmstadt Trypsin-EDTA Gibco, Darmstadt Tumor-Zellmedium (B’) Standardmedium mit 10% FCS 3.1.2 Peptid-MHC-Tetramere Tetramer Konjugation Aminosäuresequenz HLA-Restriktion Hersteller BMLF1 PE GLCTLVAML Beckman- HLA-A2 Coulter, Krefeld gp100 210M PE IMDQVPFSV (168) (mutiert) HLA-A2 BeckmanCoulter, Krefeld Melan-A PE ELAGIGILTV A27L (203) HLA-A2 (mutiert) BeckmanCoulter, Krefeld 3.1.3 Antikörper Für den Nachweis von humanen Oberflächen- oder intrazellulären Markern wurden folgende Antikörper verwendet: Spezifität Isotyp Klon Herkunft Konjugation Hersteller Anti-Maus - Polyklonal Ziege FITC Jackson Immunoresearch, Newmarket, UK CD3 IgG1 SK7 Maus FITC BD, Heidelberg CD4 IgG1 SK3 Maus FITC BD, Heidelberg CD4 IgG1 SK3 Maus PerCP BD, Heidelberg CD8 IgG1 RPA-T8 Maus APC BD, Heidelberg CD8 IgG1 SK1 Maus PeCy7 BD, Heidelberg CD8 IgG1 SK1 Maus FITC BD, Heidelberg CD8 IgG1 SK1 Maus PE BD, Heidelberg CD8 IgG1 SK1 Maus PerCP BD, Heidelberg CD25 IgG1 2A3 Maus PE BD, Heidelberg 31 FAS-L IgG1 NOK-1 Maus PE eBioscience, (CD95-L) gp100 (ic) Frankfurt IgG1 HMB45 Maus - Abcam, Cambridge, UK HLA-A2 IgG2b BB7.2 Maus FITC Acris, Herford HLA-ABC IgG1 G46-2.6 Maus PE BD, Heidelberg IgG1 - X40 Maus PE BD, Heidelberg IgG1 - X40 Maus - BD, Heidelberg IgG2b - MCP-11 Maus PE BD, Heidelberg IgG2b - MOPC-195 Maus APC Caltag, Buckingham, UK MCSP IgG1 7.1 Maus PE BeckmanCoulter, Krefeld Melan-A IgG1 A103 Maus - Santa (ic) Cruz Biotechnology, Heidelberg PD-L1 IgG1 MIH1 Maus PE eBioscience, (B7-H1) TCRαβ Frankfurt IgG2b BW242/412 Maus APC Miltenyi Biotech BergischGladbach 3.1.4 Bispecific T Cell Engagers (BiTEs) Im Rahmen einer wissenschaftlichen Kooperation mit der Firma Amgen, München, wurden zwei bispezifische Antikörperkonstrukte (BiTE™, Bispecific T Cell Engager) zur Verfügung gestellt. Diese weisen die gleiche Bindungsstelle für T-Zellen auf (CD3), unterscheiden sich jedoch in Bezug auf ihre Bindungsstelle auf der Zielzelle. Name des Konstrukts Bindungsstelle T-Zelle Bindungsstelle Zielzelle MCSP-BiTE CD3 (I2C) MCSP MEC14 BiTE (Co-BiTE) CD3 (I2C) Immunologisch irrelevantes Herbizid, Mecoprop 32 3.1.6 Oligonukleotide Name Sequenz Verwendung 18S for 5’-accgattggaagtgag-3’ 18S rev 5’-cctacggaaatacgac-3’ LMP2 for 5’-gcatataagccaggcatgtctcc-3’ LMP2 rev 5’-agctgtaatagtgaccaggtagatgac-3’ LMP7 (PSMB8) for 5’-cgggtgaacaaggtgattgag-3’ LMP7 (PSMB8) rev 5’-ccatttcgcagatagtacagcc-3’ TAP1 for 5’-ccaatatgagcaccgctacct-3’ TAP1 rev 5’-ctgcagcagctgtgatttcc-3’ TAP2 for 5’-gcccatctcacagtatgaacac-3’ TAP2 rev 5’-caccttatcatcttcgcagctc-3’ 18S LMP2 LMP7 (PSMB8) TAP1 TAP2 3.1.7 Zellkulturflaschen, -platten und -röhrchen Name Hersteller 0,5ml Cups Sarstedt, Nümbrecht 1,5ml Cups Sarstedt, Nümbrecht 10ml Pipetten Corning, New York, USA 15ml Zentrifugationsröhrchen BD, Franklin Lakes, USA 2,0ml Cups Sarstedt, Nümbrecht 200ml Zentrifugationsröhrchen BD, Franklin Lakes, USA 24-well Platten Corning, New York, USA 250ml Kulturflaschen Greiner, Frickenhausen 25ml Pipetten Corning, New York, USA 2ml Pipetten Corning, New York, USA 50ml Kulturflaschen Greiner, Frickenhausen 50ml Pipetten Corning, New York, USA 50ml Zentrifugationsröhrchen BD, Franklin Lakes, USA 5ml Pipetten Corning, New York, USA 650ml Kulturflaschen Greiner, Frickenhausen 96-well Flachbodenplatte Nunc, Langenselbold 96-well Rundbodenplatten BD, Franklin Lakes, USA Combitips plus 1,25ml Eppendorf, Hamburg Combitips plus 2,5ml Eppendorf, Hamburg 33 Combitips plus 5,0ml Eppendorf, Hamburg Einfrier-Röhrchen Greiner, Frickenhausen Einmalhandschuhe Peha-Soft, M Hartmann, Heidenheim FACS-Röhrchen unsteril Sarstedt, Nümbrecht Pipettenspitzen 1.000µl Eppendorf, Hamburg Pipettenspitzen 1.000µl mit Filter Sarstedt, Nümbrecht Pipettenspitzen 100µl mit Filter Sarstedt, Nümbrecht Pipettenspitzen 10µl Eppendorf, Hamburg Pipettenspitzen 10µl mit Filter Eppendorf, Hamburg Pipettenspitzen 200µl Eppendorf, Hamburg Pipettenspitzen 20µl Eppendorf, Hamburg Pipettenspitzen 300µl Eppendorf, Hamburg Zellsiebe (0,1µm bis 100µm) BD, Franklin Lakes, USA 3.1.8 Zelllinien Zelllinie Herkunft/Referenz Mel ImSi vgl. Blank et al. (15) Na8 vgl. Blank et al. (15) Me275 vgl. Blank et al. (15) Mel Ei vgl. Wach et al. (211) Mel624 vgl. Marincola et al. (124) Mel1300 vgl. Mackensen et al. (120) A2058 vgl. Fabricant et al. (56) MeS35 Primäre Melanomzelllinie aus Biopsie MeE384.2 Primäre Melanomzelllinie aus Biopsie Laz388 vgl. Piper et al. (150) BMLF1-Klon CD8+-T-Zell-Klon, spezifisch für BMLF16 gp100-Klon vgl. Völkl et al. (210), spezifisch für gp100 Melan-A-Klon vgl. Völkl et al. (210), spezifisch für Melan-A 3.1.9 Software Graphen wurden mit GraphPad Prism 5.02 (GraphPad, La Jolla, USA) erstellt. FACS Daten wurden mit Hilfe von BD FACSDiva Software (BD, Heidelberg) aufgezeichnet. 6 Freundlicherweise von Dr. Simon Völkl, Erlangen, zur Verfügung gestellt 34 Die PC FlowJo Software Version 7.6 (Treestar, Ashland, USA) wurde für die Analyse von FACS Daten genutzt. Die Aufzeichnung und Auswertung von qPCR Daten erfolgte mit der StepOne Software Version 2.0 (Applied Biosystems, Darmstadt). 3.2 Methoden 3.2.1 Ermittlung der Zellzahl durch Trypanblaufärbung Zur Ermittlung der Zellzahl wurden Zellen in einer Lösung von 0,4% Trypanblau in 0,9% NaCl (Merck, Darmstadt) in Aqua bidest verdünnt und in einer Neubauer improvedZählkammer mit Hilfe eines Mikroskops (Axiostar Plus, Carl Zeiss, Göttingen) gezählt. Diese Methode erlaubt die Unterscheidung von lebenden und toten Zellen, da nur abgestorbene Zellen eine Blaufärbung aufgrund fehlender Membranintegrität aufweisen. Die Zellzahl pro ml wurde mit folgender Formel berechnet: Anzahl der lebenden Zellen -------------------------------------------------- x Verdünnungsfaktor x 10.000 = Zellzahl/ml Anzahl der ausgezählten Großquadrate 3.2.2 Kryokonservierung von Zellen Die Zellen wurden gezählt und in 1ml gekühltem Einfriermedium DMSO aufgenommen. Anschließend wurde die Zellsuspension in gekühlte Einfrierröhrchen abgefüllt, wobei eine Zellzahl von 100x106 Zellen pro Einfrierröhrchen nicht überschritten wurde. Die befüllten Einfrierröhrchen wurden in eine auf 4°C vorgekühlte Cryobox „Mr. Frosty“ (Nalgene Nunc, International Hereford, UK) gestellt und über Nacht bei -80°C gelagert. Die mit Isopropanol gefüllten Einfrierboxen gewährleisten ein definiertes Abkühlen der Zellen um circa -1°C/ml pro min. Danach wurden die Zellen über flüssigem N2 gelagert. 3.2.3 Auftauen von Zellen Die tiefgekühlten Zellen wurden langsam bei RT (Raumtemperatur) erwärmt. Danach wurde den Zellen sukzessiv serumhaltiges Medium (je nach Zellart T-Zell-Medium oder FCS-haltiges Medium, RT) zugeführt. Dieses Vorgehen gewährleistet ein zügiges und schonendes Auftauen der Zellen. Im Anschluss daran wurden die Zellen sofort abzentrifugiert und in frischem Medium aufgenommen. 35 3.2.4 Kultivieren von Zelllinien 3.2.4.1 Kultivierung von Melanomzellen Adhärente Melanomzellen wurden in Kulturflaschen in Tumor-Zellmedium (B’) bei 37°C und 5% CO2 als Monolayer kultiviert. Das Wachstum wurde lichtmikroskopisch kontrolliert. Alle drei bis vier Tage wurden die Zellen mit Trypsin-EDTA vom Flaschenboden gelöst, mit PBS gewaschen, gezählt und gesplittet. Bei Bedarf erfolgte in der Zwischenzeit ein Mediumwechsel mit Tumor-Zellmedium (B’). Die Melanomzelllinien wurden in bestimmten zeitlichen Abständen auf eine Kontamination durch Mycoplasmen hin untersucht und gegebenenfalls antibiotisch mit TetracyclinHydrochlorid (Apotheke des Universitätsklinikums Erlangen) behandelt. Hierzu wurden je 250µl Kulturüberstände abgenommen, zentrifugiert, und mittels qualitativer PCR auf Mycoplasmen getestet. 3.2.4.2 Kultivierung von Laz388 Laz388 (immortalisierte, EBV-transformierte B-Lymphozyten) wurden als Suspensionszellen in Kulturflaschen in Tumor-Zellmedium (B’) bei 37°C und 5% CO2 kultiviert. Alle drei bis vier Tage wurden die Zellen mit PBS gewaschen, gezählt und gesplittet. Bei Bedarf erfolgte in der Zwischenzeit ein Mediumwechsel mit TumorZellmedium (B’). In wöchentlichen Abständen wurde Laz388 mittels qualitativer PCR auf eine Kontamination durch Mycoplasmen untersucht. Bei positivem Testergebnis wurde die Zelllinie verworfen. 3.2.4.3 Kultivierung von CD8+-T-Zell-Klonen CD8+-T-Zellen klonalen Ursprungs wurden in 96-well Rundbodenplatten in T-ZellMedium (A’) bei 37°C und 5% CO2 kultiviert. Alle zwei Wochen wurden je 2,5x104 TZellen mit 6x104 bei 30Gy bestrahlten allogenen MNCs (Mononuclear cell) und 1,5x104 bei 60Gy bestrahlten Laz388 in 225µl T-Zell-Stimulationsmedium mit PHA-L ausgesät. Die Zielkonzentration von PHA-L betrug 1µg/ml. Am Tag nach der Aussaat wurde die Hälfte des Mediums gewechselt. Sodann wurde alle drei bis vier Tage das Medium gewechselt und die Zellen bei Bedarf gesplittet. In wöchentlichen Abständen wurden die T-Zell-Klone mittels qualitativer PCR auf eine Kontamination durch Mycoplasmen untersucht. Positiv getestete Klone wurden verworfen. Reinheit und Spezifität wurden ebenfalls wöchentlich durchflusszytometrisch bestimmt. Aufgrund der Mehrfarbmessung wurde zuvor eine Kompensation durchgeführt. Es wurden für alle 36 Experimente nur T-Zell-Klone mit einem Anteil von mindestens 70% antigenspezifischer T-Zellen verwendet. 3.2.4.4 Co-Kulturen aus Melanomzellen und CD8+-T-Zell-Klonen Drei verschiedene Melanomzelllinien (Mel ImSi, A2058 und Mel624) wurden von Tag1 (1. Kill) bis Tag5 und von Tag12 (2. Kill) bis Tag16 (bzw. Tag15) mit klonalen CD8+-TZellen in verschiedenen Versuchsansätzen kultiviert. Dies geschah entweder mit MCSPBiTE (100ng/ml), mit Co-BiTE (Kontrolle) (100ng/ml) oder ohne BiTE. Das E:TVerhältnis betrug in allen Ansätzen 1:5 (ca. 133.000 T-Zellen auf 800.000 Melanomzellen). Als Medium wurde Tumor-Zellmedium (B’) verwendet. Die überlebenden Melanomzellen wurden weiter kultiviert und analysiert. 3.2.5 Durchflusszytometrie und Zellsortierung Die Durchflusszytometrie dient der Detektion von zellgebundenen Farbstoffen und liefert phänotypische Aussagen über die gefärbten Zellen. Dazu werden die Zellen in einer Trägerflüssigkeit an einem Laserstrahl vorbeigeführt. Im verwendeten Gerät (FACSCanto II, BD, Heidelberg) stehen drei Laser für die Anregung der Farbstoffe zur Verfügung. Damit können für jede Zelle bis zu acht Parameter ermittelt werden. Außerdem wird die Lichtstreuung jeder Zelle detektiert: Das „Vorwärts-Streulicht“ (Forward Scatter, FSC) liefert Informationen über die Größe der Zellen. Das „SeitwärtsStreulicht“ (Side Scatter, SSC) vermittelt Informationen über die Granularität der Zelle. Als Farbstoffkonjugate wurden FITC (Fluorothioisocyanat), PE (Phycoerythrine), PECy7, PerCP (Peridin-Chlorophyll-Protein) und APC (Allophycocyanine) verwendet. Mit Hilfe dieser Technik ist auch eine Zellsortierung anhand der gebundenen Antikörper möglich. Dies wurde mit Hilfe eines MoFlo Sorters (Cytomation, Freiburg) durchgeführt. 3.2.6 Antikörperfärbung 3.2.6.1 Direkte Antikörperfärbung Die zu untersuchenden Zellen wurden in FACS-Röhrchen geerntet und in PBS gewaschen. Anschließend wurde die vom Hersteller angegebene Menge von Antikörpern auf das Zellpellet pipettiert und für 10min bei 4°C im Dunkeln inkubiert. Nach erneuter Zentrifugation mit PBS wurden die Zellen in 250-500µl PBS aufgenommen. Stets wurde eine entsprechende Isotyp-Kontrolle zur Abschätzung der unspezifischen Antikörperbindungen an die Zielzelle mitgeführt. Mehrfachfärbungen 37 wurden nicht durchgeführt. Die Daten wurden anschließend mit der Software FlowJo Software Version 7.6 ausgewertet. 3.2.6.2 Intrazelluläre Antikörperfärbung mit Sekundärantikörpern Für die durchflusszytometrische Analyse von intrazellulären Molekülen (gp100 und Melan-A) wurden die Melanomzellen geerntet, mit PBS gewaschen und mit 250µl Fixierungs-/Permeabilisierungs-Lösung für die Dauer von 20min bei 4°C fixiert. Die permeabilisierten Zellen wurden zweimal mit Perm/Wash gewaschen, mit der vom Hersteller angegebenen Menge an Primärantikörper für die Intrazellulärfärbung für 60min bei 20°C im Dunkeln inkubiert und dann einmal mit Perm/Wash gewaschen. Danach erfolgte die Zugabe des Sekundärantikörpers in der vom Hersteller angegebenen Menge. Die Zellen wurden anschließend für 30min bei 4°C im Dunkeln inkubiert. Nach erneutem Waschen mit Perm/Wash und PBS wurden die Zellen in 250500µl PBS aufgenommen und im Durchflusszytometer analysiert. Hierbei wurde stets eine entsprechende Isotyp-Kontrolle zur Abschätzung der unspezifischen Antikörperbindungen an die Zielzelle mitgeführt. Mehrfachfärbungen wurden nicht durchgeführt. Die Daten wurden anschließend wie die Daten der direkten Antikörperfärbung ausgewertet. 3.2.6.3 Peptid-MHC-Tetramerfärbung Zum Nachweis spezifischer klonaler CD8+-T-Zellen wurden die Zellen geerntet, einmal mit PBS gewaschen und danach mit der angegebenen Menge des jeweiligen PEgelabelten Peptid-MHC-Tetramers für 30min bei RT im Dunkeln inkubiert. Im Anschluss daran wurde die Oberflächenfärbung gegen CD3, CD4 und CD8 mit direktkonjugierten Antikörpern durchgeführt. Nach der Inkubationszeit der Antikörperfärbung wurden die Zellen einmal mit PBS gewaschen, in 250-500µl PBS aufgenommen und anschließend im Durchflusszytometer analysiert. Die Daten wurden anschließend mit der Software FlowJo Software Version 7.6 ausgewertet. 3.2.7 Dichtegradientenzentrifugation Mittels Leukapherese wurde von gesunden freiwilligen Spendern Zellen gewonnen. Diese wurden anschließend 1:1 mit PBS verdünnt und auf LymphozytenseparationsLösung aufgetragen. Nach 20min Zentrifugation (900g*/RT) hatten sich die Zellen des Leukapherisats entsprechend ihrer Dichte in eine schwere Fraktion (Erythrozyten und Granulozyten), eine Interphase (MNCs) und einen Überstand getrennt. Die Zellen der 38 Interphase wurde anschließend mit einer Pipette abgesammelt, zweimal mit PBS gewaschen, gezählt und bei -80°C tiefgefroren. 3.2.8 Isolierung von Gesamt-RNA Zur Gewinnung der Gesamt-RNA wurden je 1,0x106 Zellen abzentrifugiert, in 1,5ml Cups aufgenommen und einmal mit PBS gewaschen. Um eine RNA-Degradation zu verhindern, wurden die Cups anschließend sofort in flüssigen N2 gegeben. Die Cups wurden im Anschluss entweder bei -80°C gelagert oder sofort auf Trockeneis gelegt um direkt mit der RNA-Isolation zu beginnen. Zur Isolierung der RNA wurde der RNeasy Mini Kit (Qiagen, Hilden) nach den Angaben des Herstellers benutzt. Die RNA wurde danach photometrisch (BioPhotometer, Eppendorf, Hamburg) quantifiziert. Die Integrität der isolierten Gesamt-RNA wurde im Anschluss mittels AgaroseGelelektrophorese kontrolliert. 3.2.9 Reverse Transkription Für die Einzelstrang-cDNA-Synthese wurden 500ng der isolierten Gesamt-RNA, 1µl Random Decamers (Ambion, Austin, USA) und 1µl 10mM dNTPs (Gibco, Darmstadt) mit Wasser auf 12µl Gesamtvolumen verdünnt, für 5min auf 65°C erhitzt und anschließend auf Eis gestellt. Dann wurde eine Lösung, bestehend aus 2µl 0,1M Dithiothreitol (Invitrogen, Burlington, Kanada), 4µl 5x First Strand Buffer (Invitrogen, Karlsruhe) und 1µl RNase Inhibitor Plus (Peqlab, Erlangen) zugegeben, anschließend 1µl SuperScript II RNase H-Reverse Transkriptase (Invitrogen, Karlsruhe) hinzugefügt und alles gemischt. Die Gesamtlösung wurde zunächst für 50min bei 42°C und dann für 15min bei 70°C inkubiert. Die cDNA wurde sodann direkt zur Amplifizierung eingesetzt oder bis zur weiteren Verwendung bei -20°C gelagert. 3.2.10 Quantitative Polymerase-Kettenreaktion (qPCR) Die quantitative Polymerase-Kettenreaktion (qPCR) wurde mit einem Brilliant II SYBR Green PCR Kit (Stratagene, Waldbronn) und einem StepOne Cycler (Applied Biosystems, Darmstadt) durchgeführt. Es wurden stets Duplikate aus einer Probe bestimmt. 39 Menge cDNA 1µl Brilliant II SYBR Green MasterMix 5µl Referenzfarbstoff (1:333 mit Wasser) 1µl Sense Primer 1nM Antisense Primer 1nM Gesamtvolumen ad, Nuklease-freies Wasser 10µl Das Protokoll bestand nach der 15min Aktivierung bei 95°C aus 50 Zyklen mit 5s Denaturierungsphase bei 95°C und 15s Annealing-/Elongationsphase bei 60°C. Die Fluoreszenzmessung erfolgte nach jedem Zyklus am Ende der Elongationsphase. Nach dem Ende des Amplifikationsprogramms wurde das Schmelzverhalten der amplifizierten DNA analysiert. Dazu wurde die DNA langsam (0,1°C/s) von 60°C auf 95°C erhitzt und die Fluoreszenz kontinuierlich gemessen. Die Aufzeichnung und Auswertung der qPCR Daten erfolgte mit der StepOne Software Version 2.0 (Applied Biosystems, Darmstadt). Als Haushaltsgen (housekeeping gene) wurde 18S rRNA, eine Untereinheit der ribosomalen RNA, verwendet. Es wurden stets mindestens zwei Messungen durchgeführt, wobei jeweils Duplikate bestimmt wurden. Als Referenz wurden mDCs (Mature dendritic cell) mitgeführt. 7 Hierbei handelt es sich um antigenpräsentierende Zellen, bei denen eine hohe Expression der Gene der APM anzunehmen ist. 3.2.11 Enzyme Linked Immunosorbent Assay (ELISA) Es wurden je 1,0x106 Melanomzellen einmal mit PBS gewaschen und anschließend auf einer 24-well Platte in 1ml Tumor-Zellmedium (B’) ausgesät. Die Überstände wurden nach 24h in 1,5ml Zellcups abgenommen, abzentrifugiert und in neue Zellcups gegeben. Anschließend wurden sie entweder bei -80°C gelagert oder sofort für die Messung verwendet. Zur Bestimmung der Menge an IL-10 in den Überständen wurde das Human IL-10 ELISA Set (BD, San Diego, USA) nach den Angaben des Herstellers benutzt. Der Gehalt an IL-10 wurde danach photometrisch mit einem ELISA-Reader (SpectraMax 190, Molecular Devices, Ismaning) quantifiziert. Die Sensitivität betrug 7,8pg/ml. Es wurden stets mindestens drei Messungen durchgeführt. 7 Freundlicherweise von Dr. Regina Gary, Erlangen, zur Verfügung gestellt 40 3.2.12 51Chrom-Zytotoxizitätstest Die Melanomzellen als Zielzellen wurden für 2h mit je 100µCi (3,7x106Bq) 51Cr pro 1,0x106 Zellen markiert und danach zweimal mit Tumor-Zellmedium (B’) sowie einmal mit T-Zell-Medium (A’) gewaschen. Anschließend wurden je 20.000 T-Zellen mit je 20.000 Melanomzellen (E:T-Verhältnisse von 1:1) in T-Zell-Medium (A’) auf 96-well Rundbodenplatten ausplattiert. Jedes Well enthielt ein Volumen von 200µl T-Zell Medium (A’). Dies geschah in bis zu drei verschiedenen Ansätzen: ohne BiTE, mit CoBiTE oder mit MCSP-BiTE. Hierbei wurde für das MCSP-BiTE und die entsprechende Kontrolle eine Konzentration von 100ng/ml gewählt. Es wurden stets Triplikate angesetzt und bestimmt. Um die spontane Absterberate der Melanomzellen (Basalfreisetzung) zu ermitteln, wurden diese in T-Zell-Medium (A’) ohne Effektorzellen und ohne BiTE ausplattiert. Die Maximalfreisetzung wurde ermittelt, indem zu den Melanomzellen Perchlorsäure in einer Zielkonzentration von 3% gegeben wurde. Nach einer Inkubation von 19h bei 37°C und 5% CO2 wurde je 100µl Überstand geerntet und die 51Cr-Freisetzung gemessen. Die cpm (counts per minute) wurden mit einem γ-Counter (Cobra II Auto-Gamma, Packard Instrument Company, Meriden, Connecticut, USA) bestimmt. Es wurden nur solche Messwerte als gültig angenommen, bei denen der Quotient aus cpmMaximalfreisetzung zu cpmBasalfreisetzung einen Wert größer zwei erreichte. Die Zytotoxizität wurde anschließend anhand folgender Formel ermittelt: cpmProbe - cpmBasalfreisetzung ------------------------------------------ x 100 = % spezifische Lyse cpmMaximalfreisetzung - cpmBasalfreisetzung Für alle dargestellten Werte wurden mindestens drei Messungen durchgeführt. 41 4 Ergebnisse 4.1 Charakterisierung der Melanomzelllinien Zunächst wurden verschiedene Melanomzelllinien auf ihr Wachstum in vitro untersucht. Hierzu wurden mehrere primäre humane Melanomzelllinien in Tumor-Zellmedium (B’) bei 37°C und 5% CO2 kultiviert. Folgende neun Melanomzelllinien wurden über einen längeren Zeitraum kultiviert: Mel ImSi, Na8, Me275, Mel Ei, Mel624, Mel1300, A2058, MeS35 und MeE384.2. Diese wurden anschließend auf die Expression verschiedener immunologisch relevanter Proteine untersucht. Abbildung 14 gibt eine schematische Übersicht über die Charakterisierung der Melanomzelllinien mit Hilfe unterschiedlicher Untersuchungsmethoden. Melanomzelllinien í ê î qPCR FACS ELISA LMP-2 FAS-L IL-10 LMP-7 gp100 (ic) TAP-1 HLA-A2 TAP-2 HLA-ABC MCSP Melan-A (ic) PD-L1 Abbildung 14: Übersicht über die Charakterisierung der Melanomzelllinien Mit Hilfe verschiedener Untersuchungstechniken (qPCR, FACS und ELISA) Melanomzelllinien auf die Expression immunologisch relevanter Proteine untersucht. wurden 42 4.1.1 Expression von LMP-2/-7 und TAP-1/-2 in Melanomzelllinien Wie bereits eingangs geschildert, spielen Änderungen der Expression von Bestandteilen der APM eine wichtige Rolle in der Tumorgenese des malignen Melanoms. Insbesondere LMP-2 und -7 sowie TAP-1 und -2 scheinen hierbei von Bedeutung zu sein (181). Aus diesem Grund sollte untersucht werden, inwieweit bei den oben genannten Melanomzelllinien Expressionsänderungen in diesem Bereich auftreten. Hierzu wurde aus Melanomzellen RNA extrahiert, aufgereinigt und mittels reverser Transkription in cDNA umgeschrieben. Anschließend wurde mittels qPCR die Expression von LMP-2 und -7 sowie TAP-1 und -2 bestimmt. Als Referenz wurde cDNA aus mDCs mitgeführt. Wie Abbildung 15 zeigt, fällt eine heterogene Genexpression der untersuchten Bestandteile der APM auf. Für die Melanomzelllinie MeE384.2 konnte ein kompletter Verlust der LMP-2 Expression sowie eine deutlich verringerte Expression von LMP-7 und TAP-1 detektiert werden. Abbildung 15: Relative Genexpression von LMP-2, LMP-7, TAP-1 und TAP-2 Gezeigt ist die relative Genexpression an LMP-2, LMP-7, TAP-1 und TAP-2 der neun Melanomzelllinien (schwarz hinterlegt) und von mDCs (Referenz, grau hinterlegt). Dargestellt sind Mittelwerte +SD (Standard deviation). 43 4.1.2 Expression von immunologisch relevanten Proteinen in Melanomzelllinien Des Weiteren wurden die Melanomzelllinien durchflusszytometrisch auf die Expression unterschiedlicher Proteine untersucht. Es wurden weitere wichtige Bestandteile der APM (HLA-ABC und HLA-A2), bekannte Melanom-assoziierte-Tumorantigene (gp100, Melan-A und MCSP), sowie PD-L1 und FAS-L (als inhibitorische Moleküle der T-ZellAntwort) gemessen. Zu beachten ist, dass einige Merkmale (HLA-ABC, HLA-A2, MCSP, FAS-L und PD-L1) an der Zelloberfläche, andere (gp100 und Melan-A) hingegen intrazellulär (ic) exprimiert werden. Für die intrazellulären Messungen wurde ein ungelabelter Primär- und ein fluoreszenzgekoppelter Sekundärantikörper verwendet. Zelluläre Oberflächenmerkmale wurden entweder mit einem FITC- (Fluorothioisocyanat) oder einem PE- (Phycoerythrine) konjugierten Antikörper gefärbt. Bei den Messungen wurde stets ein entsprechender Isotyp zur Abschätzung der unspezifischen Antikörperbindungen an die Zielzelle als Kontrolle mitgeführt. Von jeder Zelle wurden vier Merkmale bestimmt: das sog. „Vorwärts-Streulicht“ (Forward Scatter, FSC-A und FSC-W), das sog. „Seitwärts-Streulicht“ (Side Scatter, SSC) und die Stärke der Fluoreszenz. Anschließend wurden anhand des FSC-A, FSC-W und SSC die lebenden, vereinzelten Zellen bestimmt. In Abbildung 16 ist am Beispiel der Melanomzelllinie Na8 die allgemeine Gatingstrategie exemplarisch dargestellt. Abbildung 16: Gatingstrategie Melanomzellen wurden auf die Expression bestimmter immunologisch relevanter Proteine hin untersucht. Die Abbildung gibt am Beispiel der Melanomzelllinie Na8 (HLA-ABC) eine Übersicht über die verwendete Gatingstrategie. Abbildung 17 führt tabellarisch die Expression der verschiedenen mittels FACS untersuchten Proteine auf. Alle neun Melanomzelllinien sind positiv für HLA-ABC, vier negativ für HLA-A2 (Mel ImSi, Mel Ei, A2058 und MeS35). Drei der neun Zelllinien sind negativ für gp100 und Melan-A (Na8, A2058 und MeS35). Alle untersuchten Melanomzelllinien exprimieren MCSP, wohingegen PD-L1 bei allen Zelllinien mit 44 Ausnahme von Na8 nicht oder nur sehr gering nachweisbar ist. Keine der Zelllinien exprimiert FAS-L. FAS-L gp100 HLA-A2 HLA-ABC MCSP Melan-A PD-L1 Mel ImSi - + - + + + - Na8 - - + + + - + Me275 - + + + + + - Mel Ei - + - + + + (-) Mel624 - + + + + + (-) Mel1300 - + + + + + (-) A2058 - - - + + - (-) MeS35 - - + + + - (-) MeE384.2 - + - + + + (-) Positive ZL 0% 67% 56% 100% 100% 67% 11% Abbildung 17: Ergebnisse der Durchflusszytometrie Die Abbildung zeigt die Ergebnisse der durchflusszytometrischen Bestimmung der Expression von FAS-L, gp100 (ic), HLA-A 2, HLA-ABC, MCSP und Melan-A (ic) der Melanomzelllinien. In der untersten Zeile ist der Anteil der positiven Zelllinien in Bezug auf die Gesamtzahl der Zelllinien (n=9) in Prozent aufgeführt. 4.1.3 Sekretion von IL-10 in Melanomzelllinien Wie in der Einleitung beschrieben, können Tumorzellen verschiedene lösliche, immunsuppressive Faktoren wie z.B. IL-10 produzieren (169). Daher sollte untersucht werden, inwieweit dieser Faktor von den genannten Melanomzelllinien sezerniert wird (vgl. Abbildung 18). Es zeigte sich, dass drei der neun untersuchten Melanomzelllinien IL-10 produzieren: Mel Ei, Mel624 und Mel1300. Besonders hohe Werte von über 22.000pg/ml wurden für Mel1300 gemessen. Für die anderen sechs Melanomzelllinien lagen die Messwerte unterhalb der Nachweisgrenze. Abbildung 18: IL-10 Sekretion 1,0x10 6 Melanomzellen wurden für 24h in Tumorzellmedium (B’) kultiviert. Anschließend wurde mit Hilfe der ELISA-Technik die Sekretion von IL-10 in je 100µl Überstand bestimmt. 45 4.2 T-Zell vermittelte Immunantwort mit und ohne BiTEs Anschließend haben wir untersucht, ob die Expression einer oder mehrerer der Proteine zu einer Resistenz bzw. einer verminderten Sensitivität der Melanomzellen gegenüber einer MCSP-BiTE induzierten Immunantwort führt. In diesem Zusammenhang sollte außerdem untersucht werden, welchen Effekt MCSP-BiTE auf eine endogene T-Zell Lyse hat. Durch die Zugabe von Kontroll-BiTE sollte geklärt werden, ob T-Zellen durch Bindung des CD3-Anteils von BiTEs unspezifisch aktiviert werden und eine erhöhte Lyse gegen Melanomzellen vermitteln. 4.2.1 Charakterisierung spezifischer CD8+-T-Zell-Klone Als Effektorzellen standen drei verschiedene, HLA-A2 restringierte, CD8+-T-Zell-Klone zur Verfügung: ein Klon spezifisch für gp100, ein Klon spezifisch für BMLF1 und ein Klon spezifisch für Melan-A. Bei BMLF1 handelt es sich um ein EBV spezifisches Protein. Die Reinheit und Spezifität der Klone wurden wöchentlich mit Hilfe von gelabelten Peptid-MHC-Tetramer-Komplexen durchflusszytometrisch kontrolliert. Die allgemeine Gatingstrategie ist in Abbildung 19 exemplarisch am Beispiel des gp100Klones dargestellt. Abbildung 19: Durchflusszytometrische Kontrolle der T-Zell-Klone BMLF1, gp100 und Melan-A spezifische klonale CD8 +-T-Zellen wurden wöchentlich durchflusszytometrisch auf ihre Spezifität hin untersucht. Die Abbildung gibt am Beispiel des gp100-Klons eine Übersicht über die verwendete Gatingstrategie. 4.2.2 Zytotoxizität von klonalen T-Zellen gegen Melanomzellen Mit Hilfe eines 51 Chrom-Release-Assays wurde die anti-tumorale Immunreaktion + klonaler CD8 -T-Zellen gegen Melanomzellen ermittelt. Vorarbeiten haben gezeigt, dass eine Inkubationszeit von 19h bei einer BiTE-Konzentration von 100ng/ml sowie einem E:T-Verhältnis von 1:1 zu optimalen Messbedingungen führt (Daten nicht gezeigt). Wie 46 in Abbildung 20 gezeigt, bestätigen die Ergebnisse des 51 Chrom-Release die zuvor mittels FACS gewonnenen Daten. So fand eine antigenspezifische Lyse der Melanomzellen nur in den Ansätzen statt, in denen es die Daten der Durchflusszytometrie erwarten ließen (HLA-A2+ und gp100+ bzw. Melan-A+: Me275, Mel624 und Mel1300). In Ansätzen, in denen die Melanomzellen nicht antigenspezifisch erkannt wurden, fand keine bzw. nur eine geringe, unspezifische Lyse statt (Mel ImSi, Na8, Mel Ei, A2058, MeS35, MeE384.2). Mel ImSi Na8 Me275 Mel Ei Mel624 Mel1300 A2058 MeS35 MeE384.2 HLA-A2 - + + - + + - + - gp100 + - + + + + - - + Melan-A + - + + + + - - + ê ê ê Abbildung 20: Antigenspezfischer Kill von Melanomzellen durch klonale T-Zellen Neun verschiedene Melanomzelllinien wurden mit radioaktivem Chrom markiert und zusammen mit BMLF1-, gp100- oder Melan-A-Klon in einem E:T-Verhältnis von 1:1 in einen 51 Cr- Zytotoxizitätstest eingesetzt. Nach 19 Stunden wurden die Überstände abgenommen und die 51 Cr- Freisetzung der Zielzellen ermittelt. Dargestellt ist die Zytotoxizität in % als Mittelwert +SD von mindestens neun Messungen. Im Folgenden haben wir untersucht, ob durch BiTEs eine Veränderung der antitumoralen Immunreaktion zu beobachten ist. Es wurden drei verschiedene Ansätze gewählt: ohne BiTE, mit einem gegen ein immunologisch irrelevantes Peptid gerichteten Kontroll-BiTE (Co-BiTE) oder mit MCSP-BiTE. Nach einer Inkubationszeit von 19h wurde die 51 Cr-Freisetzung gemessen und die spezifische Lyse der Melanomzellen berechnet (siehe Abbildung 21). 47 Abbildung 21: Zytotoxizität von klonalen T-Zellen gegen Melanomzellen in An- bzw. Abwesenheit von MCSP-BiTE Melanomzellen wurden mit radioaktivem Chrom markiert und zusammen mit BMLF1, gp100 oder Melan-A spezifischen T-Zellen in einem E:T-Verhältnis von 1:1 in einen 51 Cr-Zytotoxizitätstest eingesetzt. Es wurde entweder kein BiTE (farblich grün hinterlegt), Co-BiTE (100ng/ml, farblich blau hinterlegt) oder MCSP-BiTE (100ng/ml, farblich rot hinterlegt) zugegeben. Nach 19 Stunden wurden die Überstände abgenommen und die 51 Cr-Freisetzung der Zielzellen ermittelt. Dargestellt ist die Zytotoxizität in % als Mittelwert +SD (y-Achse), getrennt für die drei T-Zell-Klone (xAchse), von mindestens neun Messungen. Wie aus Abbildung 21 hervorgeht, induzieren MCSP-BiTEs stets eine effektive Lyse von Melanomzellen durch klonale CD8+-T-Zellen. Alle neun Melanomzelllinien waren sensitiv gegenüber einer MCSP-BiTE induzierten T-Zell Lyse, unabhängig von den unter 4.1 beschriebenen Faktoren. Die Spezifität der klonalen CD8+-T-Zellen hatte hierbei keinen Einfluss auf die Stärke der BiTE induzierten Immunantwort. Die für jeweils eine Melanomzelllinie mit MCSP-BiTE gemessenen Werte sind für alle drei TZell-Klone vergleichbar. Außerdem konnte gezeigt werden, dass in Ansätzen, in denen bereits eine antigenspezifische Lyse stattfand (vgl. Me275, Mel624 und Mel1300), die Zugabe von MCSP-BiTE keine zusätzliche Verstärkung der Zytotoxizität zur Folge hatte. So wurden für diese drei Zelllinien ohne BiTE als auch mit MCSP-BiTE unter Verwendung von gp100 bzw. Melan-A spezifischer T-Zellen vergleichbare Werte gemessen. Des Weiteren wurde nachgewiesen, dass die Zugabe von Co-BiTE keinen Effekt auf die T-Zell vermittelte Immunantwort hat. 48 4.3 Tumor-Immune-Escape durch eine BiTE induzierte Immunantwort Wie unter 4.2.2 beschrieben, induzieren MCSP-BiTEs eine effektive Lyse MCSP positiver Melanomzellen. Diese Lyse ist unabhängig von verschiedenen immunologischen Faktoren (vgl. 4.1). Es ist jedoch bekannt, dass durch immunologisches Targeting selbst neue Mutationen entstehen bzw. Zellen mit bereits existierenden Mutationen selektiert werden können (39, 159). Aus diesem Grund stellt sich die Frage, ob eine MCSP-BiTE induzierte Immunantwort die Bildung bzw. Selektion von Resistenzen bzw. Immune-Escape-Mechanismen auslösen kann. Zur Klärung dieser Fragestellung wurden die drei Melanomzelllinien Mel ImSi, A2058 und Mel624 in mit klonalen CD8+-T-Zellen in verschiedenen Versuchsansätzen kokultiviert (vgl. 3.2.4.4). Dies geschah entweder mit MCSP-BiTE, mit Co-BiTE oder ohne BiTE. Die überlebenden Melanomzellen wurden anschließend weiter kultiviert, phänotypisiert und ihre Sensitivität gegenüber eines T-Zell mediierten Kills im 51Chrom Release erneut bestimmt. Für die Durchführung der Charakterisierungen und der Zytotoxizitätsassays wurden die gleichen Versuchsbedingungen wie unter 4.1 bzw. 4.2 beschrieben, gewählt. Abbildung 22 gibt einen tabellarischen Überblick über den prinzipiellen Versuchsaufbau. Klon BiTE Name ì BMLF1 + MCSP è Mel ImSi-BM î BMLF1 + Co è Mel ImSi-BC ì Melan-A + MCSP è A2058-MM î Melan-A + Co è A2058-MC ì BMLF1 + MCSP è Mel624-BM ì BMLF1 + Co è Mel624-BC è BMLF1 - è Mel624-B î gp100 - è Mel624-G î Melan-A - è Mel624-M Mel ImSi A2058 Mel624 Abbildung 22: Übersicht über den Versuchsaufbau Die Melanomzelllinien Mel ImSi, A2058 und Mel624 wurden mit klonalen CTL und MCSP-, Cooder ohne BiTE inkubiert. Die überlebenden Melanomzellen wurden weiter kultiviert und charakterisiert. 49 4.3.1 Effekt auf die Melanomzelllinie Mel ImSi Melanomzellen der Zelllinie Mel ImSi wurden von Tag1-5 und von Tag12-16 mit BMLF1 spezifischen T-Zellen und MCSP-BiTE oder Co-BiTE kultiviert. Die Mel ImSi Zellen, die mit MCSP-BiTE inkubiert wurden, werden im Folgenden als Mel ImSi-BM (BMLF1-Klon und MCSP-BiTE) bezeichnet, die mit Co-BiTE inkubierten Zellen als Mel ImSi-BC (BMLF1-Klon und Co-BiTE). Zunächst sollte untersucht werden, ob durch die Zugabe von BiTEs eine Veränderung der MCSP-Expression zu beobachten ist. Abbildung 23 zeigt die MCSP Expression von Mel ImSi-BM und Mel ImSi-BC an Tag16. Wie zu erkennen, kommt es zu keinem Verlust der MCSP Expression. Mel ImSi-BM Mel ImSi-BC Abbildung 23: MCSP Expression von Mel ImSi-BM und Mel ImSi-BC Gezeigt ist die durchflusszytometrische Messung der MCSP-Expression (rot hinterlegt) von Mel ImSi-BM und Mel ImSi-BC an Tag16. Der entsprechende Isotyp ist schwarz hinterlegt. Um zu bestimmen, ob es zur Ausbildung MCSP unabhängiger Tumor-Immune-EscapeMechanismen gekommen ist, wurde an Tag23 die Sensitivität der Melanomzellen gegenüber einem T-Zell mediierten Kill im 51 Chrom Release untersucht (siehe Abbildung 24). Es konnte demonstriert werden, dass sich Mel ImSi-BM in Anwesenheit von MCSP-BiTEs von allen drei T-Zell-Klonen lysieren lässt. Die Stärke der Lyse entspricht derjenigen von Mel ImSi-BC. In Ansätzen ohne BiTE oder mit Co-BiTE fand hingegen keine Zelllyse statt. Diese Ergebnisse deuten darauf hin, dass es weder zu einem MCSP abhängigen noch zu einem MCSP unabhängigen Tumor-Immune-EscapeMechanismus gekommen ist. 50 Abbildung 24: Sensitivität von Mel ImSi-BM und Mel ImSi-BC gegenüber einem T-Zell vermittelten Killing An Tag23 wurde mittels 51 Cr-Release die Sensitivität der zuvor mit BMLF1-Klon und MCSP-BiTE inkubierten Melanomzellen (Mel ImSi-BM) und der entsprechenden Kontrolle Mel ImSi-BC gegenüber einer T-Zell vermittelten Immunantwort bestimmt. Dargestellt ist die Zytotoxizität in % als Mittelwert +SD. 4.3.2 Effekt auf die Melanomzelllinie A2058 Analog zur Melanomzelllinie Mel ImSi wurde die Zelllinie A2058 von Tag1-5 und von Tag12-16 mit klonalen CD8+-T-Zellen und BiTEs inkubiert. Im Unterschied zu dem unter 4.3.1 beschrieben Versuch wurden diesmal jedoch Melan-A spezifische T-Zellen als Effektorzellen verwendet. Die beiden Melanomzelllinien werden im Folgenden mit A2058-MM (Melan-A-Klon und MCSP-BiTE) bzw. A2058-MC (Melan-A-Klon und Co-BiTE) bezeichnet. Zunächst sollte wieder untersucht werden, ob durch die Zugabe von BiTEs eine Veränderung der MCSP-Expression zu beobachten ist. Abbildung 25 zeigt die MCSP Expression von A2058-MM und A2058-MC an Tag23. In Übereinstimmung mit den Ergebnissen des vorherigen Versuches mit Mel ImSi, kommt es auch in diesen Ansätzen zu keinem MCSP-Verlust. A2058-MM A2058-MC Abbildung 25: MCSP Expression von A2058-MM und A2058-MC Gezeigt ist die durchflusszytometrische Messung der MCSP-Expression (rot hinterlegt) von A2058MM und A2058-MC an Tag23. Der entsprechende Isotyp ist schwarz hinterlegt. 51 An Tag29 wurden zusätzlich alle weiteren unter 4.1 beschriebenen Faktoren erneut bestimmt. Hierbei zeigte sich im FACS kein Unterschied der beiden Zelllinien zueinander noch zu A2058 (Daten nicht gezeigt). Außerdem wurden A2058-MM und A2058-MC mittels qPCR auf die Expression von LMP-2 und -7 sowie TAP-1 und -2 untersucht. Auch hier war kein Unterschied zwischen den mit MCSP-BiTE und den mit Co-BiTE inkubierten Zellen zu erkennen ist (vgl. Abbildung 26). Abbildung 26: Relative Genexpression von A2058-MM und A2058-MC Gezeigt ist die relative Genexpression an LMP-2, LMP-7, TAP-1 und TAP-2 der beiden Melanomzelllinien A2058-MM und A2058-MC (schwarz hinterlegt) an Tag29. Als Referenz wurden mDCs (grau hinterlegt) mitgeführt. Dargestellt sind Mittelwerte +SD. Anschließend wurde mit Hilfe eines ELISAs die IL-10 Sekretion von A2058-MM und A2058-MC gemessen. Diese blieb für beide Zelllinien negativ (Daten nicht gezeigt). Um die Entstehung eines anderen, bis dato nicht nachgewiesenen Tumor-Immune-EscapeMechanismus sicher ausschließen zu können, wurde an Tag29 die Sensitivität von A2058-MM und A2058-MC gegenüber einem T-Zell vermittelten Killing untersucht. Die Ergebnisse des Zytotoxizitätsassays zeigen, dass beide Zelllinien weiterhin sensitiv gegenüber einer MCSP-BiTE induzierten Immunantwort durch klonale CD8+-T-Zellen sind (vgl. Abbildung 27). 52 Abbildung 27: Sensitivität von A2058-MM und A2058-MC gegenüber einem T-Zell vermittelten Killing An Tag29 wurde mittels 51Cr-Release die Sensitivität der zuvor mit Melan-A-Klon und MCSP-BiTE inkubierten Melanomzellen (A2058-MM) und der entsprechenden Kontrolle A2058-MC gegenüber einer T-Zell vermittelten Immunantwort bestimmt. Dargestellt ist die Zytotoxizität in % als Mittelwert +SD. 4.3.3 Effekt auf die Melanomzelllinie Mel624 Die Melanomzelllinie Mel624 wurde wie Mel ImSi und A2058 mit klonalen CD8+-TZellen und BiTE inkubiert. Als Effektorzellen wurden BMLF1 spezifische T-Zellen verwendet. Die beiden Melanomzelllinien werden als Mel624-BM (BMLF1-Klon und MCSP-BiTE) bzw. Mel624-BC (BMLF1-Klon und Co-BiTE) bezeichnet. Abbildung 28 gibt eine schematische Übersicht über den Versuchsaufbau. d1 d12 d23 d36 • 1.Kill • 2.Kill • Chrom • qPCR Release d50 d61 d72 d79 d83 • Chrom • Chrom • Chrom • ELISA • Chrom Release Release Release • qPCR Release Abbildung 28: Übersicht über den zeitlichen Versuchsablauf für Mel624-BM und Mel624-BC Die Melanomzelllinie Mel624 wurde von d1 bis d5 und von d12 bis d16 mit BMLF1 spezifischen CTL und MCSP-BiTE oder Co-BiTE kultiviert. Die überlebenden Melanomzellen wurden weiter kultiviert und analysiert. Die Abbildung gibt eine Übersicht über den Versuchsaufbau. Man beachte die nicht lineare Einteilung der Zeitachse. Zunächst wurde wieder die MCSP Expression beider Zelllinien mittels FACS untersucht. Hierbei zeigte sich an Tag4 nach dem zweiten Kill (Tag16) eine deutlich erniedrigte MCSP Expression von Mel624-BM verglichen mit Mel624-BC (vgl. Abbildung 29). 53 Mel624-BM Mel624-BC Abbildung 29: MCSP Expression von Mel624-BM und Mel624-BC Gezeigt ist die durchflusszytometrische Messung der MCSP-Expression (rot hinterlegt) von Mel624-BM und Mel624-BC an Tag16. Der entsprechende Isotyp ist schwarz hinterlegt. Vor diesem Hintergrund wurde die MCSP Expression beider Zelllinien über die Dauer von mehr als 80 Tagen in bestimmten zeitlichen Abständen bestimmt. Für die Quantifizierung der Herunterregulation von MCSP wurde der für Mel624-BM gemessene Mittelwert bzw. Mean (abzüglich des Isotyps) mit dem für Mel624-BC gemessenen Mittelwert bzw. Mean (abzüglich des Isotyps) ins Verhältnis gesetzt. Die für Mel624-BC gemessenen Werte wurden hierbei als Referenz (100%) verwendet. Wie Abbildung 30 zeigt, liegen die für Mel624-BM gemessenen MCSP-Werte, verglichen mit denjenigen von Mel624-BC, über den kompletten Beobachtungszeitraum von 83 Tagen stabil bei etwa 15-20%. Abbildung 30: Relative MCSP Expression von Mel624-BM Gezeigt ist die relative MCSP Expression von MEL624-BM (bezogen auf Mel624-BC, 100%) über einen Beobachtungszeitraum von 83d. Hierfür wurden die für Mel624-BM gemessenen Mittelwerte (abzüglich des Isotyps) mit den für Mel624-BC gemessenen Mittelwerten (abzüglich des Isotyps) ins Verhältnis gesetzt. An Tag79 wurden Mel624-BM und Mel624-BC außerdem auf die Expression der unter 4.1 beschriebenen Faktoren untersucht. Für die mittels Durchflusszytometrie 54 bestimmten Faktoren konnte, mit Ausnahme von MCSP und Melan-A, kein Unterschied der beiden Zelllinien zueinander noch mit Mel624 festgestellt werden (Melan-A siehe Abbildung 31, restliche Daten nicht gezeigt). Wie aus Abbildung 31 hervorgeht, zeigt Mel624-BM eine etwas geringere Melan-A-Expression als Mel624-BC. Mel624-BM Mel624-BC Abbildung 31: Melan-A Expression von Mel624-BM und Mel624-BC Gezeigt ist die durchflusszytometrische Messung der Melan-A-Expression (rot hinterlegt) von Mel624-BM und Mel624-BC an Tag79. Der entsprechende Isotyp ist schwarz hinterlegt. Kein Unterschied konnte in Bezug auf die Expression von LMP-2 und -7 sowie TAP-1 und -2 an Tag36 und Tag79 detektiert werden (vgl. Abbildung 32). Abbildung 32: Relative Genexpression von Mel624-BM und Mel624-BC Gezeigt ist die relative Genexpression an LMP-2, LMP-7, TAP-1 und TAP-2 der beiden Melanomzelllinien Mel624-BM und Mel624-BC (schwarz hinterlegt) an Tag36 und Tag79. Als Referenz wurden mDCs (grau hinterlegt) mitgeführt. Dargestellt sind Mittelwerte +SD. Mittels ELISA erfolgte an Tag79 eine Analyse der IL-10 Sekretion. Die Bestimmung der IL-10 Sekretion ergab, dass, im Unterschied zu Mel624, beide Langzeitkulturen (Mel624-BM und Mel624-BC) kein IL-10 sezernieren (Daten nicht gezeigt). Als Nächstes sollte untersucht werden, welchen Einfluss die verminderte MCSP Expression 55 von Mel624-BM auf deren Sensitivität gegenüber einer T-Zell Immunantwort hat. Außerdem sollte geprüft werden, ob es zur Entwicklung von MCSP unabhängigen Resistenzmechanismen gekommen ist. Abbildung 33 zeigt die Ergebnisse der Zytotoxizitätsassays von Tag23 und Tag50 (Daten Tag61, Tag72 und Tag83 nicht gezeigt, vgl. Abbildung 34). Man kann hierbei eine im Vergleich mit der Kontrollzelllinie Mel624-BC geringere MCSP-BiTE induzierte Lyse von Mel624-BM durch BMLF1 spezifische T-Zellen erkennen (vgl. auch Abbildung 34). Des Weiteren geht aus den Ergebnissen hervor, dass die antigenspezifische Lyse von Mel624-BM durch gp100 spezifischen CD8+-T-Zellen derjenigen von Mel624-BC entspricht (vgl. auch Abbildung 34). Die antigenspezifische Lyse durch Melan-A spezifische T-Zellen scheint hingegen d50 d23 erniedrigt zu sein (vgl. auch Abbildung 34). Abbildung 33: Sensitivität von Mel624-BM und Mel624-BC gegenüber einem T-Zell vermittelten Killing An Tag23,Tag50, Tag61, Tag72 und Tag83 wurde mittels 51Cr-Release die Sensitivität der zuvor mit BMLF1-Klon und MCSP-BiTE inkubierten Melanomzellen (Mel624-BM) und der entsprechenden Kontrolle Mel624-BC gegenüber einer T-Zell vermittelten Immunantwort bestimmt. Dargestellt ist die Zytotoxizität in % als Mittelwert +SD an Tag23 und Tag50. In Abbildung 34 sind die über den gesamten Beobachtungszeitraum von 83Tagen erhobenen Daten des 51Chrom-Release noch einmal zusammengefasst. Die Grafik zeigt die relative Sensitivität von Mel624-BM gegenüber einem antigenspezifischen Kill auf der einen und einem MCSP-BiTE induzierten Kill auf der anderen Seite. Dazu wurden die für Mel624-BM gemessenen Werte mit denen von Mel624-BC (100%) ins Verhältnis 56 gesetzt. Aus der Grafik lassen sich drei Schlussfolgerungen ziehen: Die Sensitivität von Mel624-BM gegenüber einer MCSP-BiTE induzierten Immunantwort durch BMLF1 spezifische CD8+-T-Zellen ist dauerhaft auf etwa 25-45% erniedrigt. Die antigenspezifische Lyse von Mel624-BM durch gp100 spezifische CD8+-T-Zellen entspricht derjenigen der Kontrollzelllinie wohingegen die antigenspezifische Lyse von Mel624-BM durch Melan-A spezifische CD8+-T-Zellen auf etwa 80% reduziert ist. Abbildung 34: Relative Sensibilität von Mel624-BM gegenüber einem T-Zell vermittelten Killing Gezeigt ist die relative Sensitivität von MEL624-BM (bezogen auf Mel624-BC, 100%) gegenüber einem antigenspezifischen Kill (gp100-Klon und Melan-A-Klon) sowie einem MCSP-BiTE induzierten Kill (BMLF1-Klon + MCSP-BiTE) über einen Beobachtungszeitraum von 83d. Hierfür wurden die für Mel624-BM gemessenen Mittelwerte mit den für Mel624-BC gemessenen Mittelwerten ins Verhältnis gesetzt. Diese Ergebnisse deuten folglich auf die Entstehung eines effektiven Tumor-ImmuneEscape-Mechanismus in Mel624 hin. Alle erhobenen Daten sprechen dafür, dass dieser auf die Herunterregulation von MCSP zurückzuführen ist. Vor dem Hintergrund, dass zwar in Mel624, nicht jedoch in Mel ImSi und A2058 ein Tumor-Immune-EscapeMechanismus induziert werden konnte, sollte geprüft werden, ob speziell Mel624 besonders suszeptibel für die Entstehung von Resistenzmechanismen ist. Um diese Frage zu beantworten, wurde die Melanomzelllinie Mel624 von Tag1-5 und von Tag1215 entweder mit gp100-Klon (Mel624-G) oder Melan-A-Klon (Mel624-M) inkubiert. BiTEs wurden in keinem der Ansätze zugegeben. Die überlebenden Zellen wurden weiter kultiviert und charakterisiert. Als Kontrolle wurde hierbei ein Ansatz mit BMLF1 spezifischen CD8+-T-Zellen mitgeführt, da eine Interaktion des TCR mit den Melanomzellen aufgrund der Antigenspezifität der T-Zellen auszuschließen ist (Mel624B). Im Unterschied zu den bisher beschriebenen Versuchen wurden die vorliegenden Ansätze bereits an Tag3 nach dem 2. Kill (Tag15) gesplittet, da bei der 57 lichtmikroskopischen Kontrolle des Wachstumsverhaltens von Mel624-G nur noch wenige vitale Zellen identifiziert werden konnten. Zunächst wurde wieder die Antigen-Expression aller drei Zelllinien durchflusszytometrisch ermittelt. Hierbei konnte kein Unterschied zwischen Mel624-G bzw. Mel624-M mit der Kontrollzelllinie Mel624-B noch im Vergleich zur Ausgangslinie Mel624 festgestellt werden (vgl. Abbildung 35 für MCSP, gp100 und Melan-A, restliche Daten nicht gezeigt). Mel624-G Mel624-M Melan-A gp100 MCSP Mel624-B Abbildung 35: Antigen-Expression von Mel624-B, Mel624-G und Mel624-M Gezeigt ist die durchflusszytometrische Messung der MCSP-, gp100- und Melan-A-Expression (rot hinterlegt) von Mel624-E, Mel624-G und Mel624-M an Tag30. Der entsprechende Isotyp ist schwarz hinterlegt. An Tag30 wurde außerdem die Expression von LMP-2 und -7 sowie TAP-1 und -2 bestimmt. Hierbei konnte ebenfalls kein Unterschied zwischen den drei Zelllinien festgestellt werden (vgl. Abbildung 36). 58 Abbildung 36: Relative Genexpression von Mel624-B, Mel624-G und Mel624-M Gezeigt ist die relative Genexpression an LMP-2, LMP-7, TAP-1 und TAP-2 der drei Melanomzelllinien (schwarz hinterlegt) an Tag30. Als Referenz wurden mDCs (grau hinterlegt) mitgeführt. Dargestellt sind Mittelwerte +SD. Für alle drei Zelllinien wurde an Tag30 mittels ELISA eine geringe IL-10 Sekretion nachgewiesen (Daten nicht gezeigt). Um zu bestimmen, ob es zur Bildung eines Resistenz-Mechanismus gekommen ist, wurde an Tag12 und an Tag23 die Sensitivität der Melanomzellen gegenüber einem TZell mediierten Kill untersucht (vgl.Abbildung 37). Es konnte gezeigt werden, dass die Ergebnisse von Mel624-G und Mel624-M mit denen der Kontrollzelllinie Mel624-B übereinstimmen. Die Entwicklung eines Resistenzmechanismus scheint damit nicht stattgefunden zu haben. Eine besondere Suszeptibilität von Mel624 zur Bildung von d23 d12 Tumor-Immune-Escape-Mechanismen ist damit wahrscheinlich nicht gegeben. Abbildung 37: Sensitivität von Mel624-B, Mel624-G und Mel624-M gegenüber einem T-Zell vermittelten Killing An Tag12 und Tag23 wurde mittels 51 Cr-Release die Sensitivität von Mel624-G und Mel624-M sowie der entsprechenden Kontrolle Mel624-B gegenüber einer T-Zell vermittelten Immunantwort bestimmt. Dargestellt ist die Zytotoxizität in % als Mittelwert +SD. 59 4.4 Zytotoxisches Potential verschiedener T-Zell-Subpopulationen nach BiTE induzierter Stimulation BiTEs zeichnen sich dadurch aus, dass sie spezifisch an CD3 und somit potentiell an alle T-Zellen binden (5). Ihr Potential, T-Zellen für eine Immunantwort zu rekrutieren, ist folglich nicht auf CD8+-T-Zellen beschränkt. Daher stellt sich die Frage, welche CD3+-Effektorzellpopulationen in der Lage sind, eine BiTE induzierte Immunantwort gegen Melanomzellen zu vermitteln. Hierzu wurden MNCs von gesunden Spendern mit vier verschiedenen fluoreszenzkonjugierten Antikörpern gegen die Oberflächenmerkmale CD4 (FITC), CD8 (PeCy7), CD25 (PE) und TCRαß (APC) gefärbt. Mittels Zellsorting konnten anhand der gebundenen Antikörper folgende TZell-Subpopulationen bei einer Reinheit von über 95% gewonnen werden: CD4+-TZellen, CD8+-T-Zellen, CD4+CD25+-T-Zellen (Treg) und CD4-CD8-TCRαß+-T-Zellen (Doppelt Negative T-Zelle, DN). Die verschiedenen T-Zell-Subpopulationen wurden anschließend als Effektorzellen in einen Zytotoxizitätsassay eingesetzt. Als Zielzellen diente die mit radioaktivem 51 Cr markierte Melanomzelllinie Na8. Es wurden die gleichen Versuchsbedingungen angewandt wie unter 3.2.12 bzw. 4.2.2. Wie aus Abbildung 38 ersichtlich ist, vermittelten alle untersuchten T-Zell-Subpopulationen, wenn auch in unterschiedlichem Ausmaß, eine MCSP-BiTE induzierte Immunantwort gegen die Melanomzelllinie Na8. Die stärkste Lyse wurde hierbei von CD4+-T-Zellen (20,4%) vermittelt, gefolgt von CD8+-T-Zellen (13,2%), CD4+CD25+-T-Zellen (8,2%) und DNs (7,9%). In Ansätzen ohne BiTE bzw. mit Co-BiTE konnte hingegen keine bzw. nur eine minimale, unspezifische Zelllyse detektiert werden. Abbildung 38: BiTE induzierte Immunantwort durch verschiedener T-Zell-Subpopulationen Native CD4 +-T-Zellen, CD8 +-T-Zellen, CD4 +CD25 +-T-Zellen und DNs wurden auf ihr Potential getestet, eine BiTE induzierte Immunantwort gegen die Melanomzelllinie Na8 zu vermitteln. Dargestellt ist die Zytotoxizität in % als Mittelwert +SD von mindestens sechs Messungen. 60 5 Diskussion Für die erfolgreiche Entwicklung neuer Antitumortherapeutika ist die Auswahl eines geeigneten und stabilen Angriffspunktes für das Pharmakon von entscheidender Bedeutung. So war es durch die Entdeckung des BCR-ABL Fusionsgens auf dem „Philadelphia Chromosom“ möglich, ein wirkungsvolles Therapeutikum für die Behandlung von Patienten mit chronisch myeloischer Leukämie zu entwickeln (Imatinib bzw. Glivec/Gleevec) (41, 73, 141). Auf der anderen Seite gestaltet sich die Therapie der AIDS-Erkrankung nicht zuletzt aufgrund der hoher Mutationsrate des HIV als äußerst schwierig und komplex (153, 216). Bei dem in dieser Arbeit verwendeten BiTE handelt es sich um ein Antikörperkonstrukt, das spezifisch an MCSP (CSPG4, gp240, HMWMAA, MEL-CSPG, MCSPG bzw. NG2) bindet (198). MCSP ist ein Proteoglycan, das bereits früh in der Tumorgenese des malignen Melanoms exprimiert wird (29, 155). Es ist jedoch nicht abschließend geklärt, welche Funktion und Bedeutung MCSP in diesem Prozess zukommt (30). Ergebnissen von Burg et al. zufolge, spielt die MCSP Expression eine wichtige Rolle bei der Proliferation von Melanomzellen und trägt zu deren Metastasierungspotential bei (26). Iida et al. konnten zeigen, dass MCSP durch Wechselwirkung mit bestimmten Integrinen einen Einfluss auf die Zelladhäsion von Melanomzellen hat (85). Außerdem wiesen sie nach, dass eine Stimulation von MCSP mit einer erhöhten Aktivität der Rho-GTPase Cdc42 einhergeht, was möglicherweise das Tumorwachstum beeinflusst (52). Des Weiteren berichteten sie, dass MCSP mit MT3-MMP interagiert. Dieser Prozess scheint für die Invasion von Melanomzellen in Typ I Kollagen nötig zu sein (86). Mittels Transfektion gelang es Yang et al., MCSP in einer MCSP negativen Melanomzelllinie zu exprimieren (217). Dies führte zu einer Aktivierung von wichtigen Bestandteilen von zellulären Wachstumssignalkaskaden, wie z.B. FAK und ERK-1/-2. Zusammenfassend kann daher festgehalten werden, dass MCSP wahrscheinlich eine zentrale Rolle für das Tumorwachstum spielt und zu dessen Invasivität beiträgt (33, 52). Im Rahmen dieser Arbeit wurde die MCSP Expression von neun Melanomzelllinien durchflusszytometrisch bestimmt. Alle neun untersuchten Melanomzelllinien exprimierten MCSP (100%). Es konnte keine MCSP negative Melanomzelllinie identifiziert werden. Diese Ergebnisse stimmen mit bereits veröffentlichten Daten weitgehend überein, wonach Melanome in über 90% der Fälle MCSP exprimieren (28, 30, 58, 138, 198). Ein Zusammenhang zwischen der MCSP Expression und dem klinischen Verlauf der Erkrankung bei Patienten mit malignem Melanom besteht mit 61 Ausnahme des Akrolentiginösen Melanoms jedoch nicht (29). Für diesen Melanomtyp postulierten Kageshita et al., dass die MCSP Expression indirekt mit dem Überleben der Patienten korreliert (92, 93). Diese Behauptung ist kritisch zu bewerten. Anders als zu erwarten korrelierte die MCSP Expression zwar indirekt mit dem Überleben und dem Tumorstadium, es bestand aber keine Korrelation zwischen dem Tumorstadium und dem Überleben. Die Autoren weisen darauf hin, dass eine statistische Verzerrung der Daten (Bias) aufgrund der relativ kleinen Stichprobe nicht sicher ausgeschlossen werden kann. In einer neueren Publikation von Nishi et al. fanden die Autoren im Unterschied zu Kageshita et al. keine Korrelation zwischen dem Stadium der Erkrankung und der MCSP Expression (140). Ob die MCSP Expression mit dem Überleben korreliert, wurde von ihnen nicht untersucht. Inwieweit MCSP einen prognostischen Faktor für das Akrolentiginöse Melanom darstellt, bleibt von daher abzuwarten. Übereinstimmend wird in beiden Publikationen jedoch nachgewiesen, dass das Akrolentiginöse Melanom im Allgemeinen nur eine relativ niedrige MCSP Expression aufweist. Nishi et al. detektierten für dieses bei 51 von 95 Primärläsionen (54%) und Kageshita et al. bei neun von 32 Biopsien (28%) eine MCSP Expression (92, 140). Über die Ursache der im Vergleich zu den anderen Tumorentitäten des malignen Melanoms geringeren MCSP Expression kann derzeit nur spekuliert werden. Bis dato existieren nur sehr unzureichende Daten bezüglich der der MCSP Expression zugrunde liegenden Mechanismen. Ein Regulationsmechanismus sind wahrscheinlich epigenetische Veränderungen, wie z.B. die DNA-Methylierung. So wiesen Luo et al. nach, dass der MCSP-Promoter von MCSP negativen Melanomzellen stark methyliert ist, wohingegen der MCSP-Promoter von MCSP positiven Melanomzellen nicht methyliert ist (116). Die Autoren merken jedoch an, dass eine MCSP negative Probe (Akrolentiginöses Melanom) zwar einen unmethylierten Promoter hatte, jedoch kein MCSP exprimierte. Damit scheint die DNA Hypomethylierung zwar notwendig aber alleine nicht ausreichend für die MCSP Expression zu sein. Aufgrund der relativ kleinen Stichprobe (n=11) kann nicht sicher ausgeschlossen werden, dass das Akrolentiginöse Melanom im Vergleich zu den anderen Tumorentitäten des malignen Melanoms im Allgemeinen häufiger einen methylierten MCSP-Promoter aufweist. Die vorliegenden Forschungsergebnisse sprechen jedoch eher dafür, dass die erniedrigte MCSP Expression auf bis dato noch nicht beschriebene Faktoren bzw. Mutationen zurückzuführen ist. In ihrer Gesamtheit deuten die vorliegenden Daten dennoch darauf hin, dass MCSP von Melanomzellen zu einem hohen Anteil exprimiert wird und daher 62 für therapeutische Zwecke mit BiTEs prinzipiell ein geeignetes TAA darzustellen scheint. Die Idee, MCSP als Zielantigen für die Therapie des malignen Melanoms zu verwenden, ist nicht neu. So waren Anti-MCSP Antikörper bereits in der Vergangenheit Gegenstand verschiedener Forschungsprojekte. In Tierexperimenten wurden mit MCSP Antikörpern erfolgsversprechende Ergebnisse erzielt (24, 29, 66, 117, 125). Die Ergebnisse von klinischen Studien mit MCSP als Zielstruktur sind hingegen heterogen. Bender et al. untersuchten in einer retrospektiven Studie, an der mehr als 300 Patienten mit malignem Melanom unterschiedlicher Tumorstadien beteiligt waren, den Effekt von diagnostisch verabreichten 99m Tc gefärbten F(ab’)2-Fragmenten gegen MCSP (11). Sie wiesen nach, dass Patienten, die zwei oder mehr Injektionen mit F(ab’)2-Fragmenten erhalten hatten, ein besseres Gesamtüberleben zeigten als Patienten, die nur eine Injektion bekommen hatten. Mittelmann et al. konnten in einer Studie an 25 Patienten mit malignem Melanom im Stadium IV einen positiven Effekt von anti-idiotypischen Antikörpern, die das MCSP-Antigen nachahmen, demonstrieren (57, 130). Der therapeutische Effekt von monoklonalen Anti-MCSP Antikörpern war in bisher durchgeführten klinischen Studien allerdings begrenzt. So konnte zwar die prinzipielle Wirksamkeit von monoklonalen Anti-MCSP Antikörpern gekoppelt an ein Toxin bestätigt werden, jedoch wurden nur geringe klinische Ansprechraten beobachtet (29, 145, 188). Dies ist eventuell auf die Entstehung von neutralisierenden Antikörpern gegen die verabreichten Mausantikörpern zurückzuführen (176). Hierin liegt möglicherweise einer der entscheidenden Vorteile von MCSP Antikörpern im BiTE Format. So konnten in klinischen Studien mit Blinatumomab (CD19-BiTE) bisher keine neutralisierenden Antikörper gegen Blinatumomab nachgewiesen werden (135). Diese Daten deuten darauf hin, dass im menschlichen Körper weder präexistierende, neutralisierende Antikörper gegen BiTEs vorkommen noch durch die Gabe von BiTEs deren Bildung induziert wird. Ein weiteres Problem der Antikörpertherapie ist die Entwicklung von Autoimmuntoxizität (3, 127). Auch hier scheint das BiTE Format erfolgversprechend zu sein. In klinischen Studien mit Blinatumomab wurden bis dato keine Autoimmunphänomene beschrieben (9, 134). Hieraus lässt sich folgern, dass Antikörper des BiTE Formates an sich wahrscheinlich keine Autoimmunphänomene induzieren, wobei Ergebnisse von Studien an größeren Patientenkollektiven abzuwarten sind. Nachdem BiTEs T-Zellen unabhängig von deren Spezifität aktivieren, kann dennoch nicht ausgeschlossen werden, dass z.B. auch auto-reaktive oder entartete TZellen aktiviert werden und proliferieren. Hierdurch könnte die Entstehung von T-Zell 63 Erkrankungen, wie z.B. von Leukämien oder auch von soliden Lymphomen begünstigt werden. Speziell für MCSP-BiTEs gilt es zu beachten, dass MCSP nicht ausschließlich nur von Melanomzellen exprimiert wird, sondern auch von „normalem“ Gewebe wie z.B. Endothelzellen, aktivierten Perizyten, Chondrozyten, Muskelzellen, Keratinozyten und Zellen des Haarfollikels (30). Die therapeutische Gabe von MCSP-BiTEs könnte folglich insbesondere zu Autoimmunreaktionen gegen die genannten Strukturen führen. In den bis dato mit MCSP spezifischen Antikörpern bzw. Fragmenten durchgeführten Studien wurde aber keine Toxizität gegen „normales“ Gewebe nachgewiesen (11, 25, 54, 144, 145, 184, 188). Des Weiteren konnten Erfurt et al. sowohl bei gesunden Spendern als auch bei Melanompatienten MCSP spezifische T-Zellen nachweisen, ohne dass diese klinische Zeichen einer Autoimmuntoxizität zeigten (54). Die Verwendung von MCSP als Zielantigen von BiTEs scheint daher ein erfolgsversprechender Ansatz für die Therapie des malignen Melanoms zu sein. Diese Behauptung wird durch die Ergebnisse der vorliegenden Arbeit untermauert. So konnte gezeigt werden, dass MCSP-BiTEs in Anwesenheit von klonalen CD8+-T-Zellen in vitro eine effektive Lyse von MCSP positiven Melanomzellen vermitteln. Die Lyse ist unabhängig von der Expression wichtiger Faktoren der APM (LMP-2 und -7 sowie TAP-1 und -2). Dies ist insofern von großer klinischer Bedeutung, als dass Kageshita et al. nachweisen konnten, dass maligne Melanome häufig Mutationen in diesem Bereich aufweisen (91). So fanden sie für LMP-2 und -7 in 63% bzw. 45% sowie für TAP-1 und -2 in 52% bzw. 56% der untersuchten Primärläsionen eine heterogene bzw. verminderte Expression. In Metastasen war die Expression der vier genannten Faktoren sogar noch niedriger. Die Lyse der Melanomzellen scheint außerdem unabhängig von deren PD-L1 Expression zu sein. Wie von Blank et al. beschrieben, kann durch die Interaktion von PD-L1 mit seinem Rezeptor PD-1, der unter anderem auch von T-Zellen exprimiert wird, deren Aktivität herunterreguliert werden (15). Möglicherweise beruht auf diesem Mechanismus die Tatsache, dass die Expression von PD-L1 auf Melanomzellen laut Hino et al. einen unabhängigen prognostischen Faktor für das Überleben von Patienten mit malignem Melanom darstellt (79). Unter den neun untersuchten Melanomzelllinien war eine (Na8) deutlich positiv für PD-L1. Frühere Versuche von Blank et al. waren zu dem gleich Ergebnis gekommen (16). Sie wiesen bei zwei von acht Melanomzelllinien (darunter Na8) eine deutliche PD-L1 Expression nach. Für die von ihnen genauso untersuchten Zelllinien Mel ImSi und Me275 konnten sie ebenfalls keine PD-L1 Expression detektieren. Die Expression von PD-L1 auf Na8 hatte jedoch keine verminderte Sensibilität der Zelllinie gegenüber einer BiTE vermittelten T-Zell Lyse zur 64 Folge. Welchen Effekt hierauf die Expression des Apoptose induzierenden Proteins FAS-L hat, konnte nicht evaluiert werden, da keine der Melanomzelllinien FAS-L exprimiert (84). 1996 berichteten Hahne et al., dass Melanomzellen zum Teil FAS-L exprimieren und dadurch möglicherweise der Kontrolle durch das Immunsystems entgehen (72). Chappell et al. untersuchten 1999 mittels PCR und Funktionsassays 45 Melanomzelllinien auf FAS-L (34). Sie konnten in keiner der Zelllinien eine FAS-L Expression nachweisen und widersprachen den Daten von Hahne et al.. Die Tatsache, dass bei keiner der neun untersuchten Melanomzelllinien FAS-L detektiert werden konnte, steht damit im Einklang mit den Ergebnissen von Chappell et al.. Im Gegensatz zu anderen Tumoren, wie z.B. dem kolorektalen Karzinom scheint FAS-L damit für das maligne Melanom keine praktisch, klinische Bedeutung zu haben (196). Des Weiteren war die BiTE induzierte Lyse der Melanomzellen unabhängig von deren IL-10 Sekretion. Drei der untersuchten Melanomzelllinien (Mel Ei, Mel624 und insbesondere Mel1300) sezernierten IL-10 (33%). Dies stimmt mit in der Literatur veröffentlichen Daten weitgehend überein. Krüger-Krasagakes et al. konnten nach 48h Inkubation bei drei von 13 Melanomzelllinien mittels ELISA eine IL-10 Sekretion detektieren (23%) (101). Elias et al. wiesen nach 7d Inkubation bei acht von 17 Melanomzelllinien eine IL10 Sekretion nach (47%) (53). Die IL-10 Sekretion von Mel Ei, Mel624 und Mel1300 hatte jedoch keine verminderte Sensitivität dieser Zelllinien gegenüber einer BiTE induzierten T-Zell Lyse zur Folge. Dies ist insofern von praktischer Bedeutung, als dass Melanomzellen in vivo zu einem hohen Anteil IL-10 produzieren. Sato et al. untersuchten 35 Metastasen maligner Melanome auf deren IL-10 Produktion (169). Nach 24h Inkubation konnten sie bei 30 der 35 Proben eine IL-10 Produktion nachweisen (86%). Aus diesen 30 Proben gelang es ihnen, acht Melanomzelllinien zu etablieren. Nach acht Wochen in Kultur war jedoch nur noch bei einer der acht Zelllinien eine IL-10 Sekretion zu detektieren (13%). Dies spricht dafür, dass Melanomzellen in vivo zu einem hohen Anteil IL-10 produzieren, in vitro ihre IL-10 Produktion jedoch herunterregulieren. Zusammengefasst konnte damit nachgewiesen werden, dass MCSP-BiTEs in Anwesenheit von klonalen CD8+-T-Zellen eine effektive Lyse von MCSP positiven Melanomzellen vermitteln, unabhängig von verschiedenen relevanten immunologischen Faktoren. Die Stärke der Lyse einer Melanomzelllinie war hierbei für alle drei CD8+-T-Zell-Klone gleich. Baeuerle et al. postulierten, dass eine BiTE vermittelte T-Zell-Antwort von jeder zytotoxischen T-Zelle induziert werden kann, unabhängig von deren Spezifität und Defekten der APM der Zielzelle (5). Die 65 vorliegenden Ergebnisse bestätigen diese Aussage und erweitern sie um die Annahme, dass auch verschiedene immunsuppressive Faktoren hierauf keinen Einfluss haben. Des Weiteren geht aus den Ergebnissen des 51Chrom-Release hervor, dass in Ansätzen, in denen bereits eine antigenspezifische Lyse zu beobachten ist, die Zugabe von MCSPBiTE weder eine Verminderung noch eine Steigerung der Zytotoxizität zur Folge hatte (vgl. Me275, Mel624 und Mel1300). Die Stärke der Lyse mit MCSP-BiTE entspricht in diesen Ansätzen derjenigen ohne BiTE bzw. mit Co-BiTE. So wurde bisher zwar der Effekt einer BiTE induzierten T-Zell-Antwort gegen verschiedene Zielzellen untersucht (5). Bis dato liegen jedoch keine Daten von Experimenten bzw. Studien vor, in denen T-Zellen, welche die Zielzellen auch antigenspezifisch erkennen, verwendet wurden. Es bleibt offen, ob die beobachtete Lyse der Melanomzellen durch Interaktion des TCR mit dem MHC-I-Antigenkomplex auf den Melanomzellen, durch eine MCSP-BiTE induzierte immunologische Synapse oder durch beide Mechanismen gemeinsam vermittelt wird (17). Anzumerken ist, dass bei dem beschriebenen Experiment vorstimulierte und hochaktive T-Zellen verwendet wurden wie sie praktisch nur in vitro vorkommen. So wäre es durchaus möglich, dass in vivo CD8+-T-Zellen, welche eine antigenspezifische Lyse von Melanomzellen vermitteln, durch Zugabe von BiTEs eine noch stärkere antitumorale Aktivität entwickeln. In diesem Zusammenhang sollte außerdem geklärt werden, welchen Effekt die Zugabe von Co-BiTE in Ansätzen hat, in denen die Melanomzellen antigenspezifisch erkannt werden. Aus der Literatur ist bekannt, dass T-Zellen nur in Anwesenheit des entsprechenden Zielantigens von BiTEs aktiviert werden (22). BiTEs binden aber auch in Abwesenheit der Zielzellen an T-Zellen, ohne diese jedoch zu aktiveren (22, 45). Vor dem Hintergrund dieser Ergebnisse sollte daher untersucht werden, ob T-Zellen, die eine antigenspezifischen Lyse von Melanomzellen vermitteln, durch die Bindung des CD3 Armes des Co-BiTEs in ihrer Funktion beeinträchtigt werden. So wäre es theoretisch möglich, dass durch die Blockade von CD3 mittels Co-BiTE die Interaktion des TCR mit dem Ag-MHC-I-Komplex der Zielzelle gestört wird. Auf der anderen Seite könnten Co-BiTEs auch als co-stimulatorisches Signal fungieren und die T-Zell Immunantwort verstärken. Die Behauptung, dass BiTEs in Abwesenheit der Zielzelle an T-Zellen binden ohne diese jedoch zu aktivieren wurde bis dato, soweit bekannt, nur anhand unspezifischer T-Zellen untersucht (6, 22). Die im Rahmen dieser Arbeit gewonnenen Daten deuten darauf hin, dass keine der beiden Hypothesen zutrifft. So war in Ansätzen, in denen die Melanomzellen bereits antigenspezifisch lysiert wurden, durch Zugabe von Co-BiTE weder eine Reduktion noch eine Steigerung der 66 Zytotoxizität zu beobachten. In Ansätzen, in denen keine antigenspezifische Lyse auftrat, wurde mit Co-BiTE ebenfalls keine oder nur eine minimale, unspezifische, Zelllyse gemessen. Die Stärke der Lyse mit Co-BiTE entsprach stets derjenigen ohne BiTE. Dies lässt die Schlussfolgerung zu, dass die alleinige Bindung des CD3-Armes des Co-BiTEs an klonale CD8+-T-Zellen, diese nicht in ihrer zytotoxischen Aktivität beeinflusst - unabhängig davon, ob sie die Zielzellen antigenspezifisch erkennen oder nicht. Die vorliegenden Ergebnisse stimmen damit mit den von Torisu-Itakura et al. publizierten Daten überein, wonach kein signifikanter Unterschied in der Lyse von Melanomzellen ohne BiTE verglichen mit Co-BiTE unter Verwendung von PBMCs als Effektorzellen besteht und erweitern diese Behauptung um die Annahme, dass entsprechendes auch für einen antigenspezifischen Kontext gilt (198). Die Autoren weisen außerdem darauf hin, dass eine geringe durch allogene T-Zell vermittelte Lyse der Melanomzellen bereits ohne BiTEs auftritt. Diese Lyse war auch im Rahmen dieser Arbeit zu beobachten. Wie bereits beschrieben, vermitteln MCSP-BiTEs in Anwesenheit von CD8+-T-Zellen eine effektive Lyse von MCSP positiven Melanomzellen. Diese Lyse ist unabhängig von verschiedenen relevanten immunologischen Faktoren. Aus der Literatur ist jedoch bekannt, dass durch immuntherapeutische Maßnahmen selbst Tumor-Immune-EscapeMechanismen entstehen bzw. begünstigt werden können (182). Riker et al. untersuchten Biopsien von Melanompatienten, die eine gp100 Peptid-Vakzination erhalten hatten, auf deren gp100 Expression und verglichen die Daten mit Biopsien von Patienten, die keine gp100 Peptid-Vakzination erhalten hatten (159). Sie konnten zeigen, dass die Biopsien der immunisierten Gruppe zu einem geringeren Prozentsatz gp100 exprimieren als die Biopsien der Kontrollgruppe (18% vs. 29%). Die Daten deuten laut den Autoren darauf hin, dass Tumore durch den Verlust des entsprechenden Zielantigens einer spezifischen Immunantwort entgehen können. Yee et al. beobachteten bei drei von fünf Patienten mit malignem Melanom einen selektiven Verlust des Zielantigens nach adoptivem TZell-Transfer (218). 1999 berichteten Davis et al. erstmals von einem Patienten mit einem ursprünglich CD20+ Non-Hodgkin-Lymphom, das nach zwei Therapiezyklen mit Rituximab (anti-CD20-mAb) kein CD20 mehr exprimierte (39). Die Autoren führen weiter aus, dass dieses Phänomen durch zwei mögliche Mechanismen erklärt werden kann: Entweder durch den Verlust der CD20 Expression von primär CD20+-Zellen oder durch die Proliferation eines CD20--Zellklones innerhalb des Tumors. Weitere Studien bestätigen den Verlust der CD20 Expression als möglichen Tumor-Immune- 67 Escape-Mechanismus nach Behandlung mit Rituximab (49, 94, 122). Folglich stellt sich die Frage, ob nicht durch eine MCSP-BiTE induzierte T-Zell-Antwort gegen Melanomzellen selbst neue Immune-Escape-Mechanismen ausgelöst bzw. Melanomzellen mit präexistierenden Mutationen ausselektiert werden können. Hierfür wurden die drei Melanomzelllinien Mel ImSi, A2058 und Mel624 mit klonalen CD8+-T-Zellen und MCSP-BiTE inkubiert. Die überlebenden Zellen wurden anschließend erneut charakterisiert und ihre Sensitivität gegenüber eines T-Zell mediierten Kills bestimmt. Um unspezifische Effekte ausschließend zu können, wurde jeweils eine entsprechende Kontrolle mitgeführt. Für die beiden Melanomzelllinien Mel ImSi und A2058 konnte nach Inkubation mit klonalen T-Zellen und MCSP-BiTE bzw. Co-BiTE kein Unterschied verglichen mit den ursprünglichen Zelllinien nachgewiesen werden. Aus den Daten des 51 Chrom-Release geht außerdem hervor, dass keine Differenz in Bezug auf die Höhe des T-Zell mediierten Kills zwischen den mit MCSPBiTE und den mit Co-BiTE inkubierten Zellen besteht. Eine Induktion bzw. Selektion von Resistenzen scheint damit nicht stattgefunden zu haben. Ein anderes Bild zeigt sich für die mit klonalen T-Zellen und MCSP-BiTE inkubierte Melanomzelllinie Mel624. Für sie konnte mittels Durchflusszytometrie eine verminderte MCSP-Expression verglichen mit der Kontrolle nachgewiesen werden. Die für MCSP gemessenen Werte liegen hierbei, verglichen mit denjenigen der Kontrollzelllinie, über einen Beobachtungszeitraum von mehr als 80 Tagen stabil bei etwa 15-20%. Die Expression aller anderen mittels FACS untersuchten Proteine entsprach mit Ausnahme von MelanA (siehe unten) derjenigen der Kontrolle sowie der ursprünglichen Melanomzelllinie Mel624. Eine Veränderung der Genexpression von APM Komponenten (TAP-1 und -2 sowie LMP-2 und -7) wurde nicht detektiert. Hingegen konnte für keine der beiden Zelllinien eine IL-10 Sekretion nachgewiesen werden. Die Veränderung der IL-10 Sekretion muss daher als unspezifisches Zellkultur bzw. in vitro Phänomen gewertet werden und stimmt mit den weiter oben beschriebenen Ergebnissen von Sato et al. überein, wonach bei Melanomzellen in Kultur eine Veränderung der IL-10 Sekretion nicht ungewöhnlich ist (169). Die Daten des 51 Chrom-Release zeigen, dass die verminderte MCSP-Expression mit einer geringeren Sensitivität der Zelllinie gegenüber eines MCSP-BiTE induzierten Kills durch BMLF1 spezifische T-Zellen einherging. Diese Beobachtung lässt darauf schließen, dass es durch die Herunterregulation von MCSP zur Selektion einer in der Literatur bis dato so nicht beschriebenen, Antigen-lossVariante gekommen ist. Das steht in Analogie zu dem weiter oben beschriebenen Verlust der CD20 Expression nach Behandlung mit einem anti-CD20-mAb 68 (Rituximab). Eine verminderte Sensitivität gegenüber eines antigenspezifischen Kills durch gp100 spezifische klonale CD8+-T-Zellen wurde hingegen nicht beobachtet. Im Gegensatz dazu war die antigenspezifische Lyse durch Melan-A spezifischen T-Zellen, verglichen mit der Kontrolle, auf etwa 80% erniedrigt. Dieses Phänomen ist eventuell auf eine erniedrigte Melan-A Expression zurückzuführen. So fiel bei der Analyse der Daten auf, dass die mit MCSP-BiTEs inkubierten Zellen weniger Melan-A exprimierten als die Kontrollzelllinie. Ein möglicher Erklärungsansatz hierfür ist, dass Melanomzellen, die eine starke MCSP Expression aufweisen, gleichzeitig auch eine hohe Melan-A Expression haben (MCSPhighMelan-Ahigh), wohingegen Melanomzellen mit einer geringen MCSP Expression nur schwach Melan-A exprimieren (MCSPlowMelanAlow). Durch die Inkubation der Melanomzellen mit klonalen T-Zellen und MCSP-BiTE kann es daher gleichzeitig zu einer indirekten Selektion von Zellen mit niedriger MelanA Expression gekommen sein. Gegen diese Hypothese spricht, dass nach Inkubation von Mel624 mit Melan-A spezifischen T-Zellen keine verminderte MCSP Expression zu beobachten war (siehe auch unten). In ihrer Gesamtheit deuten die gewonnenen Daten darauf hin, dass eine MCSP-BiTE induzierte T-Zell Antwort zur Entstehung eines Tumor-Immune-Escape-Mechanismus führen kann. Dieser scheint durch die Modulation der MCSP Expression auf den Melanomzellen vermittelt zu werden. Die entscheidende Bedeutung des TAAs für eine BiTE induzierte T-Zell Antwort ist in der Literatur gut beschrieben. So erbrachten Torisu-Itakura et al. den Nachweis, dass MCSP-BiTEs keine Immunantwort gegen MCSP negative Melanomzellen induzieren (198). Offner et al. konnten für das EpCAM-BiTE zeigen, dass die Zelllyse in Anwesenheit von denjenigen mAbs, aus denen das BiTE konstruiert worden war, zum Teil geblockt wird (143). Löffler et al. untersuchten den Effekt von mAbs gegen CD3 und CD19 auf eine durch Blinatumomab (CD19-BiTE) induzierte Immunantwort. Sie stellten fest, dass die Lyse in Anwesenheit von anti-CD3 bzw. -CD19 Antikörper sogar komplett geblockt werden konnte (114). In der Literatur liegen bis dato jedoch keine Daten bezüglich einer Veränderung der MCSP Expression auf Melanomzellen nach einer Immunantwort mit MCSP als Zielantigen vor. Ferrone et al. inkubierten humane Melanomzellen mit MCSP spezifischen mAbs sowie anti-Maus Antikörpern (58). Sie konnten in der Folge keine Veränderung der MCSP Expression auf den Melanomzellen feststellen. Zu beachten ist jedoch, dass in dem beschriebenen Experiment im Gegensatz zu dieser Arbeit keine Effektorzellen zugegeben worden waren. Die Ergebnisse von Ferrone et al. deuten vielmehr darauf hin, dass die alleinige Bindung von monoklonalen anti-MCSP Antikörpern keine Veränderung der MCSP Expression 69 der Melanomzellen zur Folge hat. Daten von Experimenten mit anti-MCSP Antikörpern und Effektorzellen wurden bisher nicht publiziert. Soweit bekannt, ist dies daher das erste Mal, dass demonstriert werden konnte, dass es durch eine BiTE induzierte Immunantwort zu einer Herunterregulation des entsprechenden TAAs und damit zu einer verminderten Sensitivität der Zielzellen gegenüber einer erneuten BiTE induzierten Immunantwort kommen kann. Dies ist in Hinblick auf therapeutische Maßnahmen mit MCSP-BiTE von großer klinischer Bedeutung und würde insbesondere für die Therapie von Melanomrezidiven gelten, die zuvor schon mit MCSP-BiTE behandelt worden waren. Möglicherweise ließe sich sowohl die Entstehung eines derartigen Immune-Escapes als auch eventuell die Häufigkeit von Rezidiven durch eine Verbesserung des Killings positiv beeinflussen. Neben einer Erhöhung des E:TVerhältnis, z.B. durch Induktion der T-Zell Proliferation mit Hilfe von ILs, käme insbesondere eine Steigerung der BiTE-Konzentration in Frage. Dies könnte durch eine Erhöhung der Anzahl der therapeutischen Gaben bzw. eine kontinuierliche Gabe erreicht werden. Nachdem BiTEs im Unterschied zu mAbs nur eine Halbwertszeit von wenigen Stunden aufweisen, wurde in den bisher publizierten Studien mit Blinatumomab ohnehin eine kontinuierliche intravenöse Gabe gewählt (6, 9, 197). Diese ermöglicht wie Baeuerle et al. anmerken ein exzellentes Drug monitoring, wird wahrscheinlich jedoch auch - falls BiTEs in Zukunft kommerziell zu erwerben sein werden - mit erhöhten Kosten einhergehen (6). Vor dem Hintergrund, dass zwar in Mel624, nicht jedoch in Mel ImSi noch in A2058 eine Herunterregulation der MCSP Expression induziert werden konnte, sollte geklärt werden, ob Mel624 im Allgemeinen besonders suszeptibel für die Entstehung von Tumor-Immune-Escape-Mechanismus ist. Wie bereits beschrieben beobachteten Yee et al. bei Melanompatienten einen selektiven Verlust des Zielantigens nach adoptivem T-Zell-Transfer mit gp100 bzw. Melan-A spezifischen CD8+-T-Zellen (218). Es stellte sich daher die Frage, ob in Mel624 durch eine antigenspezifische Lyse ein entsprechender Tumor-Immune-EscapeMechanismus ausgelöst werden kann. Hierfür wurden drei Ansätze gewählt: mit gp100Klon, mit Melan-A-Klon oder mit BMLF1-Klon (Kontrolle). BiTE wurde in keinem der Ansätze zugegeben. Die überlebenden Melanomzellen wurden im Anschluss erneut charakterisiert und ihre Sensitivität gegenüber eines T-Zell mediierten Kills im 51ChromRelease ermittelt. Für die mittels FACS bestimmten Proteine zeigte sich kein Unterschied der drei Zelllinien untereinander noch mit der ursprünglichen Zelllinie Mel624. Die Genexpression von TAP-1 und -2 sowie LMP-2 und -7 blieb ebenfalls auf gleichem Niveau. Die IL-10 Sekretion aller drei Melanomzelllinien war hingegen 70 niedriger als die von Mel624. Wie für die Ansätze mit BiTE muss diese Veränderung jedoch als unspezifisch gewertet werden (vgl. Sato et al. (169)). Im Zytotoxizitätsassay zeigte sich keine verminderte Sensitivität der mit gp100 bzw. Melan-A spezifischen TZellen inkubierten Melanomzellen verglichen mit der Kontrolle. Folglich muss davon ausgegangen, dass in den Zelllinien kein Tumor-Immune-Escape-Mechanismus induziert wurde. Eine besondere Suszeptibilität von Mel624 zur Bildung von Resistenzmechanismen scheint damit nicht gegeben zu sein. Diese kann jedoch trotz des sorgfältig gewählten Versuchsaufbaus explizit für MCSP nicht sicher ausgeschlossen werden. Hierfür wäre ein weiterer Versuchsansatz unter Verwendung von MCSP spezifischen klonalen CD8+-T-Zellen nötig. Eine solcher T-Zell-Klon stand im Rahmen der vorliegenden Arbeit leider nicht zur Verfügung. Die beschriebene Vorgehensweise würde es ermöglichen gezielt zu unterscheiden, ob die beobachtete Herunterregulation von MCSP einen BiTE spezifischen Effekt darstellt oder auch durch eine antigenspezifische Lyse induziert werden kann. In den letzten Jahren wurden BiTE-Antikörper für verschiedene Zielantigene konstruiert. Ihnen allen ist gemeinsam, dass sie mit einem Arm spezifisch an CD3 und somit an T-Zellen binden. Baeuerle et al. legen dar, dass durch BiTE-Antikörper insbesondere zytotoxische T-Zellen (CD8+-T-Zellen) rekrutiert werden und in der Zielzelle Apoptose auslösen (5). Die Annahme, dass zytotoxische T-Zellen eine effektive BiTE induzierte Immunantwort vermitteln, steht im Einklang mit den im Rahmen dieser Arbeit gewonnenen Ergebnissen. Daneben ist in der Literatur beschrieben, dass BiTEs in der Lage sind auch weitere CD3+-T-Zell-Subpopulationen zu aktivieren (6). 1997 wiesen Kufer et al. nach, dass sowohl CD8+-T-Zellen als auch CD4+-T-Zellen in Anwesenheit von EpCAM-BiTEs die EpCAM positive Zelllinie Kato lysieren (104, 118). Sowohl Hoffmann et al. als auch Dreier et al. konnten zeigen, dass CD4+-T-Zellen eine Blinatumomab induzierte Immunantwort von CD19+-Tumorzellen bedingen (45, 82). Des Weiteren wurde in klinischen Studien mit Blinatumomab bei den behandelten Patienten nicht nur ein Anstieg der CD8+-T-Zellen beobachtet, sondern auch der CD4+-T-Zellen (9, 197). Topp et al. merken jedoch an, dass unklar bleibt, ob und inwieweit CD4+-T-Zellen zum therapeutischen Effekt von Blinatumomab beitragen (197). Die genaue Bedeutung von weiteren T-Zell-Subpopulationen wie z.B. Tregs auf eine BiTE vermittelte Immunantwort wird derzeit laut Baeuerle et al. noch untersucht (5). Im Rahmen des AACR 2012 präsentierten Münz et al. ihre Forschungsergebnisse wonach Tregs nach Zugabe von MT110 (EpCAM-BiTE) eine Immunantwort gegen 71 EpCAM positive Zielzellen vermitteln können (131). Die Ergebnissen der vorliegenden Arbeit sind im Einklang mit diesem Befund und deuten ebenfalls darauf hin, dass neben zytotoxischen T-Zellen und CD4+-T-Zellen auch weitere CD3+-T-Zell- Subpopulationen (CD4+CD25+ und DNs) eine BiTE induzierte Immunantwort vermitteln können. Soweit bekannt, ist dies das erste Mal, dass demonstriert werden konnte, dass DNs in der Lage sind, eine BiTE induzierte Zellzytotoxizität zu vermitteln. Wie in der Einleitung beschrieben, kommt den Tregs (CD4+CD25+-T-Zellen, ehemals Suppressor-T-Zellen) eine wichtige modulatorische Rolle innerhalb des Immunsystems zu (132). Tregs zeichnen sich dadurch aus, dass sie, indem sie andere Zellen des Immunsystems in ihrer Funktion hemmen, überschießende Immunreaktionen verhindern (166). Werden sie in ihrer Funktionsweise gestört, so können Autoimmunkrankheiten und inflammatorische Erkrankungen auftreten (166). Auf der anderen Seite wurde beobachtet, dass sowohl solide Tumore als auch maligne hämatologische Erkrankungen mit einer Erhöhung der Tregs einhergehen (12). Im peripheren Blut gesunder Spendern beträgt der Anteil Regulatorischer T-Zellen etwa fünf bis zehn Prozent der PBMCs (13). Javia et al. fanden in einer Studie an Patienten mit malignem Melanom, Stadium IV, heraus, dass dieser Anteil bei den Betroffenen auf 16,6% erhöht war (88). Viguier et al. ermittelten bei Patienten mit malignem Melanom, Stadium III, in Lymphknoten mit Metastasen und ohne Metastasen den Anteil von Regulatorischen T-Zellen an allen CD4+-T-Zellen (206). Sie wiesen nach, dass dieser in metastatischen Lymphknoten verglichen mit tumorfreien Lymphknoten etwa verdoppelt ist (11,1% vs. 6,2%). Auf welchen molekularen Mechanismen der Anstieg der Tregs beruht, ist derzeit nicht abschließend geklärt (12). Unklar ist auch, durch welche Mechanismen genau CD4+CD25+-T-Zellen ihre hemmende Wirkung auf das Immunsystem von Patienten mit malignem Melanom entfalten. Da in bisherigen Studien diesbezüglich keine humoralen Faktoren identifiziert werden konnten, postulierten Javia et al., dass der suppressive Effekt wahrscheinlich auf direktem ZellZellkontakt beruht (88). Die von Viguier et al. mittels Transwell-Assays gewonnenen Daten unterstützen diese Vermutung (206). Der Anstieg der Tregs bei Patienten mit malignem Melanom wirft folglich die Frage auf, inwieweit diese für eine BiTE induzierte Zelllyse rekrutiert werden können. Herrmann et al. untersuchten in vitro den Effekt des EpCAM-BiTEs auf das Wachstum von sogenannten Krebsstammzellen von Patienten mit kolorektalem Karzinom (74). Als Effektorzellen verwendeten sie entweder PBMCs oder aus PBMCs isolierte CD8+-T-Zellen. Aus der Tatsache, dass sie nach 20h keinen Unterschied in der Wachstumshemmung zwischen den beiden Effektorzellpopulationen 72 messen konnten, schlussfolgerten sie, dass CD3+CD8--T-Zellen wie z.B. Tregs die Lyse von Krebsstammzellen nicht nachweisbar beeinflussen. Diese Aussage muss im Kontext der von Münz et al. sowie der im Rahmen dieser Arbeit gewonnenen Ergebnisse kritisch interpretiert werden (131). So konnte nachgewiesen werden, dass CD4+CD25+-T-Zellen ebenfalls, wenn auch in geringerem Ausmaß als CD8+-T-Zellen, eine BiTE induzierte Lyse gegen Melanomzellen vermitteln können. Inwieweit CD4+CD25+-T-Zellen in vivo letztendlich genau zu einer BiTE induzierten Immunantwort beitragen bleibt abzuwarten. Es ist jedoch nicht auszuschließen, dass CD8+-T-Zellen in Synergie mit weiteren CD3+-T-Zellsubpopulationen wie z.B. CD4+CD25+-T-Zellen agieren. An diesem Prozess sind möglicherweise auch DNs (CD4-CD8-TCRαß+-T-Zellen) beteiligt. Hierbei handelt es sich um eine T-ZellSubpopulation, deren genaue Bedeutung und Funktion nicht abschließend geklärt sind. Bisher veröffentlichte Daten deuten darauf hin, dass sie wahrscheinlich an der Modulation von inflammatorischen Prozessen beteiligt sind (37). Völkl et al. hatten zeigen können, dass DNs in vitro in der Lage sind, Melanomzellen antigenspezifisch zu lysieren (210). Die Daten der vorliegenden Arbeiten deuten darauf hin, dass DNs ebenfalls eine BiTE induzierte Lyse von Tumorzellen bedingen können - wenn auch in geringeren Umfang als CD8+-T-Zellen. Ob DNs in vivo maßgeblich zu einer BiTE induzierten Immunantwort beitragen, scheint hingegen eher unwahrscheinlich zu sein. Diese Einschätzung beruht vor allem auf der geringen Anzahl von DNs im menschlichen Organismus. Kusunoki et al. wiesen nach, dass der Anteil von DNs im peripheren Blut gesunder Spender weniger als 2% der TCRαß+-T-Zellen ausmacht (106). Studien legen jedoch dar, dass eine BiTE induzierte Immunantwort abhängig vom E:T-Verhältnis ist (45, 82, 198). Zusammengefasst lässt sich daher festhalten, dass DNs zwar prinzipiell eine BiTE induzierte Immunantwort vermitteln können, diese in vivo wahrscheinlich jedoch auf dem Effekt anderer T-Zell-Subpopulationen beruht. Weitere Analysen der Daten des Zytotoxizitätsassays ergaben, dass der zytotoxische Effekt von CD4+-T-Zellen gegen die Melanomzelllinie Na8 stärker war als derjenige von CD8+-T-Zellen (20% vs. 13%). Dieser Befund erscheint vor dem Hintergrund, dass in der Literatur hauptsächlich CD8+-T-Zellen als Effektoren einer BiTE induzierten TZell-Antwort genannt werden, zunächst ungewöhnlich (5). Jedoch konnten wie bereits beschrieben, Kufer et al., Hoffmann et al. und Dreier et al. nachweisen, dass auch CD4+-T-Zellen durch BiTEs aktiviert werden und eine effektive Tumorlyse vermitteln (45, 82, 104, 118). Kufer et al. weisen in ihrer Publikation aus dem Jahre 1997 darauf hin, dass CD4+-T-Zellen und CD8+-T-Zellen hierbei jedoch einer unterschiedlichen 73 zeitlichen Kinetik unterliegen (104). So detektierten sie mittels 51 Chrom-Release für CD8+-T-Zellen bereits nach 4h eine effektive Lyse der Zielzellen, wohingegen für CD4+-T-Zellen eine Inkubationszeit von 20h nötig war. Die Ergebnisse von Dreier et al. bestätigen die zeitliche Kinetik einer BiTE vermittelten Immunantwort (4h für CD8+-T-Zellen vs. 16h für CD4+-T-Zellen) (45). Gemäß dieser Kinetik muss folglich davon ausgegangen werden, dass die im Rahmen dieser Arbeit gewählte Inkubationszeit von 19h es auch CD4+-T-Zellen ermöglicht ihre zytotoxische Wirkung zu entfalten. Aus der Veröffentlichung von Dreier et al. ist nicht ersichtlich ob nach 16h CD8+-T-Zellen oder CD4+-T-Zellen eine stärkere Lyse vermitteln (45). Die Autoren führen an, dass für CD4+-T-Zellen im 16h Assay verglichen mit dem 4h Assay ein starker Anstieg der zytotoxischen Aktivität zu beobachten war. Aus den Ergebnissen von Kufer et al. ist ersichtlich, dass CD8+-T-Zellen selbst nach 20h Inkubationszeit eine leicht höhere BiTE induzierte Lyse vermitteln als CD4+-T-Zellen (104, 118). Hierbei muss jedoch beachtet werden, dass Kufer et al. die Zytotoxizität von CD4+-T-Zellen und CD8+-T-Zellen anhand der humanen Magenkarzinomzelllinie Kato bestimmten und nicht wie in der vorliegenden Arbeit anhand einer Melanomzelllinie (Na8). Dementsprechend induzierten sie die T-Zell-Antwort nicht mittels MCSP-BiTE sondern mit einem EpCAM-BiTE. Es ist daher denkbar, dass Melanomzellen aufgrund verschiedener, während der Tumergenese entstandener Mutationen und Veränderungen der intrazellulären Signalkaskade (vgl. auch 2.2.4) möglicherweise sensibler gegenüber einer BiTE induzierten Immunantwort durch CD4+-T-Zellen sind als anderen Tumorzelllinien. In der Literatur wurden bisher nur bedingt Daten in Bezug auf die Stärke einer BiTE induzierten Lyse von Melanomzellen durch verschiedene T-ZellPopulationen veröffentlicht. Torisu-Itakura et al. bestimmten mittels Durchflusszytometrie die MCSP-BiTE induzierte Lyse der Melanomzelllinie M27-HI (198). Als Effektorzellen verwendeten sie PBMCs von Patienten mit malignem Melanom. Sie wiesen nach, dass PBMCs, die einen höheren Anteil als den Median an CD8+-T-Zellen (33,5%) aufwiesen, keine signifikant höhere Lyse der Zielzellen vermittelten als PBMCs, mit einem geringeren Anteil als den Median an CD8+-T-Zellen. Die Autoren zogen daraus die Schlussfolgerung, dass dieser Befund möglicherweise dadurch zu erklären ist, dass MCSP-BiTEs prinzipiell jede T-Zelle für die Lyse von Melanomzellen rekrutieren können. Diese Hypothese steht damit im Einklang mit den in der vorliegenden Arbeit gewonnenen Daten und unterstreicht das Potential von BiTEs, nicht nur CD8+-T-Zellen für die Tumorantwort zu rekrutieren sondern auch 74 weitere CD3+-T-Zell-Subpopulationen. Inwieweit welche T-Zell-Subpopulation in vivo letztendlich zu einer BiTE induzierte Immunantwort beiträgt bleibt abzuwarten. Die Therapie des malignen Melanoms stellt trotz der medizinischen Fortschritte der letzten Jahre eine Herausforderung an die behandelnden Ärzte dar. Ein neuartiges und erfolgsversprechendes Therapeutikum für die Behandlung der Patienten stellen die in dieser Arbeit untersuchten BiTEs dar. Wie gezeigt werden konnte, ermöglichen sie TZellen eine effektive Lyse der Zielzellen zu vermitteln. Dieser Ansatz hat sich für andere Tumorentitäten wie z.B. B-Zell Non-Hodgkin Lymphome und die ALL als vielversprechend erwiesen. Die Ergebnisse der vorliegenden Arbeit deuten darauf hin, dass BiTEs möglicherweise auch für die Therapie des malignen Melanoms geeignet sind. Diese Einschätzung beruht insbesondere auf der Tatsache, dass eine BiTE induzierte Immunantwort unabhängig von verschiedenen immunologisch relevanten Faktoren und Mutationen ist. Es konnte jedoch auch gezeigt werden, dass Tumore durch eine erniedrigte Expression des entsprechenden Zielantigens nach einer derartigen Immunantwort einer BiTE induzierten Lyse entgehen können. Inwieweit diese präklinischen in vitro Daten auf ein hochkomplexes in vivo System wie den menschlichen Organismus zutreffen, bleibt abzuwarten. 75 6 Literaturverzeichnis 1. Albini A, Sporn MB. The tumour microenvironment as a target for chemoprevention. Nat Rev Cancer. 2007 Feb; 7(2): 139-47. 2. Andriote JM. A glass half full: cancer risk for people living with HIV. Beta. 2010 Summer-Fall; 22(4): 30-41. 3. Attia P, Phan GQ, Maker AV, Robinson MR, Quezado MM, Yang JC, Sherry RM, Topalian SL, Kammula US, Royal RE, Restifo NP, Haworth LR, Levy C, Mavroukakis SA, Nichol G, Yellin MJ, Rosenberg SA. Autoimmunity correlates with tumor regression in patients with metastatic melanoma treated with anti-cytotoxic T-lymphocyte antigen-4. J Clin Oncol. 2005 Sep 1; 23(25): 6043-53. 4. Augustin M, Blome C, Rustenbach SJ, Reusch M, Radtke M. Routine skin cancer screening in Germany: First data on the impact on health care in dermatology. J Dtsch Dermatol Ges. 2010 Sep; 8(9): 674-80. 5. Baeuerle PA, Kufer P, Bargou R. BiTE: Teaching antibodies to engage T-cells for cancer therapy. Curr Opin Mol Ther. 2009 Feb; 11(1): 22-30. 6. Baeuerle PA, Reinhardt C. Bispecific T-cell engaging antibodies for cancer therapy. Cancer Res. 2009 Jun 15; 69(12): 4941-4. 7. Balch CM, Buzaid AC, Soong SJ, Atkins MB, Cascinelli N, Coit DG, Fleming ID, Gershenwald JE, Houghton A, Jr., Kirkwood JM, McMasters KM, Mihm MF, Morton DL, Reintgen DS, Ross MI, Sober A, Thompson JA, Thompson JF. Final version of the American Joint Committee on Cancer staging system for cutaneous melanoma. J Clin Oncol. 2001 Aug 15; 19(16): 3635-48. 8. Balch CM, Gershenwald JE, Soong SJ, Thompson JF, Atkins MB, Byrd DR, Buzaid AC, Cochran AJ, Coit DG, Ding S, Eggermont AM, Flaherty KT, Gimotty PA, Kirkwood JM, McMasters KM, Mihm MC, Jr., Morton DL, Ross MI, Sober AJ, Sondak VK. Final version of 2009 AJCC melanoma staging and classification. J Clin Oncol. 2009 Dec 20; 27(36): 6199-206. 9. Bargou R, Leo E, Zugmaier G, Klinger M, Goebeler M, Knop S, Noppeney R, Viardot A, Hess G, Schuler M, Einsele H, Brandl C, Wolf A, Kirchinger P, Klappers P, Schmidt M, Riethmuller G, Reinhardt C, Baeuerle PA, Kufer P. Tumor regression in cancer patients by very low doses of a T cell-engaging antibody. Science. 2008 Aug 15; 321(5891): 974-7. 10. Bedrosian I, Mick R, Xu S, Nisenbaum H, Faries M, Zhang P, Cohen PA, Koski G, Czerniecki BJ. Intranodal administration of peptide-pulsed mature dendritic cell vaccines results in superior CD8+ T-cell function in melanoma patients. J Clin Oncol. 2003 Oct 15; 21(20): 382635. 11. Bender H, Grapow M, Schomburg A, Reinhold U, Biersack HJ. Effects of diagnostic application of monoclonal antibody on survival in melanoma patients. Hybridoma. 1997 Feb; 16(1): 65-8. 76 12. 11. Beyer M, Schultze JL. Regulatory T cells in cancer. Blood. 2006 Aug 1; 108(3): 804- 13. Bignone PA, Banham AH. FOXP3+ regulatory T cells as biomarkers in human malignancies. Expert Opin Biol Ther. 2008 Dec; 8(12): 1897-920. 14. Bins A, Mallo H, Sein J, van den Bogaard C, Nooijen W, Vyth-Dreese F, Nuijen B, de Gast GC, Haanen JB. Phase I clinical study with multiple peptide vaccines in combination with tetanus toxoid and GM-CSF in advanced-stage HLA-A*0201-positive melanoma patients. J Immunother. 2007 Feb-Mar; 30(2): 234-9. 15. Blank C, Gajewski TF, Mackensen A. Interaction of PD-L1 on tumor cells with PD-1 on tumor-specific T cells as a mechanism of immune evasion: implications for tumor immunotherapy. Cancer immunology, immunotherapy : CII. 2005 Apr; 54(4): 307-14. 16. Blank C, Kuball J, Völkl S, Wiendl H, Becker B, Walter B, Majdic O, Gajewski TF, Theobald M, Andreesen R, Mackensen A. Blockade of PD-L1 (B7-H1) augments human tumor-specific T cell responses in vitro. International journal of cancer. 2006 Jul 15; 119(2): 317-27. 17. Bluemel C, Hausmann S, Fluhr P, Sriskandarajah M, Stallcup WB, Baeuerle PA, Kufer P. Epitope distance to the target cell membrane and antigen size determine the potency of T cellmediated lysis by BiTE antibodies specific for a large melanoma surface antigen. Cancer Immunol Immunother. 2010 Aug; 59(8): 1197-209. 18. Boshoff C, Weiss R. AIDS-related malignancies. Nat Rev Cancer. 2002 May; 2(5): 373-82. 19. Braun-Falco O, Plewig G, Wolff HH, Burgdorf WHC, Landthaler M. Dermatologie und Venerologie. 5. Auflage. Heidelberg. Springer Verlag; 2005. 20. Breitbart EW. Hautkrebs. Heft 22. Berlin. Gesundheitsberichterstattung des Bundes, Robert Koch-Institut (RKI); 2004. 21. Breslow A. Thickness, cross-sectional areas and depth of invasion in the prognosis of cutaneous melanoma. Ann Surg. 1970 Nov; 172(5): 902-8. 22. Brischwein K, Parr L, Pflanz S, Volkland J, Lumsden J, Klinger M, Locher M, Hammond SA, Kiener P, Kufer P, Schlereth B, Baeuerle PA. Strictly target cell-dependent activation of T cells by bispecific single-chain antibody constructs of the BiTE class. J Immunother. 2007 Nov-Dec; 30(8): 798-807. 23. Brischwein K, Schlereth B, Guller B, Steiger C, Wolf A, Lutterbuese R, Offner S, Locher M, Urbig T, Raum T, Kleindienst P, Wimberger P, Kimmig R, Fichtner I, Kufer P, Hofmeister R, da Silva AJ, Baeuerle PA. MT110: a novel bispecific single-chain antibody construct with high efficacy in eradicating established tumors. Mol Immunol. 2006 Mar; 43(8): 1129-43. 24. Bumol TF, Wang QC, Reisfeld RA, Kaplan NO. Monoclonal antibody and an antibody-toxin conjugate to a cell surface proteoglycan of melanoma cells suppress in vivo tumor growth. Proc Natl Acad Sci U S A. 1983 Jan; 80(2): 529-33. 77 25. Buraggi GL, Callegaro L, Mariani G, Turrin A, Cascinelli N, Attili A, Bombardieri E, Terno G, Plassio G, Dovis M, et al. Imaging with 131I-labeled monoclonal antibodies to a high-molecular-weight melanoma-associated antigen in patients with melanoma: efficacy of whole immunoglobulin and its F(ab')2 fragments. Cancer research. 1985 Jul; 45(7): 3378-87. 26. Burg MA, Grako KA, Stallcup WB. Expression of the NG2 proteoglycan enhances the growth and metastatic properties of melanoma cells. J Cell Physiol. 1998 Nov; 177(2): 299-312. 27. 1-27. Burnet FM. The concept of immunological surveillance. Prog Exp Tumor Res. 1970; 13: 28. Burns WR, Zhao Y, Frankel TL, Hinrichs CS, Zheng Z, Xu H, Feldman SA, Ferrone S, Rosenberg SA, Morgan RA. A high molecular weight melanoma-associated antigenspecific chimeric antigen receptor redirects lymphocytes to target human melanomas. Cancer research. 2010 Apr 15; 70(8): 3027-33. 29. Campoli M, Chang CC, Kageshita T, Wang X, McCarthy JB, Ferrone S. Human high molecular weight-melanoma-associated antigen (HMW-MAA): a melanoma cell surface chondroitin sulfate proteoglycan (MSCP) with biological and clinical significance. Crit Rev Immunol. 2004; 24(4): 267-96. 30. Campoli M, Ferrone S, Wang X. Functional and clinical relevance of chondroitin sulfate proteoglycan 4. Adv Cancer Res. 2010; 109: 73-121. 31. Carter P. Improving the efficacy of antibody-based cancer therapies. Nat Rev Cancer. 2001 Nov; 1(2): 118-29. 32. Chames P, Baty D. Bispecific antibodies for cancer therapy: the light at the end of the tunnel? MAbs. 2009 Nov-Dec; 1(6): 539-47. 33. Chang CC, Campoli M, Luo W, Zhao W, Zaenker KS, Ferrone S. Immunotherapy of melanoma targeting human high molecular weight melanoma-associated antigen: potential role of nonimmunological mechanisms. Ann N Y Acad Sci. 2004 Dec; 1028: 340-50. 34. Chappell DB, Zaks TZ, Rosenberg SA, Restifo NP. Human melanoma cells do not express Fas (Apo-1/CD95) ligand. Cancer research. 1999 Jan 1; 59(1): 59-62. 35. Chavez-Galan L, Arenas-Del Angel MC, Zenteno E, Chavez R, Lascurain R. Cell death mechanisms induced by cytotoxic lymphocytes. Cell Mol Immunol. 2009 Feb; 6(1): 15-25. 36. Clark WH, Jr., Elder DE, Guerry Dt, Epstein MN, Greene MH, Van Horn M. A study of tumor progression: the precursor lesions of superficial spreading and nodular melanoma. Hum Pathol. 1984 Dec; 15(12): 1147-65. 37. D'Acquisto F, Crompton T. CD3+CD4-CD8- (double negative) T cells: saviours or villains of the immune response? Biochem Pharmacol. 2011 Aug 15; 82(4): 333-40. 38. Dangoor A, Lorigan P, Keilholz U, Schadendorf D, Harris A, Ottensmeier C, Smyth J, Hoffmann K, Anderson R, Cripps M, Schneider J, Hawkins R. Clinical and immunological responses in metastatic melanoma patients vaccinated with a high-dose poly-epitope vaccine. Cancer immunology, immunotherapy : CII. 2010 Jun; 59(6): 863-73. 78 39. Davis TA, Czerwinski DK, Levy R. Therapy of B-cell lymphoma with anti-CD20 antibodies can result in the loss of CD20 antigen expression. Clin Cancer Res. 1999 Mar; 5(3): 611-5. 40. de Visser KE, Eichten A, Coussens LM. Paradoxical roles of the immune system during cancer development. Nat Rev Cancer. 2006 Jan; 6(1): 24-37. 41. Deininger M, Buchdunger E, Druker BJ. The development of imatinib as a therapeutic agent for chronic myeloid leukemia. Blood. 2005 Apr 1; 105(7): 2640-53. 42. Dissemond J, Goette P, Moers J, Lindeke A, Goos M, Ferrone S, Wagner SN. Immunoproteasome subunits LMP2 and LMP7 downregulation in primary malignant melanoma lesions: association with lack of spontaneous regression. Melanoma Res. 2003 Aug; 13(4): 371-7. 43. Dissemond J, Grabbe S. Vermittlung antitumoraler Mechanismen im humanen malignen Melanom durch MHC-Klasse-I-Moleküle. Hautarzt. 2006 Aug; 57(8): 690-6. 44. Dong H, Strome SE, Salomao DR, Tamura H, Hirano F, Flies DB, Roche PC, Lu J, Zhu G, Tamada K, Lennon VA, Celis E, Chen L. Tumor-associated B7-H1 promotes T-cell apoptosis: a potential mechanism of immune evasion. Nat Med. 2002 Aug; 8(8): 793-800. 45. Dreier T, Lorenczewski G, Brandl C, Hoffmann P, Syring U, Hanakam F, Kufer P, Riethmuller G, Bargou R, Baeuerle PA. Extremely potent, rapid and costimulationindependent cytotoxic T-cell response against lymphoma cells catalyzed by a single-chain bispecific antibody. International journal of cancer. 2002 Aug 20; 100(6): 690-7. 46. Dreno B, Nguyen JM, Khammari A, Pandolfino MC, Tessier MH, Bercegeay S, Cassidanius A, Lemarre P, Billaudel S, Labarriere N, Jotereau F. Randomized trial of adoptive transfer of melanoma tumor-infiltrating lymphocytes as adjuvant therapy for stage III melanoma. Cancer immunology, immunotherapy : CII. 2002 Nov; 51(10): 539-46. 47. Dudley ME, Wunderlich JR, Yang JC, Hwu P, Schwartzentruber DJ, Topalian SL, Sherry RM, Marincola FM, Leitman SF, Seipp CA, Rogers-Freezer L, Morton KE, Nahvi A, Mavroukakis SA, White DE, Rosenberg SA. A phase I study of nonmyeloablative chemotherapy and adoptive transfer of autologous tumor antigen-specific T lymphocytes in patients with metastatic melanoma. J Immunother. 2002 May-Jun; 25(3): 243-51. 48. Dudley ME, Yang JC, Sherry R, Hughes MS, Royal R, Kammula U, Robbins PF, Huang J, Citrin DE, Leitman SF, Wunderlich J, Restifo NP, Thomasian A, Downey SG, Smith FO, Klapper J, Morton K, Laurencot C, White DE, Rosenberg SA. Adoptive cell therapy for patients with metastatic melanoma: evaluation of intensive myeloablative chemoradiation preparative regimens. J Clin Oncol. 2008 Nov 10; 26(32): 5233-9. 49. Duman BB, Sahin B, Ergin M, Guvenc B. Loss of CD20 antigen expression after rituximab therapy of CD20 positive B cell lymphoma (diffuse large B cell extranodal marginal zone lymphoma combination): A case report and review of the literature. Med Oncol. 2011 Jul 31. 50. Dunn GP, Bruce AT, Ikeda H, Old LJ, Schreiber RD. Cancer immunoediting: from immunosurveillance to tumor escape. Nat Immunol. 2002 Nov; 3(11): 991-8. 51. Dunn GP, Old LJ, Schreiber RD. The immunobiology of cancer immunosurveillance and immunoediting. Immunity. 2004 Aug; 21(2): 137-48. 79 52. Eisenmann KM, McCarthy JB, Simpson MA, Keely PJ, Guan JL, Tachibana K, Lim L, Manser E, Furcht LT, Iida J. Melanoma chondroitin sulphate proteoglycan regulates cell spreading through Cdc42, Ack-1 and p130cas. Nat Cell Biol. 1999 Dec; 1(8): 507-13. 53. Elias EG, Hasskamp JH, Sharma BK. Cytokines and Growth Factors Expressed by Human Cutaneous Melanoma. Cancers (Basel). 2010; 2(2): 794-808. 54. Erfurt C, Sun Z, Haendle I, Schuler-Thurner B, Heirman C, Thielemans K, van der Bruggen P, Schuler G, Schultz ES. Tumor-reactive CD4+ T cell responses to the melanomaassociated chondroitin sulphate proteoglycan in melanoma patients and healthy individuals in the absence of autoimmunity. J Immunol. 2007 Jun 15; 178(12): 7703-9. 55. Escobar A, Lopez M, Serrano A, Ramirez M, Perez C, Aguirre A, Gonzalez R, Alfaro J, Larrondo M, Fodor M, Ferrada C, Salazar-Onfray F. Dendritic cell immunizations alone or combined with low doses of interleukin-2 induce specific immune responses in melanoma patients. Clin Exp Immunol. 2005 Dec; 142(3): 555-68. 56. Fabricant RN, De Larco JE, Todaro GJ. Nerve growth factor receptors on human melanoma cells in culture. Proc Natl Acad Sci U S A. 1977 Feb; 74(2): 565-9. 57. Ferrone S, Chen ZJ, Liu CC, Hirai S, Kageshita T, Mittelman A. Human high molecular weight-melanoma associated antigen mimicry by mouse anti-idiotypic monoclonal antibodies MK2-23. Experimental studies and clinical trials in patients with malignant melanoma. Pharmacol Ther. 1993 Feb-Mar; 57(2-3): 259-90. 58. Ferrone S, Giacomi P, Natali PG. A human high molecular weight-melanoma associated antigen (HMW-MAA) defined by monoclonal antibodies: a useful marker to radioimage tumor lesions in patients with melanoma. Fairchild RG, Brownell GL. Proceedings of the first international symposium on neutron capture therapy; 12.-14. October 1983. Cambridge, Massachusetts, U.S.A., Massachusetts Institute of Technology. 59. Ferrone S, Marincola FM. Loss of HLA class I antigens by melanoma cells: molecular mechanisms, functional significance and clinical relevance. Immunology today. 1995 Oct; 16(10): 487-94. 60. Gadiot J, Hooijkaas AI, Kaiser AD, van Tinteren H, van Boven H, Blank C. Overall survival and PD-L1 expression in metastasized malignant melanoma. Cancer. 2011 May 15; 117(10): 2192-201. 61. Gajewski TF. Identifying and overcoming immune resistance mechanisms in the melanoma tumor microenvironment. Clin Cancer Res. 2006 Apr 1; 12(7 Pt 2): 2326s-30s. 62. Gajewski TF. Failure at the effector phase: immune barriers at the level of the melanoma tumor microenvironment. Clin Cancer Res. 2007 Sep 15; 13(18 Pt 1): 5256-61. 63. Gandini S, Sera F, Cattaruzza MS, Pasquini P, Picconi O, Boyle P, Melchi CF. Meta-analysis of risk factors for cutaneous melanoma: II. Sun exposure. Eur J Cancer. 2005 Jan; 41(1): 45-60. 64. Garbe C, Schadendorf D, Stolz W, Volkenandt M, Reinhold U, Kortmann RD, Kettelhack C, Frerich B, Keilholz U, Dummer R, Sebastian G, Tilgen W, Schuler G, 80 Mackensen A, Kaufmann R, Hauschild A. Deutsche Leitlinie: Malignes Melanom. Version 15. Tübingen. 2005. 65. Garbe C, Schadendorf D, Stolz W, Volkenandt M, Reinhold U, Kortmann RD, Kettelhack C, Frerich B, Keilholz U, Dummer R, Sebastian G, Tilgen W, Schuler G, Mackensen A, Kaufmann R, Hauschild A. Short German guidelines: malignant melanoma. J Dtsch Dermatol Ges. 2008 May; 6 Suppl 1: S9-S14. 66. Ghose T, Ferrone S, Blair AH, Kralovec Y, Temponi M, Singh M, Mammen M. Regression of human melanoma xenografts in nude mice injected with methotrexate linked to monoclonal antibody 225.28 to human high molecular weight-melanoma associated antigen. Cancer immunology, immunotherapy : CII. 1991; 34(2): 90-6. 67. Gilchrest BA, Eller MS, Geller AC, Yaar M. The pathogenesis of melanoma induced by ultraviolet radiation. N Engl J Med. 1999 Apr 29; 340(17): 1341-8. 68. Ginsberg BA, Gallardo HF, Rasalan TS, Adamow M, Mu Z, Tandon S, Bewkes BB, Roman RA, Chapman PB, Schwartz GK, Carvajal RD, Panageas KS, Terzulli SL, Houghton AN, Yuan JD, Wolchok JD. Immunologic response to xenogeneic gp100 DNA in melanoma patients: comparison of particle-mediated epidermal delivery with intramuscular injection. Clin Cancer Res. 2010 Aug 1; 16(15): 4057-65. 69. Graubner B, DIMDI. Internationale statistische Klassifikation der Krankheiten und verwandter Gesundheitsprobleme (ICD); German Modification. 10. Revision; Version 2011, Stand 5. Oktober 2010. Köln. Deutscher Ärzte Verlag; 2011. 70. Grohmann U, Fallarino F, Puccetti P. Tolerance, DCs and tryptophan: much ado about IDO. Trends in Immunology. 2003 May; 24(5): 242-8. 71. Haas C, Krinner E, Brischwein K, Hoffmann P, Lutterbuse R, Schlereth B, Kufer P, Baeuerle PA. Mode of cytotoxic action of T cell-engaging BiTE antibody MT110. Immunobiology. 2009; 214(6): 441-53. 72. Hahne M, Rimoldi D, Schroter M, Romero P, Schreier M, French LE, Schneider P, Bornand T, Fontana A, Lienard D, Cerottini J, Tschopp J. Melanoma cell expression of Fas(Apo-1/CD95) ligand: implications for tumor immune escape. Science. 1996 Nov 22; 274(5291): 1363-6. 73. Heisterkamp N, Stephenson JR, Groffen J, Hansen PF, de Klein A, Bartram CR, Grosveld G. Localization of the c-ab1 oncogene adjacent to a translocation break point in chronic myelocytic leukaemia. Nature. 1983 Nov 17-23; 306(5940): 239-42. 74. Herrmann I, Baeuerle PA, Friedrich M, Murr A, Filusch S, Ruttinger D, Majdoub MW, Sharma S, Kufer P, Raum T, Munz M. Highly efficient elimination of colorectal tumor-initiating cells by an EpCAM/CD3-bispecific antibody engaging human T cells. PLoS One. 2010; 5(10): e13474. 75. Hersey P, Menzies SW, Coventry B, Nguyen T, Farrelly M, Collins S, Hirst D, Johnson H. Phase I/II study of immunotherapy with T-cell peptide epitopes in patients with stage IV melanoma. Cancer immunology, immunotherapy : CII. 2005 Mar; 54(3): 208-18. 81 76. Hersey P, Menzies SW, Halliday GM, Nguyen T, Farrelly ML, DeSilva C, Lett M. Phase I/II study of treatment with dendritic cell vaccines in patients with disseminated melanoma. Cancer immunology, immunotherapy : CII. 2004 Feb; 53(2): 125-34. 77. Hershkovitz L, Schachter J, Treves AJ, Besser MJ. Focus on adoptive T cell transfer trials in melanoma. Clin Dev Immunol. 2010; 2010: 260267. 78. Hicklin DJ, Marincola FM, Ferrone S. HLA class I antigen downregulation in human cancers: T-cell immunotherapy revives an old story. Mol Med Today. 1999 Apr; 5(4): 178-86. 79. Hino R, Kabashima K, Kato Y, Yagi H, Nakamura M, Honjo T, Okazaki T, Tokura Y. Tumor cell expression of programmed cell death-1 ligand 1 is a prognostic factor for malignant melanoma. Cancer. 2010 Apr 1; 116(7): 1757-66. 80. Hodi FS, O'Day SJ, McDermott DF, Weber RW, Sosman JA, Haanen JB, Gonzalez R, Robert C, Schadendorf D, Hassel JC, Akerley W, van den Eertwegh AJ, Lutzky J, Lorigan P, Vaubel JM, Linette GP, Hogg D, Ottensmeier CH, Lebbe C, Peschel C, Quirt I, Clark JI, Wolchok JD, Weber JS, Tian J, Yellin MJ, Nichol GM, Hoos A, Urba WJ. Improved survival with ipilimumab in patients with metastatic melanoma. N Engl J Med. 2010 Aug 19; 363(8): 711-23. 81. Hof H, Dörries R. Medizinische Mikrobiologie. 3. Auflage. Stuttgart. Thieme Verlag; 2005. 82. Hoffmann P, Hofmeister R, Brischwein K, Brandl C, Crommer S, Bargou R, Itin C, Prang N, Baeuerle PA. Serial killing of tumor cells by cytotoxic T cells redirected with a CD19-/CD3-bispecific single-chain antibody construct. International journal of cancer. 2005 May 20; 115(1): 98-104. 83. Husmann G. Krebs in Deutschland 2005/2006: Häufigkeiten und Trends. 7. Ausg. Berlin, Saarbrücken. Robert Koch-Instituts, Gesellschaft der Epidemiologischen Krebsregister in Deutschland e.V; 2010. 84. Igney FH, Krammer PH. Tumor counterattack: fact or fiction? Cancer immunology, immunotherapy : CII. 2005 Nov; 54(11): 1127-36. 85. Iida J, Meijne AM, Oegema TR, Jr., Yednock TA, Kovach NL, Furcht LT, McCarthy JB. A role of chondroitin sulfate glycosaminoglycan binding site in alpha4beta1 integrinmediated melanoma cell adhesion. J Biol Chem. 1998 Mar 6; 273(10): 5955-62. 86. Iida J, Pei D, Kang T, Simpson MA, Herlyn M, Furcht LT, McCarthy JB. Melanoma chondroitin sulfate proteoglycan regulates matrix metalloproteinase-dependent human melanoma invasion into type I collagen. J Biol Chem. 2001 Jun 1; 276(22): 18786-94. 87. Jacobs JF, Punt CJ, Lesterhuis WJ, Sutmuller RP, Brouwer HM, Scharenborg NM, Klasen IS, Hilbrands LB, Figdor CG, de Vries IJ, Adema GJ. Dendritic cell vaccination in combination with anti-CD25 monoclonal antibody treatment: a phase I/II study in metastatic melanoma patients. Clin Cancer Res. 2010 Oct 15; 16(20): 5067-78. 88. Javia LR, Rosenberg SA. CD4+CD25+ suppressor lymphocytes in the circulation of patients immunized against melanoma antigens. J Immunother. 2003 Jan-Feb; 26(1): 85-93. 82 89. Jhappan C, Noonan FP, Merlino G. Ultraviolet radiation and cutaneous malignant melanoma. Oncogene. 2003 May 19; 22(20): 3099-112. 90. Kaatsch P, Spix C, Katalinic A, Hentschel S. Krebs in Deutschland 2007/2008. 8. Ausgabe. Berlin, Saarbrücken. Robert Koch-Institut, Gesellschaft der epidemiologischen Krebsregister in Deutschland; 2012. 91. Kageshita T, Hirai S, Ono T, Hicklin DJ, Ferrone S. Down-regulation of HLA class I antigen-processing molecules in malignant melanoma: association with disease progression. The American Journal of Pathology. 1999 Mar; 154(3): 745-54. 92. Kageshita T, Kuriya N, Ono T, Horikoshi T, Takahashi M, Wong GY, Ferrone S. Association of high molecular weight melanoma-associated antigen expression in primary acral lentiginous melanoma lesions with poor prognosis. Cancer research. 1993 Jun 15; 53(12): 2830-3. 93. Kageshita T, Nakamura T, Yamada M, Kuriya N, Arao T, Ferrone S. Differential expression of melanoma associated antigens in acral lentiginous melanoma and in nodular melanoma lesions. Cancer research. 1991 Mar 15; 51(6): 1726-32. 94. Kennedy GA, Tey SK, Cobcroft R, Marlton P, Cull G, Grimmett K, Thomson D, Gill D. Incidence and nature of CD20-negative relapses following rituximab therapy in aggressive B-cell non-Hodgkin's lymphoma: a retrospective review. Br J Haematol. 2002 Nov; 119(2): 412-6. 95. Khammari A, Labarriere N, Vignard V, Nguyen JM, Pandolfino MC, Knol AC, Quereux G, Saiagh S, Brocard A, Jotereau F, Dreno B. Treatment of metastatic melanoma with autologous Melan-A/MART-1-specific cytotoxic T lymphocyte clones. The Journal of investigative dermatology. 2009 Dec; 129(12): 2835-42. 96. King J, Waxman J, Stauss H. Advances in tumour immunotherapy. Qjm. 2008 Sep; 101(9): 675-83. 97. Kirkwood JM, Lee S, Moschos SJ, Albertini MR, Michalak JC, Sander C, Whiteside T, Butterfield LH, Weiner L. Immunogenicity and antitumor effects of vaccination with peptide vaccine+/-granulocyte-monocyte colony-stimulating factor and/or IFN-alpha2b in advanced metastatic melanoma: Eastern Cooperative Oncology Group Phase II Trial E1696. Clin Cancer Res. 2009 Feb 15; 15(4): 1443-51. 98. Kischel R, Hausmann S, Blümel C, Rau D, Mangold S, Hoffmann P, Raum T, Ebert E, Baeuerle PA, Kufer P. Highly efficient elimination of melanoma cells expressing melanoma-associated chondroitin sulfate proteoglycan (MCSP) by MCSP/CD3- bispecific single-chain antibody constructs. Proc Am Assoc Cancer Res (AACR): A61; 22-26 October 2007; San Francisco2007. 99. Köhler G, Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity. Nature. 1975 Aug 7; 256(5517): 495-7. 100. Kontermann RE. Recombinant bispecific antibodies for cancer therapy. Acta Pharmacol Sin. 2005 Jan; 26(1): 1-9. 101. Krüger-Krasagakes S, Krasagakis K, Garbe C, Schmitt E, Huls C, Blankenstein T, Diamantstein T. Expression of interleukin 10 in human melanoma. Br J Cancer. 1994 Dec; 70(6): 1182-5. 83 102. Kufer P, Lutterbuse R, Baeuerle PA. The promise of bispecific antibodies. Discov Med. 2004 Oct; 4(23): 325-32. 103. Kufer P, Lutterbuse R, Baeuerle PA. A revival of bispecific antibodies. Trends Biotechnol. 2004 May; 22(5): 238-44. 104. Kufer P, Mack M, Gruber R, Lutterbuse R, Zettl F, Riethmuller G. Construction and biological activity of a recombinant bispecific single-chain antibody designed for therapy of minimal residual colorectal cancer. Cancer immunology, immunotherapy : CII. 1997 Nov-Dec; 45(34): 193-7. 105. Kumar V, Robbins SL. Robbins basic pathology. 8. Auflage. Philadelphia. Saunders/Elsevier Verlag; 2007. 106. Kusunoki Y, Hirai Y, Kyoizumi S, Akiyama M. Evidence for in vivo clonal proliferation of unique population of blood CD4-/CD8- T cells bearing T-cell receptor alpha and beta chains in two normal men. Blood. 1992 Jun 1; 79(11): 2965-72. 107. Kyte JA, Gaudernack G. Immuno-gene therapy of cancer with tumour-mRNA transfected dendritic cells. Cancer immunology, immunotherapy : CII. 2006 Nov; 55(11): 1432-42. 108. Kyte JA, Kvalheim G, Lislerud K, thor Straten P, Dueland S, Aamdal S, Gaudernack G. T cell responses in melanoma patients after vaccination with tumor-mRNA transfected dendritic cells. Cancer immunology, immunotherapy : CII. 2007 May; 56(5): 65975. 109. Kyte JA, Mu L, Aamdal S, Kvalheim G, Dueland S, Hauser M, Gullestad HP, Ryder T, Lislerud K, Hammerstad H, Gaudernack G. Phase I/II trial of melanoma therapy with dendritic cells transfected with autologous tumor-mRNA. Cancer Gene Ther. 2006 Oct; 13(10): 905-18. 110. Leitlinienprogramm Onkologie. „Diagnostik, Therapie und Nachsorge des Melanoms". Version 2.6 vom 29.06.2012. AWMF S3-Leitlinie (032-024OL), Deutsche Krebsgesellschaft e.V. und Deutsche Krebshilfe e.V.; 2012. 111. Lesimple T, Neidhard EM, Vignard V, Lefeuvre C, Adamski H, Labarriere N, Carsin A, Monnier D, Collet B, Clapisson G, Birebent B, Philip I, Toujas L, Chokri M, Quillien V. Immunologic and clinical effects of injecting mature peptide-loaded dendritic cells by intralymphatic and intranodal routes in metastatic melanoma patients. Clin Cancer Res. 2006 Dec 15; 12(24): 7380-8. 112. Lesterhuis WJ, Aarntzen EH, De Vries IJ, Schuurhuis DH, Figdor CG, Adema GJ, Punt CJ. Dendritic cell vaccines in melanoma: from promise to proof? Crit Rev Oncol Hematol. 2008 May; 66(2): 118-34. 113. Lesterhuis WJ, Schreibelt G, Scharenborg NM, Brouwer HM, Gerritsen MJ, Croockewit S, Coulie PG, Torensma R, Adema GJ, Figdor CG, de Vries IJ, Punt CJ. Wild-type and modified gp100 peptide-pulsed dendritic cell vaccination of advanced melanoma patients can lead to long-term clinical responses independent of the peptide used. Cancer immunology, immunotherapy : CII. 2011 Feb; 60(2): 249-60. 84 114. Löffler A, Kufer P, Lutterbuse R, Zettl F, Daniel PT, Schwenkenbecher JM, Riethmuller G, Dorken B, Bargou RC. A recombinant bispecific single-chain antibody, CD19 x CD3, induces rapid and high lymphoma-directed cytotoxicity by unstimulated T lymphocytes. Blood. 2000 Mar 15; 95(6): 2098-103. 115. Longmore JM. Oxford handbook of clinical medicine. 8. Auflage. Oxford. Oxford University Press; 2010. 116. Luo W, Wang X, Kageshita T, Wakasugi S, Karpf AR, Ferrone S. Regulation of high molecular weight-melanoma associated antigen (HMW-MAA) gene expression by promoter DNA methylation in human melanoma cells. Oncogene. 2006 May 11; 25(20): 2873-84. 117. Maciag PC, Seavey MM, Pan ZK, Ferrone S, Paterson Y. Cancer immunotherapy targeting the high molecular weight melanoma-associated antigen protein results in a broad antitumor response and reduction of pericytes in the tumor vasculature. Cancer research. 2008 Oct 1; 68(19): 8066-75. 118. Mack M, Gruber R, Schmidt S, Riethmuller G, Kufer P. Biologic properties of a bispecific single-chain antibody directed against 17-1A (EpCAM) and CD3: tumor cell-dependent T cell stimulation and cytotoxic activity. Journal of immunology. 1997 Apr 15; 158(8): 3965-70. 119. Mack M, Riethmuller G, Kufer P. A small bispecific antibody construct expressed as a functional single-chain molecule with high tumor cell cytotoxicity. Proc Natl Acad Sci U S A. 1995 Jul 18; 92(15): 7021-5. 120. Mackensen A, Carcelain G, Viel S, Raynal MC, Michalaki H, Triebel F, Bosq J, Hercend T. Direct evidence to support the immunosurveillance concept in a human regressive melanoma. J Clin Invest. 1994 Apr; 93(4): 1397-402. 121. Mackensen A, Meidenbauer N, Vogl S, Laumer M, Berger J, Andreesen R. Phase I Study of Adoptive T-Cell Therapy Using Antigen-Specific CD8+ T Cells for the Treatment of Patients With Metastatic Melanoma. Journal of Clinical Oncology. 2006; 24(31): 5060-9. 122. Maeshima AM, Taniguchi H, Nomoto J, Maruyama D, Kim SW, Watanabe T, Kobayashi Y, Tobinai K, Matsuno Y. Histological and immunophenotypic changes in 59 cases of B-cell non-Hodgkin's lymphoma after rituximab therapy. Cancer Sci. 2009 Jan; 100(1): 54-61. 123. Marchand M, van Baren N, Weynants P, Brichard V, Dreno B, Tessier MH, Rankin E, Parmiani G, Arienti F, Humblet Y, Bourlond A, Vanwijck R, Lienard D, Beauduin M, Dietrich PY, Russo V, Kerger J, Masucci G, Jager E, De Greve J, Atzpodien J, Brasseur F, Coulie PG, van der Bruggen P, Boon T. Tumor regressions observed in patients with metastatic melanoma treated with an antigenic peptide encoded by gene MAGE-3 and presented by HLA-A1. International journal of cancer. 1999 Jan 18; 80(2): 219-30. 124. Marincola FM, Shamamian P, Alexander RB, Gnarra JR, Turetskaya RL, Nedospasov SA, Simonis TB, Taubenberger JK, Yannelli J, Mixon A, et al. Loss of HLA haplotype and B locus down-regulation in melanoma cell lines. Journal of immunology. 1994 Aug 1; 153(3): 1225-37. 125. Matsui M, Nakanishi T, Noguchi T, Imai K, Yachi A, Ferrone S. Suppression of human melanoma growth in nude mice injected with anti high-molecular-weight melanoma-associated 85 antigen monoclonal antibody 225.28S conjugated to purothionin. Jpn J Cancer Res. 1985 Feb; 76(2): 119-23. 126. Medema JP, de Jong J, Peltenburg LT, Verdegaal EM, Gorter A, Bres SA, Franken KL, Hahne M, Albar JP, Melief CJ, Offringa R. Blockade of the granzyme B/perforin pathway through overexpression of the serine protease inhibitor PI-9/SPI-6 constitutes a mechanism for immune escape by tumors. Proc Natl Acad Sci U S A. 2001 Sep 25; 98(20): 11515-20. 127. Melero I, Hervas-Stubbs S, Glennie M, Pardoll DM, Chen L. Immunostimulatory monoclonal antibodies for cancer therapy. Nat Rev Cancer. 2007 Feb; 7(2): 95-106. 128. Meyskens FL, Jr., Farmer PJ, Anton-Culver H. Etiologic pathogenesis of melanoma: a unifying hypothesis for the missing attributable risk. Clin Cancer Res. 2004 Apr 15; 10(8): 25813. 129. Miller AJ, Mihm MC, Jr. Melanoma. N Engl J Med. 2006 Jul 6; 355(1): 51-65. 130. Mittelman A, Chen ZJ, Yang H, Wong GY, Ferrone S. Human high molecular weight melanoma-associated antigen (HMW-MAA) mimicry by mouse anti-idiotypic monoclonal antibody MK2-23: induction of humoral anti-HMW-MAA immunity and prolongation of survival in patients with stage IV melanoma. Proc Natl Acad Sci U S A. 1992 Jan 15; 89(2): 466-70. 131. Münz M, Murr A, Hoffmann P, Edinger M, Baeuerle P, Kufer P, Raum T. Lysis of cancer cells by highly purified T regulatory cells engaged via an EpCAM/CD3-bispecific BiTE antibody.pdf. AACR, Annual Meeting; March31-April4 2012; Chicago2012. 132. Murphy KM, Travers P, Walport M, Janeway C, Seidler L, Ehrenstein M. Janeway Immunologie. 7. Aufl. Heidelberg. Spektrum Akademischer Verlag; 2009. 133. Nagayama H, Sato K, Morishita M, Uchimaru K, Oyaizu N, Inazawa T, Yamasaki T, Enomoto M, Nakaoka T, Nakamura T, Maekawa T, Yamamoto A, Shimada S, Saida T, Kawakami Y, Asano S, Tani K, Takahashi TA, Yamashita N. Results of a phase I clinical study using autologous tumour lysate-pulsed monocyte-derived mature dendritic cell vaccinations for stage IV malignant melanoma patients combined with low dose interleukin-2. Melanoma Res. 2003 Oct; 13(5): 521-30. 134. Nagorsen D, Baeuerle PA. Immunomodulatory therapy of cancer with T cell-engaging BiTE antibody blinatumomab. Exp Cell Res. 2011 May 15; 317(9): 1255-60. 135. Nagorsen D, Bargou R, Ruttinger D, Kufer P, Baeuerle PA, Zugmaier G. Immunotherapy of lymphoma and leukemia with T-cell engaging BiTE antibody blinatumomab. Leuk Lymphoma. 2009 Jun; 50(6): 886-91. 136. Nagorsen D, Kufer P, Baeuerle PA, Bargou R. Blinatumomab: a historical perspective. Pharmacol Ther. 2012 Dec; 136(3): 334-42. 137. Nakai N, Asai J, Ueda E, Takenaka H, Katoh N, Kishimoto S. Vaccination of Japanese patients with advanced melanoma with peptide, tumor lysate or both peptide and tumor lysatepulsed mature, monocyte-derived dendritic cells. J Dermatol. 2006 Jul; 33(7): 462-72. 86 138. Natali PG, Giacomini P, Russo C, Steinbach G, Fenoglio C, Ferrone S. Antigenic profile of human melanoma cells. Analysis with monoclonal antibodies to histocompatibility antigens and to melanoma-associated antigens. J Cutan Pathol. 1983 Aug; 10(4): 225-37. 139. Nestle FO, Alijagic S, Gilliet M, Sun Y, Grabbe S, Dummer R, Burg G, Schadendorf D. Vaccination of melanoma patients with peptide- or tumor lysate-pulsed dendritic cells. Nat Med. 1998 Mar; 4(3): 328-32. 140. Nishi H, Inoue Y, Kageshita T, Takata M, Ihn H. The expression of human high molecular weight melanoma-associated antigen in acral lentiginous melanoma. Biosci Trends. 2010 Apr; 4(2): 86-9. 141. Nowell P, Hungerford D. A Minute Chromosome in Human Chronic Granulocytic Leukemia. Science (National Academy of Sciences). 1960 Nov 18; 132(3438): 1488-501. 142. Oble DA, Loewe R, Yu P, Mihm MC, Jr. Focus on TILs: prognostic significance of tumor infiltrating lymphocytes in human melanoma. Cancer Immun. 2009; 9: 3. 143. Offner S, Hofmeister R, Romaniuk A, Kufer P, Baeuerle PA. Induction of regular cytolytic T cell synapses by bispecific single-chain antibody constructs on MHC class I-negative tumor cells. Mol Immunol. 2006 Feb; 43(6): 763-71. 144. Oldham RK, Foon KA, Morgan AC, Woodhouse CS, Schroff RW, Abrams PG, Fer M, Schoenberger CS, Farrell M, Kimball E, et al. Monoclonal antibody therapy of malignant melanoma: in vivo localization in cutaneous metastasis after intravenous administration. J Clin Oncol. 1984 Nov; 2(11): 1235-44. 145. Oratz R, Speyer JL, Wernz JC, Hochster H, Meyers M, Mischak R, Spitler LE. Antimelanoma monoclonal antibody-ricin A chain immunoconjugate (XMMME-001-RTA) plus cyclophosphamide in the treatment of metastatic malignant melanoma: results of a phase II trial. J Biol Response Mod. 1990 Aug; 9(4): 345-54. 146. Osada T, Hsu D, Hammond S, Hobeika A, Devi G, Clay TM, Lyerly HK, Morse MA. Metastatic colorectal cancer cells from patients previously treated with chemotherapy are sensitive to T-cell killing mediated by CEA/CD3-bispecific T-cell-engaging BiTE antibody. Br J Cancer. 2010 Jan 5; 102(1): 124-33. 147. Palmieri G, Capone M, Ascierto ML, Gentilcore G, Stroncek DF, Casula M, Sini MC, Palla M, Mozzillo N, Ascierto PA. Main roads to melanoma. J Transl Med. 2009; 7: 86. 148. Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA: A Cancer Journal for Clinicians. 2005 Mar-Apr; 55(2): 74-108. 149. Phan GQ, Touloukian CE, Yang JC, Restifo NP, Sherry RM, Hwu P, Topalian SL, Schwartzentruber DJ, Seipp CA, Freezer LJ, Morton KE, Mavroukakis SA, White DE, Rosenberg SA. Immunization of patients with metastatic melanoma using both class I- and class II-restricted peptides from melanoma-associated antigens. J Immunother. 2003 Jul-Aug; 26(4): 349-56. 150. Piper AA, Tattersall MH, Fox RM. The activities of thymidine metabolising enzymes during the cell cycle of a human lymphocyte cell line LAZ-007 synchronised by centrifugal elutriation. Biochim Biophys Acta. 1980 Dec 15; 633(3): 400-9. 87 151. Post-White J. The immune system. Semin Oncol Nurs. 1996 May; 12(2): 89-96. 152. 17. Prud'homme GJ. DNA vaccination against tumors. J Gene Med. 2005 Jan; 7(1): 3- 153. Rambaut A, Posada D, Crandall KA, Holmes EC. The causes and consequences of HIV evolution. Nat Rev Genet. 2004 Jan; 5(1): 52-61. 154. Rassner G, Steinert U. Dermatologie: Lehrbuch und Atlas. 8. Auflage. München. Elsevier, Urban & Fischer Verlag; 2007. 155. 77. Reisfeld RA, Cheresh DA. Human tumor antigens. Adv Immunol. 1987; 40: 323- 156. Renz-Polster H, Krautzig S, Bätge B. Basislehrbuch Innere Medizin. 4. Auflage. München. Elsevier, Urban & Fischer Verlag; 2008. 157. Ribas A. Overcoming immunologic tolerance to melanoma: targeting CTLA-4 with tremelimumab (CP-675,206). Oncologist. 2008; 13 Suppl 4: 10-5. 158. Ribas A, Comin-Anduix B, Chmielowski B, Jalil J, de la Rocha P, McCannel TA, Ochoa MT, Seja E, Villanueva A, Oseguera DK, Straatsma BR, Cochran AJ, Glaspy JA, Hui L, Marincola FM, Wang E, Economou JS, Gomez-Navarro J. Dendritic cell vaccination combined with CTLA4 blockade in patients with metastatic melanoma. Clin Cancer Res. 2009 Oct 1; 15(19): 6267-76. 159. Riker A, Cormier J, Panelli M, Kammula U, Wang E, Abati A, Fetsch P, Lee KH, Steinberg S, Rosenberg S, Marincola F. Immune selection after antigen-specific immunotherapy of melanoma. Surgery. 1999 Aug; 126(2): 112-20. 160. Robert C, Ghiringhelli F. What is the role of cytotoxic T lymphocyte-associated antigen 4 blockade in patients with metastatic melanoma? Oncologist. 2009 Aug; 14(8): 848-61. 161. Robert C, Thomas L, Bondarenko I, O'Day S, M DJ, Garbe C, Lebbe C, Baurain JF, Testori A, Grob JJ, Davidson N, Richards J, Maio M, Hauschild A, Miller WH, Jr., Gascon P, Lotem M, Harmankaya K, Ibrahim R, Francis S, Chen TT, Humphrey R, Hoos A, Wolchok JD. Ipilimumab plus dacarbazine for previously untreated metastatic melanoma. N Engl J Med. 2011 Jun 30; 364(26): 2517-26. 162. Roberts JD, Niedzwiecki D, Carson WE, Chapman PB, Gajewski TF, Ernstoff MS, Hodi FS, Shea C, Leong SP, Johnson J, Zhang D, Houghton A, Haluska FG. Phase 2 study of the g209-2M melanoma peptide vaccine and low-dose interleukin-2 in advanced melanoma: Cancer and Leukemia Group B 509901. J Immunother. 2006 Jan-Feb; 29(1): 95-101. 163. Rosenberg SA, Dudley ME. Adoptive cell therapy for the treatment of patients with metastatic melanoma. Curr Opin Immunol. 2009 Apr; 21(2): 233-40. 164. Rosenberg SA, Packard BS, Aebersold PM, Solomon D, Topalian SL, Toy ST, Simon P, Lotze MT, Yang JC, Seipp CA, et al. Use of tumor-infiltrating lymphocytes and interleukin-2 in the immunotherapy of patients with metastatic melanoma. A preliminary report. N Engl J Med. 1988 Dec 22; 319(25): 1676-80. 88 165. Rosenberg SA, Yannelli JR, Yang JC, Topalian SL, Schwartzentruber DJ, Weber JS, Parkinson DR, Seipp CA, Einhorn JH, White DE. Treatment of patients with metastatic melanoma with autologous tumor-infiltrating lymphocytes and interleukin 2. J Natl Cancer Inst. 1994 Aug 3; 86(15): 1159-66. 166. Sakaguchi S, Yamaguchi T, Nomura T, Ono M. Regulatory T cells and immune tolerance. Cell. 2008 May 30; 133(5): 775-87. 167. Salcedo M, Bercovici N, Taylor R, Vereecken P, Massicard S, Duriau D, VernelPauillac F, Boyer A, Baron-Bodo V, Mallard E, Bartholeyns J, Goxe B, Latour N, Leroy S, Prigent D, Martiat P, Sales F, Laporte M, Bruyns C, Romet-Lemonne JL, Abastado JP, Lehmann F, Velu T. Vaccination of melanoma patients using dendritic cells loaded with an allogeneic tumor cell lysate. Cancer immunology, immunotherapy : CII. 2006 Jul; 55(7): 81929. 168. Salgaller ML, Marincola FM, Cormier JN, Rosenberg SA. Immunization against epitopes in the human melanoma antigen gp100 following patient immunization with synthetic peptides. Cancer research. 1996 Oct 15; 56(20): 4749-57. 169. Sato T, McCue P, Masuoka K, Salwen S, Lattime EC, Mastrangelo MJ, Berd D. Interleukin 10 production by human melanoma. Clin Cancer Res. 1996 Aug; 2(8): 1383-90. 170. Schaaf C, Zschocke J. Basiswissen Humangenetik. 1. Auflage. Heidelberg. Springer Verlag; 2007. 171. Schadendorf D. Tumorspezifische Therapieansätze in der Onkologie. Onkologie. 2001 Sep; 24 Suppl 5: 56-9. 172. Schadendorf D, Schuler G, Paschen A, Scheibenbogen C. Experimentelle Therapie des Melanoms. Der Onkologe. 2001; 7(1). 173. Schadendorf D, Ugurel S, Schuler-Thurner B, Nestle FO, Enk A, Brocker EB, Grabbe S, Rittgen W, Edler L, Sucker A, Zimpfer-Rechner C, Berger T, Kamarashev J, Burg G, Jonuleit H, Tuttenberg A, Becker JC, Keikavoussi P, Kampgen E, Schuler G. Dacarbazine (DTIC) versus vaccination with autologous peptide-pulsed dendritic cells (DC) in first-line treatment of patients with metastatic melanoma: a randomized phase III trial of the DC study group of the DeCOG. Ann Oncol. 2006 Apr; 17(4): 563-70. 174. Scheibenbogen C, Schadendorf D, Bechrakis NE, Nagorsen D, Hofmann U, Servetopoulou F, Letsch A, Philipp A, Foerster MH, Schmittel A, Thiel E, Keilholz U. Effects of granulocyte-macrophage colony-stimulating factor and foreign helper protein as immunologic adjuvants on the T-cell response to vaccination with tyrosinase peptides. International journal of cancer. 2003 Mar 20; 104(2): 188-94. 175. Schlereth B, Fichtner I, Lorenczewski G, Kleindienst P, Brischwein K, da Silva A, Kufer P, Lutterbuese R, Junghahn I, Kasimir-Bauer S, Wimberger P, Kimmig R, Baeuerle PA. Eradication of tumors from a human colon cancer cell line and from ovarian cancer metastases in immunodeficient mice by a single-chain Ep-CAM-/CD3-bispecific antibody construct. Cancer research. 2005 Apr 1; 65(7): 2882-9. 89 176. Schroff RW, Foon KA, Beatty SM, Oldham RK, Morgan AC, Jr. Human antimurine immunoglobulin responses in patients receiving monoclonal antibody therapy. Cancer research. 1985 Feb; 45(2): 879-85. 177. Schuler-Thurner B, Schuler G. Vakzinationstherapie des Melanoms. J Dtsch Dermatol Ges. 2005 Aug; 3(8): 630-45. 178. Schuler-Thurner B, Schultz ES, Berger TG, Weinlich G, Ebner S, Woerl P, Bender A, Feuerstein B, Fritsch PO, Romani N, Schuler G. Rapid induction of tumor-specific type 1 T helper cells in metastatic melanoma patients by vaccination with mature, cryopreserved, peptideloaded monocyte-derived dendritic cells. J Exp Med. 2002 May 20; 195(10): 1279-88. 179. Schütt C, Bröker B. Grundwissen Immunologie. 3. Auflage. Heidelberg. Spektrum Akademischer Verlag; 2011. 180. Seliger B, Maeurer MJ, Ferrone S. TAP off--tumors on. Immunology today. 1997 Jun; 18(6): 292-9. 181. Seliger B, Maeurer MJ, Ferrone S. Antigen-processing machinery breakdown and tumor growth. Immunol Today. 2000 Sep; 21(9): 455-64. 182. Sensi M, Anichini A. Unique tumor antigens: evidence for immune control of genome integrity and immunogenic targets for T cell-mediated patient-specific immunotherapy. Clin Cancer Res. 2006 Sep 1; 12(17): 5023-32. 183. Shankaran V, Ikeda H, Bruce AT, White JM, Swanson PE, Old LJ, Schreiber RD. IFNgamma and lymphocytes prevent primary tumour development and shape tumour immunogenicity. Nature. 2001 Apr 26; 410(6832): 1107-11. 184. Siccardi AG, Buraggi GL, Callegaro L, Mariani G, Natali PG, Abbati A, Bestagno M, Caputo V, Mansi L, Masi R, et al. Multicenter study of immunoscintigraphy with radiolabeled monoclonal antibodies in patients with melanoma. Cancer research. 1986 Sep; 46(9): 4817-22. 185. Siveen KS, Kuttan G. Role of macrophages in tumour progression. Immunol Lett. 2009 Apr 27; 123(2): 97-102. 186. Slingluff CL, Jr., Yamshchikov G, Neese P, Galavotti H, Eastham S, Engelhard VH, Kittlesen D, Deacon D, Hibbitts S, Grosh WW, Petroni G, Cohen R, Wiernasz C, Patterson JW, Conway BP, Ross WG. Phase I trial of a melanoma vaccine with gp100(280288) peptide and tetanus helper peptide in adjuvant: immunologic and clinical outcomes. Clin Cancer Res. 2001 Oct; 7(10): 3012-24. 187. Smithers M, O'Connell K, MacFadyen S, Chambers M, Greenwood K, Boyce A, Abdul-Jabbar I, Barker K, Grimmett K, Walpole E, Thomas R. Clinical response after intradermal immature dendritic cell vaccination in metastatic melanoma is associated with immune response to particulate antigen. Cancer immunology, immunotherapy : CII. 2003 Jan; 52(1): 41-52. 188. Spitler LE, del Rio M, Khentigan A, Wedel NI, Brophy NA, Miller LL, Harkonen WS, Rosendorf LL, Lee HM, Mischak RP, et al. Therapy of patients with 90 malignant melanoma using a monoclonal antimelanoma antibody-ricin A chain immunotoxin. Cancer research. 1987 Mar 15; 47(6): 1717-23. 189. Staerz UD, Kanagawa O, Bevan MJ. Hybrid antibodies can target sites for attack by T cells. Nature. 1985 Apr 18-24; 314(6012): 628-31. 190. Stopeck AT, Jones A, Hersh EM, Thompson JA, Finucane DM, Gutheil JC, Gonzalez R. Phase II study of direct intralesional gene transfer of allovectin-7, an HLA-B7/beta2microglobulin DNA-liposome complex, in patients with metastatic melanoma. Clin Cancer Res. 2001 Aug; 7(8): 2285-91. 191. Tagawa ST, Lee P, Snively J, Boswell W, Ounpraseuth S, Lee S, Hickingbottom B, Smith J, Johnson D, Weber JS. Phase I study of intranodal delivery of a plasmid DNA vaccine for patients with Stage IV melanoma. Cancer. 2003 Jul 1; 98(1): 144-54. 192. Thomas L. On immunosurveillance in human cancer. Yale J Biol Med. 1982 May-Aug; 55(3-4): 329-33. 193. Thumann P, Moc I, Humrich J, Berger TG, Schultz ES, Schuler G, Jenne L. Antigen loading of dendritic cells with whole tumor cell preparations. Journal of immunological methods. 2003 Jun 1; 277(1-2): 1-16. 194. Thurner B, Haendle I, Roder C, Dieckmann D, Keikavoussi P, Jonuleit H, Bender A, Maczek C, Schreiner D, von den Driesch P, Brocker EB, Steinman RM, Enk A, Kampgen E, Schuler G. Vaccination with mage-3A1 peptide-pulsed mature, monocyte-derived dendritic cells expands specific cytotoxic T cells and induces regression of some metastases in advanced stage IV melanoma. J Exp Med. 1999 Dec 6; 190(11): 1669-78. 195. Thurner B, Roder C, Dieckmann D, Heuer M, Kruse M, Glaser A, Keikavoussi P, Kampgen E, Bender A, Schuler G. Generation of large numbers of fully mature and stable dendritic cells from leukapheresis products for clinical application. Journal of immunological methods. 1999 Feb 1; 223(1): 1-15. 196. Tong Q, Liu K, Wang G. FasL expression in colorectal carcinoma and its significance in immune escape of cancer. J Huazhong Univ Sci Technolog Med Sci. 2006; 26(1): 79-81. 197. Topp MS, Kufer P, Gokbuget N, Goebeler M, Klinger M, Neumann S, Horst HA, Raff T, Viardot A, Schmid M, Stelljes M, Schaich M, Degenhard E, Kohne-Volland R, Bruggemann M, Ottmann O, Pfeifer H, Burmeister T, Nagorsen D, Schmidt M, Lutterbuese R, Reinhardt C, Baeuerle PA, Kneba M, Einsele H, Riethmuller G, Hoelzer D, Zugmaier G, Bargou RC. Targeted Therapy With the T-Cell-Engaging Antibody Blinatumomab of Chemotherapy-Refractory Minimal Residual Disease in B-Lineage Acute Lymphoblastic Leukemia Patients Results in High Response Rate and Prolonged Leukemia-Free Survival. J Clin Oncol. 2011 May 16. 198. Torisu-Itakura H, Schoellhammer HF, Sim MS, Irie RF, Hausmann S, Raum T, Baeuerle PA, Morton DL. Redirected Lysis of Human Melanoma Cells by a MCSP/CD3bispecific BiTE Antibody That Engages Patient-derived T Cells. J Immunother. 2011 Oct; 34(8): 597-605. 199. Trefzer U, Herberth G, Wohlan K, Milling A, Thiemann M, Sherev T, Sparbier K, Sterry W, Walden P. Vaccination with hybrids of tumor and dendritic cells induces tumor-specific 91 T-cell and clinical responses in melanoma stage III and IV patients. International journal of cancer. 2004 Jul 10; 110(5): 730-40. 200. Triozzi PL, Aldrich W, Allen KO, Carlisle RR, LoBuglio AF, Conry RM. Phase I study of a plasmid DNA vaccine encoding MART-1 in patients with resected melanoma at risk for relapse. J Immunother. 2005 Jul-Aug; 28(4): 382-8. 201. Tuettenberg A, Becker C, Huter E, Knop J, Enk AH, Jonuleit H. Induction of strong and persistent MelanA/MART-1-specific immune responses by adjuvant dendritic cell-based vaccination of stage II melanoma patients. International journal of cancer. 2006 May 15; 118(10): 2617-27. 202. Tuettenberg A, Schmitt E, Knop J, Jonuleit H. Dendritic cell-based immunotherapy of malignant melanoma: success and limitations. J Dtsch Dermatol Ges. 2007 Mar; 5(3): 190-6. 203. Valmori D, Fonteneau JF, Lizana CM, Gervois N, Lienard D, Rimoldi D, Jongeneel V, Jotereau F, Cerottini JC, Romero P. Enhanced generation of specific tumorreactive CTL in vitro by selected Melan-A/MART-1 immunodominant peptide analogues. Journal of immunology. 1998 Feb 15; 160(4): 1750-8. 204. van der Bruggen P, Van den Eynde BJ. Processing and presentation of tumor antigens and vaccination strategies. Curr Opin Immunol. 2006 Feb; 18(1): 98-104. 205. Vignard V, Lemercier B, Lim A, Pandolfino MC, Guilloux Y, Khammari A, Rabu C, Echasserieau K, Lang F, Gougeon ML, Dreno B, Jotereau F, Labarriere N. Adoptive transfer of tumor-reactive Melan-A-specific CTL clones in melanoma patients is followed by increased frequencies of additional Melan-A-specific T cells. Journal of immunology. 2005 Oct 1; 175(7): 4797-805. 206. Viguier M, Lemaitre F, Verola O, Cho MS, Gorochov G, Dubertret L, Bachelez H, Kourilsky P, Ferradini L. Foxp3 expressing CD4+CD25(high) regulatory T cells are overrepresented in human metastatic melanoma lymph nodes and inhibit the function of infiltrating T cells. Journal of immunology. 2004 Jul 15; 173(2): 1444-53. 207. Vilella R, Benitez D, Mila J, Lozano M, Vilana R, Pomes J, Tomas X, Costa J, Vilalta A, Malvehy J, Puig S, Mellado B, Marti R, Castel T. Pilot study of treatment of biochemotherapy-refractory stage IV melanoma patients with autologous dendritic cells pulsed with a heterologous melanoma cell line lysate. Cancer immunology, immunotherapy : CII. 2004 Jul; 53(7): 651-8. 208. Villadangos JA, Heath WR, Carbone FR. Outside looking in: the inner workings of the cross-presentation pathway within dendritic cells. Trends in Immunology. 2007 Feb; 28(2): 45-7. 209. Villanueva J, Herlyn M. Melanoma and the tumor microenvironment. Curr Oncol Rep. 2008 Sep; 10(5): 439-46. 210. Völkl S, Moore TV, Rehli M, Nishimura MI, Mackensen A, Fischer K. Characterization of MHC class-I restricted TCRalphabeta+ CD4- CD8- double negative T cells recognizing the gp100 antigen from a melanoma patient after gp100 vaccination. Cancer immunology, immunotherapy : CII. 2009 May; 58(5): 709-18. 92 211. Wach F, Eyrich AM, Wustrow T, Krieg T, Hein R. Comparison of migration and invasiveness of epithelial tumor and melanoma cells in vitro. J Dermatol Sci. 1996 Jun; 12(2): 11826. 212. Wang F, Bade E, Kuniyoshi C, Spears L, Jeffery G, Marty V, Groshen S, Weber J. Phase I trial of a MART-1 peptide vaccine with incomplete Freund's adjuvant for resected high-risk melanoma. Clin Cancer Res. 1999 Oct; 5(10): 2756-65. 213. Weber J. Overcoming immunologic tolerance to melanoma: targeting CTLA-4 with ipilimumab (MDX-010). Oncologist. 2008; 13 Suppl 4: 16-25. 214. Wei Y, Sticca RP, Holmes LM, Burgin KE, Li J, Williamson J, Evans L, Smith SJ, Stephenson JJ, Wagner TE. Dendritoma vaccination combined with low dose interleukin-2 in metastatic melanoma patients induced immunological and clinical responses. Int J Oncol. 2006 Mar; 28(3): 585-93. 215. Wolf E, Hofmeister R, Kufer P, Schlereth B, Baeuerle P. BiTEs: bispecific antibody constructs with unique anti-tumor activity. Drug Discovery Today. 2005; 10(18): 1237-44. 216. Wyatt R, Kwong PD, Desjardins E, Sweet RW, Robinson J, Hendrickson WA, Sodroski JG. The antigenic structure of the HIV gp120 envelope glycoprotein. Nature. 1998 Jun 18; 393(6686): 705-11. 217. Yang J, Price MA, Neudauer CL, Wilson C, Ferrone S, Xia H, Iida J, Simpson MA, McCarthy JB. Melanoma chondroitin sulfate proteoglycan enhances FAK and ERK activation by distinct mechanisms. J Cell Biol. 2004 Jun 21; 165(6): 881-91. 218. Yee C, Thompson JA, Byrd D, Riddell SR, Roche P, Celis E, Greenberg PD. Adoptive T cell therapy using antigen-specific CD8+ T cell clones for the treatment of patients with metastatic melanoma: in vivo persistence, migration, and antitumor effect of transferred T cells. Proc Natl Acad Sci U S A. 2002 Dec 10; 99(25): 16168-73. 219. Yuan J, Ku GY, Gallardo HF, Orlandi F, Manukian G, Rasalan TS, Xu Y, Li H, Vyas S, Mu Z, Chapman PB, Krown SE, Panageas K, Terzulli SL, Old LJ, Houghton AN, Wolchok JD. Safety and immunogenicity of a human and mouse gp100 DNA vaccine in a phase I trial of patients with melanoma. Cancer Immun. 2009; 9: 5. 220. Ziegler H, Stabenow R, Holleczek B, Stegmaier C. Krebs im Saarland. Saarbrücken. Ministerium für Justiz, Arbeit, Gesundheit und Soziales, Saarland; 2008. 93 7 Abkürzungsverzeichnis °C Grad Celsius 51 51 Cr Chrom Ag Antigen AIDS Acquired Immune Deficiency Syndrome AJCC American Joint Committee on Cancer ALL Akute lymphatische Leukämie APC Allophycocyanine (Fluorochrom) APC (Zelle) Antigen presenting cell, Antigenpräsentierende Zelle APM Antigen-Prozessierungs-Maschinerie BiTE Bispecific T Cell Engager Bq Becquerel CD Cluster of differentiation CDK Cyclin-Dependent Kinase cDNA Complementary deoxyribonucleic acid, komplementäre Desoxyribonukleinsäure Ci Curie Co Control, Kontrolle CTL Cytotoxischer T-Lymphozyt CTLA Cytotoxic T-lymphocyte antigen d Day, Tag DC Dendritic cell, Dendritische Zelle DMSO Dimethylsulfoxid DN Doppelt Negative T-Zelle dNTP Desoxynukleotidtriphosphat E Effektor EBV Epstein Barr Virus EDTA Ethylendiamintetraacetat ELISA Enzyme linked immunosorbent assay EpCAM Epithelial cell adhesion molecule, Epitheliales Zelladhäsionsmolekül FACS Fluorescence activated cell sorting FAS-L FAS-Ligand 94 Fc Fragment, crystallizable FCS Fetal calf serum, Fötales Kälberserum FITC Fluorothioisocyanat Foxp3 Forkhead box protein p3 FSC Forward Scatter, Vorwärts-Streulicht g Gramm g* Erdbeschleunigung GM-CSF Granulocyte macrophage-colony stimulating factor gp Glycoprotein Gy Gray h Hour, Stunde HLA Human leukocyte antigen, Humanes Leukozytenantigen ic Intrazellulär ICD International Classification of Diseases, Internationale Klassifikation der Krankheiten Ig Immunglobulin IL Interleukin KLH Keyhole Limpet Hemocyanin l Liter LMP Low molecular mass protein M Molar (mol/l) m Meter mAb Monoclonal Antibody, Monoklonaler Antikörper MCSP Melanoma chondroitin sulfate proteoglycan mDC Mature dendritic cell, gereifte dendritische Zelle MHC Major histocompatibility complex, Haupthistokompatibilitätskomplex MNC Mononuclear cell, Mononukleäre Zelle MRD Minimal Residual Disease PBMC Peripheral Blood Mononuclear Cell PBS Phosphate buffered saline, Phosphatgepufferte Salzlösung PD-1 Programmed death-1 PD-L1 Programmed death-ligand 1 PE Phycoerythrine PeCy7 Phycoerythrine Cyanine Dye 7 95 PerCP Peridin-Chlorophyll-Protein PHA Phytohämagglutinin PSMB8 Proteasome subunit beta type 8 qPCR Quantitative polymerase chain reaction, Quantitative Polymerase- Kettenreaktion RNA Ribonucleic acid, Ribonukleinsäure RPMI Roswell Park Memorial Institut RT Raumtemperatur S Svedberg s Sekunde scFv Single chain variable fragment SD Standard deviation, Standardabweichung SSC Side Scatter, Seitwärts-Streulicht T Target, Ziel TAA Tumorassoziiertes Antigen TAP Transporter associated with antigen processing, Antigenpeptid Transporter TCGF T cell growth factor, T Zell Wachstumsfaktor TCR T cell receptor, T-Zell Rezeptor TIL Tumorinfiltrating Lymphocyte, Tumorinfiltrierender Lymphozyt Treg Regulatorische T-Zelle U Unit, Einheit UK United Kingdom, Vereinigtes Königreich USA United States of America, Vereinigte Staaten von Amerika UV Ultraviolett ZL Zelllinie ZNS Zentrales Nervensystem 96 8 Danksagung • Mein besonderer Dank gilt meinem Doktorvater Prof. Dr. Andreas Mackensen für die Aufnahme in seine Arbeitsgruppe, für das Vertrauen, das er in mich gesetzt hat, für die kontinuierliche fachliche Begleitung meiner Arbeit sowie seine Hilfsbereitschaft bei Fragen und Problemen. Durch seine freundliche und verständnisvolle Art und Weise hat er wesentlich zur Entstehung, Durchführung und Fertigstellung dieser Arbeit beigetragen. • Bei Prof. Dr. Falk Nimmerjahn und Prof. Dr. Thomas Winkler möchte ich mich dafür bedanken, dass sie mir im Rahmen meines IZKF- Doktorandenstipendiums als zusätzliche Betreuer zur Seite gestanden sind. • Ein riesengroßes „Dankeschön“ gilt meinem Betreuer Dr. Michael Aigner (Mike) für die engagierte Begleitung meiner Arbeit während all ihrer Phasen. Dafür, dass er sich durch meine unzähligen (!) Fragen nicht aus der Ruhe hat bringen lassen und für die Freiräume, die er mir bei der Durchführung der Arbeit gelassen hat - mir gleichzeitig jedoch bei Fragen und Problemen jeglicher Art immer zur Seite gestanden ist. • Bei Steff bedanke ich mich für ihre nette Art und Weise wie sie mir die Arbeit im Labor „von der Pipette auf“ beigebracht hat, ihrer Hilfe bei der praktischen Umsetzung der Versuche & Experimente und ihrer Geduld wenn ich mal wieder nicht weiter wusste („Ich hab da mal ne Frage...“). • Danke sagen möchte ich auch Barbara, Kerstin, Steffi und Thea für ihre „helfenden Hände“. • Außerdem bedanke ich mich bei Alex, Co, Heiko, Jonas, Julian, Kathrin, Katrin, Regina, Sam, Sabine und allen anderen, die im Labor zur guten Stimmung und netten Atmosphäre beigetragen haben. • Dem IZKF Erlangen möchte ich für die Aufnahme in das Doktorandenprogramm, der damit verbundenen finanziellen Förderung, der Teilnahme an Kursen und Seminaren sowie der zusätzlichen Betreuung danken. • Last but not least danke ich meinen Eltern Helmut und Marianne, meinem Bruder Christoph und meiner Freundin Julie dafür, dass sie mich stets unterstützt und begleitet haben und immer für mich da sind und waren! Vielen Dank.