1 Einleitung
Werbung

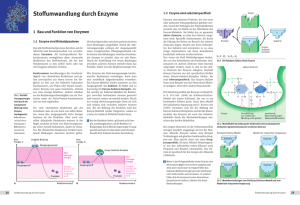
1 Einleitung Nach Schätzungen der Weltgesundheitsorganisation sind weltweit 2 Milliarden Menschen mit dem Tuberkuloseerreger infiziert und 20 Millionen erkrankt. Jährlich gibt es rund neun Millionen Neuinfektionen und ungefähr 1.6 Millionen Menschen sterben an den Folgen der Krankheit [1]. Der Tuberkuloseerreger Mycobacterium tuberculosis, welcher 1882 von dem deutschen Arzt Robert Koch entdeckt wurde, ist ein obligat aerobes, langsam wachsendes, grampositives Stäbchen der Familie der Mycobacteriaceae. M. tuberculosis ist der häufigste Erreger von Tuberkuloseinfektionen beim Menschen und H37Rv ist der am besten untersuchte Stamm in der Tuberkuloseforschung. Die deutliche Zunahme an Tuberkuloseerkrankungen und die steigende Anzahl an multiresistenten Stämmen macht die Suche nach neuen Antituberkulotika dringend erforderlich. Durch die Sequenzierung des mykobakteriellen Genoms im Jahre 1998 ergaben sich völlig neue Ansatzpunkte zur Entwicklung von neuen Medikamenten [2]. Hinsichtlich der Entwicklung neuer Antituberkulotika sind solche Enzyme von Interesse, die im Menschen nicht vorkommen. Einige dieser potentiellen Zielproteine gehören in die Klasse der Thiamindiphosphat (ThDP)-abhängigen Enzyme, von denen 15 im mykobakteriellen Genom identifiziert werden können (Tabelle A.1). Abb. 1.1: Struktur von ThDP ThDP besteht aus einer Diphosphatgruppe und zwei aromatischen Ringsystemen, einem Aminopyrimidin- und Thiazoliumring, die über eine Methylengruppe miteinander verbunden sind. Das mit einem * gekennzeichnete C2-Atom des Thiazoliumrings stellt das Reaktionszentrum des Cofaktors dar [3, 4]. Im enzymgebundenen Zustand ist der Cofaktor in der sogenannten V-Konformation (Drehwinkel φT ≈ ± 90°, φP ≈ ± 90°) stabilisiert [5, 6, 7], in welcher die 4’-Aminogruppe des Aminopyrimidinrings und das C2-Atom des Thiazoliumrings in räumlicher Nähe zueinander positioniert sind. ThDP-abhängige Enzyme katalysieren in Gegenwart von zweiwertigen Metallionen die Spaltung und Bildung von C-C-Bindungen. Ihr Cofaktor (siehe Abbildung 1.1) ist die 1 Einleitung 2 biologisch aktive Form des wasserlöslichen Vitamin B1 (Thiamin). ThDP-abhängige Enzyme gehören verschiedenen Enzymklassen an (Lyasen, Transferasen und Oxidoreduktasen) und haben eine bedeutende Rolle in zentralen Stoffwechselwegen. Im Folgenden wird insbesondere auf die ThDP-abhängigen Carboxylyasen (EC 4.1.1.) eingegangen, welche die nichtoxidative Decarboxylierung von α-Ketosäuren zu Aldehyden katalysieren. Abb. 1.2: Schematische Darstellung des Katalysezyklus ThDP-abhängiger Carboxylyasen. Erklärungen siehe Text. Schema modifiziert nach [8, 9]. 1 Einleitung 3 Der Katalysemechanismus der ThDP-abhängigen Carboxylyasen umfasst vier Reaktionsschritte (siehe Abbildung 1.2). Der initiale Schritt im katalytischen Zyklus ist die Aktivierung des Cofaktors. Dabei führt die Wechselwirkung eines konservierten Glutamatrestes im aktiven Zentrum mit dem N1’-Atom des Pyrimidinrings des ThDP zur Bildung der iminotautomeren Form des Cofaktors, welche, begünstigt durch die V-Konformation, das Proton vom C2-H-Atom abstrahiert. Das bei der Cofaktoraktivierung gebildete reaktive C2-Carbanion des Thiazoliumrings greift nachfolgend das Cα-Atom des Substrates (α-Ketosäure) an und es entsteht das erste kovalent gebundene tetrahedrale Reaktionsintermediat (I1 ). Im folgenden Schritt kommt es zur Decarboxylierung und zur Ausbildung des zweiten kovalenten Reaktionsintermediates, einem resonanzstabilisierten Carbanion/Enamin-Intermediat (I2 ). Die Protonierung des α-Carbanions führt zur Aldehydabspaltung und das verbleibende Carbanion des Cofaktors kann im nächsten Zyklus erneut mit einem Substratmolekül reagieren. Für weitere Informationen über die Wirkungsweise von Carboxylyasen und anderen ThDP-abhängigen Enzymen sei auf die Übersichtsartikel von Kluger [10], Schowen [11], Schellenberger [12] und Jordan [13] verwiesen. Abb. 1.3: Einteilung ThDP-abhängiger Carboxylyasen nach deren verschiedenen physiologischen Bedeutungen im Stoffwechsel. 1 Einleitung 4 ThDP-abhängige Enzyme, die die nichtoxidative Decarboxylierung von α-Ketosäuren zu Aldehyden katalysieren, werden in der ENZYME-Datenbank [14] in Pyruvatdecarboxylasen (BFD, EC 4.1.1.7), vatdecarboxylasen (PDC, EC 4.1.1.1), Oxalyl-CoA-Decarboxylasen (PPDC, EC 4.1.1.43), Benzoylformiatdecarboxylasen (EC 4.1.1.8), Phenylpyru- Indolpyruvatdecarboxylasen (IPDC, EC 4.1.1.71), Verzweigtketten-α-Ketosäuredecarboxylasen (BCDC, EC 4.1.1.72), 5-Guanidino-2-Oxopentanatdecarboxylasen (EC 4.1.1.75), Sulfopyruvatdecar- boxylasen (EC 4.1.1.79) und Phosphonopyruvatdecarboxylasen (EC 4.1.1.82) untergliedert. Diese Einteilung beruht auf der unterschiedlichen beobachteten Substratspezifität dieser Enzyme, die deren verschiedene physiologische Bedeutung im Stoffwechsel widerspiegelt (Abbildung 1.3). Pyruvatdecarboxylasen sind Schlüsselenzyme in der alkoholischen Gärung und katalysieren die Decarboxylierung von Pyruvat zu Acetaldehyd [15]. Der entstehende Acetaldehyd dient als Elektronenakzeptor für die in der Glykolyse oder im Entner-Doudoroff-Weg gebildeten Reduktionsäquivalente (NADH). Dadurch können Mikroorganismen auch unter anaeroben Bedingungen weiterhin Glucose zur Abdeckung ihres Energiebedarfs abbauen (siehe Abbildung 1.4). Den Indolpyruvatdecarboxylasen und den Phenylpyruvatdecarboxylasen wird eine Schlüsselrolle in der Biosynthese der Pflanzenhormone Indolessigsäure und Phenylessigsäure zugeschrieben, welche sich von den Aminosäuren Tryptophan und Phenylalanin ableiten [16, 17] (siehe Abbildung 1.4). Die Verzweigtketten-α-Ketosäuredecarboxylasen zeichnen sich durch die Umsetzung eines breiten Substratspektrums aus. Neben α-Ketosäuren, die sich von den verzweigtkettigen Aminosäuren ableiten (Leucin, Isoleucin und Valin), werden auch aromatische α-Ketosäuren decarboxyliert [18, 19]. α-Ketosäuredecarboxylasen mit breitem Substratspektrum sind Schlüsselenzyme im Ehrlichweg (siehe Abbildung 1.4) [20, 21, 22]. Der Ehrlichweg ist eine Form des Aminosäureabbaus und ermöglicht den Mikroorganismen unter Stickstoffmangelbedingungen ihren Stickstoffbedarf durch den Abbau von Aminosäuren, welche im umgebenden Medium vorliegen, zu decken [23]. Der erste Schritt dieses Stoffwechselweges ist die Transaminierung der Aminosäure zur entsprechenden α-Ketosäure. Im nachfolgenden Schritt wird diese durch eine ThDP-abhängige α-Ketosäuredecarboxylase zum entsprechenden Aldehyd decarboxyliert und in Abhängigkeit vom Redoxstatus der Zelle zu den sogenannten Fuselalkoholen oder Fuselsäuren reduziert bzw. oxidiert. In einigen thermophilen Mikroorganismen (Pyrococcus furiosus, Thermococcus litoralis) wird die nichtoxidative Decarboxylierung von α-Ketosäuren zu Aldehyden durch Ferredoxin-abhängige Oxidoreduktasen katalysiert (IPFOR - Indolpyruvat-Ferredoxin-Oxidoreduktase, VFOR - α-Ketoisovaleriat- 1 Einleitung 5 Ferredoxin-Oxidoreduktase, KGFOR - α-Ketoglutarat-Ferredoxin-Oxidoreduktase) (Abbildung 1.4, gestrichtelte Linie) [24, 25]. Diese Reaktion findet jedoch, verglichen mit der ebenfalls durch diese Enzyme katalysierten oxidativen Decarboxylierung von α-Ketosäuren zu Acyl-CoA-Derivaten, in geringerem Maße statt [26]. Abb. 1.4: Schematische Darstellung der alkoholischen Gärung und des Ehrlichwegs. (A) Die alkoholische Gärung von Pyruvat zu Ethanol wird durch Pyruvatdecarboxylasen (1) und Alkoholdehydrogenasen (2) katalysiert. Für einige thermophile Organismen ist beschrieben, dass die Decarboxylierung von Pyruvat zu Acetaldehyd in geringem Maße auch durch Pyruvat-Ferredoxin-Oxidoreduktasen (PFOR) katalysiert wird [27, 26]. (B) Am Aminosäureabbau über den sogenannten Ehrlichweg sind Aminotransferasen (1), ThDP-abhängige α-Ketosäuredecarboxylasen (2), Alkoholdehydrogenasen (3) und Aldehydoxidasen (4) beteiligt. Letztere oxidieren Aldehyde unter Reduktion eines Elektronenakzeptors zu den entsprechenden Säuren. Für einige Endprodukte des Ehrlichwegs, die sich von Tryptophan und Phenylalanin ableiten, ist bekannt, dass sie als Pflanzenhormone wirken. Der Ehrlichweg, welcher auch häufig als Aminosäuregärung bezeichnet wird, ist am umfangreichsten an Hefen untersucht worden [21, 22, 28]. Vulharan et al. zeigten, dass S. cerevisiae in Anwesenheit der Aminosäuren Leucin, Methionin und Phenyl- 1 Einleitung 6 alanin den Transkriptionslevel des Gens aro10, das für die ThDP-abhängige α-Ketosäuredecarboxylase Aro10 codiert, erhöhen, während die Transkriptionsniveaus der Gene anderer ThDP-abhängiger Decarboxylasen (PDC1, PDC5, PDC6, THI3) nahezu unverändert blieben. Da sich jedoch eine schlechte Korrelation zwischen der Transkriptmenge und der im zellfreien Extrakt gemessenen Aro10-Aktivität zeigte [28, 21], wurde postuliert, dass die Enzymaktivität von Aro10 nicht nur primär über die Transkriptrate und damit über die Enzymmenge, sondern zusätzlich auch durch einen posttranskriptionellen Mechanismus reguliert wird. Transkriptionelle und posttranskriptionelle Mechanismen zur Regulation der Enzymaktivität sind auch für die meisten Pyruvatdecarboxylasen und die Phenylpyruvatdecarboxylase aus Azospirillum brasilense (AbPPDC) beschrieben. Es konnte gezeigt werden, dass die Transkription der Gene, welche für die PDC aus Kluyveromyces lactis (KlPDC) und die AbPPDC codieren, durch geringe Sauerstoffkonzentrationen und Glucose bzw. das Auxin Indolessigsäure, induziert werden [29, 30, 31, 32]. Außerdem wurde gezeigt, dass beide Enzyme allosterisch durch ihre Substrate Pyruvat (KlPDC) [33] bzw. Indolpyruvat (AbPPDC) [34] reguliert werden. Somit können sowohl Pyruvatdecarboxylasen, als auch ThDP-abhängige α-Ketosäuredecarboxylasen die eine Rolle im Aminosäureabbau spielen, in nichtregulierte und allosterisch regulierte Enzyme untergliedert werden (Tabelle 1.1). Tab. 1.1: Untergliederung von Pyruvatdecarboxylasen und am Aminsäureabbau beteiligter α-Ketosäuredecarboxylasen in nichtregulierte und substrataktivierte Enzyme. Pyruvatdecarboxylasen α-Ketosäuredecarboxylasen beteiligt im Aminosäureabbau nichtreguliert Zymomonas mobilis (ZmPDC) [35] nichtreguliert Indolpyruvatdecarboxylase aus Enterobacter cloacae (EcIPDC) [36] α-Ketosäuredecarboxylase aus Lactococcus lactis (KdcA) [19] substrataktiviert Saccharomyces cerevisae (ScPDC) [37] Kluyveromyces lactis (KlPDC) [33] Pisum sativum (PsPDC) [38] substrataktiviert Phenylpyruvatdecarboxylase aus Azospirillum brasilense (AbPPDC) [34] Während eine Regulation auf Transkriptionsebene eine energieaufwendige und zeitlich gesehen eine langsame aber langanhaltende Regulationsmöglichkeit darstellt, kann durch die allosterische Regulation durch das Substrat eine schnelle 1 Einleitung 7 Anpassung der Enzymaktivität auf sich ändernde Bedingungen erreicht werden. Die kinetischen und strukturellen Ursachen der Substrataktivierung wurden in den letzten Jahren ausführlichst an Pyruvatdecarboxylasen aus Hefen untersucht. Die allosterische Regulation von ThDP-abhängigen Carboxylyasen durch ihre Substrate äußert sich in einer sigmoiden Abhängigkeit der katalytischen Aktivität von der Substratkonzentration, was erstmals 1969 für die PDC aus Weizensamen [39] und wenig später auch für die PDC aus Hefe beschrieben wurde [40, 41, 42]. Dieses Verhalten bezeichnet man als Substrataktivierung, welches eine Form der homotropen Kooperativität ist und in den vergangenen Jahrzehnten für weitere Pyruvatdecarboxylasen und andere ThDP-abhängige Carboxylyasen, wie die AbPPDC [34], nachgewiesen wurde. Die umfangreichsten Untersuchungen zur Substrataktivierung wurden an der ScPDC durchgeführt. 1970 zeigten Hübner et al., dass α-Ketosäureamide nicht durch die ScPDC umgesetzt werden, jedoch in der Lage sind dieses Enzym zu aktivieren, was sich im Übergang der sigmoiden v/S-Charakteristik in eine hyperbole Abhängigkeit widerspiegelt [42]. Weitere Einblicke in den Aktivierungsmechnismus der ScPDC wurden 1978 durch den Einsatz von stopped-flow-Techniken erlangt [37]. Es konnte erstmals gezeigt werden, dass die Progresskurven lag-Phasen aufweisen, welche nach einer Präinkubation mit dem Aktivator Pyruvamid nicht mehr beobachtet werden und dass die Geschwindigkeitskonstanten der Aktivierung eine hyperbole Abhängigkeit von der Substratkonzentration zeigen [37]. Ausgehend von diesen Beobachtungen wurde ein kinetisches Modell der Substrataktivierung der ScPDC aufgestellt. Dieses wurde 1991 von Alvarez et al. erweitert [43] und ist bis heute akzeptiert (Abbildung 1.5). Abb. 1.5: Kinetisches Modell der substrataktivierten ScPDC nach [43]. Enzymspezies sind mit E bezeichnet, wobei die Indizes „i“ und „a“ inaktive Enzymspezies und aktive Enzymspezies kennzeichnen. Substrate sind mit S bezeichnet und sind wenn sie links bzw. rechts neben den Enzymspezies geschrieben sind, in der regulatorischen Bindungsstelle bzw. im aktiven Zentrum des Enzyms gebunden. Isomerisierungsschritte (k iso und k −iso ) sind im Vergleich zu Substratbindungsschritten (K A , K M ) sehr langsam. Die Reaktionsprodukte (Aldehyd, CO2 ) sind mit P gekennzeichnet. 1 Einleitung 8 Das Modell beschreibt die schnelle Bindung eines Substratmoleküls in der regulatorischen Bindungsstelle des Enzyms, was einen langsamen Isomerisierungsschritt einer inaktiven in eine aktive Enzymform induziert. Es wurde postuliert, dass dieser langsame Isomerisierungsschritt mit einer konformationellen Änderung des Enzyms einhergeht [44, 45]. Ein alternatives Modell der Substrataktivierung der ScPDC von Sergienko und Jordan schlägt die Existenz von verschiedenen aktivierten Enzymspezies vor [46, 47]. Durch H/D-Austauschexperimente konnte gezeigt werden, dass die Aktivierung der ScPDC mit einer deutlichen Beschleunigung der initialen Cofaktoraktivierung (Ylidbildung) verbunden ist [48]. Wenngleich die kinetischen Aspekte der Aktivierung der ScPDC aufgeklärt wurden, existieren verschiedene Vorstellungen über die strukturellen Ereignisse, die zur Aktivierung führen. Bereits vor dem Bekanntwerden dreidimensionaler Strukturen substrataktivierter Pyruvatdecarboxylasen konnte mit SH-Gruppen-spezifischen Modifizierungsreagenzien gezeigt werden, dass Thiolgruppen einen entscheidenden Einfluss auf die katalytischen und Aktivierungseigenschaften der ScPDC besitzen [49, 50]. Jordan und Mitarbeiter führten basierend auf diesen Ergebnissen umfangreiche Mutationsstudien durch und postulierten einen Informationstransfer vom regulatorischen Zentrum zum Pyrimidinring des Cofaktors, welcher über mehrere Aminosäureseitenketten des Enzyms vermittelt wird [51, 52, 53, 54, 55, 56]. Für das 20 Å vom aktiven Zentrum entfernte Cys221 wurde eine entscheidene Rolle in der Substrataktivierung der ScPDC beschrieben. Die kovalente Bindung eines Pyruvatmoleküls an die Thiolgruppe des Cys221-Restes (Thiohemiketalbildung) soll den Startpunkt eines Signalübertragungswegs darstellen, der über die Aminosäurereste His92, Glu91, Trp412 und Teile eines loops bis in das aktive Zentrum des Enzyms führt. Diese Wechselwirkung zwischen der regulatorischen Bindungsstelle und dem aktiven Zentrum resultiert in der Ausbildung der iminotautomeren Form des ThDP, welche an der C2H-Abstraktion beteiligt ist. Ein alternatives Modell von König und Mitarbeitern schlägt vor, dass das strukturelle Ereigniss der Aktivierung der ScPDC in einer globalen Änderung der Dimeranordnung liegt, was zur Stabilisierung zweier loop-Regionen über dem aktiven Zentrum führt. Dieses Modell beruht auf der Tatsache, dass in der Röntgenkristallstruktur der aktiverten ScPDC der artifizielle Aktivator Pyruvamid nicht kovalent an das Cys221, sondern 10 Å von diesem entfernt, gebunden ist [57]. Ein Vergleich der Kristallstrukturen von nichtaktivierter und Pyruvamid-aktiverter ScPDC zeigt, dass die Aktivierung mit einer Verdrehung der katalytisch aktiven Dimere im Tetramer verbunden ist und es dadurch zum Übergang eines symmetrischen in einen asymmetrischen Te- 1 Einleitung 9 tramer kommt (Abbildung 1.6). Dieser Übergang resultiert in der Ausbildung neuer Dimer-Dimer-Wechselwirkungen und führt zur Strukturierung zweier loop-Regionen (Aminosäure 104-113 und 290-304), welche in der nichtaktivierten Form flexibel sind. Die Strukturierung dieser loop-Regionen über dem aktiven Zentrum schirmt dieses vom umgebenden Milieu ab (Lösungsmittelausschluss) und ermöglicht so die Katalyse. Die globalen strukturellen Änderungen während der Aktivierung der ScPDC wurden auch in Lösung nachgewiesen, wie die aus Röntgenkleinwinkelstreuexperimenten berechneten niedrig aufgelösten Strukturen zeigten [58]. Abb. 1.6: Vergleich der Quartärstrukturen von aktivierten und nichtaktivierten Zuständen der ScPDC und AbPPDC. Die Kristallstrukturen der nichtaktivierten ScPDC (1PVD) und der Pyruvamid-aktivierten ScPDC (1QPB) sind links, die Kristallstrukturen der nichtaktivierten AbPPDC (2NXW) und der mit Phenylpyruvat aktivierten AbPPDC (2Q5O) rechts dargestellt. Die oberen (A) und die unteren Abbildungen (B) zeigen die um jeweils 90° um die x-Achse gedrehte Orientierung der Kristallstrukturen. Die funktionellen Dimere im Tetramer sind verschiedenfarbig und die Cofaktoren (ThDP bzw. 3-Deaza-ThDP) als Kalottenmodell dargestellt. Auch die kürzlich gelösten Kristallstrukturen von nichtaktivierten und aktivierten Zuständen der AbPPDC zeigen, dass die Bindung von Substrat in der regulatorischen Bindungsstelle der AbPPDC zu globalen strukturellen Änderungen führt [59, 60]. Vergleicht man die Strukturen der AbPPDC mit denen der ScPDC fällt auf, dass die Aktivierung der AbPPDC mit dem Übergang eines asymmetrischen zu einem symmetrischen Tetramer verbunden ist und somit den entgegengesetzten Übergang während der ScPDC-Aktivierung darstellt (Abbildung 1.6). Jedoch ist auch die Aktivierung der AbPPDC mit der Strukturierung eines loops (Aminosäuren 104-120) 1 Einleitung 10 bzw. Verschiebung eines zweiten loops (Aminosäuren 280-294) über dem aktiven Zentrum verbunden. Globale strukturelle Änderungen, welche zur Strukturierung von loop-Regionen und zur Abschirmung des aktiven Zentrums führen, scheinen somit ein gemeinsames Merkmal der Aktivierung beider Enzyme zu sein. Während die soeben beschriebene Aktivierung ThDP-abhängiger Decarboxylasen durch ihr Substrat eine homotrope Kooperativität darstellt, sind für ThDP-abhängige Carboxylyasen auch heterotrope Mechanismen der Aktivierung bekannt. Die Oxalyl-CoA-Decarboxylase (EC 4.1.1.8) aus Oxalobacter formigens (Ofoxc), welche Oxalyl-CoA zu Formyl-CoA decarboxyliert, wird zum Beispiel durch ADP aktiviert [61]. Die Oxalyl-CoA-Decarboxylasen sind beim anaeroben Abbau von Oxalat von Bedeutung. Oxalat ist eine der am höchsten oxidierten in der Natur vorkommende organische Verbindung und wirkt als starker Chelator für zweiwertige Metallionen. Diese Eigenschaften limitieren dessen Katabolismus und machen Oxalat toxisch für die meisten Tiere, vor allem Säugtiere. Erhöhte Oxalatkonzentrationen im Körper sind verbunden mit verschiedenen Krankheiten wie zum Beispiel Nierensteine (Calciumoxalatsteine) [62]. Da Menschen nicht in der Lage sind Oxalsäure, welche entweder durch die Nahrung aufgenommen wurde (Rhabarber, Spinat, Mangold) bzw. im Zellstoffwechsel entstanden ist, abzubauen, muss diese über den Urin oder den Darm ausgeschieden bzw. durch Darmbakterien wie Oxalobacter formigens aber auch Enterococcus faecaelis [63], Bifdobacterien [64] und Lactobacillen [65] abgebaut werden [66, 67]. Die Fähigkeit dieser darmbewohnenden Mikroorganismen über die Nahrung aufgenommenes Oxalat abzubauen und somit dessen Resorption zu verringern, führt dazu, dass ihnen eine gesundheitsfördernde Wirkung zugeschrieben wird [68, 69]. Am anaeroben Abbau von Oxalat zu Kohlendioxid und Formiat ist neben der OxalylCoA-Decarboxylase (EC 4.1.1.8) auch die Formyl-CoA-Transferase (EC 2.8.3.16) beteiligt. Am besten untersucht ist der anaerobe Oxalatmetabolismus bei dem Darmbakterium Oxalobacter formigens, welches seinen Energiebedarf ausschließlich aus dem Oxalatabbau deckt [70] (siehe Abbildung 1.7). Ein Oxalat-Formiat-Antiporter transportiert zweifach negativ geladenes Oxalat in und einfach negativ geladenes Formiat aus der Zelle [71, 72, 73]. Oxalat wird durch eine Formyl-CoA-Transferase im Austausch gegen Formiat auf Formyl-CoA übertragen [74, 75]. Oxalyl-CoA stellt eine aktivierte Form des Oxalats dar und kann durch die ThDP-abhängige Oxalyl- 1 Einleitung 11 Abb. 1.7: Oxalatmetabolismus in O. formigens In O. formigens ist der Eintritt von zweifach negativ geladenem Oxalat an den Export seines Decarboxylierungsproduktes, des einfach negativ geladenen Formiates, gebunden. Dieser Antiport führt zur Bildung eines negativen Membranpotentials im Zellinneren. Weiterhin kommt es durch die intrazelluläre Decarboxylierung von Oxalat zum Verbrauch eines cytosolischen Protons. Diese beiden Prozesse führen zum Aufbau einer protonenmotorischen Kraft, welche die Synthese von ATP ermöglicht. Schema modifiziert nach [61]. CoA Decarboxylase zu Formyl-CoA decarboxyliert werden. Die Decarboxylierung von Oxalyl-CoA ist mit dem Verbrauch eines Protons verbunden und führt daher in Kombination mit dem elektrogenen Oxalat-Formiat-Antiport zum Aufbau eines Membranpotentials, welches O. formigens zur ATP-Synthese nutzt. Erste kinetische Untersuchungen der Oxalyl-CoA-Decarboxylase aus Oxalobacter formigens (Ofoxc) wurden von Baetz und Allison durchgeführt [76]. Im Jahre 2005 gelang es Berthold et al., die Kristallstruktur der Ofoxc aufzuklären, welche die erste Kristallstruktur einer Oxalyl-CoA-Decarboxylase darstellte [61]. Pro Ofoxc-Monomer ist neben den Cofaktoren ThDP und Magnesium auch ein ADP-Molekül gebunden. Ebensfalls durchgeführte kinetische Analysen zeigten, dass die Ofoxc durch ADP aktiviert und Coenzym A inhibiert wird [61]. Der Regulationsmechanismus der Enzymaktivität durch ADP wird als putative Anpassung der an die Decarboxylierung von Oxalat geknüpften Energiegewinnung interpretiert. In einer erst kürzlich erschienenen Arbeit gelang es, die Substratbindungsstelle zu identifizieren und die Kristallstruktur mit einem kovalent am Cofaktor gebundenen Reaktionsintermediat aufzuklären, was weitere Einblicke in den Katalysemechanismus dieses Enzyms ermöglichte [77]. 1 Einleitung 12 In den Proteindatenbanken S WISSPROT und T REMBL sind 28 Gene beschrieben, für die eine putative Funktion als Oxalyl-CoA-Decarboxylase vorhergesagt wird [78]. Diese zeichnen sich durch eine hohe Sequenzidentität aus (Tabelle A.4). Neben den oben beschriebenen symbiotischen Darmbakterien sind Oxalyl-CoA-Decarboxylasen auch in E. coli [79] und in der Familie der Mycobacteriaceae [78] anzutreffen. In M. tuberculosis ist ein knock-out des Gens rv0118c, welches für die Oxalyl-CoADecarboxylase codiert, letal [80], was das Enzym zum potentiellen Ziel für die Entwicklung von Antituberkulotika macht. Im Genom des Darmbakterium E. coli ist neben der Oxalyl-CoA-Decarboxylase auch ein Gen zu finden, das für eine Formyl-CoA-Transferase codiert [79], obwohl eine Energiegewinnung durch den Abbau von Oxalat bisher für diesen Mikroorganismus nicht beschrieben wurde [81]. Wenngleich die Kristallstruktur der Formyl-CoA-Transferase aus E. coli aufgeklärt wurde [82, 83], sind keine strukturellen und kinetischen Daten der putativen Oxalyl-CoA-Decarboxylase aus E. coli (EcyfdU ) als auch des mykobakteriellen Enzyms bekannt. Ziel der vorliegenden Arbeit war die kinetische und strukturelle Charakterisierung zweier ThDP-abhängiger Carboxylyasen. Der Schwerpunkt der Arbeit lag in der Untersuchung des mykobakteriellen Enzyms, welches durch das Gen rv0853c codiert wird. Aufgrund der Sequenzhomologie wird für dieses Enzym eine putative Funktion als Indolpyruvat- bzw. Pyruvatdecarboxylase vorhergesagt. In kinetischen Experimenten wurde sowohl die Substratspezifität als auch das Aktivierungsverhalten des Enzyms untersucht. Des Weiteren sollte die putative Oxalyl-CoA-Decarboxylase aus M. tuberculosis, welches durch das Gen rv0118c codiert wird, kinetisch und strukturell charakterisiert werden. Da das mykobakterielle Enzym nicht löslich heterolog überexprimiert bzw. enzymatisch aktiv rückgefaltet werden konnte, wurde alternativ das Enzym aus Escherichia coli untersucht (EcyfdU ). Dabei standen vor allem Analysen zur Substratbindung als auch zum Aktivierungsverhalten im Vordergrund.


![[Cr(CN) 6]3](http://s1.studylibde.com/store/data/007896457_1-9f34cb8b8a3dff76b1bab35523cab36a-300x300.png)