Klinische Chemie und Laboratoriumsdiagnostik Teil 11
Werbung
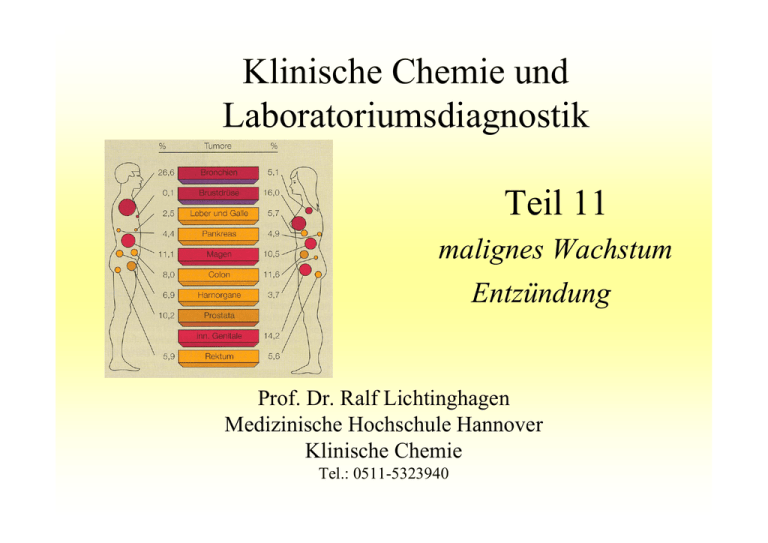
Klinische Chemie und Laboratoriumsdiagnostik Teil 11 malignes Wachstum Entzündung Prof. Dr. Ralf Lichtinghagen Medizinische Hochschule Hannover Klinische Chemie Tel.: 0511-5323940 Tumorentstehung Maligne solide Tumoren ihrer Entstehung nach: Karzinom: epithelial Sarkom: mesenchymal Klassifizierung von Tumoren (TNM-System) T: Ausdehnung des Primärtumors N: Fehlen oder Vorhandensein von regionären Lymphknotenmetastasen M: Fehlen oder Vorhandensein von Fernmetastasen prätherapeutisch und postoperativ (pTNM) Tumorentwicklung und diagnostische Erfassung Metastasierung auch hier schon möglich! Immunologische Methoden zeigen Rezidive u/o Metastasen oft bedeutend früher an (Zeitvorsprung im Durchschnitt 3-6 Monate). Tumormarker:Anforderungen an ideale Marker 1. 100%ige Unterscheidung Gesunder von Tumorkranken 2. Erfassung aller Tumorpatienten, möglichst bereits in einem frühen Stadium 3. Organspezifität, Aussage über Lokalisation des Tumors 4. Korrelation mit Tumorstadien 5. Anzeige aller Veränderungen beim Patienten unter Therapie 6. Prognostische Aussagekraft Screening wäre nur sinnvoll, wenn Punkte 1. und 2. erfüllt sind Die Rede ist hier von humoralen (idealen) Tumormarkern: Nachweis in einer Körperflüssigkeit (z.B.Serum) im Unterschied zu zellulären Tumormarkern: Nachweis histologisch am Tumorgewebe Tumormarker Allgemeine Indikatoren für ein gesteigertes Zellwachstum z.B. S-Thymidinkinase, S-β2-Mikroglobulin Allgemeine Indikatoren für gesteigerten Zellumsatz bzw. Zelluntergang z.B. LDH Charakteristische, manchmal spezifische Sekretionsprodukte von Tumorzellen diverse sogenannte Tumormarker Tumormarker: Was versteht man in der klinischen Realität darunter ? Begriff eigentlich unkorrekt, denn kein sogenannter Tumormarker ist bei Tumoren im Frühstadium immer nachweisbar und beim Gesunden immer negativ. Solche Marker geben auch oft keinen Hinweis auf die Tumorlokalisation. Als Screening-Parameter haben Tumormarker in der Regel keinen Stellenwert! d.h.: keine Messung diverser Tumormarker zum Ausschluss einer eventuell vorhandenen Tumorerkrankung Tumormarker: Marker 1. und 2.Wahl Marker 1. Wahl: Marker 2.Wahl: Tumormarker: Screening, Diagnose, Follow-up Screening (ja oder nein): noch ein Rechenbeispiel dazu: CEA beim kolorektalen Karzinom Inzidenz 37 in 100.000 Spezifität: 95% Sensitivität: 70% Falsch Positive: 4998 Richtig Positive: 26 Tumormarker: Klinische Bedeutung Tumormarkerbestimmung nach erster Therapie (OP, Radio-/Chemotherapie) als Basiswert für gesamte weitere Nachsorge. Radikaloperative Resektion: Abfall des Tumormarkers in den Medianbereich des Referenzintervalles hier liegen die Basiswerte bei 50% der tumorfreien Patienten Hinweis: bei Entfernung eines Organs, das die natürliche Primärquelle des Markers darstellt, sollte der Tumormarkermesswert sogar noch deutlicher abfallen (z.B. Prostata - PSA)! Im weiteren Krankheitsverlauf: Orientierung an individuellen Basiswerten Anstieg: mögliches Rezidiv Auch ein noch im Referenzbereich liegender Tumormarker-Messwert kann „nicht normal“ sein, wenn der individuelle Basiswert zugrunde gelegt wird. Wichtig: Für Kontrolluntersuchungen Beibehaltung des gleichen Testverfahrens und- herstellers (i. d. R. desselben Labors) Tumormarker: Methodenwechsel Minimalverlaufskurve nach erfolgtem Methodenwechsel Werte können nach Wechsel einer Bestimmungsmethode z.T. erheblich voneinander abweichen. Ursache: z.B. Verwendung von Antikörpern gegen unterschiedliche Epitope des gleichen Moleküls Nach Methodenwechsel innerhalb eines Labors empfiehlt sich eine Parallelmessung der Patientenproben für die nächsten 2-3 Bestimmungen (Praktikabilität?) Beispiel: Protatakarzinom (PCA) Tumormarker: PSA (prostataspezifisches Antigen), Referenzbereich: < 4µg/l organspezifisch trotz geringer Bildung in Mamma, Endometrium und anderen malignen Tumoren Wird in der Prostata und den periurethralen Drüsen gebildet spiegelt Größenzunahme der Prostata, entzündliche (Prostatitis) und neoplastische Veränderungen wider. (Halbwertszeit: 2-3 Tage) Einflussgröße außerdem: digital rektale Untersuchung, deshalb PSA-Bestimmung vor Untersuchung Normales PSA schließt PCA nicht aus, PSA > 10 µg/l i.d.Regel PCA Einzelwert im oberen Normbereich nicht aussagekräftig, wichtiger wäre Steilheit des Anstieges im Verlauf (>0,8 µg/l pro Jahr) auf der Grundlage individueller Basiswerte (z.B. im Alter ab 50 Jahre). PSA: komplexierte und freie Form 34 kD großes Glykoprotein mit Serinprotease-Aktivität (Verflüssigung der Samenflüssigkeit) Monomer in Seminalflüssigkeit, bildet im Plasma stabile Komplexe mit Proteinaseinhibitoren (zu 70-90 % mit α1-Antichymotrypsin (ACT), in geringem Maße mit α2-Makroglobulin (hierbei aber Epitop-Verlust im Assay), 10-30% des gesamtes PSA liegen als freies PSA im Plasma vor. Besonderheit: Beim PCA wird häufig ein niedrigerer Prozentsatz des freien PSA bezogen auf das Gesamt-PSA gefunden. Diagnostische Bedeutung für das PCA liegt (bei PSA-Werten von 2-10 µg/l) beim Verhältnis freies PSA/PSA: cut off diag. Sensitivität diag. Spezifität 0,23 90% 63% 0,19 82% 82% 0,15 27% 95% PSA: Indikationen Zur Früherkennung, Therapiekontrolle und Nachsorge des PCA Indiziert: bei jedem Mann im Alter von 50-70 Jahren (z.B. jährlich), bei Männern mit Miktionsbeschwerden nach Ausschluss eines Harnwegsinfektes, nach operativer Entfernung des PCA (Rezidivprophylaxe). PSA-Screening?? Zu bedenken wäre: nicht alle PCA sind im weiteren Verlauf klinisch relevant, Übertherapie deshalb bei manchen Betroffenen, mehr Männer sterben mit einem PCA als an einem PCA, Grenzwert von 4 µg/l nicht ausreichend gesichert, einige hochaggressive Tumoren werden trotzdem nicht erkannt. Fazit: Die PSA-Bestimmung ersetzt nicht die digital rektale Untersuchung, die Kombination aus beiden Parametern steigert die Wahrscheinlichkeit bei verdächtigen Befunden durch Biopsien ein PCA zu sichern Entzündung Zytokine: Botenstoffe Akute Entzündung: Lokale Antwort auf Schädigung von Zellen und Geweben Ziel: Zerstörung und Elimination einer schädigenden Substanz, Reparatur und Heilung des geschädigten Gewebes. Akute-Phase-Reaktion (APR): Entfernte Veränderungen durch lokale Entzündung Chron. Entzündung: Protrahierter Prozess mit persistierender APR Problem: Systemisches Inflammatory response Syndrome (SIRS), Sepsis, Multiorganversagen (MODS) Blutkörperchensenkungsgeschwindigkeit Blutkörperchensenkungsgeschwindigkeit (BKS), Synonyme: Blutsenkung, Blutsenkungsgeschwindigkeit (BSG). Bei verschiedenen Krankheiten beschleunigt sich im antikoagulierten Blut die Senkung der Blutkörperchen. Suchtest nach entzündlichen und malignen Prozessen im Körper. Beeinflussende Faktoren: Proteinzusammensetzung des Plasmas, Ladung und Dicke der Erythrozyten, Plasmaviskosität, Temperatur, Dichteunterschiede zwischen Plasma und Blutzellen. Plasmaproteine: z.B. Fibrinogen, α2-Makroglobulin, Haptoglobin, IgG, IgA wirken steigernd auf die Erthrozytenaggregation Senkungsgeschwindigkeit Viele dieser steigernden Proteine sind Akute-Phase-Proteine Blutkörperchensenkungsgeschwindigkeit Indik.: Ausschluss chronischer immunologischer Erkrankungen Ausschluss maligner Erkrankungen mit systemischer Reaktion Messung aus einer 4+1 Mischung (1,6ml + 0,4 ml) von Blut mit 3,8% Natriumzitrat Referenzbereiche (Ein-Stunden-Wert) Methode nach Westergren Ablesen der Höhe der Plasmaschicht über den Blutzellen (z.B. nach einer und zwei Stunden) Männer (<50 J) <15 mm/h Männer (>50 J) <20 mm/h Frauen (<50 J) <20 mm/h Frauen (>50 J) <30 mm/h bis 50 mm/h deutliche Senkungsbeschleunigung bis 90 mm/h starke Senkungsbeschleunigung ab 90 mm/h Sturzsenkung Blutkörperchensenkungsgeschwindigkeit Einflussgrößen menstrueller Zyklus Schwangerschaft zirkadianer Rhythmus Nahrungseinfluss Medikamente BSG steigt in prämenstrueller Phase an, sinkt während der Menstruation. steigt kontinuierlich ab der 4. SSW, Maximum zur Geburt (ca. 2x URL), Normalbereich nach 6-8 Wochen. BSG ist nachmittags höher als vormittags nach fettreicher Nahrung BSG durch Chylomikronen gesteigert orale Kontrazeptiva (Erhöhung des Fibrinogens) Fazit: Gesteigerte BSG unspezifisches Zeichen einer entzündlichen oder sonst die Proteinzusammensetzung des Blutes verändernden Erkrankung. Kann erstes Symptom einer malignen Erkrankung sein, Sturzsenkung bei monoklonaler Gammopathie. Da BSG unspezifisch: Abklärung durch weitere Untersuchungen Akute-Phase-Proteine APR: entfernt vom Entzündungsherd initiierte systemische Reaktionen, kontrollieren lokalen Entzündungsprozess (Fieber, Leukozytose, APP-Synthese...) APP: Proteine (ca. 30), deren Konzentrationen während einer entzündl. Erkrankung um mehr als 25% ansteigen oder abfallen (neg. Reaktanden). Vorwiegender Stimulus: Interleukin-6, Synthese in Hepatozyten Akute-Phase-Proteine: CRP C-reaktives Protein (CRP) ist als Akute-Phase-Protein an der Elimination toter Zellen beteiligt, bindet an körperfremde Strukturen (Bakterien, Pilze, Parasiten) Indikation: Diagnostik und Verlaufskontrolle akuter Entzündungen infektiöse Komplikationen nach OP Kontrolle infektgefährdeter Patienten Therapiekontrolle (antibiotisch, antiinflammatorisch) Abschätzung des kardiovaskulären Risikos Referenzbereiche Erwachsene <8 mg/l geringes Myokardinfarktrisiko bei Gesunden (rel. Risiko 1.0) erhöhtes Myokardinfarktrisiko bei Gesunden (rel. Risiko 2.9) (Physicians´ Health Study) <0,56 mg/l >2,1 mg/l Akute-Phase-Proteine: CRP Bakterielle/virale Infektion: bakt. Infekte häufig mit einem deutlich höheren CRP-Anstieg (z.B. bakt. Meningitis: >100 mg/l) Post-OP Nach OP CRP häufig 50-150 mg/l, bei höherem^Anstieg oder ausbleibendem Abfall am 3./4. Tag Post-OP: (später) Indikator für Komplikationen Rheum. Erkrankungen Korrelation zwischen Erkrankungsaktivität und CRP (>100 mg/l: schwere Entzündung) Falsch-negativ lokalisierte Entzündung, chronische Entzündung, Virusinfektion SIRS, Sepsis: Kriterien SIRS systemische auf unterschiedlichen Stimuli beruhende Entzündungsreaktion mit mind. zwei der folgenden Symptome Körpertemperatur > 38°C oder < 36°C Herzfrequenz >90/min Atemfrequenz >20/min oder pCO2 >32 mmHg Leukozyten >12x109/l oder < 4x 109/l oder Linksverschiebung Sepsis Zusätzlich ist der Nachweis einer Infektion erforderlich (Erregernachweis im Gewebe/ Blutkultur) Septischer Schock Schwere Sepsis mit persistierender Hypotonie MODS Versagen der Organfunktionen SIRS, Sepsis: Labordiagnostik •Akute Phase Proteine (z.B. CRP) •Zytokine (IL-6, IL-8, TNF-alpha...) Marker einer systemischen bakteriellen Infektion (Sepsis) •Procalcitonin (PCT),Prohormon von Calcitonin, Synthese-Stimulus: bakt. Endotoxine Marker einer bereits lokalen bakteriellen Infektion bei drohender Sepsis •LBP (Lipopolysaccharide (LPS, Endotoxin) binding protein) Therapie, Prognose •Erregernachweis (Blutkultur, PCR) •Genpolymorphismen in Kandidatengenen (TNF, IL-1, IL-6, IL10, HSP, CD-14, TLR-2, TLR-4....) SIRS, Sepsis: Zytokine in der Differentialdiagnostik Messgröße Messwert Interpretation IL-6 sehr guter Parameter für Prognose und Frühdiagnose (im Vgl. zu CRP), rascher Abfall nach erfolgreicher Antibiose Dänisches Adoptionsregister Sorensen et al., N Engl J Med 1988, Auswertung von Todesursachen von Adoptivkindern, deren Adoptiveltern sowie deren leiblichen Eltern: Wenn die leiblichen Eltern <50 Jahre an Infektion starben, hatten die Kinder ein 5,8faches Risiko (2,47-13,7) ebenfalls frühzeitig an einer Infektion zu versterben. Bei kardiovaskulären Ursachen war das Risiko 4,5fach (1,32-15,4) erhöht. Kinder, deren Eltern an Krebs starben, hatten kein erhöhtes Risiko. Kinder, deren Adoptiveltern an einer Krebserkrankung starben, hatten ein 5,16fach (1,32-15,4) erhöhtes Risiko ebenfalls an einer Krebserkrankung zu versterben. GENETISCHER EINFLUSS BZGL. EMPFÄNGLICHKEIT GEGENÜBER INFEKTIONEN ERSTAUNLICH HOCH











