Therapie und Betreuung HIV-infizierter Kinder
Werbung

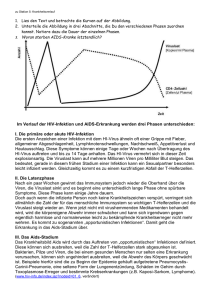
P O L I T I K MEDIZINREPORT 6. Münchner AIDS-Tage Therapie und Betreuung HIV-infizierter Kinder Der Fortschritt in der Therapierbarkeit der HIV-Erkrankung war in den letzten 16 Monaten größer als in den 16 Jahren davor. Vor allem neue Erkenntnisse in der HIV-Replikationsdynamik, die Messung der Viruslast und neue antiretrovirale Kombinationstherapien haben dies bewirkt. Eine Patientengruppe, bei der die neuen Erkenntnisse noch unzureichend in die Behandlungskonzepte eingeflossen sind, sind HIV-infizierte Kinder. In der Euphorie von Viruselimination und Aussicht auf Heilung ist auch das Engagement für opportunistische Infektionen etwas in den Hintergrund getreten. Und die größte Herausforderung, die Entwicklung eines langfristig wirksamen Impfstoffs, bleibt weiterhin bestehen. chungen in den ersten sechs Monaten können praktisch immer klären, ob ein Kind infiziert ist. Als Frühsymptome einer HIVInfektion beobachtet man im Kindesalter besonders häufig Hepatospleno- Foto: List & Partner Verlagsgesellschaft, Wien D ie Häufigkeit einer vertikalen Transmission von HIV liegt heute unter zehn Prozent, und die mittlere Überlebenszeit perinatal infizierter Kinder beträgt acht Jahre. HIV kann auf das Kind in utero, während der Geburt oder beim Stillen übertragen werden. Am häufigsten ist der zweite Weg. Je weiter fortgeschritten das Erkrankungsstadium der Mutter ist, desto höher liegt das Transmissionsrisiko. Auch geburtshilfliche Faktoren spielen eine wichtige Rolle. Die primäre Sectio scheint das Risiko der HIV-Übertragung zu halbieren. Vorzeitiger Blasensprung, Vakuum- oder Zangengeburt erhöhen das Risiko. In einer plazebokontrollierten randomisierten ACTG-Studie nahm das Transmissionsrisiko unter einer Zidovudin-Prophylaxe auf 7,6 Prozent gegenüber 22,6 Prozent ab. Das Medikament wurde dabei während der Schwangerschaft peroral, unter der Geburt intravenös und beim Kind in den ersten sechs Wochen peroral eingesetzt. Welche der drei Therapiephasen den Schutz bringt, ist noch nicht geklärt. Bis zum 18. Lebensmonat kann eine HIV-Infektion nur durch den direkten Virusnachweis gesichert werden, da in diesem Zeitraum noch mütterliche Antikörper zirkulieren. Da auch die PCR in den ersten Lebensmonaten bei nicht infizierten Kindern positiv ausfallen kann, sollten PCR und Antigentest immer parallel durchgeführt werden. Drei Untersu- Für die Wissenschaftler bleibt die Entwicklung einer HIV-Vakzine nach wie vor eine Herausforderung. megalien und generalisierte Lymphadenopathien. Für das Säuglingsalter typische Ekzeme werden verschlimmert, und es treten gehäuft bakterielle Infektionen auf. Eine thrombozytopenische Purpura und ein Herpes zoster sind typische AIDS-Erstmanifestationen, deren Auftreten im Kindesalter immer einen HIV-Test veranlassen sollte. Auch bei einer Hypergammaglobulinämie sollte ein entsprechender Verdacht geklärt wer- A-1990 (26) Deutsches Ärzteblatt 94, Heft 30, 25. Juli 1997 den. Von den opportunistischen Infektionen kommt die Pneumocystiscarinii-Pneumonie (PCP) auch im Kindesalter am häufigsten vor, kann aber schon bei normaler CD4-Zellzahl auftreten. An zweiter Stelle steht die Candida-Ösophagitis. Auch bei Kindern lassen sich in den ersten symptomfreien Jahren kaum Viruspartikel im Plasma nachweisen. In Wirklichkeit werden in dieser Zeit der scheinbaren Latenz in den lymphatischen Geweben massiv Viruspartikel produziert – mit einer Halbwertszeit von gerade sechs Stunden. Der Nachschub an CD4-Zellen vermag jahrelang mit dieser massiven Replikation Schritt zu halten. Die CD4-Zellzahl gibt also nur Aufschluß über den Zustand des Gleichgewichts. Die Dynamik der HIV-Infektion spiegelt sich in der Viruslast wider, die sich inzwischen als wichtigster prognostischer Parameter etabliert hat. Die üblichen Säuglings-Impfungen sollten bei HIV-infizierten Kindern besonders frühzeitig durchgeführt werden, da die Antikörperantwort mit zunehmendem Verlauf der Krankheit immer schwächer wird. Eine Impfung mit dem BCG-Lebendimpfstoff sollte entfallen, und die Polio-Schluckimpfung durch Injektion des inaktivierten Impfstoffs ersetzt werden. Der Masern-Lebendimpfstoff kann dagegen ohne weiteres verabreicht werden. Da auch bei normaler CD4-Zellzahl eine PCP auftreten kann, wird empfohlen, allen Säuglingen von HIVinfizierten Müttern prophylaktisch Cotrimoxazol zu geben. Diese Vorsichtsmaßnahme kann nach sechs Monaten gestoppt werden, wenn bis dahin kein HIV nachzuweisen ist. Von einer – früher routinemäßig gegebenen – Immunglobulin-Prophylaxe profitieren wahrscheinlich nur Kinder, die trotz antiretroviraler Therapie und PCP-Prophylaxe an rezidivierenden bakteriellen Infektionen leiden. Erfahrungen mit nichtnukleosidischen Substanzen und ProteinaseInhibitoren fehlen in der antiretroviralen Therapie bei Kindern noch weitgehend. Deshalb wird für Kinder heute offiziell noch eine Therapie mit ddI alleine oder in Kombination mit Zidovudin empfohlen. Doch auch im Kindesalter korreliert der Erkran- P O L I T I K MEDIZINREPORT kungsverlauf mit der Viruslast, und Kinder weisen oft im ersten Lebensjahr eine besonders hohe Viruslast auf. Es ist deshalb wahrscheinlich, daß Mehrfachkombinationen mit Reverse-Transkriptase-Hemmern und Proteinasehemmern – wie sie bei Erwachsenen mit durchschlagendem Erfolg eingesetzt werden – auch bei Kindern sehr viel wirksamer sind. Opportunistische Infektionen Die antiretrovirale Therapie und opportunistische Infektionen beeinflussen sich gegenseitig, so daß nur eine gemeinsame Betrachtung sinnvoll ist: Durch eine verbesserte antiretrovirale Therapie nimmt die Rate an opportunistischen Infektionen ab, aber auch das Spektrum verändert sich. Umgekehrt können opportunistische Infektionen den Erfolg der antiretroviralen Therapie beeinflussen. Auch nichtfatale opportunistische Infektionen erhöhen die Mortalität der Patienten unabhängig von deren immunologischer Kompetenz. Wahrscheinlich bewirken sie eine Immunaktivierung, die die HIV-Expression und damit die Viruslast steigert. Eine hohe Viruslast kann umgekehrt das Risiko für opportunistische Infektionen unabhängig von der CD4-Zellzahl steigern. Eine Analyse von mehreren ACTG-Studien an insgesamt 721 Patienten zeigte, daß das PCP-Risiko um das Zweifache und das Risiko für eine Zytomegalievirus-Infektion (CMV) beziehungsweise eine disseminierte Mykobakterium-avium-Infektion (MAI) um das Dreifache steigt, wenn die Viruslast um eine logStufe zunimmt. Bei Patienten mit CD4-Zellzahlen unter 75 pro ml war die Viruslast ein stärkerer Prädiktor für opportunistische Infektionen als die CD4-Zellzahl. Die antiretrovirale Kombinationstherapie reduziert die Viruslast, aber auch die AIDS-assoziierte Mortalität, die Hospitalisierung und die Inzidenz opportunistischer Infektionen um 50 bis 70 Prozent. Obwohl sie damit die beste Prophylaxe opportunistischer Infektionen darstellt, kann die spezifische Prophylaxe nicht unbedingt entfallen. Auch ein starker Anstieg der CD4-Zellzahl schützt nicht immer vor einer opportunistischen Infektion. Fallbeispiele von Patienten, die trotz erfolgreicher Dreifachtherapie an einer CMV-Retinitis erkrankten, belegen dies. Bei anderen Patienten waren trotz Dreifachtherapie MAI aufgetreten mit ausgeprägter Lymphadenopathie und Fieber. Die Verbesserung des Immunstatus hat in diesen Fällen offenbar dazu geführt, daß sich die entzündliche Reaktion verstärkte, konnte aber die Bakterien nicht eliminieren. Man muß deshalb die Frage stellen, ob die unter antiretroviraler Therapie neu gebildeten CD4-Zellen wirklich voll immunkompetent sind. Dafür sprechen Berichte über Patienten, deren Kryptosporidiose oder Mikrosporidiose nach Einleitung der antiretroviralen Therapie spontan ausheilte beziehungsweise sich deutlich besserte. Impfstoff-Suche bisher enttäuschend Das anspruchsvollste Ziel der AIDS-Forschung ist, Impfstoffe zu entwickeln, die eine langanhaltende Immunität induzieren und damit die Ausbreitung des Virus bei HIV-Infizierten unterdrücken können. Die Biologie von HIV erschwert die Entwicklung eines Impfstoffs erheblich. Das Virus zeigt eine hohe Sequenzvariabilität, kann sich durch Integration in das Genom der Wirtszelle dem Zugriff des Immunsystems entziehen, wird zellgebunden übertragen, weist eine hohe Turnoverrate auf und zerstört immunkompente CD4-positive Zellen. Außerdem moduliert eine HIV-Infektion nicht nur die zellvermittelte, sondern auch die humorale Immunantwort des Wirtes, zum Beispiel durch Verschiebung des Zytokinmusters. Untersuchungen von langzeitüberlebenden HIV-Infizierten, HIVinfizierten Kindern und Klinikpersonal, das wiederholt einer HIV-Kontamination ausgesetzt war, legen nahe, daß vor allem CD8-positive zytolytische T-Zellen die Virusreplikation unter Kontrolle halten und möglicherweise auch die Infektion eliminieren. Diese T-Zellen scheinen nicht nur HIV-infizierte Zielzellen zu lysie- ren, sondern die Sekretion löslicher Mediatoren zu induzieren, die die Ausbreitung des Virus hemmen. Welche Rolle die humorale Immunantwort für den Krankheitsverlauf spielt (speziell Hüllprotein-spezifische Antikörper), ist noch unklar. Ein eindeutiges Korrelat einer schützenden Immunantwort konnte tierexperimentell bisher nicht identifiziert werden. Ein Impfstoff sollte deshalb möglichst breit angreifen, das heißt, sowohl neutralisierende Antikörper als auch eine zellvermittelte Immunantwort induzieren. In einem US-amerikanischen Vakzine-Evaluationsprogramm werden derzeit in Sicherheits- und Immunogenitätsstudien (Phase I und II) 16 Kandidat-Vakzinen an mehr als 1 700 freiwilligen Testpersonen untersucht. Fast alle basieren auf den Hüllproteinen gp 160 oder gp 120 beziehungsweise Teilen davon. Sie wurden gentechnisch hergestellt oder chemisch synthetisiert. Alternativ verwendete man rekombinante Vaccinia- oder Canary-Pockenviren, die das HIV-1Hüllprotein exprimieren. Die meisten getesteten Impfstoffe lösten eine Antikörperantwort aus und stimulierten die Bildung von THelferzellen. Die höchsten Titer an neutralisierenden Antikörpern erzielte man nach mehreren Immunisierungen. Von den gereinigten Antigenen erwies sich die nativ glykolysierte HIV-Untereinheit pg 120 mit Aluminium-Adjuvans – in Säugerzellen produziert – als am stärksten immunogen. Nur die wenigsten KandidatVakzinen stimulierten eine zytolytische T-Zell-Antwort. Am erfolgreichsten waren hier die rekombinanten Canary-Pockenviren. Die weitere Beobachtung der Geimpften zeigte leider, daß diese Immunantworten bisher nicht vor einer HIV-Infektion schützen konnten. Wahrscheinlich muß ein erfolgreicher Impfstoff komplexer aufgebaut sein, darf nicht nur das HIV-Hüllprotein beeinhalten und muß auch an das jeweils regional vorherrschende Virusisolat angepaßt sein. Eine zusätzliche Modulation der Immunantwort mit Zytokinen ist ein weiterer Weg, der derzeit getestet wird, um wirksam gegen die HIV-Infektion zu impfen. Dr. med. Angelika Bischoff Deutsches Ärzteblatt 94, Heft 30, 25. Juli 1997 (27) A-1991