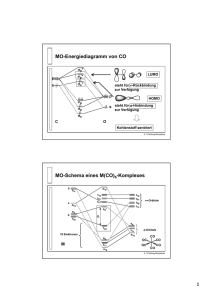
metallorganischen Chemie
Werbung

Elementarreaktionen metallorganischer Verbindungen Liganden-Substitutionsreaktionen Oxidative Addition Reduktive Eliminierung Insertion α-H -Eliminierungen β-H-Eliminierungen Metathese Reaktionen an koordinierten Liganden Charakteristische Änderung der: Koordinationszahl Oxidationsstufe Valenzelektronenzahl Reaktivität kann abgeschätzt werden 4. Elementarreaktionen Substitutions-Mechanismen Dissoziativer Mechanismus (D) + L' - CO LnM CO LnM LnM L' Zwischenstufe mit KZ -1 + CO Interchange (I) L LnM + L' L LnM -L Ln-1M L' keine Zwischenstufe, im Übergangszustand KZ +1 L' Assoziative Mechanismus (A) L nM + L' LnM L' -L Ln-1M L' Zwischenstufe mit KZ +1 4.1 Substitution 1 Kontinuum Substitutions-Mechanismen A: assoziativ Zwischenstufe mit höherer Koordinationszahl Ia: interchange eintretender Ligand bindet stärker an den Komplex Ib: interchange austretender Ligand bindet stärker an den Komplex D: dissoziativ Zwischenstufe mit niedrigerer Koordinationszahl 4.1 Substitution Substitutions-Mechanismen dissoziativer Mechanismus wird bevorzugt: in 18-Elektronenkomplexen in sperrigen Komplexen in oktaedrischen Komplexen assoziativer Mechanismus wird bevorzugt: v. a. in quadratisch-planaren 16-Elektronenkomplexen 4.1 Substitution 2 Geschwindigkeitskonstanten für Chloridsubstitution in [PtCl(R)(PEt3)2] k [s-1], 25 °C trans-Komplex R Pt Pt Pt k [s-1], 0 °C cis-Komplex 1,2 10-4 8,0 10-2 1,7 10-5 2,0 10-4 3,4 10-6 1,0 10-6 4.1 Substitution trans-dirigierende Eigenschaften von Liganden trans-dirigierene Eigenschaften H2O < OH < NH3 < RNH2 < py, Cl < Br < SCN < σ-Donoren SO3H < CH3 , C6H5 < H , PR3 < C2H4 < CN σ-Donor π-Akzeptoren σ-Donorstärke OH < NH3 < Cl < Br < CN , CO, CH3 < SCN < PR3 < H 4.1 Substitution 3 trans-dirigierende Faktoren Gute trans-dirigierende Liganden stabilisieren den trigonalbipyramidalen Übergangszustandes (ÜZ) T A M E L trans-Ligand (T) in äquatorialer Position: A Keine Konkurrenz mit trans-Liganden gute σ-Donoren T binden stärker an den ÜZ π-Akzeptoren nehmen zusätzlich Elektronen von E auf: π-Akzeptoren T binden stärker an den ÜZ Leeres dx2-y2 Orbital (in quadr.-planeren Komplexen) wird zu einem π-Orbital, kann mit π-Donoren wechselwirken kann (z. B. Cl¯ ) gute π-Donors binden etwas stärker an den ÜZ 4.1 Substitution weitere Beispiele assoziativer Substitution bei ungerader Elektronenzahl V(CO)6 +L 17 e (CO)6V L - CO (CO)5V 19 e L 17 e bei Ligandenumwandlung z. B. lineares oder gewinkeltes NO: (CO)4Mn 18 e NO +L : linear NO 3 e Donor O (CO)4Mn L - CO N 18 e : gewinkelt NO 1 e Donor (CO)3LMn NO 18 e 4.1 Substitution 4 Phosphane – Helfer in der metallorganischen Chemie Tertiäre Phosphane PR3 sind wichtig in der metallorganischen Chemie, da ihre sterischen und elektronischen Verhältnisse durch Variation von R gezielt verändert werden können. P R R R Sterische Faktoren bestimmt durch die Größe des Substituenten R, Kegelwinkel als Maß für die Größe des Liganden (Tolman-Winkel) nehmen oft ausschlaggebenden Einfluss auf den Verlauf zahlreicher Reaktionen Kegelwinkel θ M P R R PH3 θ 87° PMe3 118° PPh3 145° PMes3 212° R Elektronische Faktoren bestimmt durch die Donor- bzw. Akzeptorfähigkeit der Substituenten R z. B. PBu3 (130°) guter σ-Donor und P(OiPr)3 (130°) guter π-Akzeptor PMe3 (118°) und P(o-Tolyl) 3 (145°) sind etwa gleich gute Donoren/Akzep. 4.1 Substitution Dissoziativer Mechanismus – sterischer Einfluss von Phosphan-Liganden Abspaltung eines Phosphan-Liganden stellt oft einen entscheidenden Schritt in katalytischen Reaktionen dar (z. B. Wilkinson-Katalysator [RhCl(PPh3)3]). Beispiel: Abspaltung eines Phosphan-Liganden in [Ni(PR3)4] Komplexen PR3 Ni R3P PR3 KD PR3 PR3 PR3 θ KD + Ni R3P PR3 PR3 P(OEt)3 P(O-pTol)3 P(OiPr)3 P(O-oTol)3 PPh3 109° 128° 130° 141° 145° < 10-10 6 × 10-10 2.7 × 10-5 4 × 10-2 kein Ni(PR3)4 4.1 Substitution 5 Oxidative Addition – reduktive Eliminierung oxidative Addition [LnM] + A-B reductive Eliminierung LnM A B oxidative Addition Reaktion mit dem Substrat A-B unter Bildung neuer M-A und M-B Bindungen Einschub eines Metalles in eine Substratbindung Koordinationszahl (KZ) erhöht sich um 2 Oxidationsstufe (OZ) des Metals erhöht sich um 2 Valenzelektronenzahl (VE) erhöht sich um 2 reduktive Eliminierung umgekehrter Vorgang unter Bildung einer neuen A-B Bindung KZ, OZ und VE erniedrigen sich um 2 in katalytischen Reaktionen führt sie zur Produktbildung 4.2 Oxidative Addition und reduktive Eliminierung Vorausetzungen für oxidative Addition und reduktive Eliminierung Vorausetzungen für die oxidative Additon: Metallzentrum muss oxidiert werden können (keine Reaktion, falls das Metall bereits in seiner höchste Oxidationsstufe vorliegt) z. B. CoI < RhI < IrI und Ru0 > RhI > PdII beide Oxidationsstufen müssen stabil sein es müssen freie Koordinationsstellen vorhanden sein möglichst keine 18-Elektronenkomplexe Donorliganden stabilisieren den höheren Oxidationszustand Vorausetzungen für die reduktive Eliminierung: Metallzentrum sollte in einer höheren Oxidationsstufe vorliegen Substituenten müssen cis zueinander stehen können 4.2 Oxidative Addition und reduktive Eliminierung 6 Anwendungen oxidativer Additionen LnM + H-H Ln M LnM + R-X Ln M LnM + H-SiR3 Ln M H Hydrierungen H X Synthese von Halogenkomplexen R H SiR3 Hydrosilylierungen C-H-Bindungsaktivierung: thermodynamische Herausforderung H ∆H > O LnM + R-H LnM R BDE (kJ/mol) BDE (kJ/mol) • M-C schwächer als M-H Bdg. • negative Entropie H-H 435 M-H 210-250 C-H ~ 410 C-C ~ 375 M-C 120-170 (selten bis ~ 310) 4.2 Oxidative Addition und reduktive Eliminierung Beispiel einer C-H-Bindungsaktivierungen L H H Ir L L tBu O O CF3 + Ir L O O CF3 tBu L Ir β−H-Eliminierung IrLn H L O CF3 O H IrLn H IrLn IrLn oxidative Addition H H IrLn IrHL2 treibende Kraft: Bildung des stabilen Cp-Komplexes 4.2 Oxidative Addition und reduktive Eliminierung 7 Konzertierter Mechanismus einer oxidativen Addition Konzertierte Addition [LnM] + A-B LnM A# LnM B 18 e¯ , σ-Komplex 16 e¯ A B 18 e¯ A-B unpolare Substrate: H2, O2 oder Verb. mit C-H oder Si-H Bindg. benötigt eine freie Koordinationsstelle: in der Regel 16 e¯ -Komplexe 1. Schritt: Bildung eines σ-Komplexes mit A-B (Übergangszustand) A und B sind im Produkt cis zueinander in der Regel Reaktion 2. Ordnung mit negativer Aktivierungsentropie (geordneter ÜZ) kein Einfluss durch die Polarität des Lösungsmittels beschleunigt durch Donorliganden L 4.2 Oxidative Addition und reduktive Eliminierung SN2-Mechanismus einer oxidativen Addition SN2 Reaction L CO Ir Cl L Ir (I), 16 e¯ + MeI + Me L CO Ir Cl L I Ir (III), 16 e¯ Me CO Ir L I Ir (III), 18 e¯ L Cl A-B polare Substrate: HX, R-X (X = Halogenid), Me3SnCl 1. Schritt: Bildung eines kationischen Metallkomplexes in der Regel Reaktion 2. Ordnung mit negativer Aktivierungsentropie (geordneter ÜZ) beschleunigt durch polare Lösungsmittels (polarer ÜZ) R und X können cis oder trans zueinander sein im Produkt 4.2 Oxidative Addition und reduktive Eliminierung 8 Insertionsreaktionen Einschub eines ungesättigten Liganden A=B in eine benachbarte M-X Bindung (müssen cis zueinander stehen) 1,1-Insertion X M X X A B M +L A M B 1,2-Insertion X B M A M A A B L +L M A B X B X L Erniedrigung der Koordinationszahl um 1 (freie Koordinationsstelle wird meist durch einen Liganden L gefüllt) Erniedrigung der Valenzelektronenzahl um 2 keine Änderung der Oxidationsstufe des Metalls Insertionsreaktionen sind reversibel (z. B. α-H oder β -H-Eliminierungen) 4.3 Insertionsreaktion Wichtige Insertionsreaktionen 1,1-Insertion CO-Insertion in eine Metall-Alkyl-Bindung; AB = CO, X = CH3 CH3 M CH3 Carbonylierung CO Decarbonylierung M C O 1,2-Insertionen Alken-Insertion in eine Metall-Hydrid-Bindung; AB = Alken, X = H H M CH2 Alken-Insertion CH2 β-H-Eliminierung M CH2 CH2 H wichtige Reaktionsschritte in katalytischen Reaktionen (z. B. Hydroformylierungen oder Hydrierungen) 4.3 Insertionsreaktion 9 Insertionsreaktion am Beispiel der Carbonylierung Zwei denkbare Mechanismen CO-Insertion in die M-CH3-Bindung O C CO (CO)4Mn (CO)4Mn CH 3 C CH3 O Alkylgruppen-Wanderung auf das koordinierte CO O O C CH C 3 CO (CO)4Mn (CO)4Mn CH3 O C (CO)4Mn C CH3 O O C CH 3 (CO)4Mn C O 13CO: Beweis mit Hilfe von isotopenmarkiertem es findet eine Alkylgruppen-Wanderung statt 4.3 Insertionsreaktion Einflüsse auf die Alkylgruppen-Wanderung Beschleunigung der Alkylgruppen-Wanderung durch: e¯ –Donoreigenschaften der Alkylgruppe (gute D. wandern besser) Perfluoroalkyle wandern nur ausnahmsweise und bei hohen Temp. sterischer Anspruch der Alkylgruppe R-Gruppenwanderung in [CpFe(CO)2R] (CO Insertion): (Me3Si)2CH >> Me3CCH > s-Bu > i-Pr > Me3SiCH2 > i-Bu > Et > Me von unten nach oben innerhalb einer Triade Geschwindigkeit: 3d > 4d > 5d Anwesenheit von Lewis-Säuren 4.3 Insertionsreaktion 10 β-H-Eliminierung H H # H H H H H H C β C α H β-H-Eliminierung M Olefin-Insertion in M-H Bindung C C +L H2C M H -L L CH2 M H VE +2 KZ +2 OZ +0 Übergangszustand: Metall-, H- und beide C-Atome liegen in einer Ebene bilden einen viergliedrigen Metallazyklus Hydrid an M- und C-Atom gebunden Voraussetzungen für β-H-Eliminierung: β-H-Atom eine freie Koordinationsstelle (bzw. leeres Orbital) cis zur Alkylgruppe es muss geometrisch möglich sein, einen planaren ÜZ zu bilden 4.4 α- und β-H-Eliminierungen Experimentelle Beweise für die β-HEliminierung Substitution der β-H Atome durch Deuterium D D β-D-Elim. (Bu3P)Cu D (Bu3P)Cu + H2C D Beeinflussung durch sperrige Gruppen H2C C H Cp*2Nb H R Cp*2Nb R # +L R Cp*2Nb L 4.4 α- und β-H-Eliminierungen 11 Beispiele von β-H-Eliminierungen nBu PR3 Pt R3P [PtH(nBu)(PR3)2] + Pt(II) H H H H H H L2Pt [L2Pt] + L2Pt Pt(0) β-H-Eliminierung reduktive Eliminierung 4.4 α- und β-H-Eliminierungen α-H-Eliminierung M C R H H Alkylkomplex α-H-Eliminierung R M C H H Alkylidenhydrido-Komplex VE +2 KZ +1 OZ +2 in der Regel nur beobachtet bei Abwesenheit von β-H-Atomen Alkylidenhydrido-Komplex meist nur nur beobachtet als Intermediat, selten isoliert die Reaktion ist reversibel erfordert die Anwesenheit einer freien Koordinationstelle intramolekulare oxidative Addition 4.4 α- und β-H-Eliminierungen 12 Konkurrenz zwischen α-H and β-HEliminierungen R M C H α-H R M C H2 H R CH2 β-H M H Alkyl Alkyliden-hydrid (selten isoliert) Olefin-hydrid Reaktion ist schneller kinetisches Produkt thermodynamisches Produkt dominante Reaktion 4.4 α- und β-H-Eliminierungen Olefin-Metathese R'' R R R' LnM R' C H + H H H R'' 1. Schritt LnM H R R LnM H H R R'' H LnM R H H 3. Schritt H + H R' R H R'' H R H R' H LnM H H R' LnM H H H R R R' H H + R' H R H R R H LnM R'' R'' H R' R' R' LnM H + H + 2. Schritt R' LnM H + H R 2 LnM H R' H R + R'' H 4. Olefin-Metathese 13 σ-Bindungmetathese Zr R + H2 Cl - RH nicht möglich, da bereits in höchster Oxidationsstufe H Zr Cl H Ln M H R ox. Addition + H2 LnM R red. Eliminierung Ln M H + RH + H2 σ-Bindungsmetathese H H Ln M R H H LnM R 4. σ-Bindungsmetathese σ-Bindungmetathese Zr R + H2 Cl - RH nicht möglich, da bereits in höchster Oxidationsstufe H Zr Cl H Ln M H R ox. Addition + H2 LnM R red. Eliminierung Ln M H + RH + H2 σ-Bindungsmetathese H H Ln M R H H LnM R 4. σ-Bindungsmetathese 14 Reaktivität an koordinierten Liganden Durch Koordination werden die chemischen Eigenschaften vieler Liganden grundlegend verändert, wodurch Reaktionen am Liganden gezielt durchgeführt werden können oder erst ermöglicht werden. σ-Akzeptor π-Donor LnM Ligand wird elektrophiler nukleophiler Angriff wird gefördert Ligand wird nukleophiler elektrophiler Angriff wird gefördert Aktivierung eines Liganden durch ein LnM-Fragment mit σAkzeptor- und π-Donor-Eigenschaften durch Polarisierung 4.4 Reaktivität an koordinierten Liganden Nukleophiler Angriff an koordinierten Liganden Nukleophiler Angriff an CO Fe(CO)5 NaOHaq O (OC)4Fe Na+ C H - CO2 O Na[HFe(CO)4] Nukleophiler Angriff an Olefin Reaktivität: Fe + MeO C O in MeOH MeO C O kationische Komplexe fördern nukleophilen Angriff Fe CO C O > > > gradzahlig > ungradzahlig azyklisch > zyklisch 4.4 Reaktivität an koordinierten Liganden 15 Elektrophiler Angriff an koordinierten Liganden Ph Elektrophiler Angriff Ph P an Acylgruppe Fe Me Ph Ph P P Ph O Ph Fe+ Me P Ph OPh MeI Ph Ph P Fe I Me P Ph O Me Ph Elektrophiler Angriff an CO-Gruppe LnM C O AlX3 LnM C O AlX3 4.4 Reaktivität an koordinierten Liganden 16