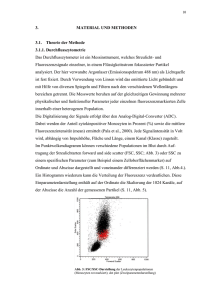
Bildung von Interleukin 1 in Nabelschnurmonozyten bei
Werbung

Aus der Klinik für Kinder- und Jugendmedizin des St. Josef Hospital -Universitätsklinikder Ruhr-Universität Bochum Direktor: Prof. Dr. C. Rieger Bildung von Interleukin 1 in Nabelschnurmonozyten bei Neugeborenen mit und ohne Atopierisiko Inaugural-Dissertation zur Erlangung des Doktorgrades der Medizin einer Hohen Medizinischen Fakultät der Ruhr-Universität Bochum vorgelegt von Claudia Julia Bockelmann aus Ostfildern 2001 Dekan: Prof. Dr. med. Muhr Referent: PD Dr. med. U. Schauer Korreferent: Prof. Dr. med. A. W. O. Jensen Tag der mündlichen Prüfung: 09.07.2002 Inhaltsverzeichnis ABBILDUNGSVERZEICHNIS .................................................................................... 2 ABKÜRZUNGSVERZEICHNIS .................................................................................. 4 1 EINLEITUNG .......................................................................................................... 5 1.1 Atopische Erkrankungen...................................................................................5 1.1.1 Pathogenese der atopischen Erkrankungen ...............................................6 1.1.2 Effektorphase.............................................................................................9 1.2 Einflußfaktoren der Atopieentwicklung............................................................9 1.3 Bakterielle Stimuli ..........................................................................................12 1.4 Die Rolle der Monozyten im Immunsystem ...................................................14 1.5 Bedeutung von IL-1 ........................................................................................15 1.5.1 Stimuli zur IL-1-Freisetzung ...................................................................15 1.5.2 Wirkung von IL-1 auf immunkompetente Zellen ...................................15 1.5.3 Wirkung von IL-1 auf nicht-immunkompetente Zellen ..........................16 1.5.4 Die besondere Rolle von IL-1 bei verschiedenen Erkrankungen............18 1.6 2 3 Fragestellung ...................................................................................................19 MATERIAL UND METHODEN ......................................................................... 20 2.1 Probandenkollektiv .........................................................................................20 2.2 Isolierung mononukleärer Zellen ....................................................................21 2.3 Untersuchung der mononukleären Zellen .......................................................21 2.3.1 Zellkultur .................................................................................................21 2.3.2 Ernten ......................................................................................................22 2.3.3 Färbung der Monozyten ..........................................................................22 2.4 Messung mit dem Durchflußzytometer...........................................................23 2.5 Nabelschnur Gesamt-IgE ................................................................................24 2.6 Statistik............................................................................................................25 ERGEBNISSE ........................................................................................................ 26 3.1 Probandenkollektiv Fragebogenauswertung / Geburtsbuch............................26 3.1.1 Atopierisikogruppe und Nicht-Risikogruppe ..........................................26 3.1.2 Die Einflußfaktoren .................................................................................27 1 3.2 Interleukin-1-Untersuchungen ........................................................................28 3.2.1 IL-1-Kinetik.............................................................................................28 3.2.2 Unstimulierte und durch Bakterienderivate stimulierte IL-1Produktion von Nabelschnurblutmonozyten ...........................................29 3.2.3 Zusammenhang der IL-1-Produktion mit dem Atopierisiko ...................30 3.2.4 IL-1- und TNFa-Produktion im Vergleich .............................................31 3.3 4 Korrelation zwischen IgE und IL-1.................................................................32 DISKUSSION......................................................................................................... 33 4.1 Bedeutung der erhöhten IL-1-Werte für die Atopieentstehung ......................33 4.2 Der IL-1-Rezeptor und die Signaltransduktion...............................................34 4.3 Die Rolle der Monozyten in der Atopieentstehung.........................................37 4.4 Charakterisierung der Nabelschnurblutmonozyten (CBMC)..........................38 4.5 Wirkung bakterieller Stimuli auf das Immunsystem ......................................39 4.5.1 LPS als Bakterienprodukt – welche Rolle spielt es bei der Auslösung von Allergien ...........................................................................................39 4.5.2 Weitere bakterielle Stimuli......................................................................40 4.6 Intrazelluläre durchflußzytometrische Zytokinbestimmung ...........................41 4.7 Einflußfaktoren der Atopieentstehung ............................................................43 4.8 Atopiemarker im Nabelschnurblut..................................................................44 5 ZUSAMMENFASSUNG ....................................................................................... 46 6 AUSBLICK............................................................................................................. 47 7 LITERATURVERZEICHNIS.............................................................................. 48 8 APPENDIX............................................................................................................. 64 Abbildungsverzeichnis Abbildung 1: Schematische Darstellung der Th1- und Th2-Differenzierung Abbildung 2: Setzen eines Lifegate um die Monozyten Abbildung 3: IL-1-Kinetik Abbildung 4: IL-1-Produktion aller Probanden mit und ohne LPS-Stimulation Abbildung 5: IL-1-Produktion im Zusammenhang mit dem Atopierisiko 2 Abbildung 6: IL-1- und TNFa-Produktion nach LPS-Stimulation Abbildung 7: IgE- und IL-1-Werte aller Probanden Abbildung 8: Signaltransduktion der IL-1-, IL-18- und TLR-4-Rezeptoren Tabellenverzeichnis Tabelle 1: IL-1-Wirkung auf diverse Zellen Tabelle 2: Charakterisierung der Probandengruppe 3 Abkürzungsverzeichnis APC Antigen Presenting Cell, Antigenpräsentierende Zelle CBMC Cord Blood Mononuclear Cell, Mononukleäre Nabelschnurblutzelle ELISA Enzyme-Linked Immuno Sorbent Assay FITC Fluoresceinisothiocyanat HBSS Hanks balanced salt solution IDC Interdigitierende Dendritische Zellen IFNg Interferon gamma IgA Immunglobulin A IgE Immunglobulin E IgG Immunglobulin G IgM Immunglobulin M IL Interleukin IRAK IL-1-Rezeptor assoziierte Kinase JNK N-terminale Kinase LAP Lipid A assoziiertes Protein LPS Lipopolysaccharid MAPK Mitogen aktivierte Proteinkinase MAS Multizentrische Allergie Studie MHC Major Histocompatibility Complex, Haupthistokompatibilitätskomplex PBMC Peripher Blood Mononuclear Cell, Mononukleäre Zelle des peripheren Blutes PCR Polymerase Chain Reaction, Polymerase Kettenreaktion PE Phycoerythrin RPMI Rothwell Park Memorial Institut 1640 Kulturmedium TCR T-Zell Rezeptor TIR Toll / IL-1-Rezeptor TLR Toll-Like-Rezeptor TNF Tumornekrosefaktor TRAF6 TNF-Rezeptor assoziierter Faktor 6 4 1 Einleitung 1.1 Atopische Erkrankungen Die Prävalenz atopischer Erkrankungen hat in den letzten Jahrzehnten ständig zugenommen und steigt weiter an (Skjonsberg et al. 1995). 25 % der Bevölkerung erkranken im Verlauf des Lebens an Asthma, Heuschnupfen oder Neurodermitis, die zum Formenkreis der Atopie gerechnet werden (Bergmann et al. 1993). Der Begriff Allergie wurde 1906 zum ersten Mal von Pirquet verwendet. Er verstand darunter eine veränderte, überschießende Immunreaktion beim zweiten oder folgenden Kontakt mit einem „Agens“. Heute wird der Begriff Allergie als Symptom der Überempfindlichkeitsreaktion vom Typ I (Allergische Reaktion vom Soforttyp nach Coombs und Gell) bezeichnet. Der Begriff Atopie wurde erstmalig 1923 von Coca und Cooce verwendet und ist eng mit dem Begriff „Allergie“ verbunden. Atopie bezeichnet die Neigung zu Überempfindlichkeitsreaktion vom Typ I. Die klinischen Leitsymptome der Atopie sind Erkrankungen wie Asthma, endogenes Ekzem, Heufieber und Urtikaria. Die Ursachen der atopischen Erkrankungen sind seit Jahrzehnten Gegenstand wissenschaftlicher Forschung. Der Pathogenese dieser Erkrankungen liegen im wesentlichen drei Faktoren zugrunde: erstens) eine genetische Prädisposition (Roorda et al.1992, Cookson und Hopkin 1988, Pöysä et al.1989), zweitens) die Allergenexposition (Bahna 1992) und drittens) verschiedene Einflußfaktoren (s.u.). Die genetische Prädisposition scheint bei der Entstehung atopischer Erkrankungen eine wichtige Rolle zu spielen. Es wird eine polygenetische und multifaktorielle Vererbung angenommen, wobei es keine Vererbung für spezifische Sensibilisierungen auf bestimmte Allergene gibt. Es wird vielmehr die Veranlagung vererbt, im späteren Leben eine pathologische Immunreaktion auf Allergene zu entwickeln (Bahna 1992). Diese „atopische Prädisposition“ ist als additive Polygenie als die Summe aller in die gleiche Richtung weisenden Gene aufzufassen (Bergmann et al. 1993). Man geht davon aus, daß für die Umwandlung der Disposition in die Krankheit ein Schwellenwert existiert, der von verschiedenen Umweltfaktoren 5 abhängig ist. Die atopischen Erkrankungen manifestieren sich klinisch erst nach der Überschreitung dieses Schwellenwertes (Kabesch 2001). Die Allergenexposition ist ein weiterer Faktor, der zur Allergieentstehung beiträgt. Dabei haben der Typ des Allergens, die Quantität, der Expositionsweg und die Expositionsdauer einen Einfluß auf die Entwicklung der Erkrankung (Bahna 1992; Holt, McMenamin und Nelson 1990). 1.1.1 Pathogenese der atopischen Erkrankungen Die atopische Erkrankung ist durch eine lokale Entzündungsreaktion gekennzeichnet, die durch Freisetzung von Entzündungsmediatoren nach Antigenkontakt mit spezifischem IgE hervorgerufen wird. Für die Allergieentstehung ist eine Regulationsstörung der IgE-Produktion im Sinne einer gesteigerten IgE-Synthese verantwortlich. Hierfür existieren verschiedene Erklärungsmodelle, von denen das folgende zunehmend an Bedeutung gewinnt: Die B-Zellen wandeln sich von IgM produzierenden B-Zellen bei wiederholtem Allergenkontakt in IgE oder IgG produzierende B-Zellen um (sog. „B-Zellswitch“). In welche Richtung dieser B-Zellswitch stattfindet, hängt von dem Zytokinprofil zum Zeitpunkt der Allergenexposition ab. Herrscht vorwiegend ein Zytokinmilieu mit Interferon-g (IFNg) vor, differenzieren sich die B-Zellen eher zu IgG produzierenden B-Zellen, während ein IL-4-Milieu zu einer Differenzierung zu IgE produzierenden B-Zellen führt (Holt et al. 1990; Bergstedt-Linquist et al. 1988; Finkelman et al. 1988; Savelkoul et al. 1988). Diese Zytokine, die für den B-Zellswitch verantwortlich sind, werden von den THelferlymphozyten (T-Helferzellen) produziert. T-Helferzellen können sich nach dem von Mosmann 1986 entwickelten Modell in zwei Populationen differenzieren, die durch ein spezifisches Zytokinprofil charakterisiert werden: einerseits in die IL-2 und IFNg produzierenden Th1-Zellen, andererseits in die IL-4, IL-5 und IL-10 produzierenden Th2-Zellen. Die Th1-Zellen sind für die zytotoxische Antwort verantwortlich, die Th2-Zellen für die humorale Antwort. Den Th1-Zellen kommt eine allergieprotektive Eigenschaft zu. Im Gegensatz dazu fördern die Zytokine der 6 Th2-Zellen die Bildung von IgE produzierenden B-Zellen, sie sind also eher allergiefördernd. Ob sich T-Helferzellen eher zu allergieprotektiven Th1-Zellen oder zu allergiefördernden Th2-Zellen differenzieren, hängt ebenfalls vom Zytokinmilieu zum Zeitpunkt der T-Zelldifferenzierung ab. Für die Differenzierung der T-Zellen sind u.a. Makrophagen, bzw. deren Zytokine verantwortlich: In in-vitro- und in-vivo-Versuchen konnte gezeigt werden, daß antigenpräsentierende Zellen (APC) Th2-Zellen als Antwort auf ein Allergen stimulieren. Die daraufhin folgende IL-4-Freisetzung veranlaßt B-Zellen zu einer IgE-Produktion. Th1-Zellen werden hingegen vornehmlich von Antigenen, wie z.B. Bakterienbestandteilen, aktiviert. Das daraufhin freigesetzte IFNg führt zu einer Produktion von IgG durch B-Zellen und zu einer Hemmung der Th2-Antwort. Th2-Zellen können durch die IL10-Produktion auch die Th1-Antwort unterdrücken und so die INFg-Freisetzung hemmen. Makrophagen sind aktivierte Monozyten und können als antigenpräsentierende Zellen (APC) agieren. Sie phagozytieren und fraktionieren das Antigen und präsentieren es zusammen mit Klasse-II-MHC auf der Zelloberfläche den THelferzellen. Die T-Helferzellen erkennen mittels eines T-Zell-Rezeptors (TCR) Peptide, die in dem MHC-Molekül eingelagert sind. Die T-Zellaktivierung findet zusätzlich auf Zytokinebene statt, z.B. durch das von Makrophagen freigesetzte IL-1. Die MHC-Präsentation und die Aktivierung durch Zytokine bezeichnet man auch als „Doppelsignal“ (Rook 1995, Kaufmann, 1991c). Unter den APC nehmen die sog. dentritischen Zellen (IDC) eine wichtige Rolle ein. Diese können mittels ihrer Fortsätze (Dendriten) ebenfalls Kontakt zu den THelferzellen aufnehmen und beschreiten so zur normalen Antigenpräsentation einen alternativen Weg der T-Zell-Aktivierung. 7 Abbildung 1: Schematische Darstellung der Th1- und Th2-Differenzierung Noch bevor die Antigenpräsentation stattfindet, sezernieren Monozyten als unspezifische Primärantwort auf eine Infektion T-Zell- und antikörperunabhängig Zytokine wie IL-1, TNFa, IL-12. Zusätzlich exprimieren sie auf ihrer Oberfläche verstärkt CD80 / CD86 (Rook 1995). Die Zusammensetzung dieser Zytokine ist entscheidend für die nachfolgenden Mechanismen der Immuneffektorsysteme, da IL-1 bzw. IL-12 die Differenzierung der T-Helferzellen beeinflussen (Manetti et al. 1994). In der Allergieentstehung spielen Makrophagen und deren sezernierte Zytokine eine entscheidende Rolle bei der frühen immunologischen Prägung des Immunsystems mit allergietypischem Reaktionsmuster. Jedoch sind die zugrundeliegenden Pathomechanismen noch ungeklärt. Welche Rolle Monozyten im Rahmen der allergischen Immunantwort spielen, und welche Zytokine hierbei wichtig sind, ist noch weitgehend unklar. 8 1.1.2 Effektorphase Bei der Typ I-Reaktion nach Coombs und Gell (Allergische Reaktion vom Soforttyp) liegt eine antikörpervermittelte Immunreaktion vor. In der ersten Phase (20 min) kommt den Mastzellen und dem IgE eine hervorstechende Bedeutung zu. Die Mastzellen und basophilen Granulozyten tragen an ihrer Oberfläche homozytotrope Immunglobuline vom Typ E (IgE). Bindet sich ein spezifisches Antigen gleichzeitig an zwei benachbarte IgE-Moleküle, so kommt es durch eine Überbrückung („bridging“) zur Freisetzung von Mediatoren (S. H. E. Kaufmann, 1991b). Die Mediatoren interagieren mit immunkompetenten Zellen sowie mit Gefäß- und Muskelzellen. Je nachdem, in welchem Gewebe der Antigenkontakt stattfindet, werden verschiedene Reaktionen hervorgerufen. In der Haut kommt es z.B. zu einer Vasodilatation (klinisch erkennbar als Erythem und Überwärmung), zu einer Erhöhung der Gefäßpermeabilität (Ödem) und zu Juckreiz. Findet der Allergenkontakt im Bronchialsystem statt, kommt es zur Vasodilatation (Schleimhautödem) und Bronchiokonstriktion (Verengung des Bronchiallumens). Diese entzündlichen Reaktionen sind klinischen Leitsymptome der atopischen Erkrankungen (hier: Urtikaria bzw. allergisches Asthma). Darüber hinaus werden die Lymphokine freigesetzt, die für weitere immunologische Reaktionen verantwortlich sind. Sie beeinflussen das entzündliche Geschehen, indem sie auf komplexe Weise mit den Immunzellen interagieren. Das von T-Zellen sezernierte IL-10 verstärkt beispielsweise die Mastzelldifferenzierung. Außerdem können die sezernierten Lymphokine eine Leukotaxis bewirken, zu einer Aktivierung oder Suppression der Immunantwort führen (s.u.). 1.2 Einflußfaktoren der Atopieentwicklung Zahlreiche Faktoren können die Entstehung einer Atopie beeinflussen, im Folgenden werden einige erläutert. Rauchen: 1995 stellten Bergmann et al. in einer Untersuchung von 6401 Neugeborenen fest, daß Rauchen einen Einfluß auf die Erhöhung der Nabelschnurblut IgE-Werte hat, und somit auch als atopiefördernder Faktor einzustufen ist. Andrae et al. fanden 1988 in einer Untersuchung (von 5301 Kindern zwischen 6 Monaten und 16 Jahren) einen 9 Zusammenhang zwischen Tabakrauchexposition und bronchialer Hyperreaktivität bei den Kindern. Außerdem besteht ein Zusammenhang zwischen Tabakrauchexposition und der Prävalenz atopischer Erkrankungen (Gortmarker et al. 1982), insbesondere der Prävalenz von Asthma (Arshad und Wallace-Hide 1992). Geschlecht: In mehreren Studien wurden höhere Nabelschnur-IgE-Werte der männlichen im Vergleich zu weiblichen Neugeborenen festgestellt (Bergmann et al. 1993 und 1995; Bahna 1992; Kuehr et al. 1992). Croner konnte hingegen keine Prädominanz eines Geschlechtes hinsichtlich eines erhöhten IgE-Wertes feststellen (Croner und Kjellman 1990). Geburtsmonat: Pöysä et al. (1989) konnten zeigen, daß Kinder, die zwischen den Monaten Januar und Februar geboren wurden, im späteren Leben eine positive Hautreaktion auf Birkenpollen zeigten. Als die Säuglinge in einem Alter von 3-6 Monaten waren, wurden sie auf Birkenpollen sensibilisiert. Daraus läßt sich schließen, daß das Immunsystem zwischen dem 3. und 6. Monat leichter durch äußere Faktoren beeinflußbar ist, als zu einem anderen Zeitpunkt. Croner und Kjellman (1986) fanden heraus, daß es bei Kindern mit erhöhten Nabelschnurblut-IgE-Werten, die im Mai geboren wurden, öfter zu einer Atopieentwicklung kam, als bei Kindern, die im November geboren wurden. Arshad und Wallace-Hide (1992) stellten fest, daß Kinder, die im Sommer geboren wurden, häufiger an Asthma erkrankten, als Kinder, die im Winter geboren wurden. Umweltverschmutzung: Umweltschadstoffe können eine allergische Sensibilisierung auslösen, was im Tierversuch bestätigt wurde (Riedel et al. 1988). Es konnte eine Beziehung zwischen Schwefeldioxid bzw. Ozon und einer bronchialen Hyperreaktivität gezeigt werden (Koenig et al. 1982; Kreit et al. 1989). Schwefeldioxide führten im Tierversuch zu einer erhöhten IgE-Produktion (Osebold, Gerschwin und Zee 1980). Corbo et al. (1993) stellten heraus, daß Luftverschmutzung nicht zum Anstieg der 10 Atopieprävalenz führt, aber die Entwicklung klinischer Symptome bereits sensibilisierter Personen fördert. Ernährung: Die Allergenexposition ist von essentieller Bedeutung für die Entwicklung einer Atopie. Im Säuglingsalter haben Nahrungsallergene die größte Bedeutung (Bahna 1992). Es konnte festgestellt werden, daß Stillen mit einer geringeren Atopieinzidenz einhergeht ( Bahna 1986 und 1991). Die Ernährung der Mutter währen der Stillzeit kann die prophylaktische Wirkung des Stillens unterstützen (Chandra et al. 1986, Zeiger et al. 1989, Hattewig et al. 1989). Schwangerschafts-, und Geburtskomplikationen: Bergmann et al. (1995) stellten keinen Zusammenhang zwischen Gestationsalter und erhöhten Nabelschnurblut IgE-Werten fest, was durch die Untersuchung von Kuehr et al. 1992 an 1470 Kindern bestätigt werden konnte. Laut Bergmann et al. (1995) bestand ebenfalls kein Zusammenhang zwischen Geburtsgewicht, APGAR Werten, Nabelschnur pH-Werten und Medikation während der Schwangerschaft und erhöhten Nabelschnur IgE-Werten. Über den begünstigenden Einfluß der Umweltfaktoren auf die Entstehung atopischer Erkrankungen wird zur Zeit kontrovers diskutiert. Einerseits soll eine hohe Luftverschmutzung für die höhere Prävalenz verantwortlich sein (Gergen et al. 1987; Ishizaki et al. 1987), andererseits konnte gezeigt werden, daß die Allergieprävalenz in luftverschmutzten Städten in Polen (Braback et al. 1994) oder in Ostdeutschland (von Mutius et al. 1994) geringer war, als in weniger schadstoffbelasteten Städten in Schweden oder in München. Der andere Lebensstil in den ehemals sozialistisch regierten Ländern könnte dafür verantwortlich sein (von Mutius et al. 1994). Mutius postulierte 1994, daß die Unterbringung der Kleinkinder in Tagesstätten und der daraus hervorgehenden Infekthäufung im Kindesalter eine allergiehemmende Wirkung hat. Wenn die Auseinandersetzung des Immunsystems mit Infekten, also mit bakteriellen Stimuli die Atopieentwicklung beeinflußt, ist die Wirkung bakterieller Reize auf das Immunsystems von großem Interesse. Es gibt zahlreiche bakterielle Stimuli. 11 1.3 Bakterielle Stimuli Bakterienbestandteile gram-positiver und gram-negativer Bakterien sind in der Lage, Monozyten zur Sekretion von Zytokinen (z.B. IL-1) zu stimulieren. Die Wichtigsten unter den Bestandteilen gram-positiver Bakterien sind Teichonsäuren, Lipid Aassoziiertes Protein (LAP), Lipoarabinomannan und Staphylokokken Superantigen, unter den der gram-negativen Bakterien LPS, LAP und Porine. Beide Bakterienarten besitzen des weiteren Peptidoglykane, wobei diese in Kombination mit eingelagerten Teichonsäuren (von Strep. pneumoniae) die potentesten IL-1-Induktoren sein sollen (Riesenfeld-Orn et al. 1989). Lipoteichonsäuren: Lipoteichonsäuren bilden den Hauptbestandteil der Zellwand gram-positiver Bakterien und gelten als Virulenzfaktoren (Riesenfeld-Orn et al. 1989). Bhakdi et al. berichteten 1991 von großen Unterschieden der Lipoteichonsäuren verschiedener Bakterien hinsichtlich ihrer Fähigkeit, Monozyten zu einer Zytokinproduktion (IL-1, IL-6 und TNFa) zu aktivieren. Lipoteichonsäuren diverser Enterokokkenarten erwiesen sich als genauso wirksam, aber weniger potent als LPS, wohingegen z.B. Lipoteichonsäuren von Staph. aureus und Strep. mutans gar keine Aktivität zeigten. Lipoteichonsäuren von Pneumokokken führten zu einer IL-1, nicht jedoch zu einer TNFa-Freisetzung, die Lipoteichonsäuren von Strep. faecales hingegen stimulierten Monozyten zu einer Freisetzung beider Zytokine (Tsutsui et al. 1991). Man erkennt, daß Lipoteichonsäuren in unterschiedlichem Maße zu einer Monozytenaktivierung und Zytokinfreisetzung führen und daher einen weniger zuverlässigen Stimulus als LPS darstellen. Lipoarabinomannan: Lipoarabinomannan ist ein Zellwandbestandteil der Mykobakterien und LPS funktionell sehr ähnlich. Zudem vermag es auch an den CD14-LPS-Rezeptor zu binden und IL-1, IL-6, TNFa und IL-10 freizusetzen. Staphylokokkentoxin: Die meisten Superantigene werden von Staph.aureus produziert und induzieren eine TNF-, IL-1-, IL-6- und IFNg-Produktion. Das Staphylokokken-Enterotoxin, ein sog. 12 „Superantigen“, wirkt direkt aktivierend auf das spezifische Immunsystem durch die Vernetzung von T-Zellen mit Monozyten bzw. Makrophagen. Es lagert sich sowohl an den T-Zell-Rezeptor als auch an die MHC-Klasse-II-Moleküle an. Porine: Porine sind Bestandteile gram-negativer Bakterien und spielen eine Rolle als Virulenzfaktoren. Porine von Salmonella typhimurium (Galdiero et al. 1993), Yersinia enteroko-litika (Tufano et al. 1994a) oder von Helicobakter pylori (Tufano et al. 1994b) stimulieren Monozyten und Lymphozyten zu einer Freisetzung verschiedener proentzündlicher und immunregulatorischer Zytokine wie IL-1, IL-4, IL-6, IL-8, TNFa, GM-CSF und IFNg. Vergleicht man die Porine von Sal. typhimurium mit LPS, so zeigen beide eine ähnliche Fähigkeit, TNF und IL-6 zu stimulieren, aber die Porine führen zu einer schwächeren Stimulation der monozytären IL-1-Freisetzung. Somit schieden sie für diese Arbeit als Stimulus aus. Surface associated material: Surface associated material (SAM) ist locker mit der Bakterienoberfläche assoziiert und kann leicht gelöst werden. Es ist teilweise biologisch aktiv. SAM kann zu einer Stimulation der Freisetzung verschiedener Zytokine wie IL-1, TNF, IL-6 und IL-8 aus verschiedenen Zellpopulationen (Monozyten, Fibroblasten, PBMC und Neutrophilen) führen. Das SAM einiger oraler Bakterien ist ein stärkerer Zytokininduktor als das korrespondierende LPS. Es ist sogar gleich stark induzierend wie das LPS von E. coli (Henderson und Wilson 1996). Bakterielle Toxine: Pneumolysin von Streptokokkus pneumoniae und Toxin B von Clostridium difficile gehören zu den potentesten Stimulatoren der proinflammatorischen Zytokinsynthese von IL-1 und TNF in Monozyten (Houldsworth et al. 1994). LPS: LPS ist Zellwandbestandteil gram-negativer Bakterien wie E.coli. Es besteht aus einem innenliegenden hydrophobischen Lipid A, einem Kernglykolipid und außenaufliegenden hitzestabilen Ketten, aus sich wiederholenden Einheiten von bis 13 zu sieben Zuckern (O-spezifischen Ketten) (Lebek und Cottier 1992, Couturier et al. 1991). Dabei ist hauptsächlich das Lipid A für die toxische Wirkung verantwortlich. E. coli gehört, in Abhängigkeit von der Ernährung, schon im Säuglingsalter zur konstanten Besiedlung des unteren Magen-Darm-Traktes (Lebek und Cottier 1992). Bei ausschließlich gestillten Säuglingen herrscht eine Besiedlung mit Laktobazillus bifidus vor, es kommt erst nach Zufütterung zu einer E. coli Besiedlung des MagenDarm-Traktes. So wird der Säugling schon in den ersten Lebensmonaten mit LPS, welches bei Zerfall des Bakteriums freigesetzt und über die Darmmukosa aufgenommen wird, konfrontiert. LPS ist also einer von vielen bakteriellen Stimuli, es ist ubiquitär weit verbreitet, gut charakterisiert und als reines Reagenz verfügbar. Was bewirkt LPS? LPS stellt einen Aktivator der makrophagozytären Zytokinproduktion dar. Es ist der Prototyp der in-vitro-Stimulation der IL-1Sekretion durch Monozyten (Anderson et al. 1992). 1.4 Die Rolle der Monozyten im Immunsystem In der vorliegenden Arbeit wurden Monozyten untersucht, da diese die wichtigsten Zellen der frühen unspezifischen Immunantwort darstellen, und ihre Rolle in der Allergieentstehung noch weitgehend ungeklärt ist. Bekannt ist die Bedeutung der Monozyten in der Immunantwort auf Infektionen bzw. Mikroorganismen: Blutmonozyten entstammen dem Knochenmark. Sie wandern aus dem zirkulierenden Blut-Pool in die verschiedenen Gewebe ein und entwickeln sich zu Makrophagen, welche die aktivierte Form der Monozyten darstellen. Für die Migration in die verschiedenen Gewebe sind u.a. Bestandteile von Mikroorganismen verantwortlich, die für die Monozyten einen chemotaktischen Reiz darstellen. Durch Aktivierung des alternativen Komplementweges erzielt das bakterielle Endotoxin diesen chemotaktischen Effekt. Im Gewebe besteht die Aufgabe des Monozyten darin, das Antigen zu phagozytieren und durch Antigenpräsentation die Entzündung auszulösen. Zur Phagozytose muß der Monozyt die Mikroorganismen mittels eines Rezeptors an seiner Oberfläche binden. Bereits aktiviertes Komplement erleichtert die Phagozytose. Das phagozytierte Antigen wird prozessiert und zusammen mit MHC-Klasse-II14 Molekülen den T-Helferzellen präsentiert. IL-1, welches gleichzeitig von den Monozyten sezerniert wird, ist ein weiterer Stimulus für die Aktivierung der TZellen (Manetti et al. 1994). Eine weitere Funktion besitzen Monozyten in der Effektorphase der zellvermittelten Antwort. Als Effektorzellen besitzen sie Antitumor- und antimikrobielle Funktionen. Zusätzlich können sie durch Zytokinproduktion als Entzündungszellen an der Immunantwort teilnehmen (Rook 1995). 1.5 Bedeutung von IL-1 IL-1 wird von Monozyten durch LPS freigesetzt. IL-1 ist das als erste beschriebene Interleukin und spielt eine Vielzahl von wichtigen Rollen als regulatorisches Zytokin. Es wird von zahlreichen Zellen als Antwort auf Traumen, Infektionen oder Antigene gebildet: von mononukleären Phagozyten, BLymphozyten, Endothelzellen, Epithelzellen, Gliazellen, Fibroblasten, Keratinozyten, Mesangialzellen und Astrozyten. 1.5.1 Stimuli zur IL-1-Freisetzung Stimuli der monozytären IL-1-Sekretion können immunologischer, mikrobieller oder anderer Art sein. Für die immunologische Stimulation werden aktivierte T-ZellZellkontakte, Ia begrenzte Lymphokine oder Immunkomplexe verantwortlich gemacht. Bakterielle Stimuli stellen das Endotoxin (Lipid A) gram-negativer Bakterien, die Zellwand, Muramyl-Dipeptid und Exotoxin gram-positiver Bakterien, Hämagglutinin und die Doppelstrang-RNA von Viren dar. Ferner kommen als Stimuli der IL-1-Sekretion Silikate, Urate und in vitro Phorbol-Mystat in Betracht (Durum et al. 1985). Ein besonders wichtiger Stimulus ist LPS. 1.5.2 Wirkung von IL-1 auf immunkompetente Zellen IL-1 wirkt auf Zellen des Immunsystems folgendermaßen: Im Zusammenspiel mit den T-Zellen bewirkt es die T-Zell-Proliferation, die Expression von IL-2Rezeptoren und die Zytokinproduktion (Fischer et al. 1990; Davis und Lipsky 1986; Williams et al. 1985; Holsti und Raulet 1989). Bei B-Zellen bewirkt IL-1 eine 15 Zellproliferation und Differenzierung zu Plasmazellen. Eine Steigerung der Prostaglandinproduktion, der zytotoxischen Aktivität und der chemotaktischen Wirkung wird bei den Makrophagen durch IL-1 vermittelt. Ferner steigert es die zytotoxische Aktivität von Killer-Zellen (Durum et al. 1985). 1.5.3 Wirkung von IL-1 auf nicht-immunkompetente Zellen Entzündungsreaktionen werden durch die IL-1 stimulierte Produktion von Prostaglandinen und katabolen Kollagenasen unterhalten, welche bei der Knorpel-, und Knochendestruktion eine besondere Rolle spielen. IL-1 kann auch als zirkulierendes Hormon agieren, so löst es als endogenes Pyrogen im Wärmezentrum des Gehirns Fieber aus und sezerniert Akutphaseproteine aus Hepatozyten (Durum et al. 1985; Dinarello 1985 und 1991). IL-1 wirkt als Entzündungsmediator auch auf viele Zellen, die nicht zum Immunsystem gehören (siehe Tabelle 1). 16 Tabelle 1: Darstellung von Prostaglandinsynthese, Proliferation, Proteinsynthese und weiterer Wirkungen auf den menschlichen Organismus von verschiedenen, nicht zum Immunsystem gehörenden Zellen . Gewebe/ Prostaglan- Zelltyp dinsynthese Gehirn + Proliferation Protein- andere Wirkung synthese Astrozyten- - tumor Fieber, Somnolenz, Anorexie Synoviazellen + - Kollagenase proteolyt. EnzymFreisetzung Knochen/ - - Kollagenase - + - Kollagenase - Osteoklasten Knorpel/ Chondrozyten Plasminogenaktivator Muskelzellen + - - proteolyt. EnzymFreisetzung Fibroblasten + + Kollagenase - Endothel + + pro Makrophagen/ koagulatorische Neutrophilen Aktivität adhäsion verstärkt Epithelzellen - + Typ-IV-Kollagen - Leber/ - - Akutphase Hepatozyten Proteine 17 1.5.4 Die besondere Rolle von IL-1 bei verschiedenen Erkrankungen IL-1 ist bei der Entstehung und Manifestation von speziellen Erkrankungen maßgeblich beteiligt: Bei der rheumatoiden Arthritis besteht ein ständiger IL-1-Überschuß in der Synovia (Mizel et al. 1981; Bodel et al. 1968). Die Plasma IL-1-Konzentration korreliert mit der systemischen Krankheitsaktivität (Eastgate et al. 1988). Bei der Psoriasis besteht eine Zytokindysregulation. Die freigesetzten proinflammatorischen und wachstumsfördernden Zytokine steigern die T-Zellantwort auf allogenetische APC. IL-1 steigert die T-Zell-APC-Interaktion und die Aktivität der Immunzellen. Es aktiviert Fibroblasten und steigert die Adhäsion zwischen Endothelzellen und Leukozyten, was zu einem Eindringen der Leukozyten in die psoriatische Haut führt (Cooper et al. 1990). In normaler Haut besteht ein Verhältnis von IL-1a zu IL-1b von 40:1. In psoriatischer Haut besteht aufgrund der IL-1a-Reduktion und der IL-1b-Steigerung ein Verhältnis von IL-1a zu IL-1b von 1:1. Jedoch ist auch das IL-1b der psoriatischen Läsionen inaktiv und es ist ausschließlich das IL-1a , obwohl es reduziert ist, das für die biologische Aktivität verantwortlich ist. Die Tatsache, daß IL-1 bei so vielen Entzündungs- und imunregulatorischen Prozessen beteiligt ist und von so vielen verschiedenen Zellen gebildet wird, stellt die besondere und zentrale biologische Bedeutung des IL-1 heraus: IL-1 gehört zu den Zytokinen, die frühzeitig ausgeschüttet werden und deshalb richtungsweisend für die Immunantwort sein können, Welche Rolle IL-1 hingegen bei der Atopieentstehung hat ist noch nicht hinreichend geklärt. 18 1.6 Fragestellung Mit der Frage, welche Ursachen der Allergieentstehung zugrundeliegen, beschäftigten sich zahlreiche Studien der letzten Jahre (von Mutius et al. 1994; Braback et al. 1994; Bergmann et al. 1995 (1993); Bahna 1992; Holt, Mc Menamin und Nelson 1990; Willies-Jakobo et al. 1993; Pöylsä 1989; Gergen et al. 1987; Ishizaki et al. 1987 ). Es wird angenommen, daß eine atopiefördernde oder atopiehemmende Prägung des Immunsystems schon in utero beginnt (Jones et al. 1996) und in den ersten Lebensmonaten oder -jahren beendet wird. Bei der Klärung der zugrundeliegenden Pathomechanismen stehen meist die Stimulierbarkeit und zentrale Rolle der T-Helferzellen sowie deren immunologische Prägung im Vordergrund. Da die durch Makrophagen sezernierten Zytokine die T-Helferzellen aktivieren, haben Makrophagen / Monozyten dadurch auch einen atopiefördernden oder atopieprotektiven Einfluß auf die Prägung der Immunsystems. Die Atopieentwicklung hängt von zahlreichen Faktoren, wie den Einflüssen bakterieller Reize ab. LPS ist ein wichtiger bakterieller Reiz für die IL-1-Freisetzung. IL-1 hat eine zentrale biologische Bedeutung. Die Rolle von IL-1 bei der Atopieentwicklung ist jedoch noch weitgehend unklar. In wieweit sich Monozyten zum Zeitpunkt der Geburt durch Bakterienderivate zu einer Zytokinantwort stimulieren lassen, wurde in dieser Arbeit anhand von in-vitro Versuchen untersucht. Es wurde auf folgende Fragestellung eingegangen: • Inwieweit können Bakterienderivate zu einer frühen unspezifischen Zytokinproduktion von Monozyten bei Neugeborenen führen? • Gibt es Unterschiede in der Stimulierbarkeit von Monozyten zwischen Neugeborenen mit und ohne Allergierisiko? Unterscheiden sie sich hinsichtlich ihrer IL-1-Produktion nach Stimulation mit Bakterienderivaten wie LPS? 19 2 Material und Methoden 2.1 Probandenkollektiv Die Nabelschnurblutproben von den 34 Neugeborenen wurden im Zeitraum vom 25.10.1994 bis zum 27.11.1994 zur Etablierung der Technik, sowie zwischen dem 28.11.1994 und dem 19.12.1994 für die Untersuchungen gewonnen. Die Kinder wurden im St. Elisabeth Hospital oder in den Augusta Krankenhaus in Bochum entbunden. Die Eltern der Neugeborenen waren über die Studie und ihre Forschungsabsichten informiert und gaben eine schriftliche Einwilligung zur Teilnahme. Um sicher zu gehen, daß das Immunsystem nicht vorzeitig aktiviert worden war, oder fehlerhaft arbeitete, stellten Schwangerschaftskomplikationen und Frühgeburtlichkeit Ausschlußkriterien dar. In der ersten Woche nach der Geburt wurden genaue Angaben über Verlauf und Komplikationen während der Schwangerschaft und der Geburt aus den Geburtsbüchern und von den Eltern erhoben. Des weiteren wurde eine gezielte Familienanamnese hinsichtlich atopischer Erkrankungen durchgeführt. Dabei wurden folgende Daten ermittelt: • Atopische Erkrankungen der Eltern und Geschwister • Anzahl der Geschwister • Schwangerschaftsanamnese: Medikamenteneinnahme, Infektionen und Schwangerschaftsdauer • Geburtskomplikationen • Geschlecht des Neugeborenen • Geburtsgröße und Geburtsgewicht • APGAR Werte Das Atopierisiko eines Neugeborenen wurde anhand des Gesamt-IgE-Wertes im Nabelschnurblut und / oder aufgrund des Ergebnisses eines validierten Fragebogens (multizentrische Atopiestudie (MAS), siehe Anhang) festgelegt. Dabei wurde ein erhöhtes Atopierisiko als positiv ausfallende MAS (siehe Anhang) oder Ig-E-Werte > 0,9 kU/l definiert. 20 Es wurden so zwei Gruppen gebildet, eine Gruppe von Neugeborenen mit erhöhtem Atopierisiko und eine ohne erhöhtes Atopierisiko. 2.2 Isolierung mononukleärer Zellen Sofort nach der Entbindung des Neugeborenen wurde Blut aus der Vena umbilicalis der Plazenta steril entnommen und in sterile 50 ml Reagenzröhrchen zu 10 ml Pufferlösung gegeben. Die Pufferlösung bestand aus 1 ml HEPES 1M, 1 ml Penicillin (10000 IE/ml) / Streptomycin (10000 m g/ml) zur Hemmung der Keimbildung, aus 1 ml Amphotericin 250 mg/ml, sowie 20 ml Heparin-Natrium100 IE/ml zur Gerinnungshemmung; ad 100 ml Hanks Salzlösung (HBSS). Das mit HBSS im Verhältnis 1:1 verdünnte Nabelschnurblut wurde an der sterilen Arbeitsbank mit Ficoll-Trennlösung (Dichte = 1,077 g/ml) unterschichtet und anschließend bei 670 x g Umdrehungen für 20 min zentrifugiert. Die mit mononukleären Zellen angereicherte Interphase wurde abpipettiert und mit HBSS wiederholt bei 300 x g für 10 min gewaschen. Die mit Türkscher-Lösung gefärbten Zellen wurden in einer Neubauer-Zählkammer gezählt und auf eine Zellkonzentration von 1 x 106 Zellen / ml Medium eingestellt. 2.3 Untersuchung der mononukleären Zellen 2.3.1 Zellkultur Das Kulturmedium bestand aus RPMI 1640 und 4 % Zusatzlösung aus : • nichtessentiellen Aminosäuren (L-Alanin, L-Asparagin x H2O, L-Asparaginsäure, L-Glutaminsäure, Glycin, L-Prolin, L-Serin), • 100 mM Natriumpyruvat, • 200 mM L-Glutamin, • 10000 IE / ml Penicillin, • 10000 mg / ml Streptomycin, im Verhältnis 1 : 1 : 1 : 0,5 : 0,5. Die auf 2 x 10 6/ ml Medium verdünnten mononukleären Zellen wurden in 2 ml Portionen in 2 Petri-Perm Schalen gegeben und mit 2,5 mM Monensin versetzt. Ein Ansatz wurde mit LPS (1 mg/ml) stimuliert. 21 Anschließend erfolgte die Kultivierung im Inkubator bei 37° C für 8 h in einer 8 % CO2-haltigen Atmosphäre. 2.3.2 Ernten Nach 8 h (Ansatz für IL-1-Messung) bzw. nach 2 Stunden (Ansatz für TNFaMessung) wurden die mononukleären Zellen „geerntet“: sie wurden mit HBSS resuspendiert und bei 300 x g für 10 min zentrifugiert. Die Zellsuspension wurde im Anschluß mit 1 ml gekühltem 4 % Paraformaldehyd fixiert und währenddessen mehrfach aufgeschüttelt. Nach 10 min wurde mit HBSS aufgefüllt, geschüttelt und zentrifugiert. Zur Zellpermeabilisierung wurde anschließend das Zellpellet in 100 ml Saponinpuffer (HBSS mit 0,01 M HEPES und 0,1 % Saponin) je Ansatz aufgenommen. 2.3.3 Färbung der Monozyten Die Färbung der Monozyten erfolgte mittels monoklonaler, gegen Monozytenoberflächenantigene und intrazelluläre Zytokine gerichteten Antikörpern, die an die Fluoreszenzfarbstoffe Fluoresceinisothiocyanat (FITC) und Phycoerythrin (PE) gekoppelt waren. Zur späteren Darstellbarkeit des intrazellulären Zytokins IL-1 wurde der an FITC gekoppelte anti-IL-1-Antikörper verwendet. Zur späteren Darstellbarkeit des intrazellulären TNFa wurde der an FITC gekoppelte anti-TNFa -Antikörper verwendet. Um die Monozytenpopulation im Folgenden darstellen zu können, wurde mittels eines anti-CD14-PE markierten Antikörpers gefärbt. 10 ml anti-IL-1-FITC bzw. anti-TNFa-FITC und 5 ml anti-CD14-PE (entsprechend Herstellerangaben) wurden in je 100 ml der Zellsuspension gegeben und bei 4° C für 20 min inkubiert. Anschließend wurde 1 ml Saponinpuffer hinzugegeben und bei 200 x g für 5 min der nicht gebundene Anteil des Antikörpers abzentrifugiert. Die Zellpellets wurden für die durchflusszytometrische Messung in 250 ml HBSS aufgenommen. 22 2.4 Messung mit dem Durchflußzytometer Mit dem Durchflußzytometer wurde der Anteil der IL-1 produzierenden Zellen bestimmt. Das Flowcytometer FACScanTM der Firma Becton Dickinson (San José, USA) bietet die Möglichkeit, die Fluoreszenzintensität einer Zelle automatisiert zu messen. Die in einer Suspension enthaltenen weißen Blutzellen werden über eine Stahlkapillare mit Überdruck in eine Meßküvette eingeführt, so daß sie wie an einer Perlenkette nacheinander die Meßküvette passieren. Dabei können für jede einzelne Zelle bis zu 5 Eigenschaften gleichzeitig gemessen werden. Zu diesem Zweck werden die einzelnen Blutzellen durch einen 488 nm-Laser bestrahlt. Sind geeignete Fluoreszenz-Marker (z.B. FITC oder PE) an Strukturen der Blutzellen gebunden, so werden diese zur Fluoreszenz angeregt und emittieren ein Licht mit einer bestimmten Wellenlänge. Dieses wird von mehreren Detektoren aufgefangen und entsprechend seiner Intensität und Wellenlänge in ein digitales Signal umgewandelt. So kann man gleichzeitig bis zu drei verschiedene Fluoreszenzen einer Zelle getrennt voneinander messen. Für die einzelnen Leukozytensubpopulationen ist die charakteristische Größe (Vorwärtslicht) und Granularität (Seitwärtslicht) bekannt, so daß man nun diese im Dot-Plot markieren kann und für die definierte Anzahl einen dritten Parameter, z.B. den Anteil der FITC-positiven Zellen bestimmen kann. Da für uns nur die Eigenschaften der Monozyten von Interesse war, wurde ein Lifegate gesetzt und somit nur diese Zellen für weitere Information gespeichert. So konnte die Anzahl der gemessenen Monozyten verhältnismäßig gesteigert werden. Des weiteren wurde um die Monozytenregion ein Gate gesetzt, und die darin enthaltenen anti CD14-PE markierten Zellen gegen die anti IL-1-FITS markierten Zellen, bzw. die CD14-PE markierten Zellen gegen die anti TNFa markierten Zellen aufgetragen. Die Messwerte werden in Prozent CD14 positiven Zellen ermittelt. 23 Lifegate Größe!! Abbildung 2: Durch Größe und Granularität können die Monozyten aus der Lymphozytenpopulation bestimmt und mit einem Lifegate markiert werden. 2.5 Nabelschnur Gesamt-IgE Die Bestimmung der Nabelschnur Gesamt-IgE-Werte erfolgte nach Beendigung der Studie mit konventionellen Immunoassays. Vollblutproben wurden, nachdem sie geronnen waren, für 15 min mit 1850 x g zentrifugiert, der Überstand in 1,5 ml Gefäße gefüllt und bei -70° C eingefroren. Zur Durchführung des Immunoassays gemäß den Herstellervorschriften wurden alle Proben aufgetaut und jeweils 100 ml zur Analyse entnommen. Die Nachweisgrenze lag bei 0,18 kU/l. Die Werte wurden nach Doppelbestimmung gemittelt. 24 2.6 Statistik Es wurde der Wilcoxon-Rangsummentest für unverbundene Stichproben (siehe Abbildung 5), sowie der Wilcoxon-Vorzeichenrangtest für verbundene Stichproben (siehe Abbildung 4) angewandt. Graphisch werden empirische Quantile einer Stichprobe in einem sogenannten Box-and-whiskers-Plot zusammengefasst (siehe Abbildung 4 und 5). Das bietet eine grobe Information über die Symmetrie der Verteilung des Medians. Die Box im Box-and-whiskers-Plot wird durch das 25 %und das 75 %-Quantil (auch als 1. und 3. Quartil bezeichnet) begrenzt. In der Mitte des Kastens ist der Median eingezeichnet. An das obere und untere Ende des Kastens schließen sich die sogenannten Whiskers („Schnurrhaare“) an. Die Whiskers werden bis zum 5 %-(95 %-) Quantil (auch 5tes bzw 95stes Perzentil bezeichnet) gezeichnet (Trampisch und Windeler 2000). Die Bestimmung des Korrelationskoeffizienten erfolgte nach Spearman. Die statistischen Berechnungen wurden mit dem Programm PC Statistik Version 1.1 durchgeführt. 25 3 Ergebnisse 3.1 Probandenkollektiv Fragebogenauswertung / Geburtsbuch An der Studie nahmen 34 Neugeborene teil, 17 weibliche und 17 männliche. Ihr Geburtsgewicht lag zwischen 2400 g und 4060 g, die Körpergröße variierte zwischen 48 cm und 56 cm. Sie wurden zwischen der 37. und 42. Schwangerschaftswoche geboren und die von einem Gynäkologen bestimmten APGAR-Werte nach 1, 5 und 10 min lagen zwischen 7 und 10. Das Alter der Mütter lag zwischen 17 und 37 Jahren, das der Väter zwischen 23 und 44 Jahren. Die Neugeborenen hatten zwischen 0 und 2 Geschwister. 3.1.1 Atopierisikogruppe und Nicht-Risikogruppe Die Probanden konnten zwei Gruppen zugeordnet werden, eine Gruppe mit erhöhtem Atopierisiko (Risikogruppe) und eine Gruppe ohne erhöhtes Atopierisiko (Kontrollgruppe). Dabei verteilten sich die Mittelwerte, Minimum / Maximum der einzelnen Parameter wie folgt: 26 Tabelle 2: Charakterisierung der Probandengruppe Alter der Mutter (Jahre) Alter des Vaters (Jahre) Geschlecht Geschwisterzahl (Zahl) Gestationsalter (SSW) Gewicht (g) Größe (cm) APGAR 1 min APGAR 5 min APGAR 10 min Risikogruppe n=19 Kontrollgruppe n=15 29,7 (22 - 37) 32,4 (23 - 44) männlich/ weiblich 10 / 9 0,8 (0 – 2) 39,2 (36 - 42) 3349 (2350 - 4250) 50,5 (45 - 54) 8,7 (8 - 10) 9,8 (9 - 10) 9,8 (9 - 10) 25,9 (17 - 34) 31,1 (26 - 40) männlich/ weiblich 7/8 0,9 (0 - 2) 39,4 (36 - 42) 3180 (2650 - 3710) 50,8 (46 - 56) 8,7 (7 - 10) 9,5 (8 - 10) 9,9 (9 - 10) Darstellung von Median und Minimum / Maximum (in Klammern) 3.1.2 Die Einflußfaktoren Die Neugeborenen der Risikogruppe und der Kontrollgruppe waren hinsichtlich ihres Gewichtes, ihrer Größe, ihrer APGAR Werte, der Schwangerschafsdauer, der Geschwisteranzahl und des Alters der Eltern normalverteilt. Diese Parameter zeigten keine statistisch signifikanten Unterschiede zwischen Risiko- und Kontrollgruppe. Es fanden sich auch keine Unterschiede zwischen den beiden Gruppen, was die Ernährung und das Rauchverhalten der Mütter betraf. Bezüglich eines vorzeitigen Blasensprungs oder Schwangerschafts- oder Geburtskomplikationen fanden sich ebenfalls keine statistisch signifikanten Unterschiede zwischen Risiko- und Kontrollgruppe. 27 3.2 Interleukin-1-Untersuchungen 3.2.1 IL-1-Kinetik Um den bestmöglichen Zeitpunkt der IL-1-Produktion herauszufinden, wurde die monozytäre IL-1-Produktion nach Stimulation mit LPS nach 2, 4, 6 und nach 8 Stunden durchflußzytometrisch gemessen. Nach 2 und nach 4 Stunden konnte noch keine IL-1-Produktion gemessen werden. Nach 6 Stunden konnte eine geringe und nach 8 Stunden eine zufriedenstellende IL-1-Produktion verzeichnet werden, so daß in dieser Arbeit im weiteren Verlauf die IL-1-Messung nach 8 Stunden erfolgte (vgl. Abb. 3). IL-1 Kinetik 6 5 % 4 3 2 1 0 2 4 6 8 Stunden nach LPS-Stimulation Abbildung 3: IL-1-Kinetik: Durchflußzytometrische Messung der IL-1 produzierenden Monozyten in Prozent nach 2, 4, 6 und 8 Stunden Stimulation mit LPS. 28 3.2.2 Unstimulierte und durch Bakterienderivate stimulierte IL-1-Produktion von Nabelschnurblutmonozyten Nach 8-stündiger Stimulation mit Lipopolysaccharid (LPS) produzieren Nabelschnur-blutmonozyten Neugeborener unabhängig von einem bestehenden Atopierisiko vermehrt IL-1. Es konnte durchflußzytometrisch ein signifikanter Anstieg (p <0,0001) der IL-1 produzierenden und mit LPS stimulierten Monozyten verzeichnet werden. In den Zellansätzen ohne LPS konnte dieser Anstieg nicht festgestellt werden (vgl. Abb. 4). IL-1 produzierende Monozyten in % IL-1 produzierende Monozyten in % 15 x 10 x x 5 0 IL-1 ohne LPS IL-1 mit LPS Abbildung 4: Einfluß von LPS auf die IL-1-Produktion aller Probanten. Vor und nach Stimulation mit LPS wurden durchflußzytometrisch die IL-1 positiven Monozyten ermittelt und in Prozent dargestellt. 29 3.2.3 Zusammenhang der IL-1-Produktion mit dem Atopierisiko Nach 8-stündiger Inkubation der mononukleären Zellen zeigten sich signifikante Unterschiede zwischen der Risikogruppe und der Kontrollgruppe hinsichtlich der IL1-Produktion von Nabelschnurblutmonozyten nach Stimulation mit LPS (vgl. Abb. 5). Abbildung 5: Nach 8-stündiger Stimulation mit LPS wurden duchflußzytometrisch die IL-1 produzierenden Nabelschnurmonozyten bestimmt und zwischen Atopierisikogruppe und der Gruppe ohne Atopierisiko verglichen. In der Atopierisikogruppe waren signifikant mehr IL-1 produzierende Monozyten in Prozent. 30 3.2.4 IL-1- und TNFa-Produktion im Vergleich Die IL-1-Produktion der Nabelschnurblutmonozyten nach Stimulation mit LPS steht in keinem Zusammenhang mit der TNFa-Produktion bei Neugeborenen mit und ohne Atopierisiko. In einem Parallelversuch dieser Studie, mit dem selben Probandenkollektiv, wurde der Anteil der TNFa produzierenden Monozyten im Nabelschnurblut festgestellt und mit dem Prozentsatz der IL-1 produzierenden Monozyten verglichen. Es konnte keine Korrelation zwischen den gemessenen Parametern der beiden Gruppen (Atopierisiko- und Kontrollgruppe) beobachtet werden (vgl. Abb. 6). Abbildung 6: Nach Stimulation mit LPS wurden durchflußzytometrisch dieTNFa produzierenden mit den IL-1 produzierenden Nabelschnurmonozyten von Risiko- und Kontrollgruppe verglichen. Es besteht keine Korrelation. 31 3.3 Korrelation zwischen IgE und IL-1 Die erhöhten IgE-Konzentrationen korrelieren nicht mit der erhöhten monozytären IL-1-Produktion im Nabelschnurblut Neugeborener mit und ohne erhöhtem Atopierisiko. Weder in der Atopierisikogruppe noch in der Kontrollgruppe korrelieren die mit Hilfe des Enzymimmunoassays bestimmten, erhöhten IgE-Werte mit der durchflußzytometrisch gemessenen erhöhten IL-1-Produktion der Nabelschnurblutmonozyten nach Stimulation mit LPS (vgl. Abb. 8). Abbildung 7: Korrelation der IgE-Konzentration (kU/l) im Nabelschnurblut mit dem Prozentsatz an IL-1 produzierenden Monozyten nach 8 stündiger LPS-Stimulation. Korrelationskoeffizient r=0,1785, Signifikanzniveau p=0,1563. 32 4 Diskussion Nabelschnurblutmonozyten von Kindern mit Atopierisiko produzieren signifikant mehr IL-1, als die Nabelschnurblutmonozyten der Kinder ohne Risiko. Diese Arbeit wurde durchgeführt um die Frage zu hinterleuchten, welche Rolle IL-1 bei der Allergieauslösung spielt. 4.1 Bedeutung der erhöhten IL-1-Werte für die Atopieentstehung Die Ergebnisse unserer Untersuchungen legen nahe, daß IL-1 eine Allergieauslösung fördert, da die Monozyten der Kinder mit erhöhtem Atopierisiko mehr IL-1 produzieren. IL-1 unterstützt anscheinend die Th2-Differenzierung So berichtet auch Manetti (1994), daß IL-1 die Prägung der T-Zellen in Richtung IL4 produzierende, allergiefördernde Th2-Zellen begünstigt, welche B-Zellen zur Produktion von IgE stimulieren (Bergstedt-Lindquist et al. 1988, Finkleman 1988, Pene et al. 1988 a/b, Del Prete et al. 1988). In der vorliegenden Arbeit ließ sich die IL-1-Produktion schon zum Zeitpunkt der Geburt steigern, es bestanden Unterschiede zwischen den Werten bei Neugeborenen mit und ohne Atopierisiko. Das könnte bedeuten, daß bereits zu diesem Zeitpunkt eine atopiefördernde Prägung des Immunsystems stattfindet oder bereits stattgefunden hat, bzw. eine genetische Veranlagungen verstärkt wird oder wurde. Manetti et al. (1994) sieht IL-1 als Kostimulator für die Th2-Proliferation an. TaylerRobinson et al. (1994) unterstützten diese These. Sie stellten heraus, daß Th2-Zellen in hoher Dichte IL-1-Rezeptoren exprimieren und durch IL-1 im Wachstum gefördert werden. Die Th1-Proliferation scheint dagegen jedoch unabhängig von IL1 zu sein. Auch Lichtman et al. (1988) sehen IL-1 als Kostimulator der Th2Proliferation, nicht jedoch der Th1-Proliferation an. Auch sie stellten fest, daß nur Th2-Zellen die hochaffinen IL-1-Rezeptoren exprimieren. Es sei darauf hingewiesen, daß andere Untersuchungen zu dem Ergebnis kamen, daß IL-1 an der Aktivierung von INF-g produzierenden Th1-Zellen beteiligt sein soll, und somit eher eine allergiehemmende Wirkung haben soll (Skeen und Ziegler 1995, Fischer et al. 1990). 33 Man darf jedoch nicht außer Acht lassen, daß IL-1 zwar wichtig für die primäre unspezifische Abwehrreaktion ist, daß es aber nur einer von vielen Faktoren ist, der zur T-Helferzellaktivierung beiträgt. Zu den früh sezernierten Monokinen gehören IL-12 und TNF, welche immunstimulierend wirken, sowie IL-10, welches eine hemmende Wirkung auf das Immunsystem hat. Diese Zytokine leisten ebenfalls einen wichtigen Beitrag zur T-Zellaktivierung. Welches dieser Zytokine die dabei vorrangige Rolle spielt, und wie diese Zytokine voneinander abhängen, ist noch nicht ganz geklärt. In einem Parallelversuch dieser Studie mit dem selben Probandenkollektiv wurde die TNFa-Produktion untersucht, in der Annahme es habe eine Bedeutung in der Allergieauslösung. Es konnte jedoch kein signifikanter Unterschied der TNFaProduktion von Nabelschnurblutmonozyten zwischen den Kindern mit und ohne Atopierisiko festgestellt werden. Anderson berichtet (1992), daß als erstes Monokin der frühen unspezifischen Abwehrreaktion TNFa 2h nach einem Antigen-Kontakt (mit LPS) sezerniert wird. Ihm folgt das IL-1 und das IL-6 nach ungefähr 4-6 h. IL-12 welches vor allem durch T N F a induziert wird, wird erst Stunden später sezerniert. Für ein intaktes Immunsystem ist ein Gleichgewicht dieser Monokine von entscheidender Bedeutung. Wenn es nun in frühen Lebensabschnitten zu einer überschießenden Aktivierung oder Hemmung dieser Zytokinproduktion kommt, kann dies zu der Entwicklung einer Atopie beitragen. Die Funktion des IL-10 z.B., welches die Produktion der anderen frühen Monokine herunterregeln kann, ist von großer Bedeutung. Es vermag das Immunsystem vor überschießenden Entzündungreaktionen zu bewahren (De Waal Malefyt et al. 1991 und Fiorentino et al. 1991). 4.2 Der IL-1-Rezeptor und die Signaltransduktion Der IL-1-Rezeptor (IL-1RI) interagiert mit dem IL-1-Rezeptor assoziiertem Protein (IL-1RAcP) und formiert einen Komplex, der die Signaltransduktion auslöst. Die Aktivierung des Komplexes durch IL-1 steigert die Bildung einer großen Anzahl entzündungstypischer Gene. Es gibt zahlreiche Rezeptoren bei Säugetieren, die homologe rezeptorartige Proteine besitzen, sowie die der Drosophila Fruchtfliege namens Toll. So existiert eine IL-1R/ toll-like receptor (TLR) superfamily mit ihrer 34 Toll/ IL-1R (TIR) Domäne. Bis jetzt sind 6 TLRs bekannt. Die Superfamilie teilt sich in 2 Hauptgruppen, die eine hat 3 Immunglobulindomänen, die andere hat extrazelluläre Leuzinketten. IL-1, IL-18 und LPS, alle zur IL-1/ TLR superfamily gehörend, haben die gleichen Aktivierungswege. MyD88 ein rein zytosolisches Protein fungiert als Adapter der Superfamilie. Es verbindet die TIR Domäne mit den stromabwärts liegenden Signalproteinen, der IL-1R assoziierte Kinase (IRAK) oder dem TNF-Rezeptor assoziierten Faktor 6 (TRAF-6). Die aktivieren wiederum den Transkriptionsfaktor NF-kB, p38 mitogen-aktivierte Proteinkinase (MAPK) und N-terminale Kinase (JNK), (O’Neill und Dinarello 2000). Siehe Abbildung 9. Aufgrund dieser Erkenntnisse gibt es Überlegungen die MyD88-Rekrutierung und somit die Signalausbreitung und die damit verbundenen Entzündungsreaktionen z.B. bei der Behandlung der Sepsis, zu unterbinden. Man ist auf der Suche nach einem Molekül, einem antiinflammatorischen Agens. 35 LPS CD14 TLR-4 IL-18RAcP IL-18R IL-1RI LBP IL-18 IL-1RAcP IL-1 TIR domain MyD88 MyD88 IRAK-1 IRAK-2 TRAF-6 ≈ ≈ ≈ NF-kB p38 JNK Abbildung 9: Signaltransduktion der IL-1-, IL-18- und TLR-4-Rezeptoren 36 Die Tatsache, daß IL-1 bei so vielen Entzündungs- und immunregulatorischen Prozessen beteiligt ist und von so vielen verschiedenen Zellen gebildet wird, stellt die besondere und zentrale biologische Bedeutung des IL-1 heraus: IL-1 gehört zu den Zytokinen, die frühzeitig ausgeschüttet werden und deshalb richtungsweisend für die Immunantwort sind, da IL-1 einen entscheidenden Einfluß auf die Differenzierung der T-Helferzellen zu allergieprotektiven Th1-Zellen oder allergiefördernden Th2-Zellen hat (vgl. 1.1) (Fischer et al. 1990, Schmitz, Assenmacher und Radbruch 1993, Tayler-Robinson und Phillips 1994, Manetti et al. 1994). In der vorliegenden Untersuchung wurde die IL-1-Produktion von Nabelschnurblutmonozyten untersucht. Für die Allergieauslösung ist die Rolle der Monozyten von großem Interesse. 4.3 Die Rolle der Monozyten in der Atopieentstehung Monozyten sind in drei verschiedenen Stadien der Immunantwort beteiligt. Zeitlich an erster Stelle steht die Beteiligung der Monozyten an dem schnellen protektiven Mechanismus der frühen unspezifischen Abwehr. Anhand der Ergebnisse der vorliegenden Arbeit scheinen die Monozyten bereits in diesem Stadium einen Einfluß auf eine Atopieentwicklung zu haben. Durch Zytokinsekretion, beispielsweise dem in dieser Arbeit gemessenen IL-1, greifen sie modulierend in das Immunsystem ein. Die Monozyten Neugeborener produzieren mit einem zum Zeitpunkt der Geburt erhöhten Atopierisiko mehr IL-1, als die Monozyten der Kontrollgruppe. Im zeitlichen Verlauf spielen die Monozyten des weiteren auch als antigenpräsentierende Zellen bei der Ausbildung einer Atopie eine Rolle. Sie können bei der T-Helferzellaktivierung zu einem atopiefördernden Th2-typischen Zytokinmuster, mit Sekretion von IL-4, IL-5, IL-10 und nachfolgender IgEFreisetzung führen (Taylor-Robinson und Phillips 1994, Lichtman et al. 1988). Zuletzt haben die Monozyten in der Effektorphase einen Einfluß auf die Entwicklung einer Atopie. Monozyten können auf bestimmte Mediatoren, die an ihre 37 Oberflächenrezeptoren binden, mit einer charakteristischen Immunantwort reagieren. Für die IgE-Bindung wird beispielsweise der niederaffine Fce RII auf der Monozytenoberfläche exprimiert. B-Zellen tragen normalerweise Fce RIIa auf ihrer Oberfläche, während die Expression des Fce RIIb auf T-Zellen, B-Zellen, Monozyten und Eosinophilen eine Induktion durch IL-4 benötigt. Bei Atopikern kann eine verstärkte Expression von dem Fce RIIb+ zeitgleich zu einem IgE-Anstieg beobachtet werden (Brostoff und Hall 1995). Es konnte festgestellt werden, daß mit spezifischem IgE sensibilisierte Alveolarmakrophagen auf einen folgenden Allergenkontakt Fce RIIb exprimieren und Enzyme sezernieren. Diese Zellen scheinen an der Entstehung von allergieinduzierten Lungenkrankheiten wie Asthma und Alveolitis beteiligt zu sein. Kim et al. fanden 1990 heraus, daß Fce RII im Nabelschnurblut von Kindern, die später eine Atopie entwickelten, höher war als im Blut von Kindern, die frei von atopischen Symptomen blieben. Die Inzidenz der Entwicklung atopischer Symptome stieg mit dem Anstieg der Nabelschnurblut Fce RII. In der vorliegenden Arbeit wurden bewußt Nabelschnurblutmonozyten untersucht, es sollte das Immunsystem zum Zeitpunkt der Geburt untersucht werden. Inwieweit sind zu diesem Zeitpunkt die Monozyten an einer Allergieauslösung beteiligt? 4.4 Charakterisierung der Nabelschnurblutmonozyten (CBMC) Die vorliegende Arbeit zeigt, daß sich schon Nabelschnurblutmonozyten, die mit Bakterienderivaten stimuliert werden, zu einer verstärkten IL-1-Produktion anregen lassen, also schon zum Zeitpunkt der Geburt über eine funktionsfähige primäre und unspezifische Abwehrreaktion verfügen. Dies ist erstaunlich, da Neugeborene über ein noch weitgehend unreifes Immunsystem verfügen (Belohradsky und Marget 1989). Die Leukozyten bestehen aus vorwiegend unreifen Vorstufen und haben ihre Funktionsfähigkeit noch nicht vollständig erlangt. Die Monozyten scheinen dabei eine Ausnahme darzustellen, da sie zu einer regelrechten Immunantwort in der Lage sind, wie Untersuchungen von Speer et al. (1986) und Roncarolo et al. (1994) belegen. Er stellte fest, daß die Adhärenz, die chemotaktische Antwort und die Phagozytosekapazität der 38 Nabelschnurmonozyten mit den Eigenschaften von Monozyten Erwachsener vergleichbar sind. Weiterhin gibt es Untersuchungen (Roncarolo et al. 1994), die zeigen, daß aktivierte Nabelschnurmonozyten die gleiche Fähigkeit zur ZellStimulation wie periphere Blut Monozyten (PBMC) haben, und daß CBMC im gleichen Maße IL-2, IL-6 und TNFa nach Aktivierung produzieren wie PBMC. 4.5 Wirkung bakterieller Stimuli auf das Immunsystem 4.5.1 LPS als Bakterienprodukt – welche Rolle spielt es bei der Auslösung von Allergien Die Ergebnisse dieser Untersuchung bestätigen, daß LPS in-vitro einen wirksamen Stimulus für die Monozyten darstellt. In dieser Arbeit wurden Nabelschnurblutmonozyten untersucht, die noch keinen Kontakt mit E. coli, bzw. LPS hatten, da sie in uteri noch nicht den Magen-Darm-Trakt des Fötus besiedeln (s.o.). Somit simulierte die in-vitro-LPS-Stimulation dieser Untersuchung die immunologischen Vorgänge, die sich in den ersten Lebenswochen im Organismus des Säuglings abspielen, wenn er in Kontakt mit dem bakteriellen Toxin von E. coli, bzw. deren pathogenen Stämmen gerät. Da LPS im in-vitro-Versuch zu einer Immunantwort mit IL-1-Sekretion der Monozyten führte, stellt sich die Frage, ob schon geringe Mengen des bakteriellen Toxins LPS, wie sie physiologisch im Körper vorkommen, ebenfalls zu einer gesteigerten IL-1-Sekretion in-vivo führen. Sind also die Ergebnisse der in-vitroVersuche auf die Immunreaktion des Säuglings in den ersten Lebenswochen übertragbar, stellt sich die Frage, ob die erhöhte IL-1-Produktion eine allergiefördernde oder -hemmende Wirkung hat. Das Immunsystem reagiert auf bakterielle Stimuli mit einer T-Zell-unabhängigen, zellvermittelten Immunabwehr durch direkte Aktivierung des Komplementsystems und unmittelbarer Stimulation von Monozyten, Neutrophilen, Makrophagen und Natürliche-Killer-Zellen. Diese Zellen werden nach Phagozytose der Bakterien oder direkt durch ein Toxin aktiviert. Lipopolysaccharid (LPS) ist ein solches bakterielles Toxin. Es bindet zusammen mit dem Lipopolysaccharid bindenden Protein (LBP) an den CD14 Rezeptor der Monozyten (Tobias und Ulevitch 1993), woraufhin diese im 39 aktivierten Zustand entzündungsfördernde Zytokine, vor allem IL-1 und TNFa sowie entzündungshemmende Zytokine wie IL-10 sezernieren (Cavaillon und HaeffnerCavaillon 1990, Couturier et al. 1991, Henderson und Wilson 1996). Die Signaltransduktionskette ist aufgeklärt (O’Neill und Dinarello 2000). Siehe Abbildung 9. Die Ergebnisse dieser Arbeit lassen die Schlußfolgerung zu, daß LPS über die Stimulation der Monozyten mit konsekutiver IL-1-Sekretion zu einer atopiefördernden Th2-Antwort des Immunsystems führt, da die IL-1-Sekretion der Monozyten von Atopieriskokindern signifikant höher als die von Nichtrisikokindern ist. Bekanntermaßen führt aber die Stimulation durch Bakterienderivate zu einer atopiehemmenden Th1-Antwort. Der Grund hierfür könnte darin liegen, daß die Zellen der Kinder ohne Risiko im Allgemeinen empfindlicher, und somit zu einer gesteigerten IL-1-Sekretion fähig sind. Es könnte auch einen Einfluß gehabt haben, daß LPS als Stimulus verwendet wurde, welcher anders als andere bakterielle Stimuli wirkt. Außerdem wurde in der vorliegenden Arbeit nur IL-1 gemessen. LPS wirkt jedoch auch auf andere Zytokine, wie beispielsweise IL-12, welches die Reaktion von IL-1 maßgeblich beeinflussen bzw. aufheben kann. Die Tatsache, daß TNFa in der vorliegenden Arbeit keine Korrelation zur IL-1-Produktion aufwies, spricht auch dafür, daß andere Zytokine andere Regulationsmechanismen haben. Aufgrund der Ergebnisse der vorliegenden Arbeit ist auch folgende Schlußfolgerung zulässig: IL-1 wirkt indirekt ebenfalls auf die Th-1-Entwicklung. Ein Entzug von LPS in den ersten Lebenstagen oder Lebensmonaten könnte dazu führen, daß die Th2-Antwort geringer ausfällt. 4.5.2 Weitere bakterielle Stimuli Bakterienbestandteile gram-positiver und gram-negativer Bakterien sind in der Lage, Monozyten zur Sekretion von Zytokinen (z.B. IL-1) zu stimulieren. Die bakteriellen Stimuli wurden bereits erläutert. Man kann feststellen, daß Bakterien neben dem LPS eine Vielzahl von zytokininduzierenden Proteinen, Carbohydraten und Lipiden beinhalten oder produzieren. Jedoch ist keines so geeignet und gut charakterisiert wie das LPS, weswegen LPS als Stimulus für die Nabelschnurblutmonozyten zur IL-1-Freisetzung in der vorliegenden Arbeit ausgewählt wurde. 40 4.6 Intrazelluläre durchflußzytometrische Zytokinbestimmung Mit dem Durchflußzytometer wurde in der vorliegenden Arbeit die monozytäre IL-1-Produktion gemessen. Mit Hilfe des Durchflußzytometers ist es möglich geworden, intrazelluläre Zytokine nach Fixierung, Permeabilisation und indirekter Immunfluoreszenzfärbung flowzytometrisch zu analysieren. Es kann somit bestimmt werden, auf welche Zellen einer heterotropen Zellpopulation die gemessene Zytokinproduktion zurückzuführen ist, ohne eine Zelltrennung vornehmen zu müssen. Die Untersuchungen mit dem Durchflußzytometer haben in den letzten Jahren zunehmend an Bedeutung gewonnen, vor allem bei der Analyse der Lymphozyten und Lymphozytensubpopulationen. In dieser Arbeit konnte erstmalig die Zytokinproduktion der Monozyten dank der von Jung entwickelten Methode zur Lymphozytendiskriminierung bestimmt werden. Diese sensitive Methode vermag die genaue Durchflußfrequenz zu bestimmen, welches heißt, daß die gemessene Zytokinproduktion auf eine bekannte Zellzahl zurückzuführen ist. Es wird der Prozentsatz der Zytokin-sezernierenden Monozyten bestimmt. Hingegen kann keine Aussage über die Produktionsrate getroffen werden, mit der man die Zytokinproduktion einzelnen Zellen zuschreiben kann. Es konnte jedoch in diversen Studien (Pohl et al. 1997, Jung et al.1993) eine hohe Konkordanz zwischen der durchflußzytometrisch bestimmten intrazellulären Zytokinmessung und der mit Hilfe eines ELISA-Testes bestimmten Zytokine im Überstand der Zellkultur festgestellt werden. So kann man in der vorliegenden Arbeit von dem Anteil der IL-1 sezernierenden Monozyten auf die realen IL-1-Konzentration rückschließen. Es gibt neben dem Durchflußzytometer verschiedene Methoden der Zytokinbestimmung. Das Fluoreszenzmikroskop beispielsweise wurde von dem Durchflußzytometer abgelöst, da jenes den wesentlichen Vorteil hat, daß es bis zu fünf Eigenschaften (davon drei verschiedene Fluoreszenzfarben) gleichzeitig messen kann. Vor allem ist das Arbeiten mit dem Durchflußzytometer schneller und objektiver und die Zahl der analysierten Zellen liegt mit ca. 1000 Zellen / Minute auch weitaus höher als beim Fluoreszensmikroskop. Der ELISA-Test ist eine Methode, mit der Zytokine im Zellüberstand einer Kultur mittels spezifischer Antikörper gemessen werden können. 41 Die Unterschiede im Ausmaß der Zytokinproduktion und Bestimmung mit dem ELISA-Test können auf die schwankenden Monozytenzahlen der untersuchten Probanden zurückgeführt werden. Bei konstanten Monozytenzahlen bestünde ein Vorteil des ELISA-Tests gegenüber dem Durchflußzytometer darin, daß die Produktionsrate exakt zu bestimmen wäre, jedoch nur bei gereinigten Zellen. Die Polymerasekettenreaktion (PCR) ermöglicht eine Zytokinanalyse auf m-RNA Niveau und läßt keine direkten Aussagen über die DNA- und die Proteinebene zu, welchen in der vorliegenden Arbeit das Interesse gilt. Quantitative Aussagen mit Hilfe der PCR stellen ein aufwendiges und kostenspieliges Verfahren dar. Im Gegensatz zum ELISA und der PCR ist die Messung mit dem Durchflußzytometer materialsparender. Es werden wesentlich geringere Blutmengen benötigt, weshalb es in dieser Arbeit, in der verschiedene Parallelversuche liefen, angewendet wurde. Messung der IL-1-Produktion: In dieser Studie wurde die IL-1-Produktion der Monozyten mit Hilfe des anti-IL-1FITC untersucht. Die Charakterisierung der Monozyten erfolgte dabei mit antiCD14-PE. Die Zugabe von Monensin sicherte, daß das IL-1 im Golgi-Apparat akkummulierte (Jung et al. 1993). Durch die zusätzliche Inkubation mit Paraformaldehyd und Saponin wurde gewährleistet, daß die Zellpermeabilität erhöht wurde, und so das von den Monozyten produzierte IL-1 das anti-IL-1 binden konnte, ohne daß Oberflächenstrukturen wie CD14 zerstört werden (De Caestecker et al. 1992). Für eine unspezifische Bindung des anti-IL-1 an andere Zellstrukturen gibt es in der Literatur keinen festen Anhalt, somit ist davon auszugehen, daß die Messung die tatsächliche IL-1-Produktion (Konzentration nach Fixierung) der Monozyten erfasste. Dies wird durch Ergebnisse anderer Studien bestätigt (De Caestecker et al. 1992, Jung et al. 1993), die mit der gleichen Methode einen reproduzierbaren Anstieg der intrazellulären IL-1-Konzentration nach LPS-Stimulation beobachten konnten. 42 4.7 Einflußfaktoren der Atopieentstehung Viele Untersuchungen beschäftigen sich mit Einflußfaktoren der Atopieentstehung. In einigen Studien wurde, wie in der vorliegenden Arbeit, Nabelschnurblut untersucht, um Aussagen über das Immunsystem zum Zeitpunkt der Geburt machen, und sich mit Präventivmaßnahmen auseinandersetzen zu können. Häufig wurden dabei erhöhte IgE-Werte mit einer Atopie gleichgesetzt, da sich IgE als prädiktiver Wert einer Atopieentstehung bewehrt hat (Croner und Kjellman 1990, Bousquet, Ménardo und Michel 1984, Odelram et al. 1995, Lilja et al. 1990, Bergmann et al. 1993 und 1995). Auch in der vorliegenden Arbeit war die IgE-Konzentration im Nabelschnurblut von Neugeborenen mit Atopierisiko signifikant höher als bei den Kindern ohne Atopierisiko. Die erhöhten IgE-Konzentrationen korrelieren jedoch nicht mit der erhöhten monozytären IL-1-Produktion von Kindern mit und ohne erhöhtem Atopierisiko. Einfluß genetischer Veranlagung auf die Atopieentwicklung: Es besteht ein Unterschied im Ausmaß der IL-1-Sekretion der Nabelschnurblutmonozyten in Abhängigkeit eines bestehenden Atopierisikos zum Zeitpunkt der Geburt. Die Tatsache, daß die Schleimhäute wie oben erwähnt noch nicht mit (fakultativ) pathogenen Bakterien bzw. Bakterienbestandteilen besiedelt sind, und die endgültige Ausreifung des Immunsystems mit der Geburt beginnt, spricht dafür, daß genetische Veränderungen zu der veränderten Reaktionsweise der CBMC beigetragen haben. Postma et al. beschrieben 1995 die enge Nachbarschaft der Gene, die für die Regulation des IgE-Niveaus und die Entwicklung eines hyperreagiblen Bronchialsystems verantwortlich sind. Die Genorte, die für die Zytokine IL-4, IL-5, IL-13 und für CD14 kodieren, konnten in nächster Nachbarschaft auf dem Chromosomen 5q31 lokalisiert werden. Es liegt die Vermutung nahe, daß sie gemeinsam vererbt werden. Der Synergismus dieser Zytokine könnte entscheidend für die Ausprägung einer Atopie sein. Inzwischen sind eine Vielzahl von Genorten lokalisiert, die für die Atopieentstehung mitverantwortlich sind (Kabesch 2001). 43 4.8 Atopiemarker im Nabelschnurblut Seit Jahren ist man auf der Suche nach Vorhersagemöglichkeiten einer Atopie bereits zum Zeitpunkt der Geburt. Es wäre erstrebenswert, anhand eines Wertes eine Aussage über eine spätere Atopiemanifestation treffen und somit geeignete Präventivmaßnahmen ergreifen zu können. Der IgE-Wert war in den 80er Jahren ein Hoffnungsschimmer bei diesen Bestrebungen. In 67 % der Fälle gehen erhöhte IgEWerte zum Zeitpunkt der Geburt mit einer späteren Atopiemanifestation einher (Croner und Kjellman 1990). Auch in der vorliegenden Arbeit konnte gezeigt werden, daß das IgE bei Neugeborenen mit Atopierisiko signifikant höher ist als bei Neugeborenen ohne Atopierisiko. Jedoch erscheint es wenig sinnvoll, IgE als Screening-Wert für die Vorhersagemöglichkeit einer Atopieentstehng einzuführen. Die IgE-Werte sind äußerst spezifisch aber nicht sehr sensitiv. Die Sensitivität der Vorhersagemöglichkeit der IgE-Werte war im Vergleich zu der der Familienanamnese niedrig, die Spezifität war hingegen im Vergleich zu der Familienanamnese sehr hoch (Croner und Kjellman 1990). Es wurden noch weitere Marker auf ihre Vorhersagemöglichkeit hinsichtlich einer Atopiemanifestation untersucht: Hattevig et al. (1984) untersuchte IgE-Werte. Er stellte fest, daß sich bei Kinder mit stark erhöhten IgE-Werten (>1,3 kU/l) eine Atopie manifestierte. Ergebnisse von Kim et al. (1990) deuteten einen Zusammenhang zwischen Fce RII und der Entwicklung einer atopischen Funktionsstörung an, denn der IgE bindende Faktor war im Nabelschnurblut von Kindern, die später eine Atopie entwickelten, höher als im Blut von Kindern, die frei von atopischen Symptomen blieben. Magnusson und De Weck (1989) betrachteten die Thrombozytenzahlen von Neugeborenen. Sie waren bei Neugeborenen mit erhöhten IgE-Werten (>1.20 kU/l) erniedrigt, und die Kinder, die im Folgenden eine Atopie entwickelten, hatten zum Zeitpunkt der Geburt niedrigere Thromozytenwerte, als solche, die keine atopischen Symptome zeigten. Des weiteren beobachteten verschiedene Autoren eine Veränderung der Fettsäurezusammensetzung bei Allergikern (Strannegard et al. 1987 und Rocklin et al. 1986). Außerdem konnte eine veränderte Phosphordiesterase-Aktivität bei Atopikern bzw. Neugeborenen mit positiver Familienanamnese festgestellt werden 44 (Grewe et al. 1982, bzw. McMillan et al. 1985). Es gibt auch Äußerungen, die eine Veränderung der T-Zellen bei Atopikern beobachtet haben wollen (Juto und Strannegard 1979): z.B. Defekte der T-Zellregulation (Chandra und Baker 1983). Zusammenfassend läßt sich sagen, daß kein Marker für sich betrachtet, ausreichen würde eine Atopieentstehung vorhersehen zu können. Außerdem sollte geklärt werden, ob diese Veränderungen im Nabelschnurblut wie die in der vorliegenden Arbeit gemessenen erhöhten IL-1-Werte oder die anderen eben erwähnten Marker, nicht sekundäre Veränderungen auf eine genetisch determinierte Veranlagung sein können. Vielleicht können die gemessenen Veränderungen aber auch eine Reaktion auf eine Sensibilisierung in uteri auf mütterliche Allergene sein. 45 5 Zusammenfassung Zahlreiche Untersuchungen konnten die zentrale Rolle der Monozyten im Immunsystem und im Speziellen die Rolle bei der Entwicklung einer Atopie herausstellen. In der vorliegenden Arbeit wurde insbesondere die Rolle der Nabelschnurblutmonozyten bei der Atopieentstehung näher beleuchtet. Ziel dieser Arbeit war es, zu zeigen, ob und in wieweit sich Monozyten zum Zeitpunkt der Geburt zu einer Zytokinantwort durch Lipopolysaccharid stimulieren lassen, und in wieweit die Stimulierbarkeit von einem bestehenden Atopierisiko der Neugeborenen abhängt. Die mononukleären Nabelschnurblutzellen von 19 Neugeborenen mit und 15 Neugeborenen ohne Atopierisiko wurden 8 Stunden mit Lipopolysaccharid (LPS) stimuliert. Anschließend konnte die Monozytenpopulation mittels des Oberflächenmarkers antiCD14-PE und des IL-1-Antikörpers (anti-IL-1-FITC) hinsichtlich ihrer IL-1Produktion durchflußzytometrisch analysiert werden. Nabelschnurmonozyten ließen sich durch LPS zu einer gesteigerten IL-1-Produktion stimulieren, wobei die Monozyten der Neugeborenen mit Atopierisiko signifikant mehr IL-1 produzierten als die Monozyten der Kinder der Kontrollgruppe. Diese Ergebnisse legen nahe, daß IL-1 eine atopiefördernde Wirkung auf das Immunsystem hat. Nabelschnurblutmonozyten verfügen zum Zeitpunkt der Geburt über eine funktionsfähige primäre unspezifische Abwehr, da sie sich durch LPS zu einer verstärkten Zytokinproduktion stimulieren lassen. Dieses zeigt, daß die Nabelschnurblutmonozyten in diesem frühen Stadium bereits einen Einfluß auf die Atopieentwicklung haben. 46 6 Ausblick Die Ergebnisse dieser Untersuchung legen nahe, daß die Monozyten an der Prägung des Immunsystems bezüglich einer Atopie beteiligt sind. Monozyten atopisch veranlagter Neugeborener produzieren vergleichsweise mehr IL-1 und können so die Prägung der T-Helferzellen stärker beeinflussen als Monozyten Neugeborener ohne erhöhtes Atopierisiko. Monozyten agieren als APC, jedoch können Dendritische Zellen im Vergleich dazu in wesentlich höherem Maße T-Zellen aktivieren und T-zellabhängige Zytokine wie das IL-2 und IFN-g induzieren. Das mag an einer höheren Expression von CD80, MHCII und ICAM I auf der Oberfläche von den Dendritischen Zellen liegen, die ihnen eine besonders wirksame Trauben-/ Gruppenbildung mit den T-Zellen ermöglicht (Kanangat et al. 1995). Anscheinend sind die Dendritischen Zellen die bedeutenderen APC, sie sind hauptsächlich für die T-Zellaktivierung mit konsekutiver Zytokinausschüttung verantwortlich. Es wäre also sinnvoll das Augenmerk bei zukünftigen Untersuchungen auf die Dendritischen Zellen und deren Rolle in der Immunantwort zu richten. Zur Klärung der Frage, welche Auswirkungen die permanente low-dose Freisetzung auf das Immunsystem hat, bedarf es zukünftig weiterer Untersuchungen, in denen mit verschiedenen LPS-Konzentrationen stimuliert werden sollte. 47 7 Literaturverzeichnis Anderson, J., Nagy, S., Björk, L., Abrams, J., Holm, S., Anderson, U. Bacterial toxin-induced cytokine production studied at the single-cell level Immnunological Reviews 127: 69-96 (1992) Andrae, S., Axelson, O., Björkstén, B., Fredriksson, M., Kjellman, N.I.M. Symptoms of bronchial hyperreaktivity and asthma in relation to environmental factors Archives Disease Childhood 63: 473-478 (1988) Arshad, S.H., Hide, D.W. Effect of environmental factors on the development of allergic disorder in infancy Allergy clin. Immunol. 90: 235-241 (1992) Bahna, S.L. Breast milk and special formulas in prevention of milk allergy Adv. Exp. Med. Biol. 310: 445-451 (1991) Bahna, S.L. Factors Determing Development of Allergy in Infants Allergy Proc. Vol. 13: 21-25 (1992) Bahna, S.L. Is breast the best? Am. J. Report Immunol. Mikrobiol. 10: 127-131 (1986) 48 Belohradsky, B.H, Marget,W. Neugeboreneninfektionen In: Bachmann, K.D., Ewersbeck, H., Joppich, G., Kleihauer, E., Rossi, E., Halder, G.R. Pädiatrie in Praxis und Klinik Gustav Fischer Verlag, Georg Thieme Verlag, Stuttgart New York (1989) Bergmann, K. E., Bergmann , R. L., Bauer, C.P., Dorsch, W., Forster, J., Schmidt, E., Schulz, J., Wahn, U. Atopie in Deutschland, Untersuchung zur Vorhersagemöglichkeit einer Atopie bei Geburt, erste Ergebnisse der Multizentrischen Allergie-Studie Deutsches Ärzteblatt 90: 1341-1347 (1993) Bergmann, R.L., Schulz, J., Gunther, S., Dudenhausen, J.W., Bergmann, K.E., Bauer, C.P., Dorsch, W., Schmidt, E., Lau, S. Determinants of cord-blood IgE concentrations in 6401 German neonates Allergy 50: 65-71 (1995) Bergstedt-Lindquist, S., Moon, H.B., Persson, U., Moller, G., Heusser, C., Severinson, E. Interleukin 4 instructs uncommitted B lymphocytes to switch to IgG1 and IgE Eur. J. Immunol. 18: 1073-1077 (1988) Bhakdi, S., Klonisch, T., Nuber, P., Fischer, W. Stimulation of monokine produktion by lipoteichoic acids Infect. Immun. 59: 4614-4620 (1991) Bjorksten, B., Kjellman, N.I.M. Effects of maternal avoidance of egg, cow’s milk and fish during lactation upon allergic manifestations in infants Clin. Exp. Allergy 19: 27-32 (1989) 49 Bodel, P.T., Hollingsworth, J.W. Pyrogen release from human synovial exudate cells Br. J.Exp.Pathol. 49: 11-19 (1968) Bousquet, J., Menardo, J.L., Michel, F.B. Predictive capacity of cord blood IgE for the development of allergy in infancy and childhood Ann. Allergy 53: 692-695 (1984) Braback, L., Breborowicz, A., Dreborg, S., Knutsson, A., Pieklik, H., Bjorksten, B. Atopic sensitization and respiratory symptoms among Polish and Swedish school childreen Clin. Exp. Allergy 24: 826-835 (1994) Brostoff, J., Hall, T. Überempfindlichkeit - Typ-I-Reaktion In: Roitt, I., Brostoff, J., Male, D. Kurzes Lehrbuch der Immunologie Georg Thieme Verlag Stuttgart New-York (1995) Cavaillon, J.M., Haeffner-Cavaillon, N. Signals involved in interleukin 1 synthesis and release by lipopolysaccharidestimulated monocytes/macrophages. Cytokine 2: 313-329 (1990) Chandra, R.K., Baker, M. Numerical and functional deficiency of suppressor T-cells precedes development of atopic eczema Lancet 2: 1393-1394 (1983) 50 Chandra, R.K., Puri, S., Suraiya, C., Cheema, P.S. Influence of maternal food antigen avoidance during pregnancy and lactation on incidence of atopic eczema in infants Clin. Allergy 16: 563-569 (1986) Cookson, W.O., Hopkin, J.M. Dominant inheritance of atopic immunglobulin-E responsivness Lancet 1: 86-88 (1988) Cooper, K.D., Hammerberg, C., Baadsgaard, O., Elder, J.T., Chan, L.S., Taylor, R.S., Voorhees, J.J., Fisher, G. Interleukin-1 in human skin: dysregulation in psoriasis J. Invest. Dermatol. 95: 24S-26S (1990) Corbo, G.M., Forastiere, F., Dell’Orco, V., Pistelli, R., Agabiti, N., De Stefanis, B, Ciappi, G., Perucci, C.A. Effects of environment on atopic status and respiratory disorders in children J. Allergy. Clin. Immunol. 92: 616-623 (1993) Couturier, C., Haeffner-Cavaillon, N., Caroff, M., Kazatchkine, M.D. Binding sites for endotoxins (lipopolysaccharides) on human monocytes J. Immunol. 147: 1899-1904 (1991) Croner, S., Kjellman, N.I.M Development of atopic disease in relation to family history and cord blood IgE levels. Eleven-year follow-up in 1654 children. Pediatr. Allergy Immunol. 1: 14-20 (1990) Croner, S., Kjellman, N.I.M. Predictors of Atopic Desease: Coord Blood IgE and Month of Birth Allergy 41: 68-70 (1986) 51 Davis, L., Lipsky, P.E. Signals involved in T cell activation J. Immunol. 136: 3588-3596 (1986) De Caestecker, M.P., Telfer, B.A., Hutchinson, I.V., Ballardie, F.W. The detection of intracytoplasmatic interleukin-1_, interleukin-1ß and tumor necrosis factor _ expression in human monocytes using two colour immunofluorescence flow cytometry J. Immunol. Methods 154: 11-20 (1992) De Waal Malefyt, R., Abrams, J., Bennett, B., Figdor, C.G., Vries, J.E. Interleukin 10 (IL-10) inhibits Cytokine synthesis by human monocytes: an autoregulatory role of IL-10 produced by monocytes J. Exp. Med. 174: 1209-1220 (1991) Dejana, E., Breviario, F., Erroi, A., Bussolino, F., Mussoni, L., Gramse, M., Pintucci, G., Casali, B., Dinarello, C.A., Van Damme, J., Mantovani, A. Modulation of endothelial cell functions by different molecular species of interleukin 1 Blood 69: 695-699 (1987) Del Prete, G., Maggi, E., Parronchi, P., Chretien, I., Tiri, A., Macchia, D., Ricci, M., Banchereau, J., De-Vries, J., Romagnani, S. IL-4 is an essential faktor for the IgE synthesis induced in vitro by human T cell clones and their supernatants J. Immunol. 140: 4193-4198 (1988) Dinarello, C.A. An update on human interleukin-1: from molecular biology to clinical relevance J-Clin. Immunol. 5: 287-297 (1985) Dinarello, C.A. Interleukin-1 and interleukin-1 antagonism Blood 77: 1627-1652 (1991) 52 Durum, S.K., Schmidt, J.A., Oppemheim, J.J. Interleukin 1: an immunological perspective Ann. Rev. Immunol. 3: 263-287 (1985) Eastgate, J.A., Symons, J.A., Wood, N.C., Grinlinton, F.M., di-Giovine, F.S., Duff, G.W. Correlation of plasma interleukin 1 levels with disease activity in rheumatoid arthritis Lancet 2: 706-709 (1988) Finkelman, F.D., Katona, I.M., Urban, J.F., Holmes, J., Ohara, J., Tung, A.S., Sample, J.V., Paul, W.E. IL-4 is required to generate and sustain in vivo IgE responses J. Immunol. 141: 2235-2241 (1988) Fiorentino, D.F., Zlotnik, A., Vieira, P., Mosmann, T.R., Howard, M., Moore, K.W., O’Garra IL-10 acts on the antigen-presenting cell to inhibit cytokine production by Th1 cells J. Immunol. 146: 3444-3451 (1991) Fischer, H., Hedlund, G., Kalland, T., Sjögren, H.O., Dohlsten, M. Independent regulation of IFN-g and tumor necrosis factor by IL-1 in human T helper cells J. Immunol. 145: 3767-3772 (1990) Galdiero, F., de-L’ero, G.C., Benedetto, N., Galdiero, M., Tufano, M.A. Release of cytokines induced by Salmonella typhimurium porins Infect. Immun. 61: 155-161 (1993) Gergen, P.J., Turkeltaub, P.C., Kovar, M.G. The prevalence of allergic skin test reactivity to eight common aeroallergens in the U.S. population: Results from the second National Health and Nutrition Examination Survey J. Allergy Clin. Immunol. 80: 669-679 (1987) 53 Gottschall, E.E., Katzuura, G., Arimura, A. Interleukin-1b is more potent than interleukin-1a in suppressing follicle stimulating hormone differentiation of ovarian granulosa cells Biochem. Biophy. Res. Commun. 163: 764-770 (1989) Grewe, S.R., Chan, S.C., Hanifin, J.M. Elevated leukozyte cyclic AMP-phosphodiesteras in atopic disease: a possible mechanism for cAMP-agonist hyporesponsiveness J. Allergy Clin. Immunol. 70: 452-457 (1982) Gortmaker, S.L., Walker, D.K., Jakobs, F.H., Ruch-Ross, H. Parental smoking and the risk of childhood asthma Am. J. Public Health 72: 574-579 (1982) Hattevig, G., Kjellman, B., Sigurs, N., Bjorksten, B., Kjellman, N.I. Effect of maternal avoidance of eggs, cow's milk and fish during lactation upon allergic manifestations in infants Clin. Exp. Allergy 19: 27-32 (1989) Hattevig, G., Kjellman, B., Johansson, S.G.O., Bjorksten, B. Clinical symptoms and IgE responses to commom food proteins in atopic and healthy children Clin. Allergy 14: 551-559 (1984) Henderson, B., Wilson, M. Cytokine induction by bacteria: beyond lipopolysaccharide Cytokine 8: 269-282 (1996) Holsti, M.A., Raulet, D.H. IL-6 and IL-1 synergize to stimulate IL-2 production and proliferation of peripheral T cells J. Immunol. 143: 2514-2519 (1989) 54 Holt, P.G., McMenamin, C., Nelson, D., Primary sensitisation to inhalent allergens during infancy Pediatr. Allergy Immunol. 1: 3-13 (1990) Houldsworth, S., Andrew, P.W., Mitchell, T.J. Pneumolysin stimulates produktion of tumor necrosis factor alpha and interleukin-1ß by human mononuclear phagocytes Infect. Immun. 62: 1501-1503 (1994) Ishizaki, T., Koizumi, K., Ikemori, R., Ishiyama, Y., Kushibiki, E. Studies of prevalence of Japanese cedar pollinosis among the resistents in a densely cultivated area Ann. Allergy 58: 265-270 (1987) Johns, M.A., Sipe, J.D., Melton, L.B., Strom, T.B., McCabe, W.R. Endotoxin-associatad protein: Interleukin-1-like activity on serum amyloid A synthesis and T-lymphocyte activation Infect. Immun. 56: 1593-1601 (1988) Jones, A.C., Miles, E.A., Warner, J.O., Colwell, B.M., Bryant, T.N., Warner, J.A. Fetal peripheral blood mononuclear cell proliferative responses to mitogenic and allergic stimuli during gestation Pediatr. Allergy Immunol. 7: 109-116 (1996) Jung, T., Schauer, U., Heusser, C., Neumann, C., Rieger, C. Detection of intracellular cytokines by flow cytometry J. Immunol. Methods 159: 197-207 (1993) Jung T., Lack G., Schauer U., Uberuck W., Renz H., Gelfand E.W., Rieger Ch. Decreased frequency of interferon-gamma-and interleukin-2-producing cells in patient with atopic disease J. Allergy Clin. Immunol. 96: 515-527 (1995) 55 Juto, P., Strannegard, Ö. T-lymphocytes and blood eosinophils in early infancy in relation to heredety to allergy and type of feeding J. Am. Clin. Immunol. 64: 38-42 (1979) Kabesch, M. Asthma und Allergie, Genetische Prädisposition und Umweltfaktoren Monatschrift Kinderheilkunde 149: 94-105 (2001) Kanangat, S., Nair, S., Babu, J.S., Rouse, B.T. Expression of cytokine mRNA in murine splenic dendritic cells and better induction of T cell-derived cytokines by dendritic cells than by macrophages during in vitro costimulation assay using specific antigens J. Leukoc. Biol. 57: 310-316 (1995) Kaufmann, S.H.E. Mononukleäre Phagozyten und Antigen-präsentierende Zellen In: Hahn, H., Falke, D., Klein, P. Medizinische Mikrobiologie Springer Verlag Berlin Heidelberg New-York London Paris Tokyo Hong-Kong Barcelona Budapest (1991 a) Kaufmann, S.H.E. Immunpathologie In: Hahn, H., Falke, D., Klein, P. Medizinische Mikrobiologie Springer Verlag Berlin Heidelberg New-York London Paris Tokyo Hong-Kong Barcelona Budapest (1991 b) 56 Kaufmann, S.H.E. T-Zellen In: Hahn, H., Falke, D., Klein, P. Medizinische Mikrobiologie Springer Verlag Berlin Heidelberg New-York London Paris Tokyo Hong-Kong Barcelona Budapest (1991 c) Kim, K.M., Inoue, Y., Uenoyama, Y., Mutoh, K.,Yodoi, J., Kaneshima, M., Mayumi, M., Mikawa, H. Prediction of the development of atopic symptoms in early childhood by cord IgEbinding factors (soluble Fc epsilon R2) Immunol. Lett. 24: 63-67 (1990) Koenig, J.Q., Pierson, W.E., Horike, M., Frank, R. Bronchoconstrictor responses to sulfur dioxide or sulfor dioxide plus sodium chloride droplets in allergic, nonasthmatic adolescents J. Allergy. Clin. Immunol. 69: 339-344 (1982) Kreit, J.W., Gross, K.B., Moore, T.B., Lorenzen, T.J., D´Arcy, J., Eschenbacher, W.I. Ozone-induced changes in pulmonary function and bronchial resonsiveness in asthmatics J. Appl. Physiol. 66: 217-222 (1989) Kuehr, J., Fischer, T., Karmaus, W., Meinert, R., Barth, R., Herman-Kunz, E., Forster, J., Urbanek, R. Early childhood risk faktors for sensitization at schoolage J. Allergy Clin. Immunol. 90: 358-363 (1992) 57 Lebek, G., Cottier, H. Notes on the bacterial content of the gut In: Cottier, H., Kraft, R. (eds) Gut-derived infectious-toxic shock (GITS) Curr. Stud. Hematol. Blood Transf. Basel, Karger 59: 1-18 (1992) Lichtman, A.H., Chin, J., Schmidt, J.A., Abbas, A.K. Role of interleukin 1 in the activation of T lymphocytes Proc. Natl. Acad. Sci. U.S.A. 85: 9699-9703 (1988) Lilja, G., Johansson, S.G.O., Kusoffsky, E., Öman, H. IgE levels in cord blood and at 4-5 days of age: relation to clinical symptoms of atopic disease up to 18 months of age Allergy 45: 436-444 (1990) Magnusson, C.G.M., De Weck, A.L. Is thrombopenia in cord blood indicative of intra-uterine sensitization? Allergy 44: 143-151 (1989) Manetti, R., Barak, V., Piccini, M.-P., Sampognaro, P., Maggi, E., Dinarello, C.A., Romagnani, S. Interleukin-1 favours the in vitro development of type 2 T helper (Th2) human T-cell clones Res. Immunol. 145: 93-100 (1994) McMillan, J.C., Heskel, N.S., Hanifin, J.M. Cyclic AMP-phospodiesterase activity and histamine release in cord blood leukocyte preparations Acta. Derm. Venereol. (Stockh.) Suppl. 114: 24-32 (1985) Mizel, S.B., Dayer, J.M., Krane, S.M., Mergenhagen, S.E. Stimulation of rheumatoid synovial cell collagenase and prostaglandin production by partially purified lymphocyte-activing factor (interleukin 1) Proc. Natl. Acad. Sci. USA 78: 2474-2477 (1981) 58 Mosmann, T.R., Cherwinski, H., Bond, M.W., Giedlin, M.A., Coffman, R.L. Two types of murine helper T cell clone J. Immunol. 136: 2348-2357 (1986) Mutius, E. von, Martinez, F.D., Fritzsch, C., Nicolai, T., Roell, G., Thiemann, H.H. Prevalence of asthma and atopy in two areas of West and East Germany Am. J. Respir. Crit. Care. Med. 149: 358-364 (1994) Odelram, H., Björksten, B., Leander, E., Kjellman, N. Predictors of atopy in newborn babies Allergy 50: 585-592 (1995) O’Neill, L. A.J., Dinarello, C.A. The IL-1 receptor/ toll-like receptor superfamily: crucial receptors for inflammation and host defense Immunology Today 21: 206-209 (2000) Osebold, J.W., Gershwin, L.J., Zee, Y.C. Studies on the enhancement of allergic lung sensitization by inhalation of ozone and sulfuric acid aerosol. J. Environ. Pathol. Toxicol. 3: 221-234 (1980) Pene, J., Rousset, F., Briere, F., Chretien, I., Bonnefoy, J.Y., Spits, H., Yokota, T., Arai, K., Banchereau, J. IgE production by normal human lymphocytes is induced by interleukin 4 and suppressed by interferon gamma and alpha and prostaglandin E2 Proc. Natl. Acad. Sci. U.S.A. 85: 6880-6884 (1988a) Pene, J., Rousset, F:, Briere, F., Chretien, I., Paliard, X., Banchereau, J., Spits, H., Vries, J. E. IgE production by normal human b cells induced by alloreactive T cell clones is mediated by IL-4 and suppressed by IFNg J. Immunol. 141: 1218-1224 (1988b) 59 Pohl, D., Bockelmann, C., Förster, K., Rieger, C., Schauer, U. Neonates at risk of atopy show impaired production of interferon-gamma after stimulation with bacterial products (LPS and SEE) Allergy 52: 732-738 (1997) Postma, D.J., Bleecker, E.R., Amelung, P.J., Holroyd, K.J., Xu, J., Panhuysen, C.I.M., Meyers, D.A., Levitt, R.C. Genetic susceptibility to asthma - bronchial hyperresponsiveness coinherited with a major gene for atopy New Engl. J. Med. 333: 894-900 (1995) Pöysä, L. Atopy in Children with and without a Family History of Atopy Acta Paediatr. Scand. 78: 902-906 (1989) Pöysä, L., Remes, K., Korppi, M., Juntunen-Backman, K., Atopy in children with and without a family history of atopy Acta Paediatr. Scand 78: 896-901 (1989) Riedel, F., Krämer, M., Scheibenbogen, C., Rieger, C. Effects of SO2 exposure on allergic sensitization in the guinea pig J. Allergy Clin. Immunol. 82: 527-534 (1988) Riesenfeld-Orn, I., Wolpe, S., Garcia-Bustos, J.F., Hoffmann, M.K., Tuomanen, E. Production of interleukin-1 but not tumor necrosis factor by human monocytes stimulated with pneumococcal cell surface components Infect. Immun. 57: 1890-1893 (1989) Rocklin, R.E., Thistle, L., Gallant, L., Manku, M.S., Horrobin, D. Altered arachidonic acid content in polymorphonuclear and mononuclear cells from patients with allergic rhinitis and/or asthma Lipids 21: 17-20 (1986) 60 Roncarolo, M.G., Bigler, M., Ciuti, E., Martino, S., Tovo, P.A. Immune responses by cord blood cells Blood Cells 20: 573-585 (1994) Rook, G. Zellvermittelte Immunantwort In: Roitt, I., Brostoff, J., Male, D. Kurzes Lehrbuch der Immunologie Georg Thieme Verlag Stuttgart New-York (1995) Roorda, R.J., Gerritsen, J., Van Aalderen, W.M., Knol, K. Influence of a positive family history and associated allergic diseases on the natural course of asthma Clin. Exp. Allergy 22: 597-599 (1992) Savelkoul, H.F., Termeulen, J., Coffman, R.L., Van-der-Linde-Preesman, R.A. Frequency analysis of functional Ig C epsilon gene expression in the presence and absence of interleukin 4 in lipopolysaccharide-reactive murine B cells from high and low IgE responder strains Eur. J. Immunol. 18: 1209-1215 (1988) Schmidt, J., Fleissner, S., Heimann-Weitschat, I., Lindstaedt, R., Pomberg, B., Werner, U., Szelenyi, I. Effect of corticosteroids, cyclosporin A and methotrexate on cytokine release from monocytes and T-cell subsets Immunopharmacology 27: 173-179 (1994) Skeen, M.J., Ziegler, H.K. Activation of gamma delta T cells for production of IFN-gamma is mediated by bacteria via macrophage-derived cytokines IL-1 and IL-12 J. Immunol. 154: 5832-5841 (1995) 61 Skjonsberg, O.H., Clench-Aas, J., Leegaard, J., Skarpaas, I.J., Giaever, P., Bartonova, A., Moseng, J. Prevalence of bronchial asthma in schoolchildren in Oslo, Norway. Comparision of data obtained in 1993 and 1981 Allergy 50: 806-810 (1995) Speer, C.P., Wieland, M., Ulbrich, R., Gahr, M. Phagocytic activities in neonatal monocytes Eur. J. Pediatr. 145: 418-421 (1986) Strannegard, I.L., Svennerholm, L., Strannegard, Ö. Essential fatty acids in serum lecithin of children with atopic dermatitis and in umbilical cord serum of infants with high or low IgE levels Int. Arch. Allergy Appl. Immunol. 82: 422-423 (1987) Tayler-Robinson, A.W., Phillips, R.S. Expression on the IL-1 receptor discriminates Th2 from Th1 cloned CD4+ T cells specific for Plasmodium chabaundi Immunology 81: 216-221 (1994) Tobias, P.S., Ulevitch, R.J. Lipopolysaccharide binding protein and CD14 in LPS dependent macrophage activation Immunobiol. 187: 227-232 (1993) Trampisch,H.J., Windeler, J. Medizinische Stastistik Springer Verlag Berlin Heidelberg New York 2000 Tsutsui, O., Kokeguchi, S., Matsumura, T., Kato, K. Relationship of the chemical structure and immunobiological activities of lipoteichoic acid from Streptococcus faecalis (Enterococcus hirae) ATCC 9790 FEMS Microbiol. Immunol. 3: 211-218 (1991) 62 Tufano, M.A., Rossano, F., Catalanotti, P., Liguori, G., Marinelli, A., Baroni, A., Marinelli, P. Properties of Yersinia enterocolitica porins: interference with biological functions of phagocytes, nitric oxide production and selective cytokine release Res. Microbiol. 145: 297-307 (1994a) Tufano, M.A., Rossano, F., Catalanotti, P., Liguro, G., Capasso, C., Ceccarelli, M.T., Marinelli, P. Immunobiological activities of Helicobacter pylori porins Infect. Immun. 62: 1392-1399 (1994b) Williams J.M., Deloria, D., Hansen, J.A., Dinarello, C.A., Loertscher, R., Shapiro, H.M., Strom, T.B. The events of primary T cell activation can be staged by use of sepharose-bound anti-T3 (64.1) monoclonal antibody and purified interleukin 1 J. Immunol. 135: 2249-2255 (1985) Willies-Jacobo, L., Denson-Lino, J.M., Rosas, A., O’Connor, R., Wilson, N.W. Socioeconomic status and allergy in children with asthma Allergy Clin. Immunol. 72: 630-636 (1993) Zeiger, R., Heller, S., Mellon, M.H., Forsythe, A.B., O’Connor, R.D., Hamburger, R.N., Schatz, M. Effect of combined maternal and infant food-allergen avoidance on development of atopy in early infancy: A randomized study J. Allergy Clin. Immunol. 84: 72-89 (1989) 63 8 Appendix Fragebogen zur Bestimmung des familienanamnestischen Allergierisikos 1 Haben oder hatten Sie ein juckendes Ekzem beim Kontakt bestimmter Dinge mit der Haut, z.B. unechtem Schmuck, oder nach Einnahme von Medikamenten? 1 Leiden oder litten Sie jemals an einer Neurodermitis (auch endogenes Ekzem oder atopische Dermatitis genannt)? 2 Hatten Sie wiederholt Nesselsucht, auch Urtikaria genannt, mit Quaddeln wie nach Brennessel-Kontakt und/oder Schwellungen an Lippen und Augen? 3 Leiden oder litten Sie - ohne dabei erkältet zu sein - an einer juckenden, verstopften oder laufenden Nase und/oder an verschwollenen, juckenden Augen, und zwar regelmäßig im Frühjahr oder Sommer oder fast immer bei Umgang mit bestimmten fell- oder federtragenden Tieren? 4 Haben oder hatten Sie einen Heuschnupfen (allergischen Schnupfen) oder allergische Bindehautentzündung? 5 Leiden oder litten Sie an allergischem Asthma (Bronchial-Asthma)? 6 Reagieren Sie regelmäßig auf bestimmte Nahrungsmittel allergisch (Nesselsucht, Verschlimmerung eines Ekzems, Übelkeit, Erbrechen, Durchfall, Asthma)? 7 Wurde bei Ihnen schon einmal eine Allergietestung vorgenommen, und hat der Test die Allergie nachgewiesen? 8 Wurde bei Ihnen schon einmal eine Hyposensibilisierung (Desensibilisierung, Spritzenkur) zur Allergie-Behandlung vorgenommen? 9 Sind bei Ihren leiblichen Kindern folgende Erkrankungen aufgetreten oder von einem Arzt diagnostiziert worden? 64 a) wiederholte Bronchitis mit pfeifender Atmung b) Asthma oder asthmoide Bronchitis c) Heuschnupfen (allergischer Schnupfen) d) Milchschorf und/oder juckendes Ekzem besonders in Ellbogen und Kniekehlen e) Nesselsucht (Urtikaria) g) Nahrungsmittelallergie (wie oben beschrieben) Auswertung des Fragebogens Das Neugeborene wurde der Atopierisikogruppe zugeordnet, wenn eine der Fragen 2, 4, 5, 6, 10b, 10c, 10e und/oder zwei oder mehr der Fragen 10a, 10d, 10f, 10g und/oder drei oder mehr der Fragen 3, 7, 8, 9 von der Mutter oder dem Vater des Kindes mit ja beantwortet wurden. 65 Danksagung Mein herzlicher Dank gilt meinem Doktorvater, Herrn PD Doktor Schauer, der mir das Thema überließ und diese Arbeit ermöglichte. Er stand mir in allen Fragen mit Rat und Tat zur Seite. Dem Team des immunologischen Labors der Kinderklinik danke ich für die Hilfsbereitschaft und Unterstützung. Außerdem möchte ich auch noch meinen Eltern und Freunden danken. Sie waren hilfsbereit, verständnisvoll und motivierten mich immer wieder. Lebenslauf Persönliche Daten Name Geburtstag/-ort Anschrift Telefon Familie Claudia Julia Bockelmann 16. November 1971, Ruit Frickestraße 49, 20251 Hamburg 040-46856181 Mutter: Wilma Bockelmann (Kinderärztin) Vater: Friedrich Bockelmann (Dipl. Ingenieur) Schwester: Bettina; 1970 (Dipl. Ingenieurin) Schulausbildung: 1978-1982 1982-1991 Juni 1991 Lindenschule (Grundschule) in Ostfildern Heinrich-Heine-Gymnasium in Ostfildern Abitur Studium: an der Ruhr-Universität Bochum 1991-1993 1993-1996 1993 1994 1996 1997-1998 1998 Vorklinischer Studienabschnitt Klinischer Studienabschnitt Physikum 1. Staatsexamen 2. Staatsexamen Praktisches Jahr in Remscheid und Neuchâtel (Schweiz) 3. Staatsexamen Auslandsfamulaturen in Chile und USA Berufliche Tätigkeit Mai 1998Oktober 2001 Arbeit als Ärztin in der Vestischen Kinderklinik Datteln. Seit November 2001 Arbeit als Assistenzärztin im Katholischen Kinderkrankenhaus Wilhelmstift in Hamburg