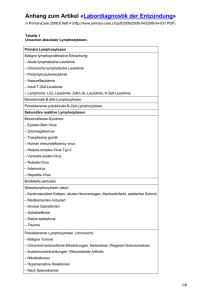
Umgang mit infektiösen Komplikationen in der Tumortherapie
Werbung

Umgang mit infektiösen Komplikationen in der Tumortherapie Prof. Dr. Georg Maschmeyer Klinikum Ernst von Bergmann Hämatologie, Onkologie und Palliativmedizin 14467 Potsdam [email protected] www.ichs.org www.dghoinfektionen.de Transparenzerklärung • Honorare für Beratungen: – Gilead; MSD; Sanofi-Aventis; Pfizer; Essex/Schering-Plough; Cephalon; Novartis; Celgene • Honorare für Vortragstätigkeiten: – Gilead; MSD; Pfizer; Cephalon; Bayer; AMGEN; Chiron; Wyeth; GlaxoSmithKline; AstraZeneca; Binding Site; Medac; JanssenCilag; Merck; Bristol-Myers Squibb; ADKA; LAGO; Bundesapothekerkammer • Honorare für Gutachten im Rahmen von Zulassungsanträgen: – Wyeth; Gilead; Pfizer; Riemser • Sponsoring von Kongressteilnahmen mit Gegenleistung: – Janssen-Cilag; Novartis; Roche; Pfizer; AMGEN; Merck Jeweils seit 2000 Die Anfänge: Tetracyclin vs Placebo => A trial of antibiotic therapy is not warranted for fever in cancer patients. Ann Intern Med 1960;53:754-64 Aktuelle DGHO-Leitlinien www.dgho-infektionen.de n = 36 in PubMed Aktuelle DGHO-Leitlinien www.dgho-onkopedia.de US-amerikanische Leitlinien J Clin Oncol 2013;31:794-810 www.idsociety.org Prädominante Erreger bei Fieber und Neutropenie Neutropenie: ESBL MRSA Gram-negative Aerobier VRE S.aureus, Streptokokken, Enterokokken, Anaerobier Koagulase-neg. Staphylokokken (ZVK) Pilze, v.a. Aspergillus, Candida, Mucoraceen T-Zellsuppression: Viren (CMV, Herpes, VZV) Pneumocystis jirovecii Pilze (s.o., plus Kryptokokken) Mykobakterien Parasiten (zB Toxoplasma gondii) Bakterien (s.o.), plus Listerien Antikörpermangel: Bakterien (s.o.), plus Pneumokokken Viren (s.o.) (selten:) Pilze Indikation zur empirischen antimikrobiellen Intervention bei Tumorpatienten • Granulozyten < 500/µl oder < 1000/µl mit erwartetem Abfall auf ≤ 500/µl • Einmalige orale Temperatur > 38.3°C – Cave antipyretischer Effekt von Steroiden, NSAID, Paracetamol, Novaminsulfon • Oder 2x ≥ 38.0°C innerhalb 12 h – oder ≥ 38.0°C über ≥ 1 h • Keine offensichtlich nicht-infektiöse Ursache – z. B. Reaktion auf Blutprodukte oder Medikamente • Therapieeinleitung innerhalb max. 2 Stunden! www.dgho-infektionen.de Fieber und Infektionen bei schwer neutropenischen Patienten Neutrophile < 1000/µl Fieber ≥ 38.5°C n = 1573 FUO n = 800 Bakteriämie/ Fungämie n = 222 51% Andere Lungeninfiltrate dokum. n = 269 Infektion n = 262 17% 14% 17% Link H et al (PEG-Studie I), Ann Hematol 1994;69:231-43 Piperacillin/Tazobactam vs Cefepim als empirische Initialtherapie bei febrilen neutropenischen Patienten • Entfieberungskurve: Bow EJ et al (multicenter), Clin Infect Dis 2006;43:447-59 Vancomycin vs Placebo bei Fieber nach 48-60 Stunden Piperacillin-Tazobactam • Doppelblind, Placebo-kontrolliert: P/T + Vancomycin (n = 86) vs P/T + Placebo (n = 79) • Mediane Neutropeniedauer < 500/µl: 14 Tage Entfieberung unter Therapie P/T + V P/T + Plc 45% 44% Tage bis zur Entfieberung (median) 3.5 ± 0.8 Infektionsbedingter Tod (Tag) 1 (14) 4.3 ± 0.8 1 (35) Cometta A et al (EORTC), Clin Infect Dis 2003;37:382-9 Linezolid vs Vancomycin empirisch bei neutropenischen Patienten mit refraktärem Fieber (n = 605) Kein signifikanter Unterschied bezüglich • Zeit bis zur Entfieberung • Todesrate Tag 16 nach Therapieende • Gesamterfolg – Keine Unterschiede bei Subgruppen mit Leukämie, Lymphom, Myelom oder anderer maligner Grunderkrankung Mikrobiologisches Ergebnis gleichwertig Jaksic B et al, Clin Infect Dis 2006;42:597-607 Empirische Antimykotika bei neutropenischen Patienten mit persistierendem FUO: Prospektiv randomisierte Studie • • Therapiewechsel nach 4-6 Tagen bei fehlendem Ansprechen Fluconazol nicht besser als kein Antimykotikum (p = 0.56) Schiel X et al (PEG-Studie II), Infection 2006;34:118-26 Algorithmus für Hochrisikopatienten mit FUO Maschmeyer G & Sandherr M, Internist 2009;50:187-202 Infektionen nach Hochdosistherapie und autologer Stammzelltransplantation Reich G et al, Bone Marrow Transplant 2001;27:525-9 Therapie invasiver Candida-Infektionen ★ ★ Nachgewiesene Sensibilität der Candida sp., keine vorherige Azolexposition, klinische Stabilität Mousset S et al (AGIHO), Ann Hematol 2013 September 12 Invasive pulmonale Aspergillose Mousset S et al (AGIHO), Ann Hematol 2013 September 12 Indikationen zur primären Modifikation der antimikrobiellen Behandlung: „Prä-Emptive“ Therapie • Lungeninfiltrate –CT typisch für Pneumocystis-Pneumonie –CT typisch für / vereinbar mit Aspergillose • Sinus- oder Kopf-CT vereinbar mit Aspergillose oder Mucormykose • Abdominelle oder perianale Infektion • ZVK-assoziierte Infektion Präemptive antimykotische Therapie: Patienten mit Fieber und Lungeninfiltraten profitieren von First-Line Amphotericin B n CR (%) NR (%) ED (%) • Zusatz von AmB nach 4-6 Tagen Non-Response 269 61.3* 17.1 21.6 • Antibiotika plus AmB von Beginn an 157 78.2* 4.2 17.6 * p < 0.01 (Fisher's exact test, zweiseitig) Link et al, Ann Hematol 1994 Schiel et al, Infection 2006 Vorgehen bei febrilen neutropenischen Patienten mit Lungeninfiltraten Maschmeyer G et al (AGIHO), Eur J Cancer 2009;45:2462–72 Entscheidend: Neutrophilenerholung - PEG-Studie I (n = 1573) - Anstieg Kein Anstieg 97.8% 86.5% < 0.001 1.5% 8.5% < 0.001 86.9% 62.3% < 0.001 7.0% 20.5% < 0.001 p FUO - Ansprechen - Tod Dokumentierte Infektion - Ansprechen - Tod Link H et al (PEG-Studie I), Ann Hematol 1994;69:231-43 Cipro/AmoxiClav oral vs Ceftriaxon/Amikacin i.v. bei febrilen Patienten mit Neutropeniedauer < 10 Tagen • n = 177 vs 176 • Neutropeniedauer nach Fieberbeginn 4 (1-18) Tage • Behandlungserfolg (ITT) 80 vs 77% - bei Pat. mit Neutropenie >7 Tage 47 vs 50% - bei Pat. mit Bakteriämie 54 vs 50% • Überleben Tag 7 – Überleben Tag 30 98 vs 97% 95 vs 95% • Nebenwirkungen – medikamentenbedingt 36 vs 31% 16 vs 15% Kern WV et al (EORTC), N Engl J Med 1999;341:312-8 Cipro + AmoxiClav oral vs Ceftazidim i.v. bei febrilen „Low-Risk“-Patienten mit Neutropenie < 10 Tagen • n = 116, doppelblind, Kinder eingeschlossen • Mediane Neutropeniedauer 3.4 vs 3.8 Tage • Erfolg (ITT) bei FUO 71 vs 67% - bei Pat. mit gesicherter Infektion • Unverträglichkeit 41 vs 33% 29 vs 7% Freifeld A et al (multicenter), N Engl J Med 1999;341:305-11 Identifikation von Niedrigrisikopatienten: MASCC Score > 21 = Low-Risk Klastersky J et al (MASCC), J Clin Oncol 2000;18:3038-51 Febrile neutropenische Niedrigrisikopatienten: 2/3 können mit oraler Antibiotikatherapie ambulant behandelt werden • 279 Episoden febriler Neutropenie, 38% MASCC low risk − 36% ungeeignet für orale antimikrobielle Therapie − 64% bekamen orale Antibiotika nach Entlassung − 95% der entlassenen Patienten blieben stabil fieberfrei − 3 notfallmäßige Wiederaufnahmen − Sterblichkeit 0% Cherif H et al (Karolinska Inst), Haematologica 2006;91:215-22 Febrile neutropenische Niedrigrisikopatienten: Therapie bei Entlassung Cherif H et al (Karolinska Inst), Haematologica 2006;91:215-22 Orales Moxifloxacin ist gleichwertig mit Cipro + AmoxiClav oral bei febrilen „Low-Risk“-Patienten Kern WV et al (EORTC), J Clin Oncol 2013;31:1149-56 Warum manchmal orale Antibiotika bei Niedrigrisikopatienten nicht möglich sind Cherif H et al (Karolinska Inst), Haematologica 2006;91:215-22 Risikoadaptierte Intervention: AGIHO www.dgho-infektionen.de Kurz angerissen • Schwere Infektionen bei älteren Patienten mit hämatologischen Neoplasien • Neue Antibiotika in der Hämatologie und Onkologie? Sterblichkeit bei Bakteriämie älterer Patienten mit hämatologischen Neoplasien • n = 358: 58% > 60 und 10% > 80 Jahre 7-Tages-Sterblichkeit: • 10% bei Patienten < 60 Jahren • 21% bei Patienten von 60-79 Jahren • 27% bei Patienten ≥ 80 Jahren Norgaard M et al (Dänemark), Br J Haematol 2006;132:25-31 Sterblichkeit bei Bakteriämie älterer Patienten: inadäquate Behandlung Norgaard M et al (Dänemark), Br J Haematol 2006;132:25-31 Neuere Antibiotika: Einsatz in der Hämatologie und Onkologie? • Daptomycin • Tigecyclin • Linezolid • Fidaxomicin Daptomycin bei neutropenischen Tumorpatienten mit G+ Bakteriämie • 84 Patienten, 86% auswertbar, davon 47% schwer neutropenisch (< 0.1 Gpt/l) • 76% Bakteriämie, meist VRE, CNS und MRSA • 88% vorbehandelt • Ansprechrate: 90% • Bei Neutropenie <0.1 Gpt/l: 85% Rolston KV et al (Registerdaten), Clin Adv Hematol Oncol 2010;8:249-56 • 37-jährige Frau mit AML unter Daptomycin entwickelte Daptomycin-resistente E. faecium-Infektion mit Bakteriämie • Entfieberung und negative Blutkulturen unter Behandlung mit Linezolid Long JK et al (Cleveland), Mayo Clin Proc 2005;80:1215-6 • Versagen bei 5/9 VRE-Bakteriämien bei neutropenischen Patienten Poutsiaka DD et al (Boston), J Infect 2007;54:567-71 Tigecyclin bei Tumorpatienten mit schweren Infektionen • 110 Pat., davon 28% neutropenisch, 25% nach SZT, 56% ITS • Bei 96% Zweitlinientherapie, 92% in Kombination • Gesamtansprechrate: 64% • 36 von 40 Versagern starben an ihrer Infektion • Bei Pneumonie: 44% Sterblichkeit Chemaly RF et al (MDACC Houston), Medicine 2009;88:211-20 Linezolid bei SZT oder Tumorerkrankungen: Klinische Ergebnisse Ergebnis Klin. Heilung* (%) Mikrobiol. Heilung* (%) Tumorpatienten Heilung Versagen Unklar 75.5 8.2 16.4 82.3 13.9 3.8 66.7** 4.2 29.1 66.6 16.7 16.7 SZT-Patienten Heilung Versagen Unklar *7-10 Tage bei Therapieende ≤ 28 Tage, 1 Mo. bei Therapie >28 Tage ** Bei neutropenischen Patienten (n=14) 85.7% Smith PF et al, Ann Oncol 2003;14:795-801 Linezolid-assoziierte Panzytopenie • 2 Patienten nach Organtransplantation • Multiresistente grampositive Infektion • Keine andere Ursache als Linezolid erkennbar • Erholung der Hämatopoese nach Absetzen von Linezolid Faguer S et al (Toulouse), Infection 2007;35:275-7 Clostridium difficile-assoziierte Diarrhoe Fidaxomicin Vancomycin Louie Cornely Louie Cornely n = 302 n =270 n = 327 n =265 Klinisches Ansprechen Rezidiv innerhalb von vier Wochen 88.2% 91.7% 85.8% 13.3% 12.7% 24% Nicht unterlegen p = 0.004 26.9% bzw. 0.0002 90.6% Louie TJ et al, N Engl J Med 2011;364:422-31 Cornely OA et al, Lancet Infect Dis 2012;12:281-9 Clostridium difficile-assoziierte Diarrhoe 84.4% Ohne B-AB 92.6% <0.001 97 h 54 h <0.001 Mit Begleitantibiotika Heilungsrate Dauer der Diarrhoe Heilungsrate Fidaxomicin 90.0% Vancomycin 79.4% Reinfektionen 16.9% 29.2% P-Wert P-Wert 0.04 <0.048 Mullane KM et al, Clin Infect Dis 2011;53:440-7 Subgruppe Tumorpatienten (n = 183): Fidaxomicin signifikant wirksamer als Vancomycin Cornely OA et al, J Clin Oncol 2013;31:2493-9