Vorlesung ACII-1 (LA) Teil 3
Werbung
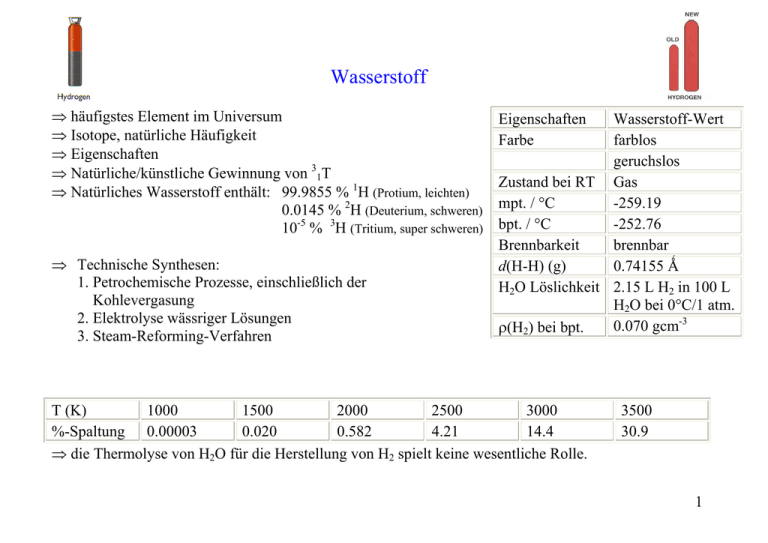
Wasserstoff
⇒ häufigstes Element im Universum
⇒ Isotope, natürliche Häufigkeit
⇒ Eigenschaften
⇒ Natürliche/künstliche Gewinnung von 31T
⇒ Natürliches Wasserstoff enthält: 99.9855 % 1H (Protium, leichten)
0.0145 % 2H (Deuterium, schweren)
10-5 % 3H (Tritium, super schweren)
⇒ Technische Synthesen:
1. Petrochemische Prozesse, einschließlich der
Kohlevergasung
2. Elektrolyse wässriger Lösungen
3. Steam-Reforming-Verfahren
Eigenschaften
Farbe
Wasserstoff-Wert
farblos
geruchslos
Zustand bei RT Gas
mpt. / °C
-259.19
bpt. / °C
-252.76
Brennbarkeit
brennbar
d(H-H) (g)
0.74155 Ǻ
H2O Löslichkeit 2.15 L H2 in 100 L
H2O bei 0°C/1 atm.
0.070 gcm-3
ρ(H2) bei bpt.
T (K)
1000
1500
2000
2500
3000
%-Spaltung 0.00003
0.020
0.582
4.21
14.4
⇒ die Thermolyse von H2O für die Herstellung von H2 spielt keine wesentliche Rolle.
3500
30.9
1
Die Gewinnung von Wasserstoff aus H2O
⇒
Elektrochemische Spaltung
Elektrolyse von H2O → H2 + O2
sehr reines Produkt
Länder mit billiger Hydro-Energie
(Ägypten, Indien, Norwegen)
⇒
Chemische Spaltung
1. Kohlevergasung
Erster Schritt liefert ’Synthese-Gas’ oder ‚Wasser-Gas’ als Produkt
(CO/H2-Mischung) (Endotherm !)
Zweiter Schritt nützt die Kohlenstoffmonoxid-Konversion (Exotherm !)
Katalysatoren: 200 ≤ T ≤ 250°C (tief-T Konversion) Cu, Zn und Al-Oxid-Mischungen
300 ≤ T ≤ 500°C (normalerweise benützte T) Fe und Chrom-Oxid-Mischungen
2
⇒
Chemische Spaltung
2. Reaktion von ‚Hydriden’ mit H2O
z. B. CaH2
Die Gewinnung von Wasserstoff aus Kohlenwasserstoffen
⇒
Chemisches Cracken von Kohlenwasserstoffen
Kombination von thermischem Kohlenwasserstoff-Cracken mit Oxidation des gebildeten
Kohlenstoffs,
nötiger Sauerstoff aus H2O,
anschließende Reaktion des mitgebildeten CO mit Dampf → CO2
3
Chemie des Wasserstoffs
⇒ Heterolytische bzw. Homolytische Spaltung der H-H-Bindung
⇒ Brønsted-Säure/-Base Eigenschaften
⇒ Lewis-Säure/-Base Eigenschaften
⇒ bildet EHn-Verbindungen mit fast allen Elementen
⇒ wirkt als Reduktions- bzw. Oxidations-Mittel
⇒ Hydrogenierungs-Reaktionen: Addition von H2 an Elemente
⇒ metallische Form bei sehr hohem Druck
⇒ Redox-Verhalten
⇒ Atomarer Wasserstoff
‚light’ (leicht):
‚heavy’ (schwer):
‚superheavy’ (super-schwer):
1
⇒ Protium
2
1H ⇒ Deuterium
3
1H ⇒ Tritium
1H
4
Chemie des ‚schweren Wasserstoffs’
⇒ Gewinnung von D2:
1. Fraktionierung von natürlichem H2
2. Spaltung von schwerem Wasser
(a) elektrolytisch (technisch)
(b) chemisch
Eigenschaften
Sdp. / K
Dampfdruck bei Smp.
(Torr)
Dissoziationsenergie
bei 298 K in kJ mol-1
H2
20.39
55.1
HD
22.13
92.9
D2
23.67
128.5
HT
23.6
124.6
DT
24.3
142.9
T2
25.04
162.0
436.2
439.6
443.6
440.9
445.5
447.2
Dissoziationsenergie, Dampfdruck, Siedepunkte
H2
D2
+
+
T2
T2
2 HT
2 DT
5
Allgemeine Formeln und Trends von Wasserstoff-Verbindungen
⇒ bildet mit jedem Element (außer den Edelgasen) mindestens eine Verbindung des Typs EHn
⇒ Hauptgruppen: stoichiometrische-Verbindungen
I
EH
II
EH2
Hauptgruppen
III
IV
V
(EH)
(EH2)
EH3
EH3
EH4
EmHn mit E-E-Bindungen
(E = B, C → Sn;
N → Sb;
O → Se)
VI
EH2
VII
EH
⇒ Nebengruppen: oft nicht-stoichiometrisch
III
EH≤3
IV
EH≤2
V
EH≤2
Nebengruppen
VI
VII
EH≤2
VIII oder 0
EH≤2
I
EH
II
EH2
6
Nomenklatur von Hauptgruppen-Wasserstoff-Verbindungen
⇒ bildet mit jedem Element (außer den Edelgasen) mindestens eine Verbindung des Typs EHn
⇒ H kann positive oder negative Partial-Ladung besitzen
⇒ Liganden, die an das Zentralatom gebunden sind, beeinflussen die Partial-Ladung des H
⇒ Ab Bor bzw. Si, Ge, Sn, Pb links = δ-H
Ab C, P, As, Sb, Bi rechts = δ+H
⇒ Nomenklatur folgt nicht der Partialladung des H
Beschreibung
Protonenaddukte von EHn
Deprotonierungsprodukte
Hydridaddukte von EHn
Name, Endung
..............onium
..............id
..............at
Beispiel
Oxonium, Telluronium
Hydrogensulfid
7
Wasserstoff-Verbindungen
⇒ Hydride (3 großen Klassen) gruppiert aufgrund von Δχ, Δ(Polarität), Strukturunterschieden
1. Kovalente oder molekulare Hydride
⇒ flüchtige, normalerweise p-Block-Hydride
⇒ kleine Δχ
⇒ H schwach positiv oder negativ polarisiert
‚Periodensystem der Elementhydride
2. Metallische Hydride
⇒ Verbindungen mit d- oder f-Block-Elementen
⇒ häufig nicht stoichiometrisch
⇒ elektrisch leitende Feststoffe
⇒ Hydrierungs-Katalysatoren
3. Salzartige Hydride
⇒ Kombination von H mit sehr elektropositiven s-Block-Metallen
⇒ nichtflüchtig
⇒ typisch ionische Strukturen
⇒ nicht-leitend im festen Zustand
8
Salzartige Wasserstoff-Verbindungen
⇒ Typisch ionische Strukturen aber kleine Δχ zwischen M und H lassen wenig ionischen Charakter erwarten:
Verbindung
LiH
NaH
KH
Gitterenergie (kJ mol-1)
913
810
712
MgH2
CaH2
SrH2
2709
2428
2261
Metallartige Wasserstoff-Verbindungen
⇒ Hauptsächlich bei Übergangsmetallen
⇒ ‚typische Metallstrukturen’, wobei der Wasserstoff eingelagert ist: ‚Einlagerungsverbindungen’
oder ‚interstitielle Verbindungen’
⇒ Wasserstoff besetzt oktaedrische bzw. tetraedrische Lücken einer verzerrte kubisch- oder hexagonaldichtesten Packung von Metall-Atomen.
9
Kovalente Wasserstoff-Verbindungen
⇒ Hydride der 13. Gruppe sind unter normalen Bedingungen polymer
⇒ δ+/δ-H-Extrem-Fälle
⇒ BH3 vs. B2H6
⇒ Anionische- bzw. kationische Wasserstoff-Brücken-Bindungen
Molekül
HF
HCl
HBr
HI
d(E-H) / Ǻ
0.917
1.274
1.415
1.609
H2O
H2S
H2Se
H2Te
0.957
1.334
1.47
1.69
10
Wasserstoff-Brücken-Bindungen
⇒ Was ist eine Wasserstoff-Brücken Bindung ?
⇒ anziehende Kraft
⇒ kovalenter Protonen-Donor
⇒ Protonen-Akzeptor-Atom
⇒ elektrostatische Wechselwirkung
⇒ korreliert mit der Acidität des H-Atoms und der Basizität von B
Eine kurze Geschichte:
⇒ Werner, 1902
Ammoniumhydroxid ist das Additions-Produkt von Ammoniak mit Wasser:
⇒ Latimer und Rodebush, 1920
(erster endgültiger Hinweis)
Wenn ein H-Atom zwischen zwei Oktetts vorliegt, dann liegt eine schwache H-Bindung
vor; ebenso kann eine Kette oder ein Netzwerk existieren.
⇒ Coulson, 1957: 3 Haupt-Beiträge und 1 Neben-Beitrag zur Gesamtenergie einer H-Bindung:
(i) Elektrostatische-Energie
(ii) Delokalisierungs-Energie
(iii) Abstoßungs-Energie
11
Experimenteller Beweis für Wasserstoff-Brücken-Bindungen
⇒ Abnormale Schmelz- und Siede-Punkte
⇒ Abnormale Dipolmomente
⇒ Hohe Viskositäten
⇒ Löslichkeit ↓
⇒ Signifikante Frequenz- und Intensitäts-Änderungen in den IR- und Raman-Spektren
⇒ Internukleare H...B Abstände < van-der-Waals-Abstände, aber > als kovalente und ionische Abstände
⇒ H-Bindung ist viel schwächer im Vergleich zu einer normalen ‘chemischen Bindung’. Die Stärke
schwankt beträchtlich mit A-H und B
12
Was sind charakteristische Eigenschaften für Wasserstoff-Brücken-Bindungen
⇒ typische Länge H.........O = ~ 1.8 Ǻ
⇒ typische Winkel: ~ 180 ± 20°
⇒ lineare und nicht lineare sind möglich
⇒ typische Energie ~ 20 kJ mol-1
⇒ symmetrisch oder antisymmetrisch möglich
⇒ Proteine, Wasser etc.
In der ersten Nährung ist es eine elektrostatische Anziehung
zwischen einem elektropositiven Wasserstoff-Atom
und einem elektronegativen Atom (oder einer Gruppe, z. B. H2O).
13
Der Einfluss der Wasserstoff-Brücken-Bindungen
⇒ Intra- und inter-molekulare Wasserstoff-Brücken-Bindungen
⇒ Warum ist der Siedepunkt von Wasser +100°C, aber der von H2S –60°C !?
⇒ Was sollte höher sein, der Siedepunkt von Ethanol (H3C-CH2-OH) oder Methoxymethan/
Dimethylether (H3C-O-CH3) und warum ?
14
Der Einfluss der Wasserstoff-Brücken-Bindungen
⇒ Warum ist die X-H Bindung in X-H··········Y länger als in freien X-H ?
⇒ Warum ist die ν(X-H) in X-H··········Y zu niedrigerer Wellenzahl verschoben im Vergleich
zu freiem X-H ?
⇒ Wie ist der Stärke der X-H Bindung in X-H··········Y im Vergleich mit freiem X-H ?
Warum eine Rot-Verschiebung?
(zu niedrigerer Wellenzahl)
⇒ Stärke der H··········Y-Bindung bzw. X-H-Bindung (vgl. freies H-X)
⇒ Länge der H-X-Bindung
⇒ Verschiebung der X-H-Bindung vgl. freies H-X
⇒ Dipolmomente
15
HF: Eine der "einfachsten" und wichtigsten fluorhaltigen Verbindungen
16
Ein Vergleich zwischen den HX-Verbindungen
Ist HF den anderen HX-Verbindungen (HCl, HBr, HI) ähnlich?
Eigenschaften
Farbe (RT)
Zustand (RT)
Siedepunkt (°C)
Schmelzpunkt (°C)
BDE (kJ mol-1)
HX · xH2O/HyOx+Xbekannt?
Dissoziation von HX in
H2O
d(H-X) / Å
ΔHf° (kJ mol-1)
HF
HCl
HBr
HI
farblos
flüssig
19.5
-83.4
574
(H2O)x HF
x = 1, 2, 4
~8%
farblos
Gas
-84.2
-114.7
428
(H2O)x HCl
x = 1, 2, 4, 6
100 %
farblos
Gas
-67.1
-88.6
363
(H2O)x HBr
x = 1, 2, 3, 4, 6
100 %
farblos
Gas
-35.1
-51.0
295
(H2O)x HI
x = 1, 2, 3, 4
100 %
0.917
-271.12
1.274
-92.31
1.414
-36.40
1.609
26.48
Greenwood, N. N. & Earnshaw, A., Chemistry of the Elements, Pergamon Press, S. 929.
17
Wie reaktiv ist HF gegenüber Glas?
Die technischen Schwierigkeiten beim Arbeiten
mit HF und Supersäuren:
(i) HF reagiert mit Glas
(ii) HF ist sehr giftig und ätzend
(iii) Wasserfreies HF ist bei RT gasförmig
(iv) Niedrige Viskosität
(v) Kann getrocknet werden
(vi) Verursacht schwere Verätzungen
Industrielle Verwendung von HF:
*
*
*
*
*
Herstellung von CFC´s (~ 37 %)
Al-Produktion (~ 40 %)
Uran-Verarbeitung (~ 7 %)
"Petroleum"-Alkylierungs-Katalysatoren (~ 5 %)
Glas-Ätzung (~ 10 %)
Bromine trif luoride
Dinitrogen tetraoxide
Fluorsulf uric acid
Hydrogen f luoride
Sulf uric acid
Sulf ur dioxide
Ammonia
Water
Liquid range/K
200
300
400
500
600
T. A. O'Donnell, Superacids and Acidic Melts as Inorganic Chemical Reaction Media, 1993, VCH, New York.
Es ist nicht einfach, mit wasserfreiem HF zu arbeiten!
18
Der Einfluss von Wasserstoff-Brücken-Bindungen
auf die Struktur von HF-Verbindungen
F
F
H
F
157 pm
H
H
H
120°
F
H
92 pm
H
F
F
Struktur von HF im festen Zustand
F
Struktur eines
(HF)6-Hexamers
H
H
F
H
F
104°
H
o
H
H
F
F
F
F
F
-
o
F
-
o
F
o
F
F
2.26
-
H 2.45 A
H
45
2.
F
A
F
H
-
F
o
H
H
-
Ho F
48
2.
F
A
F
2.28
H
H
H
Hydrogendifluorid-Ion
H 2.40 A
H
F
F
113 pm
-
F
H
-
H
F
H
F
o
32
2.
F
F
-
F
F
H
H
-
Ho F
-
2.27
H
H
F
F
F
F
H2F3-
H3F4-
H4F5-
H3F4-
H5F6-
Hollemann und Wiberg, Lehrbuch der Anorganischen Chemie, Walter de Gruyter, S. 457.
19
Superacids / Supersäuren?
IUPAC-Definition der Supersäuren:
Eine Supersäure ist eine Substanz mit hoher Acidität, die größer oder gleich ist als jene von 100%-iger-Schwefelsäure.
Beispiele der Supersäuren
Formel
HF
HSO3F
HN(SO2CF3)2
CF3SO3H
H(CB11H6X6)
Trivialname
Fluorwasserstoffsäure
Fluorschwefelsäure
kein Trivialname
Triflic / Trifluormethansulfonsäure
kein Trivialname
* Die Stärke einer Supersäure kann durch Zugabe einer LewisSäure verstärkt werden (Hammett´sche Aciditäts-Funktion).
Ho-Wert
-15.1
-15.1
-14.1
T. A. O´Donnell, Superacids and Acidic Melts as Inorganic Chemical Reaction Media, 1993, VCH Publishers, Inc.
20
Supersäuren und Hammett´sche Aciditätsfunktion
Für "normale" wässrige Säure-Base-Systeme gilt:
ΔpH = ΔpKW (Ionenprodukt des Wassers, also pH von 0 → 14)
Sehr starke Säuren: pKA < 0 (HClO4, H2SO4: pKA ≈ - 3)
Supersäuren (SS):
pKA << 0 (2 HF
H2F+ + F-)
(2 HSO3F
H2SO3F+ + SO3F-)
Noch bessere SS durch Zugabe von LS (Adduktbildung): HF / BF3 oder HSO3F / SbF5
Beispiel: 2 HSO3F + LS
H2SO3F+ + SO3F-.LS (GG nach rechts)
Messung (photometrisch) der Acidität von SS erfolgt über (sehr) schwache Indikatorbasen B
(z. B. Nitroanilin
= O2N-C6H4-NH2):
BH+
B + H+; KD = [B] [H+] / [BH+]; - log KD = pKD
pKD = - log {[B] [H+] / [BH+]} = - log [H+] - log [B] / [BH+]
Nach Hammett:
Ho ≙ - log [H+] (wenn verdünnt: Ho ≈ pH)
pKD = HO - log [B] / [BH+]
Hammett´sche Aciditätsfunktion:
Ho = pKD + log [B] / [BH+]
Maß für den pH-Wert von SS
21











