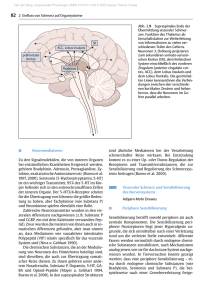
Die schwere RSV-Infektion als Risikofaktor für Giemen und eine
Werbung

Aus der Klinik für Kinderheilkunde und Jugendmedizin im St. Josef-Hospital Bochum - Universitätsklinik der Ruhr-Universität Bochum Direktor: Prof. Dr. med. E. Hamelmann Die schwere RSV-Infektion als Risikofaktor für Giemen und eine allergische Sensibilisierung im Alter von 12 Monaten Inaugural-Dissertation zur Erlangung des Doktorgrades der Medizin einer Hohen Medizinischen Fakultät der Ruhr-Universität Bochum vorgelegt von Silke Bongartz aus Viersen 2008 Dekan: Prof. Dr. med. G. Muhr Referent: Prof. Dr. med. U. Schauer Koreferent: Prof. Dr. med. L. Reinken Tag der Mündlichen Prüfung: 19.05.2009 Abstract Bongartz Silke Titel: Die schwere RSV-Infektion als Risikofaktor für Giemen und eine allergische Sensibilisierung im Alter von 12 Monaten Problem Die Genese von atopischen Erkrankungen ist ein komplexes Geschehen. Dabei nehmen sowohl endogene als auch exogene Faktoren Einfluss auf die Entstehung eines allergischen Krankheitsbildes. Ein exogener Faktor, zu dem nahezu alle Kinder bis zum zweiten Lebensjahr Kontakt haben, ist das Respiratory Syncytial Virus. Dieser Erreger von Atemwegsinfektionen zeigt in in vitro Experimenten eine Stimulation der T-Zell-Antwort zugunsten einer Th-2-gerichteten Immunantwort. Eine besondere Rolle spielt der Zeitraum des ersten Lebensjahres, in dem der Organismus nach Beendigung der mütterlichen Leihimmunität reichlich Kontakt zu verschiedenen Antigenen hat. Dabei bildet sich entweder eine immunologische Toleranz aus oder aber der Organismus reagiert mit einer allergischen Sensibilisierung. In der vorliegenden Arbeit wurde der Frage nachgegangen, ob sich auch in vivo Hinweise für eine immunmodulatorische Wirkung des RS-Virus zeigen. Anhand einer Fall-Kontroll-Studie wurde geprüft, ob eine schwere RSV-Infektion einen Risikofaktor für anhaltendes Giemen oder eine allergische Sensibilisierung darstellt. Dabei wurde insbesondere der Zeitraum des ersten Lebensjahres betrachtet, um mögliche immunmodulatorische Effekte einer RSV-Infektion zeitnah zu erfassen. Methode Dazu wurden 42 Säuglinge mit einer schweren RSV-Bronchiolitis mit 84 gesunden Säuglingen einer Kontrollgruppe über einen Zeitraum von einem Jahr miteinander verglichen. Die Gruppen wurden bezüglich des Geburtszeitraums und des Geschlechts gematcht. Anhand einer klinischen Untersuchung im durchschnittlichen Alter von 12 Monaten sowie von Fragebögen und immunologischen Laborergebnissen (Gesamt-IgE, spezifisches IgE für Inhalations- und Nahrungsmittelallergene, RSV-Antikörper) wurde insbesondere das Atopierisiko und die Atopieentwicklung beider Gruppen verglichen. Außerdem wurden Umwelteinflüsse untersucht, welche die Atopieentstehung begünstigen. Ergebnis Dabei stellte sich eine schwere RSV-Infektion als spezifischer Risikofaktor für Giemen, wiederholtes Giemen und eine allergische Sensibilisierung gegenüber Nahrungsmitteln im Alter von 12 Monaten heraus. 14 Kinder der Fallgruppe versus einem Kind der Kontrollgruppe wiesen ein erhöhtes nahrungsmittelspezifisches IgE auf, welches als Hinweis auf die immunmodulatorische Wirkung des RS-Virus gewertet wird. Auch der erhöhte Gesamt-IgE-Wert der Fallgruppe (14 versus zwei Kinder) bestärkt die Tendenz einer Th-2-gewichteten Immunantwort als Reaktion auf eine schwere RSVInfektion. Bezüglich des wiederholten Giemens zeigten sich 13 Kinder der Fallgruppe auffällig im Gegensatz zu 3 Kindern der Kontrollgruppe. Dies kann einerseits als postbronchiolitisches Giemen interpretiert werden, andererseits auf eine erhöhte bronchiale Hyperreagibilität im Rahmen eines allergischen Geschehens hinweisen. Des Weiteren ließ sich ein negativer Einfluss auf eine allergische Sensibilisierung und die Entwicklung eines Giemens durch mütterlichen Nikotinkonsum aufzeigen. Die Probanden der Fallgruppe hatten vermehrt rauchende Eltern. Dabei zeigte sich vor allem das Rauchen in der Schwangerschaft als Risikofaktor für Giemen im Alter von 12 Monaten. Eine weitere Differenzierung, ob das Giemen aufgrund einer Ziliendysfunktion im Rahmen der passiven Tabakrauchexposition zustande kommt oder eine bronchiale Hyperreagibilität im Sinne eines allergischen Geschehens eine Rolle spielt, kann durch die vorliegenden Daten nicht erfolgen. Diskussion Zusammenfassend stellt sich eine schwere RSV-Infektion als Risikofaktor für anhaltendes Giemen und eine allergische Sensibilisierung gegen Nahrungsmittel im Alter von 12 Monaten heraus. Die genauen immunologischen Mechanismen, insbesondere die Toleranzentwicklung gegenüber Umweltantigenen, bleiben aber weiterhin Gegenstand aktueller Studien. Interessant ist auch die weitere Beobachtung der beiden Gruppen. Ob das Giemen auch in den folgenden Lebensjahren relevant bleibt, und ob sich klinische Zeichen einer Nahrungsmittelallergie oder ein allergisches Asthma bronchiale zeigen, muss bei erneuten Follow-up-Untersuchungen festgestellt werden. Diese Arbeit ist meiner Familie, insbesondere meinem Mann Andreas, meiner Tochter Mirjam und meinen Eltern gewidmet. Inhaltsverzeichnis 1 EINLEITUNG 1.1 Die Bedeutung von RSV-Infektionen im Kindesalter und der mögliche Zusammenhang mit der Zunahme von Allergien 10 10 1.2 Charakterisierung des RS-Virus 12 1.2.1 Geschichte 12 1.2.2 Virologie 12 1.2.3 Epidemiologie 14 1.2.4 Klinisches Erscheinungsbild und Pathophysiologie 15 1.2.5 Differenzialdiagnose: Infektion mit humanem Metapneumovirus 16 1.2.6 Diagnostischer Nachweis von RSV 18 1.2.7 Therapie 19 1.3 Allergische Erkrankungen 1.3.1 Epidemiologie und Risikofaktoren allergischer Erkrankungen 1.3.2 Pathogenese von allergischen Erkrankungen 1.3.3 Gesamt-IgE 21 21 22 25 1.4 Auswirkungen des RS-Virus auf das menschliche Immunsystem: Induktion einer Th2-Antwort 26 1.4.1 Zelluläre Immunantwort 26 1.4.2 Humorale Immunantwort 29 1.4.3 Weitere Faktoren 30 1.5 Fragestellung: Lässt sich ein Einfluss des RS-Virus auf späteres Giemen und eine spätere allergische Sensibilisierung nachweisen? 32 2 PATIENTEN, MATERIAL UND METHODEN 33 2.1 Patienten 2.1.1 Ethik 2.1.2 Fallgruppe 2.1.3 Kontrollgruppe 33 33 33 34 2.2 Durchführung der Studie 2.2.1 Respiratory syncytial Virus ELISA 2.2.2 RSV-Schnelltest 2.2.3 IgE-Antikörpersuchtests 35 35 37 37 2.3 Definitionen der Begriffe 2.3.1 Atopische Dermatitis 2.3.2 Wiederholtes Giemen 2.3.3 Atopische Erkrankungen der Eltern oder Geschwister 38 38 39 39 2.4 39 Statistische Methoden 5 3 ERGEBNISSE 41 3.1 Die Kinder der RSV-Gruppe hatten vermehrt rauchende Eltern und mehr Geschwister 41 3.2 Erhöhtes Auftreten von Giemen, wiederholtem Giemen, erhöhtem Gesamt-IgE und einer Sensibilisierung gegen Nahrungsmittelallergene in der RSV-Gruppe 43 3.2.1 Serologische Bestätigung der stattgefundenen RSV-Infektion 43 3.2.2 Erhöhtes Gesamt-IgE, häufigeres Auftreten einer Sensibilisierung gegen Nahrungsmittelallergene, vermehrtes Giemen und wiederholtes Giemen in der RSV-Gruppe 44 3.3 RSV-Bronchiolitis als wichtigster Risikofaktor für Giemen, wiederholtes Giemen und allergische Sensibilisierung gegen Nahrungsmittelallergene im Alter von 12 Monaten 45 3.4 Bestätigung der RSV-Bronchiolitis als unabhängigem Risikofaktor für Giemen, wiederholtes Giemen und allergische Sensibilisierung gegen Nahrungsmittel im Alter von einem Jahr 49 4 51 DISKUSSION 4.1 Bedeutung einer Sensibilisierung bezüglich des klinischen Auftretens einer Allergie 4.1.1 RSV als spezifischer Risikofaktor einer Sensibilisierung gegen Nahrungsmittelallergene im Alter von 12 Monaten 4.1.2 Bedeutung eines erhöhten Gesamt-IgE-Wertes 4.1.3 Eine schwere RSV-Infektion als spezifischer Risikofaktor für Giemen im Alter von 12 Monaten 56 4.2 Hereditäre Einflüsse auf die Allergieentstehung 4.2.1 Bedeutung einer positiven Familienanamnese 4.2.2 Geschlecht 60 60 61 4.3 Allgemeine Risikofaktoren, insbesondere umweltbedingte Einflüsse, auf die Entstehung allergischer und infektiologischer Erkrankungen 4.3.1 Geschwisteranzahl 4.3.2 Geschwister als mögliche Risikofaktoren für Giemen und wiederholtes Giemen im Alter von einem Jahr, aber kein Risikofaktor für eine allergische Sensibilisierung im Alter von 12 Monaten 4.3.3 Rauchen 51 51 54 62 62 63 65 5 ZUSAMMENFASSUNG 67 6 LITERATURVERZEICHNIS 69 7 ANHANG 94 6 7.1 Fragebogen bei Geburt 7.2 Fragebogen im Alter von einem Jahr 8 DANKSAGUNG 9 LEBENSLAUF 94 100 7 Abkürzungsverzeichnis BPD Bronchopulmonale Dysplasie CD Cluster of differentiation CPAP Continuous positive airway pressure DDR Deutsche Demokratische Republik ELISA Enzyme linked immunosorbent assay GM-CSF Granulocyte-macrophage-colony stimulating factor hMPV humanes Metapneumovirus IFN Interferon Ig Immunglobulin IL Interleukin KI Konfidenzintervall MHC Major Histocompatibility Complex NK-Zellen natürliche Killerzellen NRW Nordrhein-Westfalen OR Odds Ratio PBS Phosphate buffered saline pCO2 Kohlendioxid-Partialdruck PCR Polymerase chain reaction (Polymerasekettenreaktion) RIA Radioimmunoassay RNA Ribonukleinsäure RS(V) Respiratory syncytial (virus) SSW Schwangerschaftswoche Th-Zellen T-Helferzellen TGF-β Transforming growth factor β TLR-4 Toll-like-Rezeptor 4 TNF-α Tumornekrosefaktor α WHO World Health Organisation (Weltgesundheitsorganisation) 8 Tabellenverzeichnis Tabelle 1: Anamnestisch erhobene Daten im durchschnittlichen Alter von einem Jahr bei der RSV-Gruppe und der Kontrollgruppe Tabelle 2: Allergische Symptome im Vergleich - Univarianzanalyse 42 44 Tabelle 3: Mögliche Risikofaktoren in Bezug zum Auftreten von Giemen - Univarianzanalyse mit Fisher´s Exact Test 46 Tabelle 4: Mögliche Risikofaktoren in Bezug zum Auftreten von wiederholtem Giemen – Univarianzanalyse mit Fisher´s Exact Test 47 Tabelle 5: Mögliche Risikofaktoren in Bezug zu einer allergischen Sensibilisierung - Univarianzanalyse mit Fisher´s Exact Test 48 Tabelle 6: Multivarianzanalyse möglicher Risikofaktoren in Bezug auf Giemen im Alter von einem Jahr – Analyse der in der Univarianzanalyse identifizierten möglichen Risikofaktoren (Tabelle 3) 49 Tabelle 7: Multivarianzanalyse möglicher Risikofaktoren in Bezug auf wiederholtes Giemen im Alter von einem Jahr - Analyse der in der Univarianzanalyse identifizierten möglichen Risikofaktoren (Tabelle 4) 50 Tabelle 8: Multivarianzanalyse möglicher Risikofaktoren in Bezug auf eine allergische Sensibilisierung gegenüber Nahrungsmitteln im Alter von einem Jahr - Analyse der in der Univarianzanalyse identifizierten möglichen Risikofaktoren (Tabelle 5) 50 Abbildungsverzeichnis Abbildung 1: Struktur des RS-Virus und Parainfluenzavirus 14 9 1 Einleitung 1.1 Die Bedeutung von RSV-Infektionen im Kindesalter und der mögliche Zusammenhang mit der Zunahme von Allergien Der Begriff Allergie wurde erstmals 1906 von Clemens von Piquet zur Unterscheidung von nützlichen und schädlichen Immunreaktionen geprägt (von Piquet, 1906). Heute bezeichnet man eine überschießende, krankmachende spezifische Immunreaktion (=Hyperergie) gegen eigentlich harmlose exogene Substanzen (=Allergene) als Allergie . Krankheitsbilder aus dem allergischen Formenkreis gehören zum allgemeinmedizinischen und pädiatrischen Alltag und sind von enormer sozioökonomischer Bedeutung. Die rasant steigende Anzahl von allergischen Erkrankungen im Kindesalter wirft die Frage auf, welche Gründe es für diese Zunahme in den letzten Jahrzehnten gibt. War die Lebenszeitprävalenz von Asthma bei Jungen 1985 nur 1,5%, so waren 1995 4% betroffen. Bei allen Kindern stieg die Lebenszeitprävalenz des atopischen Ekzems in diesem Zeitraum von 6% auf 12% an. Diese Daten beziehen sich auf eine Studie an sechsjährigen Kindern aus NRW (Krämer et al., 2001). Aktuelle Studien scheinen zu belegen, dass nach einem steilen Anstieg der Prävalenz inzwischen ein Plateau erreicht ist (Zollner et al., 2005). Dabei ist zu Erkrankungen berücksichtigen, multifaktoriell dass ist. die Ätiologie Genetische von Faktoren, allergischen eine frühe Allergenexposition sowie verschiedenste Umweltfaktoren spielen bei der Krankheitsentstehung eine Rolle. Die Ausprägung und der Verlauf allergischer Erkrankungen sowie die klinische Reagibilität sind individuell unterschiedlich. Beeinflusst werden kann einerseits die Bahnung Sensibilisierungsphase, allergischer andererseits der Reaktionen Übergang zur in der klinischen Manifestation. 10 Viele Forschungsteams betätigen sich rund um das Thema der Genese allergischer Erkrankungen. Im folgenden soll der Fokus auf den Bereich von Umweltfaktoren, insbesondere virale Erkrankungen, in der Sensibilisierungsphase gelenkt werden. Da im Laufe der ersten Lebensjahre nahezu alle Kinder einen RSV-Infekt erleiden, aber nur einige ein erhöhtes Risiko tragen, im weiteren Kindesalter an Asthma bronchiale oder einer anderen Erkrankung aus dem allergischen Formenkreis zu erkranken, scheint nicht die Infektion per se, sondern die klinische Verlaufsform einen Einfluss auf das spätere Outcome der Patienten zu haben. Aufgrund von epidemiologischen Beobachtungen, dass Säuglinge, die bezüglich einer RSV-Bronchiolitis stationär behandelt wurden, in den folgenden Lebensjahren vermehrt asthmatische Symptome in Form von Giemen zeigten (Sigurs et al., 2000), und dass akute Exazerbationen von bestehendem Asthma durch virale Infektionen hervorgerufen wurden (Mallia and Johnston, 2006, Hansbro et al., 2008), stellt sich die Frage nach einem möglichen Zusammenhang zwischen allergischen Erkrankungen und viralen Infektionen, insbesondere dem RS-Virus. Dieses Virus ist laut der WHO der dritthäufigste Erreger von Infektionen des unteren Atemtrakts, nach Streptococcus pneumoniae und Hämophilus influenzae (Simoes, 1999), und der häufigste Erreger von viralen Bronchiolitiden (Mansbach, 2008). Studien konnten unterschiedliche Verlaufsformen einer RSV-Infektion mit jeweils verschiedenen Antworten des T-Zell-Systems beobachten (Martinez et al., 1998). Daraus entstand die Überlegung, Kinder mit einer schweren Verlaufsform einer RSV-Erkrankung mit einer Kontrollgruppe von gesunden Kindern zu vergleichen. In vitro Versuche und Tierexperimente ergaben weitere Hinweise auf eine Wechselwirkung des menschlichen Immunsystems mit RSV (Walzl et al., 2001, Wissinger et al., 2008). Anhand der komplexen Immunantwort ist es zunächst nicht möglich, eine bestimmte Risikogruppe zu definieren, bei welcher eine präventive Maßnahme – wie beispielsweise eine Impfung gegen RSV - das spätere Giemen verhindern würde. 11 Bislang gibt es nur die Möglichkeit einer passiven Immunisierung, ein aktiver Impfstoff befindet sich in Entwicklung (Power, 2008). 1.2 Charakterisierung des RS-Virus 1.2.1 Geschichte Erstmals beschrieb J. A. Morris 1956 einen neuen Erreger von Schimpansen-Schnupfen, den R. M. Chanock 1957 auch gehäuft bei Kindern mit Atemwegsinfekten nachwies (Chanock et al., 1957). Aufgrund der Fähigkeit, respiratorische Symptome bei Infektionen hervorzurufen und in der Zellkultur große Synzytien zu bilden, entstand der Name RespiratorySyncytial-Virus. 1.2.2 Virologie Das Respiratory-Syncytial-Virus gehört zur Familie der Paramyxoviren, und zwar zum Genus der Pneumoviren. Es ist ein einsträngiges RNA-Virus mit negativer Polarität und enthält 15.222 Basenpaare, welche die zehn Proteine des Virions kodieren (Sullender, 2000). Das Genom ist eingeschlossen in ein Nukleokapsid von ungefähr 13,5 nm im Durchmesser, welches nochmals von einer Doppellipidschicht umgeben ist (envelope). Im Gegensatz zu anderen Paramyxoviren zeichnen sich die Pneumoviren dadurch aus, dass ihre envelope-Proteine keine Hämagglutinin- und keine Neuraminidase-Aktivität besitzen. Diese Bestandteile der Virushülle spielen eine wichtige Rolle beim Anheften und Eindringen in die Wirtszelle, die das RS-Virus auf andere Weise lösen muss. Das RS-Virus ist pleomorph, d.h. es kann verschiedene Formen von filamentös bis rund annehmen. Auf seiner Oberfläche sind drei Glykoproteine zu finden, das Fusionsprotein F, das Glykoprotein G und das SH-Protein. Die Funktion des SH-Proteins ist bis heute unklar. Das Fusionsprotein F ermöglicht die Penetration in die Wirtszelle und die Verbreitung der Viren von 12 Zelle zu Zelle. Das etwas größere Protein G stellt in Form von spikes den Kontakt zur Wirtszelle her, ähnlich dem Hämagglutinin der anderen Paramyxoviren (Tripp, 2004). Aufgrund der Variabilität der Oberflächenproteine, vor allem des G-Proteins, unterteilt man die RS-Viren in zwei weitere Hauptgruppen, RSV-A und RSVB. Diese Stämme unterscheiden sich hauptsächlich in der Antigenstruktur des G-Oberflächenproteins, welches nur in 5% der Fälle homologe Antigenstrukturen zwischen beiden Stämmen aufweist. Dabei bestehen Hinweise auf eine höhere Pathogenität und eine höhere Prävalenz der Gruppe A (Vieira et al., 2007). Allerdings gibt es keine Korrelation zwischen der klinischen Schwere und dem Befall mit einem der beiden Stämme (Brandenburg et al., 2000). Während einer Epidemie zirkulieren gleichzeitig beide Gruppen, wenn auch in jeweils verschiedenem Verhältnis. Das F-Protein, gegen das sich auch die monoklonalen Antikörper von Palivizumab, einem passiven Impfstoff, richten, zeigt in 50% der Fälle homologe Strukturen zwischen den A- und B-Stämmen (Sullender, 2000). Beide, sowohl G- als auch F-Protein, sind die einzigen beiden Proteine des RS-Virus, die beim Wirt eine neutralisierende Antikörperbildung hervorrufen (Simoes, 1999). Dabei spielt das Vorhandensein von sekretorischen IgAAntikörpern nur in den oberen Luftwegen eine Rolle, die Abwehr im unteren Respirationstrakt geschieht über die Serumantikörper. Das RS-Virus besitzt 8 Struktur-Proteine: Die bereits erwähnten Proteine G, F und SH sowie die Matrixproteine M1 und M2 und die Nukleokapsidassoziierten Proteine Nukleoprotein N, Phosphoprotein P und langes Protein L, welches eine RNA-Polymerase-Funktion hat. Des weiteren sind noch 2 nicht-strukturelle Proteine Bestandteil des RS-Virus, welche die InterferonAntwort unterdrücken sollen (Hall, 2001). 13 Abbildung 1: Struktur des RS-Virus und Parainfluenzavirus (nach Hall, 2001) 1.2.3 Epidemiologie RS-Viren kommen überall auf der Welt vor. Die höchste Infektionsrate in Form von Epidemien besteht im Winter in gemäßigten Klimazonen. In Deutschland liegt der Häufigkeitsgipfel in der Zeit von November bis März (Forster et al., 2003). RSV wird über direkten Kontakt mit infektiösem Sekret übertragen (Tröpfcheninfektion oder Schmierinfektion). Das Virus bleibt bis zu sechs Stunden auf Oberflächen wie Stethoskopen infektiös, bis zu 45 min auf Stoffen. Gegenüber Desinfektionsmitteln ist der Erreger sehr empfindlich (RSV-Infektionen, Robert-Koch-Institut, 2004). Die Inkubationszeit beträgt drei bis sechs Tage, die Infektiosität beginnt schon einen Tag nach der Ansteckung und ist von unterschiedlicher Dauer. Bei immunkompetenten Erwachsenen beträgt sie etwa sieben Tage, bei Früh- und Neugeborenen mit schwerer Infektion bis zu vier Wochen. Grundsätzlich können Menschen jeder Altersstufe erkranken, die höchste Morbiditätsrate aber besteht bei Kindern im Alter von sechs Wochen bis sechs Monaten. Bei Säuglingen besteht in den ersten vier bis sechs Wochen 14 ein Nestschutz durch diaplazentar übertragene Antikörper. Auch ältere Menschen haben bedrohliche Verläufe von RSV-Infekten (Elliot and Fleming, 2008). Wiederholte Infektionen, auch mit demselben Virus-Typ, im Laufe eines Lebens sind normal, verlaufen aber meist nicht so schwerwiegend wie die Erstinfektion (Black, 2003). Die Durchseuchung mit RSV bis zum Ende des zweiten Lebensjahres beträgt nahezu 100%. Jugendliche und Erwachsene können als symptomarme Überträger fungieren. Hochrisikogruppen in den Industriestaaten, die zu einem ernsthaften Krankheitsverlauf neigen, sind wie folgt definiert: Frühgeborene, Kinder mit einer bronchopulmonalen Dysplasie, mit hämodynamisch relevanten Herzvitien, mit zystischer Fibrose, immunsupprimierte Patienten, Kinder unter drei Monaten, ältere Leute. Weitere Risikofaktoren, die einen schweren Krankheitsverlauf begünstigen, sind ein niedriger sozioökonomischer Status, enge räumliche Lebensbedingungen, Rauchexposition in der Wohnung und eine positive Familienanamnese bezüglich Asthma und anderen atopischen Erkrankungen (Simoes, 1999). 1.2.4 Klinisches Erscheinungsbild und Pathophysiologie Der Verlauf einer RS-Virusinfektion tendiert vom symptomlosen Infekt bis hin zur Bronchiolitis mit Beatmungspflichtigkeit. Als Eintrittspforte dient das respiratorische Epithel der oberen Luftwege, insbesondere Nasen- und Augenschleimhaut. Von dort aus erfolgt die Ausbreitung direkt oder hämatogen auf den unteren Respirationstrakt (Krusat und Werchau, 2001). In den meisten Fällen macht sich eine Infektion mit RS-Viren zunächst durch Schnupfen, Husten und evtl. Fieber bemerkbar. Die häufigste Manifestation im Säuglingsalter besteht allerdings in einer Bronchiolitis oder einer Pneumonie (Black, 2003). Aufgrund der entzündlich verdickten Schleimhaut, zum Teil mit Epithelnekrosen, kommt es zu einer Zunahme des Atemwegswiderstandes in den kleinen Bronchien und Bronchiolen. Dabei entsteht ein Missverhältnis zwischen Ventilation und Perfusion, welches eine Hypoxämie zur Folge hat. Der pCO2 kann aufgrund der Tachypnoe zunächst 15 vermindert oder normal sein, eine Hyperkapnie tritt erst bei drohender respiratorischer Erschöpfung auf (Strauss, 2002). Über den Mechanismus des „air trapping“ fließt Luft bei der Inspiration in die distalen Lungenabschnitte, kann aber aufgrund der Obstruktion bei der Exspiration nicht wieder ausgeatmet werden. Zunächst entsteht lokal eine Überblähung, welche bei komplett verlegten Lungenabschnitten resorbiert wird und somit eine Atelektase zur Folge hat. Klinische Symptome einer Bronchiolitis sind Unruhe, Tachypnoe, Dyspnoe, intercostale und juguläre Einziehungen und Trinkschwäche. Eine Akrozyanose bei Belastung sowie ein typischer Husten können weitere Hinweise sein. Apnoen können besonders bei jüngeren Säuglingen das erste klinische Zeichen einer Bronchiolitis sein. Bei der Auskultation fallen ein Giemen und ein verlängertes Exspirium sowie Rasselgeräusche auf (Döring et al., 2005). Mögliche radiologisch sichtbare Merkmale sind eine peribronchiale Verdickung, Atelektasen, diffuse Zeichnungsvermehrung, zum Teil Infiltrate. Eine Überblähung mit weiten Rippenabständen und tiefstehenden Zwerchfellen wird als typische Veränderung erwartet (Rieger, 2001). Die größte Gefahr bildet die respiratorische Insuffizienz. Etwa 5% der erkrankten Kinder müssen maschinell beatmet werden, die Letalität beträgt 1% (Strauss, 2002). Der Verlauf einer Erkrankung kann durch eine Otitis media und andere bakterielle Superinfektionen kompliziert werden. Nosokomiale RSV-Infektionen sind die häufigsten nosokomialen Infektionen auf pädiatrischen Stationen und haben eine relativ hohe Mortalität (Forster, 2002). 1.2.5 Differenzialdiagnose: Infektion mit humanem Metapneumovirus Ein ähnliches klinisches Erscheinungsbild zeigen Infektionen mit dem humanen Metapneumovirus. Dieses gehört wie das RS-Virus zur Familie der Paramyxoviren, Genus der Pneumoviren. Es wurde erstmals 2001 in den Niederlanden bei Kindern mit Atemwegsinfektionen nachgewiesen (van den Hoogen et al., 2001). Neben RSV und Influenza A ist hMPV das dritthäufigste allgemeine virale Pathogen von Luftwegsinfekten (Wolf et al., 16 2006). In einer Untersuchung von archivierten Nasenspülwasserproben der letzten 20 Jahre zeigte sich ein prozentualer Anteil von 5% hMPV an allen oberen Luftwegsinfekten. Dabei lag das Durchschnittsalter der betroffenen Kinder bei 20 Monaten, etwa 78% der Infektionen traten in den Monaten Dezember bis Mai auf, also etwas später als RSV. Wiederholte Infektionen mit homo- und heterologen Strängen des hMPV waren zu verzeichnen. 50% der untersuchten Kinder litten neben einem oberen Luftwegsinfekt an einer Otitis media als Komplikation (Williams et al., 2006). hMPV wurde auch als Erreger unterer Atemwegsinfektionen nachgewiesen. Dabei war das Virus Auslöser von Bronchiolitiden, Pneumonien, CroupAnfällen und Asthma-Exazerbationen (Williams et al., 2004). Im Vergleich zu einer RSV-Gruppe zeigten Kinder mit hMPV zum einem größeren Anteil eine Hypoxämie, sowie häufiger die Notwendigkeit einer Behandlung auf der Intensivstation. In der hMPV-Gruppe zeigten sich häufiger lobäre Infiltrate auf dem Thorax-Röntgenbild. Ein weiterer Unterschied zur RSV-Infektion war der spätere Zeitpunkt der hMPV-Infektion, mehr als die Hälfte der 88 untersuchten hMPV-positiven Patienten waren älter als ein Jahr (Wilkesmann et al., 2006). Es werden Ko-Infektionen von RSV und hMPV beschrieben. Dabei sind die Raten an Ko-Infektionen bei hMPV-Infektionen höher als bei RSVInfektionen. Patienten mit alleiniger RSV-Infektion zeigten mehr Komplikationen und eine höhere Hypoxie-Rate als RSV-hMPV-ko-infizierte Patienten (Canducci et al., 2008). Risikofaktoren, an einer hMPV-Infektion zu erkranken, entsprechen im wesentlichen denen einer RSV-Infektion (Wilkesmann et al. 2006, von Linstow et al., 2008). Therapiemöglichkeiten beschränken sich bis jetzt auf die symptomatische Therapie, Versuche mit einer Ribavirin-Therapie fanden bis jetzt nur in vitro und als Tierversuch statt (Deffrasnes et al., 2007). Als weitere Erreger von Atemwegsinfektionen werden das humane Bocavirus und das humane Coronavirus erforscht. Diese treten entweder als alleinige oder als Ko-Infektionen bei verschiedensten Atemwegsinfekten auf (Canducci et al., 2008). Das Bocavirus gehört zu Gruppe der Parvoviren und wurde erstmals von Allander 2005 in Schweden beschrieben (Allander et al., 2005). Vom humanen Coronavirus, welches zur Familie der Coronaviridae 17 gehört, wurde neben den drei bisher bekannten humanpathogenen Stämmen ein weiterer Stamm 2003 in den Niederlanden isoliert (van der Hoek et al., 2004). Klinische Symptome sind denen einer RSV-Infektion ähnlich. 1.2.6 Diagnostischer Nachweis von RSV Serologischer Antikörpernachweis Der serologische Antikörpernachweis einer Infektion mit RS-Viren findet im klinischen Alltag kaum Anwendung, da Serumantikörper nur in geringfügiger Konzentration gebildet werden. Er erfolgt mittels spezifischem Antikörpernachweis im ELISA. Dabei kann man sowohl IgG, IgM als auch IgA nachweisen. Um eine akute Infektion nachzuweisen, benötigt man mindestens zwei Proben mit signifikantem Titeranstieg im Abstand von zwei bis vier Wochen. Dies ist klinisch ohne Relevanz, dient aber zu Studienzwecken. Eine andere Methode, spezifische Antikörper nachzuweisen, ist die Immunfluoreszenz. Die Standard-Komplement-Fixation findet aufgrund ihrer geringen Sensibilität, vor allem bei Kindern im Alter von ein bis drei Monaten, kaum noch Anwendung. Kultureller Nachweis und Schnelltests Die Anzucht von RS-Viren in der Zellkultur ist aus verschiedenen Probenarten möglich und immer noch Goldstandard in der Labordiagnostik zum RSV-Nachweis (RSV-Infektionen, Robert-Koch-Institut, 2004). Am besten ist Nasopharyngealsekret geeignet. Das Wachstum ist auf verschiedenen Nährböden möglich. Das Standardverfahren ist zeitintensiv und ermöglicht einen Virusnachweis erst nach vier bis sieben Tagen. Es findet noch Anwendung in der Qualitätskontrolle anderer Methoden. Bei der Immunfluoreszenz haben sich aus der herkömmlichen Methode, die nach Anlegen einer Zellkultur eine Ablesbarkeit nach zwei Tagen hatte, verschiedene Schnelltests entwickelt, meist auf Basis einer direkten Immunfluoreszenz, bei der fluoreszenzmarkierte Antikörper direkt an ein 18 Antigen in der Probe binden. Die RSV-Schnelltests beinhalten polyklonale Antikörper-Pools, deren Antikörper gegen verschiedene Proteine des RSVirus gerichtet sind. So erreichen sie eine höhere Spezifität. Der Nachweis gelingt patientennah innerhalb von etwa 20 Minuten mit einer Spezifität und Sensitivität von ca. 90 bis 95% (Forster et al., 2003). Allerdings nimmt die Sensitivität bei Kindern, die älter als drei Monate sind, auf bis zu 66,2% ab (Schauer et al., 2007). Im ELISA kann man auch kleine Virusmengen von 20 bis 30 ng nachweisen, Spezifität und Sensitivität sind der Immunfluoreszenz vergleichbar bei geringerem Arbeitsaufwand. Schnelltests ermöglichen ein Ablesen des Ergebnisses innerhalb von Minuten. Der Nachweis von RS-Viren im Radioimmunoassay ist unter anderem abhängig vom Alter der Patienten, von der Probenart, vom Tag der Probenentnahme bezogen auf Infektionsbeginn. Die Abhängigkeit dieser verschiedenen Variablen sollte in der Ergebnisinterpretation mit bedacht werden. Der Nachweis von RSV-Genomfragmenten in der PCR findet noch keine routinemäßige Anwendung, könnte aber in Zukunft eine Alternative zur Zellkultur sein, denn er bietet eine hohe Sensitivität und Spezifität (Schauer et al., 2007). 1.2.7 Therapie Eine kausale Therapie existiert nicht. Die Therapie von RS-Virusinfektionen beschränkt sich in den meisten Fällen auf eine symptomatische Behandlung. Diese sieht eine Flüssigkeitssubstitution zur Sekretmobilisation vor, sowie eine Sauerstoffgabe bei einer pulsoxymetrisch gemessenen Sättigung unter 92 bis 94%. Bei drohender respiratorischer Insuffizienz ist teilweise eine Atemunterstützung mittels CPAP-Maske oder eine kontrollierte Beatmung notwendig (RSV-Infektionen, Robert-Koch-Institut, 2004). „Minimal handling“, Ruhe sowie eine Oberkörperhochlagerung unterstützen den Patienten. Ein Freihalten des Nasopharynx durch abschwellende Nasentropfen und das Absaugen von Sekret, vor allem vor den Mahlzeiten, bringen dem betroffenen Patienten ebenfalls Erleichterung. 19 Der Einsatz von Beta-2-Mimetika wird kontrovers diskutiert. Einige Studien belegen die Wirksamkeit der Therapie, andere zeigen keinen Nutzen (Flores and Horwitz, 1997, Black, 2003). Es wird ein Therapieversuch unter stationären Bedingungen empfohlen, der bei Unwirksamkeit rasch beendet werden sollte. Ähnliches gilt auch für die Inhalation mit Epinephrin (Döring et al., 2005). Kortikosteroide zeigten in einer Metaanalyse keine Wirksamkeit im Vergleich zu Placebo (Patel et al., 2008), allerdings bestehen Hinweise auf eine Wirksamkeit im frühen Krankheitsverlauf (Garrison et al., 2000) und bei schweren Krankheitsverläufen (Woensel et al., 2003). Eine Vernebelung mit Ribavirin als Virostatikum zeigt sich bei betroffenen Säuglingen als hilfreich bezüglich eines geringeren Sauerstoffbedarfs, hat aber keinen Einfluss auf das Outcome dieser Patienten, so dass aufgrund der hohen Behandlungskosten und der möglichen Teratogenität meist darauf verzichtet wird (Ventre and Randolph, 2004). Eine aktive Impfung steht bisher nicht zur Verfügung, wird aber entwickelt und ist von sozioökonomischer Bedeutung (Littel-van den Hurk et al., 2007). Eine Möglichkeit der Infektionskontrolle bzw. Prävention besteht in der passiven Immunisierung mit Palivizumab, einem monoklonalen Antikörper, der gegen das F-Protein gerichtet ist. Diese ist vor allem bei Kindern mit einem erhöhten Risiko für schwere Krankheitsverläufe indiziert. Stellungnahmen verschiedener pädiatrischer Fachgesellschaften (Forster, 2003, Schmaltz, 2004) empfehlen die Anwendung bei folgenden Risikogruppen: Kinder unter zwei Jahren, die wegen bronchopulmonaler Dysplasie wenigstens drei Monate vor RSV-Saisonbeginn therapiert werden, Kinder unter zwei Jahren mit hämodynamisch signifikanter Herzerkrankung, sowie Kinder aufgrund individueller Indikationsstellung im Rahmen der Zulassung, z.B. Frühgeborene unter 35. SSW. Eine breite Anwendung ist aufgrund der hohen Kosten schwierig. 20 1.3 Allergische Erkrankungen 1.3.1 Epidemiologie und Risikofaktoren allergischer Erkrankungen Epidemiologie Die Zunahme an atopischen Erkrankungen im Säuglings- und Kleinkindesalter rückt zunehmend in das Interesse der Öffentlichkeit. Die Prävalenz von Asthma, atopischem Ekzem und allergischer Rhinokonjunktivitis ist in den letzten Jahrzehnten stark angestiegen, scheint aber derzeit ein Limit erreicht zu haben (Zollner et al., 2005). Nach der ISAAC-Studie ist die Prävalenz von Asthma am höchsten in England, Australien, Neuseeland und der Republik Irland, wohingegen die Prävalenzen von allergischer Rhinitis und atopischem Ekzem weltweit gleichmäßig gestreut sind (ISAAC, 1998). Ergebnisse der ISAAC-Studie für das Studienzentrum Münster zeigten einen Anstieg der Prävalenz von Asthmasymptomen bei Sechsjährigen von 9,8% auf 13,3% innerhalb eines fünfjährigen Intervalls von 1994/95 bis 1999/2000 (Maziak et al., 2003). Risikofaktoren Bezüglich der Risikofaktoren ist es sinnvoll, diese in drei Gruppen zu unterteilen. Dabei ist der Phänotyp des atopischen Erscheinungsbildes abhängig von der genetischen Prädisposition, dem Zeitpunkt und der Menge der ersten Allergenexposition, sowie unspezifischen Risikofaktoren (Björksten, 1994, Kabesch, 2001). Einen Risikofaktor hinsichtlich des genetischen Aspektes stellt die positive Familienanamnese, besonders mütterlicherseits, dar (Sears et al., 1996). Es gibt zahlreiche Untersuchungen, die auf eine genetische Beteiligung bei dem Erscheinungsbild Asthma hindeuten. Verschiedenste Gene wurden lokalisiert und mit bestimmten Allergie-Manifestationen assoziiert. Allerdings stellte man auch fest, dass viele Kinder, die unter einer Allergie leiden, keinen Hinweis auf eine genetische Veränderung zeigten. Vielmehr das Zusammenspiel zwischen genetischer Prädisposition und Umweltfaktoren bringt den Phänotyp Allergie hervor (Wahn and Mutius, 2001). 21 Daneben sind als nicht spezifische Risikofaktoren männliches Geschlecht, Rauchen während des letzten Schwangerschaftstrimenons und ein Geburtszeitpunkt während der Wintermonate zu nennen (Sears et al., 1996). Das Geburtsgewicht, Geschwisteranzahl, sozioökonomischer Status und Luftverschmutzung haben dagegen nur geringen bis gar keinen Einfluss auf die Entstehung von Asthma, allergischer Rhinitis oder atopischem Ekzem (Sears et al.,1996, ISAAC, 1998). In welchem Ausmaß Ernährung (Beginn und Zusammensetzung der Beikost), Exposition gegenüber Hausstaub, genetische und immunologische Reaktionen das Atopierisiko beeinflussen, wird kontrovers diskutiert. Darauf wird zu einem späteren Zeitpunkt eingegangen. 1.3.2 Pathogenese von allergischen Erkrankungen Reifung und Entwicklung des Immunsystems und der T-Zellen Ab der sechsten Schwangerschaftswoche gehen aus der embryonalen Leberanlage Stammzellen hervor, die durch Chemotaxis ab der neunten Woche im Thymus angesiedelt werden. Die Reifung der Stammzellen in der 12. bis 16. Gestationswoche erfolgt in vier Stufen: Mutationen, somatische Rekombinationen, positive Selektion und negative Selektion. Die anfänglichen Mutationen führen zum Austausch von DNA-Sequenzen, durch somatische Rekombinationen werden die Gene für den T-Zell-Rezeptor arrangiert. Dann werden die T-Zellen geprüft, ob sie körpereigene Strukturen (MHC-Komplexe) tolerieren, und die so positiv selektionierten T-Zellen nochmals sortiert, indem ihnen alle im Körper vorhandenen Strukturen in Verbindung mit MHC-Komplexen präsentiert werden. Passen sie nach dem Schlüssel-Schloss-Prinzip auf eine solche Verbindung, werden sie eliminiert, um eine gegen den eigenen Körper gerichtete Immunantwort zu verhindern. Alle übrig gebliebenen Zellen haben ihr Ziel erreicht und übernehmen nun ihre jeweilige Funktion als T-Helfer-Zelle (CD4+) oder als T-Killer-Zelle (CD8+) (Janeway et al., 2002). So ist am Ende des vierten Schwangerschaftsmonats ein zentrales Immunsystem ausgebildet, wobei bis zum Lebensende immer noch Stammzellen im Thymus reifen. 22 Gegenüber Erwachsenen ist bei Säuglingen im gesamten ersten Lebensjahr allerdings eine erhöhte T-Suppressor-Aktivität nachweisbar, der Anteil von NK-Zellen ist auf 20% erhöht gegenüber 2 bis 3% bei Erwachsenen (Holländer et al., 2005). Daneben erhält der Fetus im letzten Trimenon diaplazentar IgG-Antikörper der Mutter. Diese werden nach der Geburt erst durch kindseigene IgM-, später auch durch IgG-Antikörper ersetzt. Perinatale T-Helfer-Zell-Differenzierung Über Signale von anderen Zellen, beispielsweise antigenpräsentierenden dendritischen Zellen, wird die Differenzierung der Th0-Zelle stimuliert. Th0Zellen sind naive T-Zellen, die noch keinen Antigenkontakt gehabt haben. Bei Anwesenheit von bestimmten Interleukinen entwickeln sich entweder Th1- oder Th2-Zellen. (O´Garra, 1998) Die T-Zellen erfahren schon intrauterin ein spezifisches Priming, so dass zum Zeitpunkt nach der Geburt bei allen Neugeborenen ein Th2-Zytokinprofil nachweisbar ist. Normalerweise ändert sich die Immunantwort auf Allergene und körperfremde Substanzen innerhalb des ersten Lebensjahres in ein Th1dominiertes Zytokinprofil. Bei Atopikern ließ sich aber eine zunächst bis zum Alter von 2 Jahren anhaltende Th2-Antwort nachweisen aufgrund einer relativ zu niedrigen IFN-gamma-Produktion (Prescott et al., 1998, 1999). Th1 / Th2 – Antwort Bei der Differenzierung der T-Zellen kommt neben anderen Zytokinen dem Interleukin 12 besondere Bedeutung zu. IL-12 wird von dendritischen Zellen bei Kontakt mit bestimmten pathogenen Faktoren gebildet und stimuliert naive CD4+ T-Zellen zur Differenzierung in Th1-Zellen (Macatonia et al., 1995). Diese Th1-Zellen sind charakterisiert durch ein spezifisches Zytokinmuster, welches unter anderem IFN-gamma als charakteristisches Zytokin beinhaltet. Weitere Zytokine sind IL-2 und TNF-alpha, welche die Th1-Zelle darin unterstützen, die zelluläre Immunantwort zur Bekämpfung vor allem intrazellulärer Erreger zu initiieren. Bei Abwesenheit von IL-12 findet eher eine Differenzierung zu Th2-Zellen statt (Martinez, 1999), welche dann durch Produktion von IL-4 die Entstehung von Th1-Zellen nochmals unterdrücken. Th2-Zellen induzieren 23 eine humorale Immunreaktion vor allem gegenüber extrazellulär gelegenen Pathogenen über die Interaktion mit B-Zellen. Zum Zytokinprofil der Th2Zellen gehören neben IL-4 auch IL-5, IL-6, IL-10 und IL-13, welche die Sekretion von Immunglobulinen der B-Zellen stimulieren. IL-4 bewirkt in den B-Zellen eine verminderte Produktion von IgM zugunsten einer gesteigerten Sekretion von IgE. Das IgE wiederum bindet an entsprechende Rezeptoren auf Mastzellen, Eosinophilen und anderen Zellen, die durch Ausschüttung entsprechender Substanzen dann eine Entzündungsreaktion im Sinne einer „allergischen Reaktion“ hervorrufen. Neben den oben genannten Zytokinen sind für die Polarisierung der T-Zellen auch die Art und Menge des Antigens sowie die Herkunft der Antigenpräsentierenden Zellen von Bedeutung. Ebenso spielt die Route der Immunisierung und die genetische Disposition des Empfängers eine Rolle. Die Anwesenheit von B-Zellen und eine niedrige Antigenkonzentration fördern die Th2-Bildung, während eine hohe Antigenkonzentration eine Th1Bildung stimuliert (Holländer et al., 2005). Die Hygiene-Hypothese Zum Zeitpunkt der Geburt dominiert eine Th2-Zell-gesteuerte Immunantwort. Dauert diese länger als gewöhnlich an, besteht ein größeres Risiko für die Entwicklung allergischer Erkrankungen. Beeinflusst wird die Richtung, die das Immunsystem nimmt, durch verschiedene endogene und exogene Faktoren. Besteht ein frühzeitiger Kontakt zu bakteriellen und viralen Antigenen, so fördert dies die Entwicklung einer Th1-Antwort. Die HygieneHypothese besagt, dass durch eine gesteigerte Hygiene sowie weniger bakterielle Infekte in der ersten Lebensphase eher eine Th2-Antwort generiert und somit das Entstehen allergischer Erkrankungen begünstigt wird (Bach, 2002, Hansen, 2005, Gern and Busse, 2002). Die Zunahme allergischer Erkrankungen wird in zahlreichen epidemiologischen Studien weltweit untersucht (ISAAC, 1998, Weinmayr et al., 2007). Beurteilt werden Zusammenhänge zwischen verschiedenen viralen und bakteriellen Infektionen, das Ausmaß von Umweltfaktoren, das Zusammenspiel von genetischen Faktoren und verschiedenen äußerlich einwirkenden Agenzien 24 auf die angeborene und adaptive Immunantwort (Schaub et al., 2006, von Mutius, 2007). Aber auch der Anteil der Th1-gesteuerten Autoimmunerkrankungen wie beispielsweise Diabetes mellitus Typ I oder Morbus Crohn nimmt stetig zu (Bach, 2002). In Ländern mit Wurminfektionen als stärkstem Trigger einer Th2-Antwort sind Allergien vergleichsweise selten. Es wurde aber bei mit Schistosomen infizierten Kindern ein hoher IL-10-Spiegel entdeckt (van der Kleij et al., 2002). Dies leitet zu der Frage hin, ob es einen kausalen Zusammenhang zwischen der Abnahme bakterieller Erkrankungen in der frühen Kindheit und der Zunahme von allergischen und autoimmunologischen Erkrankungen in einer späteren Lebensphase gibt. 1.3.3 Gesamt-IgE Atopische Erkrankungen gelten allgemein als IgE-vermittelte Entzündungsreaktionen. Eine überschießende IgE-Antwort ist genetisch determiniert. Dabei ist eine allergische Reaktion nicht abhängig vom GesamtIgE-Spiegel, sondern vom Verhältnis des allergenspezifischen IgE im Verhältnis zum Gesamt-IgE, d.h. auch Menschen mit einer ausgeprägten Allergie können einen normalen Gesamt-IgE-Spiegel haben. Der Anteil der allergenspezifischen IgE-Antikörper am Gesamt-IgE beträgt weniger als 1%, kann aber bei stark atopisch reagierenden Personen auf bis zu 40% ansteigen (Palmer et al., 2000). IgE ist Teil der frühen Immunantwort und wird durch niedrige Antigendosen induziert oder entsteht als Reaktion auf Parasitenbefall. Synthetisiert wird es in B-Zellen. Die IgE-Antwort ist von kurzer Dauer und kann durch hohe Allergendosen oder wiederholte Immunisierung unterdrückt werden (Prinzip der Desensibilisierung). Die IgE-Antwort wird durch IL-4 verstärkt, welches von Th2-Zellen gebildet wird und unterdrückt durch IFN-gamma, welches von Th1-Zellen produziert wird. Auslöser der allergischen Reaktion ist aber der IgE-Rezeptor, welcher sich auf der Oberfläche von Mastzellen befindet. Dieser Rezeptor bindet die 25 zirkulierenden IgE-Antikörper an seine Oberfläche. Sind Antigene vorhanden, binden die Antigene an die auf der Oberfläche der Mastzellen sitzenden IgEAntikörper und vernetzen diese. Daraufhin setzt die Mastzelle über komplexe Signalwege bestimmte Zytokine frei, welche eine allergische Entzündungsreaktion initiieren. Zu diesen Zytokinen gehört beispielsweise das IL-4, IL-6, TNF-alpha und GM-CSF (Cookson and Moffat, 2002). Die Synthese des IgE in den B-Zellen hängt wiederum von der Zytokinproduktion der stimulierenden T-Zellen und vom Ort der Allergenpräsentation ab. Eine IgE-Antwort ist Teil der normalen Reaktion auf vielfältige Antigene. Ob daraus ein pathologisches Reaktionsmuster im Sinne einer Allergie entsteht, hängt von der weiteren Regulation der Immunantwort ab. 1.4 Auswirkungen des RS-Virus auf das menschliche Immunsystem: Induktion einer Th2-Antwort 1.4.1 Zelluläre Immunantwort Bei der Immunantwort auf das RS-Virus sind verschiedene Zelltypen beteiligt. Dabei steht der Schutz des Organismus im Vordergrund, allerdings können bestimmte Abwehrreaktionen auch Schäden hervorrufen. Nach der Abwehr mittels der angeborenen Immunität über antivirale Zytokine und NKZellen in den ersten drei postinfektiösen Tagen schreitet die erworbene Immunität über B- und T-Zellen etwa ab dem fünften postinfektiösen Tag in die Abwehr des RS-Virus ein (Tripp, 2004). Die zelluläre Kommunikation dabei funktioniert sowohl über Zytokine und Chemokine, als auch über direkten Kontakt. Antigen-präsentierende Zellen: Antigene, welche die Schleimhautbarriere überwinden, werden von antigenpräsentierenden Zellen prozessiert. In der Regel sind dies dendritische Zellen. Über eine Anzahl an Proteinen auf ihrer Oberfläche rufen sie Immunreaktionen hervor. Sie regen naive T-Zellen zu 26 einer Reaktion auf das Antigen an („Priming“). Bei in-vitro-Versuchen mit dendritischen Zellen aus Nabelschnurblut konnte nach Infektion mit RSV eine verminderte IFN-gamma-Produktion und eine gesteigerte Synthese von Prostaglandin E2, IL-10 und IL-11 festgestellt werden (Bartz et al., 2002, 2003). Dies unterstützt die These, dass das RS-Virus die ohnehin schon bei Säuglingen vorherrschende Th-2-Antwort verstärkt. CD4+ T-Helferzellen: Bezüglich der Antwort der CD4+ T-Helferzellen gibt es zahlreiche Untersuchungen, ob auf eine RSV-Infektion eher eine Th1Antwort oder Th2-Antwort generiert wird. Über Messungen des Zytokinprofils, insbesondere IL-4 und IFN-gamma, lassen sich genügend Hinweise für beide Reaktionswege finden (Varga et al., 2000). Die meisten Viren rufen, wie schon oben erwähnt, bei einem reifen Immunsystem über eine Stimulation der zellulären Abwehr eine Th1-Antwort hervor, welche durch hohe IFN-gamma-Produktion charakterisiert wird. Es gibt aber Hinweise, dass das RS-Virus über das G-Protein eine Th2-Antwort (Schwarze and Schauer, 2004) sowie eine pulmonale Eosinophilie (Johnson et al., 1998, Matthews et al., 2005) bewirkt. Blutuntersuchungen bei RSV-infizierten Kindern haben gezeigt, dass signifikant mehr B-Zellen und ein höherer Anteil von IL-4 nachweisbar waren im Vergleich zu gesunden Kindern, wohingegen die IFN-gamma-Produktion in T-Zellen stark erniedrigt war (Roman et al., 1997). Die IL-4 / IFN-gammaRatio war bei RSV-Infizierten gegenüber der Kontrollgruppe signifikant erhöht, was die Hypothese einer Th2-Antwort auf eine RS-Virusinfektion stützt. Ob nun genetisch bedingt ist, dass bestimmte Kinder mit dem Zytokinprofil einer gesteigerten Th2-Antwort reagieren, oder ob die gemessene Th2Antwort aufgrund einer durch das Virus verminderten Th1-Antwort (Aberle et al., 1998, Legg et al. 2002) das Immungeschehen dominiert, ist noch nicht geklärt. Zusammenfassend scheint aber eine Th2-Antwort bei schweren Krankheitsverläufen zu dominieren, wohingegen eine Th1-Antwort bei leichten Infektionen im Vordergrund steht (Roman et al., 1997, Renzi et al., 1999). 27 CD8+ Zytotoxische T-Zellen: CD8+ T-Zellen scheinen die Immunantwort ebenfalls mit Hilfe von IFN-gamma zu dominieren, welches insbesondere durch Stimulation des RSV-G-Proteins gebildet wird. Im Gegensatz zu den CD4+ T-Helferzellen, die sich eher im peripheren Blut befinden, sind CD8+ T-Zellen im Bereich der Mukosa lokalisiert. In den Granula der zytotoxischen T-Zellen sind verschiedene toxische Substanzen enthalten, neben Perforinen auch lysosomale Enzyme und Granzyme. Im Trachealsekret von beatmeten RSV-infizierten Kindern ließ sich im Gegensatz zu einer Kontrollgruppe eine deutlich gesteigerte Aktivität von Granzym A und B nachweisen, welches sowohl von CD8+ T-Zellen als auch von CD4+ T-Zellen und NK-Zellen stammte (Bem et al., 2008). Regulatorische T-Zellen: Es gibt verschiedene regulatorische T-Zellen, die am besten untersuchten sind die CD4+CD25+ T-Zellen, daneben sind Tr1Zellen, Th3-Zellen, NK-Tr-Zellen und CD8+ Tr-Zellen Gegenstand aktueller Forschung (Holländer et al., 2005). CD4+CD25+ regulatorische T-Zellen können überschießende Immunantworten, sowohl Th1- als auch Th2dominierte, kontrollieren, indem sie IL-10 und TGF-ß ausschütten. Regulatorische T-Zellen und ihre Rolle bei viralen Infektionen sind Gegenstand vieler derzeitiger Forschungsprojekte (Zhou, 2008). NK-Zellen: Sie können als Zellen der frühen Immunantwort das weitere Geschehen beeinflussen. Auch sie bilden IFN-gamma, und zwar zu einem Zeitpunkt der Infektion, an dem sich die Zellen des spezifischen Immunsystems differenzieren. Nach Meinung von Openshaw und Tregoning kontrollieren NK-Zellen über die Sekretion von IFN-gamma die CD8+ Antwort, wobei das IFN-gamma selbst schon virotoxisch wirkt. Sie können eine Eosinophilie des Gewebes verhindern (Openshaw and Tregoning, 2005). Bei geringer Anzahl der NK und nachfolgender verminderter CD8+TZell-Antwort resultiert eine pulmonale Eosinophilie (Hussel and Openshaw, 1997). Eosinophile Granulozyten: Kinder mit einem schweren Krankheitsverlauf und späterem dauerhaftem Giemen zeigten während der Erstinfektion mit RSV 28 eine Eosinophilie im peripheren Blut sowie erhöhte Gesamt-IgE-Werte im Serum (Martinez et al., 1998). Dies führte zur der Vermutung einer gesteigerten Th2-Antwort. Ob diese aufgrund einer angeborenen Neigung zur gesteigerten Th2-Antwort stattfindet oder ob die Reaktionsweise virusinduziert ist, bleibt offen. Es gibt Hinweise, dass eine Eosinophilie zum Zeitpunkt der RSV-Infektion mit anhaltendem Giemen im Alter von 7 Jahren assoziiert ist (Ehlenfield et al., 2000). IL-4 Rezeptor-Atypie: Untersuchungen zeigen bei schweren RSV-Verläufen im Gegensatz zu einer Kontrollgruppe einen bestimmten Polymorphismus der Genloci, welche den IL-4-Rezeptor kodieren (Hoebee et al., 2003). Eine weitere Arbeitsgruppe fand bei schweren RSV-Verläufen sowohl eine Atypie des IL-4-Rezeptorgens als auch des IL-13-Haplotyps (Puthothu et al., 2006). Dies legt die Vermutung nahe, dass aufgrund genetischer Variationen von bestimmten Rezeptoren die T-Zell-Antwort in Richtung einer Th2-Antwort gelenkt werden kann, und dass schwere Verläufe einer RSV-Bronchiolitis durch bestimmte genetische Ausprägungen bedingt sein können. TLR4 –Rezeptor: Das F-Protein des RS-Virus induziert bei menschlichen Monozyten die Bildung proinflammatorischer Zytokine wie IL-6 und IL-8. Die Bildung ist abhängig von der Expression von CD14 und TLR4 auf diesen Monozyten (Becker, 2006). Neben Monozyten wird TLR4, der signaltransduzierende Rezeptor für LPS, auch auf einer Vielzahl von anderen Zellen exprimiert. Dazu gehören auch Makrophagen, dendritische Zellen, neutrophile Granulozyten, Mastzellen und B-Lymphozyten (Holländer et al., 2005). Derzeit Polymorphismen werden des verschiedene TLR4-Rezeptors genetische für die Mutationen und Empfänglichkeit und Ausprägung einer schweren RSV-Bronchiolitis diskutiert (Puthothu et al., 2006, Tal et al., 2004, Tulic et al. 2007). 1.4.2 Humorale Immunantwort Virusspezifische Antikörper: Auf humoraler Ebene wirken RSV-spezifische Immunglobuline dem Virus entgegen. Kinder mit einem hohen Titer 29 diaplazentar erhaltener Antikörper entwickeln weniger schwere Infektionen (Holberg et al., 1991). Andererseits ist das Vorhandensein von RSVspezifischem IgE mit einem schwereren Krankheitsverlauf assoziiert (Welliver, 1999). Der Nachweis von virusspezifischem IgE stützt weiterhin die Vermutung, dass das RS-Virus eine Th2-Antwort hervorrufen könnte (Becker, 2006). In einem in vitro-Experiment ließ sich nachweisen, dass BZellen durch Stimulation der antiviralen Kinase die Produktion der Antikörper hin zum Isotyp IgE switchen können (Rager et al., 1998). Eosinophiles Neurotoxin, welches von aktivierten Eosinophilen ausgeschüttet wird, hat RNAse-Aktivität und kann die Replikation von RSV stoppen (Domachowske et al., 1998) und unterstützt somit die antivirale Wirkung der Immunantwort. 1.4.3 Weitere Faktoren Antwort der Epithelzellen Das G-Protein des RS-Virus wird von infizierten respiratorischen Epithelzellen sowohl membranständig als auch in löslicher Form präsentiert und sezerniert. Durch die Produktion von löslichem G-Protein wird der Entzündungsprozess zunächst örtlich auf den Interzellulärraum ausgedehnt, das RS-Virus kann sich währenddessen in der infizierten Zelle vermehren und weiter von Zelle zu Zelle ausbreiten (Arnold et al., 2004). Dabei wird das Virus auf der zum Bronchiallumen hin gelegenen Seite ausgeschüttet und über die Zilienbewegung auf andere Zellen übertragen (Zhang et al., 2002). Das Vorhandensein von RSV-Genomfragmenten und löslichem F- und GProtein bewirken eine gesteigerte IL-8-Synthese und Sekretion in den betroffenen Epithelzellen und begünstigen über bestimmte intrazelluläre Reaktionswege eine anhaltende Entzündungsreaktion (Tirado et al., 2005). Neben der möglichen Viruspersistenz gerade bei Früh- und Neugeborenen gibt es noch eine weitere mögliche pathophysiologische Erklärung für das postbronchiolitische Giemen. Die Reparatur der einzelnen zerstörten Zellen beginnt innerhalb einiger Tage nach Einsetzen der Symptome, aber das Wiederherstellen eines funktionstüchtigen zilientragenden Gewebes dauert einige Wochen. In dieser Zeit können noch Krankheitssymptome wie Husten, 30 Giemen und eine reduzierte Lungenfunktion nachweisbar sein (Holt and Sly, 2002). Dass bei einer RSV-Bronchiolitis der inflammatorische Vorgang länger als üblich anhält, bewies auch die Arbeitsgruppe von Smyth. Sie wies eine Anwesenheit des löslichen IL-2-Rezeptors, welcher von an der Immunantwort beteiligten Lymphozyten gebildet wird, bis zu 150 Tage nach akuter Infektion nach (Smyth et al., 1997). Rolle des Surfactant Einige Studien postulieren eine Dysfunktion des Surfactant als Ursache einer schweren RSV-Infektion. Bestimmte genetisch bedingte Polymorphismen der Surfactant-Proteine A und D sind bei schwerer RSV-Bronchiolitis nachweisbar (Sorensen et al., 2007, Hallman and Haatja, 2006). Ebenso wird eine genetische Prädisposition für schwer verlaufende RSV-Erkrankungen und Asthma aufgrund eines Surfactant-Protein C Haplotypes vermutet (Puthothu et al., 2006). Pathophysiologisch gelangen aufgrund der gestörten Surfactant-Funktion Plasmaproteine in die Alveole, mit der Folge einer Obstruktion durch Herabsetzung der Resistance (van Schaik et al., 2000). Lungengröße und Funktion Gerade in kleinen Atemwegen führt ein Epithelschaden und eine gesteigerte Schleimsekretion zu einer Obstruktion und Minderbelüftung. Diese Situation bietet optimale Bedingungen für eine persistierende Entzündungsreaktion (Openshaw, 2005). Schon früh wurde ein Zusammenhang zwischen der initialen Atemwegsgröße, der vorbestehenden Lungenfunktion und einer Anfälligkeit für wiederholtes Giemen beobachtet (Martinez et al., 1998). Es erklärt aber noch nicht, warum Kinder mit annähernd gleicher Lungenfunktion unterschiedliche Krankheitsverläufe zeigen. 31 1.5 Fragestellung: Lässt sich ein Einfluss des RS-Virus auf späteres Giemen und eine spätere allergische Sensibilisierung nachweisen? Anhand der Daten, die während des Klinikaufenthalts von Säuglingen mit einer RSV-Bronchiolitis Lebenswochen bei der gewonnen wurden, Kontrollgruppe bzw. erhoben in wurden, den und ersten einer Untersuchung beider Gruppen in einem Alter von zwölf Monaten, sollte der Frage nachgegangen werden, ob die Gruppe der RSV-infizierten Kinder im weiteren Verlauf tatsächlich mehr Symptome in Form von Giemen zeigt und ob schon im Alter von einem Jahr eine erhöhte Rate von Allergien oder allergischen Sensibilisierungen vorliegt. 32 2 Patienten, Material und Methoden 2.1 Patienten 2.1.1 Ethik Die Studie wurde von der Ethik-Kommission der Medizinischen Fakultät der Ruhr-Universität Bochum genehmigt. Vor der Teilnahme ihrer Kinder an der Studie wurden die Eltern mündlich und schriftlich informiert. Sie unterzeichneten eine entsprechend formulierte Einverständniserklärung. 2.1.2 Fallgruppe Die Kinder der Fallgruppe wurden im Zeitraum Dezember 1999 bis April 2002 aus dem Patientengut der Universitäts - Kinderklinik des St. Josef Hospitals Bochum rekrutiert. Insgesamt 48 Kinder erfüllten die Einschlusskriterien der Studie mit einem Alter unter 12 Monaten und laborchemisch nachgewiesener RSV-Infektion. Um Unreife und andere auf das Immunsystem einwirkende Faktoren ausschließen zu können, galten Frühgeburtlichkeit, Schwierigkeiten mit der Atmung in der Neugeborenenperiode sowie angeborene und chronische Erkrankungen der Atemwege, des Herzens und anderer Organe als Ausschlusskriterien. Als wegweisend für die klinische Diagnose einer akuten Bronchiolitis wurden Tachypnoe, Giemen, ein verlängertes Exspirium und Rasselgeräusche gewertet. Diese Befunde wurden entweder im Rahmen der Aufnahmeuntersuchung oder zu einem späteren Zeitpunkt im Verlauf der Erkrankung erfasst und dokumentiert. Es traten im Krankheitsverlauf häufig Fütterungsschwierigkeiten auf. Die zunächst klinische Diagnose RSV-Infektion wurde verifiziert durch den Virusnachweis aus Nasopharyngealsekret mittels eines RSV-Schnelltests. 33 Erst nach gesicherter Diagnose wurde den Eltern die Studie vorgestellt und sie wurden gefragt, ob sie und ihr Kind an einer fortlaufenden Studie bezüglich Atemwegsinfektionen und allergischen Erkrankungen teilnehmen wollen. Dem stimmten 42 Elternpaare zu. Während des stationären Aufenthalts wurden folgende Daten ermittelt: Geschlecht des Kindes Schwangerschaftsdauer Geburtsgewicht Dauer der Stillzeit Anzahl der Geschwister Rauchexposition des Kindes (Raucher in der Familie) Haustiere Atopierisiko Von den 42 Kindern waren 18 männlich, das mittlere Geburtsgewicht lag bei 3456 (3090-3820) Gramm. Das mittlere Gestationsalter betrug 39,3 (38-41) Wochen. Ein Kind zeigte Symptome einer atopischen Dermatitis vor RSVInfektion. Drei Kinder haben wahrscheinlich schon einmal etwa vier Wochen vor RSV-Infektion klinisch gegiemt. Im Durchschnitt waren die Teilnehmer der Studie bei stationärer Aufnahme 16 Wochen alt (5-42 Wochen). 35 Kinder benötigten bronchodilatatorische Medikamente, antibiotisch therapiert wurden 21. Die mittlere Aufenthaltsdauer betrug zehn Tage (3-26). 2.1.3 Kontrollgruppe Die 84 Kinder der Kontrollgruppe, davon 36 Jungen, wurden als Kohorte von Geburt an betreut. Die Familien stammen aus dem Einzugsgebiet der Kinderklinik. Ihr mittleres Geburtsgewicht betrug 3510 g (2460-4400 g), die mittlere Gestationsdauer 39,6 Wochen (37-42). Sie waren während der Neonatalzeit völlig gesund, es wurden keine Komplikationen angegeben. 34 Keines dieser Kinder wurde aufgrund eines respiratorischen Infekts stationär behandelt. 2.2 Durchführung der Studie Ziel dieser Fall-Kontroll-Studie war der Vergleich von Kindern, die an einer schweren RSV-Bronchiolitis erkrankt waren, mit Kindern, die klinisch gesund waren im Hinblick auf die Entwicklung einer Allergie im ersten Lebensjahr. Dazu wurden sowohl die Fall-Gruppe als auch die Kontroll-Gruppe im durchschnittlichen Alter von einem Jahr nochmals untersucht. Folgende Daten wurden erhoben: Größe Gewicht Dauer der Stillzeit Anzahl der Geschwister Rauchexposition des Kindes (Raucher in der Familie) Haustiere Atopierisiko Den Kindern wurde venös Blut in gängiger Punktionstechnik entnommen. Es wurden RSV-IgG-Antikörper und IgE-Antikörper gegen Nahrungsmittel- und Inhalationsantigene bestimmt. 2.2.1 Respiratory syncytial Virus ELISA Genzyme Virotech GmbH, Rüsselsheim Der qualitative und semiquantitative Nachweis der IgG-Antikörper im Patientenserum wurde mit Hilfe eines ELISA (enzyme linked immunosorbent assay) nach Angaben des Herstellers durchgeführt. 35 Testprinzip des ELISA : Virales Antigen ist am Boden eines Mikrotiterplattennapfes adsorbiert. Verdünnungen der Patientenprobe werden auf diesem Antigen inkubiert. Sind virusspezifische Antikörper in der Probe vorhanden, so binden sie an das Antigen. Nach einem Waschvorgang wird der gebundene Antikörper mit einem IgG-spezifischen Sekundärantikörper aufgesucht. Der Sekundärantikörper ist mit einem Enzym, in diesem Fall Peroxidase, konjugiert, das ein farbloses Substrat in ein lösliches farbiges Produkt konvertieren kann. Nach Zugabe einer Stopplösung schlägt die in diesem Fall blaue Lösung nach gelb um. Die optische Dichte der katalysierten Substratlösung gilt als Maß für die Menge an gebundenem Patientenantikörper. Testdurchführung: In einen Mikrotiterstreifen mit acht Einzelkavitäten werden pro Testansatz in das erste Loch 100 µl des PBS-Verdünnungspuffers als Leerwert gegeben. In die zweite Vertiefung wird die Negativ-Kontrolle, in die dritte die cut-offund in die vierte die Positivkontrolle gegeben. In die folgenden Kavitäten werden die Patientenseren in einer Verdünnung von 1:100 pipettiert. Danach erfolgt die Inkubation für 30 min. bei 37°C mit Abdeckung. Nach Ende der Inkubationszeit wird jede Vertiefung jeweils 4x mit je 350-400 µl PBS-Waschlösung gewaschen. Dann werden jeweils 100 µl des Antihuman-IgG-Konjugats in alle Kavitäten pipettiert, anschließend erfolgt wieder eine Inkubationsperiode von 30 min bei 37°C. Nach Beenden der Konjugatinkubation erfolgt nochmals ein 4-maliges Waschen mit PBS. In jede Kavität werden 100 µl einer TetramethylbenzidinSubstratlösung pipettiert, es folgt eine Inkubation in Dunkelheit für 30 min bei 37°C. Die Reaktion wird durch Zugabe von je 50 µl Citrat-Stopplösung beendet. Nach sorgfältigem Durchmischen der Flüssigkeiten erhält man eine gelbe Farbe, deren Extinktion bei 450/620 nm gemessen wird. 36 2.2.2 RSV-Schnelltest Abbott TESTPACK RSV, No. 2027-16 Der Abbott TESTPACK RSV ist ein Enzym-Immuno-Assay. Zunächst wird 0,75 ml abgesaugtes Dithiothreitol-Puffers Nasopharyngealsekret versetzt. Nach 5 min mit 3 Wartezeit Tropfen eines werden feste Sekretbestandteile von den im Puffer gelösten durch einen Filter getrennt. Dem Filtrat werden 3 Tropfen bovine RSV-Antikörper-Lösung gegen humanes RSV und 3 Tropfen einer Lösung von RSV-Antikörper- beschichteten Mikropartikeln beigegeben, die sich bei vorhandenem RSVAntigen in der Probe zu Antigen-Antikörper-Komplexen formieren. Nach 10 min Wartezeit wird die Probe auf die Reaktions-Platte aufgetragen. Auf der Reaktionsplatte erscheint ein weißes „Plus“ auf blauem Hintergrund. Es werden 3 Tropfen eines enzymgebundenen Anti-Biotin-Antikörpers auf der Platte zugesetzt. Nach 3 min werden durch Waschen mit einer GuanidinHydrochlorid-Lösung ungebundene Antikörper entfernt. 3 Tropfen eines chromogenen Substrates binden nach weiteren 3 min an die AntigenAntikörper-Komplexe und entwickeln innerhalb von 2 min den Farbumschlag. Ein Stopp-Reagens, ebenfalls Guanidin-Hydrochlorid, ermöglicht schließlich ein Ablesen des Testes. Der Test ist positiv, wenn das „Plus“ in der Mitte der Reaktionsplatte grau bis lila und dunkler als der Hintergrund ist. 2.2.3 IgE-Antikörpersuchtests FX5 und SX1; Pharmacia & Upjohn Diagnostics AB, Uppsala, Schweden Mit dem UniCAP inhalativer Allergie Test SX1 und dem UniCAP Nahrungsmittel Allergie Test FX5 werden jeweils spezifische IgE-Antikörper im menschlichen Serum oder Plasma bestimmt. Es ist ein in vitro Testsystem auf der Basis der ImmunoCAP-Technologie. Eine Mischung bestimmter Allergene, beim SX1 inhalative Allergene, beim FX5 Nahrungsmittelallergene, sind kovalent an das ImmunoCAP gebunden und reagieren mit dem spezifischen IgE der Serumproben der Patienten. 37 Nach Auswaschen von unspezifischem IgE werden enzymmarkierte Antikörper gegen IgE hinzugefügt, um einen Komplex zu bilden. Nach Inkubation wird ungebundenes Enzym-Anti-IgE ausgewaschen. Der gebundene Komplex wird anschließend mit einer Entwicklersubstanz inkubiert. Nach Abstoppen der Reaktion wird die Fluoreszenz gemessen und mit einer Referenz verglichen. Folgende Allergene sind an das SX1-ImmunoCAP gebunden: • Lieschgras • Roggen • Birke • Beifuss • Dermatophagoides pteronyssimus = Hausstaubmilbe • Katzenschuppen • Hundeschuppen • Cladosporium herbarum Folgende Allergene sind an das FX5-ImmunoCAP gebunden: • Eiklar • Milcheiweiß • Dorsch • Weizenmehl • Soja • Erdnuss 2.3 Definitionen der Begriffe 2.3.1 Atopische Dermatitis Der Begriff der atopischen Dermatitis ist nicht einheitlich definiert. Nach J. Hanifin wurden als Kriterien der atopischen Dermatitis für die Studie festgelegt (Hanifin, 1984): 38 • Chronischer oder chronisch schubweiser Verlauf • Ein juckendes, nicht-infektiöses Ekzem, bei Säuglingen vorzugsweise im Gesicht und an den Streckseiten der Extremitäten • Trockene und leicht verletzbare Haut 2.3.2 Wiederholtes Giemen Mindestens drei Episoden einer bronchialen Obstruktion waren erforderlich, um das Kriterium wiederholtes Giemen zu erfüllen. 2.3.3 Atopische Erkrankungen der Eltern oder Geschwister Die Angabe einer atopischen Erkrankung in der nahen Verwandtschaft des Probanden setzte voraus, dass diese von einem Arzt irgendwann einmal diagnostiziert wurde. Als atopische Erkrankungen galten Asthma, allergische Rhinokonjunktivitis und atopische Dermatitis. Als eine einfache Heredität wurde die atopische Erkrankung bei entweder einem Elternteil oder einem Geschwisterkind angenommen, als doppelte Vererbbarkeit das Auftreten einer Atopie bei mehr als einem Elternteil oder Geschwisterkind. 2.4 Statistische Methoden Um die Abhängigkeit zwischen zwei qualitativen Merkmalen zu prüfen, wurde in dieser Arbeit bei relativ geringem Stichprobenumfang der Fisher´s exact test gewählt. Für Vergleiche zwischen quantitativen Merkmalen wurde der Mann-WhitneyU-Test verwendet. Ein p-Wert < 0,05 wurde in beiden Tests als signifikant gewertet. Um zu bestimmen, welche angeborenen und umweltbedingten Risikofaktoren für die Entwicklung einer bronchialen Obstruktion oder allergischen Sensibilisierung von Bedeutung waren, wurde zunächst für die gesamte Gruppe von 126 Kindern der Fisher´s exact test für jeden 39 Risikofaktor und jede Variable durchgeführt. Außerdem wurden die Odds Ratios und die 95% Konfidenzintervalle berechnet. Um zu ermitteln, welche Risikofaktoren unabhängig voneinander mit bronchialen Symptomen oder allergischer Sensibilisierung einhergehen, wurde das Verfahren der Multivarianzanalyse für Risikofaktoren mit einem p < 0,1 eingesetzt. Auch in diesem Modell wurden die Odds Ratios und die 95% Konfidenzintervalle ermittelt. Die Berechnungen wurden mit Hilfe des Programms Statview Version 5.0.1 (SAS Institute, Cary, NC, USA) durchgeführt. 40 3 Ergebnisse Sowohl die 42 Kinder der Gruppe, bei denen ein stationärer Aufenthalt aufgrund einer schweren RS-Virus-Infektion notwendig war, als auch die Kontrollgruppe der 84 Kinder ohne Bronchiolitis wurden während ihres ersten Lebensjahres kontinuierlich betreut. Die beiden Gruppen wurden hinsichtlich 13 Merkmalen verglichen, die sich aus dem Fragebogen und der serologischen Untersuchung nach je einem Jahr ergaben. 3.1 Die Kinder der RSV-Gruppe hatten vermehrt rauchende Eltern und mehr Geschwister Der Fragebogen nach einem Jahr (siehe Anlage) beinhaltete Fragen nach Änderungen, die sich seit der Erstellung des ersten Fragebogens nach der Geburt bei der Kontrollgruppe bzw. dem eingetretenen Krankheitsfall bei der RSV-Gruppe ergaben. Dies betraf Änderungen bezüglich der Atopieanamnese der Mutter, dem Vater und den Geschwisterkindern sowie Fragen zu Änderungen der häuslichen Umgebung. Ebenso wurden die Daten bezüglich Längenwachstum, Kopfumfang und Gewicht der bisher durchgeführten UUntersuchungen notiert. Es wurde nach Symptomen pulmonaler und gastrointestinaler Erkrankungen sowie dem Neuauftreten von Hauterscheinungen gefragt. 41 Tabelle 1: Anamnestisch erhobene Daten im durchschnittlichen Alter von einem Jahr bei der RSV-Gruppe und der Kontrollgruppe Anamnestisch erhobenes RSV-Gruppe Kontrollgruppe Merkmal (n=42) (n=84) Einmaliges Atopieauftreten in Familie 17 49 0,09 Zweifaches Atopieauftreten in Familie 6 9 0,57 Einfaches Auftreten von Asthma 9 13 0,46 Doppeltes Auftreten von Asthma 4 5 0,48 Männliches Geschlecht 18 36 1,00 Rauchen Vater 18 20 0,04 Rauchen Mutter 18 13 <0,01 Rauchen während der Schwangerschaft 16 9 <0,001 Im Haushalt lebende Tiere 9 20 0,83 Geschwisteranzahl 1,33+-1,16 0,51+-0,75 <0,0001 Durchschnittliche Schwangerschaftsdauer 39,3+-1,3 39,6+-1,1 0,10 Durchschnittliches Geburtsgewicht 3456+-368 3510+-399 0,60 Stilldauer in Monaten 1,9+-2,6 2,0+-2,8 0,98 Durchschnittliches Gewicht in kg bei Kontrolluntersuchung 9,6+-0,9 9,7+-1,1 0,85 Durchschnittliche Länge in cm bei Kontrolluntersuchung 76,0+-3,0 75,6+-3,2 0,56 p-Wert 42 Hinsichtlich 11 von 15 Merkmalen ergaben sich keine Unterschiede zwischen beiden Gruppen. Lediglich bezüglich der Geschwisteranzahl und des Rauchens in der Familie waren signifikante Unterschiede deutlich erkennbar. Die Geschwisteranzahl war in der RSV-Gruppe deutlich höher (durchschnittlich 1,33 vs. 0,51 Geschwister). In den Familien der Kinder der RSV-Gruppe fiel auf, dass es eine vermehrte Anzahl sowohl rauchender Väter als auch rauchender Mütter gab, ebenso in der Schwangerschaft rauchender Mütter. Bezüglich im Haushalt lebender Tiere, der Stilldauer sowie des familiären Atopierisikos ergaben sich keine signifikanten Unterschiede. 3.2 Erhöhtes Auftreten von Giemen, wiederholtem Giemen, erhöhtem Gesamt-IgE und einer Sensibilisierung gegen Nahrungsmittelallergene in der RSV-Gruppe Bei der serologischen Untersuchung nach einem Jahr wurden das GesamtIgE, die IgE-Antikörper gegen Inhalations- und Nahrungsmittelallergene und RSV-IgG-Antikörper bestimmt. 3.2.1 Serologische Bestätigung der stattgefundenen RSV-Infektion In der RSV-Gruppe wurden bei 39 der 42 Kinder RSV-IgG-Antikörper serologisch nachgewiesen (93%), in der Kontrollgruppe in 29 von 84 Fällen (35%), (p<0,0001; OR 24,66; KI 7,01-86,73). Von den 29 Kindern der Kontrollgruppe ließ sich bei allen eine positive Anamnese bezüglich einer leichten Luftwegsinfektion erheben, in acht Fällen davon einschließlich des Auftretens einer pfeifenden Atmung in Form von Giemen, welche aber zu keinem Krankenhausaufenthalt während der RSV-Saison geführt hatte. Dies bestätigt nochmals nachgewiesenen die Richtigkeit der RSV-Krankheitsfälle, klinisch wobei und eine im RSV-Test entsprechende Immunantwort mit Bildung von RSV-IgG-Antikörpern stattgefunden hat, ebenso bei klinisch mildem Verlauf in der Kontrollgruppe. 43 3.2.2 Erhöhtes Gesamt-IgE, häufigeres Auftreten einer Sensibilisierung gegen Nahrungsmittelallergene, vermehrtes Giemen und wiederholtes Giemen in der RSV-Gruppe Um das Auftreten einer allergischen Sensibilisierung zu erfassen, wurde neben der serologischen Bestimmung des Gesamt-IgE und dessen oben erwähnter Differenzierung nach dem Auftreten von pfeifender Atmung im Sinne von Giemen, dem wiederholten Auftreten von Giemen und dem Auftreten eines atopischen Ekzems gefragt. Tabelle 2: Allergische Symptome im Vergleich - Univarianzanalyse Symptom RSVGruppe KontrollGruppe (n=42) (n=84) Giemen 28 13 <0,001 10,92 4,56-26,14 Wiederholtes Giemen 13 3 <0,001 12,10 3,22-45,55 Atopische Dermatitis 7 16 0,81 0,85 0,32-2,26 14 2 <0,001 20,50 4,38-95,89 Nahrungsmittelspezifisches IgE 14 1 <0,001 56,44 7,15-445,59 Inhalationsspezifisches IgE 2 1 0,26 6,38 0,64-63,39 Gesamt-IgE > 0,35 kU/l p-Wert Odds Ratio 95% Konfidenzintervall Aus den Daten der follow-up-Untersuchung ist ersichtlich, dass die Häufigkeit von wiederholtem Giemen in der Fall-Gruppe signifikant höher ist als in der Kontroll-Gruppe. Dabei war kein Zusammenhang zwischen dem Auftreten von wiederholtem Giemen und einer positiven Familienanamnese hinsichtlich atopischer Erkrankungen erkennbar, sowohl bei der RSV- als auch bei der Kontrollgruppe. 44 Bei der serologischen Untersuchung zeigten 14 der 42 Kinder der RSVGruppe ein erhöhtes Gesamt-IgE, bei der Kontrollgruppe nur zwei von 84 Kindern. Bei der weiteren Differenzierung in nahrungsmittel- und inhalationsallergenspezifisches IgE zeigten 13 Kinder der RSV-Gruppe eine alleinige Sensibilisierung gegen Nahrungsmittelallergene, ein Kind gegen Inhalationsallergene, Sensibilisierung und bei gegen zwei Kindern ließ sich Nahrungsmittelallergene sowohl eine als auch Inhalationsallergene feststellen. Es lässt sich demnach ein signifikanter Unterschied zwischen den beiden Gruppen bezüglich dem Auftreten einer Sensibilisierung gegen Nahrungsmittelallergene feststellen. Die beiden Gruppen unterschieden sich nicht in dem Auftreten einer atopischen Dermatitis. Fünf Kinder aus der RSV-Gruppe und keines der Kontrollgruppe wiesen sowohl eine serologische Sensibilisierung als auch klinisch wiederholtes Giemen auf. 3.3 RSV-Bronchiolitis als wichtigster Risikofaktor für Giemen, wiederholtes Giemen und allergische Sensibilisierung gegen Nahrungsmittelallergene im Alter von 12 Monaten In der Folge wurden von den erfragten Merkmalen mögliche genetische und umweltbedingte Risikofaktoren ermittelt und in Bezug zu dem Auftreten der Merkmale Giemen, wiederholtes Giemen und allergische Sensibilisierung im Alter von zwölf Monaten gestellt, unter Nutzung des Fisher-exakt-Testes. Ein p-Wert < 0,05 gilt als signifikant. 45 Tabelle 3: Mögliche Risikofaktoren in Bezug zum Auftreten von Giemen Univarianzanalyse mit Fisher´s Exact Test Risikofaktor p-Wert Odds Ratio 95% Konfidenzintervall <0,0001 10,92 4,56-26,14 Leichte RSV-Infektion 0,65 0,74 0,30-1,85 Rauchen Vater 0,02 2,03 1,15-5,63 Rauchen Mutter <0,0001 6,41 2,65-15,46 Rauchen während der Schwangerschaft <0,01 4,3 1,73-10,82 Haustiere 0,82 1,12 0,47-2,69 Asthma (einfach in Familie) 0,21 0,77 0,77-5,02 Asthma (zweifach in Familie) 0,15 2,81 0,71-11,10 Atopie (einfach in Familie) 1,00 0,93 0,44-1,97 Atopie (zweifach in Familie) 0,15 0,73 0,22-2,44 Männliches Geschlecht 0,06 2,22 1,04-4,47 Mehr als ein Geschwisterkind <0,01 4,47 1,23-16,23 RSV-Bronchiolitis 46 Tabelle 4: Mögliche Risikofaktoren in Bezug zum Auftreten von wiederholtem Giemen – Univarianzanalyse mit Fisher´s Exact Test Risikofaktor p-Wert Odds Ratio 95% Konfidenzintervall <0,0001 12,10 3,22-45,55 Leichte RSV-Infektion 0,36 0,44 0,09-2,06 Rauchen Vater 0,25 1,98 0,68-5,79 Rauchen Mutter <0,01 5,14 1,72-15,34 <0,0001 10,56 3,34-33,32 Haustiere 0,76 1,13 0,34-3,83 Asthma (einfach in Familie) 0,48 1,70 0,49-5,88 Asthma (zweifach in Familie) 0,32 2,10 0,40-11,14 Atopie (einfach in Familie) 0,79 1,20 0,42-3,44 Atopie (zweifach in Familie) 0,41 1,88 0,47-7,58 Männliches Geschlecht 0,79 0,77 0,26-2,27 Mehr als ein Geschwisterkind 0,03 3,80 1,20-12,00 RSV-Bronchiolitis Rauchen während der Schwangerschaft 47 Tabelle 5: Mögliche Risikofaktoren in Bezug zu einer allergischen Sensibilisierung - Univarianzanalyse mit Fisher´s Exact Test Risikofaktor p-Wert Odds Ratio 95% Konfidenzintervall <0,0001 20,50 4,38-95,89 0,12 0,20 0,02-1,55 Rauchen Vater 0,5626 1,46 0,49-4,36 Rauchen Mutter <0,0001 9,90 3,09-31,68 Rauchen während der Schwangerschaft <0,0001 10,56 3,34-33,32 Haustiere 0,12 0,20 0,02-1,55 Asthma (einfach in Familie) 1,00 1,11 0,29-4,26 Asthma (zweifach in Familie) 1,00 0,42 0,05-3,44 Atopie (einfach in Familie) 0,28 0,98 0,20-4,78 Atopie (zweifach in Familie) <0,01 6,00 1,80-19,98 Männliches Geschlecht <0,01 4,86 1,47-16,05 Mehr als ein Geschwisterkind 0,14 1,67 0,82-8,72 RSV-Bronchiolitis Leichte RSV-Infektion Dabei stellte sich die klinisch behandlungsbedürftige RSV-Bronchiolitis als wichtigster Risikofaktor für die drei Merkmale Giemen, wiederholtes Giemen und allergische Sensibilisierung im Alter von zwölf Monaten heraus. Ebenso ergab laut Aussage der Tabelle das Rauchverhalten der Mutter sowohl während der Schwangerschaft als auch nach der Geburt ein deutlich erhöhtes Risiko für die Entwicklung von Giemen, wiederholtem Giemen und einer allergischen Sensibilisierung im Alter von einem Jahr. Eine positive Familienanamnese beider Elternteile bezüglich einer Atopie und männliches Geschlecht stellten sich als mögliche Risikofaktoren einer allergischen Sensibilisierung dar. 48 3.4 Bestätigung der RSV-Bronchiolitis als unabhängigem Risikofaktor für Giemen, wiederholtes Giemen und allergische Sensibilisierung gegen Nahrungsmittel im Alter von einem Jahr Um die möglichen Risikofaktoren unabhängig voneinander bewerten zu können, wurden von Tab. 3 - 5 die Merkmale mit einem p-Wert < 0,10 genauer mittels Multivarianzanalyse untersucht und in Bezug zu den drei Merkmalen Giemen, wiederholtes Giemen und allergische Sensibilisierung gestellt. Die RSV-Bronchiolitis zeigt sich dabei als einziger unabhängiger Risikofaktor für die oben beschriebenen drei Merkmale. Rauchen in der Familie und männliches Geschlecht sind demnach als Risikofaktoren für zwei der drei Merkmale zu erkennen, nämlich für Giemen und eine allergische Sensibilisierung. Tabelle 6: Multivarianzanalyse möglicher Risikofaktoren in Bezug auf Giemen im Alter von einem Jahr – Analyse der in der Univarianzanalyse identifizierten möglichen Risikofaktoren (Tabelle 3) Risikofaktor p-Wert Odds Ratio 95% Konfidenzintervall <0,0001 10,32 3,56-29,96 Rauchen Vater 0,85 1,12 0,36-3,46 Rauchen Mutter <0,01 8,42 1,51-46,81 Rauchen während der Schwangerschaft 0,41 0,50 0,10-2,60 Männliches Geschlecht <0,01 4,24 1,49-12,05 Mehr als ein Geschwisterkind 0,19 2,25 0,68-7,46 RSV-Bronchiolitis 49 Tabelle 7: Multivarianzanalyse möglicher Risikofaktoren in Bezug auf wiederholtes Giemen im Alter von einem Jahr - Analyse der in der Univarianzanalyse identifizierten möglichen Risikofaktoren (Tabelle 4) Risikofaktor p-Wert Odds Ratio 95% Konfidenzintervall RSV-Bronchiolitis 0,01 8,92 1,42-55,88 Rauchen Mutter 0,68 0,68 0,11-4,12 Rauchen während der Schwangerschaft 0,02 6,45 1,52-27,23 Mehr als ein Geschwisterkind 0,29 2,14 0,52-8,81 Tabelle 8: Multivarianzanalyse möglicher Risikofaktoren in Bezug auf eine allergische Sensibilisierung gegenüber Nahrungsmitteln im Alter von einem Jahr - Analyse der in der Univarianzanalyse identifizierten möglichen Risikofaktoren (Tabelle 5) Risikofaktor p-Wert Odds Ratio 95% Konfidenzintervall <0,001 20,66 3,53-120,75 Rauchen Mutter 0,04 9,17 1,17-72,21 Rauchen während der Schwangerschaft 0,79 1,31 0,19-9,10 Männliches Geschlecht <0,01 12,20 2,37-62,50 Atopie (zweifach in Familie) 0,59 1,31 0,25-11,58 RSV-Bronchiolitis Eine positive Familienanamnese bezüglich Atopie, Asthma oder Neurodermitis scheint in dieser Arbeit nicht als Risikofaktor zu imponieren. 50 4 Diskussion 4.1 Bedeutung einer Sensibilisierung bezüglich des klinischen Auftretens einer Allergie Im ersten Lebensjahr des Säuglings muss sich dessen Immunsystem mit einer Fülle von neuen Antigenen auseinandersetzen. Durch den Kontakt mit Antigenen wie beispielsweise Viren, aber auch Nahrungsmitteln, bildet sich ein immunologisches Gedächtnis aus. Das Immunsystem muss lernen, zwischen körpereigenen und körperfremden Substanzen zu unterscheiden. Weiterhin muss es auch bestimmte körperfremde Substanzen tolerieren. Es finden bei einem Kontakt mit Antigenen verschiedene Möglichkeiten der Immunantwort statt. Gerade bei der Interaktion von B- und T-Zellen können je nach Zytokinprofil unterschiedliche interzelluläre Kommunikationswege genommen werden, die gänzlich verschiedene Auswirkungen auf den Gesamtorganismus haben. In den ersten Lebensmonaten ist weiterhin eine Immunmodulation möglich, gerade wenn diese interzellulären Kontakte durch bestimmte Antigene gestört werden. Es stellt sich die Frage, warum gerade Kinder mit einer schweren RSVErkrankung eine vermehrte Sensibilisierung gegenüber Nahrungs- mittelallergenen im Alter von einem Jahr haben und ob sich anhand der klinischen Studie Hinweise auf eine immunmodulatorische Wirkung des RSVirus zeigen. 4.1.1 RSV als spezifischer Risikofaktor einer Sensibilisierung gegen Nahrungsmittelallergene im Alter von 12 Monaten Im Vergleich der beiden Gruppen zeigte sich ein signifikanter Unterschied bezüglich der Sensibilisierung gegenüber Nahrungsmittelallergenen im Alter von 12 Monaten, nicht aber gegen Inhalationsallergene. Insgesamt 14 Kinder der RSV-Gruppe wiesen dabei nahrungsmittelspezifisches IgE auf im Gegensatz zu einem Probanden aus der Kontrollgruppe. 51 Eine Sensibilisierung gibt zwar keinen Hinweis auf die klinische Ausprägung des Merkmals Allergie, jedoch auf die Reaktivität des Immunsystems. Findet eine Sensibilisierung in der frühen Kindheit statt, so gilt dies als Risikofaktor für die spätere Entwicklung obstruktiver Bronchitiden (Sherrill et al., 1999). Ebenso gilt eine Sensibilisierung gegen Nahrungsmittelallergene von unter obstruktiven Atemwegserkrankungen leidenden Säuglingen als prädiktiver Faktor für die Persistenz der Asthmasymptome und die Entstehung eines allergischen Asthma bronchiale in der späteren Kindheit (Wildhaber and Sennhauser, 2002). Auch die Sensibilisierung gegen Hausstaubmilben, welche bei entsprechend hoher Allergenexposition schon im Säuglingsalter auftritt, scheint ein diagnostischer Marker für die spätere Entwicklung eines Asthma bronchiale zu sein und mit der frühkindlichen Sensibilisierung gegen Nahrungsmittelallergene verbunden zu sein (Lau, 2001). Eine serologisch nachgewiesene Sensibilisierung gegen Hühnereiweiß im Alter von 12 Monaten korreliert mit einer Sensibilisierung gegenüber Inhalationsallergenen im Alter von drei Jahren, vor allem in Kombination mit einer positiven Familienanamnese (Nickel et al., 1997). In einer anderen Studie wurde festgestellt, dass IgE-Antikörper gegen Kuhmilch und Hühnereiweiß im ersten Lebensjahr als normal und ohne Krankheitswert anzusehen sind, aber es wurde eine quantitative Erhöhung bei Kindern festgestellt, die im siebten Lebensjahr eine Allergie entwickeln (Hattevig, 2005). Die Studiengruppe um Rhodes stellte eine Sensibilisierung gegen Hühnereiweiß oder Kuhmilch im Prick-Test im Alter von einem Jahr als Risikofaktor für ein Asthma bronchiale im Erwachsenenalter fest, allerdings bei einem Risikokollektiv für atopische Erkrankungen (Rhodes et al., 2001). Um den möglichen allergiefördernden Einfluss von RSV im Alter von 12 Monaten nachzuweisen, eignet sich am ehesten der Nachweis einer Sensibilisierung gegen Nahrungsmittel, wie in dieser Alterskategorie zu diesem Zeitpunkt üblich (Wahn and Mutius, 2001). Mit der Nachweismethode in dieser Arbeit konnte die allgemeine Sensibilisierung gegen eines oder mehrere der sechs getesteten Nahrungsmittel Hühnereiweiß, Milcheiweiß, Dorsch, Weizenmehl, Soja und Erdnuss nachgewiesen werden. Eine weitere Spezifizierung, gegen welches 52 der genannten Allergene im einzelnen der jeweilige Proband Antikörper hat, erfolgte im Rahmen der Arbeit nicht. Im Vergleich zu anderen Studien, die nur die Sensibilisierung gegen Hühnereiweiß im Alter von 12 Monaten mittels Skin-Prick-Test diagnostizierten (Sigurs et al., 1995), ließen sich durch die o.g. breit gestreute Nachweismethode entsprechend häufiger mögliche Sensibilisierungen serologisch aufdecken und in einen Bezug zu einer RSVInfektion setzen. Die klinische Ausprägung der Sensibilisierungsreaktion bleibt dabei zunächst unklar. Bei der Befragung nach einem Jahr wurden keine Nahrungsmittelallergien von den Eltern angegeben. Falls gastrointestinale Symptome bejaht wurden, waren diese bei Nachfrage klinisch infektiöser Genese. Vielmehr ist die Sensibilisierungsreaktion an sich als mögliches Anzeichen einer immunmodulatorischen Wirkung des RS-Virus zu werten. Die Studiengruppe um Sigurs konnte mit dem Skin-Prick-Test im Alter von 12 Monaten keinen signifikanten Unterschied zwischen der RSV- und der Kontrollgruppe verzeichnen. Erst im Alter von drei Jahren zeigte sich ein serologisch nachgewiesener signifikanter Unterschied bezüglich der Sensibilisierung gegen Inhalationsallergene, ein Unterschied bezüglich serologischer Sensibilisierung gegen Nahrungsmittelallergene konnte in diesem Alter nicht mehr nachgewiesen werden (Sigurs et al., 2000). Dass in beiden Gruppen nur vereinzelt Sensibilisierungen gegen Inhalationsallergene nachgewiesen wurden ohne signifikanten Unterschied, erklärt sich aus dem zeitlich begrenzten Umfeld der Studie. Die Probanden haben im Alter von 12 Monaten jeweils nur eine Pollenflugsaison erlebt, in der eine Sensibilisierung hätte stattfinden können. Die klinische Ausprägung einer allergischen Reaktion mit massiver, nachweisbarer Antikörperbildung bei erneutem Kontakt zum auslösenden Agens kann aber erst in der nächsten Pollenflugsaison nach etwa einem Jahr erfolgen. Somit ist auch der Nachweis einer Sensibilisierung gegen Inhalationsallergene nicht 53 geeignet, den möglichen allergiefördernden Einfluss von RSV im Alter von 12 Monaten nachzuweisen. Diese Arbeit bezieht sich nur auf den Zeitraum von einem Jahr, so dass zunächst nur die Sensibilisierung gegen Nahrungsmittel im Vordergrund steht. Wie oben ausgeführt, könnte diese mit einer erhöhten Sensibilisierung gegen Inhalationsallergene korrelieren. Dies ist aber spekulativ und kann nur durch Follow-up Untersuchungen im weiteren Verlauf bewiesen werden. 4.1.2 Bedeutung eines erhöhten Gesamt-IgE-Wertes Ein Ergebnis dieser Arbeit ist, dass die Kinder der RSV-Gruppe im Alter von 12 Monaten ein signifikant erhöhtes Gesamt-IgE hatten. Bei weiterer Differenzierung des Gesamt-IgE zeigte sich eine Sensibilisierung hauptsächlich gegen Nahrungsmittelallergene. Eine Sensibilisierung gegen Inhalationsallergene scheint aufgrund des zeitlichen Rahmens, wie bereits oben ausgeführt, erst später eine Rolle zu spielen. IgE wird von B-Zellen produziert, und zwar nur, wenn diese von Th2-Zellen stimuliert werden. Die Regulation der IgE-gesteuerten antigenspezifischen Immunantwort wird durch bestimmte, von T-Zellen produzierte Zytokine beeinflusst. Das von Th2-Zellen gebildete IL-4 stimuliert die B-Zellen zur Produktion von IgE, wohingegen das von Th1-Zellen gebildete IFN-gamma die IgE-Produktion drosselt (Aberle et al., 1999). Kinder mit schwerer RSVBronchiolitis zeigten während der Infektion sowohl ein erhöhtes Gesamt-IgE als auch eine Eosinophilie (Martinez et al, 1998). IgE ließ sich auch in der Bronchiallavage von beatmeten RSV-Kindern nachweisen (Everard et al., 1994). Diese Erkenntnisse stützen die These, dass eine Infektion mit RSV eine Th2-gesteuerte Immunantwort hervorruft. Die Dominanz der Th2-Antwort kann auch aus einer Imbalance aufgrund einer unterdrückten Th1-Antwort resultieren (Prescott et al., 1999). Auch in 54 anderen Arbeiten wurden die Zytokinmuster während schwerer RSV- Infektionen untersucht, und erniedrigte IFN-gamma-Spiegel festgestellt. Untersuchungen zeigten, dass quantitativ verminderte Th1-Zytokine während der RSV-Infektion assoziiert sind mit einer verminderten Lungenfunktion 4,9 Monate später, und dabei niedrige IFN-gamma-Spiegel mit einem erhöhten Asthmarisiko korrelierten (Renzi et al., 1999). Über die jeweils ausgeschütteten Zytokine beeinflussen sich die T-Zellen gegenseitig in ihrem weiteren Wachstum. Bei einer hohen IL-4-Konzentration wird das Wachstum der Th1-Zellen gehemmt, und bei einer hohen IFNgamma-Produktion wird das Wachstum der Th-2-Zellen gehemmt (O`Garra, 1998). Desweiteren wird der Einfluss von regulatorischen T-Zellen diskutiert (O´Garra, 1998, Hansen, 2005). Diese regulatorischen T-Zellen produzieren sowohl IL-4 als auch IFN-gamma. Zusätzlich bilden sie TGF-beta, welches die weitere Entwicklung der Th1- und / oder der Th2-Antwort verhindert. Geht man von dieser Regulation der Immunantwort aus, könnte der Organismus sowohl eine überschiessende Th1- als auch Th2-Antwort verhindern und sich somit vor überschiessenden Reaktionen und der Entwicklung chronischer Erkrankungen schützen. Aus den oben genannten Untersuchungen lässt sich allerdings nicht ableiten, ob die gestörte Immunantwort im Falle einer RSV-Infektion aufgrund eines angeborenen Defektes (mangelnde IFN-gamma Bildung, Dysfunktion der regulatorischen T-Zellen) resultiert, oder ob das RS-Virus selbst auf bestimmte Weise die Immunantwort verändern kann. Ein weiterer möglicher Weg für die Induktion einer Th2-Antwort durch RSV wurde bereits in der Einleitung beschrieben. Unter Berücksichtigung dieser Gesichtspunkte scheint der erhöhte GesamtIgE-Wert der Fallgruppe ein Hinweis dafür zu sein, dass bei schweren RSVInfektionen eine Th2-Antwort dominiert. Diese erstreckt sich aufgrund des zeitlich begrenzten Rahmens zunächst auf Nahrungsmittelallergene. Die Frage nach einer erhöhten Inzidenz von Asthmaerkrankungen infolge 55 schwerer RSV-Infektionen lässt sich aufgrund der vorliegenden Daten nicht beantworten. Direkte Zusammenhänge zwischen einem erhöhten Gesamt-IgE und der Entwicklung eines Asthma bronchiale im späteren Kindesalter konnten auch in anderen Studien bisher nicht bewiesen werden (Sigurs et al., 1995, Cassimos et al., 2008). Es zeigte sich aber auch, dass Kinder mit einer schweren RSV-Bronchiolitis in der Säuglingszeit ein erhöhtes Risiko haben, später in der Schulzeit ein Asthma bronchiale zu entwickeln, vor allem wenn sie eine Sensibilisierung gegen mindestens ein Inhalationsallergen haben (Cassimos et al., 2008). Postuliert man, wie von Nickel und Mitarbeitern vermutet, eine Assoziation einer Sensibilisierung gegen Nahrungsmittelallergene im Alter von 12 Monaten mit einer Sensibilisierung gegenüber Inhalationsallergenen im Alter von drei Jahren, so könnte man aus den Ergebnissen dieser Arbeit einen möglichen Zusammenhang zwischen schweren RSV-Infektionen und später erhöhtem Asthmarisiko folgern. Dieses wäre nur durch konsequente weitere Kontrollen im späteren Lebensalter zu beweisen. Auch wäre eine genauere Untersuchung des Zytokinprofils während der RSV-Infektion im Gruppenvergleich interessant, aber gerade bei subklinisch verlaufenden Infektionen schwer durchführbar. 4.1.3 Eine schwere RSV-Infektion als spezifischer Risikofaktor für Giemen im Alter von 12 Monaten Betrachtet man das vermehrte Giemen in beiden Gruppen, so stellt sich eine schwere RSV-Infektion als spezifischer Risikofaktor für Giemen und wiederholtes Giemen im Alter von 12 Monaten heraus. Unter klinischen Gesichtspunkten ist es nicht weiter überraschend, dass Säuglinge nach einer schweren RSV-Infektion im weiteren Verlauf ihrer Entwicklung giemen. Das sogenannte postbronchiolitische Giemen ist inzwischen ein eingeführter Begriff im medizinischen Alltag. Verschiedene 56 Follow-up-Studien haben ein vermehrtes Giemen nach RSV-Infektion im Alter von bis zu 5 Jahren festgestellt (Sigurs et al., 2000, Murray et al., 1992). Ein kausaler Zusammenhang zum Auftreten späterer atopischer Erkrankungen wird weiterhin kontrovers diskutiert, konnte bisher allerdings nicht bewiesen werden (Stein et al., 1999). In einem Vergleich von verschiedenen Follow-up-Studien nach RSV-Infektion zeigte sich signifikant häufiger ein anhaltendes Giemen bis zum fünften Lebensjahr, in späteren Jahren verlor sich dieser Unterschied (Kneyber et al., 2000). Tritt eine chronische allergische Atemwegsentzündung in den ersten drei Lebensjahren auf, so besteht eine Korrelation zu späterem Asthma bronchiale (Illi et al., 2006). Auch andere Untersuchungen zeigten ein vermehrtes Giemen und eine Atopie im ersten Lebensjahr als Risikofaktor für ein Asthma bronchiale im Alter von 6 Jahren (Oddy et al., 2002). Es besteht auch die Möglichkeit einer Koinzidenz von schweren RSV-Erkrankungen und persistierendem Giemen, beispielsweise aufgrund bestimmter genetischer Prädispositionen (Openshaw, 2005). Die Ergebnisse dieser Arbeit zeigen, dass anhaltendes Giemen nach einer schweren RSV-Infektion gehäuft zu beobachten ist. Möglicherweise ist dies ein Risikofaktor für eine spätere Atopieentwicklung, gerade im Zusammenhang mit einer allergischen Sensibilisierung gegenüber Nahrungsmitteln im Alter von 12 Monaten. Dies kann nur durch weitere Untersuchungen eruiert werden. Interessant ist die Frage, auf welche Weise das Giemen zustande kommt, da das postbronchiolitische Giemen unabhängig vom Schweregrad der Infektionsausprägung auftritt. Zur Pathogenese des postbronchiolitischen Giemens gibt es verschiedene Thesen, die im folgenden in Bezug zu den Ergebnissen der vorliegenden Arbeit diskutiert werden. Zunächst werden in verschiedenen Arbeiten anatomische Veränderungen diskutiert, welche zu einer erhöhten Anfälligkeit gegenüber dem RS-Virus führen, ebenso wie erblich bedingte Fehler in der Immunabwehr. Umgekehrt werden Lungengewebsveränderungen infolge der RSV-Infektion postuliert. Eine weitere Möglichkeit besteht in der möglicherweise durch RSV veränderten Immunantwort, welche dauerhaft verändert zu einer anhaltenden bronchialen Hyperreagibilität führt. 57 Anatomische Veränderungen Warum es gerade bei RSV-Infektionen zu unterschiedlichen Krankheitsverläufen auch in der postinfektiösen Phase kommt, lässt sich nicht pauschal beantworten. Angeborene anatomische Unterschiede prägen die Suscepitibilität. Kinder mit einer BPD oder angeborenen Herzfehlern beispielsweise sind anfälliger für schwere respiratorische Infektionen (Black, 2003). Auch Kinder mit einer Laryngotracheomalazie oder zystischen Fibrose neigen zu einem schweren Krankheitsverlauf (Arnold, 1999). Diese Faktoren konnten in dieser Arbeit durch das Matching zu Beginn ausgeschlossen werden. Unterschiede in der Größe der Atemwege oder die Lungenfunktion bei den Teilnehmern beider Gruppen wurden nicht gemessen, diese dürften aber bei sonst gesunden Kindern der Normalverteilung der Bevölkerung entsprechen. Aufgrund des Studiendesigns bleibt häufig die Frage unbeantwortet, ob es schon vor Infektion mit RSV eine atopische Disposition bei den Probanden gegeben hat, die später eine bronchiale Hyperreagibilität zeigen (Wennergren and Kristjansson, 2001). Bei einer akuten Infektion können große Anteile des respiratorischen Epithels durch RSV zerstört werden. Im Rahmen der Entzündungsreaktion werden bestimmte Zellen wie neutrophile Granulozyten, Eosinophile und aktivierte TZellen rekrutiert und aktiviert. Gerade diese Zellarten spielen auch bei der Genese von allergischen Erkrankungen eine wichtige Rolle (Gern and Busse, 2000), und konnten auch in bronchialen Lavageproben bei RSV-infizierten Kindern nachgewiesen werden (Everard et al., 1994) . Es gibt Hinweise darauf, dass das Lungengewebe gerade durch einen chronischen Entzündungsprozess und mögliche Viruspersistenz in der Entwicklung und weiteren Ausreifung gestört wird (Riedel, 1997). Dabei sind die Viren nicht mehr auf den oberflächlichen Lungenstrukturen, sondern in tieferen Gewebsschichten nachweisbar (Openshaw, 2001). Ebenso kommt es im Zusammenhang mit einer erhöhten Gefäßpermeabilität zu einer inflammatorischen Schwellung des interstitiellen Lungengewebes und zu einer gestörten Surfactantfunktion (Black, 2003). Zusätzlich wirken einige von den beteiligten Zellen ausgeschütteten Zytokine, insbesondere Leukotriene, bronchokonstriktorisch. Diese Mechanismen bieten mögliche Erklärungsansätze für die Pathogenese des postbronchiolitischen Giemens, 58 allerdings ist es aufgrund der Fülle der Möglichkeiten und deren Zusammenhängen schwierig, eine Kausalkette zu bilden. In dieser Arbeit wurde zunächst nur der Zeitraum von 12 Monaten betrachtet, wobei aufgrund der Definition der Fallgruppe (krankenhauspflichtige, nachgewiesene RSV-Infektion im Alter bis zu 12 Monaten) keine Schlussfolgerung möglich ist, ob das Giemen im Alter von einem Jahr noch in die Phase des postbronchiolitischen Giemens fällt, oder als reaktive Atemwegserkrankung den möglichen Beginn einer atopischen Genese anzeigt. In diesem Sinne sind weitere Follow-up-Untersuchungen beider Gruppen wünschenswert. Th2-Modellierung / Immunmodulation Eine Möglichkeit, eine anhaltende bronchiale Hyperreaktivität zu entwickeln, besteht in der Induktion eines allergischen Geschehens. Wie lange diese Reaktionsweise anhält und ob sie zu Spätfolgen wie einem allergischen Asthma bronchiale führt, damit haben sich mehrere Follow-up-Studien auseinandergesetzt und verschiedene Gesichtspunkte dieses Geschehens beleuchtet. Dabei korreliert der Nachweis von RSV-spezifischem IgE kurz nach der Infektion mit vermehrtem Giemen im Alter von 3 Jahren. Die virusspezifische IgE-Produktion gibt einen Hinweis auf die immunstimulierende Wirkung der RSV-Infektion hinsichtlich einer Th-2-gesteuerten Immunantwort, welche auch nach einer Parainfluenzainfektion auftritt. Die Ergebnisse stützen die These, dass es bei den infizierten Kindern bestimmte Vorraussetzungen gibt, die für die Empfänglichkeit von pulmonalen Virusinfektionen prädisponieren (Welliver, 2002). Auch Martinez konnte bei Kindern, die im Alter von 6 Jahren persistierendes Giemen aufwiesen, eine Eosinophilie sowie eine transiente Gesamt-IgEErhöhung im Alter von 9 Monaten feststellen (Martinez et al., 1995, 1999). Eine longitudinale Kohortenstudie von Stein zeigte zunächst ebenfalls ein erhöhtes Risiko von häufigem Giemen im Alter von sechs Jahren, allerdings nahm das Risiko von vermehrtem Giemen mit zunehmendem Alter ab und im 59 Alter von 13 Jahren war kein Unterschied zwischen der RSV- und der Kontrollgruppe mehr nachweisbar (Stein et al, 1999). Betrachtet man die Ergebnisse dieser Arbeit, so lässt sich aufgrund des relativ kurzen Untersuchungszeitraumes von einem Jahr keine Aussage über eine mögliche Langzeitfolge von schweren RSV-Erkrankungen machen. 4.2 Hereditäre Einflüsse auf die Allergieentstehung 4.2.1 Bedeutung einer positiven Familienanamnese Das Atopierisiko bei Kindern, genauer gesagt die Lebenszeitprävalenz, liegt in Deutschland bei 22,9% (Schlaud et al, 2007). Weiterhin ist bekannt, dass das Risiko, an einer Atopie zu erkranken, steigt, wenn ein oder gar beide Elternteile ebenfalls Allergiker sind. Ist ein Elternteil Allergiker, so liegt das Risiko für eine Allergieentwicklung beim Kind bei 20%, sind beide Eltern betroffen, ist das Risiko 60% (Björksten, 1994). Dabei wird einerseits die Prädisposition zur Entwicklung atopischer Erkrankungen vererbt, andererseits aber auch die Beteiligung bestimmter Organe sowie der Grad der Ausprägung. Kopplungsanalysen haben verschiedene Genloci nachgewiesen, die mit der Vererbung von Atopien einhergehen (Wahn, 2002). Die komplexe Interaktion mit verschiedenen Umweltfaktoren sowie eine genetische Instabilität und die individuelle Bereitschaft zur Ausprägung eines bestimmten Phänotyps sind dabei von Bedeutung. In der vorliegenden Arbeit wurde die positive Atopieanamnese beider Elternteile als Risikofaktor einer möglichen allergischen Sensibilisierung nachgewiesen, und zwar gruppenunspezifisch. Bei den 252 Eltern in dieser Studiengruppe lag der Anteil der Atopiker (n=81) mit 32% leicht über der Norm, es gab keinen wesentlichen Unterschied zwischen der Fallgruppe (27%) und der Kontrollgruppe (34%). 60 Die Bedeutung der positiven Familienanamnese, vor allem mütterlicherseits, als Risikofaktor einer Atopieentwicklung ist unumstritten und schon in zahlreichen vorangegangenen Studien mit höherer Fallzahl nachgewiesen worden. Sie wirkt sich aber in ihrer Bedeutung für späteres Giemen und eine Atopieentwicklung erst im weiteren Verlauf des Jugend- und jungen Erwachsenenalters aus (Mandhane et al., 2005). 4.2.2 Geschlecht Bei der Auswertung der Daten stellte sich das männliche Geschlecht als Risikofaktor einer allergischen Sensibilisierung im Alter von einem Jahr heraus, ebenso als Risikofaktor für Giemen im Alter von 12 Monaten. Im Rahmen von Kohortenstudien fiel auf, dass in der Kindheit deutlich mehr Jungen als Mädchen von anhaltendem Giemen betroffen sind, nach der Pubertät kehrt sich das Verhältnis um (Melen et al., 2004, Mandhane et al., 2005, Wright et al., 2006, Almqvist et al., 2008). Einen möglichen Erklärungsansatz dafür mag eine unterschiedliche Entwicklung der Atemwege sein. Jungen haben schon im Säuglingsalter bei vergleichbaren Lungenvolumina eine geringere exspiratorische Flussrate als Mädchen (Young et al., 2000). Dies unterstützt die These, dass weibliche Säuglinge möglicherweise größere Luftwege im Verhältnis zur absoluten Lungengröße haben als männliche. Dieser strukturelle Unterschied bedingt auch funktionelle Einbußen, die in einer erhöhten Infektanfälligkeit im ersten Lebensjahr resultieren (Young et al., 2000). Weitere Untersuchungen zeigen einen geschlechtsspezifischen Unterschied in der Immunantwort. Jungen haben bei anhaltendem Giemen einen erhöhten IFN-gamma Spiegel im Alter von einem und drei Jahren, sowie eine erhöhte Sensibilisierungsrate, einen erhöhten Gesamt-IgE-Spiegel und eine vermehrte Eosinophilie im Vergleich zu Mädchen (Uekert et al., 2006). Auch die Ergebnisse dieser Arbeit belegen eine erhöhte Häufigkeit für Giemen im Alter von 12 Monaten, welche möglicherweise infektgetriggert ist. Die Tatsache, dass das männliche Geschlecht einen Risikofaktor für eine 61 allergische Sensibilisierung im Alter von einem Jahr darstellt, legt die Vermutung nahe, dass doch ein Zusammenhang zwischen vermehrten pulmonalen Infekten und einer allergischen Sensibilisierung besteht. Die Ergebnisse unterstützen damit die Hauptthese dieser Arbeit. 4.3 Allgemeine Risikofaktoren, insbesondere umweltbedingte Einflüsse, auf die Entstehung allergischer und infektiologischer Erkrankungen 4.3.1 Geschwisteranzahl Geschwister als Infektionsquelle Die Ergebnisse zeigen, dass die Kinder mit einer schweren RSV-Bronchiolitis deutlich mehr Geschwister haben. Den Kindern der RSV-Gruppe mit 1,33 Geschwistern steht die Kontrollgruppe mit 0,51 Geschwistern gegenüber. Unter infektiologischen Gesichtspunkten nehmen die Geschwisterkinder in einer Familie eine Infektionskrankheiten wichtige ein, Rolle bezüglich besonders der wenn Übertragung diese von in Gemeinschaftseinrichtungen wie Kindergarten oder Schule häufigen Kontakt zu anderen Kindern haben. Schon früh wurde vermutet, dass das Vorhandensein von älteren Geschwistern dazu beiträgt, die Wahrscheinlichkeit von RSV-Infektionen bei Säuglingen zu erhöhen, indem sie das Virus in die Familie einbringen (Hall et al., 1976). Dies wurde in der Tucson Children’s Respiratory Study bestätigt (Taussig et al., 2003). Die infektiologische Bedeutung der Geschwister scheint sich in der vorliegenden Studie auch bei relativ geringer Fallzahl zu bestätigen. Allerdings gab es kein Matching der beiden Gruppen bezüglich der Geschwisteranzahl, so dass man keine kausale Beziehung zwischen der Geschwisteranzahl und dem Auftreten einer RSV-Bronchiolitis aus den Ergebnissen direkt ableiten kann. 62 Die Ergebnisse schließen sich denen der oben genannten Studien unter dem Gesichtspunkt der Bedeutung von Geschwistern an. Sie sind diesbezüglich als Ergänzung der im Mittelpunkt stehenden Ergebnisse zu sehen, welche die RSV-Infektion in Bezug zum Auftreten von Giemen im ersten Lebensjahr stellt. 4.3.2 Geschwister als mögliche Risikofaktoren für Giemen und wiederholtes Giemen im Alter von einem Jahr, aber kein Risikofaktor für eine allergische Sensibilisierung im Alter von 12 Monaten Die Auswertung der Ergebnisse zeigte, dass das Vorhandensein von mehr als einem Geschwisterkind einen möglichen Risikofaktor für das Auftreten von Giemen und wiederholtem Giemen darstellt, nicht aber für eine allergische Sensibilisierung im Alter von 12 Monaten. Bei der genaueren Betrachtung mittels Multivarianzanalyse, die dazu benutzt wurde, die möglichen Risikofaktoren unabhängig voneinander in Bezug auf jeweils ein Merkmal beurteilen zu können, in diesem Fall Giemen, wiederholtes Giemen und die allergische Sensibilisierung, zeigte sich das Vorhandensein von mehr als einem Geschwisterkind als nicht signifikant für alle drei Merkmale. Die Vorstellung von älteren Geschwisterkindern als Infektionsüberträgern mit damit verbundenem häufigerem Giemen der Probanden im Rahmen von Infekten wurde durch diese Ergebnisse bestätigt. Auch andere Untersuchungen legen die Vermutung nahe, dass jüngere Kinder, bedingt durch die Infekttransduktion der älteren Geschwister, vermehrt zu Giemen in der Kindheit neigen, aber nicht zu dauerhaftem oder später im Leben einsetzendem Giemen (Teil der ISAAC-Studie in Italien, Rusconi et al., 1999, Sherriff et al., 2001). Untersuchungen von Kindern, die Tageskrippen in der ehemaligen DDR besuchten (Krämer et al., 1998), und auch Tagesbetreuungseinrichtungen in den USA (Ball et al., 2000), bestätigen, dass es bei diesen Patienten vermehrt zu Giemen im ersten Lebensjahr kommt, vermutlich im Rahmen von Infekten. Ob diese frühen 63 Erkrankungen möglicherweise einen Schutz vor späterer Atopieneigung darstellen, ist noch ungeklärt. Auch zeigte sich das Vorhandensein von Geschwistern nicht als Risikofaktor für eine allergische Sensibilisierung. Dieses Ergebnis stützt die These, dass häufige Infektionen im Säuglingsalter eine protektive Wirkung bezüglich des Auftretens einer Atopie haben. Im Rahmen der Diskussion um die Zunahme allergischer Erkrankungen wurde ein Zusammenhang zwischen der Anzahl der Geschwister und dem späteren Auftreten von allergischen Erkrankungen vermutet. Dabei fiel auf, dass eine umgekehrte Relation von älteren Geschwisterkindern zu der Prävalenz von allergischen Erkrankungen bestand, d.h. je mehr ältere Geschwister, desto weniger wahrscheinlich ist das Auftreten einer atopischen Erkrankung beim jüngeren Geschwisterkind (Karmaus and Botezan, 2002, Eder et al., 2006), ein Faktor, der für die in der Einleitung erwähnte HygieneHypothese spricht. Eine andere Arbeit bestätigte, dass häufige virale obere Luftwegsinfekte das Risiko verringern, im Schulalter an Asthma zu erkranken (Illi et al., 2001). Viel wichtiger hinsichtlich der Atopieentwicklung und ausprägung wurde eine positive Familienanamnese bewertet (Ball et al., 2000). Zusammenfassend kann man sagen, dass ältere Geschwisterkinder das Risiko an Infektionen, insbesondere RSV-Bronchiolitis, zu erkranken, erhöhen. Nicht herleiten kann man aus den vorliegenden Ergebnissen, dass ein Zusammenhang zwischen Giemen, wiederholtem Giemen und späterer allergischer Sensibilisierung existiert, weil diese als von einander unabhängige Merkmale in Bezug zu den vorher genannten Risikofaktoren gestellt wurden. Ein Zusammenhang zwischen allergischer Sensibilisierung in Abhängigkeit von der Geschwisteranzahl besteht ebenfalls nicht. 64 4.3.3 Rauchen Im Vergleich beider Gruppen stellte sich heraus, dass die Kinder mit einer schweren Bronchiolitis im Vergleich zur Kontrollgruppe vermehrt rauchende Eltern hatten. In der weiteren Betrachtung stellte sich das Rauchen vor allem der Mutter als Risikofaktor für Giemen, wiederholtes Giemen und als Risikofaktor einer möglichen allergischen Sensibilisierung heraus. Rauchen und auch Passivrauchen ist bekanntermaßen gesundheitsschädlich. Die Zilien des respiratorischen Epithels werden in ihrer Funktion gestört, was eine erhöhte Anfälligkeit für Infektionen zur Folge hat. Ebenso führt aktives wie passives Rauchen zu einer bronchialen Hyperreagibilität (Jensen et al., 2000, Bacharier et al., 2008). Zahlreiche Untersuchungen belegen einen Zusammenhang zwischen Rauchexposition, vermehrtem Giemen sowie einer Atopieneigung. Es wurde ein Zusammenhang von einer postnatal erniedrigten Lungenfunktion mit intrauteriner Tabakexposition festgestellt (Tager et al., 1993, Lodrup and Carlsen, 2001, Rusconi et al, 2007). Die Ergebnisse legten die Vermutung nahe, dass intrauterine Rauchexposition zu einer gestörten Morphologie und Funktion des Respirationstraktes führt. Auch Young konnte in einer prospektiven Studie beweisen, dass die Lungenfunktion bei pränataler Rauchexposition vermindert ist und ein wichtiger Risikofaktor für Giemen in der frühen Kindheit ist (Young et al., 2000). Andere Studien konnten ebenfalls einen Zusammenhang zwischen reduzierter Lungenfunktion und Rauchexposition nachvollziehen (Tepper et al., 2005). Ob dadurch aber die Wahrscheinlichkeit steigt, an Asthma zu erkranken, muss noch weiter erforscht werden. Neuere Studien zeigen einen Zusammenhang zwischen der erhöhten Rauchexposition nach RSV-Bronchiolitis und Asthma bronchiale im Schulalter (Cassimos et al., 2008). Eine positive Familienanamnese ist ebenfalls von Bedeutung. Bei genetischer Prädisposition korreliert Passivrauchen mit einer erhöhten Asthmaneigung und vermehrtem Giemen (Rusconi et al., 1999). Neuere Untersuchungen legen die Vermutung nahe, dass bestimmte Gene durch 65 den Tabakkonsum „angeschaltet“ werden, die die Ausprägung eines atopischen Phänotyps begünstigen (Meyers et al., 2005). Aus der vorliegenden Arbeit kann man zumindest das elterliche Rauchen, vor allem aber den Nikotinkonsum in der Schwangerschaft, als Risikofaktor für ein Giemen in der frühen Kindheit betonen. Ob dieses Giemen aufgrund bronchialer Hyperreagibilität im Sinne eines kindlichen Asthmas zu werten ist oder eher durch eine erhöhte Infektneigung bei Ziliendysfunktion, lässt sich durch diese Ergebnisse und auch die anderer Studien nicht herleiten. Dazu bedarf es weiterer Forschung. Einen Zusammenhang zwischen dem Rauchen der Eltern mit einer Neigung zu einer schweren RSV-Infektion kann nicht aus der vorliegenden Arbeit hergestellt werden, die beiden Gruppen wurden bezüglich des Rauchens nicht gematcht. 66 5 Zusammenfassung Die Pathogenese allergischer Krankheitsbilder ist ein komplexes Geschehen, welches sowohl durch endogene als auch durch exogene Faktoren beeinflusst wird. Es wird diskutiert, inwiefern bestimmte Infektionen, insbesondere eine RSV-Infektion, auf dieses Geschehen Einfluss nehmen. Dabei gibt es Hinweise, dass das RS-Virus die Regulation gerade der T-ZellAntwort erheblich beeinflusst. Die in in vitro Experimenten hervorgerufene überwiegende Th-2-Antwort des Immunsystems ist dabei das Ergebnis entweder einer Unterdrückung der Th-1-Antwort oder einer Funktionsstörung der regulatorischen T-Zellen. Ob dies nur Patienten mit einer eventuell angeborenen Störung der T-Zell-Antwort betrifft oder diese in bestimmten Fällen durch das RS-Virus selbst verändert wird, bleibt unklar. Ebenso lässt sich die klinisch unterschiedliche Ausprägung der RSV-Infektion bis jetzt nicht aufgrund bestimmter prädiktiver Merkmale vorhersagen. In der vorliegenden Arbeit wurde der Frage nachgegangen, ob sich in vivo Hinweise für eine immunmodulatorische Wirkung des RS-Virus zeigen. Anhand einer Fall-Kontroll-Studie wurde geprüft, ob eine schwere RSVInfektion einen Risikofaktor für anhaltendes Giemen oder eine allergische Sensibilisierung darstellt. Der Beobachtungszeitraum des ersten Lebensjahres ist dabei von besonderem Interesse, da bei Kontakt zu verschiedenen Antigenen entweder eine immunologische Toleranz oder aber eine allergische Sensibilisierung ausgebildet wird. Mögliche Auswirkungen des RS-Virus auf die allergische Pathogenese sollten zeitnah erfasst werden. Es wurden 42 Säuglinge, die an einer schweren RSV-Bronchiolitis erkrankt waren, mit 84 gesunden Säuglingen einer Kontrollgruppe über einen Zeitraum von einem Jahr miteinander verglichen. Die Gruppen wurden bezüglich des Geburtszeitraums und des Geschlechts gematcht. Anhand einer klinischen Untersuchung im Alter von 12 Monaten sowie von Fragebögen und immunologischen Laborergebnissen (Gesamt-IgE, spezifisches IgE für Inhalations- und Nahrungsmittelallergene, RSV- 67 Antikörper) wurde insbesondere das Atopierisiko und die Atopieentwicklung beider Gruppen verglichen. Außerdem wurden Umwelteinflüsse untersucht, welche die Atopieentstehung begünstigen. Im Beobachtungszeitraum von einem Jahr, den diese Arbeit umfasst, konnte ein erhöhtes Risiko von Giemen und wiederholtem Giemen nach schwerer RSV-Infektion im Alter von 12 Monaten beobachtet werden. Die Kinder der Fallgruppe zeigten zu diesem Zeitpunkt signifikant häufiger wiederholtes Giemen. Bei der Bestimmung des Gesamt-IgE-Wertes wiesen die Kinder der Fallgruppe ebenfalls häufiger einen erhöhten Wert im Alter von einem Jahr auf, was das Argument der Th-2-gewichteten Immunantwort nach RSVInfektion bestärkt. Bei der weiteren Differenzierung zeigte sich ein erhöhtes Risiko einer allergischen Sensibilisierung gegenüber Nahrungsmitteln in diesem Alter. Im Rahmen dieser Arbeit stellten sich eine Tabakrauchexposition und die Anwesenheit von älteren Geschwisterkindern als Risikofaktoren für die Entwicklung einer schweren Bronchiolitis heraus. Die Probanden der Fallgruppe hatten vermehrt rauchende Eltern. Lenkt man das Augenmerk auf die Risikofaktoren für Giemen, wiederholtes Giemen und eine allergische Sensibilisierung, so ist die Tabakrauchexposition neben einer schweren RSV-Bronchiolitis ein wichtiger Risikofaktor. Insbesondere die intrauterine Tabakrauchexposition stellte sich als Risikofaktor für Giemen im Alter von 12 Monaten heraus. Die genauen immunologischen Mechanismen, insbesondere die Toleranzentwicklung gegenüber Umweltantigenen und die verschiedenen zellulären und molekularen Möglichkeiten der Infektionsbewältigung, bleiben weiterhin Gegenstand aktueller Studien. Betrachtet man den langandauernden Effekt einer schweren RSVBronchiolitis auf die Entwicklung einer allergischen Sensibilisierung und deren möglicher klinischer Ausprägung in Form einer Atopie, so sind weitere Follow-up-Untersuchungen des Patienten- und Kontrollkollektivs notwendig. 68 6 Literaturverzeichnis Aberle, J. H., Aberle, S.W., Dworzak, M.N., Mandl, C.W., Rebhandl, W., Vollnhofer, G., Kundi, M., Popow-Kraupp, T. (1999). Reduced interferon-gamma Expression in Peripheral Blood Mononuclear Cells of infants with severe RSV-Disease. Am J Respir Crit Care Med 160, 1263-1268 Allander, T., Tammi, M.T., Eriksson, M., Bjerkner, A., Tiveljung-Lindell, A., Andersson, B. (2005). From the cover: Cloning of a human parvovirus by molecular screening of respiratory tract samples. PNAS 102, 12891-12896 Almqvist, C., Worm, M., Leynaert, B., for the working group of GA2LEN WP 2.5 ‘Gender’ (2008). Impact of gender on asthma in childhood and adolescence: a GA2LEN review Allergy 63, 47–57 Arnold, R., Konig, B., Werchau, H., Konig, W. (2004). Respiratory syncytial virus deficient in soluble G protein induced an increased proinflammatory response in human lung epithelial cells. Virology 330, 384-397 Bach, J.F. (2002). The effect of infections on susceptibility to autoimmune and allergic diseases. NEJM 347, 911-920 69 Bacharier, L.B., Boner, A., Carlsen, K.-H., Eigenmann, P.A., Frischer, T., Götz, M., Helms, P.J., Hunt, J., Liu, A., Papadopoulos, N., Platts-Mills, T., Pohunek, P., Simons, F.E.R., Valovirta, E., Wahn, U., Wildhaber, J, The European Pediatric Asthma Group (2008). Diagnosis and treatment of asthma in childhood: a PRACTALL consensus report. Allergy 63, 5-34 Ball, T.M., Castro-Rodriguez, J.A., Griffith, K.A., Holberg, C.J., Martinez, F.D., Wright, A.L. (2000). Siblings, day-care attendance and the risk of asthma and wheezing during childhood. NEJM 343, 538-543 Bartz, H., Buning-Pfaue, F., Turkel, O., Schauer, U. (2002). Respiratory syncytial virus induces prostaglandin E2, Il-10 and IL-11 generation in antigen presenting cells. Clin Exp Immunol 129, 438-445 Bartz, H., Turkel, O., Hoffjan, S., Rothoeft, T., Gonschorek, A., Schauer, U. (2003). Respiratory syncytial virus decreases the capacity of myeloid dendritic cells to induce interferon-gamma in naive T cells. Immunology 109, 49-57 Becker, Y. (2006). Respiratory syncytial virus (RSV) evades the human adaptive immune system by skewing the Th1/Th2 cytokine balance toward increased levels of Th2 cytokines and IgE, markers of allergy – a review. Virus Genes 33, 235-252 70 Bem, R.A., Bos, A.P., Bots, M., Wolbink, A.M., van Ham, S.M., Medema, J.P., Lutter, R., van Woensel, J.B. (2008). Activation of the granzyme pathway in children with severe respiratory syncytial virus infection. Pediatr Res 2008 Feb 27 (Epub ahead of print) Björksten, B. (1994). Risk factors in early childhood for the development of atopic diseases. Allergy 49, 400-407 Black, C.P. (2003). Systematic review of the biology and medical management of respiratory syncytial virus infection. Respiratory Care 48, 209-233 Brandenburg, A.H., van Beek, R., Moll, H.A., Osterhaus, A.D.M.E., Claas, E.C.J.(2000). G Protein variation in respiratory syncytial virus group A does not correlate with clinical severity. J Clin Microbiol 38, 3849-3852 Canducci, F., Debiaggi, M., Sampaolo, M., Marinozzi, M.C., Berré, S., Terulla, C., Gargantini, G., Cambieri, P., Romero, E., Clementi, M. (2008). Two-year prospective study of single infections and co-infections by respiratory syncytial virus and viruses identified recently in infants with acute respiratory disease. J Med Virol 80, 716-723 Cassimos, D.C., Anthracopoulos, Tsalkidis, M., A., Tripsianis, Ktenidou-Kartali, S., G.A., Aivazis, Stogiannidou, A., V., S., Gardikis, Chatzimichael, A. (2008). Asthma, lung function and sensitisation in school children with a history of bronchiolitis. Pediatrics International 50, 51-56 71 Chanock, R., Roizman, B., Myers, R. (1957). Recovery from infants with respiratory illness of a virus related to chimpanzee coryza agent. Am J Hyg 66, 281-290 Cookson, W., Moffat, M. (2002). Die immunologischen und genetischen Mechanismen des Asthma bronchiale. Annales Nestlé 60, 66-76 Deffrasnes, C., Hamelin, M.-E., Boivin, G. (2007). Human metapneumovirus. Semin Respir Crit Care Med 28, 213-221 Döring, G., Grote, V., Nicolai, T., Liese, J. (2005). RSV-Bronchiolitis. Monatsschrift Kinderheilkunde 153, 228-235 Domachowske, J.B., Bonville, C.A., Dyer, K.D., Rosenberg, H.F. (1998). Evolution of antiviral activity in the ribonuclease A gene superfamily: evidence for a specific interaction between eosinophil-derived neurotoxin (EDN/RNase 2) and respiratory syncytial virus. Nucleic Acids Research 26, 5327-5332 Eder, W., Ege, M.J., von Mutius, E. (2006). The asthma epidemic. NEJM 355, 2226-2235 Ehlenfield, D.R., Cameron, K., Welliver, R.C. (2000). Eosinophilia at the time of respiratory syncytial virus Bronchiolitis predicts childhood reactive airway disease. Pediatrics 105, 79-83 72 Elliot, A.J., Fleming, D.M. (2008). Influenza and respiratory syncytial virus in the elderly. Expert Rev Vaccines 7, 249-258 Everard, M.L., Swarbrick, A., Wrightham, M., McIntyre, J., Dunkley, C., James, P.D., Sewell, H.F., Milner, A.D. (1994). Analysis of cells obtained by bronchial lavage of infants with respiratory syncytial virus infection. Archives of Disease in Childhood 71, 428-432 Everard, M.L. (1999). What link between early respiratory viral infections and atopic asthma? Lancet 354, 527-528 Flores, G, Horwitz, R.I. (1997). Efficacy of ß2-Agonists in bronchiolitis: a reappraisal and meta-analysis. Pediatrics 100, 233-239 Forster, J. (2002). Intubationsbedürftige RSV-Erkrankungen. (Zugriff vom 5.3.2008) http://www.esped.uni-duesseldorf.de/ Forster, J., Berner, R., Freihorst, J., Kreth, H.W., Liese, J., Weigl, J., Müller, W., Scholz, H. (2003). Respiratory Syncytial Virus-Infektionen. in Deutsche Gesellschaft für pädiatrische Infektiologie (Hrsg.). DGPIHandbuch. Futuramed Verlag, München, 599-603 Garrison, M.M., Christakis, D.A., Harvey, E., Cummings, P., Davis, R.L. (2000). Systemic corticosteroids in infant bronchiolitis: a Meta-analysis. Pediatrics 105, e44 73 Gern, J.E., Busse, W.W. (2000). The role of viral infections in the natural history of asthma. J Allergy Clin Immunol 106, 201-212 Hall, C.B., Geiman, J.M., Biggar, R., Kotok, D.I., Hogan, P.M., Douglas, R.G. (1976). Respiratory syncytial virus infections within families. NEJM 294, 414-419 Hall, C.B. (2001). Respiratory syncytial virus and parainfluenza virus. NEJM 344, 1917-1928 Hallman, M., Haatja, R. (2006). Surfactant protein polymorphisms and neonatal lung disease. Seminars in Perinatology 30, 350-316 Hanifin, J.M. (1984). Basic and clinical aspects of atopic dermatitis. Annals of Allergy 52, 386-393 Hansbro, N.G., Horvat, J.C., Wark, P.A., Hansbro, P.M. (2008). Understanding the mechanisms of viral induced asthma: New therapeutic directions. Pharmacol Ther 117, 313-353 Hansen, G. (2005). Der Traum der Allergologen – Toleranzinduktion. Consilium infectiorum 3, 26-30 Hattevig, G. (2005). Allergic diseases and the environment. Acta Paediatrica 94, 1519-1520 74 Hoebee, B., Rietveld, E., Bont, L., Oosten, M., Hodemaekers, H.M., Nagelkerke, N.J., Neijens, H.J., Kimpen, J.L., Kimman, T.G. (2003). Association of severe respiratory syncytial virus bronchiolitis with interleukin4 and interleukin-4 receptor alpha polymorphisms. J Infect Dis 187, 2-11 Holländer, G.A., Barthlott, T., Keller, M.P., Krenger, W., Piali, L. (2005). Natürliche Killerzellen. In Wahn, U., Seger, R., Wahn, V., Holländer, G.A. (Hrsg.) Pädiatrische Allergologie und Immunologie Urban und Fischer Verlag, München Jena, 29-32 Holt, P.G., Sly, P.D. (2002). Interactions between RSV infection, asthma, and atopy: unraveling the complexities. J Exp Med 196, 1271-1275 Hussel, T., Openshaw, P.J.M. (1998). Intercellular IFN-gamma expression in natural killer cells precedes lung CD8+ T cell recruitment during RSV infection. J Gen Virology 79, 2593-2601 Illi, S., von Mutius, E., Lau, S., Bergmann, R., Niggemann, B., Sommerfeld, C., Wahn, U. and the MAS Group (2001). Early childhood infectious diseases and the development of asthma up to school age: a birth cohort study. BMJ 322, 390-395 Illi, S., von Mutius, E., Lau, S., Niggemann, B., Grüber, C., Wahn, U. and on behalf of the Multicenter Allergy Study (MAS) group (2006). Perennial allergen sensitisation early in life and chronic asthma in children: a birth cohort study. Lancet 368, 763-770 75 ISAAC (The International Study of Asthma and Allergies in Childhood steering committee) (1998). Worldwide variation in prevalence of symptoms of asthma, allergic rhinoconjunctivitis, and atopic eczema: ISAAC. Lancet 351, 1225-1232 Janeway, C.A., Travers, P., Walport, M., Shlomchik, M. (2002). Immunologie Spektrum Akademischer Verlag Heidelberg Berlin, 239-244 Jensen, E.J., Dahl, R., Steffensen, F. (2000). Bronchial reactivity to cigarette smoke; relation to lung function, respiratory symptoms, serum-immunglobulin E and blood eosinophil and leukocyte counts. Respir Med 94, 119-127 Johnson, T.R., Johnson, J.E., Roberts, S.R., Wertz, G.W., Parker, R.A., Graham, B.S. (1998). Priming with secreted Glycoprotein G of RSV augments IL5 production and tissue eosinophilia after RSV challenge. Journal of Virology 72, 2871-2880 Kabesch, M. (2001). Asthma und Allergie. Genetische Prädisposition und Umweltfaktoren. Monatsschrift Kinderheilkunde 149, 94-105 Karmaus, W., Botezan, C. (2002). Does a higher number of siblings protect against the development of allergy and asthma? A review. J Epidemiol Community Health 56, 209-217 76 Kneyber, M.C.J., Steyerberg, E.W., de Groot, R., Moll, H.A. (2000). Long-term effects of RSV bronchiolitis in infants and young children: a quantitative review. Acta Paediatr 89, 654-660 Krämer, U., Heinrich, J., Wjst, M., Wichmann, H.E. (1999). Age of entry to day nursery and allergy in later childhood. Lancet 353, 450-454 Krämer, U. (2001). Epidemiologie allergischer Erkrankungen bei Kindern. Zeitliche Trends in Deutschland und Diskussion möglicher Ursachen eines Trends. Bundesgesundheitsblatt 7, 633-642 Krusat, T., Werchau, H. (2001). Erregerspektrum und Ausbreitungswege bei der Bronchiolitis. Atemwegs- und Lungenkrankheiten 27, 473-477 Kulig, M., Bergmann, R., Niggemann, B., Burow, G., Wahn, U. and the MAS Study Group (1998). Prediction of sensitization to inhalant allergens in childhood: evaluating family history, atopic dermatitis and sensitization to food allergens. Clinical and Experimental Allergy 28, 1397-1403 Lau, S. (2001). Allergenexposition und Asthmaentstehung. Monatsschrift Kinderheilkunde 149, 106-111 Legg, J.P., Hussain, I.R., Warner, J.A., Johnston, S.L., Warner, J.O. (2002). Type 1 and type 2 cytokine imbalance in acute respiratory syncytial virus infection. Am J Repir Crit Care Med 168, 633-639 77 Little-van den Hurk, S. van Drunen, Mapletoft, J.W., Arsic, N., Kovacs-Nolan, J. (2007). Immunpathology of RSV infection: prosects for developing vaccines without this complication. Reviews in Medical Virology 17, 5-34 Lodrup-Carlsen, K.C., Carlsen, K.H. (2001). Effects of maternal and early tobacco exposure on the development of asthma and airway hyperreactivity. Curr Opin Allergy Clin Immunol 1, 139-143 Macatonia, S.E., Hosken, N.A., Litton, M., Vieira, P., Hsieh, C.-S., Culpepper, J.A., Wysocka, M., Trinchieri, G., Murphy, K.M., O´Garra, A. (1995). Dendritic cells produce IL12 and direct the development of Th1 cells from naive CD4+ T cells. J Immunol 154, 5071-5079 Mallia, P., Johnston, S.L. (2006). How viral infections cause excerbation of airway disease. Chest 130,1203-1210 Mandhane, P.J., Greene, J.M., Cowan, J.O., Taylor, D.R., Sears, M.R. (2005). Sex differences in factors associated with childhood- and adolescent-onset wheeze. Am J Respir Crit Care Med 172, 45-54 Mansbach, J.M., McAdam, A.J., Clark, S., Hain, P.D., Flood, R.G., Acholonu, U., Camargo, C.A. Jr. (2008). Prospective multicenter study of the viral etiology of bronchiolitis in the emergency department. Acad Emerg Med 15, 111-118 78 Martinez, F.D., Wright, A.L., Taussig, L.M., Holberg, C.J., Halonen, M., Morgan, W.J., and the Group Health Medical Associates (1995). Asthma and wheezing in the first six years of life. NEJM 332, 133-138 Martinez, F.D., Stern, D.A., Wright, A.L., Taussig, L.M., Halonen, M. (1998). Differential immune responses to acute lower respiratory illness in early life and subsequent development of persistent wheezing and asthma. J Allergy Clin Immunol 102; 915-920 Martinez, F. (1999). Maturation of immune responses at the beginning of asthma. J Allergy Clin Immunol 103, 355-361 Matthews, S.P., Tregoning, J.S., Coyle, A.J., Hussell, T., Openshaw, P.J.M. (2005). Role of CCL11 in eosinophilic lung disease during respiratory syncytial virus infection. J Virol 79, 2050-2057 Maziak, W., Behrens, T., Brasky, T.M., Duhme, H., Rzehak, P., Weiland, S.K., Keil, U. (2003). Are asthma and allergies in children and adolescents increasing? Results from ISAAC phase I and phase III surveys in Munster, Germany. Allergy 58, 572-579 McConnochie, K.M., Roghmann, K.J. (1984). Bronchiolitis as a possible cause of wheezing in childhood: New evidence. Pediatrics 74,1-10 Melén, E., Kere, J., Pershagen, G., Svartengren, M., Wickman, M. (2004). Influence of male sex and parental allergic disease on childhood wheezing: role of interactions. Clinical & Experimental Allergy 34, 839–844 79 Meyers, D.A., Postma, D.S., Stine, O.C., Koppelman, G.H., Ampleford, E.J., Jongepier, H., Howard, T.D., Bleecker, E.R. (2005). Genome screen for asthma and bronchial hyperresponsiveness: interactions with passive smoke exposure. J Allergy Clin Immunol 115, 1169-1175 Murray M., Webb M.S.C., O´Callaghan, C., Swarbrick, A.S., Milner, A.D. (1992). Respiratory status and allergy after bronchiolitis. Archives Dis Child 67, 482-487 Nickel, R., Kulig, M., Forster, J., Bergmann, R., Bauer, C.P., Lau, S., Guggenmoos-Holzmann, I., Wahn, U. (1997). Sensitization to hen´s egg at the age of twelve months is predictive for allergic sensitization to common indoor and outdoor allergens at the age of three years. J Allergy Clin Immunol 99, 613-617 Oddy, W.H., de Klerk, N.H., Sly, P., Holt, P.G. (2002) The effects of respiratory infections, atopy, and breastfeeding on childhood asthma. Eur Respir J 19, 899-905 O´Garra, A. (1998). Cytokines induce the development of functionally heterogeous T helper cell subsets. Immunity 8, 275-283 Openshaw, P.J.M. (2001). Potential mechanisms causing delayed effects of respiratory syncytial virus infection. Am J Respir Crit Care Med 163, 10-13 80 Openshaw, P.J.M. (2005). Antiviral immune responses and lung inflammation after respiratory syncytial virus infection. Proc Am Thorac Soc 2, 121-125 Openshaw, P.J.M., Tregoning, J.S. (2005). Immune responses and disease enhancement during respiratory syncytial virus infection. Clin Microbiol Rev 18, 541-555 Palmer, L.J., Burton, P.R., Faux. J.A., James AL; Musk AW; Cookson WO (2000). Independent inheritance of serum immunoglobulin E concentrations and airway responsiveness. Am J Respir Crit Care Med 161, 1836-1843 Patel, H., Platt, R., Lozano, J.M. (2008). Glucocorticoids for acute viral bronchiolitis in infants and young children. Cochrane Database Syst Rev (1): CD004878 Power, U.F. (2008). Respiratory syncytial virus vaccines – two steps back for one leap forward. J Clin Virol 41, 38-44. Prescott, S.L., Macaubas, C., Holt, B.J., Smallacombe, T.B., Loh, R., Sly, P.D., Holt, P.G. (1998). Transplacental priming of the human immune system to environmental Allergens: Universal skewing of initial T cell responses toward the Th2 Cytokine profile. J Immunol 160, 4730-4737 81 Prescott, S.L., Macaubas, C., Smallacombe, T.B., Holt, B.J., Sly, P.D., Holt, P.G. (1999). Development of allergen-specific T-cell memory in atopic and normal children. Lancet 353, 196-200 Puthothu, B., Forster, J., Heinzmann, A., Krueger, M. (2006). TLR-4 and CD14 polymorphisms in respiratory syncytial virus associated disease. Dis Markers 22, 303-308 Puthothu, B., Krueger, M., Heinze, J., Forster, J., Heinzmann, A. (2006). Haplotypes of surfactant protein C are associated with common paediatric lung diseases. Pediatric Allergy and Immunology 17, 572-577 Puthothu, B., Krueger, M., Forster, J., Heinzmann, A. (2006). Association between severe respiratory syncytial virus infection and IL13/IL4 haplotypes. J Infect Dis 196, 438-441 Rager, K.J., Langland, J.O., Jacobs, B.L., Proud, D., Marsh, D.G., Imani, F. (1998). Activation of antiviral protein kinase leads to immunoglobulin E class switching in human B cells. J Virol 72, 1171-1176 Renzi, P.M., Turgeon, J.P., Marcotte, J.E., Drblik, S.P., Berube, D., Gagnon, M.F., Spier, S. (1999). Reduced interferon-gamma production in infants with bronchiolitis and asthma. Am J Respir Crit Care Med 159, 1417-1422 82 Rhodes, H.L., Sporik, R., Thomas, P., Holgate, S.T., Cogswell, J.J. (2001). Early life risk factors for adult asthma: a birth cohort study at subjects of risk. J Allergy Clin Immunol 108, 720-725 Rieger, C.H.L. (2001). Bronchiolitis durch RS-Viren. Atemwegs- und Lungenkrankheiten 27, 478-480 Rohwedder, A., Keminer, O., Forster, J., Schneider, K., Schneider, E., Werchau, H. (1998). Detection of respiratory syncytial virus RNA in blood of neonates by polymerase chain reaction. Journal of Medical Virology 54, 320-327 Roman, M., Calhoun, W., Hinton, K.L., Avendano, L.F., Simon, V., Escobar, A.M., Gaggero, A., Diaz, P.V. (1997). RSV-infection in infants is associated with predominant Th-2-like response. Am J Respir Crit Care Med 156, 190-195 RSV-Infektionen (2004) (Robert-Koch-Institut, Zugriff vom 3.3.2008) http://www.rki.de/cln_048/nn_504478/DE/Content/Infekt/EpidBull/Merkblaette r/Ratgeber__Mbl__RSV.html Rusconi, F., Galassi, C., Corbo, G.M., Forastiere, F., Biggeri, A., Ciccone, G., Renzoni, E., and the SIDRIA Collaborative Group (1999). Risk factors for early, persistent, and late-onset wheezing in young children. Am J Respir Crit Care Med 160, 1617-1622 83 Rusconi, F., Galassi, C., Forastiere, F., Bellasio, M., De Sario, M., Ciccone, G., Brunetti, L., Chellini, E., Corbo, G., La Grutta, S., Lombardi, E., Piffer, S., Talassi, F., Biggeri, A., Pearce, N. and the SIDRIA-2 Collaborative Group (2007). Maternal Complications and procedures in pregnancy and at birth and wheezing phenotypes in children. Am J Respir Crit Care Med 175, 16-21 Schaub, B., Lauener, R., von Mutius, E. (2006). The many faces of the hygiene hypothesis. J Allergy Clin Immunol 117, 969-977 Schauer, U., Ihorst, G., Rohwedder, A., Petersen, G., Berner, R., Frank, H.D., Forster, J., Stephan, V. (2007). Evaluation of respiratory syncytial virus detection by rapid antigen tests in childhood. Klin Paditr. 219, 212-216 Schlaud, M., Atzpodien, K., Thierfelder, W. (2007). Allergische Erkrankungen. Ergebnisse aus dem Kinder- und Jugendgesundheitssurvey (KiGGS). Bundesgesundheitsblatt – Gesundheitsforschung – Gesundheitsschutz 50, 701-710 Schmaltz, A.A. (2004). Stellungnahme der Deutschen Gesellschaft für Pädiatrische Kardiologie. Monatsschrift Kinderheilkunde 2, 222-223 Schwarze, J., Schauer, U. (2004). Enhanced virulence, airway inflammation and impaired lung function induced by respiratory syncytial virus deficient in secreted G protein. Thorax 59, 517-521 84 Sears, M.R., Holdaway, M.D., Flannery, E.M., Herbison, G.P., Silva, P.A. (1996). Parental and neonatal risk factors for atopy, airway hyper-responsiveness, and asthma. Arch Dis Child 75, 392-398 Sears, M.R., Greene, J.M., Willan, A.R., Wiecek, E.M., Taylor, D.R., Flannery, E.M., Cowan, J.O., Herbison, P., Silva, P.A., Poulton, R. (2003). A longitudinal, population-based, cohort study of childhood asthma followed to adulthood. NEJM 349, 1414-1422 Sherriff, A., Peters, .J., Henderson, J., Strachan, D. and the ALSPAC Study Team (2001). Risk factor associations with wheezing patterns in children followed longitudinally from birth to 3 ½ years. International Journal of Epidemiology 30, 1473-1484 Sherrill, D., Stein, R., Kurziu-Spencer, M., Martinez, F. (1999). On early sensitization to allergens and development of respiratory symptoms. Clin Exp Allergy 29, 905-911 Sigurs, N.; Bjarnason, R.; Sigurbergsson, F., Kjellmann, B., Björksten, B. (1995). Asthma and immunoglobulin E antibodies after respiratory syncytial virus bronchiolitis: a prospective cohort study with matched controls. Pediatrics 95, 500-505 Sigurs, N., Bjarnason, R., Sigurbergsson, F., Kjellman, B. (2000). Respiratory syncytial virus bronchiolitis in infancy is an important risk factor for asthma and allergy at age 7. Am J Respir Crit Care Med 161, 1501-1507 85 Sigurs, N., Gustafsson, P.M., Bjarnason, R., Lundberg, F., Schmidt, S., Sigurbergsson, F., Kjellman, B. (2005). Severe respiratory syncytial virus bronchiolitis in infancy and asthma and allergy at age 13. Am J Respir Crit Care Med 171, 137-1141 Simoes, E. (1999). Respiratory syncytial virus infection. Lancet 354, 847-852 Smyth, R.L., Fletcher, J.N., Thomas, H.M., Hart, C.A. (1997). Immunological responses to RSV-infection in infancy. Arch Dis Child 76, 210-214 Sorensen, G.L., Husby, S., Holmskov, U. (2007). Surfactant protein A and surfactant protein D variation in pulmonary disease. Immunobiology 212, 381-416 Srikiatkhachorn, A., Chang, W., Braciale, T.J. (1999). Induction of Th1 and Th2 responses by RSV attachment glycoprotein is epitope and MHC independent. J of Virology 73, 6590-6597 Stein, R.T., Sherrill, D., Morgan, W.J., Holberg, C.J., Halonen, M., Taussig, L.M., Wright, A.L., Martinez, F.D. (1999). Respiratory syncytial virus in early life and risk of wheeze and allergy by age 13 years. Lancet 354, 541-45 Strauss, J.M. (2002). Bronchiolitis. In Kretz, F.-J., Beushausen, T. (Hrsg.). Kinder Notfall Intensiv. Urban und Fischer Verlag, München Jena, 250-251 86 Sullender, W.M. (2000). Respiratory syncytial virus geneticand antigenetic diversity. Clinical Microbiology Reviews 1, 1-15 Tager, I.B., Hanrahan, J.P., Tosteson, T.D., Castile, R.G., Brown, R.W., Weiss, S.T., Speizer, F.E. (1993). Lung function, pre- and post-natal smoke exposure, and wheezing in the first year of life. Am Rev Respir Dis 147, 811-817 Tal, G., Mandelberg, A., Dalal, I., Cesar, K., Somekh, E., Tal, A., Oron, A., Itskovich, S., Ballin, A., Houri, S., Beigelman, A., Lider, O., Rechavi, G., Amariglio, N. (2004). Association between common Toll-like receptor 4 mutations and severe respiratory syncytial virus disease. J Infect Dis 189, 2057-2063 Taussig, L.M., Wright, A.L., Holberg, C.J., Halonen, M., Morgan, W.J., Martinez, F.D. (2003). Tucson children´s respiratory study : 1980 to present. J All Immunol 111, 661-675 Tebbey, P., Hagen, M., Hancock, G. (1998). Atypical pulmonary eosinophilia is mediated by a speccific amino acid sequence of the attachment G-protein of respiratory syncytial virus. J Exp Med 188, 1967-1972 Tepper, R.S., Williams-Nkomo, T., Martinez, T., Kisling, J., Coates, C., Daggy, J. (2005). Parental smoking and airway reactivity in healthy infants. Am J Respir Crit Care Med 171, 78-82 87 Tirado, R., Ortega, A., Sarmiento, R.E., Gomez, B. (2005). Interleukin-8 mRNA synthesis and protein secretion are continuously upregulated by respiratory syncytial virus persistently infected cells. Cell Immunol 233, 61-71 Tripp, R.A. (2004). Pathogenesis of respiratory syncytial virus infection. Viral Immunology 17, 165-181 Tulic, M.K., Hurrelbrink, R.J., Prele, C.M., Laing, I.A., Upham, J.W., Le Souef, P., Sly, P.D., Holt, P.G. (2007). TLR4 polymorphisms mediate impaired responses to respiratory syncytial virus and lipopolysaccharide. J Immunol 179, 132-140 Uekert, S.J., Akan, G., Evans, M.D., Li, Z., Roberg, K., Tisler, C., Dasilva, D., Anderson, E., Gangnon, R., Allen, D.B., Gern, J.E., Lemanske, R.F. Jr. (2006). Sex-related differences in immune development and the expression of atopy in early childhood. J Allergy Clin Immunol 118, 1375-1381 Van der Hoek, L., Pyrk, K., Jebbink, M.F., Vermeulen-Oost, W., Berkhout, R.J.M., Wolthers, K.C., Wertheim-van Dillen, P.M.E., Kaandorp, J., Spaargaren, J., Berkhout, B. (2004). Identification of a new human coronavirus. Nature Medicine 10, 368-273 88 Van der Kleij, D., Latz, E., Brouwers, J.F.H.M., Kruize, Y.C.M., Schmitz, M., Kurt-Jones, E.A., Espevik, T., de Jong, E.C., Kapsenberg, M.L., Golenbock, D.T., Tielens, A.G.M., Yazdanbakhsh (2002). A Novel Host-Parasite Lipid Cross-talk. Schistosomal Lysophosphatidylserine activates toll-like receptor 2 and effects immune polarization. J Biol Chem 277, 48122-48129 Van den Hoogen, B.G., de Jong, J.C., Groen, J., Kuiken, T., de Groot, R., Fouchier, R.A., Osterhaus, A.D. (2001). A newly discovered human pneumovirus isolated from young children with respiratory tract disease. Nature Medicine 7, 719-724 van Schaik, S.M., Welliver, R.C., Kimpen, J.L.L. (2000). Novel pathways in the pathogenesis of RSV disease. Pediatric pulmonology 30, 131-138 Varga, S.M., Wissinger, E.L., Braciale, T.J. (2000). The attachmant (G) glykoprotein of RSV contains a single immunodominant epitope that elicits both Th1 and Th2 CD4+ T cell responses. J Immunol 165, 6487-6495 Ventre, K., Randoplh, A.G. (2004). Ribavirin for respiratory syncytial virus infection of the lower respiratory tract in infants and young children. The Cochrane Library 4, CD000181 Vieira, S.E., Gilio, A.E., Durigon, E.L., Ejzenberg, B. (2007). Lower respiratory tract infection caused by respiratory syncytial virus in infants: the role played by specific antibodies. Clinics 62, 709-716 89 Von Linstow, M.-L., Hogh, M., Nordbo, S.A., Eugen-Olsen, J., Koch, A., Hogh, B. (2008). A community study of clinical traits and risk factors for human metapneumovirus and respiratory syncytial virus infection during the first year of life. Eur J Pediatr, Online First, ISSN 1432-1076, Zugriff vom 16.5.2008 Von Mutius, E., Martinez, F.D., Fritzsch, C., Nicolai, T., Reitmeir, P., Thiemann, H.-H. (1994). Skin test reactivity and number of siblings. BMJ 308, 692-695 Von Mutius, E. (2007). Allergies, infections und the hygiene-hypothesis – the epidemiological evidence. Immunobiology 212, 433-439 Von Piquet, C. (1906). Allergie. Münchener Medizinische Wochenschrift 30, 1457-1458 Wahn, U.; Mutius, E. v. (2001). Childhood risk factors for atopy and the importance of early intervention. J Allergy Clin Immunol 107, 567-574 Walzl, G., Matthews, S., Kendall, S., Gutierrez-Ramos, J.C., Coyle, A.J., Openshaw, P.J.M., Hussel, T. (2001). Inhibition of T1/ST2 during respiratory syncytial virus infection prevents T helper cell type 2 but not Th1-driven immunopathology. J Exp Med 193, 785-792 90 Weinmayr, G., Weiland, S.K., Björksten, B., Brunekreef, B., Büchele, G., Cookson, W.O.C., Garcia-Marcos, L., Gotua, M., Gratziou, C., van Hage, M., von Mutius, E., Riikjärv, M.-A., Rzehak, P., Stein, R.T., Strachan, D.P., Tsanakas, J., Wickens, C., Wong, G.W., and the ISAAC Phase Two Study Group (2007). Atopic sensitisation and the international variation of asthma symptom prevalence in children. Am J Respir Crit Care Med 176, 565-574 Welliver, R.C. (1999). Immunologic mechanisms of virus-induced wheezing and asthma. Journal of Pediatrics 135, 14-20 Welliver, R.C. (2002). Respiratory syncytial virus and other respiratory viruses. Pediatr Infect Dis J 22, 6-12 Wennergren, G., Kristjansson, S. (2001). Relationship between RSV bronchiolitis and future obstructive airway disease. Eur Respir J 18, 1044-1058 Wildhaber, J.H., Sennhauser, F.H. (2002). Asthma bronchiale im Kindesalter: Diagnose und Therapie. Annales Nestlé 60, 87-97 Wilkesmann, A., Schildgen, O., Eis-Hübinger, A.M., Geikowski, T., Glatzel, T., Lentze, M.J., Bode, U., Simon, A. (2006). Human metapneumovirus infections cause similar symptoms and clinical severity as respiratory syncytial virus infections. European Journal of Pediatrics 165, 467-475 91 Williams, J.V., Harris, P.A., Tollefson, S.J., Halburnt-Rush, L.L., Pingsterhaus, J.M., Edwards, K.M., Wright, P.F., Crowe, J.E. Jr. (2004). Human metapneumovirus and lower respiratory tract disease in otherwise healthy infants and children. NEJM 350, 443-450 Williams, J.V., Wang, C.K., Yang, C.-F., Tollefson, S.J., House, F.S., Heck, J.M., Chu, M., Brown, J.B., Lintao, L.D., Quinto, J.D., Chu, D., Spaete, R.R., Edwards, K.M., Wright, P.F., Crowe, J.E. Jr. (2006). The role of human metapneumovirus in upper respiratory tract infections in children: a 20-year experience. JID 193, 387-395 Wissinger, E.L., Stevens, W.W., Varga, S.M., Braciale, T.J. (2008). Proliferative expansion and acquisition of effector activity by memory CD4+ T cells in the lungs following pulmonary virus infection. J Immunol 180, 2957-2966 Woensel, J.B.M. v., Aalderen, W.M.C.v., Weerd, de W., Jansen, N.J.G., Gestel, J.P.J.v., Markhorst, D.G., Vught, A.J.v., Bos, A.P., Kimpen, J.L.L. (2003). Dexamehtasone for treatmentof patients mechanically ventilated for lower respiratory tract infection caused by respiratory syncytial virus. Thorax 58, 383-387 Wolf, D.G., Greenberg, D., Kalkstein, D., Shemer-Avni, Y., Givon-Lavi, N., Saleh, N., Goldberg, M.D., Dagan, R. (2006). Comparison of human metapneumovirus, respiratory syncytial virus and influenza A virus lower respiratory tract infections in hospitalized young children. Pediatric Infectious Disease Journal 25, 320-324 92 Wright, A.L., Stern, D.A., Kauffmann, F., Martinez, F.D. (2006). Factors influencing gender differences in the diagnosis and treatment of asthma in childhood: the Tucson Children´s Respiratory Study. Pediatr Pulmonol 41, 318-325 Young, S.; Sherrill, D.L., Arnott, J., Diepeveen, D., LeSouef, P.N., Landau, L.I. (2000). Parental factors affecting respiratory function during the first year of life. Pediatr Pulmonol 29, 331-340 Zhang, L., Peeples, M.E., Boucher, R.C., Collins, P.L., Pickles, R.J. (2002). Respiratory syncytial virus infection of human airway epithelial cells is polarizes, specific to ciliated cells, and without obvious cytopathology. J Virol 76, 5654-5666 Zhou, Y. (2008). Regulatory T cells and viral infections. Front Biosci 13, 1152-1170 Zollner, I.K., Weiland, S.K., Piechotowski, I., Gabrio, T., von Mutius, E., Link, B., Pfaff, G., Kouros, B., Wuthe, J. (2005). No increase in the prevalence of asthma, allergies, and atopic sensitisation among children in Germany: 1992-2001. Thorax 60, 545-548 93 7 Anhang 7.1 Fragebogen bei Geburt Grunddaten Geburtsdatum (Geburtsdatum) Geschlecht (männlich / weiblich) Mutter Alter (Alter) Neurodermitis Leiden oder litten Sie jemals an einer Neurodermitis (auch endogenes Ekzem oder atopische Dermatitis genannt)? (ja / nein) Allergische Rhinitis Leiden oder litten Sie – ohne dabei erkältet zu sein – an einer juckenden, verstopften oder laufenden Nase und / oder an verschwollenen, juckenden Augen, und zwar regelmäßig im Frühjahr oder Sommer, oder fast immer beim Umgang mit bestimmten fell- oder federtragenden Tieren? Haben oder hatten Sie einen Heuschnupfen (allergischen Schnupfen oder allergische Bindehautentzündung)? (ja / nein) Asthma Leiden oder litten Sie an allergischem Asthma (Bronchialasthma)? (ja / nein) Allergietest Wurde bei Ihnen schon einmal eine Allergietestung vorgenommen, und hat der Test die Allergie nachgewiesen? (ja/nein) 94 Vater Alter (Jahre) Neurodermitis Leiden oder litten Sie jemals an einer Neurodermitis (auch endogenes Ekzem oder atopische Dermatitis genannt)? (ja / nein) Allergische Rhinitis Leiden oder litten Sie – ohne dabei erkältet zu sein – an einer juckenden, verstopften oder laufenden Nase und / oder an verschwollenen, juckenden Augen, und zwar regelmäßig im Frühjahr oder Sommer, oder fast immer beim Umgang mit bestimmten fell- oder federtragenden Tieren? Haben oder hatten Sie einen Heuschnupfen (allergischen Schnupfen oder allergische Bindehautentzündung)? (ja / nein) Asthma Leiden oder litten Sie an allergischem Asthma (Bronchialasthma)? (ja / nein) Allergietest Wurde bei Ihnen schon einmal eine Allergietestung vorgenommen, und hat der Test die Allergie nachgewiesen? (ja / nein) Geschwister Anzahl (Anzahl) Allergieanamnese Sind bei Ihren leiblichen Kindern folgende Erkrankungen aufgetreten oder von einem Arzt diagnostiziert worden? a) wiederholte Bronchitis mit pfeifender Atmung (ja/nein) 95 b) Asthma oder asthmoide Bronchitis (ja/nein) c) Heuschnupfen (allergischer Schnupfen) (ja/nein) d) Milchschorf und / oder juckendes Ekzem besonders in Ellenbogen und Kniekehlen (ja/nein) e) Neurodermitis (atopische Dermatitis) (ja/nein) f) Nesselsucht (Urtikaria) (ja/nein) g) Nahrungsmittelallergie (wie oben beschrieben) (ja/nein) Positiv, wenn eine der Fragen b, c, e und / oder zwei oder mehr der Fragen a, d, f, g beantwortet wurde (negativ / positiv) Umgebungsbedingungen Was ist der höchste Berufsabschluß von Vater oder Mutter des Kindes? (niedrig – keine Berufsausbildung / mittel – abgeschlossene Berufsausbildung / gehoben – Hochschule) Wie alt ist Ihre Wohnung? (>10 Jahre, 1-10 Jahre, Neubau) Finden sich in Ihrer Wohnung Spuren von Feuchtigkeit? (keine, ja) Finden sich in Ihrer Wohnung Schimmelflecke oder Stockflecke? (keine, ja) Sind die Böden in Ihrer Wohnung mit Teppichboden ausgelegt? (nein, Teppichboden) Halten Sie Pflanzen im Wohnbereich? (keine, ja) Halten Sie Tiere in der Wohnung? (keine, ja) Ist die Decke Ihres Kindes waschbar? (nicht waschbar, waschbar) 96 Wird in Ihrer Wohnung geraucht? (niemand raucht, ja) Schwangerschaft Komplikationen Gab es während der Schwangerschaft Komplikationen? (ja / nein) Vorzeitige Wehen? (keine / vorzeitige Wehen) Blutungen in der Schwangerschaft? (keine / Blutungen) Gab es eine Infektion in der Schwangerschaft, die antibiotisch behandelt werden musste? (keine / bakterielle Infektion) Wurden in der Schwangerschaft Medikamente eingenommen? (ja / nein) Jod? (ja / nein) Folsäure? (ja / nein) Eisenpräparat? (ja / nein) Magnesium? (ja / nein) Calcium? (ja / nein) Antibiotikum? (ja / nein) Rauchen Rauchen vor der Schwangerschaft (ja / nein) Rauchen in der Schwangerschaft (ja / nein) Änderungen der Ernährung in der Schwangerschaft (keine Änderung / geändert) Nüsse (keine Änderung / mehr / weniger) Fisch (keine Änderung / mehr / weniger) Milch + Milchprodukte (keine Änderung / mehr / weniger) Eier (keine Änderung / mehr / weniger) Getreideprodukte (keine Änderung / mehr / weniger) 97 Geburt Schwangerschaftsdauer (Schwangerschaftswochen) Geburtsmodus (normal / Vakuumextraktion / Sectio) Besonderheiten bei Geburt (ja / nein) Abfall der kindlichen Herztöne (ja / nein) Vorzeitiger Blasensprung (ja / nein) Infektion bei Geburt (ja / nein) Kindliche Größe als Geburtshindernis (ja / nein) Grünes Fruchtwasser (ja / nein) Besonderheiten postpartal (ja / nein) Postpartale Anpassungsstörung (ja / nein) V.a. Infektion (ja / nein) Infektion des Neugeborenen (ja / nein) Ikterus (ja / nein) Frühgeburtlichkeit (ja / nein) SGA (small for gestational age) (ja / nein) Kind diabetischer Mutter (ja / nein) Behandlung in Kinderklinik (ja / nein) Erforderliche Therapie Phototherapie (ja / nein) Beatmung (ja / nein) Antibiotikatherapie (ja / nein) 98 Vorsorgeheft U1 U1 Länge in cm U1 Länge, Percentilen U1 Gewicht in g U1 Gewicht, Percentilen U1 Kopfumfang in cm U1 Kopfumgang, Percentilen 99 7.2 Fragebogen im Alter von einem Jahr Mutter Haben sich seit der Geburt des Kindes Änderungen ergeben? (ja / nein) Neurodermitis Leiden oder litten Sie jemals an einer Neurodermitis (auch endogenes Ekzem oder atopische Dermatitis genannt)? (ja / nein) Allergische Rhinitis Leiden oder litten Sie – ohne dabei erkältet zu sein – an einer juckenden, verstopften oder laufenden Nase und / oder an verschwollenen, juckenden Augen, und zwar regelmäßig im Frühjahr oder Sommer, oder fast immer beim Umgang mit bestimmten fell- oder federtragenden Tieren? Haben oder hatten Sie einen Heuschnupfen (allergischen Schnupfen oder allergische Bindehautentzündung)? (ja / nein) Asthma Leiden oder litten Sie an allergischem Asthma (Bronchialasthma)? (ja / nein) Allergietest Wurde bei Ihnen schon einmal eine Allergietestung vorgenommen, und hat der Test die Allergie nachgewiesen? (ja/nein) Vater Haben sich seit der Geburt des Kindes Änderungen ergeben? (ja / nein) Alter (Jahre) Neurodermitis 100 Leiden oder litten Sie jemals an einer Neurodermitis (auch endogenes Ekzem oder atopische Dermatitis genannt)? (ja / nein) Allergische Rhinitis Leiden oder litten Sie – ohne dabei erkältet zu sein – an einer juckenden, verstopften oder laufenden Nase und / oder an verschwollenen, juckenden Augen, und zwar regelmäßig im Frühjahr oder Sommer, oder fast immer beim Umgang mit bestimmten fell- oder federtragenden Tieren? Haben oder hatten Sie einen Heuschnupfen (allergischen Schnupfen oder allergische Bindehautentzündung)? (ja / nein) Asthma Leiden oder litten Sie an allergischem Asthma (Bronchialasthma)? (ja / nein) Allergietest Wurde bei Ihnen schon einmal eine Allergietestung vorgenommen, und hat der Test die Allergie nachgewiesen? (ja / nein) Geschwister Haben sich seit Geburt des Kindes Änderungen ergeben? (ja / nein) Anzahl (Anzahl) Allergieanamnese Sind bei Ihren leiblichen Kindern folgende Erkrankungen aufgetreten oder von einem Arzt diagnostiziert worden? a) wiederholte Bronchitis mit pfeifender Atmung (ja/nein) b) Asthma oder asthmoide Bronchitis (ja/nein) c) Heuschnupfen (allergischer Schnupfen) (ja/nein) d) Milchschorf und / oder juckendes Ekzem besonders in Ellenbogen und Kniekehlen (ja/nein) 101 e) Neurodermitis (atopische Dermatitis) (ja/nein) f) Nesselsucht (Urtikaria) (ja/nein) g) Nahrungsmittelallergie (wie oben beschrieben) (ja/nein) Positiv, wenn eine der Fragen b, c, e und / oder zwei oder mehr der Fragen a, d, f, g beantwortet wurde (negativ/positiv) Kontakte zu Kindern Wo hat das Kind Kontakte zu anderen Kindern: Zu Hause (ja/nein) In der Krabbelgruppe (ja/nein) Im Kindergarten (ja/nein) In der Schule (ja/nein) Umgebungsbedingungen Haben sich seit Geburt des Kindes Änderungen ergeben? (ja/nein) Was ist der höchste Berufsabschluß von Vater oder Mutter des Kindes? (niedrig – keine Berufsausbildung / mittel – abgeschlossene Berufsausbildung / gehoben – Hochschule) Wie alt ist Ihre Wohnung? (>10 Jahre, 1-10 Jahre, Neubau) Finden sich in Ihrer Wohnung Spuren von Feuchtigkeit? (keine, ja) Finden sich in Ihrer Wohnung Schimmelflecke oder Stockflecke? (keine, ja) Sind die Böden in Ihrer Wohnung mit Teppichboden ausgelegt? (nein, Teppichboden) 102 Halten Sie Pflanzen im Wohnbereich? (keine, ja) Halten Sie Tiere in der Wohnung? (keine, ja) Ist die Decke Ihres Kindes waschbar? (nicht waschbar, waschbar) Wird in Ihrer Wohnung geraucht? (niemand raucht, ja) Vorsorgeheft U2 U2 Länge in cm U2 Länge, Percentilen U2 Gewicht in g U2 Gewicht, Percentilen U2 Kopfumfang in cm U2 Kopfumgang, Percentilen Vorsorgeheft U3 U3 Länge in cm U3 Länge, Percentilen U3 Gewicht in g 103 U3 Gewicht, Percentilen U3 Kopfumfang in cm U3 Kopfumgang, Percentilen Vorsorgeheft U4 U4 Länge in cm U4 Länge, Percentilen U4 Gewicht in g U4 Gewicht, Percentilen U4 Kopfumfang in cm U4 Kopfumgang, Percentilen Vorsorgeheft U5 U5 Länge in cm U5 Länge, Percentilen U5 Gewicht in g U5 Gewicht, Percentilen U5 Kopfumfang in cm 104 U5 Kopfumgang, Percentilen Husten Hat Ihr Kind seit unserem letzten Treffen jemals unter Husten gelitten? (ja / nein) Wie war dieser Husten? Trockener Reizhusten (ja, immer / ja, manchmal / nein, nie) Bellender, heiserer Husten (ja, immer / ja, manchmal / nein, nie) Feuchter, verschleimter Husten (ja, immer / ja, manchmal / nein, nie) Hustenanfall (ja, immer / ja, manchmal / nein, nie) Anders (ja, immer / ja, manchmal / nein, nie) Giemen Haben Sie bei Ihrem Kind seit unserem letzten Treffen ein pfeifendes oder giemendes Atemgeräusch gehört? (vormachen oder beschreiben: eher leises aus der Tiefe kommendes, helles, pfeifendes Geräusch beim Ausatmen) (ja/nein) Stridor Haben Sie bei Ihrem Kind seit unserem letzten Treffen eine geräuschvolle, ziehende Einatmung erlebt? (vormachen oder beschreiben: schärferes, scheinbar aus der Halsgegend kommendes Geräusch) (ja/nein) Rhinitis Hat ihr Kind seit unserem letzten Treffen unter einer verstopften oder laufenden Nase gelitten? (ja/nein) Welcher Art waren diese Beschwerden genau Verstopfte Nase (ja, immer / ja, manchmal / nein, nie) Laufende Nase mit wässrig-klarem Schleim (ja, immer / ja, manchmal / nein, nie) 105 Laufende Nase mit eitrigem, grün.-gelbem Schleim (ja, immer / ja, manchmal / nein, nie) Niesanfälle (mehr als 5x hintereinander) (ja, immer / ja, manchmal / nein, nie) Juckende Nase (ja, immer / ja, manchmal / nein, nie) Anderes (ja, immer / ja, manchmal / nein, nie) Traten diese Beschwerden im Rahmen einer Erkältungskrankheit auf? (nein, nie / ja, manchmal / ja,immer) Haben Sie jemals beobachtet, dass Ihr Kind nachts schnarcht? (ja, oft oder ständig / ja, manchmal / nein, nie) Konjunktivitis Hat Ihr Kind seit unserem letzten Treffen unter beiderseits geröteten, tränenden oder geschwollenen Augen gelitten? (ja / nein, nie) Welcher Art waren diese Beschwerden genau? Augen gerötet (ja, immer / ja, manchmal / nein, nie) Augen geschwollen (ja, immer / ja, manchmal / nein, nie) Wässrig, glasig tränende Augen (ja, immer / ja, manchmal / nein, nie) Grün-gelb, eitrig tränende Augen (ja, immer / ja, manchmal / nein, nie) Juckende Augen (ja, immer / ja, manchmal / nein, nie) Anderes (ja, immer / ja, manchmal / nein, nie) Erbrechen Hat Ihr Kind seit unserem letzten Treffen jemals erbrochen oder gespuckt? (gelegentliches Erbrechen nach zu hastigem Trinken oder zu reichlichen Mahlzeiten ist hier nicht gemeint) (ja/nein) Erbricht das Kind nur flüssige Flaschenmahlzeiten oder auch Brei und angedickte Flaschenmahlzeiten? (nur Flüssiges / auch Festeres / weiß nicht (nicht probiert)) Welcher Art war / ist dieses Erbrechen? Nur ein bisschen gespuckt (ja, immer / ja, manchmal / nein, nie) Ganz schön viel erbrochen (ja, immer / ja, manchmal / nein, nie) Im Strahl (in hohem Bogen) (ja, immer / ja, manchmal / nein, nie) Roch säuerlich (ja, immer / ja, manchmal / nein, nie) Enthielt Schleim (ja, immer / ja, manchmal / nein, nie) 106 Enthielt Blut (ja, immer / ja, manchmal / nein, nie) Das Kind schrie und erbrach gleichzeitig (ja, immer / ja, manchmal / nein, nie) Anderes (ja, immer / ja, manchmal / nein, nie) Durchfall Hat Ihr Kind seit unserem letzten Treffen unter Durchfall gelitten? (normale Muttermilchstühle sind nicht gemeint, sondern für die Gewohnheit des Kindes auffällig dünne, möglicherweise übelriechende Stühle) (ja / nein,nie) Wie sah der Stuhl dabei aus Wasserdünn (ja, immer / ja, manchmal / nein, nie) Wie ein dünner Brei (ja, immer / ja, manchmal / nein, nie) Massenhaft breiig (ja, immer / ja, manchmal / nein, nie) Fettig glänzend (ja, immer / ja, manchmal / nein, nie) Übelriechend (ja, immer / ja, manchmal / nein, nie) Enthielt Blut (ja, immer / ja, manchmal / nein, nie) Enthielt Schleim (ja, immer / ja, manchmal / nein, nie) Anderes (ja, immer / ja, manchmal / nein, nie) Hat Ihr Kind dabei gleichzeitig unter Erbrechen gelitten? (ja, immer / ja, manchmal / nein, nie) Bauchschmerzen Haben Sie den Eindruck das Ihr Kind unter Bauchschmerzen litt oder noch darunter leidet? (ja / nein, nie) Sind in diesem Zusammenhang schon öfter folgende Erscheinungen aufgetreten: Plötzlich einsetzende Schreiphasen (ja, immer / ja, manchmal / nein, nie) Schwer beeinflussbare Unruhe (ja, immer / ja, manchmal / nein, nie) Geblähter Bauch (ja, immer / ja, manchmal / nein, nie) Vermehrter Abgang von Winden (ja, immer / ja, manchmal / nein, nie) Krampfartige Anziehen der Beine (ja, immer / ja, manchmal / nein, nie) Anderes (ja, immer / ja, manchmal / nein, nie) Wie haben sich diese Beschwerden in der Zwischenzeit entwickelt? (unverändert / weniger geworden / vollständig abgeklungen / zugenommen) 107 Hautsymptome Hat oder hatte Ihr Kind eine auffallend trockene Haut? (ja / nein / weiß nicht) Wie oft kratzt sich Ihr Kind? (ab und zu / sehr oft / fast ständig / nie) Sind Ihnen bei Ihrem Kind seit dem letzten Treffen folgende Hauterscheinungen aufgefallen: Gelbe Kopf-Schuppen (ja / nein) Wangenekzem (ja / nein) Ekzem an anderen Körperstellen (ja / nein) Einrisse am Ohr (ja / nein) Länger bestehende, gerötete, kleine Hautstelle(n), die evtl. schuppt(en) und juckt(en) (ja / nein) Lippenschwellungen (ja / nein) Wundsein im Windelbereich (ja / nein) 108 8 Danksagung Herzlich bedanken möchte ich mich bei: Herrn Prof. Dr. med. U. Schauer für die Überlassung dieser Arbeit und seine Unterstützung zu jeder Zeit; Frau Dr. med. Mirjam Triebel für ihre konstruktive Kritik Angelika Michel und Veronika Baumeister vom Immunologischen Labor der Kinderklinik für Ihre Hilfsbereitschaft Allen Kindern und deren Eltern, die sich bereit erklärt haben, an der Studie teilzunehmen 9 Lebenslauf Silke Bongartz, geboren am 26.06.1976 in Viersen, verheiratet, eine Tochter, römisch-katholischen Bekenntnisses 1995 Abitur, Albertus-Magnus-Gymnasium, Viersen-Dülken 1997 Ärztliche Vorprüfung, Ruhr-Universität Bochum 1998 1. Ärztliches Staatsexamen, Ruhr-Universität Bochum 2001 2. Ärztliches Staatsexamen, Ruhr-Universität Bochum 2001 – 2002 Praktisches Jahr am Sana-Klinikum Remscheid, Wahlfach Kinderheilkunde Mai 2002 3. Ärztliches Staatsexamen, Ruhr-Universität Bochum Seit Juli 2002 Ärztin im Praktikum und Assistenzärztin, Klinik für Kinder-heilkunde und Jugendmedizin (Chefarzt Prof. Dr. J. R. Pfefferkorn), Grafschafter Klinikum, Nordhorn Seit 2002 Dozentin für die Fächer Anatomie, Physiologie und Pädiatrie an der (Kinder-)Krankenpflegeschule des Grafschafter Klinikums 2001 – 2004 Fortbildung Traditionelle Chinesische Medizin und Akupunktur, Universität Witten-Herdecke November 2007 Zusatzbezeichnung Akupunktur