Normale Entwicklung des Embryos/Feten Teil I
Werbung

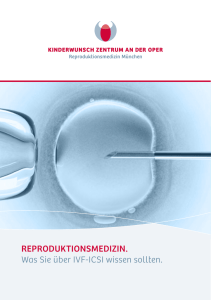
Normale Entwicklung des Embryos/Feten Teil I Dr. sc. nat. Oliver Sterthaus University Hospital Basel 1 Embryologie Gametogenese Fertilisation Preimplantation Implantation -Embryonalscheibe Text und Bilder sind vom http://www.embryology.ch 2 Gametogenese • • • • Die Keimbahn - Ursprung der Keimzellen Die Determinierung des Geschlechts Spermatogenese Oogenese 3 Die Keimbahn - Ursprung der Keimzellen Wanderung der Keimzellen Vom primären Ektoderm wandern die Urkeimzellen in der dritten Woche amöboid in die Wand des Dottersacks ein und sammeln sich nahe des Abgangs der Allantois an. Die Urkeimzellen sind nun extraembryonal im Endoderm und Mesoderm der Dottersackwand gelegen. Durch die kraniokaudale Krümmung und die laterale Abfaltung des Embryos begünstigt, wandern die Urkeimzellen zwischen der vierten und sechsten Woche wieder zurück in den Embryo. Sie bewegen sich entlang der Dottersackwand zum Dottergang und in die Wand des Enddarms. Nach der Durchquerung des dorsalen Mesenteriums treffen sie in der Genitalleiste ein. Während ihrer Wanderung, aber auch noch in der Genitalleiste, vermehren sich die Urkeimzellen durch mitotische Teilungen. 1 Urkeimzellen 2 Allantois 3 Enddarm 4 Ektoderm 5 Vorderdarm 6 Herzanlage 7 sekundärer Dottersack 8 Endoderm (gelb) 9 Mesoderm (rot) 10 Amnionhöhle 1 2 3 4 5 6 7 Enddarm Dottergang Allantois Urnierenleiste(rosa) Genitalleiste (grün) Urkeimzellen Herzvorwölbung 4 Die Determinierung des Geschlechts Männliche Gonadenanlage Der Schlüssel zur Sexualdifferenzierung liegt auf dem Y Chromosom in der SRY (Sex determining region of the Y chromosome), welches die männliche Entwicklung induziert. Die Expression des Gens SRY stimmt mit dem Zeitpunkt der Geschlechtsdeterminierung überein, denn es wird in den somatischen Zellen der männlichen Genitalleiste exprimiert. Unter anderem wird im Hoden Testosteron ab der 7. Woche gebildet. Ist kein Y-Chromosom und somit kein SRY vorhanden, kommt es zur Ausbildung eines weiblichen Phänotyps. 1 Ductus mesonephricus (Wolff) 2 PGC 3 Peritonealhöhle 4 Aorta 5 Tubulus mesonephricus 6 Gonadenstränge 7 Zölomepithel 8 Darm 9 Mesenterium 10 Anlage des Ductus paramesonephricus (Müller) 11 Rückbildung der Mesonephros-Nephrone 5 Die Determinierung des Geschlechts Weibliche Gonadenanlage Die Keimstränge im Bereich des Markes degenerieren, da im weiblichen Körper kein SRY existiert. In der Rindenregion bleibt hingegen die Proliferation des Zölomepithels erhalten, und umgeben die sich vermehrenden Keimzellen. Diese bleiben aber in der Nähe der Oberfläche und werden im Unterschied zu den primären Keimsträngen Rindenstränge genannt. Im 4. Monat zerfallen die Rindenstränge in einzelne Zellhaufen und die Epithelzellen umgeben eine bis zwei Urkeimzellen. Die Urkeimzellen differenzieren sich in Oogonien und beginnen mit der ersten Reifeteilung als primäre Oozyte, während aus den Epithelzellen die Follikelzellen entstehen. Die dann einsetzende Interaktion mit den sie umgebenden Follikelzellen stoppt die Vollendung der ersten Reifeteilung bis zum Einsetzen der Pubertät. 6 Spermatogenese Mit dem Eintritt in die Pubertät setzt im Hoden des Mannes die Spermatogenese ein. Diese umfasst die gesamte Entwicklung von der Spermatogonie (ehemalige Urkeimzellen) bis zum Spermium. Die bis dahin soliden Keimstränge im kindlichen Hoden erhalten zu Beginn der Pubertät ein Lumen. Sie wandeln sich damit in Samenkanälchen um, die eine Länge von ca. 50-60cm erlangen. Sie werden als Tubuli seminiferi contorti bezeichnet, die so zahlreich sind, dass ihre Gesamtlänge beim erwachsenen Mann 300 bis 350m erreicht. Sie werden von einem Keimepithel ausgekleidet das zwei verschiedene Zellpopulationen aufweist:Einmal Stützzellen (= Sertolizellen) und zum überwiegenden Teil die verschiedenen Stadien der sich teilenden und differenzierenden Keimzellen. 7 • • Spermatogenese Offenbar braucht es für eine optimale Spermienproduktion ein bestimmtes Milieu. So ist durch die Verlagerung des Hodens ins Skrotum die Hodentemperatur 2-3ºC niedriger als die Körpertemperatur. Im Weiteren ist ein leicht erhöhter Umgebungsdruck notwendig. Deshalb quillt beim Anritzen der straffen Tunica albuginea das Hodenparenchym von selbst heraus. Erhöhter Druck und niedrige Temperatur sind offenbar beide nötig für die Spermienbildung. Die Entwicklung der Keimzellen beginnt mit den Spermatogonien aussen an der Basalmembran des Samenkanälchens und schreitet lumenwärts über Spermatozyten I (primäre Spermatozyten) und Spermatozyten II (sekundäre Spermatozyten) und Spermatiden bis zu den reifen Spermien fort. 1 Basalmembran (nicht erkennbar) 2 Myofibroblast 3 Fibrozyt 4 Sertolizelle 5 Spermatogonie A 6 verschiedene Stadien der Keimzellen während der Spermatogenese 7 Spermium 8 Lumen 8 Spermatogenese Entwicklungsstadien der Spermatogenese http://scientopia.org/blogs/scicurious/2010/03/10/basics-guest-post-2spermatogenesis 9 Spermatogenese Spermatogenese und Strukturen der Spermienzelle 1 Axonemale Struktur, erste Geisselanlage 2 Golgi Apparat 3 Akrosomales Bläschen 4 Zentriolenpaar (distales und proximales) 5 Mitochondrium 6 Kern 7 Geisselanlage 8 Mikrotubuli 9 Spermienschwanz 10 Akrosomenkappe 10 Oogenese Struktur des Ovars 1 Primordialfollikel 2 Primärfollikel 3 Sekundärfollikel 4 Tertiärfollikel 5 Antrumfollikel 6 Cumulus oophorus 11 Oogenese Vom Primordialfollikel bis zum Tertiarfollikel Primordialfollikel und Primärfollikel A Primordialfollikel B Primärfollike 1 Oozyte 2 Follicular epithelium Sekundärfollikel Tertiärfollikel 1 Oozyte 2 Zona Pellucida 3 Stratum granulosum 4 Theca Zellen 1 Oocyte 2 Zona Pellucida 3 Stratum granulosum 4 Theca interna 5 Theca externa 6 Antralfollikel 7 Cumulus oophorus 8 Basal lamina 12 Oogenese Zeitlicher Verlauf der Keimzellenzahl / Follikelzahl Phase A: Urkeimzellen wachsen ein, proliferieren und werden vom Zölomepithel eingescheidet . Keimstränge (Rindenstränge) entstehen; 6.-8.Woche. Phase B: Wachstumsschub: Es bilden sich Zellklone von Oogonien, wobei die Zellen untereinander durch Zellbrücken verbunden bleiben. 9.-22.Woche. Phase C: Die Oogonien werden zu primären Oozyten, die in die Prophase der ersten Reifeteilung eintreten. 12.-25. Woche. Phase D: Die primäre Oozyten werden im Diktyotän der Prophase arretiert: Es entstehen die Primordialfollikel, 16.-29. Woche. Phase E: Es setzt etwa um die 14. Woche ein mengenmässig ansteigender Untergang von Keimzellen ein, sowie eine Atresie in allen Follikelstadien. 13 Gegenüberstellung der Spermatogenese und der Oogenese Spermatogenese Oogenese Anzahl der Gameten Prinzip: kontinuierliche Neubildung. Obwohl von der Pubertät bis zum Tod immer Spermien produziert werden, unterliegt die Produktion extremsten Schwankungen in Bezug auf Quantität und Qualität. Prinzip: Aufbrauchen des Vorrats. Kontinuierlich stattfindende Abnahme der Eizellen von der Fetalzeit an. Erschöpfung des Vorrats mit der Menopause. Output der Meiose Am Ende der Meiose finden sich vier Am Ende der Meiose findet sich eine funktionstüchtige Gameten Oozyte und drei Polkörperchen. Fetalperiode Kein Eintritt in die Meiose Eintritt in die Meiose (wird im Dyktiotän angehalten) Keine Keimzellproduktion Produktion des ganzen Vorrats an Keimzellen 14 Fertilisation • Ovulation • Die Bereitstellung der Spermien • Der Weg der Spermien bis zur Oozyte - Die Kapazitation • Der Weg der Spermien bis zur Oozyte - Die Akrosomalreaktion • Das Eindringen des Spermatozoons in die Oozyte • Die Fertilisation wird abgeschlossen. Die Ausbildung der Zygote 15 Ovulation Im Zentrum dieser hormonellen Steuerung ist das HypothalamusHypophysen-System mit dem GnRH und den beiden Gonadotropinen FSH und LH. Die pulsatile Freisetzung des GnRH ist die fundamentale Voraussetzung für eine normale hypothalamisch-hypophysäre Kontrolle der zyklischen Ovarialfunktion. FSH und LH wirken anregend auf die Reifung der Follikel im Ovar und lösen die Ovulation aus. Während des Ovarialzyklus werden von den Zellen der Theka interna Östrogene (sogenannte Follikelphase) und vom Corpus Luteum das Progesteron (sogennannte Sekretionsphase) gebildet. http://commons.wikimedia.org/wiki/File:MenstrualCycle.png 16 Ovulation Heranreifen der Eizelle im dominanten Follikel kurz vor der Ovulation 1 Theca interna und externa 2 Basalmembran zwischen Theka und Granulosa 3 Granulosa 4 Graafscher Follikel mit Follikelflüssigkeit 5 primäre Oozyte 6 Cumulus oophorus 7 Ovarielles Gewebe 8 Tunica albuginea des Ovars 9 Peritonealhöhle 10 Zona pellucida 11 Kern in der Diakinese 12 Granulosazelle 13 Zellausläufer der Granulosazelle 14 Mikrovilli der Eizelloberfläche 17 Ovulation Beendigung der ersten Reifeteilung 1 Zona Pellucida 2 Perivitelliner Spaltraum 3 Spindelpapparat in Anaphase der 1. RT 4 Zellausläufer der Granulosazelle 5 Mikrovilli der Eizelloberfläche 6 Granulosazelle 7 Polkörper 18 Ovulation Sprungbereiter Follikel Oozyte umgeben von einer Kumuluszellwolke (Corona radiata) 1 Peritonealhöhle 2 Sprungbereiter Follikel mit Follikelflüssigkeit (stark Hyaluronsäure und Progesteron haltig) 3 Kumuluszellwolke mit Oozyte 4 Aufgelockerter Kumulus 5 Sekundäre Oozyte 6 Corona radiata 7 Ovarielles Gewebe 1 Spindelapparat mit Chromosomen, die die Metaphasenplatte bilden 2 Arretierter Spindelapparat im Polkörper 3 Perivitelliner Spaltraum 19 Ovulation 1 Aufgeschnittene Tube mit in Falten gelegter Tubenschleimhaut 2 Dicht anliegende Fimbrien 3 heraugeflossene Follikelflüssigkeit 4 sekundäre Oozyte mit Corona radiata 5 Ovar mit atretischen Follikeln in verschiedenen Stadien 6 Zona Pellucida 7 erster Polkörper 8 sekundäre Oozyte 9 Zellen der Corona radiata 10 Arretierter Spindelapparat Die Eizelle "wartet" nun in der Tube auf eine Befruchtung durch die Spermien. Die Matrix aus Hyaluronsäure hält sie sozusagen in der Tube "gefangen". Nach etlichen Stunden verflüssigt sich die Matrix immer mehr und die Eizelle wird allmählich durch den Zilienschlag der Tubenepithelzellen uteruswärts transportiert. Da die Eizelle nach der Ovulation auch nur einige Stunden befruchtungsfähig ist, muss die Befruchtung fast zwangsläufig im ampullären Teil der Tube stattfinden. 20 Ovulation 21 Ovulation 22 Die Bereitstellung der Spermien - Der Weg der Spermien bis zur Oozyte Der Weg der Spermien bis zur Oozyte - Die Kapazitation - Die Akrosomalreaktion 23 Die Bereitstellung der Spermien Reifungsschritte der Spermien 1 Schwanz 2 Kopf 3 Akrosom Die Reifung und Aktivierung des Spermatozoons erfolgt durch die folgenden vier Schritte: Lagerung im Nebenhoden Ejakulation Aszension zum Ovar In der Nähe der Oozyte Reifung Aktivierung Kapazitation Akrosomalreaktion 24 Die Bereitstellung der Spermien Das Seminalplasma Die chemischen Funktionen des Ejakulats werden vom Seminalplasma wahrgenommen. Das Zusammenmischen der verschiedenen Drüsenfraktionen führt zu einem Koagulieren des frischen Ejakulats im hinteren Scheidengewölbe binnen einer Minute. Auf diese Weise wird in der Vagina ein Spermiendepot errichtet. Nach ca. 15-20 Minuten verflüssigt sich das koagulierte Ejakulat wieder. Wegen seiner leichten Alkalinität (leicht alkalischer Puffer) ist es aber auch für die Schaffung eines für die Spermien günstiges Milieus im normalerweise sauren Scheidenmilieu zuständig. Das Seminalplasma hat folgende Aufgaben zu erfüllen: • Schaffung eines alkalisch gepufferten Milieus in der Scheide • Koagulieren des Ejakulats und Errichten eines Spermiendepots in der Vagina • Anlagerung von Kapazitationsinhibitoren an die Spermien • Aktivierung und Verstärkung der Motilität der Spermien • Bereitstellen von Nährstoffen für die Spermien • Verflüssigung des Ejakulats nach 15-20min Zusammensetzung des Seminalplasmas Menge 2-6ml pH Wert 7-8 (leicht alkalischer Puffer) Samenblasensekret 75% des Volumens, alkalisches fructosereiches Sekret (1,5-6,5mg/ml Fructose), Phosphorylcholin, Ascorbinsäure Prostatasekret 20%-25% des Volumens, Biogene Amine (Spermidin, Spermin), Zitronensäure, Cholesterin, Phospholipide, Proteasen zur Verflüssigung des Ejakulats (Fibrinolysin, Fibrinogenase) 25 Weitere Bestandteile Phosphat und Bikarbonat als Puffer, Prostaglandine, Hyaluronidase, Zelldetritus aus Sertolizellen, Zellen aus Vorstufen der Spermiogenese, Lymphozyten. Der Weg der Spermien bis zur Oozyte - Die Kapazitation 1 hinteres Scheidengewölbe 2 Portio / Muttermund 3 Cervixkanal 4 Tubenwinkel 5 Ampullärer Teil der Tube (Ampulle) 6 Ovar mit angelegten Fimbrien 7 Endometrium 8 Myometrium 9 Cavum uteri 10 Treffpunkt der Spermien mit der Oozyte Von den ca. 200 Millionen ejakulierten Spermien schaffen nur einige hundert den langen Weg durch den Muttermund (Cervix), die Gebärmutter (Uterus) und über den Tubenwinkel in den Eileiter bis in die ampulläre Region des Eileiters, um dort die Eizelle zu treffen. Unterwegs können ganze Pulks von Spermien an bestimmten Orten anhalten und in eine Phase geringerer Aktivität eintreten. Deshalb behält ein Teil der Spermien seine Befruchtungsfähigkeit bis zu 4 Tagen bei. 26 Der Weg der Spermien bis zur Oozyte - Die Kapazitation Cervixkanal 1 Spermien 2 Schleimfäden (stark vernetzt) 3 Krypte einer Cervixdrüse 4 Schleimfäden (weitmaschig) 5 Portioeingang Vor der Ovulation ist der Cervixkanal eng und der Cervixschleim stark vernetzt (er bildet den sogenannten Cervixpfropf) was eine Spermienpassage verhindert. Mit der Ovulation wird die Cervix locker und der Kanal weit. Die Schleimhautfalten nehmen zu und lassen tiefere und verzweigte Krypten entstehen, es gibt mehr Cervixdrüsen. Unter dem Einfluss des kurz vor der Ovulation ansteigenden Östradiols wird der Cervixschleim umstrukturiert. Der Schleimpfropf wird dadurch für Spermien durchgängig. 27 Der Weg der Spermien bis zur Oozyte - Die Kapazitation Die Kapazitation ist eine funktionelle Reifung des Spermatozoons. Die Veränderungen laufen über die Spermienzellmembran ab, bei der durch das Abtragen einer Glycoproteinschicht möglicherweise Rezeptoren freigegeben werden. Auch der Bereich der Akrosomal-Kappe wird dadurch so verändert, dass die Akrosomalreaktion möglich wird. Durch die Membranveränderungen ändern sich auch die motilen Eigenschaften des Spermatozoons. Es kommt zu ausladenden Peitschenschlagbewegungen des Schwanzes gepaart mit grösseren seitlichen Pendelbewegungen des Kopfes. Diese Art der Motilität wird als Hyperaktivität bezeichnet. Man kann also sagen, dass die sichtbare Folge der Kapazitation in einer Hyperaktivität des Spermatozoons besteht. Da sich der genaue Zeitpunkt, wann sich Oozyte und Spermatozoon treffen, nicht voraussagen lässt, sind die Reifungsmechanismen so ausgelegt, dass verschiedene Gruppen (Pulks) von Spermien über einen relativ langen Zeitraum nach der Kohabitation die Befruchtungschancen aufrecht erhalten. Die ejakulierten Spermien werden zu diesem Zweck nicht alle gleichzeitig ihre Kapazitation 28 beenden, so dass es zur Bildung heteroger Gruppen von Spermien kommt. Die Spermien treffen auf die Oozyte - Die Akrosomalreaktion Die Penetration der Kumuluszellen 1 Zentrum der Oozyte 2 Corona radiata (umschliesst und verdeckt teilweise die Oozyte) 3 Kopf des Spermatozoons Bei einem kleinen Prozentsatz der Spermien läuft die Akrosomalreaktion spontan ab, so wie es auch bei einem kleinen Prozentsatz der Spermien gleich nach der Ejakulation spontan zur Kapazitation kommt. Diese Tatsache hilft mit, dass gleich von Beginn weg, wenn die Woge Spermien auf die Eizelle trifft, eine geringe Menge an Hyaluronidase frei ist und dazu beiträgt, einigen Spermien den Weg zur Zona pellucida zu bahnen. An der Zona pellucida angekommen, werden diese Spermien akrosomalreagieren und weitere Mengen an Hyaluronidase und anderen Enzymen freisetzen. Auf diese Weise wird der Kumuluszellhaufen weiter aufgelöst und immer mehr Spermien erhalten die Möglichkeit, an der Zona pellucida selber die Akrosomalreaktion zu durchlaufen. 29 Die Spermien treffen auf die Oozyte - Die Akrosomalreaktion Der Kontakt mit der Zona Pellucida 1 Poren 2 Austritt von akrosomalem Inhalt 3 innere Akrosomalmembran 4 Akrosomaler Inhalt (Enzyme) 5 äusseren Akrosomalmembran 6 Zellmembran A Kopf B Hals C Mittelstück Voraussetzung für ein Gelingen der Akrosomalreaktion ist die vorgängige Bindung des Spermatozoons an die Zona pellucida. Die in unmittelbarer Nähe der Zona pellucida bei der Akrosomalreaktion freigesetzten Enzyme lösen diese lokal auf und gestatten dem Spermium so den Durchtritt durch die Zona pellucida. Es handelt sich um eine Vielzahl von freigesetzten Enzymen, wovon die bekanntesten die schon erwähnte Hyaluronidase und das Akrosin sind, wobei das Akrosin für den Durchtritt des Spermatozoons durch die Zona pellucida sorgt. 30 Das Eindringen des Spermatozoons in die Oozyte Der Andockmechanismus des Spermatozoons an die Oozyte (das Schlüssel-Schloss Prinzip) 1 Postakrosomaler Bezirk 2 Oolemma mit Mikrovilli 3 Periviteliner Spalt 4 Zona pellucida 5 Vesikel an der Oberfläche der Oozyte Das Andocken löst eine Kaskade von Ereignissen mit folgenden Zielen aus: - Polyspermieblock: Das Eindringen weiterer Spermien soll verhindert werden. - Verhärtung der Zona pellucida als mechanischer Schutz des Embryos - Aufnahme des Spermatozoons in die Oozyte - Beenden der 2. Reifeteilung der Oozyte mit Ausstossen des 2. Polkörpers - Vorbereitungen auf molekularer Ebene in der Oozyte zur Entpackung der väterlichen DNS 31 Das Eindringen des Spermatozoons in die Oozyte Einführung in die Bildung und Entwicklung der Vorkerne 1 Teilungsspindel mit Chromatiden 2 1. Polkörper 3 Zona pellucida 4 Perivitelliner Spalt 5 Zellmembran Spermatozoon (Rest als Anhängsel) 6 Kinozilium 7 Kern (kompakt) des Spermatozoons 8 Proximales Zentrosom des Spermatozoons 1 Polkörper 2 Kern (leicht dekondensiert) des Spermatozoons 3 Proximales Zentrosom des Spermatozoons 4 2. Polkörper (im Entstehen) 5 Reste der Teilungsspindel mit mütterlichen Chromosomen 1n,1C Das Beenden der zweiten Reifeteilung bedeutet die Teilung der sekundären Oozyte (1n,2C) zur reifen Oozyte (1n,1C) 32 unter Ausstossung des 2. Polkörpers (1n,1C) in den perivitellinen Spalt. In vitro fertilisation 33 Die Fertilisation wird abgeschlossen Die Ausbildung der Zygote 34 Die Fertilisation wird abgeschlossen Die Ausbildung der Zygote Einführung in die Bildung und Entwicklung der Vorkerne 1 Vorkern väterlicherseits 2 Vorkern mütterlicherseits 3 Zentrosom vom Spermatozoon eingebracht 4 Ansammlung der Polkörper Der mütterliche Vorkern ist den Polkörpern am nächsten. Der väterliche bildet sich in der Nähe der Spermien Eintrittsstelle aus, die sich fast immer mit einem gewissen Abstand zu den Polkörpern befindet. 35 Die Fertilisation wird abgeschlossen Die Ausbildung der Zygote Annäherung der Vorkerne 1 Väterlicher Vorkern 2 Mütterlicher Vorkern 3 Väterliches Zentrosom 4 "Inner bodies" 5 Mütterliche Astral-Mikrotubuli 36 Die Fertilisation wird abgeschlossen Die Ausbildung der Zygote 1 Kernmembran der Vorkerne, in Auflösung begriffen 2 Mikrotubuli der Teilungsspindel Nachdem sich die Vorkerne maximal angenähert haben, findet keine Verschmelzung der beiden Vorkerne statt, d.h. ein Zusammenlegen der Chromosomen beider Vorkerne innerhalb einer einzigen Kernmembran, findet nicht statt. Vielmehr lösen sich die Kernmembranen beider Vorkerne auf und die Chromosomen beider Vorkerne ordnen sich im Spindelapparat in der Äquatorialebene an. Durch die Anordnung der mütterlichen zusammen mit den väterlichen Chromosomen in einem gemeinsamen Spindelapparat entsteht die Zygote, die erste Zelle des neuen Organismus mit individuellem Genom (2n4C). 37 Preimplantation • Die Furchungsteilungen und die Migration des Embryos durch die Tube 38 Preimplantation Die Furchungsteilungen bis zur Morula 39 Preimplantation Preimplantation 41 Preimplantation Das Schlüpfen der Blastozyste (Hatching) 1 Zona pellucida 2 Trophoblast (äussere Zellmasse) 3 Hypoblast (Teil der inneren Zellmasse) 4 Blastozystenhöhle 5 Epiblast (Teil der inneren Zellmasse) 42 Preimplantation Blastocyst morphology Proposal for a universal minimum information convention for the reporting on the derivation of human embryonic stem cell lines. Stephenson EL, Braude PR, Mason C. Regen Med. 2006 Nov;1(6):739-50. 43 Preimplantation Die Migration des Embryos durch die Tube 1 Ovar 2 Tube 3 Endometrium 4 Myometrium 5 Cavum uteri A Spermatozoon penetriert in Oozyte (Konzeption), Tag 0 B Zweizellstadium, Tag 1 C Vierzellstadium, Tag 2 D Achtzellstadium, Tag 3 E Morula (16-32 Zellen), Tag 4 F Freie Blastozyste (nach Hatching), Tag 6 44 Implantation • Etappen der Implantation • Embryonalscheibe – – Die zweiblättrige Embryonalscheibe (2. Woche) Die dreiblättrige Embryonalscheibe (3. Woche) 45 Implantation Etappen der Implantation Normale Implantationszone 1 Uterushöhle 2 Isthmus uteri 3 Tuba Uterina 4 Cervix Uteri) Damit die Implantation korrekt ablaufen kann, müssen die Blastozyste und die Uterusschleimhaut interagieren können. Diese beiden voneinander unabhängigen Strukturen müssen sich also synchronen Veränderungen unterziehen. Die Implantation findet normalerweise in der superioren und posterioren Wand des Corpus uteri statt. Genauer gesagt in der funktionellen Schicht des Endometriums, während der sekretorischen Phase des Menstruationszyklus. 46 Implantation Adhäsion der Blastozyste an das Endometrium A Menstruation B Proliferation C Sekretion D Implantationsfenster In Folge der Apposition der freien Blastozyste auf das Uterusepithel interagieren die Mikrovilli auf der Oberfläche der zu äusserst gelegenen Trophoblastzellen mit den Epithelzellen des Uterus. Es bilden sich Verbindungskomplexe, die für eine stärkere Adhäsion verantwortlich sind. In diesem Stadium kann die Blastozyste nicht mehr durch einfaches Auswaschen eliminiert werden. Die Adhäsion der Blastozyste an das Endometrium kommt durch Oberflächenglykoproteine zustande, der spezifische Mechanismus ist jedoch nicht im Detail bekannt. 47 Implantation 1 Epithel der Uterusschleimhaut 2 Hypoblast 3 Synzytiotrophoblast 4 Zytotrophoblast 5 Epiblast 6 Blastozystenhöhle 1 Synzytiotrophoblast (ST) 2 Zytotrophoblast (ZT) 3 Epiblast 4 Hypoblast 5 Blastozystenhöhle 6 Mütterliche Blutkapillare 7 Amnionhöhle 8 Amnioblasten 9 Fibrinpfropf 10 Trophoblastlakunen 11 sich vermehrender Hypoblast 1 Sich vermehrender Hypoblast 2 Erodierte mütterliche Kapillare 3 Extra-embryonales Retikulum 4 Heuser´sche Membran 5 Amnionhöhle 6 Zytotrophoblast 7 Synzytiotrophoblast 8 Lakune, gefüllt mit Blut In der Peripherie bildet der Synzytiotrophoblast ein Synzytium, d.h. eine mehrkernige Schicht ohne Zellgrenzen, das aus der Fusion der äusseren Zytotrophoblastenzellen stammt. Der Synzytiotrophoblast besitzt lytische Enzyme und sezerniert Faktoren, die eine Apoptose der epithelialen Zellen der Uterusschleimhaut bewirken. Der Synzytiotrophoblast durchquert auch die Basallamina und dringt in das darunterliegende Stroma ein, das in Kontakt mit den uterinen Blutgefässen steht. Es sind zahlreiche "Implantationsfaktoren" bekannt: 48 Das Interleukin 1 (IL-1), der Inhibitionsfaktor für Leukozyten (LIF), der koloniestimulierende Faktor (CSF), sowie der epitheliale Wachstumsfaktor (EGF) und sein Rezeptor EGF-R. Embryonalscheibe Die zweiblättrige Embryonalscheibe (2. Woche) 1 Extra-embryonales Mesoblast 2 Amnionhöhle 3 Primäres Nabelbläschen Bei der zweischichtige Anlage des Embryos (Hypoblast bzw. primäres Endoderm und Epiblast) erkennt man im hohen Epithel des Epiblasten einen mit Flüssigkeit gefüllten Raum, die erste Anlage der Amnionhöhle. Ventral wird das Dach des noch unvollständig ausgekleideten primären Nabelbläschens (vorher Blastozystenhöhle) durch den Hypoblast gebildet Zusammen bilden sie schematisch zwei Halbkugeln mit zwei eng aneinander liegenden Blättern, die die eigentliche erste Anlage des Embryos darstellen. Jedoch ist lediglich der Epiblast für die Bildung des embryonalen Gewebes zuständig. Der Hypoblast bildet einen Teil der extraembryonalen Anhangsgebilde. 49 Embryonalscheibe Die dreiblättrige Embryonalscheibe (3. Woche) Bildung des Primitivstreifens 1 Primitivrinne 2 Primitivgrube 3 Primitivknoten 4 Membrana oropharyngea 5 kardiogene Platte 6 Schnittrand des Amnions 7 Mesoderm 8 Endoderm 9 künftige Membrana cloacalis 1+2+3 = Primitivstreifene 1 Primitivgrube 2 Epiblast 3 Extraembryonales Mesoderm 4 definitives Endoderm 5 Einwanderung von Epiblastzellen für die Bildung des intraembryonalen Mesoderms 6 Hypoblast Die zweiblätterige Keimscheibe differenziert sich weiter zur dreiblätterigen Keimscheibe, indem Zellen über den Primitivstreifen zwischen die beiden bereits bestehenden Keimblätter einströmen und so das dritten embryonalen Keimblatt (Mesoblast/derm) bilden. Dieses Phänomen wird auch als Gastrulation bezeichnet . In diesem Stadium erfährt der Embryo tiefgreifende Veränderungen. Ab diesem Zeitpunkt spricht man vom dorsal liegenden Ektoblasten/derm und nicht mehr vom Epiblasten/-derm, vom intermediären Mesoblasten/-derm, sowie vom ventral liegenden Endoblasten/-derm, welcher den Hypoblasten ersetzt. Um einen besseren Überblick zu erhalten, sollte die dritte Woche der Entwicklung in mehrere Phasen unterteilt werden. Man muss dabei in Erinnerung behalten, dass diese nicht immer 50 aufeinander folgen, sondern ebenso gleichzeitig verlaufen können. Embryonalscheibe Entstehung der Chorda dorsalis Chordafortsatz ca. 19-21 Tag (Stadium 7) 1 Chordafortsatz 2 Primitivknoten 3 Embryonaler Endoblast 4 Amnionhöhle 5 Haftstiel 6 Extraembryonales Mesenchym 7 Allantois 51 Embryonalscheibe Chordafortsatz ca. 25-28 Tag (Stadium 9-10) 1 Chordafortsatz 2 Embryonaler Endoblast 3 Amnionhöhle 4 Neuralrohr 5 Haftstiel 6 Intraembryonaler Mesoblast 7 Prächordalplatte 8 Rachenmembran 9 Kloakenmembran 10 Aorten 11 Umbilikalvenen 12 kardiogene Platte 13 Allantois Zusammenfassung: Die Chorda dorsalis bestimmt die Longitudinalachse des Embryos. Sie legt die zukünftige Lage der Wirbelkörper fest und induziert den Ektoblasten bei dessen Differenzierung zur Neuralplatte. 52 Embryonalscheibe Zielort der Epiblastzellen und Entwicklung des Primitivstreifens Dorsalansicht des Primitivstreifens ca. 17 Tag 19 Tag 1 Primitivstreifen 2 Prächordalplatte 3 Primitivknoten 4 Neuralplatte 5 Kloakenmembran 6 Chordafortsatz 21 Tag 1 Primitivstreifen 2 Primitivknoten 3 Neuralrohr 4 Kloakenmembran 5 Prächordalplatte 6 Chordafortsatz 23 Tag 53 Embryonalscheibe Induktion der Neuralplatte - Neurulation Neuralplatte 19 – 23 Tag 25 Tag 1 Neuralplatte 2 Primitivstreifen 3 Primitivknoten 4 Neuralrinne 5 Somiten 6 Schnittrand des Amnion 7 Neuralfalten Neuralrohr ca. 28. Tagen 29 Tag 1 Neuralrohr 2 Neuralfalte 3 Neuralrinne 4 Somiten 5 Neuralleiste 6 Vorwölbung des Perikards 7 Kranialer Neuroporus 8 Kaudaler Neuroporus Die Somiten sind embryonale Übergangsorgane, die durch die Segmentierung des paraxialen Mesenchyms gebildet werden. Sie organisieren sich ohne Zelldifferenzierung (primäre Organe). Sie sind für die segmentale Organisation des Embryos zuständig und tragen zur Restrukturierung des Embryos bei. Sie enthalten das Zellmaterial für das Achsenskelett (Sklerotome), der quergestreiften Muskulatur des Halses, des Rumpfes und der Extremitäten (Myotome), sowie das der subkutanen Gewebe und der Haut (Dermatom). Die Somiten sind Voraussetzung für die Metamerie. Die metamere Aufteilung der Wirbelsäule, des Neuralrohrs, der Rumpfwand und des Thorax (Rippen) hängt von der 54 ordentlichen Anlage der Somiten ab. Missbildungen während der SS Der Abschnitt A weist auf die Embryonalperiode hin, in welcher der Embryo besonders sensibel ist in Bezug auf Missbildungen. Das Vorkommen von Missbildungen (blaue Kurve), welche zu Spontanaborten führen, nimmt im Verlaufe der ersten acht Wochen von mehr als 10% auf 1% ab. Die Häufigkeit von Neuralrohrmissbildungen nimmt bis zum Ende der Embryonalperiode von 2.5 % auf 0.1% ab (grüne Kurve). A Embryonalperiode B Fetalperiode 0-3 Woche Tot des Embryos möglich 3-8 Woche Erhöhte Anfälligkeit für Missbildungen 8-38 Woche Funktionelle Abnormalitäten möglich 55 Danksagung Prof. Dr. med. Christian De Geyter Physicians Dr. med. R. Moffat Dr. med. G. Sartorius Dr. med. A . Raggi Dr. Astrid Ahler Technicians Helga Grässlin Kornelia Weber Nicole Crisante Nadja Kuratli Mylène Eby Clinical Researcher Dr. Maria De Geyter Dr. Sofia Forte Nurses Sandra Brodbeck Jacqueline Amstutz Simone Gänser Britta Bernauer Caroline Bamert Lorenza Tinelli Evelyne Dold Researchlab Dr. Hong Zhang Dr. Anne-Catherine Feutz Schneider Brigitte PhD Student Nadira M'Rabet Xiaoli Shen Flurina Pletscher Wang Xinggan Administration Florije Gashi Secretary Hanna Flükiger 56